UREA-ZEOLIT-ASAM HUMAT
Oleh :
GANDA DARMONO NAINGGOLAN A14052121
MAYOR MANAJEMEN SUMBERDAYA LAHAN DEPARTEMEN ILMU TANAH DAN SUMBERDAYA LAHAN
FAKULTAS PERTANIAN INSTITUT PERTANIAN BOGOR
RINGKASAN
GANDA DARMONO NAINGGOLAN. Pola Pelepasan Nitrogen dari Pupuk
Tersedia Lambat (Slow Release Fertilizer) Urea-Zeolit-Asam Humat. Di bawah bimbingan SUWARDI dan DARMAWAN.
Nitrogen (N) merupakan unsur hara esensial ba gi tanaman sehingga bila kekurangan unsur tersebut menyebabkan tanaman tidak dapat tumbuh dengan normal. Nitrogen mudah hilang dari tanah sehingga perlu mengurangi kehilangannya dengan membentuk pupuk dalam bentuk tersedia lambat (slow
release). Beberapa bahan yang dapat digunakan untuk membuat slow release
diantaranya adalah yang memiliki kapasitas tukar kation (KTK) tinggi seperti zeolit dan asam humat. Penelitian ini bertujuan untuk mengetahui laju dan pola pelepasan nitrogen dari formula slow release fertilizer (SRF) campuran urea, zeolit dan asam humat (UZA) dan membandingkannya dengan pupuk urea pril.
Tanah yang digunakan untuk penelitian adalah tanah sawah dari daerah Situ Gede Bogor. Pupuk slow release yang digunakan dalam penelitian ini dibuat dari campuran urea, zeolit dengan perbandingan 70:30 dan asam humat diberikan dengan kadar 0%, 1%, 2%, 3%, 4% dan 5%. Pengukuran laju pelepasan nitrogen pupuk dilakukan dengan metode inkubasi. Tiap periode waktu tertentu yaitu pada minggu ke 1, 2, 3, 4, 6, 8, 10 dan 14, selama masa inkubasi dilakukan analisis konsentrasi amonium dan nitrat, pH dan daya hantar listrik (DHL). Penetapan kadar amonium dan nitrat dilakukan dengan metode destilasi menggunakan ekstraktan KCl 1N+HCl 0,1 N. Pada minggu ke-14 juga dilakukan analisis tanah akhir meliputi N-Total, C-Organik, P-Tersedia, KTK, basa-basa dan Kejenuhan Basa (KB).
Hasil penelitian menunjukkan bahwa formulasi SRF dalam bentuk UZA dapat memperlambat laju perubahan amonium menjadi nitrat, sekitar dua minggu bervariasi berdasarkan kadar humatnya. Pupuk UZA mampu mempertahankan keberadaan nitrat hingga minggu ke-14 lebih dari 90% dibandingkan dengan urea yang hanya 60% dari pupuk yang diberikan. Hasil analisis tanah akhir menunjukkan, nilai dari P-tersedia dan basa-basa yaitu Mg, K dan Na mengalami peningkatan. Nilai KTK tanah juga mengalami peningkatan sejalan dengan waktu inkubasi. Secara umum pH tanah menurun sedangkan DHL meningkat selama waktu inkubasi. Hal ini disebabkan oleh penurunan jumlah amonium dan peningkatan jumlah nitrat.
GANDA DARMONO NAINGGOLAN. Pattern of Nitrogen Release from Slow
Release Fertilizer of Urea-Zeolite-Humic Acid. Under the guidance of
SUWARDI and DARMAWAN.
Nitrogen (N) is an essential nutrient for plants, so the lack of this element can cause the plant does not grow normally. Nitrogen easily lost from the soil, so fertilizer should be formed of a slow release fertilizer. Materials that can be used to make slow release fertilizer is, among other, material with high cation exchange capacity (CEC), like zeolites and humic acid. This study aims to determine the rate and pattern of nitrogen release from slow release fertilizer (SRF) that is a mixture of urea, zeolite and humic acid (UZA) and its comparison to urea.
Soil samples used in this research were taken from paddy fields at Situ Gede Bogor. Slow release fertilizer was made from a mixture of urea pril and zeolite with a ratio of 70:30 with adition of humic acid at 0%, 1%, 2%, 3%, 4% and 5%. The release rate of N was measured by incubation of UZA in the soil samples. During the incubation period the content of ammonium and nitrate concentrations (%), pH and EC (μS/cm) were analyzed at week 1, 2, 3, 4, 6, 8, 10 and 14. Determination of ammonium and nitrate levels was done by distillation method using KCl 1N+HCl 0.1 N. Final soil analysis performed at week 14 that includes N-total, C-Organic, Available P, CEC, bases and base saturation (KB).
The results showed that the SRF in the form of UZA has reduced the rate of change of ammonium into nitrate, about two weeks slower then the urea varied with humic level. UZA fertilizer was able to maintain the existence of nitrate up to 90% until week 14 compared with that of urea that was only 60% of total N from the fertilizer. The results of final soil analysis shows that available P, and the exchangeable Mg, K and Na increased. Soil CEC also increased with incubation time. In general, soil pH decreased while EC increased dur ing the incubation time. This was caused by the decrease in the amount of ammonium and increase the number of nitrate.
POLA PELEPASAN NITROGEN DARI
PUPUK TERSEDIA LAMBAT (SLOW RELEASE FERTILIZER)
UREA-ZEOLIT-ASAM HUMAT
Oleh :
GANDA DARMONO NAINGGOLAN A14052121
Skripsi
Sebagai salah satu syarat untuk me mperoleh gelar Sarjana Pertanian pada
Departemen Ilmu Tanah dan Sumbe rdaya Lahan Fakultas Pe rtanian
Institut Pe rtanian Bogor
MAYOR MANAJEMEN SUMBERDAYA LAHAN DEPARTEMEN ILMU TANAH DAN SUMBERDAYA LAHAN
FAKULTAS PERTANIAN INSTITUT PERTANIAN BOGOR
Nama Mahasiswa : Ganda Darmono Nainggolan Nomor Pokok : A14052121
Menyetujui
Pembimbing Skripsi I Pembimbing Skripsi II
Dr. Ir. Suwardi, M. Agr. Dr. Ir. Darmawan, M. Sc. NIP. 19630607 198703 1 003 NIP. 19631103 199002 1 001
Mengetahui, Ketua Departemen
Ilmu Tanah dan Sumberdaya Lahan
Dr. Ir. Syaiful Anwar, M. Sc. NIP. 19621113 198703 1 003
RIWAYAT HIDUP
Penulis dilahirkan di kota Jayapura (Papua) pada tanggal 15 Mei 1988 dari ayah Hendro Hotman Nainggolan dan ibu Nurlina br. Simanjuntak (Alm.). Penulis adalah anak pertama dari 6 bersaudara. Penulis lulus Sekolah Dasar di SD YPPK Gembala Baik Jayapura pada tahun 1999. Kemudian melanjutkan pendidikan di SMP YPPK Santo Paulus Jayapura sampai tahun 2002, selanjutnya penulis melanjutkan pendidikan di SMA YPPK Taruna Tegasa Keerom dan lulus pada tahun 2005.
Pada tahun 2005, penulis lulus seleksi masuk ke Institut Pertanian Bogor melalui jalur Seleksi Penerimaan Mahasiswa Baru (SPMB). Pada tahun berikutnya (2006), penulis diterima di Departemen Ilmu Tanah dan Sumberdaya Lahan, Fakultas Pertanian, Institut Pertanian Bogor dengan mayor Manajemen Sumberdaya Lahan. Selama kuliah di IPB, penulis aktif mengikuti berbagai kegiatan di kampus, beberapa diantaranya adalah, anggota Himpunan Mahasiswa Ilmu Tanah (HMIT) sebagai Staf Pengembangan Sumberdaya Manusia serta mengikuti program pengabdian masyarakat, gerakan masa pembuatan sejuta lubang resapan biopori dan pengembangan kampung biopori di DKI Jakarta Desember 2007. Selama menjalani pendidikan perguruan tinggi, penulis juga pernah bergabung dalam kegiatan kemahasiswaan seperti kepanitiaan MPD (Masa Perkenalan Departemen) periode 2007/2008. Selain itu penulis pernah menjadi asisten praktikum Morfologi dan Klasifikasi Tanah semester ganjil dan genap tahun ajaran 2008/2009, asisten praktikum Survei dan Evaluasi Sumberdaya Lahan semester genap tahun ajaran 2008/2009 dan asisten praktikum Pengantar Ilmu Tanah semester ganjil tahun ajaran 2009/2010. Selain dari kegiatan tersebut, penulis juga pernah menjadi pemakalah pada seminar nasional yang ke VI Ikatan Zeolit Indonesia (IZI) November 2009 dengan topik makalah sesuai dengan judul penelitian ini.
KATA PENGANTAR
Puji syukur penulis panjatkan ke Hadirat Tuhan Yang Maha Esa, yang telah memberikan hikmat dan karunia-Nya, sehingga penulis dapat menyelesaikan penelitian dan penulisan skripsi. Skripsi yang berjudul “Pola Pelepasan Nitrogen dari Pupuk Tersedia Lambat (Slow Release Fertilizer) Urea-Zeolit-Asam Humat“ ini merupakan salah satu syarat untuk mendapatkan gelar Sarjana Pertanian pada Departemen Ilmu Tanah dan Sumberdaya Lahan, Fakultas Pertanian, Institut Pertanian Bogor.
Pada kesempatan ini penulis ingin menyampaikan ucapan terimakasih yang sebesar-besarnya kepada:
1. Dr. Ir. Suwardi, M.Agr sebagai dosen pembimbing skripsi dan pembimbing akademik yang telah memberikan bimbingan, pengarahan, serta masukan selama masa perkuliahan, pelaksanaan penelitian, maupun saat penyusunan skripsi ini.
2. Dr. Ir. Darmawan, M.Sc sebagai dosen pembimbing skripsi yang telah memberikan bimbingan, pengarahan, serta masukan selama penyusunan skripsi ini.
3. Dr. Ir. Sri Djuniwati, M.Sc sebagai dosen penguji yang telah memberikan saran dan masukan dalam penulisan skripsi ini.
4. Keluarga tercinta papa, mama (Alm.), tante, dan adik-adikku Hosiana Marthauly br. Nainggolan, Hendra Wiwin Nainggolan, Bunga Herlina br. Nainggolan, Sara br. Nainggolan dan Saskia br. Nainggolan atas doa, dukungan, cinta, kasih sayang, perhatian, kepercayaan dan kesabaran selama ini, sehingga penulis dapat menyelesaikan penyusunan skripsi ini. 5. Keluarga Ompung Prof. Dr. Ir. W.H. Limbong, MS dan O mpung boru
(Alm.) serta bapak dan Ibu, tua Moreno dan keluarga, tua Louis dan keluarga, tua Armindo dan keluarga, uda Yaya dan keluarga, bou Kiki, bou Lily dan bou Lady atas bimbingan, perhatian, kepercayaan dan nasehat kepada penulis selama menjalani masa perk uliahan di IPB.
6. Seluruh staf dan laboran Departemen Ilmu Tanah dan Sumberdaya Lahan. 7. Semua rekan MSL 42, Genesis Crew, senior dan alumni Tanah, Ikatan
Zeolit Indonesia (IZI), Team Pesta Bujang (TPB) dan All Soiler.
Bogor, Februari 2010 Penulis
iii
DAFTAR ISI
Halaman KATA PENGANTAR... ii DAFTAR TABEL ... v DAFTAR GAMBAR ... vi I. PENDAHULUAN... 1 1.1. Latar Belakang ... 1 1.2. Tujuan Penelitian... 2II. TINJAUAN PUSTAKA... 3
2.1. Nitrogen... 3
2.1.1. Nitrogen di Dalam Tanah... 4
2.1.2. Kehilangan Nitrogen... 5
2.2. Zeolit... 7
2.2.1. Sifat Mineral Zeolit... 9
2.2.2. Zeolit sebagai Campuran Pupuk... 12
2.3. Asam Humat... 12
2.3.1. Humus dan Asam Humat... 14
2.3.2. Ekstraksi Bahan Humat... 15
2.3.4. Manfaat Asam Humat dalam Pertumbuhan Tanaman... 16
III. BAHAN DAN METODE... 18
3.1. Waktu dan Tempat... 18
3.2. Bahan dan Alat... 18
3.3. Metode Penelitian... 19
a. Pembuatan Pupuk UZA... 19
IV. HASIL DAN PEMBAHASAN... 21
4.1. Laju Pelepasan Nitrogen dari Pupuk UZA dan Pupuk Urea Pril Ditinjau dari Konsentrasi Amonium dan Nitrat yang Terbentuk... 21
4.2. Perubahan pH dan DHL selama Inkubasi, Peningkatan KTK Tanah dan Analisis Akhir Sifat-sifat K imia Tanah……….. 27
4.3 Mekanisme Slow Release dari Slow Release Fertilizer Urea-Zeolit-Asam Humat... 28
V. KESIMPULAN DAN SARAN... 29
5.1. Kesimpulan... ` 29
5.2. Saran... 29
DAFTAR PUSTAKA... 30
v
DAFTAR TABEL
Nomor Halaman
Teks
1. Jenis Pupuk SRF, Perbandingan Urea : Zeolit, Konsentrasi
Humat dalam Pupuk dan Kandungan Nitrogen dalam Tanah………... 18 2. Pelepasan Nitrogen dalam Bentuk N-NH4+ (%) dari Pupuk UZA dan
Pupuk Urea Pril selama 14 Minggu Inkubasi ………. 21 3. Pelepasan Nitrogen dalam Bentuk N-NO3- (%) dari Pupuk UZA
dan Urea Pril selama 14 Minggu Inkubasi……….. 24
Lampiran
1. Metode Analisis Tanah yang Digunakan dalam Penelitian... 33 2. Kriteria Penilaian Data Analisis Sifat Kimia Tanah
Menurut Pusat Penelitian Tanah………... 34 3. Hasil Analisis Pupuk UZA………... 35 4. Hasil Analisis pH selama 14 Minggu Inkubasi………... 36 5. Hasil Analisis DHL (µS/cm) selama 14 Minggu Inkubasi………… 36 6. Data Analisis Tanah Awal………... 37 7. Data Analisis Tanah Akhir………. 37
DAFTAR GAMBAR
Nomor Halaman
Teks
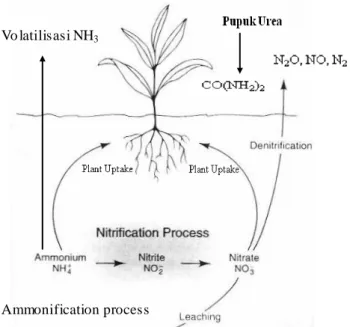
1. Gejala Defisiensi Nitrogen... 3 2. Siklus Nitrogen di dalam Tanah... 4 3. Mineral Zeolit... 10 4. Diagram Pemisahan Senyawa-senyawa Humat ke dalam Fraksi- fraksi
Humat yang Berbeda………... 15 5. Ciri-ciri Fisik Asam Humat... . 16 6. Inkubasi di Ruangan Terbuka Laboratorium... 20 7. Grafik Pelepasan Nitrogen dalam Bentuk Amonium (%) dari Pupuk
UZA dan Pupuk Urea Pril selama 14 Minggu Inkubasi... 23 8. Skema Proses Terjadinya Pengikatan Ion Amonium ke dalam Rongga
Zeolit... 24 9. Grafik Pelepasan Nitrogen dalam Bentuk Nitrat (%) dari Pupuk UZA
dan Pupuk Urea Pril selama 14 Minggu Inkubasi... 26 10. Ilustrasi Pelepasan Amonium dari Pupuk Urea- Zeolit-Asam Humat... 28
I. PENDAHULUAN
1.1. Latar Belakang
Nitrogen (N) merupakan unsur hara esensial bagi tanaman, sehingga bila kekurangan unsur tersebut menyebabkan tanaman tidak dapat tumbuh dengan normal. N itrogen merupakan unsur hara penentu produksi atau sebagai faktor pembatas utama produksi. Nitrogen sangat penting karena merupakan penyusun utama protein dan beberapa molekul biologik lainnya, nitrogen diperlukan baik oleh tumbuhan maupun hewan dalam jumlah yang besar (Sanchez, 1979).
Nitrogen merupakan salah satu unsur pupuk yang diperlukan dalam jumlah paling banyak namun keberadaannya dalam tanah sangat mobil sehingga mudah hilang dari tanah melalui pencucian maupun menguap ke udara. Sejumlah besar nitrogen hilang dari dalam tanah karena tanah mengalami pencucian oleh gerakan aliran air dan volatilisasi. Banyaknya nitrogen yang tersedia langsung bagi tumbuhan sangatlah sedikit (Nasoetion, 1996).
Jumlah nitrogen dalam tanah bervariasi, sekitar 0,02% sampai 2,5% dalam lapisan bawah dan 0,06% sampai 0,5% pada lapisan atas (Alexander, 1997). Pada kedalaman tanah yang berbeda terdapat perbedaan kandungan nitrogen. Kandungan nitrogen yang tertinggi terdapat pada permukaan tanah dan umumnya semakin menurun dengan kedalaman tanah.
Nitrogen dalam tanah berasal dari : (1) mineralisasi N dari bahan organik dan immobilisasinya, (2) fiksasi N dari udara oleh mikroorganisme (penambatan N2 atmosfer oleh mikroorganisme secara simbiotik maupun non-simbiotik), (3)
melalui hujan dan bentuk presipitasi yang lain, (4) pemupukan (Soepardi, 1983; Leiwakabessy, 1988).
Jenis pupuk N yang banyak dijumpai di pasaran Indonesia adalah dalam bentuk urea (CO(NH2)2). Pupuk ini mudah larut dalam air dan menguap ke udara
tanah untuk mengurangi penguapan (volatilisasi). Dalam prakteknya, untuk mengurangi kehilangannya petani sering melakukan pemupukan padi dua atau tiga kali dalam satu musim tanam. Nitrogen merupakan pupuk yang rendah efisiensinya. Nitrogen yang diberikan ke dalam tanah, hanya sekitar 30-40% diambil oleh tanaman dan sekitar 60% mengalami kehilangan akibat volatilisasi, denitrifikasi maupun pencucian.
Salah satu usaha untuk mengurangi kehilangan nitrogen adalah dengan membuat pupuk tersebut dalam bentuk slow release. Zeolit merupakan salah satu bahan yang dapat mengikat nitrogen sementara. Zeolit memiliki nilai kapasitas tukar kation (KTK) yang tinggi (antara 120-180 me/100g) yang berguna sebagai pengadsorbsi, pengikat dan penukar kation (Suwardi, 2000). Pupuk dalam bentuk
slow release dapat mengoptimalkan penyerapan nitrogen oleh tanaman karena slow release fertilizer (SRF) dapat mengendalikan pelepasan unsur nitrogen
sesuai dengan waktu dan jumlah yang dibutuhkan tanaman, serta mempertahankan keberadaan nitrogen dalam tanah dan jumlah pupuk yang diberikan lebih kecil dibandingkan metode konvensional. Cara ini dapat menghemat pemupukan tanaman yang biasanya dilakukan petani tiga kali dalam satu kali musim tanam, cukup dilakukan sekali sehingga menghemat penggunaan pupuk dan tenaga kerja (S uwardi, 1991).
Dalam pembuatan pupuk slow release dapat digunakan asam humat. Asam humat dapat berfungsi memperbaiki pertumbuhan tanaman secara langsung dengan meningkatkan permeabilitas sel atau melalui kegiatan hormon pertumbuhan (Tan, 1992). Tan dan Napamornbodi (1979 dalam Tan, 1992) memaparkan bahwa asam humat bermanfaat bagi pertumbuhan akar dan bagian atas tanaman.
1.2. Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui laju dan pola pelepasan nitrogen dari formula slow release fertilizer (SRF) campuran urea, zeolit dan asam humat serta membandingkannya dengan pupuk urea pril.
II. TINJAUAN PUSTAKA
2.1 Nitrogen
Nitrogen (N) merupakan unsur hara esensial bagi tanaman, sehingga bila kekurangan unsur tersebut menyebabkan tanaman tidak dapat tumbuh dengan normal. Menurut Sanchez (1979) nitrogen merupakan unsur hara penentu produksi atau sebagai faktor pembatas utama produksi. Nitrogen merupakan salah satu unsur pupuk yang diperlukan dalam jumlah paling banyak namun keberadaannya dalam tanah sangat mobil sehingga mudah hilang dari tanah melalui pencucian maupun menguap ke udara.
Pemberian pupuk nitrogen yang berlebihan menyebabkan pertumbuhan vegetatif tanaman sangat hebat dan warna daun menjadi hijau tua. Kelebihan N dapat memperpanjang umur tanaman dan memperlambat proses kematangan karena tidak seimbang dengan unsur lain seperti P, K, dan S.
Gambar 1. Gejala Defisiensi Nitrogen; (a) Tanaman Kekurangan Unsur Nitrogen yang Ditunjukkan oleh Klorosis (Menguning) pada Daun, (b) Daun Tanaman yang Mengalami Kekurangan Unsur Nitrogen Berwarna
Hijau Kekuningan, Sempit dan Berukuran Lebih Kecil. (Sumber: http://www.litbang.deptan.go.id)
Kekurangan unsur nitrogen mengakibatkan tanaman mengalami gejala defisiensi yang ditunjukkan oleh klorosis (menguning) pada daun, yang dimulai dari daun tertua. Kekurangan unsur nitrogen menyebabkan tanaman kerdil, daun yang lebih tua atau seluruh tanaman berwarna hijau kekuningan, daun yang masih muda berukuran sempit, pendek , tegak dan berwarna hijau kekuningan.
2.1.1. Nitrogen di Dalam Tanah
Nitrogen di dalam tanah berasal dari: (1) mineralisasi N dari bahan organik dan immobilisasinya, (2) fiksasi N dari udara oleh mikroorganisme (penambatan N2 atmosfer oleh mikroorganisme secara simbiotik maupun non-simbiotik), (3)
melalui hujan dan bentuk presipitasi yang lain, (4) pemupukan (Soepardi, 1983; Leiwakabessy, 1988).
Jumlah nitrogen dalam tanah bervariasi, sekitar 0,02% sampai 2,5% dalam lapisan bawah dan 0,06% sampai 0,5% pada lapisan atas (Alexander, 1997). Pada kedalaman tanah yang berbeda terdapat perbedaan kandungan nitrogen. Kandungan nitrogen yang tertinggi terdapat pada permukaan tanah dan umumnya semakin menurun dengan kedalaman tanah.
Unsur N yang ditemukan dalam tanah secara umum dapat dibagi menjadi dua bagian besar, yaitu bentuk N-organik dan N- inorganik. Bentuk N-organik meliputi asam amino atau protein asam amino bebas, gula amino dan senyawa kompleks yaitu amonium yang berasosiasi dengan lignin dan polimer-polimernya. Bentuk N-inorganik terdapat dalam bentuk amonium (NH4+), nitrat (NO3-), nitrit
(NO2-), oksida nitrous (N2O), oksida nitrit (NO) dan gas N2 akibat perombakan
mikrobia. N2O dan N2 adalah bentuk yang hilang dari tanah dalam bentuk gas
sebagai akibat dari proses denitrifikasi (Leiwakabessy, 1988).
Vo latilisasi NH3
Ammonification process
5
2.1.2. Kehilangan Nitrogen
Kehilangan nitrogen dalam tanah terutama disebabkan ole h proses denitrifikasi, volatilisasi, penguraian, pencucian, aliran permukaan, diserap oleh tanaman, serta pemanenan. Denitrifikasi adalah perubahan nitrogen dari keadaan teroksidasi seperti nitrat (NO3-) dan nitrit (NO2-) menjadi bentuk yang lebih
tereduksi seperti gas-gas oksida nitrit (NO), oksida nitrous (N2O) dan unsur
nitrogen bebas (N2). Kehilangan terbesar terjadi dalam bentuk oksida nitrous pada
pH 4,9-5,6, sedangkan pada pH 7,3-7,9 adalah dalam bentuk gas N2 dan sedikit
oksida nitrous (Leiwakabessy, 1988). Kehilangan melalui proses denitrifikasi ini dapat mencapai lebih dari 20%.
Volatilisasi merupakan salah satu penyebab kehilangan nitrogen tanah yang dapat disebabkan oleh dua hal, yaitu penguapan melalui sistem kapiler tanah dimana NH4+ yang terlarut dalam air bergerak ke lapisan atas dan hilang melalui
proses evaporasi dan kedua disebabkan penempatan pupuk amonium yang kurang tepat di permukaan tanah menyebabkan penguapan secara langsung akibat suhu yang tinggi. Pelepasan dari pupuk urea yang diberikan ke dalam tanah dapat mencapai 10-15% (Leiwakabessy, 1988).
Mineralisasi bahan organik tanah terjadi melalui tiga tahap reaksi utama, yaitu aminisasi, amonifikasi, dan nitrifikasi. Aminisasi dan amonifikasi berlangsung di bawah aktifitas mikroorganisme yang heterotrof sedangkan nitrifikasi dipengaruhi oleh bakteri autotrof (Leiwakabessy, 1988).
Aminisasi adalah pembentukan senyawa amino dari bahan organik (protein) oleh bermacam- macam mikroorganisme (hidrolisis protein dan pembebasan amina-amina dan asam-asam amino). Mikroorganisme heterotrof yang terlibat dalam proses aminisasi dan amonifikasi terdiri dari banyak jenis. Salah satu tahap terakhir dari proses dekomposisi bahan organik ialah hidrolisa protein dan pembebasan amina-amina dan asam-asam amino.
Amonifikasi adalah pembentukan amonium dari senyawa-senyawa amino oleh mikroorganisme. Amina-amina dan asam-asam amino yang dimanfaatkan oleh golongan bakteri heterotrof yang lain dan membebaskan senyawa amonium. Senyawa amonium yang dihasilkan adalah konversi ke nitrit dan nitrat, diambil langsung oleh tanaman, dan dipakai langsung oleh bakteri dalam melanjutkan proses dekomposisi serta difiksasi oleh mineral liat tertentu dari tipe 2:1.
R-NH2+ + HOH R-OH+ + NH3 + Energi
NH3 + HOH NH4OH NH4+ + OH
-Nitrifikasi adalah perubahan dari amonium (NH4+) menjadi nitrit (oleh
bakteri nitrosomonas), kemudian menjadi nitrat (oleh nitrobakter). Proses oksidasi biologi ini dibedakan dalam 2 tahap yaitu : Perubahan amonium menjadi nitrit oleh bakteri nitrosomonas (tergolong bakteri obligat autotrof) dan Perubahan nitrit menjadi nitrat oleh golongan bakteri obligat autotrof (nitrobakter).
2NH4+ + 3 O2 2 NO2- + 4 H+ + H2O
2 NO2- + O2 2NO3
-Di daerah-daerah dengan curah hujan tinggi maka bentuk nitrat ini akan hilang tercuci dari dalam tanah dan pada musim kemarau yang kuat ia akan bergerak lagi ke lapisan- lapisan di atasnya bersama-sama dengan pergerakan air ke atas secara kapiler.
Pada tanah sawah yang digenangi, ditemukan lapisan tipis di permukaan bersifat aerobik dan pada lapisan ini terjadi proses nitrifikasi sehingga pembentukan senyawa NO3- yang stabil dalam keadaan oksidatif. Karena kadar
NO3- di lapisan bawahnya yang anaerob lebih rendah, maka terjadilah proses
difusi NO3- ke lapisan bawah tersebut dan mengalami proses denitrifikasi menjadi
N2 gas dan mungkin N2O yang hilang dari tanah. Cepat hilangnya NO3- dari tanah
tergenang diperkirakan karena denitrifikasi, tercuci, dan diserap tanaman (De Datta dalam Situmorang dan Sudadi, 2001).
Menurut Buckman dan Brady (1969), bentuk N-NH4+ agak tahan terhadap
pencucian karena dapat difiksasi oleh mineral liat tipe 2:1. Fiksasi ini terjadi di dalam kisi-kisi kristal seperti halnya K+ pada mineral liat tipe 2:1, misalnya montmorilonit, ilit, dan vermikulit.
7
Urea (CO(NH2)2) merupakan pupuk nitrogen yang telah lama dan banyak
digunakan untuk meningkatkan hasil produksi tanaman pangan. Efisiensi serapan pupuk N (urea) di daerah tropika oleh tanaman padi sawah relatif rendah 30-50%. Hal ini menunjukkan bahwa lebih dari 50% pupuk yang diberikan tidak dapat diambil oleh tanaman padi (Prasad dan De Datta, 1979). Efisiensi pupuk urea yang rendah tersebut disebabkan oleh kehilangan akibat denitrifikasi, pencucian, terbawa aliran permukaan dan volatilisasi.
Urea termasuk pupuk yang higroskopis (mudah menarik uap air) pada kelembaban 73%. Untuk dapat diserap oleh tanaman, nitrogen dalam urea harus dikonversi terlebih dahulu menjadi amonium (N-NH4+) dengan bantuan enzim
urease melalui proses hidrolisis. Namun bila diberikan ke tanah, proses hidrolisis tersebut akan cepat sekali terjadi sehingga mudah menguap sebagai amoniak (Soepardi dan Djokosudardjo, 1980). Pemberian urea dengan disebar akan cepat terhidrolisis (dalam 2-4 hari) dan ini rentan terhadap kehilangan melalui volatilisasi.
Salah satu cara untuk mengurangi kehilangan N adalah dengan memodifikasi bentuk fisik dan kimia pupuk urea sehingga diharapkan dapat memperlambat proses hidrolisis. Pembuatan pupuk urea dalam bentuk ukuran butiran besar dapat meningkatkan ketersediaan pupuk sehingga dapat bertahan lebih lama dan banyak diserap tanaman serta lebih sedikit yang hilang dibandingkan dengan urea pril. Beberapa contoh bentuk baru dari urea a ntara lain; urea super granule, urea briket yang diaplikasikan dengan cara dibenamkan sedalam 15 cm dari lapisan atas (Prasad dan De Datta, 1979).
2.2. Zeolit
Mineral zeolit diketahui pertama kali pada tahun 1756 oleh seorang ahli mineralogi Swedia bernama Freiherr Axer Frederick Cronsteadt. Nama zeolit berasal dari bahasa Yunani, yaitu dari kata; Zein (mendidih) dan Lithos (batuan) yang artinya batu mendidih. Karena mineral ini mengeluarkan buih bila dipanaskan, sehingga kelihatan seperti mendidih (Gottardi, 1978; Mumpton, 1984).
Zeolit merupakan mineral kristalin dari kelompok tektosilikat, yaitu alumino-silikat terhidrasi dengan kation alkali dan alkali tanah seperti kalium, natrium, kalsium dan magnesium yang mengisi rongga-rongga kerangka alumino-silikat dan mempunyai struktur tiga dimensi. Susunan strukturnya adalah (Si, Al)O4 tetrahedral, memiliki pori yang berisi molekul air dan kation yang dapat
dipertukarkan. Zeolit dicirikan oleh kemampuannya menyerap dan mengeluarkan air serta menukarkan bagian kationnya tanpa merubah struktur kristalnya.
Rumus umum zeolit menurut Gottardi (1978) adalah :
(Mx+My2+) (Al(x+2y) Sin-(x+2y) O2n) . MH2O
M+ dan M2+ adalah kation monovalen (Na, K) dan divalen (Mg, Ca, Sr, dan Ba), x dan y adalah bilangan tertentu, m adalah jumlah molekul air kristal dan n adalah muatan ion logam.
Mineral zeolit mempunyai saluran dan rongga yang teratur dalam ukuran tertentu bersambungan. Sebagai kristal aluminosilikat terhidrasi dengan kation alkali ataupun alkali tanah, zeolit memiliki struktur dalam tiga dimensi yang tidak terbatas dalam bentuk-bentuk rongga. Unit struktur kristal zeolit terdiri dari kelompok senyawa tetrahedral alumina dan silikat yang bentuknya tergantung dari perbandingannya menurut jenis dan spesies zeolit. Struktur yang dimiliki zeolit menyebabkan mineral zeolit mempunyai karakter yang spesifik (Mumpton, 1984). Stuktur kristalnya terbuka dengan volume ruang hampa cukup besar dengan garis tengah antara 2-8 Ao tergantung dari tipe atau jenis mineral zeolit. Volume dan ukuran garis tengah ruang hampa dalam kisi-kisi kristal merupakan dasar penyaring molekul dalam penggunaan mineral zeolit (Gottardi, 1978).
Zeolit dapat diklasifikasikan menjadi dua kelompok besar yaitu zeolit alam dan zeolit sintetis. Zeolit alam terbentuk karena adanya proses perubahan alam (zeolitisasi) dari batuan vulkanik tuf, sedangkan zeolit sintetis direkayasa oleh manusia secara kimia dari bahan baku tertentu (Suwardi, 2002). Jumlah dan komposisi kation dalam zeolit tergantung dari jenis zeolit dan lingkungan pembentukannya, misalnya Mordenit umumnya banyak mengandung kalsium sedangkan K linoptilotit mengandung kalium. Zeolit yang terbentuk pada
9
lingkungan marin, mengandung banyak natrium sedangkan zeolit yang terbentuk pada lingkungan volkanik mempunyai kadar kalium dan magnesium yang tinggi.
Sampai saat ini deposit yang telah diketahui di Indonesia tidak kurang dari 47 lokasi yang tersebar dari pulau Sumatera, Jawa, Lombok dan Sumba. Lokasi yang telah diteliti secara intensif adalah di daerah Jawa Barat yaitu Bayah (Banten Selatan), Cikembar (Sukabumi), Nanggung (Bogor) dan Cikalong (Tasikmalaya) (Suwardi, 1991).
Mineral zeolit di alam telah banyak ditemukan dalam beberapa jenis, tetapi hanya 10 jenis yang memiliki nilai ekonomis baik dalam bidang industri maupun dalam bidang pertanian yaitu analsim, khabasit, k linoptilotit, erionit, heulandit, laumontit, mordenit dan philipsit, wairakit dan natrolit. Dari ke 10 jenis tersebut hanya 5 jenis yang telah terbukti bermanfaat untuk pertanian, yaitu; klinoptilotit, mordenit, erionit, khabasit dan philipsit. (Suwardi, 2002).
2.2.1. Sifat Mine ral Zeolit
Pada prinsipnya penggunaan zeolit didasarkan atas sifat-sifat mineralogi, fisik dan kimia yang dimiliki mineral ini. Sifat mineralogi zeolit dapat dipelajari dengan menggunakan bantuan alat mikroskop polarisasi DTA (Diffrential
Thermal Analysis). Beberapa sifat yang ditetapkan antara lain meliputi struktur
kristal, volume rongga, rasio Si/Al, ukuran rongga dimensi saluran, jumlah tetrahedral dan arah sumbuh kristal. Beberapa bentuk struktur kristal zeolit; kubik, hexagonal dan monoklin tetapi yang lebih dominan adalah monoklin (Suwardi, 2002).
Sifat-sifat fisik zeolit sangat beragam dan yang terpenting adalah warna, kerapatan isi, kadar air, besar dan jumlah rongga. Warna zeolit pada umumnya kehijau-hijauan sampai keabu-abuan, oleh karena itu zeolit juga disebut batu hijau. Selain itu, zeolit memiliki warna putih, putih kekuningan, merah muda, coklat kemerahan, dan hijau tua coklat kekuningan. Perbedaan wa rna zeolit disebabkan oleh jenis mineral pengotor diantaranya mineral liat, kuarsa, dan feldspar. Mineral pengotor dapat berubah warna pada kadar air yang berbeda. Kerapatan isi atau bobot isi zeolit lebih ringan dibandingkan dengan mineral
golongan silikat lainnya, yaitu berkisar antara 1.9-2.4 g/cm3. Hal ini dikarenakan mineral zeolit memiliki struktur berongga. Bobot isi sangat erat hubungannya dengan volume rongga dalam zeolit. Volume rongga zeolit berkisar 20-50% dari volume zeolit, jika volume rongga zeolit semakin besar maka bobot isinya semakin rendah (Suwardi, 1997).
Gambar 3. Mineral Zeolit, Digunakan dalam Bidang Pertanian karena Memiliki Sifat-sifat Mineralogi, Fisik dan Kimia yang Bermanfaat dalam Pengembangan Slow Release Fertilizer (Sumber: www.google.co.id)
Sifat kimia zeolit antara lain pH, daya hantar listrik, kapasitas tukar kation (KTK), susunan kimia. Hasil analisis zeolit dari beberapa lokasi (Suwardi, 1997) menunjukkan bahwa pH zeolit berkisar 6.3-8.2 (rata-rata 7.2), dimana pH terendah (6.3) terdapat pada zeolit dari Lampung dan tertinggi (8.2) dari Nanga Panda. Daya hantar listrik zeolit sangat rendah berkisar dari 0.02-0.15 dS/m (rata-rata 0.06 dS/m), karena dalam larutan sedikit mengeluarkan garam- garam yang dapat menghantarkan listrik, sehingga zeolit banyak dimanfaatkan sebagai media tumbuh tanaman. KTK zeolit berkisar antara 71.9-167 me/100g (rata-rata 104.6 me/100g) dengan KTK terendah (71.9 me/100g) terdapat pada zeolit dari Cikembar dan tertinggi (167 me/100g) dari Nanga Panda. Semakin tinggi KTK zeolit menunjukkan sifat zeolit semakin baik.
Zeolit terutama terdiri dari SiO2, Al2O3, K2O, CaO, Na2O, MnO, Fe2O3,
MgO. Zeolit dari Indonesia kaya akan K2O dan CaO. Sifat kimia zeolit terpenting
yang dimanfaatkan di bidang pertanian adalah sifat adsorpsi dan sifat pertukaran kation.
Adsorpsi dapat diartikan sebagai suatu proses melekatnya molekul-molekul atau zat pada permukaan zat yang lain atau terkonsentrasinya berbagai substansi terlarut dalam larutan antara dua buah permukaan. Zeolit memiliki
11
kemampuan dalam mengikat sejumlah molekul dan ion yang terdapat dalam larutan maupun gas. Adsorpsi molekul oleh zeolit dapat terjadi bila air dihilangkan dari kristal zeolit melalui pemanasan dengan suhu antara 350- 400 0C (Mumpton, 1984). Dalam hal ini, berbagai molekul adsorbate yang berdiameter sama atau lebih kecil dari diameter rongga dapat diadsorpsi, sedangkan molekul yang berdiameter lebih besar dari pori-pori zeolit akan tertahan. Akibat dari pemanasan maka air akan menguap, pada keadaan demikian, rongga maupun saluran-saluran dalam zeolit akan dapat berfungsi sebagai penyaring molekul (Astiana, 1993). Zeolit yang telah kehilangan air dari rongganya dinamakan zeolit yang telah teraktivasi yang dapat berfungsi sebagai pengabsorpsi kation yang efektif.
Pertukaran kation merupakan proses dimana kation-kation yang dapat diadsorpsi dapat ditukar dengan kation-kation lainnya. Pertukaran kation zeolit pada dasarnya adalah fungsi dari derajat substitusi silika oleh aluminium dalam struktur kristal zeolit. Semakin banyak jumlah aluminium menggantikan posisi silika maka semakin banyak muatan negatif yang dihasilkan, sehingga makin tinggi KTK zeolit tersebut dan penetralan dilakukan oleh kation alkali tanah. Susunan kation yang dapat dipertukarkan pada zeolit tergantung pada komposisi mineralnya. Kation-kation yang dapat dipertukarkan ataupun molekul air yang terdapat pada zeolit tidak terikat secara kuat dalam kerangka karenanya dapat dipisahkan atau dipertukarkan secara mudah dengan cara pencucian dengan larutan yang mengandung kation lain (Mumpton, 1984). O leh karena itu zeolit merupakan salah satu dari banyak bahan penukar kation yang mempunyai kapasitas tukar kation yang tinggi. Kapasitas tukar kationnya dapat mencapai 200 sampai 300 me/100g. Kapasitas tukar kation dari zeolit ini terutama merupakan fungsi dari tingkat penggantian Al untuk Si dalam struktur rangka.
Fraksi ukuran butir mineral zeolit yang digunakan ternyata mempengaruhi nilai kapasitas tukar kation, dimana butir berukuran 48 sampai 60 mesh nilainya adalah 96.5 sampai 115.1 me/100g dan ukuran 200 mesh nilainya adalah 109.9 me/100g. Penggerusan mineral zeolit yang lebih halus, menyebabkan kerusakan pada struktur kristal sehingga nilai kapasitas tukar kationnya turun. Ukuran butir
yang terbaik untuk digunakan sebagai penukar kation dalam reaksi pertukaran adalah 48 sampai 60 mesh (Astiana dan Wiradinata, 1989).
2.2.2. Zeolit sebagai Campuran Pupuk
Salah satu aspek penggunaan zeolit dalam bidang pertanian adalah sebagai bahan campuran pupuk, khususnya pupuk nitrogen. Hal ini berdasarkan pada selektivitas adsorpsi zeolit yang tinggi terhadap ion amonium yang mampu mengefisiensikan penggunaan pupuk kimia nitrogen sehingga penyerapan pupuk menjadi lebih efisien. Oleh karena itu zeolit dapat digunakan sebagai bahan pupuk tersedia lambat (slow release fertilizer).
Penambahan zeolit pada pupuk nitrogen akan menjerap amonium yang dikeluarkan oleh pupuk. Jika konsentrasi nitrat dalam tanah menurun, amonium yang telah dijerap oleh zeolit akan dilepaskan kembali ke dalam larutan tanah, dengan cara demikian N yang diberikan ke dalam tanah dapat tersedia dalam waktu yang lama. Pupuk dalam bentuk slow release fertilizers (SRF), dapat mengoptimalkan penyerapan hara oleh tanaman dan mempertahankan keberadaan hara dalam tanah, karena SRF dapat mengendalikan pelepasan unsur sesuai dengan waktu dan jumlah yang dibutuhkan tanaman. Melalui cara ini, pemupukan tanaman, yang biasanya dilakukan petani tiga kali dalam satu kali musim tanam, cukup dilakukan sekali sehingga menghemat penggunaan pupuk dan tenaga kerja (Suwardi, 1991)
Zeolit dapat mencegah terjadinya nitrifikasi karena mineral zeolit dapat menjerap NH4+ pada kisi-kisinya (diameter rongga klinoptilotit 3.9-5.4 Ao
sedangkan diameter NH4+ 1.4 Ao), sehingga bakteri nitrifikasi tidak dapat masuk
karena ukuran tubuh dari bakteri tersebut 1000 kali lebih besar dari diameter rongga zeolit (Alexander, 1977).
2.3. Asam Humat
Menurut Detmer (1871 dalam Orlov, 1985), asam humat adalah “massa hitam berkilau dengan suatu pecahan berkilau yang menyerupai kubah pecah”. Sementara menurut Schubler menyatakan bahwa dalam keadaan kering asam
13
humat “berubah menjadi tidak beraturan, berupa potongan-potongan kecil dengan pecahan berkilau dan berwarna hitam berkilau”. Kerapatan asam humat dalam keadaan rata-rata mendekati 1.6 g/cm3. Dengan rata-rata nilai kerapatan 1.6 g/cm3, asam humat dapat direkomendasikan untuk penggunaan di lapangan sesuai dengan teori yang dipelajari. Kerapatan asam humat cenderung meningkat seiring dengan meningkatnya derajat dekomposisi (Orlov, 1985).
Unsur atau penyusun utama asam humat ialah karbon. Kandungan karbon yang dimiliki asam humat berfluktuasi pada kisaran 56-62%. Sementara kandungan hidrogen dan nitrogen berturut-turut berada pada kisaran 2-5.5% dan 2-8% (Orlov, 1985; Orlov, 1992). Data lain menunjukkan kandungan karbon asam humat berkisar antara 41-57% (Tan, 1992). Asam humat tidak hanya mengandung C, N, H, dan O tapi juga terdapat sulfur dan fosfor. Asam humat juga mengandung unit aromatik dengan ikatan asam amino (organik N), peptida, asam alipatik dan bahan campuran lain yang tipe dan jumlahnya akan tergantung kepada jenis tanah dan tanaman (Orlov, 1985). Menurut Eggertz (1888 dalam Orlov, 1985), di dalam asam humat terdapat 0.6-1.1% sulfur dan 0.2-3.7% P. Dalam hal ini Eggertz juga menemukan bahwa asam humat mengandung 5.6% aluminium, 0.05-0.15% sodium, lebih dari 0.6% potasium dan sedikit magnesium dan Mn.
Berdasarkan tingginya karbon yang terdapat dalam asam humat, asam humat dikelompokkan ke dalam kelas carbonized (carbon-rich) compounds. Banyak bagian residu tanaman mengandung karbon tidak kurang dari asam humat, tetapi adakalanya kurang dari asam humat. Misalnya lignin mengandung 65% C dan lipid sekitar 72%. Pada saat yang sama karbohidrat relatif miskin karbon dan kaya akan oksigen, dimana glukosa mengandung karbon mendekati 40%. Jadi dalam komposisi elemen, asam humat menempati posisi menengah antara lignin dan karbohidrat, sementara asa m fulvat mendekati kandungan elemen yang dimiliki karbohidrat dan protein (Orlov, 1992).
Kemasaman total atau kapasitas tukar senyawa-senyawa humat tanah dikarenakan oleh kehadiran proton yang dapat terdisosiasi atau ion-ion H pada gugus karboksil aromatik dan alifatik dan gugus hidroksil fenolik. Asam humat
dicirikan oleh kemasaman total dan kadar karboksil yang lebih rendah daripada asam fulvat, kemasaman total asam humat umumnya adalah sebesar 5-6 mEk/g (Tan, 1992).
Selain unsur-unsur yang sudah disebutkan di atas, asam humat juga mengandung asam amino. Komposisi asam amino yang terdapat dalam asam humat bervariasi. Menurut Sowden (1970 dalam Orlov, 1985), terdapat 18 jenis asam amino yaitu asam aspartat, threonin, serin, asam glutamat, prolin, gysin, alanin, valin, cystein, methionin, isoleusin, leusin, tyrosin, phenilalanin, ornithin, lysin, histidin, dan arginin. Diantara asam amino tersebut, asam aspartat, asam glutamat, glysin, alanin, dan leusin berada cukup banyak di dalam asam humat.
2.3.1. Humus dan Asam Humat
Tanah disusun oleh beberapa komponen, diantaranya adalah : bagian anorganik, bahan organik (bahan organik tanah), dan jasad hidup yang terdapat dalam tanah (Orlov,1995). Bahan organik tanah terbagi dalam dua kelompok utama yaitu : (1) bahan-bahan tanaman yang sifat aslinya masih nampak; (2) bahan-bahan yang telah mengalami transformasi (Tan,1992).
Bahan organik tanah tersusun oleh senyawa-senyawa organik. Senyawa-senyawa organik penyusun bahan organik tersebut adalah : (1) karbohidrat (monosakarida, oligosakarida, dan polisakarida); (2) asam amino dan protein; (3) selulosa dan hemiselulosa; (4) lignin; (5) lipid; (6) asam nukleat; (7) humus (Orlov, 1992; Tan, 1992). Selain itu bahan organik tanah sering dipisahkan menjadi bahan terhumifikasi dan tak terhumifikasi (Tan,1992). Humifikasi merupakan salah satu dari proses transformasi sisa-sisa bahan organik (Orlov, 1985). Fraksi bahan organik yang telah mengalami humifikasi dikenal sebagai humus dan dapat dianggap sebagai hasil akhir dekomposisi bahan tanaman di dalam tanah (Orlov, 1995; Orlov, 1985; Tan, 1992).
Humus mengandung bahan-bahan humat (humic substances) dan bahan bukan humat (non-humic substances) (Orlov, 1995; Tan, 1992). Bahan humat bersifat amorf (amorphous), polimer (polymeric), dan berwarna kecoklatan (brown-colored matter) yang mempunyai sifat dan stuktur yang kurang diketahui.
15
Konfigurasi kimia dari bahan humat sampai saat ini kurang diketahui dan tidak dapat didefenisikan secara pasti. Berbeda dengan bahan bukan humat yang telah banyak dikenal dalam bidang kimia organik. Berdasarkan kelarutannya dalam asam dan alkali, fraksi humat (kecuali humin) dapat larut dalam alkali. Asam humat merupakan fraksi humat yang larut dalam alkali, namun tidak larut (mengendap) dalam asam dan alkohol (Tan, 1992).
2.3.2. Ekstraksi Bahan Humat
Ekstraksi bahan humat dalam tanah dapat digolongkan ke dalam beberapa fraksi humat tanah yaitu asam humat (humic acid), asam fulvat (fulvic acid) dan humin (Tan 1992). Walaupun demikian, Orlov (1995) menggolongkan klasifikasi fraksi humat ke dalam humin (prohic substances dan non-hydrolysable residues) dan asam humat (Mull acids). Mull acids sendiri dibagi ke dalam asam humat, asam hymatomelanic dan asam fulvat. Untuk menghindari destruksi, asam humat harus berada dalam keadaan kering pada temperatur yang tidak melebihi 60-70oC. Sementara untuk asam fulvat tidak melebihi 40oC. Metode pengeringan terbaik adalah dengan menjaga asam humat dan asam fulvat dalam vacum dengan P2O5
(Orlov, 1985).
Gambar 4. Ciri-ciri Fisik Asam Humat, Terbuat dari Bahan Organik dan
merupakan Fraksi Humat yang Larut dalam Alkali, namun Tidak Larut (Mengendap) dalam Asam dan Alkohol, Asam Humat Digunakan untuk Meningkatkan Pertumbuhan dan Produksi Tanaman
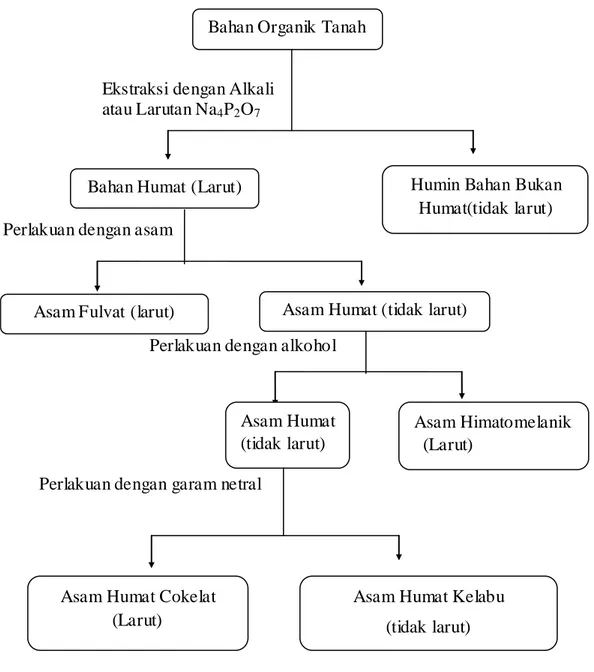
Ekstraksi dengan Alkali atau Larutan Na4P2O7
Perlakuan dengan asam
Perlakuan dengan alkohol
Perlakuan dengan garam netral
Gambar 5. Diagram Pemisahan Senyawa-senyawa Humat ke dalam Fraksi- fraksi Humat yang Berbeda
2.3.3. Manfaat Asam Humat dalam Pe rtumbuhan Tanaman
Pengaruh bahan organik terhadap pertumbuhan tanaman telah diketahui cukup lama. Keuntungan utama dari humus tanah terhadap pertumbuhan tanaman dihasilkan secara tidak langsung melalui perbaikan sifat-sifat tanah seperti agregasi, aerasi, permeabilitas, dan kapasitas memegang air. Namun seiring dengan perkembangan pengetahuan tentang bahan organik melalui penemuan tentang kimiawi asam humat, pengaruh humus terhadap pertumbuhan tanaman dapat lebih ditingkatkan.
Bahan Organik Tanah
Bahan Humat (Larut) Humin Bahan Bukan Humat(tidak larut)
Asam Humat (tidak larut)
Asam Humat (tidak larut)
Asam Himatomelanik (Larut)
Asam Humat Cokelat (Larut)
Asam Humat Kelabu (tidak larut) Asam Fulvat (larut)
17
Bahan-bahan humat bertanggung jawab atas sejumlah aktivitas kimia dalam tanah. Mereka terlibat dalam reaksi kompleks dan dapat mempengaruhi pertumbuhan tanaman secara langsung maupun tidak langsung. Secara tidak langsung asam humat diketahui memperbaiki kesuburan tanah dengan mengubah kondisi fisik, kimia, dan biologi dalam tanah. Secara langsung, asam humat telah dilaporkan merangsang pertumbuhan tanaman melalui pengaruhnya terhadap metabolisme dan terhadap sejumlah proses fisiologi lainnya. Senyawa humat juga berperan serta dalam pembentukan tanah dan memainkan peranan pent ing khususnya dalam translokasi atau mobilisasi aluminium dan besi, yang menghasilkan perkembangan horison spodik dan horison argilik (Tan, 1992).
Asam humat dapat berfungsi memperbaiki pertumbuhan tanaman secara langsung dengan meningkatkan permeabilitas sel atau melalui kegiatan hormon pertumbuhan (Tan, 1992). Tan dan Napamornbodi (1979 dalam Tan, 1992). Memaparkan bahwa asam humat bermanfaat bagi pertumbuhan akar dan bagian atas tanaman. Selain itu, terdapat peningkatan yang nyata dalam kandungan N bagian atas semai dan produksi bahan kering dari pemanfaatan asam humat.
3.1. Tempat dan Waktu
Penelitian dilaksanakan di Laboratorium Pengembangan Sumberdaya Fisik Lahan Departemen Ilmu Tanah dan Sumberdaya Lahan, Fakultas Perta nian, Institut Pertanian Bogor. Penelitian dilakukan dari bulan Maret sampai dengan bulan September 2009.
3.2. Bahan dan Alat
Pupuk yang digunakan dalam penelitian ini dibuat dari campuran urea, zeolit dan asam humat. Pupuk ini selanjutnya disebut UZA (urea- zeolit-asam humat). Pupuk UZA menggunakan perbandingan urea dan zeolit yaitu 70:30. Asam humat diberikan dengan kadar 0%, 1%, 2%, 3%, 4% dan 5% seperti terlihat pada Tabel 1. Asam humat cair dengan jumlah tersebut di atas dicampurkan ke urea-zeolit.
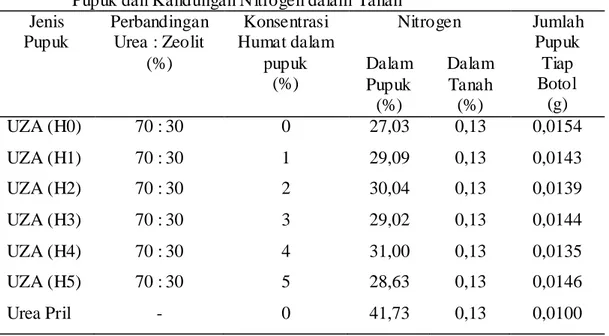
Tabel 1. Jenis Pupuk SRF, Perbandingan Urea : Zeolit, Konsentrasi Humat dalam Pupuk dan Kandungan Nitrogen dalam Tanah
Jenis Pupuk Perbandingan Urea : Zeolit (%) Konsentrasi Humat dalam pupuk (%) Nitrogen Jumlah Pupuk Tiap Botol (g) Dalam Pupuk (%) Dalam Tanah (%) UZA (H0) 70 : 30 0 27,03 0,13 0,0154 UZA (H1) 70 : 30 1 29,09 0,13 0,0143 UZA (H2) 70 : 30 2 30,04 0,13 0,0139 UZA (H3) 70 : 30 3 29,02 0,13 0,0144 UZA (H4) 70 : 30 4 31,00 0,13 0,0135 UZA (H5) 70 : 30 5 28,63 0,13 0,0146 Urea Pril - 0 41,73 0,13 0,0100
19
Tanah yang digunakan untuk penelitian adalah tanah sawah dari daerah Situ Gede, Bogor. Tanah diambil secara komposit pada kedalaman 0-20 cm kemudian dikeringudarakan. Untuk analisis sifat-sifat kimia di laboratorium, tanah ditumbuk dan diayak sampai lolos saringan 2 mm.
3.3. Metode Penelitian
a. Persiapan Pe mbuatan Pupuk UZA
Tahap pertama dalam pembuatan pupuk slow release dilakukan dengan mempersiapkan bahan-bahan utama yang dibutuhkan yaitu; urea, zeolit dan asam humat. Formula SRF (slow release fertilizer) dari ketiga bahan tersebut (urea-zeolit-asam humat) dinamakan pupuk UZA. Pupuk UZA dibuat dengan cara melapisi campuran urea-asam humat dengan zeolit. Pupuk UZA menggunakan perbandingan urea dan zeolit yaitu 70:30. Pupuk campuran urea- zeolit dengan perbandingan 70:30 merupakan perbandingan yang paling baik menurut temuan Suwardi (2005). Asam humat diberikan dengan kadar 0%, 1%, 2%, 3%, 4% dan 5%. Urea dan zeolit dipersiapkan dalam bentuk bubuk (powder) dengan ukuran 60-100 mesh. Urea diberi asam humat sesuai dosis, dosis asam humat dengan kadar 1% berarti setiap pembuatan 100 gram pupuk UZA membutuhkan asam humat sebanyak 1 ml. Urea yang telah diberi asam humat diaduk hingga homogen yang ditunjukkan oleh warna pupuk yang cokelat kehitaman. Setelah campuran urea-asam humat homogen, masukkan zeolit yang telah dicampur dengan pati (3.75 gram/100 gram pupuk UZA) yang digunakan sebagai perekat pupuk ke dalam campuran urea-asam humat. Setelah itu campuran urea-zeolit-asam humat diaduk hingga homogen yang ditunjukkan oleh warna pupuk yang coklet keabu-abuan. Kemudian pupuk UZA yang telah homogen diletakkan ke dalam wadah dan dibentuk granul. Pupuk UZA yang telah berbentuk granul dimasukkan ke dalam wadah untuk di oven selama 3 jam pada suhu ± 60 oC. Pupuk UZA yang digunakan berukuran sedang (tidak lolos saringan 2 mm).
b. Percobaan Inkubasi
Tanah kering udara sebanyak 113,79 g atau setara 100 g BKM (berat kering mutlak) dengan kadar air tanah 13,79% dimasukkan ke dalam wadah plastik berbentuk tabung silinder dengan diameter 6.00 cm dan tinggi 6.70 cm. Pupuk UZA pada setiap perlakuan ditimbang sesuai dosis yang ditentukan. Dosis pupuk untuk semua perlakuan adalah 4,17 mg N/100 gram tanah. Pupuk yang telah ditimbang kemudian dimasukkan ke dalam tanah. Jenis dan jumlah pupuk yang ditambahkan ke dalam wadah plastik yang berisi tanah seperti pada Tabel 1. Pupuk yang telah dimasukkan ke dalam tanah diberi air sampai mencapai kadar air kapasitas lapang (57,34%). Tanah dan pupuk dalam tabung ditutup dengan plastik polyethelene kemudian diinkubasi di ruangan terbuka laboratorium.
Tiap periode waktu tertentu yaitu pada minggu ke 1, 2, 3, 4, 6, 8, 10 dan 14 selama masa inkubasi dilakukan analisis amonium (%), nitrat (%), pH dan EC (µS/cm). Karena ada 7 perlakuan dan tiap perlakuan diulang 3 kali selama 8 kali pengamatan, maka jumlah tabung silinder yang digunakan sebanyak 7 x 3 x 8 = 168.
Penetapan kadar amonium dan nitrat dilakukan dengan mengekstrak tanah dengan metode destilasi menggunakan ekstraktan KCl 1N+HCl 0,1 N, lalu hasil ekstrak dianalisis dengan metode Destilasi. Seluruh contoh tanah pada minggu ke 14 dianalisis amonium, nitrat, pH, DHL dan analisis tanah akhir N-Total, C-Organik, P-Tersedia, KTK, basa-basa dan KB.
IV. HASIL DAN PEMBAHASAN
4.1. Pola Pelepasan Nitrogen dari Pupuk UZA dan Pupuk Urea Pril Ditinjau dari Laju Konsentrasi Amonium dan Nitrat yang Terbentuk
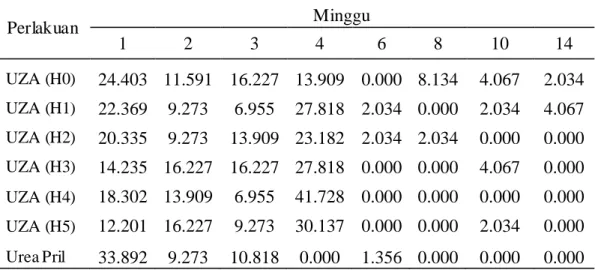
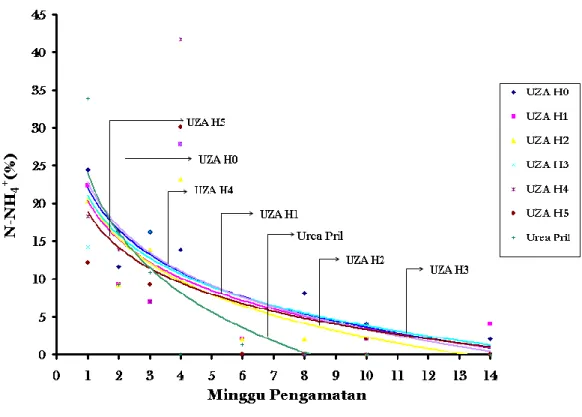
Perbandingan laju pelepasan nitrogen dari pupuk UZA dan pupuk urea pril menjadi amonium selama 14 minggu waktu inkubasi disajikan pada Tabel 2 dan Gambar 7. Dapat dilihat (Tabel 2) bahwa pupuk urea melepaskan nitrogen dalam bentuk amonium lebih banyak bila dibandingkan dengan pupuk UZA. Konsentrasi amonium yang terekstrak dari pupuk urea masih tinggi sampai minggu ke-3. Sedangkan pupuk UZA masih menghasilkan amonium sampai minggu ke-10. Tabel 2. Pelepasan Nitrogen dalam Bentuk N-NH4+ (%) dari Pupuk UZA dan
Pupuk Urea pril selama 14 Minggu Inkubasi
Perlakuan Minggu 1 2 3 4 6 8 10 14 UZA (H0) 24.403 11.591 16.227 13.909 0.000 8.134 4.067 2.034 UZA (H1) 22.369 9.273 6.955 27.818 2.034 0.000 2.034 4.067 UZA (H2) 20.335 9.273 13.909 23.182 2.034 2.034 0.000 0.000 UZA (H3) 14.235 16.227 16.227 27.818 0.000 0.000 4.067 0.000 UZA (H4) 18.302 13.909 6.955 41.728 0.000 0.000 0.000 0.000 UZA (H5) 12.201 16.227 9.273 30.137 0.000 0.000 2.034 0.000 Urea Pril 33.892 9.273 10.818 0.000 1.356 0.000 0.000 0.000 Data pada Tabel 2 juga menunjukkan bahwa pada minggu pertama pupuk urea melepaskan nitrogen dalam bentuk amonium sebanyak 33%, jumlah ini lebih besar bila dibandingkan dengan amonium yang dihasilkan pupuk UZA. Jumlah maksimum amonium yang dapat dihasilkan adalah 100%, namun dari hasil pengamatan amonium yang terekstrak hanya berkisar antara 12%-33% pada minggu pertama. Hal ini menunjukkan bahwa tidak semua amonium langsung dilepaskan ke dalam tanah, sebagian besar amonium masih belum mengalami perubahan bentuk. Pupuk urea (CO(NH2)2) memiliki sumber nitrogen dalam
bentuk NH2.Perubahan pembentukan NH2 menjadi amonium (NH4+) dari pupuk
minggu ke-6. Berbeda dengan urea, pupuk UZA masih menghasilkan amonium rata- rata sampai minggu ke-4, namun pada minggu ke-6 sampai minggu ke-14 pupuk UZA menghasilkan amonium dalam jumlah yang berbeda-beda. Dari kecenderungan yang dapat dilihat dari data hasil pengamatan, bahwa pupuk UZA menghasilkan amonium berbeda-beda sesuai dengan kadar humat dari masing-masing pupuk. Semakin tinggi kadar humat yang diberikan ke dalam pupuk mengakibatkan laju pembentukan amonium semakin cepat. Hal ini dapat dilihat dari amonium yang masih dihasilkan pupuk UZA (H0 dan H1) sampai minggu ke-14 dibandingkan pupuk UZA (H2, H3, H4 dan H5).
Data tersebut (Tabel 2) memperlihatkan peran dari zeolit yang membantu mengikat amonium pada kisi-kisinya sehingga amonium tidak cepat dilepas ke dalam tanah sampai minggu ke-4, sedangkan peran asam humat terlihat dari variasi amonium yang terekstrak pada minggu ke-6 sampai minggu ke-14. Asam humat memiliki pH yang tinggi (berkisar antara 8-11) yang memungkinkan terjadinya proses amonifikasi yang berjalan secara cepat. Laju dari proses amonifikasi salah satunya dipengaruhi o leh pH, pH yang tinggi mempengaruhi laju proses amonifikasi yang juga mempengaruhi proses kehilangan melalui penguapan (Leiwakabessy, 1988).
Pada Gambar 7 dapat dilihat laju perubahan bentuk nitrogen menjadi amonium (NH4+). Grafik tersebut menunjukkan peran dari zeolit dan asam humat
dalam memperlambat laju pelepasan nitrogen dari urea (CO(NH2)2) menjadi
amonium (N H4+). Dapat dilihat bahwa pupuk UZA mampu mengefisiensikan laju
pembentukan amonium yang ditunjukkan oleh pergeseran posisi grafik pupuk UZA sampai minggu ke-14 dibandingkan grafik pupuk urea yang hanya minggu ke-6. Pupuk UZA diharapkan mampu meningkatkan efisiensi pupuk urea dengan mempertahankan jumlah amonium di dalam tanah.
23
Gambar 7. Grafik Pelepasan Nitrogen dalam Bentuk Amonium (%) dari Pupuk UZA dan Pupuk Urea Pril selama 14 Minggu Inkubasi
Zeolit memiliki nilai KTK yang tinggi, yang berguna sebagai pengadsorpsi, pengikat dan penukar kation. Karena memiliki KTK yang tinggi maka semakin banyak jumlah kisi-kisi pertukaran di dalam zeolit, sehingga semakin banyak jumlah NH4+ yang berasal dari formula SRF dan pupuk urea yang
telah mengalami hidrolisis menjadi amonium dapat dijerap oleh kisi-kisinya. Penjerapan NH4+ ini di dalam rongga/kisi-kisi zeolit hanya bersifat sementara dan
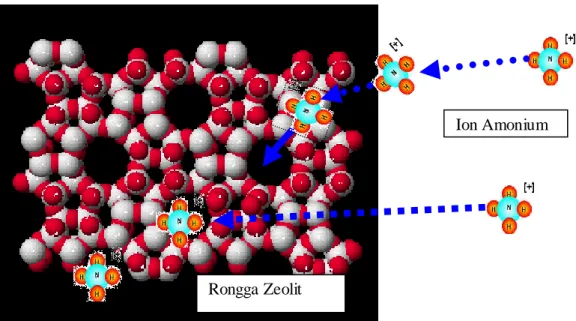
dengan mudah akan diberikan kepada tanaman pada saat diperlukan (Suwardi, 1991). Amonium yang dijerap zeolit tidak segera dilepas ke dalam larutan tanah selama jumlah amonium dalam tanah masih tinggi. Setelah amonium dalam tanah berubah menjadi nitrat, persediaan amonium dalam rongga zeolit dilepaskan ke dalam larutan tanah. Jadi zeolit menghambat proses perubahan amonium menjadi nitrat. Zeolit dapat mencegah terjadinya nitrifikasi karena mineral zeolit dapat menjerap NH4+ pada kisi-kisinya (diameter rongga klinoptilotit 3.9-5.4 Ao
sedangkan diameter NH4+ 1.4 Ao), sehingga bakteri nitrifikasi tidak dapat masuk
karena ukuran tubuh dari bakteri tersebut 1000 kali lebih besar dari diameter rongga zeolit (Alexander, 1977).
Gambar 8. Skema Proses Terjadinya Pengikatan Ion Amonium ke dalam Rongga Zeolit
Proses pembentukan nitrat disebut nitrifikasi yang dilakukan oleh nitrosomonas dalam perubahan amonium menjadi nitrit dan nitrobakter yang berperan dalam perubahan nitrit menjadi nitrat. Dari Tabel 3 dapat dilihat bahwa pupuk urea mengalami perubahan bentuk menjadi nitrat pada minggu pertama sampai minggu ke-3 dalam jumlah yang cukup besar. Pada minggu ke-4 pupuk urea telah mengalami perubahan bentuk menjadi nitrat hampir mencapai 100%. Berbeda dengan urea, pupuk UZA (H0-H5) mengalami perubahan bentuk menjadi nitrat secara lambat sampai minggu ke-14. Jumlah nitrat dari pupuk urea dan pupuk UZA (Tabel 3) sampai angka ± 100% menunjukkan bahwa nitrogen dalam pupuk seluruhnya telah mengalami perubahan pembentukan menjadi nitrat.
Rongga Zeolit
25
Tabel 3. Pelepasan Nitrogen dalam Bentuk N-NO3- (%) dari Pupuk UZA dan
Pupuk Urea Pril selama 14 Minggu Inkubasi
Perlakuan Minggu 1 2 3 4 6 8 10 14 UZA (H0) 48.442 50.039 51.636 64.908 80.318 85.921 97.128 98.529 UZA (H1) 45.248 46.845 48.442 41.093 56.502 62.106 76.115 97.128 UZA (H2) 46.312 47.909 49.506 63.040 78.45 84.053 89.657 97.595 UZA (H3) 50.571 52.168 53.765 45.762 61.172 66.776 72.379 93.392 UZA (H4) 43.118 44.715 46.312 39.225 54.635 60.238 65.842 93.859 UZA (H5) 46.951 48.548 50.145 42.587 57.997 63.600 69.204 90.217 Urea Pril 23.067 48.619 55.007 99.307 65.063 62.262 62.884 60.394 Dari Tabel 3 dapat dilihat juga pupuk UZA mampu mempertahankan keberadaan nitrat hingga minggu ke-14 lebih dari 90% dibandingkan dengan urea yang hanya 60%. Pupuk urea yang telah menghasilkan nitrat pada minggu ke-4 lebih dari 90% telah mengalami kehilangan 30% nitrogen. Kehilangan ini mungkin disebabkan oleh penguapan ataupun terjadi pengikatan oleh KTK tanah maupun asam humat.
Pada minggu pertama jumlah nitrat lebih tinggi jika dibandingkan dengan pupuk UZA, hal ini dipengaruhi oleh jumlah amonium yang dihasilkan pada minggu pertama. Jumlah nitrat dari pupuk urea pril bertambah pada minggu ke-2 (Tabel 3) karena terjadi perubahan bentuk dari amonium yang dihasilkan pada minggu pertama (Tabel 2).
Pada minggu ke-14 nitrat yang dihasilkan oleh UZA (H0), UZA (H1) dan UZA (H2) lebih tinggi jika dibandingkan dengan UZA (H3), UZA (H4) dan UZA (H5). Hal ini juga di pengaruhi oleh produksi amonium sampai minggu ke-14 dari UZA (H0) dan UZA (H1) seperti terlihat pada Tabel 2 yang mampu mempertahankan jumlah nitrat sampai minggu ke-14 (Tabel 3), sedangkan UZA (H2) menghasilkan nitrat yang lebih tinggi daripada UZA (H3), UZA (H4) dan UZA (H5) karena dipengaruhi oleh kadar asam humat.
Dapat dilihat pada Tabel 2 dan 3, terdapat kecenderungan bahwa jumlah amonium dan nitrat belum mencapai 100% sampai minggu ke-10, hal ini karena nitrogen masih diikat dalam bentuk amonium di dalam rongga zeolit untuk sementara waktu dan kemudian akan dilepas pada saat jumlah amonium dalam tanah berkurang.
Gambar 9 menunjukkan konsentrasi nitrat mengalami peningkatan sejalan dengan waktu inkubasi. Dari grafik tersebut dapat dilihat peran dari zeolit dan asam humat dalam memperlambat laju pembentukan amonium (NH4+) yang
secara langsung mempengaruhi laju perubahan amonium menjadi nitrat (NO3-).
Gambar 9. Grafik Pelepasan Nitrogen dalam Bentuk Nitrat (%) dari Pupuk UZA dan Pupuk Urea pril selama 14 Minggu Inkubasi
Gambar 9 juga menunjukkan peran dari zeolit dan asam humat dalam memperlambat perubahan bentuk amonium menjadi nitrat yang dapat dilihat dari peningkatan konsentrasi nitrat yang terjadi secara lambat (slow release) di dalam tanah. Zeolit dan asam humat berperan dalam memperlambat proses pembentukan amonium yang diharapkan dapat memperlambat laju pembentukan nitrat. Amonium merupakan bahan baku untuk proses nitrifikasi maka syarat utama ialah harus tersedia amonium (Leiwakabessy, 1988).
27
4.3. Perubahan pH dan DHL selama Inkubasi, Peningkatan KTK Tanah dan Analisis Akhir Sifat-sifat Kimia Tanah
Secara umum pH tanah menurun sejalan dengan waktu inkubasi. Hal ini terjadi karena penurunan jumlah amonium dan peningkatan jumlah nitrat dalam tanah. Reaksi pembentukan nitrat akan membebaskan H+ yang merupakan sebab terjadinya pengasaman tanah (Leiwakabessy, 1988). Berbeda dengan pH, Nilai daya hantar listrik (DHL) mengalami peningkatan sejalan dengan waktu inkubasi. Perubahan DHL juga tergantung dari proses nitrifikasi dari amonium menjadi nitrat. Nitrat yang merupakan anion dari asam kuat bila berada dalam jumlah yang tinggi dapat menghantarkan listrik yang ditunjukkan dengan nilai DHL yang tinggi.
Nilai KTK tanah juga mengalami peningkatan sejalan dengan waktu inkubasi. Analisis tanah awal menunjukkan nilai KTK tanah berada pada kisaran sedang (19.00 me/100g). Inkubasi selama 14 minggu dengan perlakuan SRF (slow
release fertilizer), analisis tanah akhir menunjukkan bahwa nilai KTK tanah
mengalami peningkatan (berkisar antara 20,174-23,292 me/100g), sedangkan pada perlakuan pupuk urea pril KTK mengalami penurunan (18.707 me/100g). Nilai KTK tanah yang mengalami peningkatan dipengaruhi oleh zeolit dan asam humat yang memiliki KTK yang tinggi.
Hasil analisis kimia tanah awal (Tabel Lampiran 6) menunjukkan bahwa tanah sawah (Inceptisol) yang digunakan dalam percobaan ini mempunyai reaksi tanah yang masam (pH 5.62), C-organik rendah (1.20%), N-Total rendah (0.13%). Kriteria penilaian disajikan pada Tabel Lampiran 2. Analisis tanah sebelum perlakuan pupuk menunjukkan bahwa P-tersedia rendah (6.7 ppm), Ca tinggi (11.66 me/100g), Mg tinggi (2.75 me/100g), sedangkan nilai dari K sangat rendah (0.09 me/100g). Tanah-tanah di daerah tropika basah umumnya mempunyai kandungan Kalium (K) yang relatif rendah.
4.3. Mekanisme Slow Release dari Slow Release Fertilizer Urea-Zeolit-Asam Humat
Pupuk urea (CO(NH2)2) memiliki sumber nitrogen dalam bentuk NH2,
pupuk urea kemudian dilapisi dengan asam humat. Asam humat yang diberikan pada pupuk urea berperan sebagai selimut yang membantu melindungi urea dari penguapan. Hal ini ditunjukkan pada saat urea diberi asam humat, sifat volatile (menguap) dari urea tampak berkurang. Proses perubahan bentuk NH2 dari pupuk
urea melepaskan nitrogen dalam bentuk ion amonium (NH4+). Ion amonium yang
keluar dari lapisan asam humat tidak semua masuk ke dalam rongga zeolit. Amonium yang tidak masuk ke dalam rongga dilepaskan ke tanah.
Gambar 10. Ilustrasi Pelepasan Amonium dari Pupuk Urea-Zeolit-Asam Humat Amonium yang dijerap zeolit tidak segera dilepas ke dalam larutan tanah selama jumlah amonium dalam tanah masih tinggi. Setelah amonium dalam tanah berubah menjadi nitrat, persediaan amonium dalam rongga zeolit dilepaskan ke dalam larutan tanah. Melalui mekanisme slow release ini diharapkan pupuk UZA dalam pengaplikasiannya mampu meningkatkan efisiensi dari pupuk urea serta dapat menekan laju kehilangan nitrogen yang disebabkan oleh volatilisasi, denitrifikasi maupun pencucian. Selain itu, dengan adanya asam humat dalam pupuk UZA diharapkan mampu memperbaiki pertumbuhan tanaman, meningkatkan permeabilitas sel dan kegiatan hormon pertumbuhan (Tan, 1992).
Urea Asam Hu mat Zeolit Campuran Urea-Zeolit-Asam humat Nitrogen lepas dari urea-asa m humat sebagai amoniu m
Ion amoniu m ada yang terikat pada
kisi-kisi zeo lit, ada juga yang di lepaskan ke tanah
Ion Amonium
Ca mpuran Urea-Asam humat
V. KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari hasil penelitian yang telah dilakukan dapat diambil kesimpulan yaitu: 1. Formulasi SRF dalam bentuk UZA dapat memperlambat laju perubahan
amonium menjadi nitrat, sekitar dua minggu bervariasi berdasarkan kadar humatnya.
2. Pupuk UZA mampu mempertahankan keberadaan nitrat hingga minggu ke 14 lebih dari 90% dibandingkan dengan urea yang hanya 60% dari pupuk yang diberikan.
5.2. Saran
Perlu dilakukan penelitian untuk aplikasi pupuk UZA di lapang serta analisis pelepasan nitrogen melalui pengamatan amonium dan nitrat serta faktor-faktor yang mempengaruhi pelepasan nitrogen tersebut sehingga diketahui pengaruh pupuk UZA terhadap pertumbuhan tanaman dan serapan unsur hara lainnya pada tanaman tersebut.
Alexander, M. 1997. Introduction to Soil Microbiology.2nd ed. Jhon Wiley and Sons. Inc. New York.
Astiana, S. 1993. Perilaku Mineral Zeolit dan Pengaruhnya Terhadap Perkembangan Tanah (Disertasi). Program Pasca Sarjana, IPB. Bogor. Astiana dan Wiradinata. 1989. Peranan Zeolit dalam Meningkatkan Produksi
Pertanian. Jurusan Tanah, Fakultas Pertanian, IPB. Bogor.
Buckman, H. O. and N. C. Brady. 1969. The Nature and Properties of Soils. The Mac millan Co. New York.
Gottardi, G. 1978. Mineralogy and Crystal Chemistry of Zeolites. P. 31-44. In Natural Zeolites: Occurrence, Properties, Use (Sand, L. B. and Mumpton, F.A., eds.). Pergamon Press, Oxford, New York.
Leiwakabessy, F. M. 1988. Kesuburan Tanah. Departemen Tanah, Fakultas Pertanian, IPB. Bogor.
Mumpton, F. A. 1984. Natural Zeolites. In W. G. Pond and F. A. Mumpton (eds.) Zeo-Agriculture: Use of Natural Zeolites in Agriculture and Aquaculture. West View Press, Boulder, Colorado.
Nasoetion, A. H 1996. Pengantar ke Ilmu- ilmu Pertanian. Pustaka Literatur Antar Nusa. 133 hal.
Orlov, D. S. 1985. Humus acids of Soils. Oxinion Press. Pvt. Ltd. New Delhi. 387 pp.
Orlov, D. S.1992. Soil C hemistery. Russian Translations Series 92. A.A. Balkema Publisher. Brookfield. 390 pp.
Orlov, D. S. 1995. Humic Substances of Soils and General Theory of Humification. Russian Translation Series III. A.A. Belkema Publisher. Brookfield. 323 pp.
Prasad, R. And S. K. De Datta. 1979. Increasing Fertilizer Nitrogen Efficiency in Wett Land Rice, In Nitrogen and Rice. 1979. IRRI. Los Banos, Laguna, Philippines.
Sanchez, P. A. 1979. Properties and Management of Soil in Tropics. Jhon Wiley and Sons. New York.
31
Situmorang, R. dan U. Sudadi. 2001. Tanah Sawah. Jurusan Tanah. Fakultas Pertanian. Institut Pertanian Bogor. 105 hal.
Soepardi, G. 1983. Sifat dan Ciri Tanah. Departemen Ilmu Tanah, Fakultas Pertanian Bogor, IPB. Bogor.
Suwardi. 1991. The Mineralogical and Chemical Properties of Natural Zeolite and Their Application Effect for Soil Amandement. A Thesis for the Degree of Master. Laboratory of Soil Science. Departemen Of Agriculture Chemistry, Tokyo University of Agriculture.
Suwardi. 1997. Studies on Agricultural Utilization of Natural Zeolite in Indonesia. Dissertation. Graduate School of Agric ulture. Tokyo University of Agriculture.
Suwardi. 2000. Pemanfaatan Zeolit sebagai Media Tumbuh Tanaman Hortikultura. Departemen Tanah, Fakultas Pertanian IPB, Prosiding, Temu Ilmiah IV. PPI. Tokyo, Jepang; 1-3 September 1995.
Suwardi. 2002. Pemanfaatan Zeolit Sebagai Media Tumbuh Tanaman Pangan, Peternakan, dan Perikanan. Makalah Disampaikan pada Seminar Teknologi Aplikasi Pertanian Bogor IPB.
Tan, K. H. 1992. Dasar-dasar K imia Tanah. Edisi ketiga (Terjemahan). Gadjah Mada Univ. Press. Yogyakarta. 295pp.
33
Lampiran 1. Metode Analisis Tanah yang Digunakan dalam Penelitian. Sifat Tanah (Satuan) Metode pH H2O (1:1) Elektrometri
C-Organik (%) Walkey dan Black
N-Total (%) Kjeldhal Amonium-Nitrat (ppm) Destilasi P-tersedia Bray 1 Kandungan basa-basa Ca (me/100g) N NH4OAc pH 7.0 Mg (me/100g) N NH4OAc pH 7.0 K (me/100g) N NH4OAc pH 7.0 Na (me/100g) N NH4OAc pH 7.0 KTK (me/100g) N NH4OAc pH 7.0 Daya Hantar Listrik (DHL) (µS/cm) EC meter
Lampiran 2 : Kriteria Penilaian Data Analisis Sifat Kimia Tanah Menurut Pusat Penelitian Tanah (1983)
Sifat Kimia Tanah Sangat Rendah
Rendah Sedang Tinggi Sangat Tinggi N-Total (%) < 0.1 0.1-0.2 0.21-0.5 0.51-0.75 > 0.75 C-Organik (%) < 1.0 1-2 2.01-3.0 3.1-5.0 > 5 C/N < 5 5-10 11-15 16-25 > 25 P-tersedia (Bray 1.ppm) < 4 5-7 8-10 11-15 > 16 KTK (Me/100g) < 5 5-16 17-24 25-40 > 40 K (me/100g) < 0.1 0.1-0.3 0.4-0.5 0.6-1.0 > 1 Ca (me/100g) < 2 2-5 6-10 11-20 > 20 Mg (me/100g) < 0.3 0.4-1.0 1.1-2.0 2.1-8 > 8 Na (me/100g) < 0.1 0.1-0.3 0.4-0.7 0.8-1 > 1 KB (%) < 20 20-40 41-60 61-80 > 80 Kejenuhan Al (%) < 5 5-10 11-20 21-40 > 40 Reaksi Tanah Sangat Masam Rendah Agak Masam Netral Agak alkalis alkalis pH H2O < 4.5 4.5-5.5 5.6-6.5 6.6-7.5 7.6-8.5 >8.5
35
Lampiran 3 : Hasil Analisis Kandungan Nitrogen (%) Pupuk Urea dan Pupuk UZA
No Jenis Pupuk Kandungan Nitrogen (%) Rata-Rata (%) 1 UZA Humat 0% 25,85 27,035 2 UZA Humat 0% 28,22 3 UZA Humat 1 % 27,31 29,09 4 UZA Humat 1% 30,87 5 UZA Humat 2% 30,58 30,04 6 UZA Humat 2% 29,50 7 UZA Humat 3% 28,79 29,02 8 UZA Humat 3% 29,25 9 UZA Humat 4% 30,54 31 10 UZA Humat 4% 31,46 11 UZA Humat 5% 28,33 28,63 12 UZA Humat 5% 28,93 13 Urea Pril A 40,50 41,735 14 Urea Pril B 42,97