i REFERAT
HALAMAN JUDUL
Diajukan sebagai salah satu persyaratan PPDS 1 Radiologi
GAMBARAN CT PERFUSI PADA STROKE ISKEMIK AKUT
Oleh: dr. Shiska Novalia
Pembimbing: dr. Hesti Gunarti, Sp.Rad
Bagian Radiologi Fakultas Kedokteran Universitas Gadjah Mada
Yogyakarta 2013
ii HALAMAN PENGESAHAN
GAMBARAN CT PERFUSI PADA STROKE ISKEMIK AKUT
Dipresentasikan pada tanggal 19 Desember 2013
Diajukan sebagai salah satu persyaratan PPDS1 Radiologi Fakultas Kedokteran Universitas Gadjah Mada
Pembimbing
dr. Hesti Gunarti, Sp.Rad
Ketua Program Studi PPDS 1 Radiologi FK UGM
Kepala Bagian Radiologi FK UGM
iii DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PENGESAHAN... ii
DAFTAR ISI ... iii
BAB I PENDAHULUAN ... 1
BAB II TINJAUAN PUSTAKA ... 3
A. Sirkulasi Cerebri ... 3 1. Sirkulasi Anterior ... 3 2. Sirkulasi Posterior ... 4 B. Fisiologi ... 4 C. Stroke Iskemik... 5 1. Patogenesis ... 5 2. Patofisiologi ... 5 3. Jaringan Iskemik ... 6
D. Computed Tomography (CT) Scan ... 6
E. CT Perfusi (CTP) ... 7
1. Prinsip CTP ... 7
2. Metode Analisis CTP ... 8
3. Perfusi Cerebri dan Temuan pada CT ... 9
4. Pola Perfusi ... 10
BAB III PEMBAHASAN ... 12
A. Autoregulasi dan Gambaran pada CTP ... 12
B. Stadium Stroke: Patologi dan Temuan pada Pencitraan, Khususnya CT Scan ... 12
1. Stadium Hiperakut: Kurang dari 12 Jam ... 12
2. Stadium Akut: 12 – 24 Jam ... 14
3. Stadium Subakut: 2 Hari – 2 Minggu ... 14
4. Stadium Kronis: 2 Minggu – 2 Bulan ... 15
C. Pitfall pada CTP ... 15 1. Pitfall Teknis ... 15 2. Pitfall Diagnostik ... 16 BAB IV SIMPULAN ... 19 DAFTAR PUSTAKA LAMPIRAN
1 BAB I
PENDAHULUAN
Stroke adalah sindroma yang ditandai oleh onset akut defisit neurologis yang menetap selama minimal 24 jam, menggambarkan keterlibatan fokal dari sistema saraf pusat (central nervous system, CNS), dan merupakan akibat gangguan sirkulasi cerebri. Stroke dihasilkan dari gangguan vaskular yaitu iskemia atau hemoragi. Iskemia merupakan penyebab terbanyak stroke.1
Menurut World Health Organization, sekitar 15 juta orang menderita stroke di seluruh dunia setiap tahun. Lima juta di antara penderita stroke tersebut meninggal dan lima juta lainnya mengalami kecacatan permanen.2
Pada tahun 1990-an terjadi perkembangan pesat penatalaksanaan stroke iskemik. Hasil akhir perawatan ditentukan seberapa cepat reperfusi tercapai, yang tentu saja tergantung pada sedini apa diagnosis dibuat.3
Computed tomography (CT) merupakan modalitas pencitraan yang tersedia luas dan memiliki kemampuan menghasilkan akuisisi gambar dengan cepat.3 Oleh karena itu, CT dapat digunakan untuk membantu diagnosis stroke secara dini. Di samping itu, CT mampu dan dapat dipercaya dalam mengeksklusi perdarahan.3 Namun, pada jam-jam pertama CT mungkin tidak dapat menunjukkan kelainan morfologis pada otak.4 Di sisi lain, ada kebutuhan untuk dapat mengenali dan membedakan lesi yang dapat diselamatkan dengan reperfusi dan lesi yang tidak diselamatkan. Oleh karena itu, pencitraan perfusi sangat penting dalam penatalaksanaan pasien dengan stroke iskemik akut.
Berbagai teknik pencitraan telah digunakan untuk menilai perfusi cerebri, termasuk
positron emission tomography (PET), single photon emission computed tomography (SPECT), xenon computed tomography (CT), dan magnetic resonance (MR) perfusi; namun modalitas ini
2 terhambat oleh ketersediaan yang terbatas, biaya, dan/atau toleransi pasien. CT perfusi (computed tomography perfusion, CTP) telah diperkenalkan sebagai alat yang sederhana dan tepat waktu untuk menilai perfusi cerebri. CTP dapat dilakukan dengan cepat dengan spiral CT
scanner modern dan power injector standar. Peta CTP dapat dihasilkan dengan cepat dan mudah pada workstation yang dilengkapi dengan software yang tepat. Multidetector-row CT scanner
lebih disukai karena memungkinkan peningkatan cakupan anatomis.5 Tujuan penulisan referat ini adalah membahas peran dan interpretasi CTP pada stroke iskemik akut.
3 BAB II
TINJAUAN PUSTAKA A. Sirkulasi Cerebri
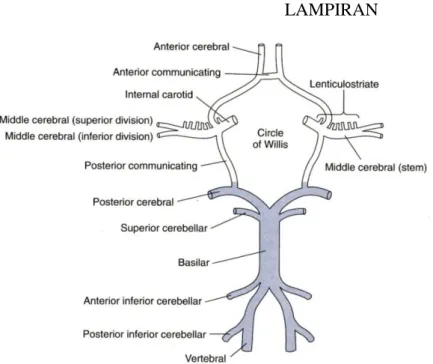
Cerebri mendapat vaskularisasi dari dua sistem sirkulasi arteria, yaitu sirkulasi anterior dari arteria carotis interna, yang kedua sisi terhubung oleh arteria communicans anterior, dan sirkulasi posterior dari sistema arteria vertebralis atau arteria basilaris (Gambar 1).1,4
1. Sirkulasi Anterior
Sirkulasi cerebri anterior, yang memperdarahi sebagian besar cortex cerebri dan
substatia alba subcorticalis, ganglia basalis, dan capsula interna, terdiri dari arteria carotis interna dan cabang-cabangnya: arteria choroidea anterior, arteria cerebri anterior, dan arteria cerebri media. Arteria cerebri media memvaskularisasi pada cabang-cabang lenticulostriata
(Gambar 2). Area vaskularisasi spesifik tiap pembuluh-pembuluh darah ini ditunjukkan pada Tabel 1.1
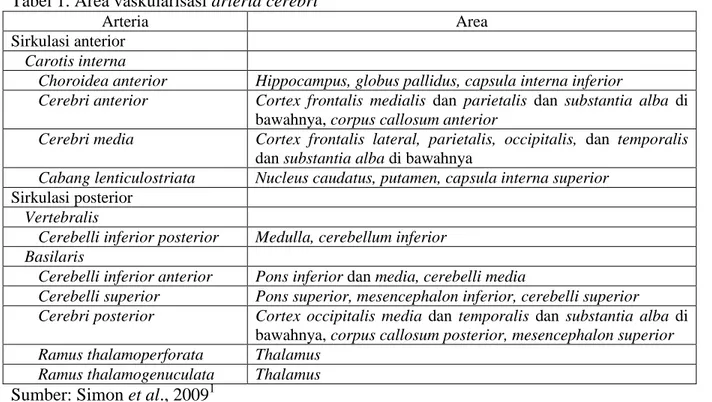
Tabel 1. Area vaskularisasi arteria cerebri
Arteria Area
Sirkulasi anterior Carotis interna
Choroidea anterior Hippocampus, globus pallidus, capsula interna inferior
Cerebri anterior Cortex frontalis medialis dan parietalis dan substantia alba di bawahnya, corpus callosum anterior
Cerebri media Cortex frontalis lateral, parietalis, occipitalis, dan temporalis dan substantia alba di bawahnya
Cabang lenticulostriata Nucleus caudatus, putamen, capsula interna superior Sirkulasi posterior
Vertebralis
Cerebelli inferior posterior Medulla, cerebellum inferior Basilaris
Cerebelli inferior anterior Pons inferior dan media, cerebelli media
Cerebelli superior Pons superior, mesencephalon inferior, cerebelli superior Cerebri posterior Cortex occipitalis media dan temporalis dan substantia alba di
bawahnya, corpus callosum posterior, mesencephalon superior Ramus thalamoperforata Thalamus
Ramus thalamogenuculata Thalamus
4 2. Sirkulasi Posterior
Sirkulasi cerebri posterior memperdarahi medulla oblongata, cerebellum, dan thalamus
dan bagian lobus occipitalis dan temporalis. Sirkulasi ini terdiri dari sepasang arteria vertebralis,
arteria basilaris, dan cabang-cabangnya: arteria inferior posterior cerebelli, arteria inferior anterior cerebelli, arteria superior cerebelli, dan arteria cerebri posterior (lihat Gambar 2).
Arteria cerebri posterior juga memberikan ramusthalamoperforata dan thalamogeniculata.1 B. Fisiologi
Membran neuron dibentuk oleh dua lapis fosfolipid yang mempertahankan voltage gradient melalui membran dengan bantuan ion channel dan ion pumps. Sebagai contoh, pompa natrium-kalium menghasilkan perbedaan potensial tegangan melalui membran 70 mV yang membantu menghasilkan potensial aksi. Mempertahankan ionic gradient merupakan proses yang membutuhkan banyak energi yang memerlukan asupan konstan glukosa dan oksigen pada sel saraf (neuron). Penurunan asupan glukosa dan oksigen akan mempengaruhi potensial listrik dan ion gradient dan kemudian mempengaruhi fungsi sel.3
Istilah “perfusi cerebri” secara tidak langsung menyatakan aliran darah ke otak pada
tingkat jaringan yang dapat digambarkan dengan sejumlah parameter – terutama, cerebral blood volume (CBV), cerebral blood flow (CBF), dan mean transit time (MTT). CBV didefinisikan sebagai volume darah total di suatu volume tertentu dari otak. Volume ini termasuk darah di arteria, arteriola, kapilar, venula, dan vena. CBV memiliki satuan milliliter darah per 100 g jaringan otak. CBF didefinisikan sebagai volume darah yang bergerak melalui suatu volume tertentu otak per satuan waktu. CBF memiliki satuan milliliter darah per 100 g jaringan otak per menit.3,6 MTT didefinisikan sebagai rerata waktu lintas darah melalui regio otak tertentu. MTT ini tergantung pada jarak yang ditempuh antara aliran masuk arterial dan aliran keluar venosa.
5 MTT berhubungan dengan CBV dan CBF tergantung pada prinsip volume sentral, yang dinyatakan dalam MTT = CBV / CBF.3
C. Stroke Iskemik 1. Patogenesis
Dua mekanisme patogenesis dapat menghasilkan stroke iskemik, yaitu trombosis dan embolisme. Trombosis menghasilkan stroke dengan mengoklusi arteria cerebri yang besar (khususnya arteria carotis interna, arteria cerebri media, atau arteria basilaris), arteria kecil yang mempenetrasi (seperti pada stroke lakunar), vena cerebri, atau sinus venosus. Emboli menghasilkan stroke ketika arteria cerebri teroklusi oleh pasase trombus dari jantung, arcus aorta, atau arteria besar pada cerebri ke distal.1
2. Patofisiologi
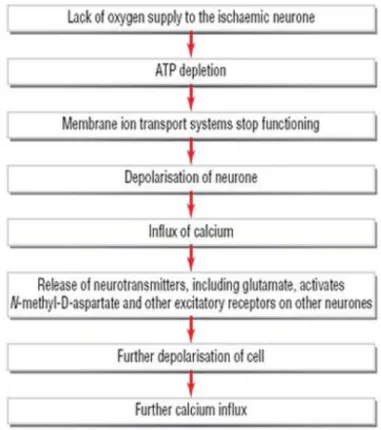
Stroke iskemik akut merupakan hasil dari oklusi vaskular karena penyakit tromboembolik. Iskemia menghasilkan hipoksia sel dan deplesi adenosine triphosphate (ATP) selular. Tanpa ATP, kegagalan energi menghasilkan ketidakmampuan mempertahankan gradien ionik membran sel dan depolarisasi sel. Influks ion natrium dan kalsium dan aliran masuk air ke sel secara pasif, menghasilkan edema sitotoksik. Kemudian depolarisasi sel membawa pada pelepasan glutamate dan radikal bebas, kerusakan mitokondria dan membrane, dan cascade yang membawa pada kematian sel apoptotik.7
Iskemia juga secara langsung menghasilkan disfungsi pembuluh darah cerebri, dengan kerusakan blood-brain barrier dalam 4-6 jam setelah infark. Setelah kerusakan blood-brain barrier, aliran protein dan air ke ruang ekstraselular mengarah pada edema vasogenik. Edema vasogenik menghasilkan pembengkakan otak yang lebih berat dan efek massa yang mencapai
6 puncak pada 3-5 hari dan menghilang beberapa minggu kemudian dengan resorpsi air dan protein.7
Infark menghasilkan kematian astrosit dan juga sel penyokong oligodendroglia dan mikroglia. Jaringan yang mengalami infark secara bertahap mengalami nekrosis likuefaksi dan dihilangkan oleh makrofag dengan perkembangan hilangnya volume parenkimal. Regio densitas rendah menyerupai cairan cerebrospinal dengan batas tegas secara bertahap terlihat, terdiri dari
encephalomalacia dan perubahan kistik. Evolusi perubahan kronis ini dapat terlihat dalam beberapa minggu hingga beberapa bulan setelah infark.7
3. Jaringan Iskemik
Jaringan iskemik dapat secara fungsional terbagi menjadi infarct core yang mengalami kerusakan ireversibel dan penumbra iskemik di sekitarnya. Infarct core merupakan zona sentral jaringan yang mati atau sekarat dalam area iskemik. Di sekitar infarct core adalah jaringan dengan reduksi aliran darah yang lebih ringan yang mungkin dapat diselamatkan dengan reperfusi awal, yang disebut penumbra iskemik, dan jaringan oligemik di perifernya. Tanpa reperfusi, zona infark dapat meluas melibatkan penumbra. Tujuan diagnosis dan terapi stroke iskemik modern terdapat pada mengidentifikasi infarct core dan menentukan apakah ada jaringan yang dapat diselamatkan.7
D. Computed Tomography (CT) Scan
Ada tiga macam teknik pemeriksaan computed tomography (CT) scan dalam pencitraan stroke iskemik, yaitu CT tanpa kontras (non-contrast computed tomography; NCCT), computed tomography angiography (CTA), dan CT perfusi (computed tomography perfusion; CTP). NCCT tetap merupakan uji diagnostik lini pertama untuk evaluasi emergensi stroke akut karena kecepatannya, ketersediaannya pada sebagian besar rumah sakit, dan kemampuannya untuk
7 menggambarkan perdarahan intracranial secara sensitif. Ciri khusus yang sesuai pada penilaian stroke termasuk hipoatenuasi parenkimal fokal (terutama insular ribbon atau lenticular nuclei
untuk infark MCA), oedema cerebri (manifestasi sebagai pendangkalan sulci atau ventriculi), dan tanda MCA hiperdens. Hipoatenuasi parenkimal merupakan temuan paling penting.9-11 CTA memberikan informasi penting pada stroke iskemik akut mengenai lokasi oklusi, panjang segmen arterial yang teroklusi, dan arteria yang mengalami penyangatan di luar oklusi sebagai perkiraan aliran darah kolateral.12 CTP merupakan teknik pencitraan yang memungkinkan penilaian kuantitatif perfusi cerebral secara cepat dan noninfasif dengan menghasilkan peta cerebral blood flow (CBF), cerebral blood volume (CBV), dan mean transit time (MTT). Kunci aplikasi klinis CTP termasuk diagnosis iskemia dan infark cerebral, dan evaluasi vasospasme setelah perdarahan subarachnoid.5
E. CT Perfusi (CTP) 1. Prinsip CTP
Untuk mendapatkan informasi fungsional aliran darah otak, pada PCT bolus cepat bahan kontras intravenosa digunakan pada satu slice, atau pada MSCT beberapa slices, bisa didapatkan berulang-ulang pada interval waktu yang sama. Biasanya, sebagai contoh, 40 ml bahan kontras diberikan dengan periode pemindaian 45 detik dan frekuensi pencitraan 1 gambar/detik.6
Pemeriksaan berdasarkan indikator teori dilusi: setelah pemberian bolus bahan kontras intravenosa densitas sinar X otak meningkat secara temporer (Gambar 4). Kesimpulan mengenai aliran darah otak (cerebral blood flow) dapat diambil dari luas dan perkembangan peningkatan densitas. Dengan menggunakan berbagai algoritma matematis, parameter yang menandakan perfusi cerebri dapat dihitung dan ditampilkan dalam bentuk gambar parameter dengan kode warna.6
8 2. Metode Analisis CTP
Inspeksi visual CTP color map dapat menjadi cara efektif mengidentifikasi area core infarct dan penumbra dan mungkin cukup untuk memandu keputusan intervensi. Inspeksi visual memiliki keunggulan kecepatan dan kesederhanaan penggunaan; namun, teknik kualitatif ini tergantung pada interpretasi pengguna.13
Sebagai tambahan, juga memungkinkan untuk menghitung parameter CTP kuantitatif (Gambar 5). Cara ini terbukti efektif dalam menunjukkan iskemia akut, membedakan jaringan yang dapat diselamatkan dan tidak dapat diselamatkan, dan memprediksi luaran terapi, walau protokol dan panduan untuk ambang kuantitatif bervariasi. Perbedaan hardware dan software
CTP mempengaruhi sistem pengukuran dan penentuan ambang untuk panduan terapi harus distandardisasi. Beberapa penelitian menyarankan penggunaan ambang CBF untuk membedakan area infark adalah CBF < 24 mL x 100 g-1 x min-1. Pada analisis 130 pasien dengan stroke akut. Wintermark et al. dalam Lui et al. menyarankan penggunaan absolute CBV < 2 mL x 100 g-1 untuk menentukan core infarct dan peningkatan MTT > 145% untuk menentukan penumbra. Murphy et al. dalam Lui et al. menunjukkan CBF x CBV sebagai prediktor terbaik untuk membedakan core infarct dan penumbra, lebih baik daripada ambang CBF atau CBV saja. Ambang spesifik juga spesifik untuk program software perfusi yang digunakan dan tidak secara otomatis dapat ditransfer ke vendor, scanner, and bahkan versi software lain. Saat ini banyak upaya dilakukan untuk menstandardisasi metode CTP kuantitatif , yang pada masa depan, diharapkan ada kerja sama dalam pencitraan stroke akut.13
Sebagai alternatif, beberapa peneliti mengusulkan mengadaptasi metode semikuantitatif penilaian visual, dengan menerapkan teknik Alberta Stroke Program Early CT Score (ASPECTS) untuk evaluasi CTP (Gambar 5).14 ASPECTS merupakan teknik yang pada mulanya
9 dibuat untuk menentukan grade pada kondisi sindroma stroke MCA akut pada NCCT dari regio yang divaskularisasi MCA pada 10-point grading system (Gambar 6).15 Saat diterapkan pada CTP, ASPECTS scoring peta parametrik telah terbukti meningkatkan identifikasi perubahan iskemik awal dan memprediksi perluasan infark dan luaran trombolisis dibandingkan dengan NCCT saja. Metode semikuantitatif mudah untuk dilaksanakan, berguna, dan metode analisis yang menjanjikan.13
3. Perfusi Cerebri dan Temuan pada CT
Fungsi neuronal sangat tergantung pada aliran darah dan otak memiliki sistem kontrol yang rumit untuk mempertahankan perfusi cerebri. Sistem autoregulasi ini digambarkan oleh temuan CT pada pasien dengan iskemia cerebri (Tabel 2). Perfusi cerebri normal adalah sekitar 50-60 ml min-1 100g-1. Reduksi ringan perfusi cerebri terkait dengan dilatasi kompensatoris pembuluh darah cerebri. Pada kondisi ini, pengukuran perfusi pada CT tetap normal tapi volume darah dan transit time meningkat. Saat tekanan perfusi jatuh, perfusi tidak dapat dipertahankan pada tingkat normal walaupun terjadi vasodilatasi lebih lanjut. Ketika perfusi jatuh di bawah ambang sekitar 20 ml min-1 100 g-1, metabolisme cerebri mengalami kerusakan yang reversibel. Walaupun begitu, perkembangan jaringan yang iskemik ini menjadi kerusakan yang ireversibel, yaitu infark, terus berlanjut seiring waktu. Kerusakan ireversibel terkait dengan hilangnya vasodilatasi autoregulatoris dan oleh karenanya terjadi berkurangnya volume darah. Oleh karena itu, CT perfusi mampu membedakan iskemia cerebri yang reversibel dan ireversibel tidak hanya dengan menunjukkan berkurangnya perfusi di area infark tetapi juga menunjukkan ketidakcocokan (mismatch) antara perfusi dan volume darah. Berkurangnya perfusi dengan volume darah menetap atau meningkat menandakan iskemia reversible sedangkan reduksi pada perfusi dan volume menandakan infark.17
10 Tabel 2. Rangkuman temuan CT fungsional
Perfusi Volume darah Transit time
Rentang autoregulasi N + + Oligemia (misery perfusion) - ++ ++ Iskemia (kelainan metabolik) - + ++ Ireversibel (nekrosis) -- - -/+
Keterangan: N, normal; +, meningkat; -, menurun Sumber: Miles and Griffiths, 200317
4. Pola Perfusi a. Perfusi normal
Pada kasus perfusi normal (Gambar 7), ada perfusi simetris bilateral dari seluruh parameter CTP. CBF dan CBV lebih tinggi pada substantia grisea daripada substantia alba
karena perbedaan fisiologis normal antara jaringan-jaringan ini.13,18 b. Infark akut
Diagnosis stroke iskemik akut dibuat berdasarkan CTP dengan identifikasi area dengan CBF dan CBV yang menurun, dan MTT dan TTP yang meningkat. Abnormalitas perfusi yang cocok pada peta CBV dan MTT menggambarkan area jaringan otak yang tidak dapat diselamatkan dan kematian neuronal, juga dikenal sebagai “core infarct” (Gambar 8).13,18
Di sisi lain, pada kondisi infark akut, adalah mungkin untuk mendapatkan regio jaringan yang menunjukkan CBF menurun dengan CBV menetap yang menandakan jaringan yang dapat diselamatkan atau penumbra (Gambar 9). Area tersebut juga dapat menandakan MTT memanjang di luar area core infarct dan disebut CBV/MTT mismatch.13,18
Sebagai alternatif pengamatan visual CBV/MTT mismatch, saat ini telah ada pembuatan peta penumbra secara otomatis terkomputerisasi, yang dapat menghasilkan penaksiran core infarct dan regio penumbra secara mudah (Gambar 10). Laporan memudahkan untuk menjangkau intravascular therapeutic window dengan identifikasi penumbra.13
11 c. Hiperperfusi pascaiskemik
Hiperperfusi pascaiskemik mencerminkan restorasi tekanan perfusi pada area
cerebrovascular yang mengalami iskemia berat ke nilai normal atau mendekati normal, baik karena rekanalisasi spontan maupun terapetik. Hiperperfusi setelah iskemia cerebri pada stadium akut awal berpotensi berlangsung singkat dan berhubungan dengan prognosis baik. Sebaliknya, hiperperfusi pascaiskemik yang menetap hingga stadium subakut menandakan prognosis yang kurang baik dan terkait dengan edema yang meningkat dan perdarahan.13
Pada kondisi oklusi pembuluh darah utama yang diikuti dengan rekanalisasi, CBV dan CBF meningkat di distal dari area yang semula iskemik dibandingkan dengan otak kontralateral (Gambar 11). Ketika menginterpretasi CTP pada kondisi sindroma stroke akut, seseorang harus waspada akan fenomena ini. Korelasi dengan riwayat klinis mungkin berguna. Area hiperperfusi setelah kejadian iskemik sebaiknya tidak rancu diidentifikasi sebagai area hipoperfusi kontralateral dan infark akut.13
12 BAB III
PEMBAHASAN
CT perfusi (CTP) menyediakan alat yang cepat dan sederhana untuk mengevaluasi perfusi cerebri pada pasien yang menampilkan gejala stroke akut, yang telah menjalani CT tanpa kontras (NCCT) untuk menyingkirkan perdarahan intracranial. Temuan iskemia
cerebri akut dapat berupa lesi yang samar atau tidak ada pada NCCT. Sebagai tambahan, kedatangan terapi trombolitik untuk stroke nonhemoragik akut telah memperkuat kebutuhan akan tersedianya teknik cepat untuk membantu mengidentifikasi dan menghitung adanya dan luas penumbra iskemik, atau jaringan berisiko. Jaringan berisiko dapat diselamatkan dengan pemberian agen trombolitik, sedangkan ireversibilitas kerusakan infark tidak akan mendapatkan keuntungan dari reperfusi dan dapat meningkatkan risiko perdarahan setelah terapi trombolitik. CTP menyediakan alat yang tepat waktu dan mudah untuk identifikasi
penumbra iskemik, memungkinkan triase cepat pasien yang mungkin dapat diuntungkan dengan reperfusi.5
A. Autoregulasi dan Gambaran pada CTP
Perbedaan antara infark dan penumbra dari data CTP adalah berdasarkan konsep autoregulasi vaskular cerebri. Dalam core infarct, autoregulasi hilang, dan baik MTT maupun CBV rendah; dalam penumbra autoregulasi tetap ada, MTT meningkat tapi CBV dipertahankan atau bahkan meningkat.5
B. Stadium Stroke: Patologi dan Temuan pada Pencitraan, Khususnya CT Scan 1. Stadium Hiperakut: Kurang dari 12 Jam
Temuan pencitraan pada stadium ini terutama untuk mendiagnosis edema sitotoksik. Pada dekade lalu diagnosis stroke hiperakut berdasarkan CT sulit dilakukan. Sekarang, karena resolusi lebih tinggi tersedia pada scanner lebih baru dan kemampuan untuk mengatur
13 adalah memungkinkan untuk menduga diagnosis stroke hiperakut pada CT. Riwayat klinis dan temuan pemeriksaan fisik penting untuk meningkatkan angka deteksi stroke secara bermakna.3
CT dan CT perfusi memiliki peran utama pada diagnosis dan perawatan stroke karena dua alasan utama: ketersediaan dan akuisisi yang cepat. Sebagai tambahan, CT mampu dan dapat dipercaya dalam mengeksklusi perdarahan.3
CT. Tanda awal stroke pada CT disebabkan oleh kandungan air pada area yang mengalami infark yang menyebabkan penyamaran struktur anatomis normal. Tanda ini meliputi hilangnya insular ribbon, penyamaran nucleus lentiformis, hilangnya diferensiasi
substantia grisea dan substantia alba, dan hilangnya sulci (Gambar 12). Perhatikan bahwa tanda awal stroke mungkin tidak terlihat pada CT hingga 8 jam.3
Hyperdense middle cerebral artery (MCA) sign (Gambar 13) merupakan indikator tromboembolisme proksimal dalam MCA (segmen M1) dan merupakan penanda indirek infark akut. Tanda ini memiliki spesifisitas tinggi (~ 100%) tapi sayangnya terlihat hanya pada 17-50% kasus. Densitas tinggi ini desebabkan oleh bekuan intraluminal dengan nilai atenuasi 60-90 HU. Hyperdense MCA sign berhubungan dengan luaran klinis yang buruk karena infark dengan area luas dan terlibatnya peningkatan perdarahan. Diagnosis banding termasuk nilai hematokrit tinggi dan kalsifikasi pembuluh darah, pada keduanya terjadi bilateral. Ketika hiperdensitas terlihat pada cabang MCA (M2, M3) dalam fissura sylvii, hiperdensitas ini disebut “MCA dot sign” dan infark terbatas pada cortex insularis dan cortex frontalis terkait.3
Pencitraan perfusi, khususnya CT perfusi. Tujuan utama pencitraan perfusi adalah untuk mendiagnosis infark dan menghitung ukuran core dan penumbra—untuk
mengidentifikasi ketidakcocokan antara ukuran inti (core) infark (jaringan otak yang ireversibel) dan penumbra iskemik (jaringan yang berpotensi bertahan hidup jika reperfusi).3
14
Penumbra yang ditentukan secara operasional digunakan untuk menggambarkan volume jaringan dalam regio dengan mismatch CBF-CBV pada peta CT perfusi. Regio abnormalitas dengan CBV menggambarkan core jaringan yang mengalami infark, dan
mismatch CBF-CBV pada CT (Gambar 14) menggambarkan regio sekitarnya yang hipoperfusi tapi dapat diselamatkan (penumbra). Jika parameter-parameter ini cocok (CBF-CBV pada CT), jika ini disebut “matched defect” (misal, tidak ada penumbra untuk diobati) (Gambar 15). Beberapa pemeriksaan ditemukan bahwa CBF lebih berguna daripada MTT dalam membedakan bagian-bagian yang berbeda dari penumbra. Peta MTT kurang berguna karena peta ini menampilkan kekacauan sirkulatoris yang tidak diperlukan dalam menggambarkan perubahan iskemik termasuk oklusi pembuluh darah besar dengan kolateralisasi, autoregulasi, dan hiperemia reperfusi setelah revaskularisasi.3
2. Stadium Akut: 12 – 24 Jam
Selama stadium akut, ada peningkatan lebih lanjut edema sitotoksik dan Ca2+ intraselular. Aktivasi sistema enzim (protease, lipase, dan nuclease) dalam rentang yang luas dan produksi radikal bebas oksigen membawa pada kerusakan membran sel, DNA, dan protein neuronal struktural pada akhirnya membawa pada kematian sel. Peningkatan air jaringan menghasilkan menghilangnya kecekungan sulci dan pembengkakan ringan gyri
tanpa efek massa.3
3. Stadium Subakut: 2 Hari – 2 Minggu
Karena kerusakan BBB dan ruptur sel yang mengalami pembengkakan, ada peningkatan cairan ekstraselular (yaitu edema vasogenik). Peningkatan cairan ekstraselular ini berkembang dalam sekitar 18–24 jam dan mencapai puncaknya pada 48–72 jam. Pada fase ini, pencitraan menunjukkan peningkatan edema, efek massa, dan kemungkinan herniasi tergantung pada ukuran dan lokasi infark (Gambar 16).3
15 Transformasi hemoragis mengacu pada perdarahan pada area yang mengalami infark. Insidensi transformasi hemoragis bervariasi terbanyak saat stadium subakut. Beratnya perdarahan dapat berkisar dari sedikit petekia hingga hematoma luas dengan efek massa. Patofisiologi transformasi hemoragis tidak sepenuhnya diketahui. Transformasi hemoragis diduga karena kombinasi cedera vaskular, reperfusi, dan permeabilitas yang berubah.3
4. Stadium Kronis: 2 Minggu – 2 Bulan
Stadium kronis mulai dengan pemulihan BBB, teratasinya edema vasogenik, dan pembersihan dari jaringan nekrotik. Secara patologis dan pencitraan, fase ini ditandai oleh atrofi otak lokal, gliosis, pembentukan cavitas, dan dilatasi ex vacuo dari ventriculus yang terkait. Pada dasarnya, ada kehilangan jaringan otak dan fungsi yang terkait.3
C. Pitfall pada CTP 1. Pitfall Teknis
Pitfall teknis dapat terjadi pada penentuan slice atau pada arterial input function
(AIF) dan venous output function (VOF). Sebagian besar protokol menggunakan potongan
axial melalui ganglia basalis untuk menampilkan area yang divaskularisasi MCA. Protokol seperti demikian dapat menghasilkan eksklusi area perfusi abnormal (Gambar 17). Untuk mengevaluasi iskemia sirkulasi posterior, protokol harus disesuaikan untuk mencakup bagian lebih bawah (Gambar 18). Kewaspadaan harus dilakukan dalam menampilkan volume otak yang tepat terkait sindroma klinis.13
Ketersediaan AIF dan VOF yang cukup diperlukan untuk mendapatkan peta CTP yang valid. Pada kasus seperti bolus kontras yang suboptimal, aritmia jantung, penyempitan vaskular yang berat, atau emboli intracranial multipel, kurangnya aliran yang adekuat dalam pembuluh darah circulus Willisii dapat menghalangi penghitungan peta CTP diagnostik (Gambar 19). Serupa dengan hal tersebut, ROI venous outflow yang buruk juga dapat menjadi
16 masalah (Gambar 20). Masalah teknis dapat menghasilkan gambaran yang menyerupai hipoperfusi global.13
ROI arterial dan venosa dan nilai cutoff sebelum dan sesudah penyangatan dipilih dari CTP source imaging untuk membuat kurva waktu-atenuasi dari arterial input dan venous outflow yang tepat, yang kemudian digunakan untuk menghitung parameter CTP. AIF biasanya diperoleh dari segmen A2 ACA. Karena ia berjalan tegak lurus terhadap bidang axial, segmen A2 ACA terlihat pada beberapa gambar, dan mudah untuk melatih teknisi untuk menemukan pembuluh darah ini. Pada dasarnya, arteria lain juga dapat digunakan sebaik ICA dan MCA. Bahkan cabang arteria carotis externa juga dapat digunakan sebagai wakil AIF dan telah menunjukkan korelasi yang baik dengan ACA. Venous outflow sering diperoleh dari salah satu sinus venosus dural (Gambar 20) penempatan ROI yang tidak tepat mempengaruhi penilaian CTP baik secara visual maupun kuantitatif.13
2. Pitfall Diagnostik a. Infark kecil dan kronis
Peta CTP yang dihitung relatif memiliki resolusi yang rendah. Infark kecil dapat terlewatkan; walaupun, lesi ini dapat sangat symptomatic ketika terdapat di area yang memiliki peran pada banyak fungsi (Gambar 21).13
Area infark kronis sering kali nyata pada NCCT; namun, tampilan perfusi infark kronis dapat membingungkan. Pemeriksaan dengan pencitraan nuklir menunjukkan sebagian besar jaringan di regio infark kronis menampilkan derajat metabolisme dan CBF rendah namun persisten. Ada perfusi menetap pada sel-sel glial dan neuronal yang tersisa dalam parenkima otak yang mengalami gliosis, membawa pada perfusi yang menurun tapi persisten dan dapat diukur (Gambar 22). Adalah penting untuk menginterpretasi CTP dengan mengkaitkannya dengan NCCT dan riwayat klinis untuk menghindarkan misinterpretasi
17 infark kronis sebagai lesi yang baru. Area infark akut yang berada di dekat infark lama mungkin sulit untuk diidentifikasi.13
b. Iskemia mikrovaskular
Regio iskemia mikrovaskular kronis banyak dijumpai pada pasien dengan faktor risiko cerebrovascular dan sering ditemukan pada interpretasi CTP. Reduksi CBF pada pareknima otak yang dipengaruhi oleh penyakit substantia alba telah ditunjukkan dengan menggunakan berbagai modalitas, dan CTP menyokong temuan ini. Ketika perubahan mikrovaskular asimetris, berpotensi disalahartikan sebagai regio iskemia akut (Gambar 21).13 c. Stenosis ekstrakranial dan intrakranial
Asimetri perfusi pada kondisi stenosis sulit dievaluasi. Hipoperfusi cerebri dapat dihasilkan dari berbagai etiologi ektrakranial, termasuk stenosis arteria carotis ekstrakranial, stenosis intrakranial proksimal, dan cerebrovascular steal syndromes. Area poststenotic dapat menyerupai atau menyebabkan perkiraan luas area yang berlebihan dari penumbra iskemik akut. Oleh karena itu, evaluasi pembuluh darah dengan CTA secara bersamaan harus dilakukan secara rutin (Gambar 23).13
d. Penilaian cerebrovascular reserve
Regio poststenotic dapat lebih lanjut dievaluasi dengan menggunakan CTP dengan uji acetazolamide untuk menilai cerebrovascular reserve. Stenosis atau oklusi vaskular menyebabkan tekanan perfusi distal menurun. Derajat stenosis tidak secara tepat memprediksi hemodynamic compromise. Ada mekanisme lain yang mungkin mengkompensasi, termasuk sirkulasi kolateral dan refleks vasodilatasi autoregulatoris. Pada pasien dengan lesi stenotik, peta CTP dasar tidak berperan dalam memprediksi
cerebrovascular reserve; tetapi, perubahan pada CBF dan MTT setelah uji acetazolamide berkorelasi dengan hemodynamic reserve (Gambar 24). Regio yang menunjukkan perubahan mencolok pada MTT setelah acetazolamide harus dipertimbangkan sebagai area berisiko.13
18 e. Vasospasme
Vasospasme berat berkorelasi dengan abnormalitas CTP sementara. Abnormalitas yang ditemukan terutama adalah MTT memanjang dan CBF menurun.13
f. Kejang
Kejang dapat menjadi dilema diagnostik karena status epilepticus dan postictal paralysis mirip dengan stroke akut, dan pada komplikasi lebih lanjut, kejang dapat menampilkan gejala stroke kortikal. CTP mungkin menunjukkan ictal area hiperperfusi (Gambar 25). Dengan interpretasi peta warna secara visual. Peta ini dapat disalahartikan sebagai area iskemia kontralateral.13
19 BAB IV
SIMPULAN
CT perfusi (CTP) unggul dalam pengidentifikasian lesi iskemik (penumbra) dan infark (core infarct) pada stroke fase hiperakut (kurang dari 12 jam). Pada infark autoregulasi telah hilang sehingga gambaran core infarct pada CTP adalah abnormalitas pada semua parameter (match), yaitu cerebral blood flow (CBF) dan cerebral blood volume (CBV) menurun dan mean transit time (MTT) memanjang. Pada iskemik autoregulasi masih ada sehingga gambaran
penumbra pada CTP adalah abnormalitas parameter yang mismatch, yaitu penurunan CBF, MTT memanjang, sedangkan CBV menetap atau bahkan meningkat. Pitfall dalam diagnosis yang sering dijumpai adalah infark kronis, stenosis vaskular, perubahan substantia alba kronis, kejang, dan vasospasme. Pitfall teknis antara lain dalam pemilihan slice dan pemilihan pemilihan ROI pascapemrosesan.
20 DAFTAR PUSTAKA
1. Simon RP, Greenberg DA, and Aminoff MJ. Chapter 9, Stroke. In: Simon RP, Greenberg DA, and Aminoff MJ. Clinical Neurology. 7th ed. New York: Lange Medical
Books/McGraw-Hill; 2009. pp 292-327.
2. Stroke Statistics [internet]. The Internet Stroke Center; © 1997-2013. [cited 2013 Dec 4]. Available from: http://www.strokecenter.org/patients/about-stroke/stroke-statistics/
3. Kanekar SG, Zacharia T, and Roller R. Imaging of Stroke: Part 2, Pathophysiology at the Molecular and Cellular Levels and Corresponding Imaging Changes. Am J Roentgenol. 2012; 198:63–74.
4. Grumme T, Kluge W, kretzchmar K, and Roesler A. Chapter 7, Vascular Diseases. In: Grumme T, Kluge W, kretzchmar K, and Roesler A. Cerebral and Spinal Computed Tomography. 3rd ed. Berlin: Blackwell Science; 1998. pp 94-116.
5. Wintermark M. Chapter 9, Cerebral Perfusion CT: Technique and Applications. In: Reiser MF, Becker CR, Nikolau K, Glazer G, editors. Multislice CT. 3rd Revised Edition. Berlin: Springer; 2009. p.111-21.
6. Wiesmann M. CT Perfusion of the Brain: The Basics of the Method and Interpreting Images. Visions 9.06. [cited: 2011 Apr 18]. Available from: http://www.visions-journal.com/GB-2006-V09/S06-08.pdf
7. Velayudhan V. Stroke Imaging. Medscape [homepage in the internet]. New York: Web MD LLC © 1994-2013 [updated 2012 Dec 5; cited 2013 Sept 30]. Available from:
http://emedicine.medscape.com/article/338385-overview#showall
8. Carroll KAL and Chataway J. Understanding stroke: Pathophysiology, presentation, and investigation. studentBMJ. 2006;14:309-52.
9. Lev MH, Farkas J, Gemmete JJ, Hossain ST, Hunter GJ, Koroshetz WJ, et al. Acute Stroke: Improved Nonenhanced CT Detection—Benefits of Soft-Copy Interpretation by Using Variable Window Width and Center Level Settings. Radiology. 1999;213:150–5. 10.Thurrnher M. Brain Ischemia – Imaging in Acute Stroke. Radiology Assistant [homepage
in the internet]. [updated 2008 June 30; cited 2013 Nov 14]. Available from:
http://www.radiologyassistant.nl/en/p483910a4b6f14/brain-ischemia-imaging-in-acute-stroke.html
11.von Kummer, Borquain H, Bastianello S, Bozzao L, Manelfe C, Meier D, et al. Early Prediction of Irreversible Brain Damage after Ischemic Stroke at CT. Radiology. 2001;219:95-100.
12.Knauth M, von Kummer R, Jansen O, Hähnel S, Döfler A, and Sartor K. Potential of CT Angiography in Acute Ischemic Stroke. Am J Neuroradiol. 1997;18:1001–10.
13.Lui YW, Tang ER, Allmendinger AM, and Spektor V. Evaluation of Perfusion in the Setting of Cerebral Ischemia: Patterns and Pitfalls. Am J Neuroradiol. 2010;31:1552–63. 14.Aviv RI, Mandelcorn J, Chakraborty S, Gladstone D, Malham S, Tomlinson G, et al.
Alberta Stroke Program Early CT Scoring of CT Perfusion in Early Stroke Visualization and Assessment. Am J Neuroradiol. 2007;28:1975-80.
15.Pexman JHW, Barber PA, Hill MD, Sevick RJ, Demchuk AM, Hudon ME, et al. Use of Alberta Stroke Program Early CT Score (ASPECTS) for Assessing CT Scans in Patients with Acute Stroke. Am J Neuroradiol. 2001;22:1534-42.
21 16.Alberta Health Services [homepage in the internet]. Calgary: Faculty of Medicine, University of Calgary [cited 2013 Dec 6]. Available from:
http://www.aspectsinstroke.com/aspects/what-is-aspects/.
17.Miles KA and Griffiths MR. Perfusion CT: a worthwhile enhancement? Br J Radiol. 2003;76:220-31.
18.Allmendinger AM, Tang ER, Lui YW, and Spektor V. Imaging of Stroke: Part 1, Perfusion CT—Overview of Imaging Technique, Interpretation Pearls, and Common Pitfalls. Am J Roentgenol. 2012; 198:52–62.
22 LAMPIRAN
Gambar 3. Arteria dari sirkulasi cerebrianterior (putih) dan posterior (biru) dalam hubungannya dengan circulus Willisii
Sumber: Simon et al., 20091
Arteria cerebri anterior Arteria cerebri media Arteria cerebri posterior Arteria cerebelli Arteria choroidea anterior Arteriae lenticulostriata Arteria choroidea posterior Arteria basilaris Gambar 2. Area vaskularisasi arteriae cerebri. Tiap area dapat bervariasi dalam rentang tertentu.
23 Gambar 3. Ischemic cascade
Sumber: Carroll and Chataway, 20068
Gambar 4. Kurva waktu/densitas setelah injeksi bolus bahan kontras pada CTP.
Rangkaian densitas diukur pada pembuluh darah arterial (ramus media arteria cerebri: biru), pembuluh darah venosa (confluens sinum: kuning) dan di parenkima cerebri (thalamus: merah). Perhatikan perkembangan yang berurutan antara kurva waktu/densitas arterial dan venosa; dan rangkaian mendatar dan perubahan densitas sedikit lambat pada parenkima dibandingkan dengan kurva arterial.
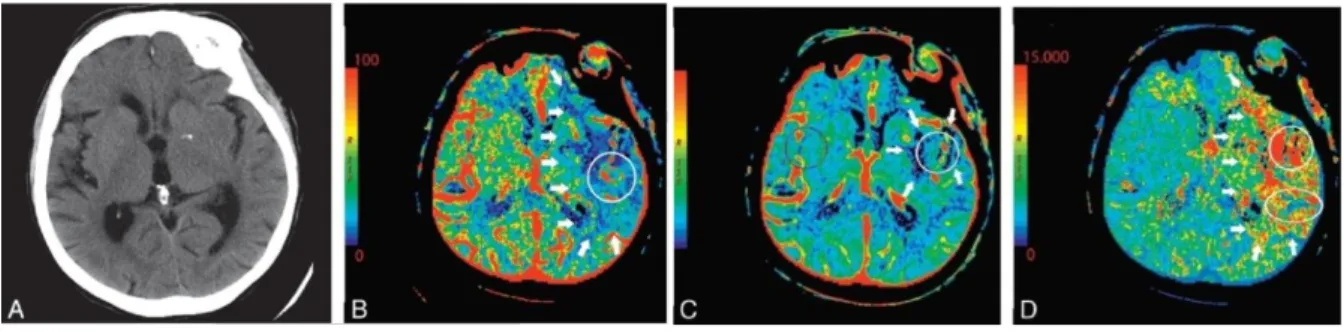
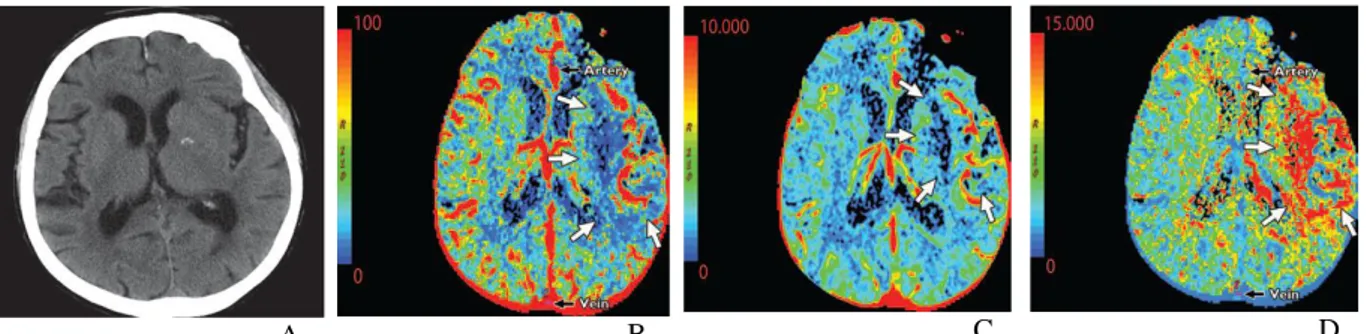
24 Gambar 5. Laki-laki 76 tahun dengan gejala sisi kanan akut. A, NCCT normal. CTP menunjukkan stroke MCA kiri yang luas dengan penumbra. B, peta CBF dan D peta MTT menunjukkan aliran MTT yang menurun dan memanjang pada sebagian besar area vaskularisasi MCA kiri (panah) dengan CBF (10 mL 100 g-1 min-1). C, pada peta CBV, ada regio dengan perfusi menurun pada ganglia basalis sinistra saja (panah). kondisi ini menunjukkan CBV/MTT mismatch atau penumbra iskemik. CBV pada sisi iskemik 0,6 mL x 100 g-1. MTT relatif pada sisi iskemik 500% meningkat dalam core dan 200 % meningkat pada penumbra dibandingkan dengan otak kontralateral yang homolog.
Sumber: Lui et al., 201013
Gambar 6. 10 poin yang dinilai pada Alberta Stroke Program Early CT score (ASPECTS) Sumber: Alberta Health Services, 201316
25
A B C D
Gambar 7. Laki-laki sehat dengan 53 tahun.
CT scan tanpa kontras (A) dan peta CT menunjukkan cerebral blood flow (B), cerebral blood volume (C), dan
mean transit time (D) menunjukkan perfusi otak simetris normal. Seluruh peta warna diberi kode merah untuk nilai tinggi dan biru untuk nilai rendah.
Sumber: Allmendinger et al., 201218
A B C D
Gambar 8. Wanita 88 tahun dengan kelumpuhan wajah sisi kanan dan afasia.
A, CT scan tanpa kontras menunjukkan tidak ada area perfusi abnormal yang menandakan infark akut.
B-D, peta CT perfusi menunjukkan cerebral blood flow (B), cerebral blood volume (CBV) (C), dan mean
transit time (MTT) (D) menggambarkan area luas dengan defisit yang cocok pada peta CBV dan MTT (panah)
yang menandakan inti (core) infark pada area yang divaskularisasi arteria cerebri media sinistra. Seluruh peta
warna diberi kode merah untuk nilai tinggi dan biru untuk nilai rendah.
Sumber: Allmendinger et al., 201218
A B C D
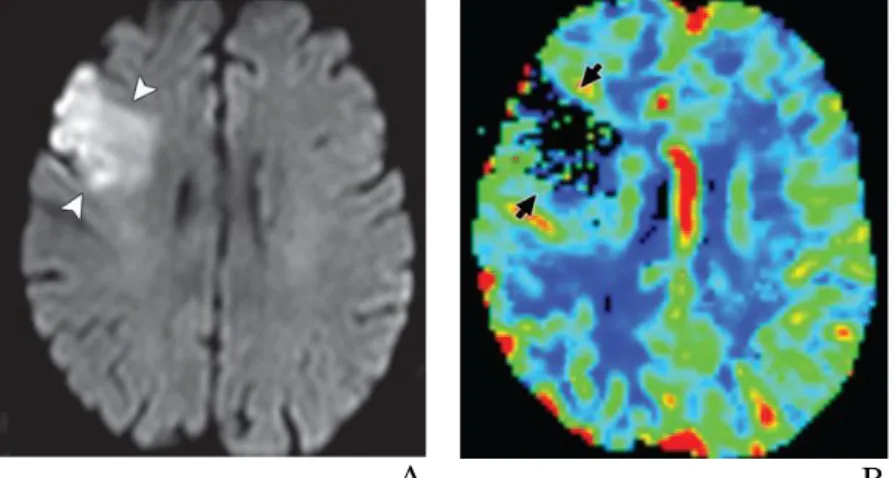
Gambar 9. Laki-laki 51 tahun dengan kelumpuhan wajah kanan dan afasia akut. A, CT scan tanpa kontras menunjukkan tidak ada bukti infark akut.
B, pada peta CT perfusi tampak cerebral blood flow menampilkan regio dengan perfusi yang menurun di area yang divaskularisasi arteria cerebri media (MCA) (panah). Seluruh peta warna diberi kode merah untuk nilai tinggi dan biru untuk nilai rendah.
C, pada peta CT perfusi tampak cerebral blood volume menunjukkan aliran darah yang relatif simetris. Seluruh area yang divaskularisasi MCA di sini menunjukkan area penumbra
iskemik.
26 Gambar 10. Survey CT modern pada pasien laki-laki 57-tahun dibawa ke ruang gawat darurat dengan hemisindroma sinistra, termasuk CT tanpa kontras (baris pertama), CT perfusi (baris 2 hingga 5) dan CT angiogram (CTA) (kolom kanan). CT tanpa kontras menyingkirkan perdarahan cerebri. Dari data kasar CT perfusi, tiga peta parametrik diperoleh, yang berhubungan dengan mean transit time (MTT, baris kedua), cerebral blood flow (CBF, baris ketiga), dan cerebral blood volume (CBV, baris keempat),penerapan konsep autoregulasi vaskular cerebri membawa pada peta prognostik (baris kelima), yang menggambarkan infark pada merah dan penumbra pada hijau, penumbra merupakan target terapi reperfusi akut. CTA mengidentifikasi oklusi pada M1-M2 junction (panah) sebagai asal gangguan hemodinamik yang ditunjukkan CT perfusi. CTA juga menyatakan plak atheromatosa terkalsifikasi pada
bifurcatiocarotis dextra (kepala panah). Sumber: Wintermark, 20095
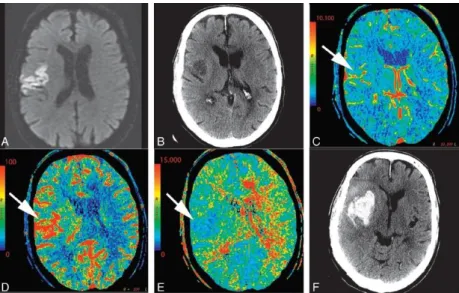
27 Gambar 11. Laki-laki 74 tahun yang dibawa ke instalasi gawat darurat setelah jatuh dengan kelemahan sisi kiri. Temuan CT awal normal (tidak ditunjukkan). A, DWI sequence diperoleh 2 hari kemudian menunjukkan infark akut/subakut. B, beberapa jam kemudian, pasien mendapatkan gejala baru di kontralateral, yang menyebabkan dilakukannya pemeriksaan CTP ini. CT tanpa kontras saat itu menunjukkan infark right frontal opercular. C-E, CT perfusi menunjukkan perfusi asimetris dengan CBV relative meningkat (C), CBF meningkat (D), dan MTT menurun (E) pada regio ini dibandingkan dengan otak kontralateral. Temuan ini konsisten dengan hiperperfusi pascaiskemik. F, hari berikutnya, gejala pasien makin parah, dan CT scan tanpa kontras follow up menunjukkan perdarahan pada regio infark subakut.
Sumber: Lui, 201013
Gambar 12. Wanita usia 61 tahun dengan kelemahan sisi kiri. CT scan otak tanpa kontras menunjukkan hipodensitas di area yang divaskularisasi arteria cerebri media dextra (panah putih), menghilangnya kecekungan sulci, dan hilangnya diferensiasi substantia grisea-alba. Ada pengaburan caput nucleus dextra (kepala panah putih) dan sebagian hipoatenuasi putamen dextra (kepala panah hitam). Perhatikan insular ribbon yang hiperdens (panah hitam) di sisi kiri.
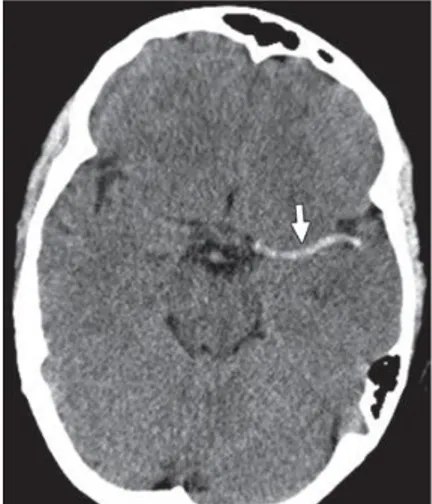
28 Gambar 13. CT scan tanpa kontras dari laki-laki 61 tahun dengan hemiplegia dextra menunjukkan trombus hiperdens pada segmen M1 dari arteria cerebri media (middle cerebral artery (MCA) sinistra. Temuan ini disebut sebagai dense MCA sign.
Sumber: Kanekar et al., 20123
A B C D
Gambar 14. Stroke hiperakut dengan pola penumbra pada laki-laki 56 tahun.
A-C, Gambar cerebral blood flow (CBF) (A), cerebral blood volume (CBV) (B), dan mean transit time (MTT) (C) dari CT perfusi menunjukkan area dengan mismatch antara CBF dan CBV, yang diduga penumbra. Area dengan CBV yang tereduksi (oval putih, B) pada daerah yang divaskularisasi arteria cerebri media (MCA) sinistra lebih kecil daripada defek terkait yang lebih besar pada CBF (kepala panah, A dan C). Penumbra = CBF – CBV. Ada jaringan yang dapat bertahan hidup dan pasien akan mendapat manfaat dari terapi trombolitik.
D, Diffusion-weighted image irisan aksial yang diperoleh 24 jam setelah CT perfusi menunjukkan area dengan difusi berkurang yang terbatas pada nucleus lentiformis dan bagian
lobus frontotemporalis. Sumber: Kanekar et al., 20123
29
A B
Gambar 15. Stroke hiperakut tanpa penumbra pada laki-laki 57 tahun dengan kelemahan sisi kiri yang mulai 3 jam lebih awal. A dan B, Gambar diffusion-weighted irisan aksial (A) dan
cerebral blood flow (CBF) (B) dari MRI perfusi menunjukkan area dengan difusi berkurang (kepala panah, A) pada lobus frontalis dextra dengan matched defect dari perfusi menurun (panah, B) pada CBF—yang, tidak ada penumbra.
Sumber: Kanekar et al., 20123
Gambar 16. Infark subakut pada laki-laki 66 tahun.
CT scan otak tanpa kontras menunjukkan hipodensitas (kepala panah) pada daerah yang divaskularisasi arteria cerebri media (MCA) dextra dengan hilangnya diferensiasi substantia grisea – substantia alba dan menghilangnya kecekungan sulci dengan efek masa di sekitar parenkima otak dan ventriculus lateralis ipsilateral.
30 Gambar 17. Laki-laki 58 tahun dengan hemiparesis kiri akut dan suspek acute right MCA syndrome. A, CTP saat masuk menunjukkan perfusi simetris dan normal; gambar CBV. B, infark akut tampak pada DWI di luar volume yang digambarkan pada CTP.
Sumber: Lui et al., 201013
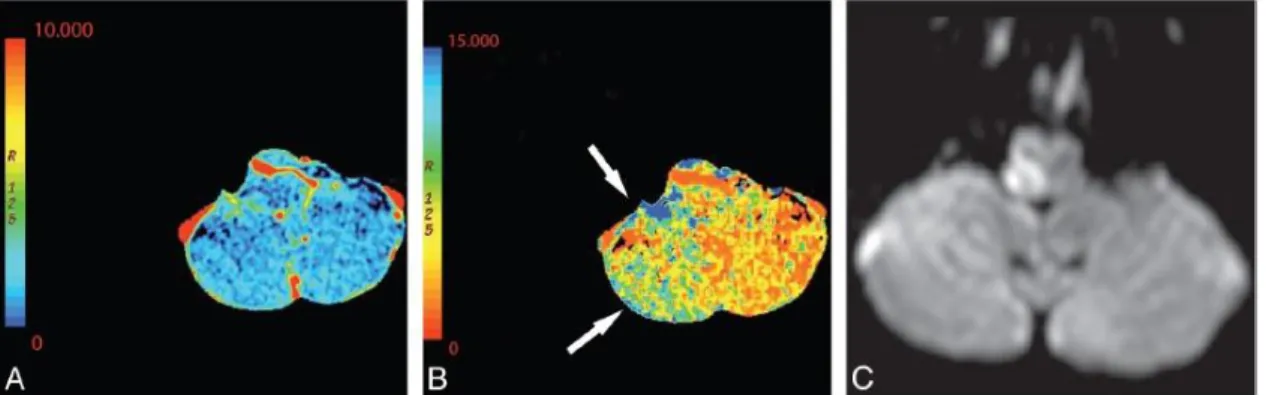
Gambar 18. Laki-laki usia 61 tahun dengan Wallenberg syndrome kanan akut. Peta CBV (A) dan MTT (B) diperoleh di setinggi fossa posterior menunjukkan area penumbra iskemik di area arteria cerebelli posterior inferior dextra (panah); pada gambar ini MTT ditunjukkan dalam skema gambar yang dibalik. C, DWI mengkonfirmasi infark medullaris lateral dextra
dengan penumbra hemispherium inferior cerebelli dextra. Sumber: Lui et al., 201013
Gambar 19. Perempuan 55 tahun dengan hemiparesis kiri dan temuan normal pada CT kepala. A, CTP source image menunjukkan opasifikasi kontras yang buruk di ACA kanan (panah). Biasanya segmen A2 ACA dapat digunakan untuk penempatan AIF. Pada kasus ini, ada ketidakcukupan dan menghasilkan peta CTP yang tidak diagnostik. B, CBV ditampilkan sebagai contoh.
31 Gambar 20. A, pemilihan ROI venosa yang tidak tepatmenghasilkan tampilan CBV menyerupai hipoperfusi global. Pada gambar berikut (B dan C), dengan peletakan ROI yang benar, menunjukkan perfusi normal simetris. B, Contoh penempatan ROI AIF dan VOF yang tepat pada ACA dan sinus sagittalis superior. C, Temuan normal pada CBV.
Sumber: Lui et al., 201013
Gambar 21. Perempuan 58 tahun dengan kelemahan sisi kiri. NCCT (A) menunjukkan perubahan iskemik mikrovaskular periatrial kiri (panah) sesuai dengan abnormalitas peta perfusi CBF (B), CBV (C) dan MTT (D) (panah). Infark yang berlokasi strategis dapat memiliki gejala yang nyata walau kecil dan sulit dideteksi. Tidak ada perfusi yang asimetris yang luas terdeteksi pada regio capsula interna interna. E, DWI yang dilakukan pada hari yang sama menunjukkan infark kecil akut di crus posterior capsula interna dextra.
32 Gambar 22. Perempuan 44 tahun dengan riwayat kelainan ansietas memiliki gejala kelemahan wajah kanan dan afasia. Tidak diketahui adanya riwayat stroke sebelumnya. CTP menunjukkan area fokal hipoperfusi di lobus frontalis sinistra dalam area infark yang tampak kronis (panah). infark kronis terukur walau perfusi minimal. Area infark akut di dekat infark kronis mungkin sulit terdeteksi. NCCT (A), CBF (B), CBV (C) saat masuk rumah sakit; DWI (D) 1 hari setelahnya.
Sumber: Lui et al., 201013
Gambar 23. Laki-laki 76 tahun dengan perubahan status mental, temuan NCCT normal (tidak ditunjukkan). CBF menurun (A) dan MTT memanjang (C) di area vaskularisasi MCA dan ACA kanan dengan CBV normal (B). CTA menampilkan stenosis ICA kanan yang berat (panah) (D).
33 Gambar 24. Perempuan usia 54 tahun dengan pusing dan kelemahan sisi kanan. A, NCCT menunjukkan tidak ada kelainan. B, coronal MIP dari CT angiography menunjukkan M1 dari MCA kiri yang berat dan pembuluh darah kolateral yang prominen (panah). C-H CTP sebelum dan setelah pemberian acetazolamide: gambar CBF sebelum (C) dan sesudah (D), CBV sebelum (e) dan sesudah (F), MTT sebelum (G) dan sesudah (H). teknik dan pembuatan skala gambar sebelum dan setelah pemberian acetazolamide identik. Ada peningkatan bihemisferik pada CBF dan CBV setelah pemberian acetazolamide; namun, ada peningkatan perfusi asimetris antara area poststenotic (kiri) dan nonstenotic (kanan) seperti yang terlihat pada ROI oval. Kondisi ini paling jelas terlihat pada MTT memanjang setelah acetazolamide pada bagian area MCA kiri relatif terhadap CTP scan awal.
Sumber: Lui et al., 201013
Gambar 25. Laki-laki usia 55 tahun dengan perubahan status mental, kelumpuhan wajah kanan, kelemahan anggota gerak kanan atas, dan kejang generalized tonic-clonic. Temuan pada NCCT (tidak ditunjukkan) dan DWI (A) normal. CBV menunjukkan hipoperfusi di
hemispherium sinistra, menyerupai core infarct (B). Pemeriksaan electroencephalography
dan PET (tidak ditampilkan) kemudian menunjukkan focus kejang hemisferik kanan, menyokong CTP hipoperfusi ictal terkait kejang daripada hipoperfusi relative terkait infark hemisferik kiri. Gejala pasien teratasi.