KLASIFIKASI UNSUR- UNSUR DALAM TABEL PERIODIK
KLASIFIKASI UNSUR- UNSUR DALAM TABEL PERIODIK UNSUR UNSUR I.PENDAHULUAN
I.PENDAHULUAN Bebera
Beberapa pa unsuunsur r telah sejak telah sejak lama menjadi bagian lama menjadi bagian kehidkehidupan manusiupan manusia.a. Dalam ilmu kimia kita mempelajari lebih dari 100 unsur di alam. Setiap unsur Dalam ilmu kimia kita mempelajari lebih dari 100 unsur di alam. Setiap unsur memili
memiliki ki sifat-ssifat-sifat ifat yang khas, yang khas, disamdisamping itu ping itu terdapterdapat at pula unsur-unpula unsur-unsur yangsur yang mem
memilikiliki i kemkemiripiripan-kan-kemiemiripripan. an. OleOleh h karkarena ena jumjumlah lah ununsur sur cukcukup up banbanyakyak,, maka perlu diklasifikasikan kedalam golongan-golongan berdasarkan maka perlu diklasifikasikan kedalam golongan-golongan berdasarkan per
persamsamaan aan sifsifat-sat-sifaifatnytnya. a. SifSifat-sat-sifat ifat unsunsur ur yanyang g berberagaagam m mismisalnalnya ya wujwujudud uns
unsur ur daldalam am suhsuhu u kamkamar ar ada ada yanyang g padpadat, at, cair dan cair dan gasgas. . PenPengelgelompompokkokkanan uns
unsur-ur-unsunsur ur ini ini sansangat gat memmembanbantu tu kitkita a daldalam am memmemahaahami mi kemkemiriiripan pan dandan perbedaan diantara unsur-unsur, sehingga memudahkan kita untuk perbedaan diantara unsur-unsur, sehingga memudahkan kita untuk mempelajari mekanisme dan sifat-sifat yang ditunjukkan ketika suatu unsur mempelajari mekanisme dan sifat-sifat yang ditunjukkan ketika suatu unsur bergabung dengan unsur lain.
bergabung dengan unsur lain.
II.RUMUSAN MASALAH II.RUMUSAN MASALAH a.
a. Bagaimana sBagaimana sistem klasifikistem klasifikasi unasi unsur-unsur sur-unsur dalam tabdalam tabel periodik el periodik unsur?unsur? 1.
1. Klasifikasi uKlasifikasi unsur-unsur nsur-unsur berdasarkan berdasarkan sifat logam sifat logam dan dan nonlogamnonlogam 2.
2. Klasifikasi Klasifikasi unsur-unsur unsur-unsur berdasarkan berdasarkan Hukum Hukum TriadeTriade 3.
3. Klasifikasi Klasifikasi unsur-unsur unsur-unsur berdasarkan berdasarkan Hukum Hukum Oktaf Oktaf 4.
4. Klasifikasi Klasifikasi unsur-unsur unsur-unsur berdasarkan berdasarkan Hukum Hukum MendeleyevMendeleyev 5.
5. Klasifikasi Klasifikasi unsur-unsur unsur-unsur berdasarkan berdasarkan sistem sistem periodik periodik ModernModern 6.
6. Klasifikasi Klasifikasi unsur-unsur unsur-unsur berdasarkan berdasarkan struktur struktur elektronelektron b.
b. Bagaimana hBagaimana hubungan ubungan sistem psistem periodik deriodik dengan engan konfigurasi konfigurasi electronelectron
III.PEMBAHASAN III.PEMBAHASAN A.
A. Sistem klasifikasSistem klasifikasi unsur-unsur di unsur-unsur dalam Tabel Peralam Tabel Periodik Unsuriodik Unsur
Sistem periodik unsur adalah sistem pengelompokkan unsur Sistem periodik unsur adalah sistem pengelompokkan unsur berdasarkan hukum periodik, mencakup periode dan golongan yang keduanya berdasarkan hukum periodik, mencakup periode dan golongan yang keduanya saling berhubungan dan menentukan keperiodikkan sifat unsur, disajikan ke saling berhubungan dan menentukan keperiodikkan sifat unsur, disajikan ke dalam bentuk tabel yang disebut Tabel Periodik Unsur
dalam bentuk tabel yang disebut Tabel Periodik Unsur ..11 Unsur-unsur dapatUnsur-unsur dapat 1 Mulyono, Ham,
diklasifikasikan menurut banyak cara. Cara yang paling tegas ialah diklasifikasikan menurut banyak cara. Cara yang paling tegas ialah berdasarkan wujud pada keadaan SATP
berdasarkan wujud pada keadaan SATP (Standard Ambient Temperature and (Standard Ambient Temperature and Pressure)
Pressure). Atas dasar ini unsur-unsur dibedakan dalam wujud gas (11 unsur),. Atas dasar ini unsur-unsur dibedakan dalam wujud gas (11 unsur), wujud cair (2 unsur), dan sisanya wujud padat.
wujud cair (2 unsur), dan sisanya wujud padat.22 Adapun modelAdapun model pen
pengelgelompompokaokan n unsunsur-ur-unsunsur ur daldalam am TPU TPU secsecara ara umuumum m dibdibedaedakan kan sebsebagaagaii berikut:
berikut:
1.
1. KlasifiKlasifikasi Unsur-Unkasi Unsur-Unsur berdassur berdasarkan sifaarkan sifat logam dant logam dan nonlogam
nonlogam Peng
Pengelompelompokan dengan okan dengan dasar sifat dasar sifat logam dan logam dan nonlononlogam gam merupmerupakanakan met
metode ode penpengelgelompompokkokkan an yanyang g palpaling ing sedsederherhanaana. . UnsUnsur ur ada ada yag yag berberrsirsifatfat logam, nonlogam dan diantara keduanya (metaloid). Ciri-ciri unsur logam logam, nonlogam dan diantara keduanya (metaloid). Ciri-ciri unsur logam dan nonlogam
dan nonlogam
L
Looggaam m NNoonnllooggaamm Kerapatan tinggi Kerapatan tinggi Keras, padat Keras, padat Bersifat konduktor Bersifat konduktor Mengkilap Mengkilap elektropositif elektropositif
Oksidanya bersifat basa Oksidanya bersifat basa
Kerapatan rendah Kerapatan rendah Rapuh Rapuh Bersifat isolator Bersifat isolator Tidak mengkilap Tidak mengkilap elektronegatif elektronegatif
Oksidanya bersifat asam Oksidanya bersifat asam
Lebih dari 70% unsur-unsur adalah logam. Logam mempunyai sifat Lebih dari 70% unsur-unsur adalah logam. Logam mempunyai sifat yang sama dalam kemampuannya mengubah bentuk tanpa pecah jika ditempa yang sama dalam kemampuannya mengubah bentuk tanpa pecah jika ditempa denga
dengan n pemukpemukul ul atau ditarik atau ditarik untuk melurusuntuk meluruskannkannya. ya. UnsuUnsur r yang termasuk yang termasuk golongan logam diantaranya Aluminium, Magnesium, Perak, Tembaga, Seng. golongan logam diantaranya Aluminium, Magnesium, Perak, Tembaga, Seng. a.
a. NoNonlnlogogamam
Kebanyakan unsur nonlogam jarang dijumpai dalam bentuk Kebanyakan unsur nonlogam jarang dijumpai dalam bentuk unsurnya yang murni, dalam kehidupan sehari-hari, yang sering dijumpai unsurnya yang murni, dalam kehidupan sehari-hari, yang sering dijumpai ialah dalam
ialah dalam bentubentuk k senyasenyawa wa kimiakimia. . UnsuUnsur r yang termasuk golongyang termasuk golonganan nonl
nonlogam ogam yaitu yaitu KarbonKarbon, , BeleraBelerang, ng, FosfoFosfor, r, NitroNitrogen, gen, OksiOksigen, gen, HidrogHidrogen,en,
2 Kristian, sugiyanto,
Fluor, Brom, Iodium. Fluor, Brom, Iodium. b.
b. MetMetaloaloidid
Metaloid disebut juga semimetal yaitu unsur yang mempunyai sifat Metaloid disebut juga semimetal yaitu unsur yang mempunyai sifat ant
antara ara loglogam am dan dan nonnonloglogam. am. ConContohtohnya nya : : BorBoron, on, SilSilikoikon, n, ArsArsen,en, Germanium,dll.
Germanium,dll.33
2.
2. KlasifikKlasifikasi unsur-unsur berdasarkan Hukum Triadeasi unsur-unsur berdasarkan Hukum Triade Dobereiner
Dobereiner J.W
J.W DoberDobereiner einer merupmerupakan akan orang pertama orang pertama yang mengelomyang mengelompokkapokkann un
unsursur-un-unsur sur berberdasdasarkarkan an sifsifat at khakhas s atoatom m dan dan masmassa sa atoatomnymnya. a. Dari Dari hahasilsil pengamatannya menunjukkan bahwa tiap tiga unsur yang mempunyai pengamatannya menunjukkan bahwa tiap tiga unsur yang mempunyai per
persamsamaan aan sifsifat, at, jikjika a disdisusuusun n daldalam am satsatu u kelkelompompok ok yanyang g disdisebuebut t TriTriade,ade, ternyata massa atom relatif unsur ditengah mendekati setengah jumlah massa ternyata massa atom relatif unsur ditengah mendekati setengah jumlah massa atom relatif unsur pertama dan ketiga.
atom relatif unsur pertama dan ketiga.44 Contoh
Contoh : : Li Li Na Na K K
6,94 23,02 39,10 6,94 23,02 39,10
Ar unsur-unsur yang ditengah menurut Triade Ar unsur-unsur yang ditengah menurut Triade
Sistem ini dinilai kurang efisien karena ternyata ada beberapa unsur Sistem ini dinilai kurang efisien karena ternyata ada beberapa unsur lain yang tidak termasuk dalam satu Triade, tetapi mempunyai lain yang tidak termasuk dalam satu Triade, tetapi mempunyai sifat-sifat yang mirip dengan Triade tersebut.
sifat yang mirip dengan Triade tersebut.
3.
3. KlasifikKlasifikasi asi usur-unsuusur-unsur r berdasarkaberdasarkan n Hukum Hukum Oktaf Oktaf Newlands
Newlands
John Newlands menemukan hubungan antara sifat unsur dengan massa John Newlands menemukan hubungan antara sifat unsur dengan massa atom relatifnya. Jadi unsur ke delapan mempunyai sifat yang sama dengan atom relatifnya. Jadi unsur ke delapan mempunyai sifat yang sama dengan unsur pertama atau dengan kata lain sifat unsur yang pertama akan terulang unsur pertama atau dengan kata lain sifat unsur yang pertama akan terulang sec
secara ara perperiodiodik ik padpada a uruurutan tan ke ke deldelapaapan. n. PenPenemuemuan an JoJohn hn NewNewlanlands ds dikdikenaenall
3
3 James Brady.James Brady.Kimia Universitas Asas & Struktur jilid 1Kimia Universitas Asas & Struktur jilid 1, (jakarta: Binarupa Akasa), hlm.143-, (jakarta: Binarupa Akasa),
hlm.143-146 146
4 Nurchasanah,dkk.
dengan
dengan hukum oktaf.hukum oktaf.55
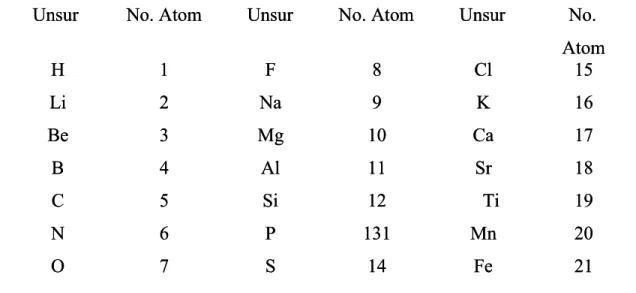
Tabel Pengelompokkan unsur-unsur berdasarkan hukum oktaf Newlands Tabel Pengelompokkan unsur-unsur berdasarkan hukum oktaf Newlands
U
Unnssuur r NNoo. . AAttoom m UUnnssuur r NoNo. . AAttoom m UUnnssuur r NNoo.. Atom Atom H H Li Li Be Be B B C C N N O O 1 1 2 2 3 3 4 4 5 5 6 6 7 7 F F Na Na Mg Mg Al Al Si Si P P S S 8 8 9 9 10 10 11 11 12 12 131 131 14 14 Cl Cl K K Ca Ca Sr Sr Ti Ti Mn Mn Fe Fe 15 15 16 16 17 17 18 18 19 19 20 20 21 21
Sistem ini hanya berlaku untuk unsur-unsur ringan yang memiliki massa Sistem ini hanya berlaku untuk unsur-unsur ringan yang memiliki massa taom relatif (Ar) rendah. Namun demikian, hukum oktaf John Newlands taom relatif (Ar) rendah. Namun demikian, hukum oktaf John Newlands telah menuju usaha yang tepat
telah menuju usaha yang tepat untuk menyusun diagram unsur.untuk menyusun diagram unsur. 4.
4. Tabel Tabel periodik periodik unsur unsur MendeleyMendeleyevev
Pada tahun 1869, guru kimia Dimitri Mendeleyef menyusun daftar Pada tahun 1869, guru kimia Dimitri Mendeleyef menyusun daftar unsur-unsur berdasarkan sifat-sifat fisika dan kimia dan diurutkan unsur-unsur berdasarkan sifat-sifat fisika dan kimia dan diurutkan menurut massa relatifnya,hukum periodik Mendeleyef berbuny
menurut massa relatifnya,hukum periodik Mendeleyef berbunyii66::
Dengan daftar sistem periodik unsur Mendeleyev ini dapat diketahui : Dengan daftar sistem periodik unsur Mendeleyev ini dapat diketahui : a.
a. PerubPerubahan sifaahan sifat-sifat yant-sifat yang teratur dari unsg teratur dari unsur-unur-unsur dalam satsur dalam satu golonu golongangan
5 Sri juari santoso, dkk.
5 Sri juari santoso, dkk.Kimia Untuk kelas X Kimia Untuk kelas X , (klaten : PT. Intan Pariwara, 2005), Hlm.37, (klaten : PT. Intan Pariwara, 2005), Hlm.37 6 Gatot Luhbandjono,
ke golongan lain ke golongan lain
b.
b. Hubungan antara valensi tertinggi unsur dengan nomor golongannyaHubungan antara valensi tertinggi unsur dengan nomor golongannya..
c.
c. Ramalan sifat-sifat Ramalan sifat-sifat unsur unsur yang yang belum belum diketahui diketahui pada spada saat ituaat itu d.
d. Daftar ini tidak banyDaftar ini tidak banyak berubah walauak berubah walaupun unsupun unsur-unsr-unsur gas mulia telahur gas mulia telah ditemukan
ditemukan
Daftar Mendeleyef ini mempunyai keterbatasan-keterbatasan diantaranya: Daftar Mendeleyef ini mempunyai keterbatasan-keterbatasan diantaranya: a.
a. PanjaPanjang ng perioperiodenya denya tidak tidak samasama b.
b. BeberaBeberapaa upaa unsur nsur ada yada yang ang terbalterbalik ik c.
c. Selisih Selisih massa massa atom relatif atom relatif yang yang tidak tidak berurutan tidberurutan tidak teratur ak teratur d.
d. Perubahan sPerubahan sifat unsur ifat unsur ini lambat ini lambat dari elektromegatif dari elektromegatif menjadi elektroposmenjadi elektropositif itif e.
e. Unsur-unsur Unsur-unsur dari lanthaniddari lanthanida dimasuka dimasukkan kan kedalam satu kedalam satu golongangolongan f.
f. BesarnBesarnya valenya valensi unsusi unsur yang lebr yang lebih dari satu mih dari satu macam valenacam valensi sukar dsi sukar diramaliramal kedudukannya dalam sistem periodik
kedudukannya dalam sistem periodik g.
g. SifSifat at anoanomalmali i unsunsur ur perpertamtama a setsetiap iap golgolongongan an tidtidak ak ada ada hubhubungungannannyaya dengan massa atom relatif
dengan massa atom relatif
h.
h. Jika daftar disusun berdasarkan massa atom relatif,maka isotop unsur yangJika daftar disusun berdasarkan massa atom relatif,maka isotop unsur yang
sama harus ditempatkan pada golongan yang berbeda, sedangkan isobar sama harus ditempatkan pada golongan yang berbeda, sedangkan isobar seperti: 40Ar, 40K, 40Ca harus dimasukkan dalam
seperti: 40Ar, 40K, 40Ca harus dimasukkan dalam satu golongan.satu golongan.77
5.
5. SistSistem em PeriPeriodik odik ModeModernrn
Daftar asli Mendeleyev mengalami banyak perubahan, namun masih Daftar asli Mendeleyev mengalami banyak perubahan, namun masih terlihat pada sistem periodik modern. Ada berbagai macam sistem terlihat pada sistem periodik modern. Ada berbagai macam sistem periodik, tetapi yang lebih sering digunakan adalah sistem periodik periodik, tetapi yang lebih sering digunakan adalah sistem periodik panjang. Daftar ini disusun berdasarkan konfigurasi elektron dari atom panjang. Daftar ini disusun berdasarkan konfigurasi elektron dari atom unsur-unsur. Unsur-unsur dengan konfigurasi elektron yang mirip unsur-unsur. Unsur-unsur dengan konfigurasi elektron yang mirip
7
7 http://eddysyahrizal.blogspot.com/2008/08/sejarahttp://eddysyahrizal.blogspot.com/2008/08/sejarah-sistem-periodik-unsur.htmlh-sistem-periodik-unsur.html
5 5
mempunyai sifat-sifat kimia yang mirip. Jadi sifat unsur ini ada mempunyai sifat-sifat kimia yang mirip. Jadi sifat unsur ini ada hubungannya dengan konfigurasi elektron.hubungan ini dapat disimpulkan hubungannya dengan konfigurasi elektron.hubungan ini dapat disimpulkan sebagai berikut:
sebagai berikut: 1.
1. ElektElektron-eleron-elektron ktron tersustersusun dun dalam oalam orbitalrbital 2.
2. Hanya dHanya dua elektron ua elektron saja yang saja yang dapat mdapat mengisi setiap engisi setiap orbitalorbital 3.
3. Orbital-orbital Orbital-orbital dikelompokkan dikelompokkan dalam dalam kulitkulit 4. .Hanya n
4. .Hanya n22 orbital yang dapat mengisi kulit ke-norbital yang dapat mengisi kulit ke-n 5.
5. Ada berbagai macam Ada berbagai macam orbital dengan orbital dengan bentuk yang bentuk yang berbeda.berbeda. a.Orbital-s,satu orbital setiap kulit
a.Orbital-s,satu orbital setiap kulit b.Orbital –p,tiga orbital setiap kulit b.Orbital –p,tiga orbital setiap kulit c.Orbital-d,lima orbital setiap kulitnya c.Orbital-d,lima orbital setiap kulitnya d.Orbital –f,tujuh orbital setiap kulitnya d.Orbital –f,tujuh orbital setiap kulitnya
6.
6. ElektElektron terluron terluar yang paliar yang paling menenng menentukan situkan sifatfat kimianya,yang disebut dengan elektron valensi. kimianya,yang disebut dengan elektron valensi. 7.
7. Unsur Unsur dalam dalam satu satu gologolongan ngan mempmempunyaiunyai ele
elektrktron on valvalensensi i yang yang samsama a sehsehinginggaga mempunyai sifat yang mirip
mempunyai sifat yang mirip 8.
8. Satu Satu golongan golongan unsur unsur berubah berubah secaraa teratur secaraa teratur 9.
9. UnUnsusur r dadalam lam sasatu tu peperiorioda da memempmpununyayai i sisifafatt yang berubah secara teratur
yang berubah secara teratur
Dari penguraian diatas dapat disimpulkan sebagai berikut,bahwa: Dari penguraian diatas dapat disimpulkan sebagai berikut,bahwa:
1.Sifat unsur merupakan fungsi berkala dari nomor atom 1.Sifat unsur merupakan fungsi berkala dari nomor atom
2.Sifat unsur bergantung pada konfigurasi elektron. 2.Sifat unsur bergantung pada konfigurasi elektron.
6. Klasifikasi unsur-unsur berdasarkan struktur elektron 6. Klasifikasi unsur-unsur berdasarkan struktur elektron
Unsur-unsur diklasifikasikan 4 kelompok : Unsur-unsur diklasifikasikan 4 kelompok :
a.
a. KelomKelompok upok unsur-nsur-unsuunsur iner inert atau rt atau gas mgas muliaulia
Unsur-unsur inert disebut juga sebagai unsur gas mulia (noble gas) Unsur-unsur inert disebut juga sebagai unsur gas mulia (noble gas) terdiri atas
terdiri atas 22He,He, 1010Ne,Ne, 1818Ar,Ar, 3636Kr,Kr, 5454Xe, danXe, dan 8686Rn. Unsur-unsur ini dikenalRn. Unsur-unsur ini dikenal sebagai unsur yang sangat stabil. Hal ini dikarenakan konfigurasi sebagai unsur yang sangat stabil. Hal ini dikarenakan konfigurasi elektronnya penuh untuk setiap orbital dan dengan elektron valensi ns elektronnya penuh untuk setiap orbital dan dengan elektron valensi ns22 npnp44 (kecuali He, mempunyai konfigurasi penuh 1s
(kecuali He, mempunyai konfigurasi penuh 1s22), karena konfigurasi), karena konfigurasi ele
elektrktronionik k ununsursur-un-unsur sur gas gas mulmulia ia diadianggnggap ap sudsudah ah penpenuh, uh, makmaka a unsunsur- ur-uns
unsur ur ini ini dipdipakaakai i sebsebagaagai i stastandandar r untuntuk uk menmenyatyatakaakan n penpenuh uh atau atau tidtidak ak penuhnya konfigurasi elektron kelompok unsur-unsur lain.
penuhnya konfigurasi elektron kelompok unsur-unsur lain. b.
b. Kelompok Kelompok unsur-unsur unsur-unsur utama utama atau atau representativerepresentative
Unsur-unsur ini ditandai dengan konfigurasi elektronik tidak
Unsur-unsur ini ditandai dengan konfigurasi elektronik tidak penuhpenuh pada satu kulit terluar, ns
pada satu kulit terluar, ns11-ns-ns22npnp(0-5)(0-5). Seperti unsur-unsur :. Seperti unsur-unsur : 30 30ZZnn= (= (1515Ar) 3dAr) 3d10104s4s22 48 48Cd = (Cd = (3636Kr) 4dKr) 4d10105s5s22 80 80Hg = (Hg = (5454XXee) 4f ) 4f 14145d5d10106s6s22
Unsur-unsur di atas dapat membentuk ion M
Unsur-unsur di atas dapat membentuk ion M2+2+ seperti golongan Mseperti golongan M22 (Be,(Be, Mg, Ca, dll) dengan beberapa kemiripan, namun dengan beberapa Mg, Ca, dll) dengan beberapa kemiripan, namun dengan beberapa perbe
perbedaan. Salah daan. Salah satu perbedaansatu perbedaannya adalah nya adalah unsuunsur-unsr-unsur ur Zn dan Zn dan CdCd mempunyai sifat kecenderungan lebih besar untuk membentuk mempunyai sifat kecenderungan lebih besar untuk membentuk senyawa-senyawa kompleks dengan NH
senyawa kompleks dengan NH33, ion-ion X, ion-ion X-- dan CNdan CN--. Hal ini disebabkan. Hal ini disebabkan adanya perbedaan konfigurasi elektronik terluar yaitu 18 elektron ion M adanya perbedaan konfigurasi elektronik terluar yaitu 18 elektron ion M2+2+ untuk kelompok ini.
untuk kelompok ini.88 c.
c. Kelompok Kelompok unsur-unsur unsur-unsur transisi dtransisi dan an transisi dalam transisi dalam (inner trans(inner transisi)isi)
Unsur-unsur keluarga A sering disebut sebagai unsur-unsur Unsur-unsur keluarga A sering disebut sebagai unsur-unsur
8 Kristian H. Sugiyanto,
golongan utama dan unsur-unsur dalam keluarga B sebagai unsur deret golongan utama dan unsur-unsur dalam keluarga B sebagai unsur deret transisi dan deret transisi dalam ke-58 unsur dalam dan deret terakhir ini, transisi dan deret transisi dalam ke-58 unsur dalam dan deret terakhir ini, semuanya adalah logam. Unsur-unsur transisi adalah unsur-unsur keluarga semuanya adalah logam. Unsur-unsur transisi adalah unsur-unsur keluarga B dalam periode 4,5,6, dan 7. Sedangkan deret lantanida dalam periode ke B dalam periode 4,5,6, dan 7. Sedangkan deret lantanida dalam periode ke enam dan deret aktinida dalam periode ke-7 disebut unsur-unsur transisi enam dan deret aktinida dalam periode ke-7 disebut unsur-unsur transisi dalam umumnya unsur-unsur transisi dapat di tempat, liat dan pengantar dalam umumnya unsur-unsur transisi dapat di tempat, liat dan pengantar panas dan listrik yang baik, dan memiliki kilap logam, golongan transisi panas dan listrik yang baik, dan memiliki kilap logam, golongan transisi meliputi keluarga stanium, vanadium, krom, magan, besi, platinum, meliputi keluarga stanium, vanadium, krom, magan, besi, platinum, tembaga, zink, dan skondium.
tembaga, zink, dan skondium.99
B.
B. Hubungan SisHubungan Sistem Periodtem Periodik dengan Konfik dengan Konfigurasi Elektigurasi Elektronron Pen
Penyusyusunaunan n unsunsur-ur-unsunsur ur daldalam am sissistem tem perperiodiodik ik panpanjanjang g dapdapatat dihu
dihubungbungkan kan dalam konfiguradalam konfigurasi si elektrelektron on dalam orbital dalam orbital atom. Sesuatu halatom. Sesuatu hal ini, hukum berkala dapat diungkapkan secara lain yaitu sifat-sifat unsur ini, hukum berkala dapat diungkapkan secara lain yaitu sifat-sifat unsur berhu
berhubungbungan an langslangsung ung dengadengan n konfikonfigurasgurasi i elektroelektron n dalam dalam atom atom unsuunsur r tersebut.
tersebut.
Unsur-unsur dalam sistem periodik dapat dikelompokkan dalam Unsur-unsur dalam sistem periodik dapat dikelompokkan dalam jalur vertikal yang disebut golongan dan jalur horisontal disebut periode. jalur vertikal yang disebut golongan dan jalur horisontal disebut periode.1010
a.
a. PePerioriodede
Nama periode dari atas ke bawah menunjukkan bilangan Nama periode dari atas ke bawah menunjukkan bilangan kuantum utama terbesar yang dapat dimiliki oleh atom dari unsur-unsur kuantum utama terbesar yang dapat dimiliki oleh atom dari unsur-unsur yang terdapat dalam periode tersebut. Ada tujuh periode dalam sistem yang terdapat dalam periode tersebut. Ada tujuh periode dalam sistem peiode panjang masing-masing periode tersebut adalah:
peiode panjang masing-masing periode tersebut adalah:
a) Perioda 1 terdiri atas 2
a) Perioda 1 terdiri atas 2 unsuunsur r ko
konfnfigigururasasi i didianantatararanynyaa menyangkut orbital
menyangkut orbital ss..
9 Keenan, dkk, 1978,
9 Keenan, dkk, 1978, Kimia Untuk Universitas, Jilid 2Kimia Untuk Universitas, Jilid 2, Jakarta : Erlangga hlm. 150-151, Jakarta : Erlangga hlm. 150-151 10 Collins, Gem,
b) Peri
b) Perioda 2 oda 2 terdirterdiri i atas 8 atas 8 unsuunsur r ko
konfnfigigururasasi i didianantatararanynyaa menyangkut orbital
menyangkut orbital s, ps, p.. c)
c) PePeririododa 3 tera 3 terdidiri atri atas 8 unas 8 unsusur r ko
konfnfigigururasasi i didianantatararanynyaa menyangkut orbital
menyangkut orbital s, ps, p.. d)
d) PePeririododa a 4 4 teterdrdiriri i atatas as 18 18 ununsusur r ko
konfnfigigururasasi i didianantatararanynyaa menyangkut orbital
menyangkut orbital s, p, d s, p, d .. e)
e) PePeririododa a 5 5 teterdrdiriri i atatas as 18 18 ununsusur r ko
konfnfigigururasasi i didianantatararanynyaa menyangkut orbital
menyangkut orbital s, p, d s, p, d .. f)
f) PePeririododa a 6 6 teterdrdiriri i atatas as 32 32 ununsusur r ko
konfnfigigururasasi i didianantatararanynyaa menyangkut orbital
menyangkut orbital s, p, d, f s, p, d, f .. g) Peri
g) Perioda 7 oda 7 terdirterdiri i atas 8 atas 8 unsuunsur r ko
konfnfigigururasasi i didianantatararanynyaa menyangkut orbital
menyangkut orbital s, p, d, f s, p, d, f ..
Dari perioda tersebut, perioda 2 dikenal dengan perioda pendek Dari perioda tersebut, perioda 2 dikenal dengan perioda pendek per
pertamtama. a. PerPeriodioda a ketketiga dikeiga dikenal sebagnal sebagai ai perperiodioda a penpendek kedudek kedua. a. MulMulaiai per
periodioda a keekeempampat t dikdikenaenal l sebsebagaagai i perperiodioda a panpanjanjang g perpertamtama, a, kedkedua ua dandan seterusnya.
seterusnya.
b.
b. GoGolonlongangan Unsu
Unsur-unsr-unsur ur dengdengan an konfikonfigurasgurasi i elektrelektron on mirip mirip mempumempunyainyai sifat yang mirip karena bergantung pada konfigurasi elektron. Elektron sifat yang mirip karena bergantung pada konfigurasi elektron. Elektron yan
(elektron valensi). (elektron valensi).
Elektron valensi adalah elektron terluar yang tidak terikat kuat Elektron valensi adalah elektron terluar yang tidak terikat kuat yang mempunyai peranan dalam pembentukan ikatan kimia. yang mempunyai peranan dalam pembentukan ikatan kimia. Berdasarkan konfigurasi elektron, unsur-unsur dalam sistem periodik Berdasarkan konfigurasi elektron, unsur-unsur dalam sistem periodik dibagi menjadi 4 blok, yaitu :
dibagi menjadi 4 blok, yaitu :
a)
a) UnsUnsur-ur-unsunsur ur bloblok k ss, , konfkonfigurasigurasii elektronnya = n
elektronnya = nss1-21-2 b)
b) UnsUnsur-ur-unsunsur ur bloblok k p,p, konfigurasikonfigurasi elektronnya = n
elektronnya = npp1-61-6 c)
c) UnsUnsur-ur-unsunsur ur bloblok k d d , , konfikonfigurasgurasii elektronnya = (n-1)
elektronnya = (n-1)ss22 (n-1)(n-1)pp22 (n- (n-1)
1)d d 1-101-10nnss22 d)
d) UnsuUnsur-unsr-unsur ur blok blok f f konfigurasikonfigurasi elektronnya =
elektronnya = (n-2)(n-2)f f 1-141-14 (n-1)(n-1)ss22 (n- (n-1)
1)pp22(n-1)(n-1)d d 1-101-10nnss22 Oleh
Oleh karkarena ena unsunsur-ur-unsunsur ur golgolongongan an gas gas mulmulia ia dahdahulu ulu diddidugauga tidak dapat bereaksi maka unsur-unsur ini biasanya disebut golongan tidak dapat bereaksi maka unsur-unsur ini biasanya disebut golongan 0(
0(nonol). l). SPSPU U didibabagi gi ataatas s 8 8 gogololongnganan. . SeSetitiap ap gogololongngan an didibabagi gi atatasas golongan utama(A) dan golongan transisi (B). Penomoran golongan golongan utama(A) dan golongan transisi (B). Penomoran golongan dilakukan berdasarkan elektron valensi yang dimiliki
dilakukan berdasarkan elektron valensi yang dimiliki oleh suatu unsur.oleh suatu unsur. Jika konfigurasi elektron berakhir di blok s dan p maka pasti Jika konfigurasi elektron berakhir di blok s dan p maka pasti menempati golangan A.
menempati golangan A.
Jika konfigurasi elektron berakhir di blok d maka menempati golongan Jika konfigurasi elektron berakhir di blok d maka menempati golongan B
B Jik
Jika a konkonfigfiguraurasi si elekelektrotron n berberakhakhir ir di di bloblok k f f makmaka a paspasti ti menmenempempatiati golongan B (Lantanida n=6 dan Aktinida n=7(golongan radio
Contoh
Contoh 1111Na = 1sNa = 1s222s2s222p2p66 3s3s11
Dapat diketahui bahwa elektron terakhir pada n=3 memiliki elektron valensi Dapat diketahui bahwa elektron terakhir pada n=3 memiliki elektron valensi 1,
1, berberarti golonarti golongan 1 gan 1 serserta ta berberakhakhir ir di di susubkubkulit lit s s berberartarti i golgolongongan an A.A. Sehingga letak unsur tersebut dalam TPU adalah golongan 1A periode 3. Sehingga letak unsur tersebut dalam TPU adalah golongan 1A periode 3.
IV.KESIMPULAN IV.KESIMPULAN
1.
1. Sistem Sistem periodik periodik unsur unsur dapat dapat diklasifikasikan diklasifikasikan berdasarkan:berdasarkan:
•
• Sifat logam dan non logamSifat logam dan non logam
•
• Hukum triadeHukum triade
•
• Hukum Oktaf Hukum Oktaf
•
• Hukum MendeleyevHukum Mendeleyev
•
• Sistem Periodik ModernSistem Periodik Modern
•
• ElektronElektron
2.
2. PenyuPenyusunan unssunan unsur-unur-unsur dalam sistem periosur dalam sistem periodik panjang dapadik panjang dapatt dihubungkan dalam konfigurasi elektron dalam orbital atom. dihubungkan dalam konfigurasi elektron dalam orbital atom. Sesua
Sesuatu tu hal ini, hal ini, hukuhukum m berkalberkala a dapat diungkdapat diungkapkan secara lainapkan secara lain yaitu sifat-sifat unsur berhubungan langsung dengan yaitu sifat-sifat unsur berhubungan langsung dengan konfigurasi elektron dalam atom unsur tersebut.
konfigurasi elektron dalam atom unsur tersebut. Uns
Unsur-ur-ununsur sur daldalam am sissistem tem perperiodiodik ik dapdapat at dikdikeloelompompokkakkan n daldalam am jaljalur ur vertikal yang disebut golongan dan jalur
vertikal yang disebut golongan dan jalur horisontal disebut periode.horisontal disebut periode. 3.
3. UnsurUnsur-uns-unsur ur dengadengan n konfkonfigurasigurasi i elektrelektron on yang yang miripmirip mempunyai sifat-sifat kimia yang mirip. Jadi sifat unsur ini ada mempunyai sifat-sifat kimia yang mirip. Jadi sifat unsur ini ada hubungannya dengan konfigurasi elektron.
V.PENUTUP V.PENUTUP
Demikian makalah ini kami buat, dalam pembuatan makalah ini Demikian makalah ini kami buat, dalam pembuatan makalah ini tentunya masih jauh dari kesempurnaan. Oleh karena itu, kritik dan saran tentunya masih jauh dari kesempurnaan. Oleh karena itu, kritik dan saran yang konstruktif senantiasa kami harapkan demi perbaikan makalah yang konstruktif senantiasa kami harapkan demi perbaikan makalah selanjutnya. Semoga makalah ini bermanfaat bagi pembaca.
selanjutnya. Semoga makalah ini bermanfaat bagi pembaca.
DAFTAR PUSTAKA DAFTAR PUSTAKA
Brady, Jaames.
Brady, Jaames. Kimia Universitas Asas dan Struktur Jilid 1Kimia Universitas Asas dan Struktur Jilid 1 , Jakarta : Bina, Jakarta : Bina rupa Aksara
rupa Aksara Gem, Collins. 2008.
Gem, Collins. 2008. Kamus Saku Kimia.Kamus Saku Kimia. Jakarta : ErlanggaJakarta : Erlangga H. Sugiyanto, Kristian,2004,
Ham,
Ham, Mulyono. Mulyono. 2007.2007. Kamus KimiaKamus Kimia. Jakarta : Bumi Aksara. Jakarta : Bumi Aksara Juari Santosa, Sri, dkk. 2005.
Juari Santosa, Sri, dkk. 2005. Kimia kelas X.Kimia kelas X. Klaten : PT. Intan PariwaraKlaten : PT. Intan Pariwara Keenan, dkk, 1978,
Keenan, dkk, 1978, Kimia Untuk Universitas, Jilid 2Kimia Untuk Universitas, Jilid 2 , Jakarta : Erlangga, Jakarta : Erlangga Luhbandjono,Gatot, 2004,
Luhbandjono,Gatot, 2004, Kimia Dasar 1Kimia Dasar 1, Semarang: UPT UNNES Press, Semarang: UPT UNNES Press Nurchasanah, dkk. 2006.
Nurchasanah, dkk. 2006. Kimia untuk SMA/MA Kelas X Kimia untuk SMA/MA Kelas X . Semarang :. Semarang : Aneka Ilmu
Aneka Ilmu Sukarna, I Made. 2003.
Sukarna, I Made. 2003. Kimia Dasar 1Kimia Dasar 1. Yogyakarta : JICA. Yogyakarta : JICA
http://eddysyahrizal.blogspot.com/2008/08/sejarah-sistem-periodik http://eddysyahrizal.blogspot.com/2008/08/sejarah-sistem-periodik unsur.html unsur.html KLASIFIKASI UNSUR-UNSUR KLASIFIKASI UNSUR-UNSUR DALAM TABEL PERIODIK UNSUR DALAM TABEL PERIODIK UNSUR
Makalah Makalah
Disusun Guna Memenuhi Tugas Disusun Guna Memenuhi Tugas Mata Kuliah :
Dosen Pengampu :
Dosen Pengampu : Atik Rahmawati, S.Pd. M.SiAtik Rahmawati, S.Pd. M.Si
Oleh Oleh ::
Ag
Agusustitina na NoNovivitatasasari ri (083(083717110100202)) Dwi
Dwi kukusumsuma a W W (0(083783711011007)07) Mit
Mita a WidWidyawyawati ati (0(083783711011013)13) R
Riirriin n IIssnnaawwaatti i ((008833771111003333))
FAKULTAS TARBIYAH FAKULTAS TARBIYAH
INSTITUT AGAMA ISLAM NEGERI WALISONGO INSTITUT AGAMA ISLAM NEGERI WALISONGO
SEMARANG SEMARANG
2010 2010