i
LAJU KOROSI STAINLESS STEEL 304 DALAM LARUTAN
HNO
3TUGAS AKHIR
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Teknik
Jurusan Teknik Mesin
disusun oleh :
HENDRIKUS DWIJAYANTO WIBOWO SUTARJO
NIM : 045214039
PROGRAM STUDI TEKNIK MESIN
JURUSAN TEKNIK MESIN
FAKULTAS SAINS & TEKNOLOGI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
2011
ii
CORROSION RATE OF STAINLESS STEEL 304 IN HNO
3SOLUTION
A FINAL PROJECT
Submit for The Partial Fulfillment of Requirements to Obtain the Sarjana Technic Degree
In Mechanical Engineering
By :
HENDRIKUS DWIJAYANTO WIBOWO SUTARJO Student number : 045214039
MECHANICAL ENGINEERING STUDY PROGRAM
MECHANICAL ENGINEERING DEPARTMENT
SCIENCE & TECHNOLOGY FACULTY
SANATA DHARMA UNIVERSITY
YOGYAKARTA
2011
v
HALAMAN PERSEMBAHAN
Tugas Akhir ini aku persembahkan untuk:
Bapa, Bunda Maria, Yesus Kristus,
Universitas Sanata Dharma,
Keluargaku terutama BAPAK, IBU
”
Aku Sayang Kalian ” yang telah TUHAN
gunakan untuk memberi motivasi padaku
dalam penyelesaian TUGAS AKHIR ini.
vi
PERNYATAAN
Dengan ini penulis menyatakan bahwa dalam Tugas Akhir ini tidak terdapat karya yang pernah diajukan untuk memperoleh gelar kesarjanaan di suatu Perguruan Tinggi, dan sepanjang pengetahuan penulis juga tidak terdapat karya atau pendapat yang pernah ditulis atau diterbitkan oleh orang lain, kecuali yang secara tertulis diacu dalam naskah ini dan disebutkan dalam daftar pustaka.
Yogyakarta, 12 Januari 2011
Penulis
vii
LEMBAR PERNYATAAN PERSETUJUAN
PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN
AKADEMIS
Yang bertanda tangan dibawah ini, saya mahasiswa Universitas Sanata Dharma: Nama : Hendrikus Dwijayanto Wibowo Sutarjo
Nomor Mahasiswa : 045214039
Demi perkembangan ilmu pengetahuan, saya memberikan kepada perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
LAJU KOROSI STAINLESS STEEL 304 DALAM LARUTAN HNO3
Beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di Internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini saya buat dengan sebenarnya.
Yogyakarta, 12 Januari 2011 Yang menyatakan,
viii
KATA PENGANTAR
Puji syukur kepada Tuhan Yang Maha Esa atas berkat dan bimbingan-Nya hingga terselesaikannya penyusunan Tugas Akhir ini, dengan judul “Laju Korosi Stainless Steel 304 Dalam Larutan HNO3”. Adapun penyusunan tugas akhir ini
merupakan salah satu syarat memperoleh gelar Sarjana Teknik Jurusan Teknik Mesin Fakultas Sains & Teknologi Universitas Sanata Dharma. Dalam penyusunan Tugas Akhir ini, penulis meneliti Laju Korosi Stainless Steel 304 dalam larutan HNO3 pada suhu 70oC selama 6 jam dilanjutkan pada suhu 290C
selam 18 jam.
Pada kesempatan ini penulis mengucapakan terima kasih atas segala bantuan sehingga tugas akhir ini dapat terselesaikan dengan baik, kepada :
1. Romo Dr. Ir. P. Wiryono P., S.J., Rektor Universitas Sanata Dharma.
2. Bapak Yosep Agung Cahyanta, S.T., M.T., Dekan Fakultas Sains & Teknologi Universitas Sanata Dharma.
3. Bapak Budi Sugiharto, S.T., M.T., ketua Program Studi Teknik Mesin Universitas Sanata Dharma.
4. Bapak Wibowo Kusbandono S.T., MT., dosen Pembimbing Akademik. 5. Bapak Budi Setyahandana, S.T., M.T., dosen pembimbing utama penyusunan
Tugas Akhir.
6. Bapak Doddy Purwadianto S.T., M.T., Kepala Laboratorium Ilmu Logam Universitas Sanata Dharma.
ix
7. Bapak Martono, Laboran Laboratorium Ilmu Logam Universitas Sanata Dharma.
8. Bapak Kunto, Laboran Laboratorium Farmasi Universitas Sanata Dharma. 9. Bapak Intan, Laboran Laboratorium Proses Produksi Universitas Sanata
Dharma.
10. Kedua orang tua penulis Bapak M.Sutarjo. dan Ibu Yuliana Yati. 11. Kakakku, FX Sulistiyanto W.S., s.Si., APT dan Lice Sabata, A., Md. 12. Teman-teman.
13. Rekan-rekan seperjuangan TM 03, TM 04, dan TM 05 maupun dari berbagai angkatan yang telah berbagi suka dan duka serta pendorong semangat saya dalam penyelesaian Tugas Akhir ini.
14. Teman-teman dan semua pihak yang tidak dapat penulis sebutkan satu persatu yang telah membantu sehingga Tugas Akhir ini dapat terselesaikan.
Penulis menyadari masih banyak kekurangan, demi kesempuranan tugas ini penulis dengan kesungguhan hati dan lapang dada menerima kritik dan saran yang bersifat membangun guna lebih sempurnanya tugas akhir ini. Akhir kata semoga tugas akhir ini dapat bermanfaat bagi pembaca pada umumnya. Terima kasih.
Yogyakarta,12 Januari 2011 Penulis
x
DAFTAR ISI
HALAMAN JUDUL ... i
TITLE PAGE ... ii
HALAMAN PERSETUJUAN PEMBIMBING………..………..…….iii
HALAMAN PENGESAHAN ... iv
HALAMAN PERSEMBAHAN ... v
PERNYATAAN HASIL KARYA……… vii
KATA PENGANTAR ... viii
DAFTAR ISI ... .x
DAFTAR GAMBAR ... xiii
DAFTAR TABEL ... xv
INTISARI ... xvi
BAB I PENDAHULUAN ... 1
1.1. Latar Belakang Masalah... 1
1.2. Tujuan Penelitian ... 1
1.3. Batasan Masalah ... 2
1.4. Sistematika Penulisan ... 2
BAB II TINJAUAN PUSTAKA ... 4
2.1. Klasifikasi Stainless Steel ... 4
2.2. Baja Tahan Karat ( Stainlees Steel ) ... 4
xi
2.2.2 Ferritic Stainless Steel ... 5
2.2.3 Martensit Stainless Steel ... 5
2.2.4 Duplex Stainless Steel ... 5
2.3 Pengaruh Unsur Paduan Pada Stainless Steel ... 6
1. Kromium ( Cr ) ... 6 2.Nikel ( Ni ) ... 6 3.Mangan ( Mn ) ... 6 4.Molybdenum ( Mo ) ... 6 5.Karbon ( C ) ... 6 6. Nitrogen ( N ) ... 7
2.4. Korosi Pada Logam ... 7
2.4.1 Korosi Secara Umum ... 7
2.4.2 Jenis-Jenis Korosi Pada Stainless Steel ... 8
2.4.2.1. Uniform Corrosion ... 9
2.4.2.2. Pitting Corrosion ... 10
2.4.2.3 Crevice Corrosion ... 12
2.4.2.4 Stress Corrosion Cracking ... 13
2.4.2.5 Intergranular Corrosion ... 15
2.4.2.6 Galvanic Corrosion ... 16
2.5. Pengelasan Berperisai Tungsen ( TIG ) ... 17
xii
BAB III METODE PENELITIAN ... 21
3.1. Bagan Alir penelitian ... 21
3.2. Bahan dan Peralatan ... 22
3.2.1 Bahan ... 22
3.2.2 Peralatan ... 22
3.3. Proses Pembuatan HNO3 pH 0,2 Dan pH 0,5 dan Proses Perendaman ... 25
3.4. Analisis Hasil ... 26
BAB IV HASIL DAN PEMBAHASAN ... 27
4.1. Larutan HNO3 pH 0,5 ... 27
4.2. Larutan HNO3 pH 0,2 ... 35
4.3. Pembahasan ... 45
BAB V KESIMPULAN DAN SARAN ... 46
5.1. Kesimpulan ... 46
5.2. Saran ... 46
DAFTAR PUSTAKA ... 47 LAMPIRAN
xiii
DAFTAR GAMBAR
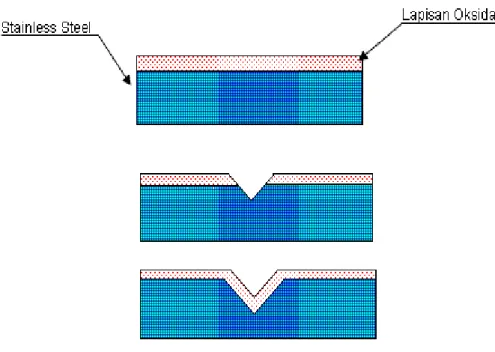
Gambar 2.1 Pembentukan spontan lapisan oksida ... 8
Gambar 2.2 Korosi uniform ... 10
Gambar 2.3 Ilustrasi pitting corrosion pada SS ... 12
Gambar 2.4 Skema proseskimia pitting corrosion ... 12
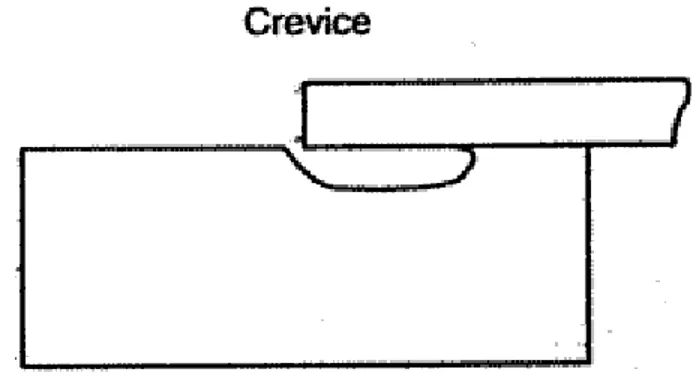
Gambar 2.5 Ilustrasi crevice corrosion ... 13
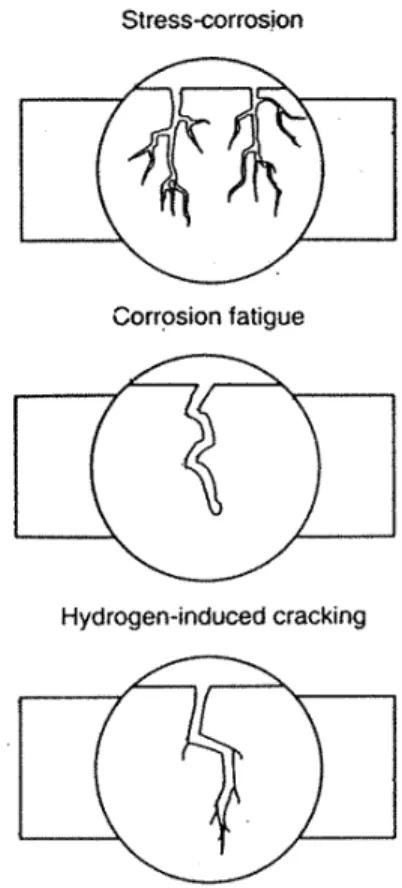
Gambar 2.6 Ilustrasi stress cracking corrosion ... 15
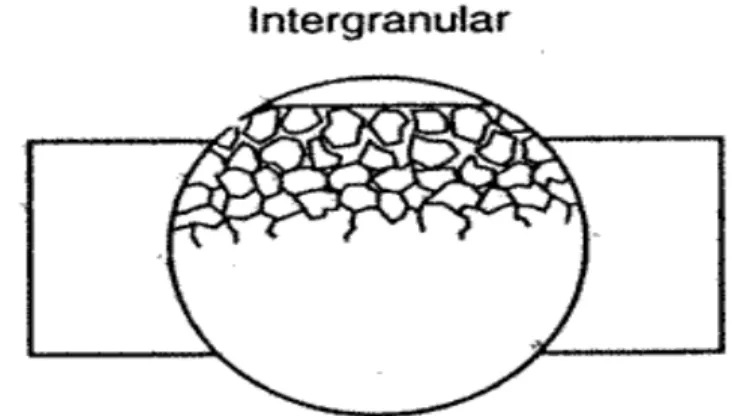
Gambar 2.7 Ilustrasi korosi pada butir ... 16
Gambar 2.8 Ilustrasi terjadinya korosi antara dua logam ... 17
Gambar 2.9 Alat pengelasan TIG ... 18
Gambar 2.10 Alat pengelasan busur listrik ... 20
Gambar 3.1 Diagram alir penelitian ... 21
Gambar 3.2. Baja Tahan Karat 304 yang dilas ... 22
Gambar 3.3. Larutan HNO3 pekat 65% ... 22
Gambar 3.4. Tabung reaksi ... 23
Gambar 3.5 pH meter digital... 23
Gambar 3.6 Timbangan digital ... 24
Gambar 3.7 Water bath ... 24
Gambar 4.1 Benda uji I mula-mula ... 27
Gambar 4.2 Keterangan luas benda uji ... 28
Gambar 4.3 Benda uji II mula-mula ... 30
Gambar 4.4 Gambar benda uji III selama 13 minggu ... 33
xiv
Gambar 4.6 Gambar benda uji V selama 12 minggu...38
Gambar 4.7 Gambar benda uji VI selama 12 minggu...40
Gambar 4.8 Grafik laju korosi SS 304 dalam larutan HNO3 dengan pH 0,5...43
Gambar 4.9 Grafik laju korosi SS 304 dalam larutan HNO3 dengan pH 0,2...43
Gambar 4.10 Grafik laju korosi per bulan pada pH 0,5...44
xv
DAFTAR TABEL
Tabel 4.1 Data perubahan berat benda uji I pada larutan HNO3 pH 0,5 ... 29
Tabel 4.2 Laju korosi benda uji I pada larutan HNO3 pH 0,5 ... 30
Tabel 4.3 Data perubahan berat benda uji II pada larutan HNO3 pH 0,5 ... 31
Tabel 4.4 Laju korosi benda uji II pada larutan HNO3 pH 0,5 ... 32
Tabel 4.5 Data perubahan berat benda uji III pada larutan HNO3 pH 0,5 ... 34
Tabel4.6 Laju korosi benda uji III pada larutan HNO3 pH 0,5...35
Tabel 4.7 Data perubahan berat benda uji IV pada larutan HNO3 pH 0,2...36
Tabel 4.8 Laju korosi benda uji IV pada larutan HNO3 pH 0,2...37
Tabel 4.9 Data perubahan benda uji V pada larutan HNO3 pH 0,2...38
Tabel 4.10 Laju korosi benda uji V pada larutan HNO3 pH 0,2...39
Tabel 4.11 Data perubahan berat benda uji VI pada larutan HNO3 pH 0,2...41
xvi
INTISARI
Penelitian ini bertujuan untuk mengetahui laju korosi stainless steel 304 dalam larutan HNO3. Proses pencelupan dilakukan pada suhu 700C selama 6 jam
dilanjutkan dengan suhu 290C selama 18 jam setiap 7 hari. Hal ini untuk mendekatkan penggunaan stainless steel secara nyata di dalam pemakaian tabung reaktor SAMOP (Sub Critical Assembly for Mo99 Prad Action).
Spesimen yang telah mengalami pengelasan TIG dan busur listrik dibersihkan dari kotoran kemudian diukur, digambar, ditimbang dan dicatat berat awalnya. Selanjutnya spesimen dicelup di dalam larutan HNO3 pH 0,2 dan 0,5
pada suhu 700C selama 6 jam dilanjutkan pada suhu 290C selama 18 jam setiap 7 hari selama 3 bulan. Pencatatan berat dilakukan setiap minggu.
Hasil penelitian menunjukkan adanya penyusutan berat pada semua specimen. Hal ini terlihat jelas pada laju korosi pH 0,5 pada las busur listrik 0,105 gram/dm2/bulan, untuk laju korosi tanpa las adalah 0,026 gram/dm2/bulan. Pada pH 0,2 pada las busur listrik adalah 0,045 gram/dm2/bulan pada pH 0,2 tanpa las 0,02 gram/dm2/bulan. Benda uji yang telah mengalami pengelasan dibanding dengan benda uji yang tidak mengalami pengelasan terjadi perbedaan laju korosi yang signifikan.
xvii
ABSTRACT
This research purpose to find out corrosion rate Stainless Steel 304 in sulfuric acid. Immerse process do in 700C temperature for 6 hours and than in 290C temperature for 18 hours every day. This condition aim to get closer to the actual use in the manufacture of tubes of reactor SAMOP (Sub Critical Assembly for Mo99 Prad Action).
Specimen atfer TIG welding and electric arc welding cleaned from crust and than measured, drawing, balanced, and record the first weight. And than specimen innerse to sulfuric acid pH 0,2 and 0,5 in 700C temperature for 6 hours and than in 290C temperature for 18 hours every day for 3 month. Weight recording has done every week.
The survey findings show heavy shrinkage sample, it is well visible on the corrosion pH 0.5 in electric arc welding of 0.105 gram/dm2/month for corrosion 0.026 gram/dm2/month without welding and pH 0.2, arc welding of 0.045 gram/dm2/month, pH 0.2 no Las 0.02 gram/dm2/month. Specimen that has been welded have significant differences in corrosion rate compare to specimen that have not weld..
1
BAB I
PENDAHULUAN
1.1 Latar Belakang Masalah
Berkembangnya jaman dan teknologi mempengaruhi keanekaragaman kebutuhan manusia. Penerapan teknologi di negara- negara industri maju dengan pesat. Hampir semua peralatan dan mesin-mesin industri serta komponen komponennya dirancang sedemikian rupa sehingga dapat diketahui kekuatan maksimum dan umur pakainya. Hal ini membutuhkan waktu penelitian dan ketelitian yang tinggi. Serangkaian proses kimia diperlukan untuk mendapatkan baja dengan sifat mekanik yang diinginkan, misalnya : keuletan, ketangguhan, kekerasan, tahan korosi dan lain-lain.
Dalam tugas akhir ini penulis melakukan penelitian pengaruh larutan HNO3 dengan pH 0,2 dan 0,5 terhadap laju korosi Stainless Steel 304.
Stainless steel jenis ini digunakan untuk tabung Reaktor SAMOP (Sub Critical Assembly for ܯଽଽ Prad Action). Selanjutnya, parameter suhu, waktu dan keasaman, semua dibuat menyerupai kondisi operasi reaktor SAMOP yang sesungguhnya.
1.2 Tujuan Penelitian
Tujuan penelitian ini adalah untuk mengetahui laju korosi Stainless Steel 304 yang telah mengalami pengelasan dalam lingkungan HNO3
2
1.3 Batasan Masalah
Judul dari Tugas Akhir yang penulis susun sebenarnya bisa mencakup permasalahan yang luas, maka agar pembahasannya tidak terlalu banyak dan lebih terarah, maka penulis memberikan batasan permasalahan sebagai berikut:
1. Bahan yang digunakan dalam penelitian adalah stainless steel tipe 304 yang telah mengalami pengelasan.
2. Proses pembuatan larutan HNO3 dengan pH 0,2 dan 0,5 dengan
kondisi awal HNO3 pekat 65 %.
3. Benda uji yang akan diteliti dimasukkan ke dalam tabung kimia berisi larutan HNO3 dengan pH 0,2 dan 0,5. Kemudian tabung ditutup
supaya gas dari larutan tidak mengkorosi lingkungan sekitar.
1.4 Sistematika Penulisan
Penulisan Tugas Akhir ini akan dibagi dalam beberapa bagian, yaitu : 1. Bab I membahas mengenai latar belakang penelitian, batasan masalah,
tujuan penelitian, dan sistematika penulisan.
2. Bab II membahas mengenai tinjauan pustaka yang berisi klasifikasi besi dan baja, sifat-sifat baja, pengaruh unsur spesifik pada baja, struktur mikro besi dan baja, jenis-jenis korosi, pengelasan TIG, dan pengelasan busur listrik yang dilakukan.
3. Bab III membahas mengenai metode penelitian yang berisi skema penelitian, bahan yang digunakan, alat-alat yang digunakan.
3
4. Bab IV membahas mengenai hasil penelitian dan pembahasan yang berisi data dan perhitungan laju korosi benda uji.
5. Bab V membahas mengenai kesimpulan yang diambil dari perhitungan dan data yang ada, serta saran-saran yang diajukan oleh penulis.
4
BAB II
TINJAUAN PUSTAKA
2.1. Klasifikasi Stainless Steel
Dengan pesatnya perkembangan teknologi, manfaat nuklir yang dahulunya dipakai sebagai senjata perang maka sekarang nuklir banyak dimanfaatkan untuk mencukupi kebutuhan manusia. Pemanfaatan teknologi nuklir memiliki banyak keunggulan oleh adanya sifat radiasi yang mudah dideteksi sampai kadar yang sangat rendah, berdaya tembus besar dan dapat dikendalikan baik arah, luas berkas maupun energi partikelnya. Baja tahan karat (stainless steel) sangat cocok untuk pembuatan tabung-tabung reaksi untuk reaksi-reaksi nuklir. Contoh penggunaan stainless steel adalah tabung Reaktor SAMOP (Sub Critical Assembly for ܯଽଽ Prad Action).
2.2. Baja Tahan Karat ( Stainless Steel )
Baja tahan karat (stainless steel) adalah paduan antara besi (Fe) dengan kandungan Cr minimal 12 %. Reaksi oksidasi antara oksigen (O2) dengan
chrom (Cr) membentuk protektif layer (lapisan pelindung anti korosi). Untuk memperbaiki sifat-sifat stainless steel sesuai dengan aplikasinya maka unsur-unsur lain juga ditambahkan. Unsur-unsur-unsur lain yang ditambahkan antara lain Ni (nickel), Mo (molibdenum), Co(copper), Ti (titanium) yang berfungsi untuk meningkatkan ketahanan terhadap temperatur serta korosi.
Golongan utama baja tahan karat (stainless steel) adalah austenit, ferrit, martensit, duplex.
5
2.2.1 Austenit Stainless Steel
Komposisi austenit stainless steel antara 18% Cr dan 8% Ni atau biasa disebut sebagai baja tahan karat delapan belas delapan. Baja tahan karat austenit ketahanan karatnya lebih baik, mampu bentuk dan mampu las. Jenis ini sering digunakan pada berbagai industri kimia, untuk bahan konstruksi, perabot dapur, turbin, mesin jet, mobil, komponen berputar, bangunan kapal,reactor atom, dan sebagainya.
2.2.2 Ferritic Stainless Steel
Kadar chrom sekitar 16% sampai 18% dan kadar nickel sekitar 2%. Ketahanan korosi kurang begitu baik dan relatif sulit untuk difabrikasi atau dimachining. Sifat yang menguntungkan dari baja tahan karat ferit adalah tanpa kandungan Ni sulit untuk terjadi retakan korosi tegangan.
2.2.3 Martensit Stainless Steel
Komposisi baja tahan karat martensit adalah 12%-13% Cr dan 0,1%-0,3% C. Kadar Cr antara 12%-13% merupakan batas terendah untuk ketahanan asam. Baja tahan karat martensit mempunyai ketahanan panas yang baik, dengan pengerasan dan penemperan dapat diperoleh sifat-sifat mekanik yang baik. Baja tahan karat jenis ini digunakan untuk alat potong dan perkakas.
2.2.4 Duplex Stainless Steel
Baja tahan karat jenis duplex mempunyai fasa ganda yaitu fasa austenit dan ferit. Umumnya mempunyai komposisi 12% Cr + 5% Ni + 1,5% Mo + 0,03% C. Memiliki sifat kombinasi antara sifat austenite dan
6
ferit yang saling menutupi. Sebagai contoh, tegangan mulur yang rendah dari sifat austenit diperbaiki dengan adanya sifat ferit. Dan keuletan rendah dari sifat ferit diperbaiki oleh sifat austenit. Ketahanan korosi pada umumnya melebihi baja 18-8, terutama baja yang mempunyai kadar Cr tinggi dan mengandung Mo sangat baik dalam ketahanan korosi lubangnya sehingga baja ini dapat dipakai untuk penukar panas yang menggunakan air laut.
2.3 Pengaruh Unsur Paduan Pada Stainless Steel
Dalam aplikasi, stainless steel selain dibutuhkan sebagai logam yang tahan terhadap korosi juga dibutuhkan sifat tambahan guna meningkatkan sifat mekaniknya. Peningkatan sifat mekanik ini tergantung pada sejumlah unsur yang terkandung dalam stainless steel. Unsur-unsur tambahan dalam stainless steel antara lain sebagai berikut :
1. Kromium (Cr) berguna untuk membentuk lapisan pasif untuk melindungi dari korosi.
2. Nikel (Ni) sebagai penstabil austenit, meningkatkan sifat mekanik, meningkatkan ketahanan korosi pada lingkungan asam mineral.
3. Mangan (Mn) membantu fungsi Ni.
4. Molybdenum (Mo) sebagai penstabil lapisan pasif dalam lingkungan yang mengandung banyak ion klorida (Cl - ), seperti lingkungan air laut (NaCl).
5. Karbon (C) meningkatkan kemampuan dikeraskan (hardenability) dari material Stainless Steel.
7
6. Nitrogen (N) membentuk duplex stainlees steel dengan meningkatkan terbentuknya austenit, meningkatkan sifat mekanik Stainless Steel. 2.4 Korosi Pada Logam
2.4.1 Korosi Secara Umum
Stainless steel (SS) secara mendasar bukanlah logam mulia seperti halnya emas (Au) & platina (Pt) yang hampir tidak mengalami korosi karena pengaruh kondisi lingkungan, sementara SS masih mengalami korosi. Daya tahan korosi SS disebabkan karena adanya lapisan yang tidak terlihat (invisible layer) yang terjadi akibat oksidasi SS dengan oksigen yang akhirnya membentuk lapisan pelindung anti korosi (protective layer). Sumber oksigen bisa berasal dari udara maupun air. Material lain yang memiliki sifat sejenis antara lain titanium (Ti) dan juga aluminium (Al). Secara umum protective layer terbentuk dari reaksi kromium + oksigen secara spontan membentuk krom-oksida. Jika lapisan oksida S tergores/terkelupas, maka protective layer akan segera terbentuk secara spontan, tentunya jika kondisi lingkungan cukup mengandung oksigen (Gambar 2.1). Walaupun demikian kondisi lingkungan tetap menjadi penyebab kerusakan protective layer tersebut. Pada keadaan dimana protective layer tidak dapat lagi terbentuk, maka korosi akan terjadi. Banyak media yang dapat menjadi penyebab korosi, seperti halnya udara, cairan/ larutan yang bersifat asam/basa, gas-gas proses (misalnya gas asap hasil buangan ruang bakar atau reaksi kimia lainnya), logam yang berlainan jenis dan saling berhubungan dan sebagainya.
8
Gambar 2.1 Pembentukan spontan lapisan oksida
2.4.2 Jenis-Jenis Korosi Pada Stainless Steel
Meskipun alasan utama penggunaan stainless steel adalah ketahanan korosinya, tetapi pemilihan stainless steel yang tepat harus disesuaikan dengan aplikasi yang tepat pula. Pada umumnya, korosi menyebabkan beberapa masalah seperti :
1. Terbentuknya lubang-lubang kecil/halus pada tangki dan pipa-pipa sehingga menyebabkan kebocoran cairan ataupun gas.
2. Menurunnya kekuatan material disebabkan penyusutan atau pengurangan ketebalan atau volume material sehingga kekuatan juga menurun, akibatnya dapat terjadi retak, bengkok, patah dan sebagainya.
9
3. Penampilan permukaan material menjadi tidak menarik disebabkan kerak karat ataupun lubang-lubang
4. Terbentuknya karat-karat yang mungkin mengkontaminasi zat atau material lainnya, hal ini sangat dihindari khususnya pada proses produksi makanan.
Secara umum korosi pada stainless steel dapat dikategorikan sebagai berikut. :
1. Uniform Corrosion 2. Pitting Corrosion
3. Crevice Corrosion
4. Stress Corrosion Cracking 5. Intergranular Corrosion 6. Galvanic Corrosion
2.4.2.1 Uniform Corrosion
Uniform corrosion terjadi disebabkan rusaknya sebagian atau seluruh protective layer pada SS sehingga SS secara merata akan berkurang/aus terlihat pada (Gambar 2.2). Korosi ini terjadi umumnya disebabkan oleh cairan atau larutan asam kuat maupun alkali panas. Asam hidroklorit dan asam hidrofluor adalah lingkungan yang perlu dihindari SS apalagi dikombinasikan dengan temperatur serta konsentrasi yang cukup tinggi.
10
Gambar 2.2 Korosi uniform yang menyebabkan berkurangnya dimensi permukaan benda secara merata. (Sumber: Surdia, T., Saito, S.)
2.4.2.2 Pitting Corrosion
Korosi berupa lubang-lubang kecil sebesar jarum, dimana dimulai dari korosi lokal (bukan seperti uniform corrosion). Pitting corrosion ini awalnya terlihat kecil dipermukaan SS tetapi semakin membesar pada bagian dalam SS yang tersaji pada (Gambar 2.3). Korosi ini terjadi pada beberapa kondisi pada lingkungan dengan PH rendah, temperatur moderat, serta konsentrasi klorida yang cukup tinggi (misal NaCl atau garam di air laut). Pada konsentrasi klorida yang cukup tinggi, awalnya ion-ion klorida merusak protective layer pada permukaan SS terutama permukaan yang cacat. Timbulnya cacat ini dapat disebabkan oleh kotoran sulfida, retak-retak kecil akibat penggerindaan, pengelasan, penumpukan kerak, penumpukan larutan padat. Proses kimia yang terjadi saat pitting korosi ini dapat dilihat dalam (Gambar 2.4). Umumnya SS berkadar krom (Cr), molybdenum (Mo) dan nitrogen (N) yang tinggi cenderung lebih tahan terhadap pitting corrosion. Pada industri petrokimia korosi ini sangat berbahaya karena menyerang permukaan dan penampakan visualnya sangat kecil, sehingga sulit untuk
11
diatasi dan dicegah terutama pada pipa-pipa bertekanan tinggi. Ketahanan material terhadap pitting korosi jenis ini di formulasikan sbb :
PREN = %Cr + (3,3 x %Mo) + (16 x %N)
Satu hal yang menyebabkan pitting corrosion sangat serius bahwa ketika lubang kecil terbentuk, maka lubang ini akan terus cenderung berkembang (lebih besar dan dalam) meskipun kondisi SS tersebut sangat tertutup atau tidak dapat tersentuh sama sekali. Oleh karena itu dalam mendesain material untuk lingkungan kerja yang besar kemungkinan terjadinya pitting korosi digunakan nilai PREN, sebagai acuan. Contohnya bila dibandingkan antara SS austenitik seperti 304, 316L, dan SS super-austenitik seperti UR 6B. SS 304 memiliki komposisi (dalam %): < 0,015 C, 18.5 Cr, 12 Ni sedangkan untuk SS 316L memiliki komposisi : < 0,030 C, 17.5 Cr, 13,5 Ni, 2,6 Mo. SS super-austenitik UR 6B memiliki komposisi : < 0,020 C, 20 Cr, 25 Ni, 4,3 Mo, dan 0,13 N. Dengan komposisi yang berbeda maka nilai PREN untuk masing-masing SS adalah: 304 = 18, 316L = 26, dan UR B6 = 37. Dengan demikian UR B6 memiliki ketahanan akan pitting korosi paling kuat sedangkan 304 memiliki ketahanan pitting korosi yang terlemah.
12
Gambar 2.3 IIustrasi pitting corrosion pada material SS. (Sumber: Surdia, T., Saito, S.)
Gambar 2.4 Skema proses kimia yang terjadi saat pitting corrosion menyerang dan terus merusak logam SS.(Sumber: Surdia, T., Saito, S.)
2.4.2.3 Crevice Corrosion
Korosi jenis ini sering terjadi di daerah yang kondisi oksidasi terhadap krom (Cr) SS sangat rendah bahkan tidak ada sama sekali (miskin oksigen). Sering pula terjadi akibat desain konstruksi peralatan yang tidak memungkinkan terjadinya oksidasi tersebut misal celah antara gasket/packing, celah yang terbentuk akibat pengelasan yang tidak sempurna, sudut-sudut yang sempit, celah/sudut antara 2 atau lebih lapisan metal, celah
13
antara mur/baut dsb. Peristiwa korosi ini terjadi di daerah yang sangat sempit (celah, sudut, takik dsb) seperti disajikan pada (Gambar 2.5). Crevice Corrosion dapat dipandang sebagai pitting corrosion yang lebih berat/hebat dan terjadi pada temperatur di bawah temperature moderat yang biasa menyebabkan pitting corrosion. Cara untuk menghindari masalah ini, salah satunya dengan membuat desain peralatan lebih 'terbuka' walaupun kenyataannya sangat sulit untuk semua aplikasi.
Gambar 2.5 Ilustrasi crevice corrosion yang menyerang saat 2 material bertemu dan membentuk celah sempit, sehingga terjadi perbedaan kandungan oksigen yang menyebabkan korosi. (Sumber: Surdia, T., Saito, S.)
2.4.2.4 Stress Corrosion Cracking
Dalam kondisi kombinasi antara tegangan (baik tensile, torsion, compressive maupun thermal) dan lingkungan yang korosif maka SS cenderung lebih cepat mengalami korosi. Karat yang mengakibatkan berkurangnya penampang luas efektif permukaan SS menyebabkan tegangan kerja (working Strees) pada SS akan bertambah besar. Korosi ini dapat terjadi pula misalnya pada pin, baut-mur dengan lubangnya/ dudukannya, SS yang
14
memiliki tegangan sisa akibat rolling, bending, welding dan sebagainya. Ilustrasi dari korosi ini dapat dilihat pada (Gambar 2.6). Korosi ini meningkat jika part yang mengalami stress berada di lingkungan dengan kadar klorida tinggi seperti air laut yang temperaturnya cukup tinggi. Sebagai akibatnya aplikasi SS dibatasi untuk menangani cairan panas bertemperatur di atas 50 0C bahkan dengan kadar klorida yang sangat sedikit sekalipun (beberapa ppm). SS yang cocok korosi ini adalah austenitic SS disebabkan kadar Nikel-nya (Ni) relatife tinggi. Grade 316 secara siknifikan tidak lebih tahan dibanding 304. Duplex SS (misal 2205/UR 45N) lebih tahan dibanding 304 atau 316, bahkan sampai temperature aplikasi 150ºC dan super duplex akan lebih tahan lagi terhadap stress corrosion cracking. Pada beberapa kasus, korosi ini dapat dikurangi dengan cara penembakan permukaan logam dengan butir pasir logam, atau juga meng-annealing setelah SS selesai proses permesinan, sehingga dapat mengurangi tegangan pada permukaan logam.
15
Gambar 2.6 Ilustrasi stress-cracking-corrosion akibat adanya tegangan sisa dan lingkungan korosif. (Sumber: Surdia, T., Saito, S.)
2.4.2.5 Intergranular Corrosion
Korosi ini disebabkan ketidaksempurnaan mikrostruktur SS. Ketika austenic SS berada pada temperatur 425-850º C (temperatur sensitasi) atau ketika dipanaskan dan dibiarkan mendingin secara perlahan (seperti halnya sesudah welding atau pendinginan setelah annealing) maka karbon akan menarik krom untuk membentuk partikel kromium karbida (chromium carbide) di daerah batas butir (grain boundary) struktur SS. Formasi kromium karbida yang terkonsentrasi pada batas butir akan menghilangkan/mengurangi sifat perlindungan kromium pada daerah tengah
16
butir. Sehingga daerah ini akan dengan mudah terserang oleh korosi (Gambar 2.7). Umumnya SS dengan kadar karbon kurang dari 2 % relative tahan terhadap korosi ini. Ketidaksempurnaan mikrostruktur ini diperbaiki dengan menambahkan unsur yang memiliki daya tarik terhadap karbon lebih besar untuk membentuk karbida, seperti Titanium (missal pada SS 321) dan Niobium (misal pada SS 347). Cara lain adalah dengan menggunakan SS berkadar karbon rendah yang ditandai indeks 'L' -low carbon steel- (misal 316L atau 304L). SS dengan kadar karbon tinggi akan tahan terhadap korosi jenis ini asalkan digunakan pada temperatur tinggi pula (misal 304H, 316H, 321H, 347H).
Gambar 2.7 Ilustrasi korosi pada butir akibat terjadinya sensitasi krom (Cr).
(Sumber: Surdia, T., Saito, S.)
2.4.2.6 Galvanic Corrosion
Galvanic corrosion terjadi disebabkan sambungan dissimilar material (2 material yang berbeda terhubung secara elektris/ tersambung misal baut dengan mur, paku keling/rivet dengan bodi tangki, hasil welding dengan benda kerja) dan atau terendam dalam larutan elektrolit, sehingga dissimilar
17
material tersebut menjadi semacam sambungan listrik. Mekanisme ini disebakan satu material berfungsi sebagai anoda dan yang lainnya sebagai katoda sehingga terbentuk jembatan elektrokimia tersaji pada (Gambar 2.8). Dengan terjadinya hubungan elektrik tersebut maka logam yang bersifat anoda akan lebih mudah terkorosi. Urutan tersebut ditunjukkan pada seri elektrokimia logam berikut . Logam deret sebelah kiri cenderung menjadi anoda (mudah berkarat) sementara logam sebelah kanan cenderung menjadi katoda. Galvanic corrosion ini tergantung pada :
1. Perbedaan ke-mulia-an dissimilar material
2. Rasio luas permukaan dissimilar material, dan konduktifitas
Gambar 2.8 Ilustrasi terjadinya korosi antara dua logam yang berbeda jenis keaktifannya (logam A dan B). (Sumber: Surdia, T., Saito, S.)
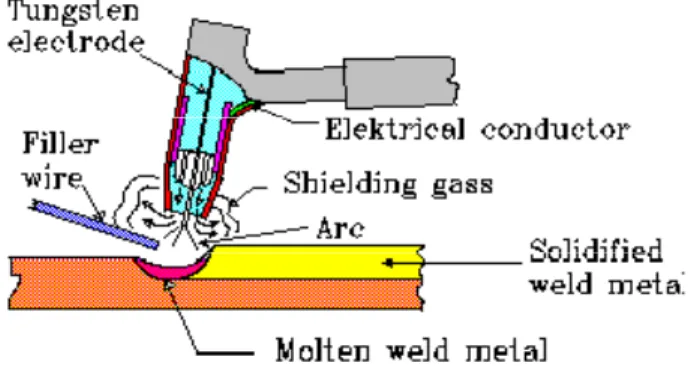
2.5 Pengelasan Berperisai Tungsen (TIG)
Proses ini merupakan suatu metode pengelasan dengan jalan dimana suatu busur api listrik dipertahankan diantara sebuah elektroda tungsen yang bukan mampu habis yang pada hakekatnya berdiri sendiri, dalam suatu atmosfer argon murni, dengan atau tanpa tambahan kecil gas-gas
18
berfaedah lain. Perisai gas mencegah kontaminasi logam las oleh udara. Permukaan paduan alumunium ditutupi oleh lapisan oksida tahan api bertitik lebur tinggi yang harus dihilangkan sebelum suatu las yang memuaskan dapat dibuat. Suatu kawat pengisi dapat juga ditambahkan pada tepi depan genangan cairan untuk membentuk las. Ini merupakan salah satu sifat busur api arus bolak-balik sehingga menghilangkan oksida yang kuat selama proses pengelasan. Proses pengelasan TIG dipakai bila diperlukan las yang rapi, berkualitas tinggi, dan ekonomis untuk ketebalan sampai 6 mm. Untuk ketebalan yang lebih dari 6 mm, biasanya digunakan pengelasan MIG, atau proses pengelasan busur api logam lainnya. Lubang-lubang akar, di dalam sambungan pipa dengan atau tanpa sisipan yang mampu lebur dimasuki dengan menggunakan pengelasan TIG karena penetrasi dapat dikontrol untuk memberikan suatu akhir siraman yang halus.
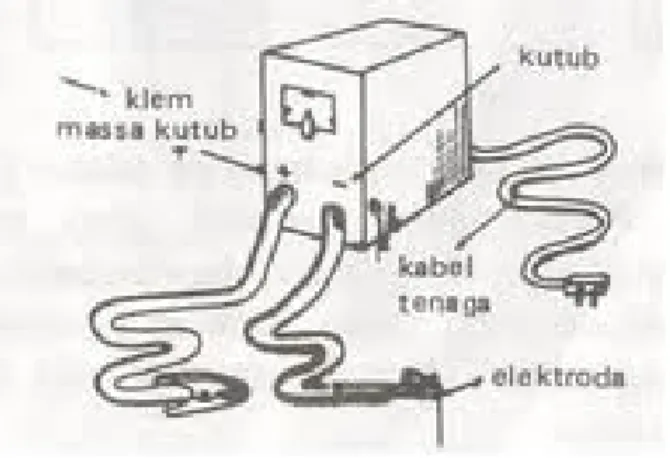
Gambar 2.9 Alat pengelasan TIG 2.6 Las Busur Listrik
Las busur listrik adalah salah satu cara menyambung logam dengan jalan menggunakan nyala busur listrik yang diarahkan ke permukaan logam yang akan disambung. Pada bagian yang terkena busur listrik tersebut akan
19
mencair, demikian juga elektroda yang menghasilkan busur listrik akan mencair pada ujungnya dan merambat terus sampai habis. Logam cair dari elektroda dan dari sebagian benda yang akan disambung tercampur dan mengisi celah dari kedua logam yang akan disambung, kemudian membeku dan tersambunglah kedua logam tersebut. Mesin las busur listrik dapat mengalirkan arus listrik cukup besar tetapi dengan tegangan yang aman (kurang dari 45 volt). Busur listrik yang terjadi akan menimbulkan energi panas yang cukup tinggi sehingga akan mudah mencairkan logam yang terkena. Besarnya arus listrik dapat diatur sesuai dengan keperluan dengan memperhatikan ukuran dan type elektrodanya. Pada las busur, sambungan terjadi oleh panas yang ditimbulkan oleh busur listrik yang terjadi antara benda kerja dan elektroda. Elektroda atau logam pengisi dipanaskan sampai mencair dan diendapkan pada sambungan sehingga terjadi sambungan las. Mula-mula terjadi kontak antara elektroda dan benda kerja sehingga terjadi aliran arus, kemudian dengan memisahkan penghantar timbullah busur. Energi listrik diubah menjadi energi panas dalam busur dan suhu dapat mencapai 5500 °C. Ada tiga jenis elektroda logam, yaitu elektroda polos, elektroda fluks dan elektroda berlapis tebal. Elektroda polos terbatas penggunaannya, antara lain untuk besi tempa dan baja lunak. Biasanya digunakan polaritas langsung. Mutu pengelasan dapat ditingkatkan dengan memberikan lapisan fluks yang tipis pada kawat las. Fluks membantu melarutkan dan mencegah terbentuknya oksida-oksida yang tidak diinginkan.
20
Tetapi kawat las berlapis merupakan jenis yang paling banyak digunakan dalam berbagai pengelasan komersil
21
BAB III
METODE PENELITIAN
3.1 Bagan Alir penelitian
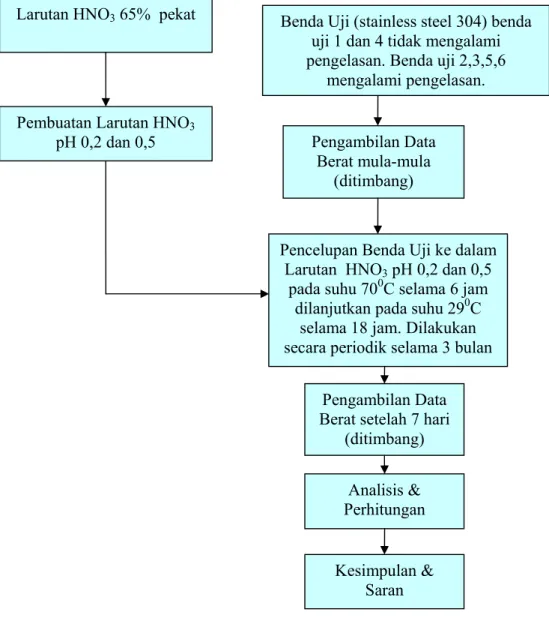
Bagan alir penelitian ditunjukkan di dalam Gambar 3.1 :
Gambar 3.1 Diagram alir penelitian
Benda Uji (stainless steel 304) benda uji 1 dan 4 tidak mengalami pengelasan. Benda uji 2,3,5,6
mengalami pengelasan. Larutan HNO3 65% pekat
Pengambilan Data Berat setelah 7 hari
(ditimbang)
Kesimpulan & Saran Analisis & Perhitungan Pembuatan Larutan HNO3
pH 0,2 dan 0,5
Pencelupan Benda Uji ke dalam Larutan HNO3 pH 0,2 dan 0,5
pada suhu 700C selama 6 jam dilanjutkan pada suhu 290C
selama 18 jam. Dilakukan secara periodik selama 3 bulan
Pengambilan Data Berat mula-mula
3 3.2 Baha 3.2.1 1 2 3.2.2 P an dan Pera 1 Bahan 1. Spesim Bahan 304, de 0,047% Ga 2. Larutan Larutan Univers 2 Peralata Peralatan yan alatan men / benda u yang digun engan komp %, Fe = 70,47 ambar 3.2. St n HNO3 65% n HNO3 65% sitas Sanata Gambar 3.3 an ng digunakan uji nakan sebaga posisi : Cr 7% ainless steel 3 %. % ini dibeli Dharma Yo 3. Larutan HN n dalam pen ai spesimen = 18,358% 304 yang dila dari laborat ogyakarta. NO3 65%. nelitian ini ad n adalah stai %, Ni = 8,4 as torium jurus dalah : 22 inless steel 408%, C = san farmasi
23
1. Tabung Reaksi, milik Laboratorium Analisis, Jurusan Farmasi Universitas Sanata Dharma, Yogyakarta.
Gambar 3.4 Tabung Reaksi
2. pH meter Elektrik Digital, milik Laboratorium Analisis, Jurusan Farmasi Universitas Sanata Dharma, Yogyakarta.
24
3. Timbangan Elektrik Digital, milik Laboratorium Analisis dan Instrumen, Jurusan Farmasi Universitas Sanata Dharma,
Yogyakarta, dengan ketelitian sampai 1000
1
gram.
Gambar 3.6 Timbangan Digital
4. Water Bath dan Thermometer , milik Laboratorium Analisis, Jurusan Farmasi Universitas Sanata Dharma, Yogyakarta.
25
4. Proses Pembuatan Larutan HNO3 pH 0,2 dan 0,5 Dan Proses
Perendaman
Proses pembuatan larutan HNO3 pH 0,2 dan 0,5 dari larutan HNO3
pekat 65% dilakukan pencampuran dengan aquades. Langkah-langkah dalam proses tersebut :
1. Peralatan dan bahan yang disiapkan : a. Tabung reaksi
b. Larutan HNO3 65%
c. Pipet
d. pH Meter Elektrik Digital e. Aquades
2. Dalam keadaan normal kadar 1 normalitas (N) HNO3 = 63 gr/ltr HNO3
murni. Maka untuk memperoleh larutan HNO3 dengan pH 0,2 dari
larutan HNO3 65 % dengan berat jenis 1,39 diambil 34,23 ml. Ini
diperoleh dari : pH 0,2 = 10−0,2N = 0,631 N Maka, 63 39 , 1 1 65 100 631 , 0 × × × = 43,9 ml/ltr
Untuk memperoleh larutan HNO3 pH 0,5 dari larutan HNO3 65 %
dengan berat jenis 1,39 diambil 22,05 ml. Ini diperoleh dari : pH 0,5 = 10−0,5N
26 Maka, 63 39 , 1 1 65 100 3162 , 0 × × × = 22,05 ml/ltr
kemudian HNO3 65 % dimasukan ke dalam tabung reaksi dan
ditambahkan aquades sedikit demi sedikit sampai volumenya 1 liter. Kemudian diukur pHnya dengan menggunakan pH meter.
3. Spesimen dimasukkan ke dalam masing-masing tabung reaksi yang telah berisi Larutan HNO3 pH 0,2 dan 0,5.
4. Tabung reaksi dimasukkan ke dalam water bath yang telah diatur suhunya.
5. Proses pencelupan dilakukan pada suhu larutan dalam tabung 700 C selama 6 jam dan suhu 290C selama 18 jam. Hal ini untuk mendekatkan pada penggunaan secara nyata di dalam prakteknya. 6. Dalam waktu 1 minggu spesimen diambil, dikeringkan dan ditimbang.
Setelah itu spesimen dicelup ke dalam larutan yang sama dengan volume sama yaitu 1 liter. Karena adanya penguapan maka setiap hari perlu ditambahkan larutan untuk menjaga pH dan kejenuhannya.
5. Analisis Hasil
Secara garis besar, penelitian ini bertujuan untuk mendapatkan laju korosi Stainless Steel 304 yang telah mengalami pengelasan TIG & busur listrik dalam larutan HNO3 pH 0,2 dan 0,5 pada suhu 700C selama 6 jam
27
BAB IV
HASIL DAN PEMBAHASAN
4.1 Larutan HNO3 pH 0,5
A. Stainless Steel Tanpa Mengalami Pengelasan TIG (Benda Uji I)
Benda uji I merupakan pelat stainless steel tanpa mengalami pengelasan,direndam pada larutan HNO3 pH 0,5.
Gambar 4.1 Benda uji I sebelum mengalami perendaman selama 3 bulan Data Spesimen I :
1. Tebal benda uji = 3 mm
2. Berat mula-mula = 14,608 gram 3. Panjang benda uji = 34 mm 4. Lebar benda uji = 18 mm Analisis Perhitungan
Rumus laju korosi:
t
A
y
korosi
Laju
.
∆
=
Dengan:28
t = Waktu (Jam, Bulan, Tahun) A = Luas permukaan (mm2
, dm2)
Dalam persoalan ini digunakan ∆ y dengan satuan gram dan waktu dihitung dalam satuan Jam. Hal ini dikarenakan untuk mempermudah pengamatan. Dalam penelitian ini benda uji dicelupkan kedalam larutan HNO3 pH 0,5 dengan suhu 700C selama
6 jam dilanjutkan pada suhu 290C selama 18 jam setiap harinya. Hal ini untuk mendekatkan pada keadaan sebenarnya.
Gambar 4.2 Keterangan luas benda uji Luas spesimen = luas I +luas II + luas III Luas I = (34 mm x 18 mm) x 2 = 1224mm2 Luas II = (34 mm x 3 mm) x 2 = 204 mm2 Luas III = (18 mm x 3 mm) x2 = 108 mm2 Luas spesimen = (1224 mm2 + 204 mm2 + 108 mm2) Luas I Luas II Luas III
29
= 1536 mm2 = 0,1536 dm2
Data perubahan berat benda uji I pada larutan HNO3 pH 0,5
Tabel 4.1 Data perubahan berat benda uji I pada larutan HNO3 pH 0,5. No Minggu ke- Berat benda uji
(gram) 1 0 14,608 2 I 14,608 3 II 14,607 4 III 14,606 5 IV 14,606 6 V 14,603 7 VI 14,601 8 VII 14,601 9 VIII 14,598 10 IX 14,597 11 X 14,597 12 XI 14,596 13 XII 14,596
Dari data diperoleh maka laju korosi :
∆y = Berat mula-mula – Berat pada minggu I Laju korosi minggu II =
2 ) 0,1536 ( 001 , 0 x = 0,013 gram/dm 2/minggu.
30
Tabel 4.2 Laju korosi benda uji I pada larutan HNO3 pH 0,5
No Minggu Ke - Berat Awal (gram) Berat Akhir (gram) Penurunan Berat (gram) Luas (mm2) Laju Korosi (gram/dm2/jam) 1 1 14,608 14,608 - 0,1536 0 2 2 14,608 14,607 0,001 0,1536 0,013 3 3 14,607 14,606 0.001 0,1536 0,019 4 4 14,606 14,606 - 0,1536 0 5 5 14,606 14,603 0,003 0,1536 0,097 6 6 14,603 14,601 0,002 0,1536 0,078 7 7 14,601 14,601 - 0,1536 0 8 8 14,601 14,598 0,003 0,1536 0,156 9 9 14,598 14,597 0,001 0,1536 0,058 10 10 14,597 14,597 - 0,1536 0 11 11 14,597 14,596 0,001 0,1536 0,0716 12 12 14,596 14,596 - 0,1536 0
B. Stainless Steel Yang Mengalami Pengelasan TIG (Benda Uji II)
Data percobaan laju korosi Stainless Steel 304 yang telah mengalami pengelasan pada larutan HNO3 pH 0,5.
Gambar benda uji II :
Gambar 4.3 Benda uji II mula – mula Data Spesimen (benda uji II)
1. Tebal benda uji = 3 mm
31
3. Panjang benda uji = 35 mm 4. Lebar benda uji = 16,5 mm
Data perubahan berat Stainless Steel 304 yang telah mengalami pengelasan pada larutan HNO3 pH 0,5 :
Tabel 4.3 Data perubahan berat Stainless Steel 304 yang telah mengalami pengelasan pada larutan HNO3 pH 0,5
No Minggu ke- Berat benda uji (gram) 1 0 13,795 2 I 13,795 3 II 13,793 4 III 13,789 5 IV 13,786 6 V 13,783 7 VI 13,780 8 VII 13,778 9 VIII 13,776 10 IX 13,772 11 X 13,771 12 XI 13,770 13 XII 13,770
Luas spesimen = luas I + luas II + luas III Luas I = (35 mm x 16,5 mm) x 2 = 1155mm2 Luas II = (35 mm x 3 mm) x 2 = 210 mm2 Luas III = (16,5 mm x 3 mm) x2 = 99 mm2 Luas spesimen = (1155 mm2 + 210 mm2 + 99 mm2) = 1464 mm2 = 0,1464 dm2
32
Dari data diperoleh laju korosi : Laju korosi pada minggu II :
Berat mula-mula = 13,795 gram Berat pada minggu II = 13,793 gram
Waktu = 168 jam
Maka diperoleh,
∆y = Berat mula-mula – Berat pada minggu II = 13,795gram – 13,793 gram = 0,002 gram Laju korosi minggu II =
2 ) 0,1464 ( 002 , 0 x = 0,027 gram/dm 2/minggu.
Tabel 4.4 Laju korosi SS 304 setelah mengalami pengelasan dalam larutan HNO3 pH 0,5
No Minggu Ke -Berat Awal (gram) Berat Akhir (gram) Penurunan Berat (gram) Luas (dm2) Laju Korosi (gram/dm2/jam) 1 1 13,795 13,795 - 0,1464 0 2 2 13,795 13,793 0,002 0,1464 0,027 3 3 13,793 13,789 0,004 0,1464 0,081 4 4 13,789 13.786 0,003 0,1464 0.081 5 5 13,786 13.783 0,003 0,1464 0,102 6 6 13,783 13.780 0,003 0,1464 0,122 7 7 13,780 13.778 0,002 0,1464 0,095 8 8 13,778 13,776 0,002 0,1464 0,109 9 9 13,776 13,772 0,004 0,1464 0,245 10 10 13,772 13,771 0,001 0,1464 0,068 11 11 13,771 13,770 0,001 0,1464 0,075 12 12 13,770 13,770 - 0,1464 0
33
C. Stainlees Steel Yang Mengalami Pengelasan Busur Listrik
(Benda Uji III)
Benda uji III merupakan pelat stainless steel 304 yang telah mengalami pengelasan busur listrik.
Gambar benda uji III :
Gambar 4.4 Benda uji III setelah mengalami perendaman selama 13 minggu Data Spesimen III
1. Tebal benda uji = 3 mm
2. Berat mula-mula = 16,081 gram 3. Panjang benda uji = 36 mm 4. Lebar benda uji = 17 mm
Luas spesimen = luas I +luas II + luas III Luas I = (36 mm x 17 mm) x 2 = 1224mm2 Luas II = (36 mm x 3 mm) x 2 = 216 mm2 Luas III = (17 mm x 3 mm) x2 = 102 mm2
34
Luas spesimen = (1224 mm2 + 216 mm2 + 102 mm2) = 1542 mm2 = 0,1542 dm2 Data perubahan berat benda uji III pada larutan HNO3 pH 0,5 :
Tabel 4.5 Data perubahan berat benda uji III pada larutan HNO3 pH 0,5
No Minggu ke- Berat benda uji (gram) 1 0 16,081 2 I 16,081 3 II 16,074 4 III 16,058 5 IV 16,046 6 V 16,041 7 VI 16,041 8 VII 16,039 9 VIII 16,038 10 IX 16,035 11 X 16,033 12 XI 16,032 13 XII 16,031
Laju korosi minggu II =
2 ) 0,1542 ( 007 , 0 x = 0,09 gram/dm 2/minggu.
35
Tabel 4.6 Laju korosi benda uji III pada larutan HNO3 pH 0,5
No Minggu Ke -Berat Awal (gram) Berat Akhir (gram) Penurunan Berat (gram) Luas (mm2) Laju Korosi (gram/dm2/jam) 1 1 16,081 16,081 - 0,1542 -2 2 16,081 16,074 0,007 0,1542 0,09 3 3 16,074 16,058 0.006 0,1542 0,116 4 4 16,058 16,046 0,001 0,1542 0,025 5 5 16,046 16,041 0,005 0,1542 0,162 6 6 16,041 16,041 - 0,1542 -7 7 16,041 16,039 0,002 0,1542 0,09 8 8 16,039 16,038 0,001 0,1542 0,051 9 9 16,038 16,035 0,003 0,1542 0,175 10 10 16,035 16,033 0,002 0,1542 0,129 11 11 16,033 16,032 0,001 0,1542 0,071 12 12 16,032 16,031 0,001 0,1542 0,077 4.2 Larutan HNO3 pH 0,2
A. Stainless steel Tanpa Mengalami Pengelasan TIG (Benda Uji IV)
Data percobaan laju korosi stainless steel 304 tanpa mengalami pengelasan pada larutan HNO3 pH 0,2.
Gambar benda uji IV :
36
Data Spesimen IV :
1. Tebal benda uji = 3 mm
2. Berat mula-mula = 13,478 gram 3. Panjang benda uji =33,5 mm 4. Lebar benda uji = 17 mm
Luas spesimen = luas I +luas II + luas III Luas I = (33,5 mm x 1 mm) x 2 = 1139mm2 Luas II = (33,5 mm x 3 mm) x 2 = 201 mm2 Luas III = (17 mm x 3 mm) x2 = 102 mm2 Luas spesimen = (1139 mm2 + 201 mm2 + 102 mm2) = 1442 mm2 = 0,1442 dm2
Tabel 4.7 Data perubahan berat benda uji IV pada larutan HNO3 pH 0,2 No Minggu ke- Berat benda uji
(gram) 1 0 13,478 2 I 13,478 3 II 13,476 4 III 13,473 5 IV 13,470 6 V 13,469 7 VI 13,466 8 VII 13,466 9 VIII 13,462 10 IX 13,460 11 X 13,460
37
12 XI 13,460
13 XII 13,469
Dari data diperoleh maka laju korosi : Laju korosi minggu II =
2 ) 0,1442 ( 002 , 0 x = 0,027 gram/dm 2/minggu.
Tabel 4.8 Laju korosi benda uji IV pada larutan HNO3 pH 0,2 No Minggu Ke -Berat Awal (gram) Berat Akhir (gram) Penurunan Berat (gram) Luas (mm2) Laju Korosi (gram/dm2/jam) 1 1 13,478 13,478 - 0,1442 -2 2 13,478 13,476 0,002 0,1442 0,027 3 3 13,476 13,473 0,003 0,1442 0,062 4 4 13,473 13,470 0.003 0,1442 0.083 5 5 13,470 13,469 0,001 0,1442 0,034 6 6 13,469 13,466 0,003 0,1442 0,124 7 7 13,466 13,466 - 0,1442 -8 8 13,466 13,462 0,004 0,1442 0,221 9 9 13,462 13,460 0.002 0,1442 0,124 10 10 13,460 13,460 - 0,1442 -11 11 13,460 13,460 - 0,1442 -12 12 13,460 13,469 0,001 0,1442 0,083
B. Stainless Steel Yang Mengalami Pengelasan TIG (Benda Uji V)
Data percobaan laju korosi stainless steel 304 yang telah mengalami pengelasan pada larutan HNO3 pH 0,2.
38
Gambar benda uji V :
Gambar 4.6 Benda uji V setelah mengalami perendaman selama 12 minggu Data Spesimen V :
1. Tebal benda uji = 3 mm
2. Berat mula-mula = 14,364 gram 3. Panjang benda uji = 35 mm 4. Lebar benda uji = 16,5 mm
Data perubahan berat benda uji V pada larutan HNO3 pH 0,2
Tabel 4.9 Data perubahan berat benda uji V pada larutan HNO3 pH 0,2 No Minggu ke- Berat benda uji
(gram) 1 0 14,364 2 I 14,364 3 II 14,362 4 III 14,358 5 IV 14,352 6 V 14,359 7 VI 14,356 8 VII 14,355 9 VIII 14,352 10 IX 14,349 11 X 14,349 12 XI 14,349 13 XII 14,348
39
Luas spesimen = luas I +luas II + luas III Luas I = (35 mm x 16,5 mm) x 2 = 1155mm2 Luas II = (35 mm x 3 mm) x 2 = 210 mm2 Luas III = (16,5 mm x 3 mm) x2 = 99 mm2 Luas spesimen = (1155 mm2 + 210 mm2 + 99 mm2) = 1464 mm2 = 0,1464 dm2 Tabel 4.10 Laju korosi benda uji V pada larutan HNO3 pH 0,2. No Minggu Ke -Berat Awal (gram) Berat Akhir (gram) Penurunan Berat (gram) Luas (mm2) Laju Korosi (gram/dm2/ja m) 1 1 14,364 14,364 - 0,1464 -2 2 14,364 14,362 0,002 0,1464 0,027 3 3 14,362 14,358 0,004 0,1464 0,081 4 4 14,358 14,352 0.006 0,1464 0,163 5 5 14,352 14,359 0,003 0,1464 0,102 6 6 14,359 14,356 0,003 0,1464 0,122 7 7 14,356 14,355 0,001 0,1464 0,047 8 8 14,355 14,352 0,003 0,1464 0,163 9 9 14,352 14,349 0.003 0,1464 0,184 10 10 14,349 14,349 - 0,1464 -11 11 14,349 14,349 - 0,1464 -12 12 14,349 14,348 0,001 0,1464 0,081
C. Gamba Stainless S (Benda Uj Ben mengalami Gambar be ar 4.7 Benda Data Spesim 1. Tebal b 2. Berat m 3. Panjang 4. Lebar b Luas spesim Luas I Luas II Luas III Steel Yang M i VI)
nda uji III m i pengelasan enda uji VI : uji VI setelah men VI benda uji = 3 mula-mula = g benda uji = benda uji = 1 men = luas I = (36 = 1224 = (36 = 216 = (17 = 102 Mengalami merupakan p n busur listrik h mengalami p 3 mm 16,081 gram = 36 mm 17 mm I +luas II + lu mm x 17 mm 4mm2 mm x 3 mm mm2 mm x 3 mm mm2 Pengelasan pelat stainles k. perendaman s m uas III m) x 2 m) x 2 m) x2 n Busur List ss steel 304 selama 12 mi 40 trik yang telah inggu
41
Luas spesimen = (1224 mm2 + 216 mm2 + 102 mm2) = 1542 mm2 = 0,1542 dm2
Data perubahan berat benda uji VI pada larutan HNO3 pH 0,2 :
Tabel 4.11 Data perubahan berat benda uji VI pada larutan HNO3 pH 0,2
No Minggu ke- Berat benda uji (gram) 1 0 18,238 2 I 18,238 3 II 18,236 4 III 18,233 5 IV 18,231 6 V 18,228 7 VI 18,225 8 VII 18,224 9 VIII 18,223 10 IX 18,219 11 X 18,218 12 XI 18,218 13 XII 18,217
Laju korosi minggu II =
2 ) 0,1542 ( 007 , 0 x = 0,09 gram/dm 2/minggu.
Tabel 4.12 Laju korosi benda uji VI pada larutan HNO3 pH 0,5 No Minggu Ke -Berat Awal (gram) Berat Akhir (gram) Penurunan Berat (gram) Luas (mm2) Laju Korosi (gram/dm2/jam) 1 1 18,238 18,238 -0,1542 -2 2 18,238 18,236 0,002 0,1542 0,09 3 3 18,236 18,233 0.003 0,1542 0,058 4 4 18,233 18,231 0,002 0,1542 0,051
42 5 5 18,231 18,228 0,003 0,1542 0,097 6 6 18,228 18,225 0,003 0,1542 0,116 7 7 18,225 18,224 0,001 0,1542 0,045 8 8 18,224 18,223 0,001 0,1542 0,051 9 9 18,223 18,219 0,004 0,1542 0,223 10 10 18,219 18,218 0,001 0,1542 0,064 11 11 18,218 18,218 -0,1542 -12 12 18,218 18,217 0,001 0,1542 0,077
Tabel 4.13 Laju korosi rata-rata selama 3 bulan pada pH 0,5
No Benda Uji Berat Awal (gram) Berat Akhir (gram) Luas (mm²) Rata-rata Laju Korosi (gram/dm²/bulan) 1 I 14,608 14,590 0,1536 0,026 2 II 13,795 13,770 0,1464 0,056 3 III 13,478 13,469 0,1542 0,105
Tabel 4.14 Laju korosi rata-rata selama 3 bulan pada pH 0,5
No Benda Uji Berat Awal (gram) Berat Akhir (gram) Luas (mm²) Rata-rata Laju Korosi (gram/dm²/bulan) 1 IV 13,478 13,469 0,1442 0,02 2 V 14,364 14,348 0,1464 0,036 3 VI 13,795 13,770 O,1542 0,045
43
4.4 Grafik Laju Korosi
A. Larutan HNO3 pH 0,5
Gambar 4.8 Grafik laju korosi stainless steel 304 dalam larutan HNO3 dengan pH 0,5
B. Larutan HNO3 pH 0,2
Gambar 4.9 Grafik laju korosi stainless steel 304 dalam larutan HNO3 dengan pH 0,2.
0 0.05 0.1 0.15 0.2 0.25 0.3 1 2 3 4 5 6 7 8 9 10 11 12 Laju Kor o si (gram/ d m 2/j a m ) T itl e Minggu Ke-benda uji I tanpa las benda uji 2 pengelasan TIG benda uji 3 pengelasan busur listrik 0 0.05 0.1 0.15 0.2 0.25 1 2 3 4 5 6 7 8 9 10 11 12 La ju K o ro si (gram/ d m 2/j a m ) T itl e Minggu Ke-benda uji IV tanpa las benda uji V pengelasan TIG benda uji VI pengelasan busur listrik
44
C. Laju korosi per bulan pada pH 0,5
Gambar 4.10 Grafik laju korosi per bulan pada pH 0,5 D. Laju korosi per bulan pada pH 0,2
Gambar 4.11 Grafik laju korosi per bulan pada pH 0,2 0 0.02 0.04 0.06 0.08 0.1 0.12
Tanpa las Las TIG Las Busur Listrik
gr am /dm ²/ bulan Stainlees Steel 304 0 0.005 0.01 0.015 0.02 0.025 0.03 0.035 0.04 0.045 0.05
Tanpa Las Las TIG Las Busur Listrik
gram/ d m ²/bu la n Stainless Steel
45
4.4 Pembahasan
Benda uji yang telah mengalami pengelasan maupun yang tidak mengalami pengelasan dapat terkorosi, ini dapat diketahui karena adanya pengurangan berat dari benda uji setelah mengalami perendaman dalam larutan HNO3 pH 0,5 dan juga pada pH 0,2. Korosi yang terjadi secara
merata pada seluruh permukaan dikarenakan adanya kerusakan lapisan protective layer yang melindungi stainless steel dari korosi. Antara benda uji yang mengalami pengelasan dengan benda uji yang tidak mengalami pengelasan terjadi perbedaan laju korosi yang signifikan. Laju korosi spesimen las busur listrik paling tinggi dikarenakan metode pengelasan kurang baik. Pada pengelasan ini,sewaktu pendinginan banyak Cr yang teroksidasi sehingga protektive layer menjadi kurang sempurna. Pada saat terjadi pengurangan berat benda uji maka benda uji mengalami korosi karena ada sebagian dari lapisan protective layer yang rusak. Pada saat benda uji kembali tidak mengalami pengurangan berat atau beratnya stabil, itu berarti benda uji tidak mengalami korosi. Kemungkinan lapisan protective layer yang telah rusak kembali terbentuk setelah terjadi reaksi oksidasi antara Cr yang ada pada stainless steel dengan oksigen yang ada di lingkungan bebas pada saat dilakukan penjemuran dibawah sinar matahari sebelum dilakukan pengukuran berat pada setiap satu minggu sekali. Dari penampilan visual benda uji terjadi perubahan warna dari sebelum dilakukan perendaman dengan setelah dilakukan perendaman.
46
BAB V
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari hasil penelitian selama 12 minggu dapat diambil kesimpulan, antara benda uji yang telah mengalami pengelasan dengan benda uji yang tidak mengalami pengelasan ada perbedaan yang signifikan laju korosinya dalam larutan HNO3. Semuanya sama-sama mengalami korosi baik yang mengalami pengelasan maupun yang tidak mengalami pengelasan, tetapi korosi tertinggi terdapat pada las busur listrik. Korosi yang terjadi merata pada seluruh permukaan benda uji karena rusaknya sebagian dari lapisan protective layer. Untuk laju korosi tertinggi pada pH 0,5 yaitu 0,245 gram/dm2/minggu, sedangkan untuk laju korosi tertinggi pada pH 0,2 adalah 0,223 gram/dm2/minggu.
5.2 Saran
1.Apabila ada SS yang dilas sebaiknya mengunakan las TIG karena ketahanan korosinya cukup baik terhadap HNO3
2. Gunakanlah alat penimbang berat benda uji yang akurat dan jangan ganti-ganti timbangan.
47
DAFTAR PUSTAKA
Chamberlain, J. & Trethewey, KR. Korosi Untuk Mahasiswa Dan Rekayasawan, Gramedia Pustaka Utama, Jakarta.
Kenyon, W, Diterjemahkan Dines Ginting, 1985, Dasar-dasar Pengelasan, Erlangga, Jakarta.
Setyahandana, B., Bahan Kuliah Bahan Teknik Manufaktur, Universitas Sanata Dharma, Yogyakarta.
Surdia, T., Saito, S.,1985, Pengetahuan Bahan Teknik, Pradnya Paramita, Jakarta. Korosi, www.tasteel/main.php, diakses 05 April 2009
TIG Welding Proces, www.alu-info.dk/Html/alulib/modul/A00537.htm, diakses 23 juni 2009