POTENSI PREBIOTIK PATI UBI UWI (Dioscorea alata L)YANG TERMODIFIKASI PROPILEN OKSIDA
Miksusanti
Jurusan Kimia FMIPA UNSRI Kampus Indralaya OKI
Abstrak
Pada penelitian ini dilakukan pengujian kemampuan pati uwi termodifikasi dengan propilen oksida sebagai prebiotik. Bakteri probiotik yang digunakan dalam penelitian ini adalah Lactobacillus plantarum. Pati ubi uwi di modifikasi dengan 0,2% propilen oksida. Uji tantang untuk melihat kemampuan bakteri probiotik dilakukann terhadap Escherichia coli (E. coli). Hasil penelitian menunjukkan pati ubi uwi yang termodifikasi dengan propilen oksida yang difortifikasi dalam media MRS dapat menstimulasi pertumbuhan lactobacillus plantarum sebesar 1,5 log pada inkubasi 48 jam. Uji tantang terhadap Escherichia coli, menunjukkan bahwa Lactobacillus plantarum yang ditumbuhkan pada media pati ubi uwi termodifikasi dapat menurunkan jumlah Escherichia coli sebanyak 1 log CFU/mL pada inkuibasi 48 jam.
Kata Kunci: Pati ubi uwi, propilen oksida, prebiotik, Lactobacilluis plantrarum, E. coli
PENDAHULUAN
Prebiotik merupakan bahan pangan yang tidak dapat dicerna maupun diserap usus
halus sehingga dapat digunakan sebagai substrat (makanan) oleh mikroflora usus yang
menguntungkan seperti Lactobacillus dan Bifidobacteria. Peningkatan aktivitas dan
pertumbuhan mikroflora usus yang menguntungkan (LactobacillusdanBifidobacteria) akan
menghambat pertumbuhan bakteri patogen seperti Escherichia coli, dan clostridia yang
menghasilkan toksin sehingga mampu menurunkan resiko berbagai penyakit dan
meningkatkan imunitas tubuh (Roberfroid 2002).
Modifikasi pati banyak dilakukan dengan berbagai cara untuk memperoleh pati
dengan karakteristik tertentu sesuai keperluan seperti modifikasi dengan ikatan silang
(Munarsoet al, 2004), oksidasi (Sandhu et al, 2008), esterifikasi (Dzulkeflyet al, 2007), dan
penelitian ini dilakukan modifikasi pati dengan menggunakan propilen oksida karena pati
hasil modifikasi tersebut menghasilkan pati dengan suhu gelatinisasi yang lebih rendah,
granula yang mudah membengkak dan tidak mudah mengalami retrograsi (Lawal, 2009).
Pada penelitian ini sumber pati yang akan dimodifikasi adalah dari pati ubi uwi. Ubi
uwi adalah salah satu jenis umbi-umbian pangan yang pemanfaatannya belum dilakukan
secara maksimal (Richana dan Sunarti, 2004).
BAHAN DAN METODA
Bahan-bahan yang digunakan pada penelitian ini adalah natrium hidroksida, propilen
oksida (C3H6O), natrium sulfat, alkohol, asam asetat, asam klorida, asam sulfat, asam sitrat,
kristal triketohidrin, natrium bisulfit, propilen glikol, Nutrient Broth (NB) (OXOID), MRS
(de Mann Rogosa) broth (OXOID), MRS agar (OXOID), MRS basic (komposisi pada
Lampiran 1), Eosine Methylene Blue Agar (EMBA) (MERCK), gliserol 2%, H2SO40.05 M,
KOH 0.05 N, NaCl 0.85%, aquades dan spiritus.
Peralatan analisis BAL dan bakteri pathogen meliputi autoklaf, inkubator 37oC,
anaerobic jar, ANOXOMATtm, Laminar hood, refrigerator, cawan petri, tabung reaksi, alat
laboratorium berbahan gelas, vorteks, pH meter, membran filter steril 0.2 m (Millipore),
micropippette100-1000 m, tips 100-1000 m,syringe, bunsen dan ose.
Ekstraksi Tepung Ubi Uwi (Sukmawati, 1987)
Umbi ubi uwi segar dikupas, kemudian dipotong kecil-kecil, setelah itu ditimbang.
Potongan-potongan umbi dicuci dengan air kran sambil digosok berkali-kali kemudian
direndam dalam larutan garam. Setelah direndam umbi dicuci dengan air kran sambil
digosok-gosok dengan tangan, kemudian dihancurkan dengan blender. Hancuran uwi
ditambah air kemudian diperas-peras dengan tangan dan disaring dengan menggunakan kain
saring. Air yang digunakan selama pemerasan berbanding 9:1 (v/b) dengan berat uwi.
Larutan pati yang diperoleh diendapkan selama 20 jam. Setelah pati mengendap air dibagian
atas dibuang.
Endapan pati yang diperoleh dicuci dengan air kran, dengan cara mengaduk-aduk
endapan dengan pengaduk gelas. Pencucian dilakukan sampai tiga kali. Larutan pati
Endapan pati yang telah dicuci dikeringkan dibawah sinar matahari dengan wadah
nampan sampai kering. Pati yang telah kering dihaluskan dengan mortar dan diayak dengan
ayakan 100 mesh.
Modifikasi Pati Ubi Uwi
Tahap ini dilakukan untuk mendapatkan pati ubi uwi yang termodifikasi merupakan
yang akan menjadi salah satu komposisi median pertumbuhan BAL. Perlakukan dalam
penelitian ini adalah konsentrasi reagen propilen oksida (C3H6O) yaitu 10%. Prosedur
modifikasi pati ubi uwi dibuat sesuai dengan prosedur Ya-Jane dan Lingfeng (2000) dalam
Yuniar (2006).
Natrium sulfat sebanyak 15 g (15% dari bobot kering pati ubi uwi) dilarutkan dalam
186 mL air bebas ion dalam labu erlenmeyer 300 mL pada suhu ruang, sehingga terbentuk
larutan natrium sulfat. Pati ubi uwi ditimbang 100 g (berat kering) lalu dimasukkan ke dalam
larutan natrium sulfat dengan pengaduk magnetik sehingga terbentuk suspensi. Selanjutnya
pH dinaikkan sampai 11,5 dengan penambahan larutan 1% NaOH dan diaduk selama 10
menit.
Setelah ditambahkan propilen oksida dengan konsentrasi 10%(v/b) dari bobot kering
pati ke dalam suspensi, labu ditutup dan larutan diaduk pada suhu ruang selama 1 jam
sebelum suhu naik mencapai 45 0C. Suspensi tadi diaduk terus pada suhu 450C. Pengadukan
dilanjutkan terus dengan menggunakan inkubator kering pada kecepatan 150 rpm selama 24
jam dan selanjutnya pH diturunkan menjadi 5,5 dengan menggunakan HCl 1 N. Suhu
suspensi diturunkan sampai 300C. Suspensi tadi disaring dengan menggunakan kertas
whatman no. 4, sambil dicuci dengan air destilata sebanyak 5 kali. Pengeringan dilakukan
pada suhu 400C dengan oven selama 18 jam.
Total Bakteri Asam Laktat (AOAC, 1999)
Jumlah BAL dihitung dengan metode agar tuang, Perhitungan BAL pada 0 jam
dilakukan pemupukan 105-108, pada 24 jam dan 48 jam dilakukan pemupukan pada 106
-109. Setelah pemupukan, cairan berisi BAL dituang dengan media MRSA sebanyak 12-15
ml. Setelah agar membeku dilakukan inkubasi pada suhu 37oC selama 48 jam dengan posisi
PertumbuhanL. plantarum pada pati ubi uwi termodifikasi
Disiapkan pati ubi uwi hasil modifikasi, air steril masing-masing 50 ml/sampel dan
MRSB steril tanpa dekstrosa (MRSB racikan) masing-masing 50ml/sampel. Sebanyak 2.5
ml BAL yang berumur 1 hari dipipet dan dimasukkan ke dalam campuran larutan 50 ml
MRSB racikan + 2.5% pati uwi termodifikasi dan larutan 50 ml air steril + 2.5% pati uwi
termodifikasi. Larutan ini kemudian diinkubasi selama 24 jam pada suhu 370C. Setelah
inkubasi 24 jam, 1 ml larutan dipipet dan imasukkan ke dalam larutan pengencer NaCl
0.85% 10 ml dan divortex untuk memperoleh pengenceran 10-1. Selanjutnya dibuat
pengenceran sampai 10-7 dengan cara yang sama. Pemupukan dilakukan pada pengenceran
10-5-10-8 dengan menggunakan media MRSA dalam cawan petri. Cawan petri selanjutnya
diinkubasi pada suhu 370C dalam posisi terbalik. Pemupukan dilakukan triplo setiap
pengenceran. Perhitungan koloni dilakukan setelah 48 jam berdasarkan metode ISO
(Harrigan, 1998) dan dinyatakan dalam CFU/ml.
Kompetisi Antara Bakteri Asam Laktat dan Bakteri Patogen pada ekstrak pati ubi
uwi termodifikasi
Pengujian kompetisi pertumbuhan BAL dan bakteri patogen dilakukan dengan
menginokulasikan secara bersama-sama BAL dan bakteri patogen ke dalam satu medium.
Medium yang digunakan MRS racikan yang ditambah pati ubi uwi termodifikasi. Sebanyak
8.1 ml MRS steril ditambahkan pati ubi uwi sesuai komposisi MRS racikan untuk sumber
karbon. Bakteri Asam Laktat yang digunakan adalah L. plantarum. Bakteri patogen yang
digunakan adalah Escherichia coli.
Jumlah BAL yang diinokulasi ke dalam media kompetisi sejumlah 108 CFU/ml,
sedangkan jumlah patogen yang diinokulasi ke dalam media kompetisi adalah sejumlah 104
CFU/ml. Inokulum disiapkan dengan perhitungan jumlah kultur terlebih dahulu bila jumlah
kultur melebihi jumlah yang akan dikompetisikan, maka dilakukan pengenceran. BAL segar
dipersiapkan dengan mensentrifuse 3000 rpm selama 15 menit. Filtrat di buang dengan cara
dipipet sebanyak 9 ml dan di peroleh endapan BAL (pellet). Endapan BAL dimasukkan
pengenceran. Untuk mendapatkan jumlah awal patogen 104 CFU/ml makaEscherichia coli
diencerkan 1000 kali.
Sebanyak 1 ml BAL dan 0.1 ml patogen (setelah pengenceran) diinokulasikan ke
dalam media kompetisi. Untuk menghindari kontaminasi dalam setiap hari pengamatan
maka media kompetisi dibagi dalam 3 tabung terpisah yang akan diamati pada 0 jam, 24
jam dan 48 jam perlakuan. Perhitungan BAL dan patogen dilakukan secara kuantitatif
dengan metode agar tuang.
Penentuan Jumlah Patogen (AOAC, 1995)
Total patogen dihitung dengar metode agar tuang. Perhitungan bakteri patogen pada
0 jam dengan pemupukan 101-104, 24 jam dilakukan pemupukan 102-105dan pada 48 jam
dilakukan pemupukan 103-106. Sebanyak 1 ml dari masing-masing pengenceran di plating
(memasukkan kultur ke dalam cawan petri steril) dan dituang dengan media EMBA untuk
pertumbuhan Escherichia coli. Setelah agar memadat dilakukan inkubasi pada suhu 37oC
selama 24 jam. Koloni tipikal hijau metalik menunjukkan pertumbuhan E .coli. Jumlah
koloni kemudian dihitung dengan rumus TPC berikut :
Ket : N = Jumlah mikroba (cfu/ml)
n1= Jumlah cawan pada tingkat pengenceran tertinggi
n2= Jumlah cawan pada tingkat pengenceran terendah
c = Jumlah total koloni yang terhitung pada cawan
d = Tingkat pemupukan tertinggi yang dapat dihitung
HASIL DAN PEMBAHASAN
Pati uwi mengandung 22,96 % amilosa. Kandungan karbohidrat ini dalam pati ubi
uwi menunjukan terdapat cukup sumber monosakarida yang mudah untuk dimetabolisme
oleh BAL.Menurut Luet al(2001), glukosa merupakan sumber energi yang disukai sebagai
sumber karbón oleh sebagian besar mikroorganisme.
n
n
d
c
N
Setelah inkubasi 24 jam dan 48 jam terjadi pengingkatan jumlah BAL pada media
baik yang mengandung pati termodifikasi maupun pada media pati uwi kontrol. Hal ini
mengindikasikan potensi sifat prebiotik pati uwi termodifikasi (Mandersonet al. 2005).
Tabel 1.PertumbuhanLactobacillus plantarum pada Pati Ubi Uwi
Bakteri Probiotik Media Pertumbuhan Waktu/jam CFU/mL±SD
Dengan termodifikasinya pati ubi uwi dengan propilen oksida, diharapkan pati ini
menjadi bersifat lebih resisten (resisten starch). Serat tipe ini tidak dapat dicerna di usus
halus manusia yang sehat, sehingga resisten starch ini akan mencapai kolon dan akan
difermentasi oleh mikroflora (Bakteri asam laktat dan Bifidobacteria). Setelah mencapai
kolon, resisten starchakan difermentasi oleh mikroflora usus dan menghasilkan asam lemak
rantai pendek (Short chain fatty acid/SCFA) (Sajilata, 2006). SCFA dapat digunakan
sebagai sumber energi, efek stimulasi yang selektif terhadap pertumbuhan bakteri probiotik
terutama Bifidobakteria dan Lactobacillus. Selama fermentasi, dibentuk SCFA seperti asam
asetat, propionat dan butirat. Asam–asam lemak lemak rantai pendek ini dapat menghambat
pertumbuhan bakteri patogen sepertiEscherichia coli.
Escherichia coli merupakan mikroflora alami pada tubuh manusia dan pada hewan
berdarah panas. Kebanyakan Escherichia coli merupakan bakteri yang kurang bahaya
namun beberapa jenis dapat menyebabkan diare dan infeksi pada tubuh manusia.
Escherichia coli O157:H7 diidentifikasi memproduksi Shiga Toxin yang dapat
menyebabkan diare berdarah (Doyle, 2001). Pemanfaatan bakteri baik (probiotik) dapat
mencegah dan menyembuhkan penyakit diare.
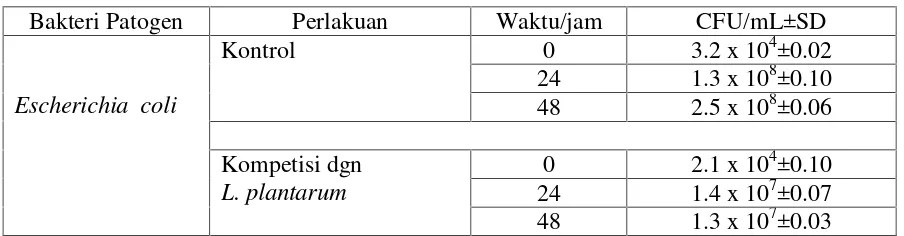
Dari tabel 2 terlihat bahwa pertumbuhan Escherichia coli terhambat dengan adanya
L. plantarum pada media yang mengandung pati uwi yang termodifikasi. Penghambatan
Escherichia coli sebesar 1 log. CFU/ml. Hal ini menunjukkan pertumbuhan L. plantarum
produksi metabolit sekunder yang banyak dan menurunkan pH lingkungan sehingga terjadi
penurunan pertumbuhanEscherichia coli, bahkan menyebabkanEscherichia colimati.
Tabel 2. Kompetisi BAL denganEscherichia coli
Bakteri Patogen Perlakuan Waktu/jam CFU/mL±SD
Escherichia coli
Kontrol 0 3.2 x 104±0.02
24 1.3 x 108±0.10 48 2.5 x 108±0.06
Kompetisi dgn L. plantarum
0 2.1 x 104±0.10 24 1.4 x 107±0.07 48 1.3 x 107±0.03
Media yang mengandung pati uwi termodifikasi menghasilkan pertumbuhan
L. paltarum yang sama baik dengan media pertumbuhan BAL kontrol. Pertumbuhan
Escherichia coli relatif lebih rendah pada media yang mengandung pati uwi termodifikasi.
Hal ini menunjukkan bahwa pati uwi termodifikasi bersifat selektif terhadap pertumbuhan
Escherichia coli. Akan tetapi nilai pertumbuhan pathogen tersebut masih menunjukkan nilai
positif. Meskipun Escherichia coli berada pada lingkungan yang minim sumber karbon,
akan tetapi bakteri tersebut memiliki kemampuan dapat bertahan hidup pada kondisi minim
nutrisi seperti.
KESIMPULAN
Berdasarkan hasil penelitian ini pati ubi uwi yang termodifikasi dengan propilen
oksida, dapat meningkatkan pertumbuhan lactobacillus plantarum dengan baik. Bakteri
lactobacillus plantarum yang ditumbuhkan pada media yang mengandung pati uwi
termodifikasi dapat menurunkan pertumbuhan bakteri patogen Escherichia coli sebanyak
1 log CFU/ml.
SARAN
Perlu dilakukan pengujian secara invivo untuk melihat sejauh mana potensi pati ubi
UCAPAN TERIMAKASIH
Ucapan terimakasih ditunjukkan kepada Wiwin Y mahasiswa UNSRI dan Eva
Syilvianora mahasiswa IPB yang telah membantu terlaksanya penelitian ini.
PUSTAKA
AOAC. 1999. Official Methods of Analysis of AOAC International16th. USA.
Aziz, Azronnizan., Rusli Daik., Maarul Abd.Ghani., Nik Ismail Nik Daud and BohariM.Yamin.2004. Hydroxypropil ation and Acetylation of Sago Strach. Malaysian Journal of Chemistry,2004, Vol.6, No. 1, 048-054.
AOAC. 1995. Official Methods of Analysis. Association of Analytical Chemistry International. 16th.Vol 2. USA: Maryland
Choi, S.G and W. L. Kerr. 2003. Effect of Hydroxypropylation onRetrogradation and Water Dynamics in Wheat Starch Gels Using 1H NMR. Journal Cereal Chem.80(3):290– 296.
Doyle MP, LR Beuchat, TJ Montville. 2001. Food Microbiology. ASM Press. Washington DC.
Emanuel, Cynthia. 2005. Pengaruh Fosforilasi dan Penambahan Asam Stearat dan Karakteirstik Film Edible Pati Sagu. Tesis. Bogor: Pasca Sarjana IPB.
Lawal, Olayide S. 2009. Starch hydroxyalkylation: Physicochemical properties and enzymatic digestibility of native and hydroxypropylated finger millet (Eleusine coracana) starch. Journal Food Hydrocolloids 23 (2009) 415–425.
Lu Z, HP Fleming dan RF Mc Feeters. 2001. Differential glucose and fructose utilization during cucumber juice fermentation.J. Food Science66 (1) :162-166
Munarso S., Joni Munarso., D. Muchtadi., D.Fardiaz., dan R. Syarief. 2004. Perubahan Sifat Fisikokimia dan Fungsiona Tepung Beras Akibat Proses Modifikasi Ikatan Silang. Jurnal Pascapanen1(1) 2004: 22-28
Manderson K, Pinar M, Tuhoy KM, Race WE, Otckiss AT, Widmer W, Yadhav MP,Gibson R, Rastall RS. 2005. In vitro determination of prebiotic properties of oligosaccharides derived from an orange juice manufacturing by-product stream.App and Env
Richana, Nur dan Titi Chandra Sunarti. 2004. Karakterisasi Sifat Fisikokimia Tepung Umbi dan Tepung Pati dari Umbi Ganyong, Suweg, Ubi Kelapa dan Gembili. Jurnal Pascapanen1(1) 2004 : 29-37.
Roberfroid M. 2002. Functional food concept and its application to prebiotics. J. Digest Liver Dis. 34: S105-110.
Sukmawati, Nurtjahjani Dwi. 1987. Perubahan Karbohidrat Umbi Uwi (Dioscorea alata L) Selama Penyimpanan. Skripsi. Bogor: Fakultas Teknologi Pertanian Institute Pertanian Bogor.
Sajilata, M. G. Rekha S. Singhai, dan Puspha R. Kulkarni. 2006. Resistant Starch-A Review.Comprehensive Reviews in Food Science and Food Safety. Vol 5, 2006.
Sandhu, Kawaljit Singh., Maninder Kaura., Narpinder Singhb., and Seung-Taik Lim. 2008. A comparison of native and oxidized normal and waxy corn starches: Physicochemical, thermal, morphological and pasting properties.Journal Science LWT41 (2008),1000