ii
ALANIN-AMINOTRANSFERASE (ALT)
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh :
Stephanie Gunawan
NIM : 038114070
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
vi
sehingga penulis dapat menyelesaikan skipsi berjudul “Efek Hepatoprotektif Infusa Daun Ceplikan (Ruellia tuberosa Linn.) Terhadap Mencit Jantan Terinduksi Parasetamol: Kajian Terhadap Serum Alanin-aminotransferase (ALT)” dengan baik.
Skripsi ini dibuat untuk memenuhi salah satu syarat memperoleh gelar Sarjana Farmasi (S.Farm.) program studi farmasi Universitas Sanata Dharma Yogyakarta.
Penulis menyadari bahwa dalam pelaksanaan maupun penyusunan skripsi ini, tidak lepas dari bantuan dari berbagai pihak oleh karena itu, saat ini penulis ingin mengucapkan terima kasih kepada:
1. Tuhan Yang maha Penyayang atas kasih dan karunia-Nya.
2. Ibu Rita Suhadi, M.Si., Apt., selaku dekan Fakultas Farmasi Universitas Sanata Dharma.
3. Ibu dr. Luciana Kuswibawati, M.Kes., sebagai pembimbing utama atas bimbingan, arahan, kesabaran, waktu, dan kesediaannya.
4. Bapak Drs. Mulyono, Apt., sebagai dosen penguji atas kesediaan, waktu, ide, dan sarannya.
5. Bapak Yosef Wijoyo, M.Si., Apt., sebagai dosen penguji atas kesediaan, waktu, ide, saran, dan informasinya.
vii tanaman ceplikan.
9. Hendro Gunawan (Papi), Susi Anggraeni (Mami), dan Rudi Sukamto (Koko) yang selalu mendukung dan menyemangati sampai dengan selesainya skripsi ini.
10.Essie, teman, partner kerja sedari awal kuliah sampai skripsi, saudara, sahabatku.
11.Sisar yang selalu sabar mengantar dan menunggu.
12.Para sahabatku: Dessy, Hani, Milo, Nia, Silih, dan Endah, atas dukungan dan persahabatan kalian.
13.Mas Par, Mas Heru, dan Mas Kayat yang sangat membantu selama penelitian. 14.Teman-teman seperjuangan di Laboratorium lantai dua: Shyu, Tata, Punto,
Jeppi, Yeyen, Shinta, Syuryach, Angga, Galleah, Agnes, Nia. 15.Kelompok praktikum D atas kenangan selama ini.
16.Erika Hikaru Spears dan Karina Metasari atas kenangan kalian. 17.Bapak dan ibu dosen Fakultas Farmasi atas ilmunya.
18.Anin yang telah meluangkan pulsa dan waktunya. 19.Soca atas kameranya.
viii
Yogyakarta, 27 Juli 2007
x
sudah mulai berkembang. Hal ini sangat tepat untuk diterapkan di Indonesia karena Indonesia termasuk negara yang memiliki keanekaragaman hayati yang kaya. Maka muncullah pemikiran untuk membuktikan kemampuan infusa daun ceplikan menurunkan aktivitas serum ALT pada kerusakan hati mencit jantan akibat pembeian parasetamol, di mana ceplikan (juga dikenal dengan nama pletekan) dikenal sebagai obat kencing batu dan penurun kadar glukosa dalam darah.
Penelitian ini merupakan penelitian eksperimental murni dengan rancangan acak lengkap pola searah. Sejumlah tiga puluh lima ekor mencit jantan dibagi secara acak menjadi tujuh kelompok perlakuan. Kelompok I sebagai kontrol negatif, diberikan CMC-Na. Kelompok II sebagai kontrol positif, diberikan parasetamol dosis hepatotoksik (berdasarkan hasil orientasi). Kelompok III sebagai kontrol perlakuan diberi infusa daun ceplikan dosis tertinggi (3333,3 mg/kgBB). Kelompok IV-VII diberi perlakuan infusa daun ceplikan secara peroral masing-masing dengan peringkat dosis 987,7; 1481,5; 2222,2; dan 3333,3 mg/kgBB selama enam hari berturut-turut kemudian pada hari ketujuh diberi parasetamol dosis hepatotoksik. Hewan uji kemudian diambil darahnya dari sinus orbitalis mata selang 24 jam pemberian parasetamol untuk kemudian diukur aktivitas serum ALT-nya. Data serum ALT yang didapat dianalisis dengan uji Kolmogorov Smirnov untuk melihat distribusi datanya, jika didapatkan distribusi data yang normal analisis dilanjutkan dengan uji One Way ANOVA dan uji LSD, dan jika didapatkan distribusi data yang tidak normal analsis dilanjutkan dengan uji Krukal Wallis dan uji Mann Whitney.
Dari penelitian ini didapatkan bahwa infusa daun ceplikan dosis 2222,2 dan 3333,3 mg/kgBB mampu menurunkan aktivitas serum ALT pada kerusakan hati mencit jantan akibat pemberian parasetamol.
xi
recently have started to expand. This is very precise to be applied in Indonesia because Indonesia is inclusive of state owning rich of variety involve.Hence emerge the opinion to prove the ability of ceplikan leaves infusion degrade the activity of ALT serum of male mice liver damage by paracetamol induced, where ceplikan (is also recognized by the name of pletekan) known as urine drug petrify and decrease glucose rate in blood.
This research was performed following a pure experimental research with complete random design pattern.A number of thirty five male mice divided random become seven treatment group. Group I as negative control, given by CMC-Na. Group II as positive control, given by acetaminophen of hepatotoxic dose (pursuant to orient result). Group III as treatment control given the highest dose of ceplikan leaves infusion ( 3333,3 mg/kgBB). Group IV-VII given the treatment of ceplikan leaves infusion each orally by dose level 987,7; 1481,5; 2222,2; and 3333,3 mg/kgBB during six day successively then given acetaminophen of hepatotoxic dose on the seventh. Then the animal test's blood are taken from sine of orbitalis eye certain period 24 hour of acetaminophen gave to measured it's ALT serume activity. Data of serum ALT got to be analysed with Kolmogorov Smirnov test to see its data distribution, if got a normal data distribution analyse continued with One Way ANOVA test and LSD test, and if got an abnormal data distribution analyse continued with Krukal Wallis test and Mann Whitney test.
From this research got that ceplikan leaves infusion dose 2222,2 and 3333,3 mg/kgBB able to degrade the activity of ALT serum of male mice liver damage by paracetamol induced.
xii
HALAMAN JUDUL ... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN ... iv
HALAMAN PERSEMBAHAN ... v
PRAKATA ... vi
PERNYATAAN KEASLIAN KARYA ... ix
INTISARI ... x
ABSTRACT ... xi
DAFTAR ISI ... xii
DAFTAR TABEL ... xv
DAFTAR GAMBAR ... xvii
DAFTAR LAMPIRAN ... xix
BAB I PENGANTAR ... 1
A. Latar Belakang ... 1
1. Rumusan masalah ... 4
2. Keaslian penelitian ... 4
3. Manfaat penelitian ... 5
B. Tujuan penelitian ... 5
1. Tujuan umum ... 5
xiii
C. Anatomi dan fisiologi hati... 8
D. Kerusakan hati ... 10
E. Hepatotoksin ... 11
F. Parasetamol ... 12
G. Tes laboratorium pada penyakit hati ... 15
H. Metode uji antihepatotoksin ... 17
I. Polifenol ... 18
J. Keterangan empiris ... 19
BAB III METODOLOGI PENELITIAN ... 20
A. Jenis dan rancangan penelitian ... 20
B. Variabel-variabel penelitian ... 20
C. Alat dan bahan penelitian ... 21
D. Subjek uji ... 22
E. Tatacara penelitian ... 22
1. Pengumpulan bahan ... 22
2. Determinasi tanaman ceplikan ... 22
3. Pembuatan simplisia daun ceplikan ... 23
4. Pembuatan infusa daun ceplikan ... 23
5. Pembuatan suspensi parasetamol 1% ... 23
xiv
F. Analisis hasil ... 26
BAB IV HASIL DAN PEMBAHASAN ... 29
A. Determinasi tanaman ceplikan ... 29
B. Uji pendahuluan ... 29
1. Penetapan dosis hepatotoksik parasetamol ... 29
2. Penetapan waktu pencuplikan darah ... 32
3. Penetapan lama pemejanan infusa daun ceplikan ... 34
C. Pengelompokan dan perlakuan hewan uji ... 37
1. Kontrol negatif CMC-Na ... 37
2. Kontrol positif hepatotoksin ... 38
3. Kontrol positif infusa dosis tertinggi ... 38
4. Kelompok perlakuan ... 39
D. Rangkuman pembahasan ... 43
BAB V KESIMPULAN DAN SARAN ... 46
A. Kesimpulan ... 46
B. Saran... 46
DAFTAR PUSTAKA ... 47
xv
(2006d) ... 26 Tabel II Data aktivitas serum ALT akibat pemberian parasetamol dosis 225;
230; 237,5; dan 250 mg/kgBB pada jam ke 24 ... 30 Tabel III Perbedaan nilai aktivitas serum ALT setelah pemberian
parasetamol dosis 225; 230; dan 237,5 mg/kgBB pada jam ke 24 berdasarkan uji Mann Whitney ... 30 Tabel IV Data aktivitas serum ALT setelah pemberian parasetamol dosis
237,5 mg/kgBB pada jam ke 24 dan 48 ... 32 Tabel V Perbedaan nilai aktivitas serum ALT setelah pemberian
parasetamol dosis 237,5 mg/kgBB pada jam ke 24 dan 48 berdasarkan uji T ... 33 Tabel VI Data aktivitas serum ALT setelah pemejanan infusa daun ceplikan
selama 2, 4, 6, dan 8 hari ... 34 Tabel VII Persen perbedaan nilai aktivitas serum ALT mencit terinduksi
parasetamol edngan praperlakuan infusa daun ceplikan selama 2, 4, 6, dan 8 hari berdasarkan uji Mann Whitney... 35 Tabel VIII Persen proteksi setelah praperlakuan infusa daun ceplikan dosis
xvi
237,5 mg/kgBB dengan waktu pencuplikan 24 jam ... 39 Tabel X Persen perbedaan nilai aktivitas serum ALT praperlakuan infusa
daun ceplikan dosis 987,6; 1481,5; 2222,2; dan 3333,3 mg/kgBB selama 6 hari berturut-turut pada mencit jantan terinduksi Parasetamol dosis 237,5 mg/kgBB ... 42 Tabel XI Data aktivitas serum ALT mencit jantan setelah pemejanan CMC
Na (kontrol negatif), parasetamol (kontrol positif), infusa daun ceplikan dosis tertinggi (kontrol positif), dan setelah praperlakuan infusa daun ceplikan dosis 987,7; 1481,5; 2222,2; dan 3333,3 mg/kgBB selama 6 hari berturut-turut terhadap parasetamol dosis 237,5 mg/kgBB dengan waktu pencuplikan 24 jam ... 59 Tabel XII Persen proteksi setelah praperlakuan infusa daun ceplikan selama 6
xvii
Gambar 2 Struktur parasetamol ... 12 Gambar 3 Lobus hati normal (kiri) dan lobus hati yang mengalami
kerusakan nekrosis sentrilobuler (kanan) ... 13 Gambar 4 Mekanisme metabolisme parasetamol dalam tubuh... 14 Gambar 5 Beberapa struktur senyawa yang termasuk polifenol ... 15 Gambar 6 Diagram batang aktivitas serum ALT setelah pemberian
parasetamol dosis 225; 230; dan 237,5 mg/kgBB pada jam ke 24 27 Gambar 7 Grafik aktivitas serum ALT setelah pemberian parasetamol dosis
237,5 mg/kgBB pada jam 24 dan 48 ... 33 Gambar 8 Grafik aktivitas serum ALT setelah pemejanan infusa daun
ceplikan selama 2, 4, 6, dan 8 hari ... 37 Gambar 9 Diagram batang aktivitas serum ALT setelah pemejanan infusa
daun ceplikan dosis 987,7; 1481,5; 2222,2; dan 3333,3 mg/kgBB selama 6 hari berturut-turut terhadap mencit jantan terinduksi parasetamol dosis 237,5 mg/kgBB dengan waktu pencuplikan 24 jam ... 40 Gambar 10 Diagram batang aktivitas serum ALT kontrol negatif, kontrol
xix
Lampiran 2 Gambar tanaman ceplikan ... 51
Lampiran 3 Foto vitalab mikro ... 52
Lampiran 4 Leaflet reagen DyaSys ALAT (GPT) FS* ... 53
Lampiran 5 Foto hati kontrol negatif CMC-Na ………. 55
Lampiran 6 Foto hati kontrol hepatotoksin ………... . 56
Lampiran 7 Foto hati kontrol infusa dosis tertinggi ……….. 57
Lampiran 8 Perhitungan dosis infusa daun ceplikan (Ruellia tuberosa Linn.) . 58 Lampiran 9 Konversi dosis infusa daun ceplikan yang mampu menurunkan aktivitas serum ALT pada kerusakan hati mencit jantan akibat pemberian parasetamol ke manusia ... 59
Lampiran 10 Tabel XI. Data aktivitas serum ALT mencit jantan stelah pemejanan CMC Na (kontrol negatif), parasetamol (kontrol positif), infusa daun ceplikan dosis tertinggi (kontrol positif), dan setelah pemejanan infusa daun ceplikan dosis 987,7; 1481,5; 2222,2; dan 3333,3 mg/kgBB selama 6 hari berturut-turut terhadap mencit jantan terinduksi parasetamol dosis 237,5 mg/kgBB dengan waktu pencuplikan 24 jam ... 60
xx
Lampiran 13 Hasil analisis Kolmogorov Smirnov yang dilanjutkan dengan uji T pada penetapan waktu pencuplikan darah ... 68 Lampiran 14 Hasil analisis Kolmogorov Smirnov yang dilanjutkan dengan uji
Kruskal Wallis dan uji Mann Whitney pada penetapan lama pemejanan infusa daun ceplikan ... 70 Lampiran 15 Hasil analisis Kolmogorov Smirnov yang dilanjutkan dengan uji
BAB I
PENGANTAR
A. Latar Belakang
Dalam proses fisiologis, hati berperan dalam sebagian besar metabolisme dan mempunyai sejumlah fungsi dalam tubuh, diantaranya yaitu detoksifikasi obat, penyimpanan glikogen, dan sintesis protein plasma. Hati juga menghasilkan empedu yang penting untuk pencernaan. Hati mempunyai kapasitas cadangan yang besar, dan hanya dengan 10 – 20% jaringan yang berfungsi, hati mampu mempertahankan kehidupan (Price and Wilson, 1994).
Mengingat pentingnya fungsi hati bagi kelangsungan hidup, sudah sepantasnya diberikan perhatian besar terhadap penanggulangan penyakit pada hati. Kerusakan hati dapat disebabkan oleh mikroorganisme maupun senyawa kimia (Price and Wilson, 1994). Hingga saat ini belum ditemukan obat yang secara spesifik dapat mengatasi hepatitis. Menurut Donatus (1992), kelangkaan obat hepatitis kemungkinan berhubungan dengan kerumitan sasaran terapi dan keidealan obat hepatitis tersebut.
Sasaran terapi hepatitis dikaji dari aspek kuratif, preventif, dan suportif. Aspek kuratif meliputi penghilangan virus penyebab, penanggulangan radang, dan perangsangan regenerasi sel. Aspek preventif meliputi pencegahan komplikasi, pencegahan kekambuhan, dan perlindungan hati dari aneka hepatotoksin. Aspek suportif meliputi pengelolaan menu makanan, pemasokan sumber energi, pembangkit energi, dan pengelolaan keaktifan fisik. Idealnya, obat hepatitis mampu
memperlihatkan ketiga aspek tersebut (Donatus, 1992). Oleh sebab itu, untuk mendapatkan obat hepatitis yang ideal tidaklah mudah, perlu dilakukan penelitian, salah satunya adalah dengan menggunakan obat-obatan yang berasal dari alam.
Parasetamol merupakan analgesik-antipiretik yang sering digunakan oleh masyarakat. Penggunaan parasetamol yang melebihi dosis dapat menyebabkan kerusakan hati. Hepatotoksisitas dapat terjadi pada pemberian dosis tunggal 10 – 15 g (200 – 250 mg/kgBB) parasetamol. Parasetamol merupakan salah satu senyawa model yang dapat digunakan untuk menggambarkan kerusakan hati bilamana diberikan pada dosis yang berlebih (Donatus, 2001).
Masyarakat Indonesia telah mengenal dan menggunakan obat tradisional sejak dulu. Beberapa tahun terakhir ini, terapi penyembuhan penyakit dengan menggunakan tanaman obat tradisional berdasarkan pengalaman empirik yang turun-temurun belakangan ini mulai berkembang. Hal ini dikarenakan Indonesia kaya akan tanaman obat sehingga bahan mudah diperoleh, dan cara penggunaannya pun mudah.
1. Rumusan masalah
Berdasarkan latar belakang yang telah penulis kemukakan, maka permasalahan dalam penelitian ini adalah apakah infusa daun ceplikan mampu menurunkan aktivitas serum ALT pada kerusakan hati mencit jantan yang diakibatkan pemberian parasetamol?
2. Keaslian Penelitian
Penelitian yang menggunakan daun ceplikan pernah dilakukan oleh Sutinah (1986) tentang isolasi dan identifikasi senyawa golongan flavonoid dari bunga Ruellia tuberosa Linn., De Jesus and Rodriguez (2002) tentang efek anti inflamasi daun Ruellia tuberosa Linn., dan Ismayani (2004) tentang efek hipoglikemi rebusan daun pletekan (Ruellia tuberosa Linn.) pada tikus putih jantan terbebani glukosa dengan metode spektrofotometri visibel.
Adapun hasil penelitian dari Sutinah adalah bahwa dalam bunga Ruellia tuberosa Linn. terdapat senyawa glikosida flavon; dari De Jesus and Rodriguez diperoleh hasil adalah bahwa daun Ruellia tuberosa Linn. Mempunyai khasiat sebagai obat anti inflamasi; dan dari penelitian Ismayani diperoleh hasil bahwa rebusan daun pletekan (Ruellia tuberosa Linn.) mempunyai efek hipoglikemik.
3. Manfaat Penelitian
a. Manfaat teoritis
Penelitian ini diharapkan dapat bermanfaat bagi pengembangan ilmu kefarmasian, ilmu kedokteran, dan pengetahuan masyarakat tentang obat-obat tradisional khususnya tanaman ceplikan.
b. Manfaat praktis
Penelitian ini juga diharapkan dapat memberikan informasi kepada masyarakat tentang kemampuan infusa daun ceplikan dalam menurunkan aktivitas serum ALT pada kerusakan hati pada mencit yang diakibatkan pemberian parasetamol.
B. Tujuan Penelitian
1. Tujuan umum
Penelitian ini bertujuan untuk mengembangkan ilmu pengetahuan tentang obat tradisional terutama tentang tanaman ceplikan.
2. Tujuan khusus
BAB II
PENELAAHAN PUSTAKA
A. Tanaman Ceplikan
1. Sinonim
Ruellia tuberosa Linn. (Anonim, 2006a)
2. Nama daerah
Di Indonesia, tanaman ini dikenal dengan nama ceplikan, pletekan (Jawa) (Anonim, 2006a).
3. Klasifikasi tanaman ceplikan
Divisi : Spermatophyta Subdivisi : Angiospermae Kelas : Dicotyledoneae Bangsa : Solanales
Suku : Acanthaceae
Marga : Ruellia
Jenis : Ruellia tuberosa Linn. (Anonim, 2006a)
4. Morfologi tanaman
Tanaman ceplikan termasuk dalam habitus terna, semusim, tinggi 0,4 – 0,9 m. Batang tegak, pangkal sedikit berbaring, bersegi, masif, dan berwarna hijau. Daun tunggal, bersilang berhadapan, berbentuk solet, ujung membulat, pangkal runcing, tepi bergigi, panjang 6 – 18 cm, lebar 3 – 9 cm, licin, pertulangan menyirip, dan
berwarna hijau. Bunga majemuk, bentuk payung, tumbuh diketiak daun, terdiri 1 – 15 bunga, kelopak 2 – 3 cm, benang sari melekat pada tabung mahkota berjumlah 4, dasar mahkota membentuk tabung, ujung berlekuk 5, panjang 3,5 – 5 cm, dan berwarna ungu. Buah kotak, lonjong, kering, berbiji banyak, panjang 2 – 3 cm, membuka dengan 2 katup, dan berwarna hijau. Biji bulat, kecil, dan berwarna coklat. Akar tunggang, membentuk umbi, dan berwarna coklat (Anonim, 2006a).
5. Kandungan kimia
Daun: saponin dan polifenol. Akar: saponin dan flavonoid. (Anonim, 2006a)
6. Khasiat dan kegunaan
Khasiat: obat sakit kencing batu (Anonim, 2006a), anti inflamasi (De Jesus and Rodriguez, 2002), dan penurun kadar glukosa darah (Ismayani, 2004).
B. Infusa
1. Definisi
Infusa adalah sediaan cair yang dibuat dengan mengektraksi simplisia nabati dengan air pada suhu 90°C selama 15 menit dan infusa yang mengandung bukan bahan berkhasiat keras dibuat dengan menggunakan 10% simplisia (Anonim, 1995).
2. Pembuatan
Kemudian diserkai selagi panas dengan kain flanel, dan ditambahkan air panas secukupnya melalui ampas hingga diperoleh volume infusa yang dikehendaki (Anonim, 1995).
C. Anatomi dan Fisiologi Hati
Hati merupakan organ dalam terbesar pada tubuh manusia. Pada manusia dewasa, berat hati sekitar 1,3 kg dan merupakan organ lunak, berwarna merah muda kecoklatan yang berbentuk seperti boomerang. Secara anatomi, letaknya dalam tubuh adalah di bawah diafragma, sebelah kanan atas rongga perut (Fox, 2004).
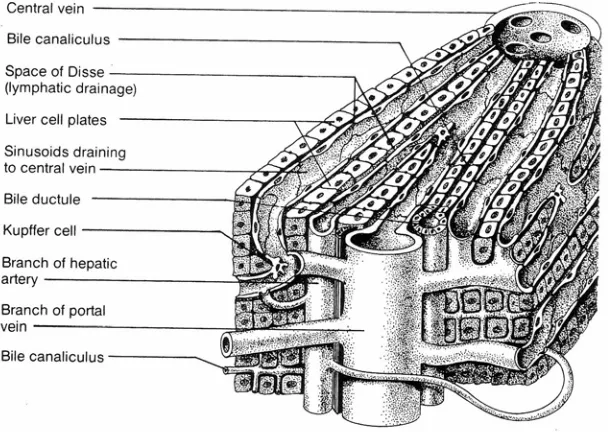
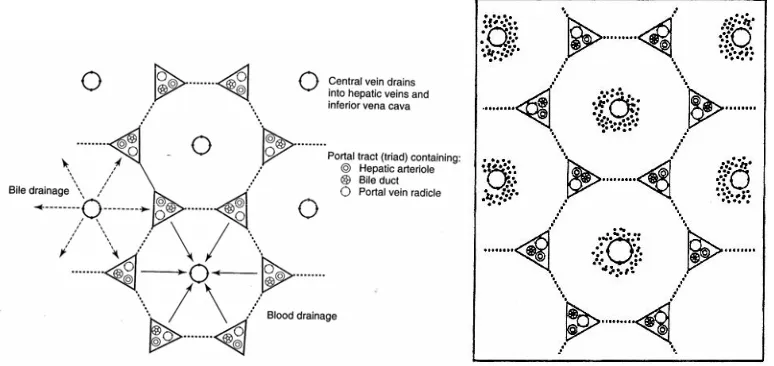
Gambar 1. Struktur mikroskopik hati (Chandrasoma and Taylor, 1995)
Sel-sel hati tersusun atas bentuk heksagonal yang disebut lobulus. Sel-sel epitel disebut hepatosit menyebar dari central vein (yang sebenarnya merupakan cabang dari hepatic vein). Kolom hepatosit berada diantara saluran yang disebut sinusoid yang dibatasi oleh sel-sel endotelial yang sangat permeabel dan mengandung sel-sel fagositik yang disebut sel Kupffer (Stine and Brown, 1996).
Menurut Fox (2004), fungsi hati yaitu:
a. memproduksi dan mensekresi empedu. Hati memproduksi empedu 250 – 1500 ml per hari. Unsur pokok empedu adalah pigmen empedu (bilirubin), garam empedu, fosfolipid (sebagian besar lesitin), kolesterol, dan ion-ion inorganik. b. detoksifikasi. Hati dapat mengekskresi hormon, mendetoksifikasi obat, dan
molekul biologis aktif yang lain dari darah dengan (1) ekskresi senyawa-senyawa dalam empedu; (2) fagositosis melalui sel-sel Kupffer; (3) perubahan kimia dari molekul-molekul tersebut dalam hepatosit.
c. berperan dalam metabolisme karbohidrat: gluconeogenesis (pembentukan glukosa dari asam amino, laktat, atau gliserol); glycogenolysis (pembentukan glukosa dari glikogen); glycogenesis (pembentukan glikogen dari glukosa); dan pemecah insulin dan hormon lainnya.
d. hati juga berperan dalam metabolisme lipid: mensintesis kolesterol dan memproduksi trigliserida.
e. memproduksi faktor-faktor koagulasi.
D. Kerusakan Hati
Menurut Treinen and Moslen (2001), beberapa macam kerusakan hati, yaitu: a. steatosis atau perlemakan hati, secara biokimia digambarkan sebagai suatu
peningkatan jumlah lipid hepatik atau pada hepatosit terkandung lemak yang berlebih. Perlemakan hati dapat dikarenakan beberapa penyebab, diantaranya adalah: hati kelebihan suplai asam lemak bebas, gangguan pada siklus trigliserida, peningkatan sintesis atau esterifikasi asam lemak, penurunan oksidasi asam lemak, penurunan sintesis apoprotein, dan penurunan sintesis atau sekresi very low density lipoprotein (VLDL).
b. kematian sel, sel hati dapat mati melalui dua cara, nekrosis atau apoptosis. Nekrosis ditandai dengan bentuk sel yang bergelombang, kebocoran, disintegrasi nuclear, dan influks pada sel yang radang. Apoptosis ditandai dengan penyusutan ukuran sel, fragmentasi nuclear, dan tidak terjadi inflamasi.
c. kolestasis, secara biokimia digambarkan dengan penurunan jumlah serum yang terdapat dalam empedu, terutama garam empedu dan bilirubin. Ketika ekskresi empedu pigmen bilirubin kekuning-kuningan rusak, pigmen ini terakumulasi di kulit dan mata, menyebabkan jaundice, dan masuk ke urin, menyebabkan urin berwarna kuning kecoklatan atau coklat gelap.
lemah untuk bertahan, dan biasanya merupakan akibat keterulangan dari tidak terlindunginya hati dari bahan kimia yang bersifat toksik.
E. Hepatotoksin
Obat atau senyawa kimia yang dapat menyebabkan kerusakan hati dapat dibedakan menjadi 2, yaitu:
1. hepatotoksin teramalkan (intrinsik)
Merupakan obat atau senyawa kimia yang pada dasarnya mempunyai sifat toksik terhadap sel hati. Contoh hepatotoksin teramalkan yang dapat menimbulkan kerusakan nekrosis hepatoseluler adalah racun jamur (Amanita phalloides), aflatoksin, karbontetraklorida, kloroform, parasetamol, dan lain sebagainya (Chandrasoma and Taylor, 1995).
2. hepatotoksin tak teramalkan (idiosinkratik)
F. Parasetamol
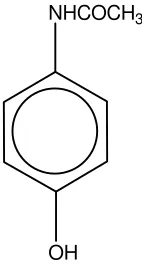
NHCOCH3
OH
Gambar 2. Struktur Parasetamol (Anonim, 1995)
Parasetamol berbentuk serbuk hablur, berwarna putih, tidak berbau dan rasanya sedikit pahit (Anonim, 1995). Parasetamol digunakan secara luas sebagai analgesik. Nama kimia parasetamol adalah N-acetyl-p-aminophenol (APAP). Dalam dosis terapi, parasetamol mempunyai profil keamanan yang sangat baik, tetapi jika digunakan dalam dosis yang berlebihan dapat mengakibatkan hepatotoksisitas (Tucker, 2003). Efek toksik parasetamol dapat mengakibatkan nekrosis sentrilobuler pada hati (Lee, 1995; Wilmana, 2002). Hepatotoksisitas parasetamol dapat terjadi pada pemberian dosis tunggal 10 – 15 gram (200 – 250 mg/kgBB) (Wilmana, 2002). Hepatotoksisitas parasetamol menyebabkan peningkatan serum ALT hingga mencapai 5000 u/l (Zimmerman, 1978).
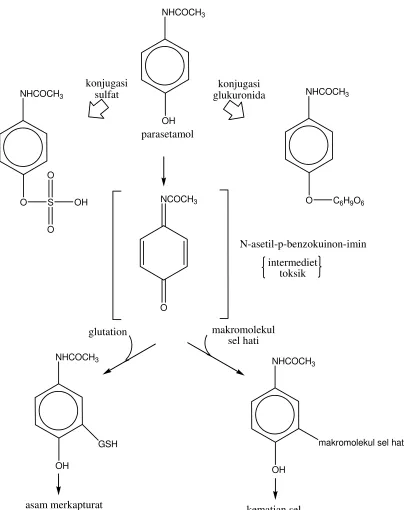
gugus sulfhidril yang mampu menkonjugasi NAPBKI menjadi konjugat merkapturat yang kemudian diekskresi melalui urin (Dollery, 1999; DiPiro, 2005).
Pada kondisi overdosis akut parasetamol, persediaan sulfat tidak memadai untuk mengkonjugasi seluruh parasetamol sehingga lebih banyak parasetamol yang dimetabolisme oleh sitokrom P450, dengan demikian jumlah glutation yang digunakan untuk mendetoksifikasi metabolit reaktif juga tidak memadai. Kemudian NAPBKI bereaksi dengan gugus sulfidril lain yang terdapat dalam hepatoselular seperti sitosol, dinding sel, dan retikulum endoplasma. Hal ini mengakibatkan nekrosis sentrilobuler hepatik (DiPiro, 2005).
NHCOCH3
O
NHCOCH3
OH
NHCOCH3
O NCOCH3
O
intermediet toksik
glutation makromolekul
sel hati NHCOCH3
OH
GSH
NHCOCH3
OH
makromolekul sel hati
kematian sel asam merkapturat
konjugasi glukuronida konjugasi
sulfat
parasetamol
S O
OH
O
C6H9O6
N-asetil-p-benzokuinon-imin
G. Tes Laboratorium Pada Penyakit Hati
Adapun macam-macam tes laboratorium kimia darah dan darah rutin untuk mengetahui fungsi hati, yaitu:
a. Alanin-aminotransferase (ALT)
Alanin-aminotransferase (ALT) dulu bernama glutamat-piruvat transaminase (GPT) (Widmann, 1992). Alanin-aminotransferase merupakan suatu enzim yang diproduksi dalam hepatosit. Jumlah ALT dalam darah meningkat pada kondisi dimana hepatosit rusak atau mati (Worman, 1998).
b. Aspartat-aminotransferase (AST)
Aspartat-aminotransferase (AST) dulu bernama glutamat-oksaloasetat transaminase (GOT) (Widmann, 1992). Aspartat-aminotransferase ditemukan dalam hepatosit, miocardial muscles, otot skeletal, otak, dan ginjal (Tietze, 2004).
c. Alkalin-fosfatase (ALP)
Alkalin-fosfatase adalah enzim yang paling sering diukur untuk menyatakan adanya obstruksi saluran empedu. ALP terdapat di saluran empedu dan epitel hati dan juga dalam osteoblas sebagai sel-sel pembentuk tulang baru, dalam usus, tubulus proksimal ginjal, placenta, dan dalam kelenjar susu yang sedang memproduksi susu. Jadi kadar ALP juga meningkat pada pembentukan tulang yang aktif, wanita hamil, pada beberapa macam disfungsi usus, dan beberapa jenis infark ginjal (Widmann, 1992).
d. Gamma-glutamil transpeptidase (GGT)
termasuk alkohol, dan aktivitas serumnya mungkin meningkat pada peminum berat meskipun peminum tersebut tidak mengalami kerusakan hati atau inflamasi (Worman, 1998).
e. Bilirubin
Bilirubin merupakan salah satu hasil perombakan hem. Bilirubin pasca hepatik yang terkonjugasi bereaksi cepat dalam tes-tes yang biasa dipakai disebut bilirubin direk, dan bilirubin pre-hepatik yang tak terkonjugasi atau terikat protein disebut bilirubin indirek (Widmann, 1992).
f. Albumin
Albumin merupakan protein utama yang beredar dalam aliran darah. Albumin disintesis oleh hati dan disekresikan ke dalam darah. Rendahnya konsentrasi serum albumin mengindikasikan fungsi hati yang buruk (Worman, 1998). Hipoalbuminemia tidak selalu disebabkan oleh penyakit hati (Widmann, 1992). Jumlah albumin bisa rendah pada kondisi yang berbeda (selain penyakit hati) yaitu pada kondisi malnutrisi, beberapa penyakit ginjal, dan pada kondisi lain yang jarang terjadi (Worman, 1998).
g. Laktat dehidrogenase (LDH)
h. Prothrombin time (PT)
Banyak faktor pembekuan darah yang dihasilkan di hati. Prothrombin time adalah tipe faktor pembekuan darah yang digunakan untuk tes di laboratorium dan akan memanjang jika konsentrasi faktor pembeku darah yang dihasilkan oleh hati menurun (Worman, 1998).
i. Platelet count
Platelet adalah sel darah yang paling kecil yang termasuk dalam faktor pembekuan darah. Pada penyakit hati yang kronis, platelet count biasanya menurun (Worman, 1998).
H. Metode Uji Antihepatotoksin
CH3 HC NH2
COO -+ COO-C CH2 O CH2 COO - COO-HC NH2
CH2 CH2 COO -+ C CH3 O COO
-L-Alanin 2-Oksoglutarat L-Glutamat Piruvat
ALT
(Pathegini and Van Solinge, 2006) CH3
C O
COO
-+ NADH +H
LDH CH3 CHOH COO -+ NAD Piruvat Laktat
(Colombo and Peheim, 1981) L-Alanin dan laktat dehidrogenase (LDH) terdapat dalam reagen 1, sedangkan 2-Oksoglutaratdan NADH terdapat dalam reagen 2 (Anonim, 2006b).
I. Polifenol
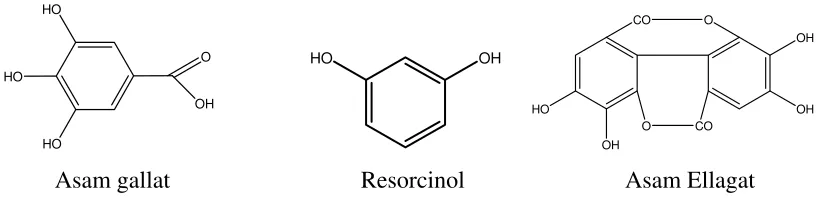
mengurangi resiko penyakit jantung dan sebagai antiinflamasi. Adapun beberapa struktur dasar polifenol adalah sebagai berikut:
HO
HO
HO
OH O
HO OH
OH OH O
CO
O CO OH
HO
Asam gallat Resorcinol Asam Ellagat
Gambar 5. Beberapa stuktur senyawa yang termasuk polifenol (Evans, 1989; Arts dan Hollman, 2005)
J. Keterangan Empiris
BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk jenis penelitian eksperimental murni dengan menggunakan rancangan penelitian acak lengkap pola searah.
Penelitian ini dilakukan dengan tujuan untuk mendapatkan data yang dapat membuktikan kemampuan infusa daun ceplikan menurunkan aktivitas serum ALT pada kerusakan hati hewan uji akibat pemberian parasetamol.
B. Variabel-variabel Penelitian
1. Variabel utama
a. Variabel bebas : dosis infusa daun ceplikan. Dosis infusa daun ceplikan adalah sejumlah (g) simplisia daun ceplikan tiap satuan kg berat badan subyek uji yang bersangkutan.
b. Variabel tergantung : kerusakan hati yang dilihat dari peningkatan aktivitas serum ALTnya.
2. Variabel pengacau terkendali
a. Subyek uji : mencit jantan galur Swiss, berat badan 20 – 30 gram, umur 2 – 3 bulan, dan diperoleh dari laboratorium Farmakologi dan Toksikologi, Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
b. Bahan uji : daun ceplikan dalam kondisi yang masih segar dan berwana hijau.
3. Variabel pengacau tak terkendali
Keadaan patologis hewan uji.
C. Alat dan Bahan Penelitian
1. Alat Penelitian
a. seperangkat alat gelas (Pyrex) b. panci lapis alumunium
c. heater (Thermolyne, Cimarec 2)
d. timbangan elektrik (Mettler Toledo, tipe AB 204, Switzerland) e. spuit per oral dan syringe 3 cc (Terumo® Syringe)
f. pipa kapiler (Brand, Micro haematocrit, Cat. No. 7493 11) g. vitalab mikro (Microlab 200, Merck)
h. sentrifuse (Heraus Christ, Labofuge A) i. kamera (Canon, PowerShot tipe A620)
2. Bahan penelitian
a. Bahan uji yang diujikan adalah daun ceplikan dalam bentuk infusa. Daun ceplikan yang masih segar dan berwarna hijau ini dipetik dari daerah Kutoarjo, Jawa Tengah pada bulan Oktober 2006. Infusa daun ceplikan berwarna hijau kecoklatan.
Farmakologi dan Toksikologi, Fakultas Farmasi, Universitas Sanata Dharma Yogyakarta.
c. CMC-Na sebagai pensuspensi hepatotoksin parasetamol (CMC-Na ini merupakan produksi Brataco Chemica).
d. Aquades sebagai kontrol negatif dan aquabides sebagai pencuci kolom vitalab mikro yang diperoleh dari Laboratorium Farmakologi dan Toksikologi Fakultas Farmasi Universitas Sanata Dharma.
e. Pereaksi siap pakai (kit) DyaSis ALAT (ALT) FS* without pyridoxal-5-phosphate (Dyasis, Germany) untuk mengukur aktivitas ALT serum.
D. Subjek Uji
Hewan uji yang digunakan yaitu mencit jantan galur Swiss, berat badan 20 – 30 gram, umur 2 – 3 bulan, diperoleh dari laboratorium Farmakologi dan Toksikologi, Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
E. Tatacara Penelitian
1. Pengumpulan Bahan
Bahan uji yang digunakan adalah daun ceplikan yang masih segar, berwarna hijau yang dipetik di daerah Kutoarjo, Jawa Tengah.
2. Determinasi tanaman ceplikan (Ruellia tuberosa Linn.)
determinasi yang digunakan ada dua, yaitu (1) Van Stenis (2002) dan (2) Backer and Bakhuizen Van den Brink (1965).
3. Pembuatan simplisia daun ceplikan
Daun ceplikan dicuci bersih di bawah air mengalir. Setelah bersih daun diangin-anginkan hingga daun tidak tampak basah lagi kemudian untuk mengoptimalkan pengeringan, pengeringan dilakukan dengan menggunakan oven pada suhu 50 – 60°C. Setelah kering daun dirajang dan diserbuk.
4. Pembuatan infusa daun ceplikan
Konsentrasi infusa daun ceplikan yang digunakan adalah 10%. Sejumlah (g) simplisia daun ceplikan dicampur dengan air secukupnya, dipanaskan di atas tangas air selama 15 menit terhitung mulai suhu mencapai 90°C sambil sesekali diaduk. Kemudian diserkai selagi panas dengan kain flanel, dan ditambahkan air panas secukupnya melalui ampas hingga diperoleh volume infusa yang dikehendaki.
5. Pembuatan suspensi parasetamol 1%
Suspensi parasetamol 1% dibuat dengan cara mensuspensi sejumlah gram parasetamol yang ditimbang seksama ke dalam CMC 1% hingga konsentrasi yang ditetapkan.
6. Uji pendahuluan
a. Penetapan dosis hepatotoksik parasetamol
berbeda, kelompok I kontrol negatif CMC-Na, kelompok II dengan dosis 225 mg/kgBB; kelompok III dengan dosis 230 mg/kgBB; kelompok IV dengan dosis 237,5 mg/kgBB; kelompok V dengan dosis 250 mg/kgBB kemudian aktivitas serum ALT-nya diukur 24 jam setelah pemejanan.
b. Penetapan waktu pencuplikan darah
Untuk mendapatkan waktu pencuplikan darah dilakukan orientasi dengan 2 kelompok waktu. Dosis hepatotoksin yang digunakan adalah 237,5 mg/kgBB. Kelompok I dan II diberi hepatotoksin, kelompok I 24 jam setelah pemberian hepatotoksin diukur aktivitas serum ALT-nya dan kelompok II 48 jam setelah pemberian hepatotoksin diukur aktivitas serum ALT-nya.
c. Penetapan lama pemenjanan infusa daun ceplikan
dan aktivitas serum ALT-nya diukur 24 jam setelah pemejanan senyawa hepatotoksin.
7. Pengelompokan dan perlakuan hewan uji
Sejumlah 35 ekor mencit jantan dibagi secara acak ke dalam tujuh kelompok masing-masing kelompok berisi lima ekor. Kelompok I (kontrol negatif) dipejankan aquades ad libitium. Kelompok II (kontrol positif) dipejankan suspensi parasetamol dosis 237,5 mg/kgBB. Setelah 24 jam (hasil orientasi) mencit diambil darahnya melalui sinus orbitalis mata kemudian diambil serumnya dan ditetapkan aktivitas serum ALT-nya. Kelompok III (kontrol positif) diberi infusa daun ceplikan dengan dosis tertinggi (3333,3 mg/kgBB). Kelompok IV diberi infusa daun ceplikan dosis 987,7 mg/kgBB, kelompok V diberi infusa daun ceplikan dosis 1481,5 mg/kgBB, kelompok VI diberi infusa daun ceplikan dosis 2222,2 mg/kgBB, dan kelompok VII diberi infusa daun ceplikan dosis 3333,3 mg/kgBB. Pemberian infusa daun ceplikan dilakukan selama enam hari berturut-turut secara per oral, kemudian pada hari ke tujuh kelompok perlakuan ini diberi parasetamol dosis hepatotoksik sebesar 237,5 mg/kgBB. Setelah 24 jam hewan uji diambil darahnya melalui sinus orbitalis mata kemudian diambil serumnya untuk diukur aktivitas serum ALT-nya.
8. Pembuatan serum
9. Pengukuran aktivitas Serum ALT
Alat yang digunakan untuk menganalisis aktivitas serum ALT adalah vitalab-mikro. Pada analisis fotometri aktivitas serum ALT ini dilakukan sejumlah pereaksi seperti yang tersaji pada tabel I.
Tabel I. Prosedur Penetapan Aktivitas Serum ALT berdasarkan Anonim (2006b)
Serum atau plasma 10µl Larutan NaCl 0,9% 90µl Reagen1 1000µl Vortex
Reagen 2 250µl Campur dan baca penurunan serapan dalam 1 menit
Adapun komponen dari reagen 1 adalah TRIS (pH 7,15), L-Alanin, dan LDH (laktat dehidrogenase) dan komponen dari reagen 2 adalah 2-oksaglutarat dan NADH.
Aktivitas enzim dibaca pada panjang gelombang 340nm, suhu 37°C, dengan faktor koreksi -1745. Aktivitas serum ALT dinyatakan dalam u/l. Pengukuran aktivitas serum ALT dilakukan di laboratorium Farmakologi-Toksikologi, Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
F. Analisis Hasil
1. Penetapan dosis hepatotoksik parasetamol
kelompok. Tetapi jika didapat distribusi data yang tidak normal, analisis dilanjutkan dengan analisis non parametrik yaitu uji Kruskal Wallis untuk melihat perbedaan aktivitas serum ALT antar kelompok. Selanjutnya diuji dengan uji Mann Whitney untuk melihat perbedaan tiap kelompok.
2. Penetapan waktu pencuplikan darah
Data serum ALT dianalisis dengan uji Kolmogorov Smirnov untuk melihat distribusi data tiap kelompok. Jika didapatkan distribusi normal, maka analisis dilanjutkan dengan uji T untuk melihat perbedaan kedua kelompok.
3. Penetapan lama pemejanan infusa daun ceplikan
Data serum ALT dianalisis dengan uji Kolmogorov Smirnov untuk melihat distribusi data tiap kelompok. Jika didapat distribusi data yang normal maka analisis dilanjutkan dengan analisis pola searah (One Way ANOVA) dengan taraf kepercayaan 95% yang dilanjutkan dengan uji LSD untuk mengetahui perbedaan masing-masing kelompok. Tetapi jika didapat distribusi data yang tidak normal, analisis dilanjutkan dengan analisis non parametrik yaitu uji Kruskal Wallis untuk melihat perbedaan aktivitas serum ALT antar kelompok. Selanjutnya diuji dengan uji Mann Whitney untuk melihat perbedaan tiap kelompok.
4. Perlakuan hewan uji
BAB IV
HASIL DAN PEMBAHASAN
A. Determinasi Tanaman Ceplikan (Ruellia tuberosa Linn.)
Hasil determinasi menunjukkan bahwa tanaman yang digunakan dalam penelitian ini adalah Ruellia tuberosa Linn. Hasilnya adalah sebagai berikut:
1b – 2b – 3b – 4b – 6b – 7b – 9b – 10b – 11b – 12b – 13b – 14b – 16a (golongan 10) 239b – 243b – 244b – 248b – 249b – 250b – 266b – 267b – 273b – 276b – 278b – 279b – 282b – 283b – 284b – 285b - ...115. Achantaceae 1a – 2b – 7a – 8b – 10a – 11b – 13b – 14b – 16a - ...10. Ruellia 1... Ruellia tuberosa Linn. Surat pengesahan determinasi dapat dilihat pada lampiran 1. Foto tanaman ceplikan dapat dilihat pada lampiran 2.
B. Uji Pendahuluan
1. Penetapan dosis hepatotoksik parasetamol
Penetapan dosis hepatotoksik parasetamol ini mempunyai tujuan yaitu untuk mengetahui besar kisaran dosis parasetamol yang dapat menyebabkan derajat kerusakan hati yang tertinggi dilihat dari peningkatan aktivitas serum ALT. Peringkat dosis yang digunakan dalam penetapan dosis hepatotoksik ini adalah 225; 230; 237,5; dan 250 mg/kgBB. Peringkat dosis ini ditentukan berdasarkan dosis hepatotoksik parasetamol adalah 200 – 300 mg/kgBB (Donatus, 1994). Data aktivitas serum ALT akibat pemberian parasetamol dapat dilihat pada tabel II.
Tabel II. Data aktivitas serum ALT akibat pemberian parasetamol dosis 225; 230; 237,5; 250 mg/kgBB pada jam ke 24
Nilai Aktivitas Serum ALT mencit
ke-Dosis Hepatotoksik Parasetamol
1 2 3
Dosis 225 mg/kgBB 250 u/l 110 u/l 110 u/l Dosis 230 mg/kgBB 180 u/l 650 u/l 440 u/l Dosis 237,5 mg/kgBB 4670 u/l 5690 u/l 4150 u/l Dosis 250 mg/kgBB 14030 u/l 10100 u/l Mati
Berdasarkan hasil yang didapatkan, tampak bahwa peningkatan aktivitas serum ALT dosis 250 mg/kgBB paling tinggi, namun pada dosis tersebut juga terjadi kematian hewan uji sehingga dosis ini tidak disertakan pada analisis selanjutnya. Data yang didapatkan diuji dengan uji Kolmogorov Smirnov untuk melihat distribusi data pada tiap kelompok. Dan didapatkan distribusi data yang normal sehingga analisis dilanjutkan dengan uji One Way ANOVA tapi ternyata varian data tidak homogen, padahal salah satu syarat untuk analisis dengan uji One Way ANOVA adalah varian data harus homogen. Oleh sebab itu, analisis dilanjutkan dengan uji Kruskal Wallis untuk melihat perbedaan pada semua kelompok dan kemudian untuk melihat perbedaan antara kelompok satu dengan kelompok lainnya dilakukan analisis dengan uji Mann Whitney. Rangkuman hasil analisis statistik dapat dilihat pada tabel III dan analisis statistiknya dapat dilihat pada lampiran 12.
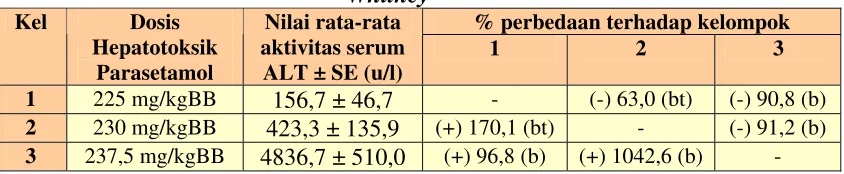
Tabel III. Perbedaan nilai aktivitas serum ALT setelah pemberian parasetamol dosis 225; 230; dan 237,5 mg/kgBB pada jam ke 24 berdasarkan uji Mann
Whitney
% perbedaan terhadap kelompok Kel Dosis
Hepatotoksik Parasetamol
Nilai rata-rata aktivitas serum
ALT ± SE (u/l)
1 2 3
Keterangan :
(b) = berbeda bermakna (p < 0,05) (bt) = berbeda tidak bermakna (p > 0,05) (-) = mengalami penurunan
(+) = mengalami peningkatan
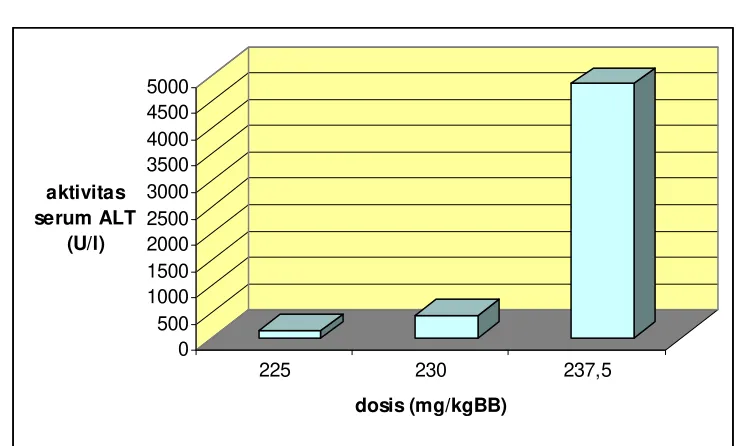
0 500 1000 1500 2000 2500 3000 3500 4000 4500 5000
aktivitas serum ALT
(U/l)
225 230 237,5
dosis (mg/kgBB)
Gambar 6. Diagram Batang Aktivitas Serum ALT setelah Pemberian Parasetamol dosis 225; 230; dan 237,5 mg/kgBB pada jam ke 24
bahwa tingkat kerusakan hati yang terjadi pada mencit yang telah diberi parasetamol dosis 237,5 mg/kgBB mengalami nekrosis hati. Dan berdasarkan analisis statistik, perbedaan kelompok parasetamol dosis 237,5 mg/kgBB terhadap kelompok parasetamol dosis 225 dan 230 mg/kgBB adalah berbeda bermakna. Oleh sebab itu, dosis hepatotoksin yang digunakan dalam penelitian ini adalah 237,5 mg/kgBB.
2. Penetapan waktu pencuplikan darah
Setelah didapatkan dosis hepatotoksik parasetamol yang akan digunakan dilakukan penetapan waktu pencuplikan darah. Penetapan waktu pencuplikan darah mempunyai tujuan yaitu untuk menentukan waktu pencuplikan darah yang menunjukkan selang waktu yang dibutuhkan untuk mencapai peningkatan aktivitas serum ALT yang paling optimal. Dosis hepatotoksin yang digunakan adalah 237,5 mg/kgBB. Waktu pencuplikan yang digunakan adalah 24 dan 48 jam. Data aktivitas serum yang didapatkan dapat dilihat pada tabel IV.
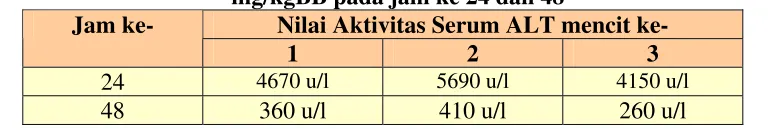
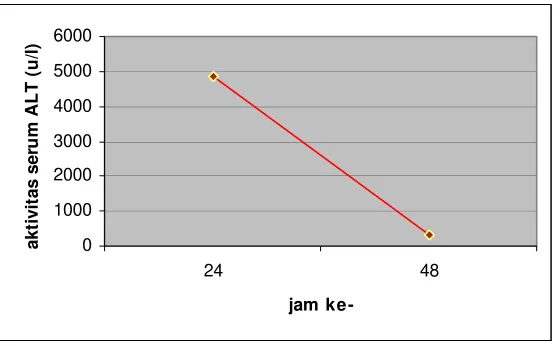
Tabel IV. Data aktivitas serum ALT setelah pemberian parasetamol dosis 237,5 mg/kgBB pada jam ke 24 dan 48
Nilai Aktivitas Serum ALT mencit ke- Jam ke-
1 2 3
24 4670 u/l 5690 u/l 4150 u/l
48 360 u/l 410 u/l 260 u/l
Tabel V. Perbedaan nilai aktivtas serum ALT setelah Pemberian Parasetamol dosis 237,5 mg/kgBB pada jam ke 24 dan 48 berdasarkan uji T
Keterangan :
(b) = berbeda bermakna (p < 0,05) (bt) = berbeda tidak bermakna (p > 0,05) (-) = mengalami penurunan
(+) = mengalami peningkatan
0 1000 2000 3000 4000 5000 6000 24 48
jam
ke-akt ivi tas ser u m A L T ( u /l )
Gambar 7. Grafik Aktivitas Serum ALT setelah Pemberian Parasetamol dosis 237,5 mg/kgBB pada jam ke 24 dan 48
Dari tabel V dan gambar 7, tampak bahwa peningkatan aktivitas serum ALT dengan waktu pencuplikan 24 jam (4836,7 ± 452,3 u/l) lebih tinggi dibanding aktivitas serum ALT dengan waktu pencuplikan 48 jam (343,3 ± 44,1 u/l) dan secara statistik perbedaan kedua kelompok adalah berbeda bermakna (p < 0,05). Jadi, waktu pencuplikan 24 maupun 48 jam menunjukkan bahwa waktu pencuplikan mempengaruhi peningkatan aktivitas serum ALT. Oleh sebab itu, dalam penelitian ini digunakan waktu pencuplikan 24 jam.
% perbedaan terhadap kelompok
Kel Jam
ke
Nilai rata-rata aktivitas serum
ALT ± SE (u/l)
1 2
3. Penetapan lama pemejanan infusa daun ceplikan
Penetapan lama pemejanan infusa daun ceplikan bertujuan untuk mengetahui waktu yang dibutuhkan oleh infusa daun ceplikan untuk dapat menurunkan aktivitas serum ALT yang paling besar. Karena diharapkan dengan penurunan yang paling besar maka infusa akan mempunyai daya proteksi yang paling besar pula terhadap hati.
Adapun kelompok waktu yang digunakan untuk menentukan lama waktu pemejanan infusa daun ceplikan adalah 2, 4, 6, dan 8 hari, dan dosis infusa yang digunakan adalah 2222,2 mg/kgBB. Data aktivitas serum ALT setelah pemejanan infusa daun ceplikan selama 2, 4, 6, dan 8 hari dapat dilihat pada tabel VI.
Tabel VI. Data Aktivitas Serum ALT Setelah Pemejanan Infusa Daun Ceplikan selama 2, 4, 6, dan 8 hari
Nilai Aktivitas Serum ALT mencit ke-Lama pemejanan
1 2 3
2 hari 12250 U/L 10570 U/L 11650 U/L
4 hari 6990 U/L 8410 U/L 12310 U/L
6 hari 2540 U/L 2280 U/L 2440 U/L
8 hari 3490 U/L 4670 U/L 2720 U/L
dengan uji Mann Whitney. Rangkuman hasil penurunan aktivitas serum ALT setelah pemejanan infusa daun ceplikan selama 2, 4, 6, dan 8 hari dapat dilihat pada tabel VII dan analisis statistiknya dapat dilihat pada lampiran 14.
Tabel VII. Persen perbedaan nilai aktivitas serum ALT mencit terinduksi parasetamol dengan praperlakuan infusa daun ceplikan selama 2, 4, 6, dan 8
hari berdasarkan uji Mann Whitbney
% perbedaan terhadap kelompok Kel Lama pemejanan infusa Nilai rata-rata aktivitas serum ALT ±
SE (u/l)
I II III IV
I 2 hari 11490 ± 491,5 - (+) 24,4 (bt)
(+) 374,8 (b)
(+) 216,8 (b)
II 4 hari 9236,7 ± 1590,4
(-) 19,6 (bt)
- (+) 281,6 (b)
(+) 154,7 (b)
III 6 hari 2420 ± 75,7 (-) 78,9 (b)
(-) 73,8 (b)
- (-) 33,3 (b)
IV 8 hari 3626,7 ± 567,0 (-) 68,4 (b) (-) 60,7 (b) (+) 49,7 (b) - Keterangan :
(b) = berbeda bermakna (p < 0,05) (bt) = berbeda tidak bermakna (p > 0,05) (-) = mengalami penurunan
(+) = mengalami peningkatan
Tabel VIII. Persen proteksi setelah praperlakuan infusa daun ceplikan dosis 2222,2 mg/kgBB selama 2, 4, 6, dan 8 hari pada mencit jantan terinduksi
parasetamol Kelompok
(hari)
n Nilai rata-rata aktivitas serum ALT ± SE (U/L)
% Efek Proteksi
2 3 11490 ± 491,5 (-) 137,7
4 3 9236,7 ± 1590,4 (-) 91,0
6 3 2420 ± 75,7 (+) 50,0
8 3 3626,7 ± 567,0 (+) 25,0
pada pemakaian jangka pendek infusa daun ceplikan belum dapat memberikan proteksi terhadap kerusakan hati akibat pemberian parasetamol. Pada lama pemejanan infusa selama 6 hari (2420 ± 75,7 u/l) dan 8 hari (3626,7 ± 567,0 u/l) terjadi penurunan aktivitas serum ALT bila dibandingkan dengan kontrol hepatotoksin (4836,7 ± 510,0 u/l), berarti pada pemakaian selama 6 dan 8 hari infusa daun ceplikan sudah dapat memberikan proteksi terhadap kerusakan hati akibat pemberian parasetamol.
-150 -100 -50 0 50 100
2 hari 4 hari 6 hari 8 hari
lama pemejanan infusa
%
p
ro
te
ksi
Gambar 8. Grafik Aktivitas Serum ALT setelah Pemejanan Infusa Daun Ceplikan Selama 2, 4, 6, dan 8 hari
C. Pengelompokan dan perlakuan hewan uji
1. Kontrol Negatif CMC-Na
Tujuan digunakan kontrol negatif adalah sebagai kelompok pembanding hati yang tidak mengalami kerusakan. Perlakuan pada kontrol negatif yang digunakan adalah CMC-Na karena CMC-Na merupakan pensuspensi parasetamol. Disamping itu juga dapat dilihat apakah kerusakan hati hanya diakibatkan oleh parasetamol saja ataukah pensuspensinya juga mengakibatkan kerusakan hati.
2. Kontrol Positif Hepatotoksin
Tujuan digunakannya kontrol positif adalah untuk membandingkan peningkatan nilai aktivitas serum ALT pada hati yang mengalami kerusakan akibat pemberian hepatotoksin (parasetamol).
Nilai aktivitas serum ALT yang dihasilkan setelah pemberian parasetamol dosis 237,5 mg/kgBB adalah 4836,7 ± 315,3 u/l. Sedangkan, nilai aktivitas serum ALT kontrol negatif pemberian CMC-Na 1% adalah 153,3 ± 5,8 u/l. Bila nilai aktivitas serum ALT kedua kelompok tersebut dibandingkan maka perbedaan nilai aktivitas serum ALT mengalami peningkatan sebesar 3054,4%, nilai ini menunjukkan perbedaan yang bermakna. Dilihat dari persentase perbedaan tersebut dapat disimpulkan bahwa parasetamol menyebabkan kerusakan hati.
Dilihat secara makroskopis (lampiran 6), hati berwarna merah kecoklatan dan terdapat bintik-bintik putih pada permukaan hati.
3. Kontrol Positif Infusa Daun Ceplikan Dosis Tertinggi
Pada kelompok ini, mencit diberi infusa daun ceplikan selama 6 hari berturut-turut dan pada jam ke-24 setelah pemenjanan infusa hari ke-6 nilai aktivitas serum ALT mencit diukur. Tujuan dilakukan kontrol positif infusa daun ceplikan dosis tertinggi ini adalah untuk mengetahui toksisitas infusa daun ceplikan.
(lampiran 7), hati berwarna merah kecoklatan dan tidak terdapat bintik-bintik putih dipermukaannya.
4. Kelompok Perlakuan
Pada kelompok perlakuan ini terdapat 4 kelompok perlakuan yaitu, kelompok I diberi infusa daun ceplikan dosis 987,7 mg/kgBB, kelompok II diberi infusa daun ceplikan dosis 1481,5 mg/kgBB, kelompok III diberi infusa daun ceplikan dosis 2222,2 mg/kgBB, dan kelompok IV diberi infusa daun ceplikan dosis 3333,3 mg/kgBB. Data aktivitas serum ALT setelah pemejanan infusa daun ceplikan dosis 987,7; 1481,5; 2222,2; dan 3333,3 mg/kgBB selama 6 hari berturut-turut terhadap parasetamol dosis 237,5 mg/kgBB dengan waktu pencuplikan 24 jam dapat dilihat pada tabel IX.
Tabel IX. Data Aktivitas Serum ALT Setelah Pemejanan Infusa Daun Ceplikan dosis 987,7; 1481,5; 2222,2; dan 3333,3 mg/kgBB selama 6 hari berturut-turut terhadap Mencit Jantan Terinduksi Parasetamol dosis 237,5 mg/kgBB dengan
waktu pencuplikan 24 jam Dosis Infusa n Rata-rata Aktivitas Serum
ALT ± SE
% Proteksi
987,7 mg/kgBB 5 8916 ± 404,4 U/L -92,2%
1481,5 mg/kgBB 5 6652 ± 304,3 U/L -43,4%
2222,2 mg/kgBB 5 2374 ± 173,4 U/L 48,8%
3333,3 mg/kgBB 5 584 ± 75,9 U/L 87,4%
melihat perbedaan antara kelompok satu dengan kelompok lainnya dilakukan analisis dengan uji Mann Whitney. Hasil analisis statistik tersebut dapat dilihat pada lampiran 15.
-100 -80 -60 -40 -20 0 20 40 60 80 100
% proteksi
987,7 1481,5 2222,2 3333,3
dosis infusa daun ceplikan (mg/kgBB)
Gambar 9. Diagram Batang Aktivitas Serum ALT setelah Pemejanan Infusa Daun Ceplikan Dosis 987,7; 1481,5; 2222,2; dan 3333,3 mg/kgBB selama 6 hari berturut-turut terhadap terhadap Mencit Jantan Terinduksi Parasetamol dosis
237,5 mg/kgBB dengan waktu pencuplikan 24 jam
serum ALT bila dibandingkan dengan kontrol positif. Pemejanan infusa dosis 2222,2 mg/kgBB dapat menurunkan aktivitas serum ALT hingga 48,8% dan pemejanan infusa dosis 3333,3 mg/kgBB dapat menurunkan aktivitas serum ALT hingga 87,4% bila dibandingkan dengan kontrol hepatotoksin. Berarti, pada dosis 2222,2 dan 3333,3 mg/kgBB infusa daun ceplikan mampu memberikan proteksi terhadap kerusakan hati akibat pemberian parasetamol.
Terjadinya peningkatan aktivitas serum ALT pada kelompok perlakuan infusa dosis 987,7 dan 1481,5 mg/kgBB kemungkinan karena adanya senyawa yang terkandung dalam infusa daun ceplikan yang dapat menginduksi sitokrom P450 atau menghambat pengikatan NAPBKI dengan glutation. Hal ini mengakibatkan meningkatnya jumlah NAPBKI yang berikatan dengan makromolekul sel yang ditunjukkan oleh peningkatan aktivitas serum ALT.
Terjadinya penurunan aktivitas serum ALT pada mencit yang terinduksi parasetamol ini kemungkinan karena adanya aktivitas antioksidan dari senyawa polifenol yang terdapat dalam daun ceplikan. Kemungkinan mekanisme penurunan aktivitas serum ALT yang terjadi ini karena aktivitas senyawa polifenol yang terdapat dalam infusa daun ceplikan mampu meningkatkan jumlah glutation. Oleh sebab itu, mekanisme perusakan sel hati oleh N-asetil-p-benzokuinon-imin (NAPBKI) bisa dihambat.
selama 6 hari berturut-turut terhadap parasetamol dosis 237,5 mg/kgBB dengan waktu pencuplikan 24 jam dapat dilihat pada tabel IX.
Tabel X. Persen perbedaan nilai aktivitas serum ALT praperlakuan infusa daun ceplikan dosis 987,6; 1481,5; 2222,2; dan 3333,3 mg/kgBB selama 6 hari berturut-turut pada mencit jantan terinduksi Parasetamol dosis 237,5 mg/kgBB
% perbedaan terhadap kelompok
kel n
Nilai rata-rata aktivitas serum ALT ± SE (u/l)
I II III IV V VI VII
I 5 136 ±
4,0 - (-) 97,1 (b) 0 (bt) (-) 6455,9 (b) (-) 4791,2 (b) (-) 94,3 (b) (-) 76,7 (b)
II 5 4640 ±
315,3
(+)3311,8
(b) -
(+)3311,8 (b) (-) 48,0 (b) (-) 30,2 (b) (+) 95,5 (b) (+) 694,5 (b)
III 5 136 ±
2,4 0 (bt)
(-) 97,1 (b) - (-) 98,5 (b) (-) 98,0 (b) (-) 94,3 (b) (-) 76,7 (b)
IV 5 8916 ±
404,4 (+)6455,9 (b) (+)92,2 (b) (+)6455,9
(b) -
(+)34,0 (b) (+)275,6 (b) (+)1426,7 (b)
V 5 6652 ±
304,3 (+)4791,1 (b) (+)43,4 (b) (+)4791,1 (b) (-) 25,4 (b)
- (+)180,2 (b)
(+)1039,0 (b)
VI 5 2374 ±
173,4 (+)1645,6 (b) (+)48,8 (b) (+)1645,6 (b) (-) 73,4 (b) (-) 64,3 (b)
- (+) 306,5 (b)
VII 5 584 ±
75,9 (+)329,4 (b) (-) 87,4 (b) (+)329,4 (b) (-) 93,4 (b) (-) 91,2 (b) (-) 75,4
(b) -
Keterangan:
I : Kelompok kontrol negatif II : Kelompok kontrol hepatotoksin
III : Kelompok kontrol positif infusa dosis tertinggi
V : Kelompok perlakuan infusa dosis 1481,5 mg/kgBB + parasetamol dosis 237,5 mg/kgBB
VI : Kelompok perlakuan infusa dosis 2222,2 mg/kgBB + parasetamol dosis 237,5 mg/kgBB
VII : Kelompok perlakuan infusa dosis 3333,3 mg/kgBB + parasetamol dosis 237,5 mg/kgBB
0 1000 2000 3000 4000 5000 6000 7000 8000 9000
Aktivitas Serum ALT
(U/L)
1 2 3 4 5 6 7
Kelompok Perlakuan
Gambar 10. Diagram Batang Aktivitas Serum ALT Kontrol Negatif, Kontrol Hepatotoksin, Kontrol Positif Infusa Dosis Tertinggi, dan Setelah Pemejanan Infusa Daun Ceplikan Dosis 987,7; 1481,5; 2222,2; dan 3333,3 mg/kgBB selama
6 hari berturut-turut pada Mencit Jantan Terinduksi Parasetamol dosis 237,5 mg/kgBB dengan waktu pencuplikan 24 jam
D. Rangkuman Pembahasan
jangka pendek belum dapat memberikan proteksi terhadap kerusakan hati akibat pemberian parasetamol. Dan pada penggunaan infusa dosis tinggi dan pada jangka panjang terjadi penurunan nilai aktivitas serum ALT. Hal ini berarti pada penggunaan infusa daun ceplikan dosis tinggi dan jangka panjang dapat memberikan proteksi terhadap kerusakan hati akbibat pemberian parasetamol.
Peningkatan aktivitas serum ALT setelah praperlakuan infusa daun ceplikan kemungkinan karena adanya senyawa yang terkandung dalam infusa daun ceplikan yang dapat menginduksi sitokrom P450 atau menghambat pengikatan NAPBKI dengan glutation. Hal ini mengakibatkan meningkatnya jumlah NAPBKI yang berikatan dengan makromolekul sel yang ditunjukkan oleh peningkatan aktivitas serum ALT.
Penurunan aktivitas serum ALT setelah praperlakuan infusa daun ceplikan diduga karena adanya kandungan polifenol yang mempunyai khasiat sebagai antioksidan yang mampu meningkatkan jumlah glutation dalam hati. Dengan meningkatnya jumlah glutation maka jumlah NAPBKI yang berikatan dengan makromolekul sel semakin sedikit.
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Dari hasil analisis data, dapat ditarik kesimpulan bahwa infusa daun ceplikan dosis 2222,2 dan 3333,3 mg/kgBB mampu menurunkan aktivitas serum ALT pada kerusakan hati mencit jantan akibat pemberian parasetamol.
B. Saran
Perlu dilakukan penelitian lebih lanjut tentang:
1. kandungan kimia yang pasti di dalam infusa daun ceplikan yang dapat meningkatkan maupun menurunkan efek hepatoprotektor daun ceplikan.
2. kisaran dosis efektif infusa daun ceplikan untuk dapat memberikan efek hepatoprotektif.
3. uji histopatologi hati mencit untuk melihat efek hepatoprotektor infusa daun ceplikan secara mikroskopis.
4. uji keteratogenikan infusa daun ceplikan. 5. uji analgesik infusa daun ceplikan.
DAFTAR PUSTAKA
Anonim, 1995, Farmakope Indonesia, edisi IV, 9, 649, Departemen Kesehatan Republik Indonesia, Jakarta.
Anonim, 2006a, Ruellia tuberosa L., http ://bebas.vlsm.org/v12/artikel/ttg_tanaman_obat/depkes/buku4/4-079.pdf.
Diakses pada 29 April 2006.
Anonim, 2006b, ALAT (GPT) FS*, Diagnostic Systems International, DiaSys Diagnostic Systems GmbH, Alte Strasse 9, 65558 Holzheim, Germany.
Arts, I. C. and P. C. Hollman, 2005, Polyphenols and Disease Risk in Epidemiologic Studies, Am J Clin Nutr, 81,317 – 325.
Backer, C. A., and Bakhuizen Van den Brink, R. C., 1965, Flora of Java, volume II, 557, N. V. P. Noordhoff, The Netherlands.
Bruneton, J., 1999, Pharmacognosy: Phytochemistry Medical Plants, diterjemahkan oleh Caroline K. Hatton, 2nd edition, 227 – 243, 671 – 677, Lavoisier, France.
Chandrasoma, P., and Taylor, C. R., 1995, Concise Pathology, 2nd edition, 621, 629, FRC Path Prentice Hall International, USA.
Colombo, J. P., and Peheim, E., 1981, 1981, Liver, in Richterich, R., Colombo, J. P., (Eds.), Clinical Chemistry, 606 – 610, John Wiley & Sons, USA.
De Jesus, S., and Rodriguez, E., 2002,
http://labs.plantbio.cornell.edu/cubl./emanv4p54b.html. Diakses pada 29 April 2006.
DiPiro, J. T., Talbert, R. L., Yee, G.I., Matzke, G.R., Wells, B.G., and Posey, L.M., 2005, Pharmacotherapy A Pathopysiologic Approach, I edition, 133, McGraw Hill Companies, United States of America.
Dollery, C., 1999, Therapeutic Drugs, 19 – 21, 2nd edition, Harcourt Brace and Company Ltd., United Kingdom.
Donatus, I. A., 1994, Antaraksi Kurkumin dengan Parasetamol: Kajian Terhadap Aspek Farmakologi dan Toksikologi Perubahan Hayati Parasetamol, Disertasi, Universitas Gadjah Mada, Yogyakarta.
Donatus, I. A., 2001, Toksikologi Dasar, 200 – 202, Laboratorium Farmakologi dan Toksikologi, Fakultas Farmasi, Universitas Gadjah Mada, Yogyakarta.
Evans, W. C., 1989, Trease and Evans’ Pharmacognosy, 13th edition, 378 – 423, El BS., London.
Fox, S. I., 2004, Human Physiology, 8th edition, 575 – 580, McGraw-Hill, New York.
Ismayani, S., 2004, Efek Hipoglikemi Rebusan Daun Pletekan (Ruellia tuberosa Linn.) pada Tikus Putih Jantan Terbebani Glukosa dengan Metode Spektrofotometri Visibel, Skripsi, Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
Klaasen, C. D., 2001, Principles of Toxicology and Treatment of Poisoning, in Hardman, J. G., Limbird, L. E., Goodman and Gilman’s The Pharmacological Basis of Therapeutics, 10th edition, McGraw-Hill Companies, United States of America.
Lee, W. M., 1995, Drug-Induced Hepatotoxicity, The New England Journal of Medicine, 333, 1118 – 1127.
Madona, V., 2004, Efek Hepatoprotektif Sari Umbi Wortel (Daucus carota L.) Tipe Imperator, Chantenay, dan Nantes pada Mencit Jantan Terinduksi Parasetamol, Skripsi, Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
Panteghini, M., and Van Solinge, W. W., 2006, Enzymes, in C. A. Burtis, E. R. Ashwood, D. E. Bruns, Tietz Textbook of Clinical Chemistry and Molecular Diagnostic, 604 – 606, El Sevier Inc., United States of America.
Price, S. A., and Wilson, L. M., 1994, Pathophysiology, diterjemahkan oleh Adji Dharma, Ed. 4, 426 – 457, EGC, Jakarta.
Purwandani, Y. L., 2005, Efek Hepatoprotektif Ekstrak Etanol Daging Buah Makuto Dewo (Phaleria macrocarpa (Sheff.) Boerl.) Pada Mencit Jantan Terinduksi Parasetamol, Skripsi, Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
Stine, K. E., and Brown, T. M., 1996, Principles of Toxicology, 149, Lewis Publisher, USA.
Sutinah, S., 1986, Isolasi dan Identifikasi Senyawa Golongan Flavonoid dari Bunga Ruellia tuberosa Linn, Penelitian Tanaman Obat di Beberapa Perguruan Tinggi di Indonesia, Fakultas Farmasi, Universitas Airlangga, Surabaya. Treinen, M., and Moslen, 2001, Toxic Responses of The Liver, Casarett and
Doull’s. Toxicology: The Basic Science of Poison, 476 – 478, McGraw-Hill, New York.
Tietze, K. J., 2004, Clinical Skills for Pharmacist A Patient-Focused Approach, second edition, 116 – 117, Mosby Inc., Missouri.
Tucker, J., 2003, Acetaminophen Toxicity, http :// www.emedicine.com/cgi-bin/foxweb.exe/screen@d:\em\ga?book=ped&authorid=1729&topicid7. Diakses pada 10 Oktober 2006.
Van Stenis, C. G. G. J, Bloembergen, S., and Eyma, P. J., 2002, Flora, diterjemahkan oleh Moeso Surjowinoto, Soenarto Hardjosuwarno, Soerjo Sodo Adisewojo, Wibisono, Margono Partodidjojo, dan Soemantri Wirjahardja, cetakan 8, 378 – 382, PT. Pradnya Paramitha, Jakarta.
Widmann, F. K., 1992, Clinical Interpretation of Laboratory Tests, diterjemahkan oleh Kresno, S. B., Gandasoebrata, R., Latu, J., edisi 9, 301 – 341, Penerbit Buku Kedokteran EGC, Jakarta.
Wilmana, P. F., 2002, Analgesik – Antipiretik Analgesik Anti-Inflamasi Nonsteroid dan Obat Pirai, Farmakologi dan Terapi, edisi 4, 214 – 215, Gaya Baru, Jakarta.
Worman, H. J., 1998, Common Laboratory Test in Liver Diseases, http ://cpmcnet.columbia.edu/www/search.cgi?/dept/gi/labtests.html. Diakses pada 29 April 2006.
Lampiran 1
Lampiran 2
Lampiran 3
Lampiran 4
Lampiran 5
Foto hati kontrol negatif CMC-Na
(hati difoto dengan kamera 7,1 megapiksel)
Lampiran 6
Foto hati kontrol hepatotoksin
(hati difoto dengan kamera 7,1 megapiksel)
Lampiran 7
Foto hati kontrol infusa dosis tertinggi
(hati difoto dengan kamera 7,1 megapiksel)
Lampiran 8
Perhitungan dosis infusa daun ceplikan (Ruellia tuberosa Linn)
Konsentrasi infusa daun ceplikan yang digunakan adalah 10% (Anonim, 1995). Perhitungan dosis tertinggi pada mencit 30 g adalah sebagai berikut:
Dosis infusa =
kgBB 0,03
ml 1 x ml g/100 10 BB
V x C
=
= 3333,3 mg/kgBB
Lampiran 9
Konversi dosis infusa daun ceplikan yang mampu menurunkan aktivitas serum
ALT pada kerusakan hati mencit jantan akibat pemberian parasetamol ke
manusia
Dosis infusa daun ceplikan yang mampu menurunkan akivitas serum ALT pada kerusakan hati mencit jantan akibat pemberian parasetamol adalah 2222,2 dan 3333,3 mg/kgBB. Maka konversi dosis tersebut pada manusia dengan berat badan 70 kg adalah :
Dosis 2222,2 mg/kgBB Dosis 3333,3 mg/kgBB
= 2222,2 mg/1000 gBB = 3333,3 mg/1000 gBB
= 44,4 mg/20 gBB = 66,6 mg/20 gBB
= 44,4 mg x 387,9 = 66,6 mg x 387,9
= 17222,8 mg/70 kgBB = 25834,1 mg/70 kgBB
Lampiran 10
Tabel XI. Data aktivitas serum ALT mencit jantan setelah pemejanan CMC Na (kontrol negatif), parasetamol (kontrol positif), infusa daun ceplikan dosis tertinggi (kontrol positif), dan setelah praperlakuan infusa daun ceplikan dosis 987,7; 1481,5; 2222,2; dan 3333,3 mg/kgBB selama 6 hari berturut-turut terhadap parasetamol dosis 237,5 mg/kgBB dengan waktu pencuplikan 24 jam
Kelompok I II III IV V VI VII
130 4670 140 9060 6860 2540 730
140 5690 140 8300 5660 2280 430
130 4150 140 10400 7360 2440 450
130 3860 130 8130 7090 1780 510
Serum ALT(U/L)
150 4830 130 8690 6290 2830 800
Rata-rata 136 4640 136 8916 6652 2374 584
SE 4,0 315,3 2,4 404,4 304,3 173,4 169,6
Keterangan:
I : Kelompok kontrol negatif CMC Na II : Kelompok kontrol positif parasetamol
III : Kelompok kontrol negatif infusa daun ceplikan dosis tertinggi
IV : Kelompok perlakuan infusa daun ceplikan dosis 987,7 mg/kgBB + parasetamol dosis 237,5 mg/kgBB
V : Kelompok perlakuan infusa daun ceplikan dosis 1481,5 mg/kgBB + parasetamol dosis 237,5 mg/kgBB
VI : Kelompok perlakuan infusa daun ceplikan dosis 2222,2 mg/kgBB + parasetamol dosis 237,5 mg/kgBB
Lampiran 11
Tabel XII. Persen proteksi setelah praperlakuan infusa daun ceplikan selama 6 hari berturut-turut pada mencit jantan terinduksi parasetamol
Kelompok Persen proteksi (%)
I -92,2
II 43,4
III 48,8
IV 87,4
Keterangan:
I : Kelompok perlakuan infusa daun ceplikan dosis 987,7 mg/kgBB selama 6 hari berturut-turut + parasetamol dosis 237,5 mg/kgBB
II : Kelompok perlakuan infusa daun ceplikan dosis 1481,5 mg/kgBB selama 6 hari berturut-turut + parasetamol dosis 237,5 mg/kgBB
III : Kelompok perlakuan infusa daun cepliksn dosis 2222,2 mg/kgBB selama 6 hari berturut-turut + parasetamol dosis 237,5 mg/kgBB
IV : Kelompok perlakuan infusa daun ceplikan dosis 3333,3 mg/kgBB selama 6 hari berturut-turut + parasetamol dosis 237,5 mg/kgBB
Rumus perhitungan persentase efek hepatoprotektif:
Lampiran 12
Hasil Analisis Kolmogorov Smirnov yang dilanjutkan dengan uji Kruskal Wallis
dan uji Mann Whitney pada Penetapan Dosis Hepatotoksik Parasetamol
NPar Tests
One-Sample Kolmogorov-Smirnov Test
ALT
N 3
Mean 153.33
Normal Parameters(a,b)
Std. Deviation 5.774
Absolute .385
Positive .385
Most Extreme Differences
Negative -.282
Kolmogorov-Smirnov Z .667
Asymp. Sig. (2-tailed) .766
a Test distribution is Normal. b Calculated from data.
NPar Tests
One-Sample Kolmogorov-Smirnov Test
ALT
N 3
Mean 156.67
Normal Parameters(a,b)
Std. Deviation 80.829
Absolute .385
Positive .385
Most Extreme Differences
Negative -.282
Kolmogorov-Smirnov Z .667
Asymp. Sig. (2-tailed) .766
NPar Tests
One-Sample Kolmogorov-Smirnov Test
ALT
N 3
Mean 423.33
Normal Parameters(a,b)
Std. Deviation 235.443
Absolute .195
Positive .183
Most Extreme Differences
Negative -.195
Kolmogorov-Smirnov Z .338
Asymp. Sig. (2-tailed) 1.000
a Test distribution is Normal. b Calculated from data.
NPar Tests
One-Sample Kolmogorov-Smirnov Test
ALT
N 3
Mean 4836.67
Normal Parameters(a,b) Std. Deviation
783.411
Absolute .251
Positive .251
Most Extreme Differences
Negative -.195
Kolmogorov-Smirnov Z .435
Asymp. Sig. (2-tailed) .992
a Test distribution is Normal. b Calculated from data.
Oneway
Descriptives
ALT
N Mean
Std.
Deviation Std. Error
95% Confidence Interval for Mean
Mini mum
Maxi mum
Bound Lower Bound Upper
Test of Homogeneity of Variances
ALT
Levene
Statistic df1 df2 Sig.
24.190 3 7 .000
ANOVA
ALT
Sum of
Squares df Mean Square F Sig. Between Groups 40005363.
636 3 13335121.212 144.902 .000 Within Groups 644200.00
0 7 92028.571
Total 40649563.
636 10
NPar Tests
Kruskal-Wallis Test
Ranks
dosis N Mean Rank
ALT kontrol CMC 3 4.00
dosis 225 3 3.33
dosis 230 3 7.67
dosis 237.5 3 11.00
Total 12
Test Statistics(a,b)
ALT
Chi-Square 8.805
df 3
Asymp. Sig. .032
NPar Tests
Mann-Whitney Test
Ranks
dosis N Mean Rank
Sum of Ranks
ALT kontrol CMC 3 4.00 12.00
dosis 225 3 3.00 9.00
Total 6
Test Statistics(b)
ALT
Mann-Whitney U 3.000
Wilcoxon W 9.000
Z -.674
Asymp. Sig. (2-tailed) .500 Exact Sig. [2*(1-tailed
Sig.)] .700(a)
a Not corrected for ties. b Grouping Variable: dosis