1
BAB I PENDAHULUAN A. Latar Belakang
Indonesia merupakan negara megabiodiversitas yang memiliki kekayaan hayati begitu besar. Dari 40 ribu spesies tanaman, sebanyak 30 ribu terdapat di Indonesia. Yang berpotensi menjadi obat berkisar 9 ribu jenis tanaman, namun sampai sekarang yang digunakan untuk membantu pelayanan pengobatan tradisional hanya 400 tanaman. Saat ini para ahli obat sedang melakukan penelitian terhadap lebih dari 120 jenis tanaman, yang berarti potensi obat tradisional masih banyak dan jika terus dikembangkan maka akan menciptakan masyarakat Indonesia yang makmur, cerdas, dan sehat.
Beberapa jenis tanaman khas Indonesia yang saat ini sedang dikembangkan adalah keladi tikus (Typhonium flagelliforme (Lodd.) Blume), sirih merah (Piper crocatum Ruiz & Pav.), dan meniran (Phyllanthus niruri L.) yang diformulasikan dalam sebuah produk oleh GamaHerbal, selanjutnya disebut produk KSM. Kombinasi herbal tersebut telah diketahui memiliki aktivitas imunomodulator, secara spesifik yakni imunostimulator dimana konsumsi produk KSM dengan dosis 500 mg tiga kali sehari dapat memodulasi sistem imun tubuh dengan cara menstimulasinya.
Imunomodulator menjadi esensial saat ini seiring dengan maraknya pembangunan di Indonesia yang meningkatkan polusi udara, perubahan pola makan dan gaya hidup, perubahan cuaca, bahkan pencegahan sampai terapi suportif terhadap penyakit degeneratif. Dengan adanya kondisi-kondisi tersebut,
manusia dituntut untuk senantiasa menjaga kesehatan tubuhnya dan mencegah dirinya terserang berbagai penyakit. Dari hal ini maka kebutuhan manusia akan suplemen untuk meningkatkan imunitas tubuh tidak diragukan lagi.
Dengan pesatnya perkembangan penelitian mengenai suplemen dan obat-obatan, uji terhadap keamanan konsumsinya juga turut dilakukan. Konsumsi suplemen atau obat-obatan pada manusia harus memenuhi persyaratan yakni
safety, effication, and acceptable. Diantara ketiga syarat utama tersebut, yang paling penting adalah safety atau keamanan. Oleh karena itu diperlukan adanya uji toksisitas pada produk farmasi sebelum digunakan sebagai bukti bahwa produk farmasi tersebut memenuhi aspek keamanan terkhusus pada organ ginjal yang seringkali menjadi sasaran efek toksik. Sama halnya dengan produk KSM, maka pada penelitian ini dilakukan uji toksisitas subkronis produk KSM untuk mengetahui keamanan produk tersebut pada penggunaan terhadap ginjal tikus betina galur SD di tingkat subkronis.
B. Rumusan Masalah
Rumusan masalah dalam penelitian ini adalah:
1. Bagaimana wujud efek toksik pemberian produk KSM secara subkronis pada fungsi ginjal tikus betina galur SD?
2. Bagaimana hubungan dosis dan efek toksik pemberian produk KSM secara subkronis terhadap tikus betina galur SD?
3. Bagaimana sifat efek toksik pemberian produk KSM secara subkronis terhadap tikus betina galur SD?
C. Tujuan Penelitian
Tujuan penelitian ini adalah:
1. Mengetahui wujud efek toksik pemberian produk KSM secara subkronis pada fungsi ginjal tikus betina galur SD.
2. Mengetahui hubungan dosis dan efek toksik pemberian produk KSM secara subkronis terhadap fungsi ginjal tikus betina galur SD.
3. Mengetahui sifat efek toksik pemberian produk KSM secara subkronis terhadap tikus betina galur SD.
D. Pentingnya Penelitian Diusulkan
Mengetahui potensi ketoksikan dari pemberian produk KSM pada fungsi ginjal tikus betina galur SD dari dosis yang telah ditentukan sehingga dapat diperkirakan bagaimana efeknya apabila sediaan diberikan pada manusia.
E. Tinjauan Pustaka
1. Keladi Tikus (Typhonium flagelliforme (Lodd.) Blume)
Tanaman keladi tikus berasal dari kerajaan Plantae, divisi Tacheophyta, kelas
Liliopsida, bangsa Alismatales, suku Araceae, marga Typhonium, dan jenis
Typonium flagelliforme (Lodd.) Blume (Anonim, 2013).
Keladi tikus adalah tanaman herbal yang dapat tumbuh sampai setinggi 30 cm. Tanaman ini memiliki umbi berwarna keputihan berbentuk bujursangkar, dengan daun berbentuk segitiga, agak melebar di bagian samping, membulat di bagian ujung dan menyambung pada batang berwarna agak kekuningan (Ridley, 1967; Hsuan et al., 1998).
Skrining fitokimia membuktikan bahwa keladi tikus mengandung alkaloid, flavonoid, terpenoid, dan steroid (Nobakht et al., 2010). Senyawa lain yang terkandung antara lain ester asam lemak jenuh pada asam linoleat, asam heksadekanoat, asam oktadekanoat, 9-asam oktadekenoat dan 9,12-asam oktadekadienoat (Choo et al., 2001). Selain itu, tanaman ini juga mengandung enzim interseluler dan ekstraseluler seperti peroksidase, tirosinase, reduktase, azo reduktase, dan riboflavin reduktase (Kagalkar et al., 2010).
Tanaman keladi tikus merupakan tanaman obat tradisional yang memiliki berbagai khasiat untuk menyembuhkan berbagai penyakit seperti luka, udem, penyakit yang berhubungan dengan paru-paru, serta perdarahan (Nobakht et al., 2010). Penelitian oleh Lai et al. pada tahun 2008 membuktikan bahwa tanaman ini memiliki aktivitas antikanker terhadap sel kanker paru manusia secara in vitro. Penelitian lain oleh Choo et al. pada tahun 2001 juga membuktikan aktivitas sitotoksik dari tanaman ini terhadap sel leukimia. Aktivitas farmakologi lain dari tanaman ini yakni melegakan batuk, menghilangkan dahak, sedatif, antiasma,
antiinflamasi, dan analgetik (Zhong et al., 2001). Penelitian terbaru tahun 2015 yang dilakukan Nurrochmad et al. membuktikan bahwa tanaman keladi tikus memiliki aktivitas imunomodulator dimana dapat meningkatkan proliferasi limfosit, aktivitas fagositosis makrofag, profil sel T CD8+, dan meningkatkan level sitokin.
Senyawa dapat dikatakan toksik apabila memiliki LC50<1000 ppm. Ekstrak heksan dari keladi tikus terbukti toksik ringan dengan metode Brine Shrimp Lethality Test (BSLT) yang memiliki LC50 sebesar 762,08 ppm (Sianipar et al., 2013).
2. Sirih Merah (Piper crocatum Ruiz & Pav.)
Tanaman sirih merah berasal dari kerajaan Plantae, divisi Magnoliophyta, kelas Magnoliopsida, bangsa Piperales, suku Piperaceae, marga Piper, dan jenis
Piper crocatum Ruiz & Pav. (Backer, 1963).
Tanaman ini telah lama digunakan secara empiris untuk mengobati berbagai penyakit seperti diabetes mellitus, hemorhoid, peningkatan kadar asam urat, kanker, hepatitis, hipertensi, dan gartritis (Sudewo, 2007; Manoi, 2007). Efektivitas tanaman ini dalam menghambat proliferasi sel kanker payudara
(T47D) manusia telah terbukti dalam penelitian yang dilakukan oleh Wicaksono
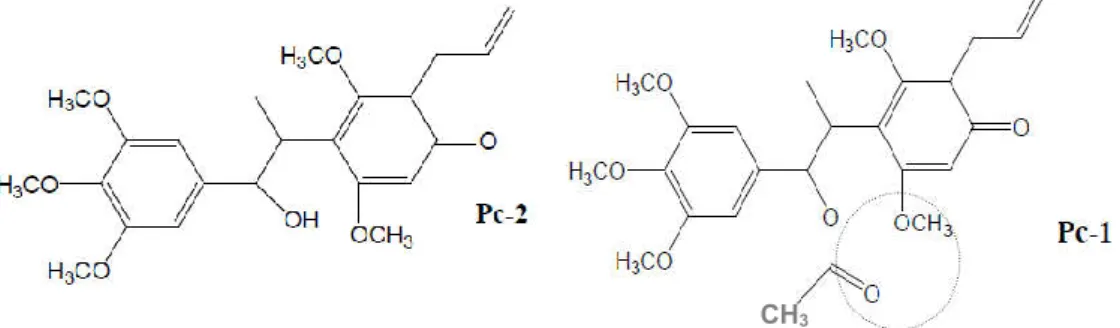
et al. pada tahun 2009. Sirih merah juga memiliki khasiat antiseptik dan antibakteri karena mengandung flavonoid, alkaloid, tanin, dan minyak atsiri (Safihtri & Fahma, 2008). Sementara skrining fitokimia yang dilakukan oleh Lister et al. pada tahun 2014 menunjukkan adanya alkaloid, flavonoid, saponin, triterpenoid, dan tanin dalam ekstrak metanolik sirih merah. Pada penelitian terdahulu oleh Paula Maria Kustiawan tahun 2012, telah diketahui bahwa daun sirih merah memiliki efek imunomodulator terhadap tikus dengan senyawa yang bertanggung jawab di dalamnya adalah senyawa neolignan yakni 2-allyl-4-(1'-hydroxy-1'-(3",4",5"-trimethoxyphenyl)propan-2'-yl)-dimethoxycyclohexa 3,5-dienone dan 2-allyl-4-(1'-acetyl-1'-(3",4",5"-trimethoxyphenyl)propan-2'-yl)-3,5-dimethoxycyclohexa-3,5-dienone yang disebut krokatidin dan deasetil krokatidin. Kedua senyawa ini terbukti dapat meningkatkan fagositosis makrofag dan produksi nitrit oksida (Hartini et al., 2014).
Pengujian toksisitas akut rebusan daun sirih merah menunjukkan selama 24 jam pertama sampai 7 hari masa percobaan tidak ada tikus yang mati untuk semua dosis yang diujikan. Maka dapat dikatakan rebusan daun sirih merah tidak bersifat
Gambar 3. Senyawa Krokatidin (kiri) dan Deasetil Krokatidin (kanan) (Kustiawan, 2012)
toksis (Safithri et al., 2012). Namun pada uji toksisitas dengan metode BSLT, nilai LC50 rebusan daun sirih merah sebesar 544,82 ppm. Karenanya, rebusan daun sirih merah dapat dikategorikan toksik sedang atau toksik menengah menurut skala toksisitas Hodge dan Sterner (Safithri et al., 2012). Selain menunjukkan toksisitas, nilai tersebut juga menunjukkan bahwa rebusan daun sirih merah memiliki aktivitas biologis seperti antibakteri, antidiabetes, antikanker, dan lain-lain (Meyer et al., 1982).
3. Meniran (Phyllanthus niruri L.)
Tanaman meniran berasal dari kerajaan Plantae, divisi Magnoliophyta, kelas
Magnoliopsida, subkelas Rosidae, bangsa Euphorbiales, suku Euphorbiaceae, marga Phyllanthus, dan jenis Phyllanthus niruri auct. non L. (Anonim, 2010).
Herba meniran adalah tanaman ramuan yang tegak, kecil, dan tumbuh tahunan dengan tinggi 30 40 cm. Tanaman ini merupakan tanaman asli dari hutan Amazon dan daerah tropis lainnya seperti Asia
Gambar 4 Meniran (Phyllanthus niruri L.)
Gambar 5. Senyawa Astragalin (Cho
Tenggara, India Selatan, dan Cina (Girach et al., 1994).
Tanaman ini tersebar secara luas di dunia dan sudah sejak lama digunakan sebagai terapi yang efektif untuk mengobati batu empedu dan batu ginjal. Di Malaysia, tanaman meniran digunakan sebagai diuretik, tonik untuk wanita pasca keguguran atau melahirkan, dan untuk menangani masalah ginjal (Dharmaraj et al., 2006).
Zat-zat yang terkandung dalam tanaman ini antara lain lignan, tanin, alkaloid, flavonoid, asam ftalat, asam galat, dan asam repandusinat (Anonim, 2003; Balawant et al., 1986; Joao et al., 1998; Suharmi & Ustariana, 2000; Williams, 2001). Pemberian ekstrak meniran dapat meningkatkan respon imun nonspesifik dan spesifik, baik humoral maupun seluler. Efek terhadap respon imun nonspesifik berupa peningkatan fagositosis makrofag, kemotaksis neutrofil, sitotoksisitas sel NK, dan hemolisis komplemen. Terhadap imunitas humoral, meniran dapat meningkatkan produksi imunoglobulin M dan imunoglobulin G (IgM dan IgG). Sementara terhadap imunitas seluler, meniran dapat meningkatkan
aktivitas limfosit T, limfosit B, sekr et al.,
1992). Astragalin merupakan senyawa flavonoid yang diketahui memiliki kemampuan untuk mengatur respon imun pada manusia dengan meningkatkan fagositosis, meningkatkan jumlah makrofag, dan memacu sintesis antibodi (Gan, 1998).
Meniran merupakan salah satu tanaman yang memiliki aktivitas imunostimulator yang akan meningkatkan sistem imun baik pada hewan percobaan maupun pada manusia (Simanjuntak, 1993). Dilihat dari segi
toksisitasnya, ekstrak etanol meniran yang diberikan selama 90 hari tidak bersifat toksik terhadap fungsi hati dilihat dari parameter SGPT, SGOT dan histopatologi organ hati (Sujono et al., 2015).
4. Toksikologi
a. Definisi Toksikologi
Secara sederhana toksikologi didefinisikan sebagai kajian tentang hakikat dan mekanisme efek toksik berbagai bahan terhadap makhluk hidup dan sistem biologik lainnya (Lu, 2010). Pada dasarnya, toksikologi berkenaan dengan sifat dan mekanisme luka toksik dan evaluasi kualitatif maupun kuantitatif spektrum perubahan biologis, yang ditimbulkan oleh pemejanan yang disengaja atau tak disengaja dari zat toksik racun (Donatus, 2005). Secara lebih luas toksikologi juga dapat didefinisikan sebagai studi mengenai deteksi, kejadian, sifat, efek, dan regulasi zat beracun (Hodgson, 1932). Sedangkan definisi toksisitas adalah kapasitas suatu zat kimia/ beracun (xenobiotik) untuk dapat menimbulkan efek toksik tertentu pada makhluk hidup (Priyanto, 2009).
b. Asas Umum Toksikologi
Ketoksikan suatu senyawa ditentukan dari keberadaan (kadar dan lama tinggal) senyawa itu atau metabolitnya di tempat aksi dan keefektifan antaraksinya (mekanisme aksi). Berdasarkan alur peristiwa timbulnya efek toksik, maka ada empat asas utama dalam toksikologi. Empat asas tersebut meliputi kondisi pemejanan dan kondisi makhluk hidup, mekanisme aksi, wujud dan sifat efek toksik atau pengaruh berbahaya racun (Donatus, 2005).
1). Kondisi efek toksik
Kondisi efek toksik menentukan keberadaan zat racun di dalam tubuh yang terdiri dari kondisi pemejanan dan kondisi makhluk hidup. Dengan kata lain, kondisi efek toksik mencakup berbagai faktor atau keadaan yang mempengaruhi efektivitas absorpsi dan distribusi suatu zat dalam tubuh. Kondisi pemejanan adalah semua faktor yang mempengaruhi keberadaan racun di tempat aksi tertentu di dalam tubuh, yang berkaitan dengan pemejanannya pada makhluk hidup. Kondisi pemejanan meliputi jenis, jalur, lama, kekerapan, saat dan takaran pemejanan (Donatus, 2005; Priyanto, 2009).
a). Jenis pemejanan. Jenis pemejanan dapat dibagi berdasarkan waktu dan peristiwa. Berdasarkan waktu, jenis pemejanan terdiri dari 2 macam yakni akut dan kronis. Pemejanan akut merupakan pemejanan tunggal dimana sejumlah racun tertentu masuk ke dalam tubuh makhluk hidup. Pemejanan kronis merupakan pemejanan racun berulang kali sehingga menyebabkan efek toksik yang kumulatif. Berdasarkan peristiwa, jenis pemejanan dapat dibagi menjadi pemejanan disengaja dan tidak disengaja.
b). Jalur pemejanan. Jalur pemejanan memegang peranan penting dalam menentukan ketersediaan senyawa toksik ataupun metabolitnya di suatu tempat aksi.
c). Lama dan kekerapan pemejanan. Lama pemejanan racun adalah batas kurun waktu pemejanan suatu racun terhadap makhluk hidup tertentu. Kekerapan pemejanan adalah batas pemejanan racun terhadap makhluk
hidup tiap satuan waktu, dengan takaran atau dosis serta melalui jalur pemejanan tertentu.
d). Saat dan takaran pemejanan. Saat pemejanan ialah waktu yang menunjukkan kapan senyawa toksik dipejankan. Saat pemejanan merupakan salah satu faktor penting yang mempengaruhi respon makhluk hidup terhadap ketoksikan suatu zat toksik. Selain itu, ketersediaan zat toksik di tempat aksi tertentu juga dipengaruhi besar takaran atau dosis zat toksik yang masuk. Semakin besar takaran pemejanan maka semakin besar pula kadar yang ada di tempat aksi.
(Donatus, 2005) Kondisi makhluk hidup mencakup keadaan fisiologi dan patologi yang mempengaruhi ketersediaan racun di sel sasaran. Terdapat dua jenis kondisi makhluk hidup yakni kondisi normal dan tidak normal. Kondisi normal atau sering dikenal sebagai keadaan fisiologi memiliki banyak kaitan dengan efektivitas antaraksi zat toksik dengan sel sasaran serta ketersediaan racun di sel sasaran. Keadaan fisiologi meliputi berat badan, umur, suhu tubuh, kecepatan pengosongan lambung, kecepatan alir darah, status gizi, kehamilan, jenis kelamin, genetika, ritme sirkadian dan diurnal. Kondisi tidak normal sering disebut keadaan patologi. Keadaan patologi yang penting dan dapat mempengaruhi ketersediaan racun di tempat aksi antara lain penyakit saluran cerna, kardiovaskular, hati, dan ginjal (Donatus, 2005). Kedua kondisi tersebut, baik kondisi pemejanan maupun kondisi makhluk hidup, dapat
mempengaruhi ketersediaan biologi zat kimia di sel sasaran sehingga dapat menentukan efeknya pula (Priyanto, 2009).
2). Mekanisme efek toksik
Mekanisme aksi toksik dapat digolongkan menjadi 3 yaitu mekanisme berdasarkan sifat dan tempat kejadian awal (fenomena patologi), mekanisme berdasarkan sifat antaraksi antara racun dan tempat aksinya (toksikodinamik), dan mekanisme berdasarkan risiko penumpukan racun dalam gudang penyimpanan tubuh (sekuestrasi fisik) (Ariens & Simonis, 1982; Glaister, 1986; Donatus, 2005).
a). Mekanisme aksi toksik berdasarkan sifat dan tempat kejadian awal.Dapat dibagi menjadi dua, yaitu mekanisme luka intrasel dan mekanisme luka ekstrasel. Mekanisme luka intrasel atau mekanisme primer adalah luka sel yang diawali oleh aksi langsung zat beracun atau metabolitnya pada tempat aksi tertentu di tempat sel sasaran. Sebaliknya mekanisme luka ekstrasel terjadi secara tidak langsung. Artinya zat beracun pada awalnya beraksi di lingkungan luar sel yang berakibat terjadinya luka di dalam sel (Donatus, 2005; Sulistyowati, 2008).
b). Mekanisme aksi toksik berdasarkan sifat antaraksi. Digolongkan menjadi 2 yaitu aksi toksik yang didasarkan atas antaraksi yang terbalikkan dan yang tak terbalikkan. Antaraksi yang terbalikkan terjadi antara molekul racun dan tempat aksi yang khas seperti reseptor neurotransmitter, tempat aktif enzim, dan lain-lain. Sedangkan antaraksi yang tak terbalikkan terjadi dengan melibatkan pembentukan ikatan kovalen yang menghasilkan luka
kimia dan selanjutnya efek toksik. Ciri khas reaksi tak terbalikkan adalah terjadinya penumpukan efek toksik (Donatus, 2005).
c). Mekanisme aksi toksik berdasarkan risiko penumpukan. Peristiwa penumpukan seringkali relatif tidak membahayakan, karena dalam gudang penyimpanan senyawa bersifat tak aktif. Namun secara perlahan senyawa akan terlepas ke sirkulasi dan meningkatkan kadarnya dalam cairan tubuh. Jika kadar melebihi KTM (kadar toksik minimum) maka akan menimbulkan efek toksik yang tidak diinginkan (Donatus, 2005).
3). Wujud efek toksik
Wujud efek toksik suatu racun dapat berwujud perubahan biokimia, fisiologi (fungsional), dan struktural yang memiliki sifat khas yakni terbalikkan atau tak terbalikkan (Donatus, 2005; Priyanto, 2009).
a). Respon dan perubahan biokimia. Misalnya pengurangan aktivitas transpor elektron di mitokondria, sintesis protein, gangguansistem hormonal, dan sebagainya (Priyanto, 2009). Respon tersebut pada awalnya mungkin bersifat adaptif, namun dapat berlanjut menjadi perubahan biokimia yang bersifat patologis. Perubahan biokimia biasanya bersifat terbalikkan yang artinya apabila pemejanan terhadap makhluk hidup dihentikan, maka ketoksikan dapat segera hilang. Jenis efek toksik yang terjadi antara lain penghambatan respirasi seluler, perubahan keseimbangan cairan dan elektrolit, dan gangguan pasok energi (Donatus, 2005).
b). Respon dan perubahan fisiologi (fungsional). Interaksi zat toksik dan reseptor dapat mempengaruhi fungsi organ-organ tertentu. Perubahan
fungsional dapat terjadi dari yang ringan seperti efek sedasi sampai yang berat seperti aritmia jantung. Pada umumnya perubahan fungsional bersifat terbalikkan. Perubahan biokimia maupun perubahan fungsional seringkali merupakan tahap awal terjadinya perubahan struktural. Jenis efek toksik yang terjadi antara lain anoksia, gangguan pernapasan, gangguan sistem saraf pusat, hipertensi atau hipotensi, hiperglikemi atau hipoglikemi, perubahan keseimbangan cairan dan elektrolit, perubahan kontraksi atau relaksasi otot, dan hipertermia atau hipotermia (Loomis, 1978; Timbrell, 1989; Timbrell, 2000; Donatus, 2005; Priyanto, 2009).
c). Respon histopatologi dan perubahan struktural. Racun dapat menimbulkan luka seluler melalui aksi langsung pada sel sasaran atau tak langsung pada lingkungan ekstrasel menuju ke perubahan morfologi yang pada akhirnya menjadi kerusakan struktural. Akibat kerusakan struktural ini, terjadilah respon histopatologi yang meliputi degenerasi, proliferasi, dan inflamasi atau perbaikan. Respon histopatologi tersebut mendasari berbagai perubahan morfologi atau struktural dalam berbagai wujud seperti nekrosis, karsinogenesis, dan sebagainya. Degenerasi dan proliferasi merupakan respon intrasel, sementara inflamasi merupakan respon ekstrasel. Jenis efek toksik yang terjadi antara lain perlemakan sel yang bersifat terbalikkan, nekrosis sel, karsinogenesis, mutagenesis, dan teratogenesis yang bersifat tidak terbalikkan (Donatus, 2005; Priyanto, 2009).
4). Sifat efek toksik
Sifat efek toksik suatu racun dapat dibedakan menjadi terbalikkan (reversible) dan tak terbalikkan (irreversible) (Priyanto, 2009). Ciri dari efek toksik yang terbalikkan adalah apabila kadar racun yang ada dalam tempat aksi maka reseptor akan kembali kepada keadaan semula, efek toksik yang ditumbulkan akan segera kembali kepada kondisi normal (Sulistyowati, 2008). Ciri dari efek toksik yang tak terbalikkan yaitu kerusakan yang terjadi sifatnya menetap, pemejanan berikutnya akan menimbulkan kerusakan yang sifatnya sama sehingga memungkinkan terjadinya penumpukan efek toksik (Priyanto, 2009).
c. Uji Toksikologi
Uji toksisitas merupakan salah satu uji pra klinik yang dilakukan pada hewan uji untuk tes keamanan suatu obat baru yang akan dikembangkan. Uji toksisitas mengungkapkan serangkaian efek akibat pemejanan zat toksik pada berbagai peringkat dosis dengan waktu pemberian bervariasi serta menunjukkan organ sasaran, sistem yang terpengaruh atau toksisitas khusus yang muncul (Lu, 2010).
Tujuan uji toksisitas secara umum adalah untuk menentukan dosis suatu sediaan uji yang dapat menimbulkan kematian atau gejala toksik pada organ atau jaringan, mengidentifikasi hubungan kausatif antara dosis yang diberikan dengan terjadinya perubahan fisiologis, dan morfologis suatu organisme, serta melakukan monitoring terkait variasi hewan uji dengan responnya terhadap sediaan uji (Donatus, 2005).
Uji toksisitas dibagi menjadi uji toksisitas tak khas dan khas. Uji toksisitas tak khas adalah uji toksikologi yang dirancang untuk mengevaluasi keseluruhan atau spektrum efek toksik suatu senyawa pada aneka ragam jenis hewan uji. Termasuk uji toksisitas tak khas adalah uji ketoksikan akut, subkronis, dan kronis. Uji toksisitas khas ialah uji toksikologi yang bertujuan untuk mengevaluasi secara rinci efek yang khas dari suatu senyawa pada aneka ragam jenis hewan uji. Termasuk dalam uji tosksitas khas adalah uji potensiasi, kekarsinogenikan, kemutagenikan, keterarogenikan, reproduksi, kulit dan mata, dan perilaku (Loomis, 1978).
5. Uji Toksisitas Subkronis
Uji toksisitas subkronis sering dikenal sebagai uji toksisitas subakut ialah uji ketoksikan suatu senyawa yang diberikan dengan dosis berulang pada hewan uji tertentu, selama kurang dari tiga bulan. Uji ini ditujukan untuk mengungkap spektrum efek toksik senyawa uji, serta untuk memperlihatkan apakah ada keterkaitan antara spektrum efek toksik dengan takaran dosis (Donatus, 2005). Menurut Loomis (1978), tujuan dari uji toksisitas subkronis adalah mengevaluasi dan menggolongkan secara umum segala efek senyawa apabila senyawa itu diberikan berulang-ulang, biasanya sekali sehari selama masa waktu tiga sampai empat bulan untuk memberi informasi tambahan yang dapat digunakan dalam merancang uji toksisitas kronis.
Pada dasarnya, pemilihan hewan uji pada uji ketoksikan ini yakni dipilih yang peka dan memiliki pola metabolisme terhadap senyawa uji yang semirip mungkin dengan manusia. Jumlah hewan uji yang digunakan paling tidak 10 ekor untuk
masing-masing jenis kelamin dalam setiap kelompok takaran dosis yang diberikan. Takaran dosis diberikan dalam bentuk peringkat dosis dimana satu kelompok harus menerima dosis toksik yang dapat membunuh beberapa hewan uji atau yang memperlihatkan gejala toksik yang nyata. Sedangkan kelompok yang lain harus menerima takaran dosis yang sama sekali tidak menimbulkan efek atau gejala toksik (Donatus, 2005).
Uji toksisitas subkronis menyangkut penerapan teknik analitis untuk menentukan efek pada kimia darah, sel-sel darah, kimia air kencing, dan fungsi organ tertentu. Pemeriksaan rutin wajib dilakukan baik pada kelompok kontrol maupun kelompok perlakuan untuk melihat adanya hubungan antara pemejanan senyawa beserta pengaruh dosis dengan fungsi organ (Ecobichon, 1997).
Hasil uji ketoksikansubkronis ini selanjutnya dapat digunakan untuk merancang uji ketoksikan kronis sebagai penelitian lebih lanjut dan lebih lama (Donatus, 2005; Loomis, 1978; Anonim, 1978).
Dalam penelitian ini, pedoman yang digunakan yaitu Peraturan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia Nomor 7 Tahun 2014 Tentang Pedoman Uji Toksisitas Non Klinik Secara In Vivoyang juga mengacu pada OECD 408 Repeated Dose 90-day Oral Toxicity Study in Rodents. Pengamatan yangdilakukan dalam uji ketoksikan subkronis meliputi perubahan berat badan yang diperiksa paling tidak 7 hari sekali, asupan makanan dan minuman untuk masing-masing hewan atau kelompok hewan uji paling tidak 7 hari sekali, gejala-gejala klinis umum yang diamati setiap hari, pemeriksaan hematologi paling tidak diperiksa dua kali, yaitu ada awal dan akhir uji coba, pemeriksaan kima darah
yang dilakukan paling tidak sama dengan pemeriksaan hematologi, pemeriksaan urin paling tidak sekali, pemeriksaan histopatologi organ pada hewan yang mati pada masa pengujiandan pada seluruh hewan pada akhir uji coba(Anonim, 1998; Loomis, 1978; Donatus, 2005).
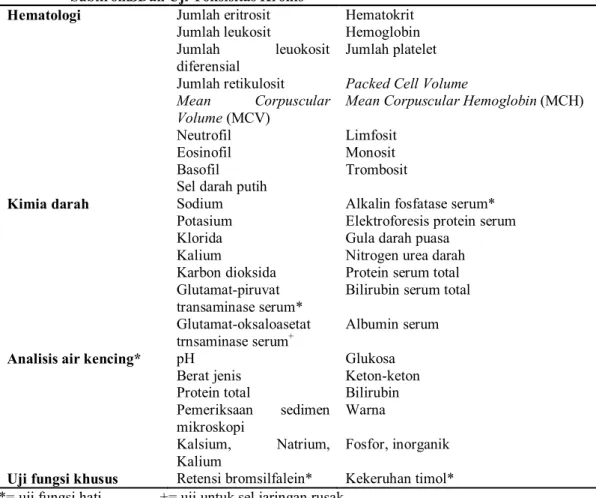
Ringkasan tipe analitis dan uji fungsional yang biasanya diamati dalam uji toksisitas subkronis dapat dilihat pada Tabel 1.
*= uji fungsi hati += uji untuk sel jaringan rusak
(Loomis, 1978; Ecobichon, 1997)
6. Ginjal
Ginjal merupakan organ yang berfungsi untuk menyingkirkan buangan metabolisme normal dan mengeksresi xenobiotik dan metabolitnya. Ginjal
Tabel I. Uji Analitis dan Uji Fungsional yang Digunakandalam Uji Toksisitas SubkroniSDan Uji Toksisitas Kronis
Hematologi Jumlah eritrosit Hematokrit Jumlah leukosit Hemoglobin Jumlah leuokosit
diferensial
Jumlah platelet Jumlah retikulosit Packed Cell Volume
Mean Corpuscular
Volume (MCV)
Mean Corpuscular Hemoglobin (MCH) Neutrofil Limfosit
Eosinofil Monosit
Basofil Trombosit
Sel darah putih
Kimia darah Sodium Alkalin fosfatase serum*
Potasium Elektroforesis protein serum Klorida Gula darah puasa
Kalium Nitrogen urea darah Karbon dioksida Protein serum total Glutamat-piruvat
transaminase serum*
Bilirubin serum total Glutamat-oksaloasetat
trnsaminase serum+
Albumin serum
Analisis air kencing* pH Glukosa
Berat jenis Keton-keton Protein total Bilirubin Pemeriksaan sedimen mikroskopi Warna Kalsium, Natrium, Kalium Fosfor, inorganik Uji fungsi khusus Retensi bromsilfalein* Kekeruhan timol*
menjalankan fungsinya dengan melakukan filtrasi plasma dalam jumlah besar lewat kapiler glomerulus, tubulus, dan dilanjutkan dengan reabsorpsi senyawa-senyawa yang masih diperlukan tubuh ke dalam darah. Senyawa tersebut antara lain glukosa, asam amino, air dalam jumlah yang cukup, serta ion-ion. Dalam proses tersebut, ginjal mengekskresi senyawa yang merupakan produk akhir metabolisme dan tidak dibutuhkan lagi oleh sel tubuh seperti urea, asam urat, ion dan air yang berlebih dari tubuh (Guyton & Hall, 2016). Ekskresi dari ginjal dipengaruhi oleh produksi urin. Urin adalah jalur utama ekskresi sebagian besar senyawa toksik dari dalam tubuh. Akibatnya ginjal memiliki volume aliran darah yang tinggi, mengkonsentrasikan senyawa toksik pada filtrat yang menyebabkan ginjal menjadi sasaran utama efek toksik (Lu, 2010). Dalam penelitian yang dirancang khusus untuk nefrotoksisitas, biasanya digunakan hewan yaitu anjing, kelinci, dan tikus.
Manifestasi klinis dari penyakit ginjal dapat dibagi berdasarkan letak kerusakannya yaitu penyakit yang disebabkan gangguan glomerulus dan penyakit yang disebabkan gangguan pada ginjal (Kumar et al., 2013).
a. Produksi Urin
Urin merupakan cairan biologis yang dikeluarkan oleh tubuh makhluk hidup untuk mengekskresikan sisa-sisa metabolisme. Urin pada tikus dan anjing biasanya bersifat asam, sementara pada primata dan babi biasanya bersifat basa. Urin tikus banyak mengandung protein yang jumlahnya bervariasi tergantung jenis kelamin dan umur dari tikus tersebut (Paget, 1970).
Produksi urin dimulai dengan filtrasi pada glomerulus. Pada manusia, kira-kira 180 mL filtrat terbentuk setiap hari. Namun hanya 500-2500 mL urin diekskresikan, sehingga 90% air yang tersaring diserap kembali. Reabsorpsi air terjadi pada tubulus proksimal, lengkung Henle, dan tubulus distal. Besarnya pembuangan air dari tubulus bergantung pada aktivitas hormon antidiuretik (ADH). ADH mengurangi volume urin dengan meningkatkan permeabilitas struktur ADH terhadap air (Lu, 2010).
b. Analisis Urin
Parameter urin yang umum digunakan antara lain warna, pH, berat jenis, protein total, glukosa, keton-keton, bilirubin, sedimen mikroskopi, dan lain-lain (Loomis, 1978; Ecobichon, 1997). Namun, parameter yang harus diamati pada setiap pengujian menggunakan sampel urin antara lain warna, volume, dan pH yang diukur dengan pH meter (Paget, 1970).
Tabel II. Penyebab Non-patologis dan Patologis Abnormalitas terhadap Parameter Urin
Parameter Penyebab non-patologis Penyebab patologis pH Rendah: diet tinggi protein
Tinggi: diet rendah protein, setelah makan
Rendah: asidosis
Tinggi: asidosis tubular, UTI Berat jenis Rendah: polidipsi
Tinggi: intake air rendah
Rendah: DI, disfungsi tubular Tinggi: deplesi volume Bercak darah Menstruasi, trauma kateterisasi,
olahraga
Gangguan glomerular, gangguan tubular, Protein Proteinuria ortostatik, demam,
olahraga
Gangguan glomerular, gangguan tubular, UTI
Glukosa Renal glikosuria DM, Fanconi Syndrome
Keton Intake karbohidrat yang terbatas DM
Bilirubin Tidak ada Hepatitis, obstruksi empedu
Urobilinogen Rendah: terapi antibiotik sistemik Hepatitis, hemolisis intravaskular
Nitrit Tidak ada UTI
LE Demam UTI, glomerulonefritis,
inflamasi pelvis
c. Analisis Darah
Pengukuran kadar senyawa-senyawa khususnya urea dan kreatinin dalam darah sangat dibutuhkan untuk menilai kondisi ginjal. Senyawa-senyawa yang tergolong senyawa nitrogen non-protein ini merupakan merupakan produk akhir metabolisme protein dan harus dikeluarkan dari tubuh untuk menjaga keberlanjutan metabolisme protein normal dalam sel (Guyton & Hall, 2016). Kreatinin yang merupakan hasil akhir dari metabolisme kreatin dan urea yang merupakan hasil akhir dari metabolisme protein, secara normal difiltrasi dari plasma oleh ginjal dan hanya direabsorpsi dalam jumlah yang sedikit. Oleh karena itu kedua parameter ini sering dijadikan indikator untuk menggambarkan klirens ginjal (Evans, 2005).
1). Urea
Segala bentuk urea dalam tubuh disintesis dalam hati. Selama metabolisme asam amino, terjadi deaminasi yang melepaskan amonia. Dua molekul amonia yang bereaksi dengan karbondioksida akan menghasilkan urea. Setelah terbentuk, urea akan berdifusi dari sel-sel hati menuju aliran darah dan diekskresi ginjal (Guyton & Hall, 2016).
Konsentrasi urea dalam darah merupakan salah satu indikator terbaik untuk melihat fungsi ginjal pada manusia (Paget, 1970).Jika kadar urea dalam darah meningkat, maka menunjukkan kerusakan glomerulus. Namun kadar urea dalam darah juga dapat dipengaruhi oleh kurangnya zat makanan dan hepatotoksisitas yang merupakan efek umum beberapa toksikan (Lu, 2010).
Umumnya, kadar urea pada pria sedikit lebih tinggi dari pada wanita. Hal ini disebabkan karena pria memiliki lean body mass yang lebih besar. Kadar urea dalam darah dapat meningkat jika seseorang mengkonsumsi makanan yang mengandung banyak protein secara berkepanjangan (Widmann, 1983). 2). Kreatinin
Kreatinin adalah produk akhir dari metabolisme kreatin. Kreatin terutama disintesis hati, terdapat hampir pada semua otot rangka, dan terikat secara reversibel dengan fosfat dalam bentuk fosfokreatin sebagai senyawa penyimpan energi.Akan tetapi, sebagian kecil dari kreatin secara ireversibel berubah menjadi kreatin yang tidak berfungsi dan keberadaannya dalam darah hanya untuk diangkut ke ginjal serta dieskresi seluruhnya dalam urin melalui filtrasi glomerulus (Widmann, 1983; Lu, 2010). Meningkatnya kadar kreatinin dalam darah merupakan indikasi rusaknya fungsi ginjal. Selain itu, data kadar kreatinin dalam darah dan jumlahnya dalam urin dapat digunakan untuk memperkirakan laju filtrasi glomerulus (GFR) (Lu, 2010).
d. Histopatologi
Histopatologi adalah cabang ilmu patologi yang bertujuan untuk menemukan dan mendiagnosis penyakit dari pemeriksaan jaringan. Pemeriksaan tersebut terdiri dari pemeriksaan makroskopis jaringan dan seleksi sampel untuk pengamatan mikroskopis. Pada umumnya, diagnosis histopatologi dilakukan dari jaringan blok parafin yang diwarnai dengan hematoksilin-eosin (Underwood, 2000).
Respon histopatologi yang biasanya terjadi sebagai tanggapan atas adanya luka seluler antara lain degenerasi, prolifersi, dan inflamasi atau perbaikan.
1). Degenerasi
Degenerasi ditandai dengan perubahan yang regresif seperti pengecilan sel atau pengurangan jumlah organel. Proses ini mencakup berbagai respon morfologi yang berkisar dari homeostasis adaptif sampai perubahan tak terbalikkan seperti kematian sel. Perubahan regresif yang paling lazim dijumpai yakni atropi, akumulasi intrasel, dan nekrosis (Donatus, 2005). a). Atropi. Atropi adalah mengecilnya sel atau berkurangnya jumlah sel yang
dapat menyebabkan penyusutan organ atau jaringan yang terpengaruh. b). Akumulasi intrasel. Keadaan ini dapat mengganggu keseimbangan antara
kompartemen intrasel dan antarsel lingkungan sekitar. Ditunjukkan dengan terjadinya penumpukan berbagai macam bahan di sitoplasma atau organel-organel sel. Penumpukan intrasel yang paling banyak dijumpai antara lain penumpukan air, lemak, dan bermacam jenis inklusi (bahan-bahan granul atau padat).
c). Nekrosis. Nekrosis disebut juga kematian sel. Kematian sel dapat terjadi pada makhluk hidup sebagai respon degenerasi terhadap luka sel dan merupakan kerusakan yang biasanya terjadi. Keadaan ini merupakan hasil akhir dari berbagai macam mekanisme luka sel baik intrasel maupun ekstrasel seperti apoptosis, interaksi ireversibel, dan hipoksia-anoksia. Kerusakan sel jenis ini bersifat tak terbalikkan.
2). Proliferasi
Proliferasi merupakan salah satu respon sel terhadap luka kimia dengan cara meningkatkan pertumbuhan pada sembarang tingkat struktural, dari tingkat molekuler sampai seluler. Proliferasi dapat dibedakan menjadi beberapa macam.
a). Hipertropi. Merupakan respon proliferasi berupa pembesaran sel.
b). Hiperplasia. Merupakan peningkatan jumlah sel dalam jaringan atau organ tertentu secara mutlak.
c). Metaplasia. Merupakan proliferasi dimana salah satu jenis sel yang mengalami diferensiasi diganti dengan jenis lain sel yang mengalami diferensiasi.
d). Displasia. Merupakan proliferasi nirneoplastik yang paling kacau dimana juga terjadi hiperplasia, metaplasia, serta peningkatan aktivitas mitotik yang menghasilkan berlimpahnya sel dengan bentuk, ukuran, serta tingkat diferensiasi berpola struktural yang kacau.
e). Proliferasi nirneoplastik. Bentuk proliferasi terkendali yang meliputi regenerasi, hiperplasia, metaplasia, dan displasia.
f). Proliferasi neoplastik. Bentuk proliferasi sel yang ditandai dengan hilangnya sebagian atau keseluruhan respon terhadap kendali pertumbuhan normal.
3). Inflamasi dan perbaikan
Inflamasi merupakan proses yang dinamis dan luas. Sifat inflamasi tergantung dari tingkat dan lamanya luka. Proses inflamasi meliputi respon vaskular, neurologis, hormonal, dan seluler pada tempat luka. Inflamasi dapat dibagi menjadi 2 yaitu inflamasi akut dan kronis (Donatus, 2005).
Perbaikan juga merupakan proses yang dinamis yang terdiri dari regenerasi dan fibrosis. Inflamasi dan perbaikan sering terjadi secara bersamaan (Glaister, 1986; Donatus, 2005).
F. KETERANGAN EMPIRIS
Penelitian ini bersifat eksploratif untuk mengetahui gambaran toksisitas pemberian produk KSM secara berulang selama 90 hari berupa wujud efek toksik, hubungan dosis pemberian terhadap efek toksik, dan sifat efek toksik pada fungsi ginjal dari tikus betina galur SD.