Uji NaF dilakukan untuk mengetahui keberadaan alofan dalam sampel tanah andisol. Dari hasil uji NaF diperoleh nilai pH 10,18 sehingga dapat disimpulkan bahwa pada sampel tanah andisol mengandung alofan yang memadai. Munir (1996) menyatakan bahwa kandungan alofan dalam tanah dapat diketahui dengan mengukur pH dari 1 gram tanah dalam 50 ml larutan NaF 1 M selama 2 menit dan apabila nilai pH lebih besar dari 9,4 menunjukkan bahwa terdapat kandungan alofan yang tinggi dalam tanah. NaF dapat memberikan reaksi yang cepat ketika ditambahkan ke dalam sampel alofan, yaitu F dapat bereaksi dengan Al dan memecah struktur sehingga akan melepaskan OH- (Parfit and Henmi, 1980). 2. Analisis Fourier Tranform Infra-Red (FT-IR)
Analisis FT-IR dilakukan bertujuan untuk mengetahui gugus fungsional utama di dalam struktur lempung dan andisol. Pengamatan sampel lempung dan andisol dilakukan pada bilangan gelombang antara 400 – 4000 cm-1 dengan menggunakan butiran pellet KBr. Hasil spektra FT-IR ditunjukkan pada Gambar 4 dan 5.
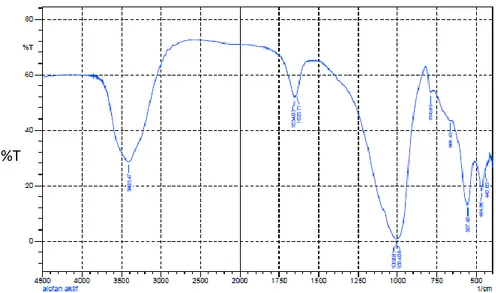
Gambar 4. Spektra FT-IR andisol %T
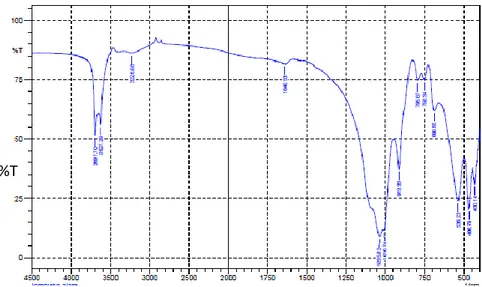
Gambar 5. Spektra FT-IR lempung
Data hasil analisis gugus fungsi lempung dan andisol dapat dilihat pada Tabel 1. Dari tabel tersebut dapat diamati perbandingan serapan bilangan gelombang pada sampel dengan hasil analisis dari penelitian yang lain.
Tabel 1. Data hasil analisis gugus fungsi lempung dan andisol
Gugus Fungsi
Bilangan gelombang (cm-1)
Pustaka Lempung Andisol
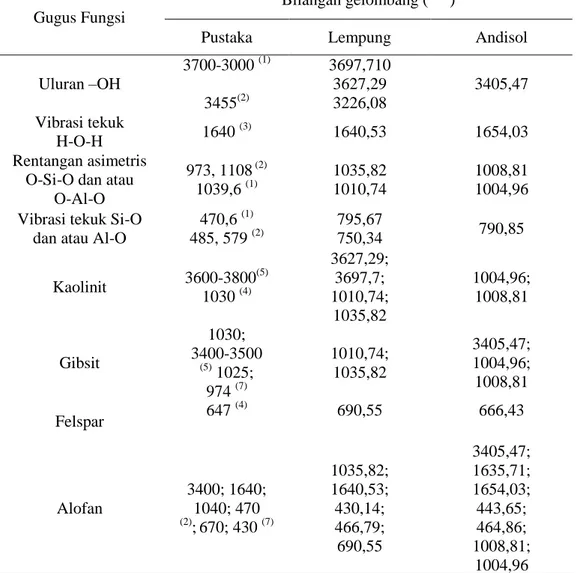
Uluran –OH 3700-3000 (1) 3455(2) 3697,710 3627,29 3226,08 3405,47 Vibrasi tekuk H-O-H 1640 (3) 1640,53 1654,03 Rentangan asimetris O-Si-O dan atau
O-Al-O 973, 1108 (2) 1039,6 (1) 1035,82 1010,74 1008,81 1004,96 Vibrasi tekuk Si-O
dan atau Al-O
470,6 (1) 485, 579 (2) 795,67 750,34 790,85 Kaolinit 3600-3800 (5) 1030 (4) 3627,29; 3697,7; 1010,74; 1035,82 1004,96; 1008,81 Gibsit 1030; 3400-3500 (5) 1025; 974 (7) 1010,74; 1035,82 3405,47; 1004,96; 1008,81 Felspar 647 (4) 690,55 666,43 Alofan 3400; 1640; 1040; 470 (2) ;670; 430 (7) 1035,82; 1640,53; 430,14; 466,79; 690,55 3405,47; 1635,71; 1654,03; 443,65; 464,86; 1008,81; 1004,96
Keterangan: (1): Wijaya dalam Wogo, dkk. (2013); (2): Devnita, dkk. (2005); (3): Permanasari,dkk. (2010), (4) Hemamalini et al., (2011); (5) Tan (1982); Plasvic et al., (1999); (7) Iyoda et al, (2011);
Serapan-serapan tersebut dapat disimpulkan bahwa dalam sampel tanah lempung maupun andisol terdapat kandungan alofan dengan ditandai adanya gugus-gugus Si-O atau Al-O, O-Si-O atau O-Al-O, dan –OH.
3. Analisis X-Ray Diffraction (XRD)
Analisis kualitatif XRD digunakan untuk menentukan jenis mineral yang terkandung dalam lempung dan andisol. Hasil analisis tersebut ditunjukkan pada Gambar 6.
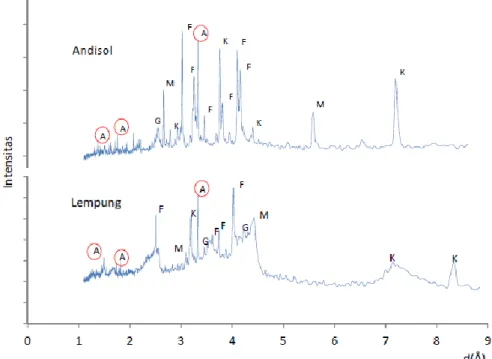
Gambar 6. Difraktogram XRD lempung dan andisol
Tabel 2. Hasil Analisis XRD tanah Lempung dan Andisol
d (Å)
Gugus Fungsi Pustaka Sampel Lempung Sampel Andisol
Alofan 3,3000; 2,2500; 1,8000; 1,4000(1) 3,3280; 1,8129 3,2868; 1,7412; 1,3581 Felspar 4,00-4,20; 6,30-6,45; 3,80-3,90; 3,73-3,75; 3,64-3,67;3,44-3,48; 3,00-3,25 (2) 3,2755; 3,2266; 3,5931; 3,7574; 3,4384; (3) 4,0260; 4,2201; 3,7400; 3,6120; 3,1987 4,0414; 3,7136; 3,7006; 6,4687; 3,2171; 3,1978; 2,9829 Gibsit 4,34; 4,83; 3,30 (2) 4,8500; 4,3600; 2,4500; 2,3800 (4) 3,4471; 2,5273; 3,4138 Kaolinit 7,10-7,20; 4,45-4,46; 4,35- 4,36; 4,17; 4,12; 3,84; 3,56-3,58 (2) 8,9059; 4,6513; 4,1447; 3,8126; 3,5100 (5) 8,3402; 7,1353; 7,0865; 3,7553; 3,8919; 4,3423 Monmorilonit 12,00-15,00; 5,90 (2) 15,00; 1,49; 2,53; 1,29; 4,05 (6) 2,5098; 1,4862 5,4808; 2,6191 Keterangan : (1)=JCPDS 38-0449, (2)=Tan (1982), (3)=JCPDS 70-1862, (4)=JCPDS 01-0264, (5)=JCPDS 72-2300, (6)=JCPDS 02-0014
Hasil analisis berdasarkan Gambar 3 dan Tabel 2 menunjukkan bahwa sampel lempung dan andisol yang akan digunakan dalam penelitian ini mengandung beberapa mineral yang dibuktikan dengan munculnya puncak-puncak difraksi pada d(Å) yang karakteristik. Mineral yang terkandung dalam penjerap tanah lempung dan tanah andisol, yaitu alofan, felspar, gibsit, kaolin dan monmorilonit. 4. Analisis Luas Permukaan
Luas permukaan merupakan faktor penting dalam proses adsorpsi karena semakin besar luas permukaan maka semakin besar pula kemampuan adsorpsinya. Luas permukaan dinyatakan dalam jumlah total luas permukaan sampel yang berbentuk serbuk dalam setiap massa sampel. Analisis yang digunakan untuk menentukan luas permukaan dilakukan dengan SAA.
Tabel 3. Data penentuan luas permukaan
Sampel Luas permukaan (m2/g)
Andisol 245,7900 (1)
Lempung 56,5410
Keterangan : (1) Sistha (2013)
Berdasarkan data pada Tabel 3 tersebut dapat dilihat bahwa luas permukan andisol lebih besar dengan perrbedaan secara signifikan. Luas permukaan inilah yang menyediakan luasan area pada permukaan lempung maupun andisol dalam proses adsorpsi terhadap ion logam kadmium (Cd) yang berlangsung.
5. Analisis Keasaman
Analisis keasaman dilakukan dengan menggunakan metode adsorpsi basa amonia, yaitu melalui pengukuran jumlah basa amonia yang bereaksi dengan gugus asam padatan, dimana jumlah basa amonia yang diadsorpsi oleh permukaan padatan adalah sebanding dengan jumlah asam pada permukaan padatan yang menyerap basa tersebut.
Tabel 4. Data penentuan keasaman
Sampel Keasamaan (mmol/g)
Andisol 2,352
Lempung 3,529
Berdasarkan data pada Tabel 4 tersebut dapat dilihat bahwa keasaman lempung lebih tinggi dibandingkan andisol. Hal tersebut menunjukkan bahwa permukaan lempung menyediakan situs aktif yang lebih banyak daripada permukaan andisol dimana situs aktif ini akan menjadi media dalam proses adsorpsi ion logam kadmium (Cd).
B. UjiKinerja Adsorben terhadap Ion Logam Kadmium (Cd) Aktivasi dilakukan pada tanah lempung dan andisol untuk meningkatkan karakter fisika kimia. Aktivasi dilakukan secara kimia hanya untuk tanah andisol yang mengandung alofan, yaitu dengan perendaman NaOH 3M selama 5 jam, karena aktivasi kimiawi menggunakan larutan basa mampu melarutkan pengotor yang dapat larut dalam basa yang berada dibagian luar kerangka dan yang menutupi pori-pori permukaan. Penambahan NaOH juga berfungsi untuk melarutkan pengotor-pengotor organik maupun anorganik yang mengisi rongga dan pori-pori pada tanah andisol sehingga pori-pori pada permukaannya menjadi terbuka. Dengan berkurangnya pengotor pada rongga-rongga tanah andisol maka permukaan padatannya menjadi bersih dan luas serta keasamannya juga meningkat. Hal ini sesuai dengan penelitian yang telah dilakukan oleh Husna (2012) yang mengalami peningkatan luas permukaan sebesar 22,661% dan keasaman sebesar 63,704% pada tanah andisol alam setelah diaktivasi dengan NaOH. Secara fisik, tanah andisol yang telah diaktivasi dengan NaOH mempunyai warna yang lebih terang dibandingkan tanah andisol tanpa aktivasi. Tanah andisol tanpa aktivasi berwarna coklat gelap, sedangkan setelah aktivasi warna coklat gelap memudar menjadi warna coklat terang.
Lempung yang digunakan dalam penelitian ini tidak dilakukan aktivasi secara kimia. Hal ini didasarkan pada penelitian sebelumnya yang telah dilakukan oleh Lihin, dkk. (2012) dimana lempung yang diaktivasi kimia dan lempung tanpa aktivasi kimia memiliki nilai kapasitas adsorpsi yang tidak berbeda signifikan. Kemampuan lempung ini dapat ditingkatkan dengan cara aktivasi fisik maupun kimia (Talaat et al., 2011). Oleh karena itu, pada penelitian ini lempung tidak dilakukan aktivasi secara kimia.
Tanah andisol dilakukan aktivasi secara kimia, selanjutnya dilakukan pembuatan variasi komposisi perbandingan lempung:tanah andisol (0:100, 20:80, 40:60, 50:50, 60:40, 80:20 dan 100:0). Masing-masing campuran tersebut selanjutnya dilakukan aktivasi secara fisika menggunakan variasi suhu kalsinasi, yaitu 100, 200, dan 4000C. Sama halnya dengan aktivasi kimia, aktivasi fisika ini juga berfungsi untuk melarutkan pengotor-pengotor organik maupun anorganik yang mengisi rongga dan pori-pori pada adsorben sehingga pori-pori pada permukaannya menjadi terbuka.
Proses adsorpsi dipengaruhi oleh beberapa faktor, diantaranya yaitu tingkat keasaman (pH), waktu kontak, ukuran partikel, dan suhu. Pada penelitian ini, faktor yang ingin diketahui pengaruhnya adalah komposisi penyusun adsorben, suhu kalsinasi adsorben, dan waktu kontak adsorpsi terhadap ion logam kadmium (Cd) dimana akan dibuktikan dengan nilai kapasitas adsorpsi atau % adsorpsi yang diperoleh.
Adsorben yang telah diaktivasi selanjutnya digunakan dalam proses adsorpsi terhadap larutan kadmium (Cd) 6 ppm dengan variasi waktu kontak 30, 60, dan 120 menit menggunakan metode batch. Hasil kurva standar untuk ion logam kadmium (Cd) dapat dilihat pada Lampiran 6. Adsorben dengan variasi komposisi lempung:tanah andisol, suhu kalsinasi, dan waktu kontak adsorpsi terbaik ditentukan dari nilai kapasitas adsorpsi atau % adsorpsi yang tertinggi. Data hasil adsorpsi yang diperoleh dapat dilihat pada lampiran 7-8. Berdasarkan data hasil adsorpsi tersebut dapat disimpulkan bahwa variasi adsorben terbaik diperoleh pada perbandingan lempung:tanah andisol 60:40 dengan suhu kalsinasi 200⁰C menggunakan waktu kontak adsorpsi60 menit.
Variasi komposisi adsorben terbaik diperoleh pada perbandingan lempung dan tanah andisol 60:40. Jika dilihat dari gugus aktif keduanya, lempung dan tanah andisol termasuk dalam kelompok mineral alumino silikat alam yang memiliki gugus aktif berupa Si-OH, Al-OH, dan –OH sehingga keduanya dapat menyediakan muatan elektronegatif pada permukaannya yang memungkinkan terjadinya pertukaran kation maupun proses adsorpsi ion logam kadmium (Cd). Sifat lempung yang lekat sewaktu basah membantu melekatnya tanah andisol pada lempung sehingga semakin banyak kandungan lempung dari pada tanah andisol pada perbandingan lempung dan tanah andisol tersebut menyebabkan daya adsorp optimal. Tingginya perbandingan komposisi lempung pada kondisi ini juga didukung dengan suhu kalsinasi yang hanya 200⁰C dimana lempung memiliki ketahanan terhadap panas dan kapasitas adsorpsi optimum pada suhu 100 ≤ T ≤ 200⁰C(Igbokwe, et al., 2011). Dari segi praktisnya, preparasi lempung lebih mudah dilakukan karena pada penelitian ini lempung yang digunakan tidak perlu diaktivasi secara kimia untuk meningkatkan kemampuan adsorpsinya sedangkan tanah andisol diaktivasi secara kimia. Selain itu, keberadaan lempung juga lebihmelimpah dibandingkan tanah andisol dimana tanah andisol merupakan bagiankecil yang terkandung dalam mineral lempung (Sajidu, et al., 2006).
Adsorben tanah lempung dan andisol mempunyai afinitas yang tinggi terhadap ion logam karena keduanya mempunyai gugus-gugus aktif Si-OH, Al-OH dan –Al-OH sehingga keduanya mampu menyediakan muatan elektronegatif pada permukaannya yang memungkinkan terjadinya pertukaran kation dalam proses adsorpsi ion logam kadmium (Cd) dalam larutan (Itou et al., 2009; Schulze, 2005). Kemampuan jerapan mineral silikat berasal dari banyaknya muatan negatif pada struktur mineral silikat. Muatan negatif tersebut akan dinetralkan dengan penjerapan ion terjerap bermuatan positif, misalnya kation logam berat (Visekruna et al., 2011). Berdasarkan data hasil adsorpsi pada lampiran di bawah ini menunjukkan bahwa kedua adsorben tanah lempung dan andisol keduanya mempunyai kemampuan menjerap ion logam dengan kapasitas adsorben yang berbeda.
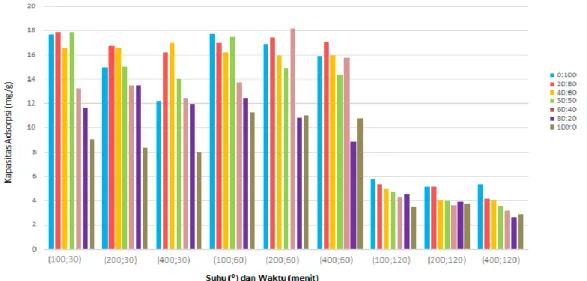
Gambar 7. Perbandingan Kapasitas Adsorpsi Berbagai Variasi Suhu Aktivasi dan Waktu Kontak terhadap Komposisi Adsorpsi
Penjerap dengan komposisi 100% tanah andisol (0:100) mempunyai kapasitas jerapan yang lebih besar dibandingkan penjerap tanah lempung 100% (100:0). Jumlah ion logam yang teradsorp semakin berkurang dengan meningkatnya prosentase penjerap lempung dalam komposisi penjerap campuran tanah lempung dan andisol. Hal ini memperlihatkan bahwa keberadaan tanah lempung dalam campuran adsorben kurang mendukung kemampuan penjerap dalam menjerap ion logam kadmium (Cd). Berkurangnya kemampuan adsorpsi dari campuran tanah lempung dan andisol ini dapat dijelaskan berdasarkan data luas permukaan maupun bilangan keasaman dari masing-masing penjerap.
Luas permukaan merupakan salah satu faktor yang menentukan dalam proses adsorpsi karena luas permukaan inilah yang menyediakan luasan area pada permukaan adsorben dalam proses adsorpsi terhadap ion logam kadmium (Cd). Sehingga semakin besar luas permukaan adsorben maka kapasitas adsorpsinya semakin besar pula. Tanah lempung mempunyai luas permukaan sebesar 245,7900 m2/gram, sedangkan tanah andisol mempunyai luas permukaan jauh lebih besar, yaitu 56,5410 m2/gram. Sanchez et al., (1999) telah membuktikan bahwa luas permukaan berpengaruh terhadap kapasitas adsorpsi. Hasil penelitiannya menjelaskan bahwa adsorben sepiolite dengan ukuran partikel kecil
mempunyai kapasits jerapan yang lebih baik dibanding dengan penjerap dengan ukuran partikel lebih besar. Ukuran partikel yang kecil mampu menyediakan bidang adsorpsi yang lebih besar dibanding partikel dengan ukuran yang lebih besar oleh karena itu interaksinya dengan ion logam lebih maksimal. Penelitian lain juga menjelaskan bahwa keberadaan material lain dalam campuran adsorben dengan alofan dapat meningkatkan kapasitas adsorpsinya atau justru menurunkan kapasitas adsorpsinya.
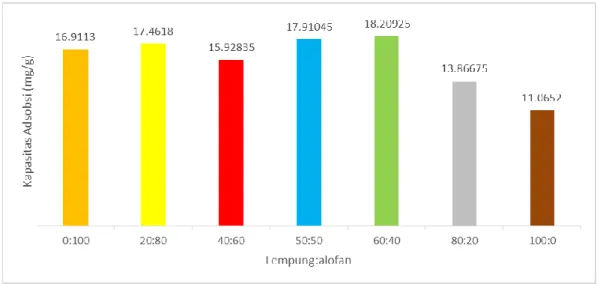
Efektivitas perbandingan komposisi lempung:tanah andisol pada kondisi terbaik tersebut terhadap ion logam kadmium (Cd) dapat dilihat pada Gambar 8.
Gambar 8. Perbandingan kapasitas adsorpsi adsorben terbaik dengan komposisi lempung:andisol 200 C dan waktu kontak 60 menit. Berdasarkan diagram pada Gambar 8 dapat ditunjukkan bahwa kapasitas adsorpsi komposisi lempung dan tanah andisol pada kondisi terbaik (60:40) sebesar 18,2092. Kemudian jika dibandingkan antara komposisi lempung:tanah andisol 0:100 dan 100:0 terdapat perbedaan yang cukup signifikan dengan kapasitas adsorpsi 16,9113 dan 11,0652. Hal ini membuktikan bahwa besarnya prosentase tanah andisol dalam campuran penjerap berpengaruh besar terhadap kapasitas jerapannya terhadap ion logam kadmium (Cd).
Pemanasan penjerap pada berbagai suhu aktivasi dilakukan untuk membersihkan pengotor organik dan anorganik sehingga permukaan rongga lebih bersih dan pori akan terbuka. Hal ini menyebabkan luas permukaan spesifik penjerap menjadi lebih besar sehingga meningkatkan kapasitas jerapan dalam
menyerap molekul adsorbat. Pemanasan pada campuran penjerap tanah lempung dan andisol juga dimaksudkan untuk membebaskan molekul air, baik air yang terikat secara fisik maupun yang terikat secara kimia dalam bentuk terhidrat (Hartopo, 2014).
Pembebasan molekul air yang terikat secara lemah (fisik) dapat dilakukan dengan pemanasan pada temperatur diatas titik didih air. Namun pada pembebasan molekul air terhidrat, diperlukan temperatur yang lebih tinggi (400 – 500°C) dan dikenal dengan istilah kalsinasi. Pada penelitian ini aktivasi penjerap dilakukan pada variasi suhu 100, 200 dan 400°C. Melalui aktivasi pada ketiga variasi suhu tersebut akan diketahui pengaruh perbedaan suhu terhadap kemampuan penjerap dalam menyerap ion logam kadmium (Cd).
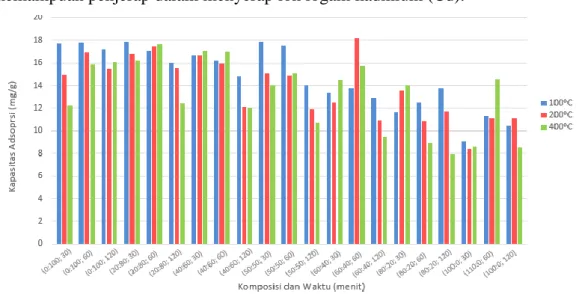
Gambar 9. Perbandingan Kapasitas Adsorpsi Berbagai Komposisi Adsorben dan Waktu Kontak terhadap Suhu Aktivasi
Berdasarkan Gambar 9, adsorben dengan suhu aktivasi 100°C dan 200°C mempunyai kapasitas adsorpsi yang relatif sama dengan sebagian besar variasi komposisi campuran adsorben. Kapasitas adsorpsi semakin turun dengan meningkatnya suhu aktivasi menjadi 400°C. Tingginya kapasitas adsorpsi pada variasi suhu aktivasi 100°C dan 200°C, dan semakin berkurangnya kapasitas adsorpsi pada variasi suhu aktivasi 400°C dapat dijelaskan berdasarkan luas permukaan spesifiknya. Peningkatan suhu aktivasi mampu membebaskan molekul air yang terperangkap dalam matrik tanah lempung dan andisol sehingga
meninggalkan struktur rongga berpori dan meningkatkan luas permukaan bidang adsorpsinya. Suhu aktivasi yang lebih tinggi dari pada suhu optimum menyebabkan rusaknya struktur adsorben dan menyebabkan penurunan luas permukaannya sehingga media jerapannya terbatas (Alemayehu et al., 2012).
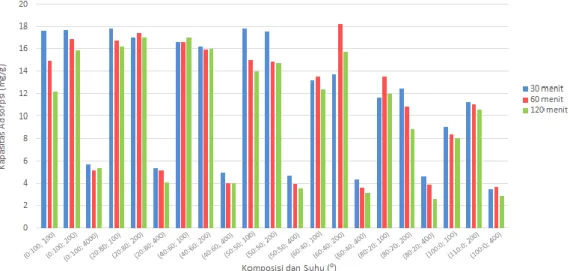
Gambar 10 menunjukkan bahwa pada perbandingan antara lempung dan tanah andisol 0:100 mengalami penurunan kapasitas adsorpsi dengan meningkatnya variasi suhu kalsinasi dan waktu kontak adsorpsi atau dengan kata lain nilai kapasitas adsorpsi yang terbaik diperoleh dengan suhu 200⁰C dan waktu 60 menit. Hal ini dapat disebabkan oleh terjadinya proses desorpsi ketika suhu ditingkatkan menjadi 400⁰C serta waktu kontak ditingkatkan menjadi 90 menit.
Gambar 10. Perbandingan kapasitas adsorpsi variasi komposisi lempung:tanah andisoldan suhu kalsinasi terhadap variasi waktu kontak.
Perbandingan antara lempung dan tanah andisol 0:100, 20:80, 40:60, 50:50, 60:40, 80:20 dan 100:0 pada suhu 200⁰C memiliki kapasitas adsorpsi yang meningkat dengan bertambahnya waktu kontak. Sedangkan ketika suhu kalsinasi ditingkatkan menjadi 400⁰C dan dengan bertambahnya waktu kontak, perbandingan lempung:andisol tersebut memiliki kapasitas adsorpsi yang semakin menurun. Hal ini dapat menunjukkan bahwa pada suhu 200⁰C, pengotor sudah hilang dan pori-pori pada permukaan lempung maupun tanah andisol sudah dapat terbuka sehingga menyediakan luasan area untuk terjadinya proses adsorpsi, sedangkan suhu yang lebih tinggi kemungkinan sudah melebihi batas ketahanan
suhu dari lempung tanah andisol sehingga mengakibatkan kurang optimalnya proses adsorpsi.
Disamping itu, waktu kontak juga sangat menentukan dalam proses adsorpsi. Perbandingan lempung:tanah andisol 0:100 dan 100:0 atau dengan kata lain komposisi ini hanya terdiri dari tanah andisol dan lempung saja memiliki waktu kontak optimum 60 menit. Selama 60 menit terjadi proses difusi dan penempelan ion logam kadmium (Cd) pada gugus aktif yang dimiliki tanah andisol maupun lempung. Akan tetapi, konsentrasi ion logam kadmium (Cd) akan mengalami penurunan ketika waktu kontaknya telah cukup. Ketika waktu kontak telah cukup atau bahkan berada pada titik jenuh, maka akan terjadi peristiwa desorpsi atau ion logam kadmium (Cd) tidak diterima lagi oleh permukaan adsorben melainkan akan dilepas kembali ke dalam larutan. Oleh karena itu, nilai kapasitas adsorpsinya menurun ketika waktu ditambah menjadi 120 menit.
Pada waktu kontak 60 menit, sebagian besar situs aktif pada permukaan tanah lempung dan andisol telah ditempati oleh ion logam kadmium (Cd) dan terjadi gaya tolak antar ion logam kadmium (Cd) terjerap dan ion logam dalam larutan untuk menempati situs-situs aktif sehingga dengan adanya gaya tolak dan persaingan antar ion logam kadmium (Cd) tersebut menyebabkan kapasitas jerapan ion logam kadmium (Cd) menjadi berkurang (Alemayehu etal.,2012; Eba et al., 2010). Penyebab lainnya, dengan bertambahnya waktu kontak maka semakin banyak terbentuk kation terhidrat dengan jari-jari yang lebih besar dari pada jari-jari ion logamnya sehingga menghalangi proses jerapan (Hartopo, 2014 ; Muhdarina, dkk., 2010).
C. Penentuan Isoterm Adsorpsi
Penentuan jenis adsorpsi dilakukan melalui penentuan isoterm adsorpsi. Penentuan ini dilakukan dengan melakukan adsorpsi ion logam kadmium (Cd) dengan adsorben terbaik pada perbandingan komposisi lempung dan andisol 60:40 pada suhu 200⁰C dan waktu kontak 60 menit terhadap variasi konsentrasi larutan kadmium (Cd) 2, 4, 6, 8, dan 10 ppm.
Berdasarkan data pada Lampiran 12 tersebut kemudian dilakukan uji secara regresi linear sederhana dengan menggunakan persamaan Langmuir dan Freundlich. Persamaan isoterm Langmuir ditentukan dengan menggunakan
persamaan isoterm Langmuir lalu dibuat kurva Ce vs dengan hasil kurva isoterm yang diperoleh seperti dibawah ini:
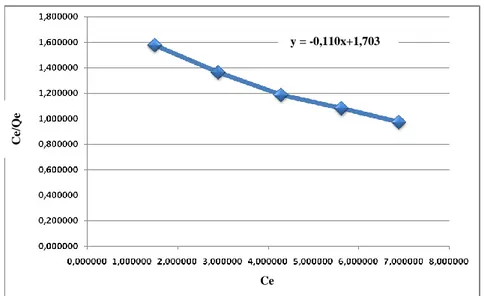
Gambar 11. Kurva Isoterm Langmuir Ion Logam Kadmium (Cd)
Selanjutnya, persamaan isoterm Freundlich ditentukan dengan menggunakan persamaan isoterm Freundlich Log Q = Log K + Log C lalu dibuat kurva Log C
vs Log Q dengan hasil kurva isoterm yang diperoleh seperti dibawah ini: Ce Qe 1 K Qmax Ce Qmax + = y = -0,110x+1,703 Ce Qe 1 n C e/ Qe Ce
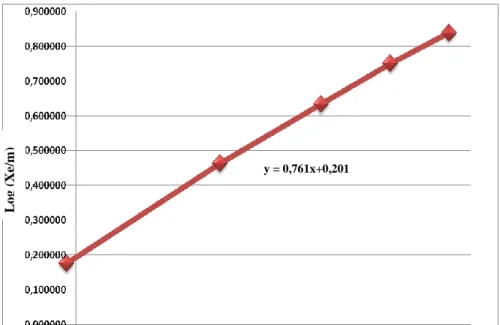
Gambar 10. Kurva Isoterm Freundlich Ion Logam Kadmium (Cd)
Dari hasil perhitungan keduanya, diperoleh kurva linear antara Ce dan untuk persamaan Langmuir dan kurva linear antara log Ce dan Log
Qe untuk persamaan Freundlich. Untuk melihat persamaan isoterm yang sesuai untuk penelitian ini, maka dapat dibuktikan melalui koefisien korelasi (R2) yang ditunjukkan pada grafik linear masing-masing persamaan dimana nilai R2 yang mendekati 1 maka dapat dikatakan jenis isoterm adsorpsi mengikuti persamaan isoterm tersebut.
Berdasarkan Gambar 9 dan 10 serta Tabel 5 menunjukkan bahwa persamaan
isoterm Langmuir memiliki R2 sebesar 0,979 dengan persamaan garisnya y = -0,110x+1,703. Sedangkan untuk persamaan Freundlich diperoleh nilai R2
sebesar 0,998 dengan persamaan garisnya y = 0,761x+0,201. Jika dilihat dari nilai R2 keduanya, nilai R2 dari persamaan Freundlich lebih besar daripada nilai R2 dari persamaan isoterm Langmuir, sehingga dapat disimpulkan jenis isoterm pada penelitian ini mengikuti persamaan Freundlich dengan harga konstanta dapat dilihat pada Tabel 5 di bawah ini.
y = 0,761x+0,201 Ce Qe Lo g (Xe /m ) Log Ce
Tabel 5. Harga konstanta Freundlich
Jenis Isoterm Konstanta Harga
Freundlich k 1,59
n 1,314
Isoterm Freundlich merupakan isoterm yang menggambarkan proses adsorpsi secara fisika. Persamaan isoterm Freundlich menjelaskan bahwa jerapan terjadi pada lebih dari satu permukaan (multilayer) dan penjerap mempunyai bidang permukaan heterogen dengan energi pengikat yang berbeda-beda. Jerapan ion logam kadmium (Cd) oleh penjerap campuran tanah lempung dan andisol terjadi secara fisisorpsi. Jenis jerapan ini cocok untuk mekanisme jerapan yang membutuhkan proses regenerasi karena zat yang terjerap hanya terikat lemah pada permukaan penjerap. Hasil perhitungan menunjukkan bahwa nilai k sebesar 1,59 dan n sebesar 1,314 dengan isoterm Freundlich. Sebagai perbandingan, adsorpsi ion logam kadmium (Cd) oleh adsorben cangkang telur bebek mengikuti isoterm Freundlich dengan nilai k sebesar 1,4077 mg/g dan nilai n sebesar 0,9969 (Krisnawati dkk, 2013).
Malik (2002) menyatakan bahwa koefisien adsorpsi k secara kasar dapat digunakan sebagai indikator kapasitas adsorpsi dan adalah intensitas adsorpsi. Secara umum, semakin tinggi nilai k, semakin tinggi juga kapasitas adsorpsi. Sementara itu, nilai eksponen memberikan indikasi yang mendukung adsorpsi, nilai n >1 merupakan adsorpsi yang disukai.
D. Teknologi Penjernih Air
Air di bumi umumnya tidak dalam keadaan murni (H2O), melainkan
mengandung berbagai zat baik terlarut maupun tersuspensi termasuk mikroba, oleh karena itu sebelum dikonsumsi, air arus diolah terlebih dahulu untuk menghilangkan atau menurunkan kadar bahan pencemar sampai tingkat yang aman untuk dikonsumsi. Menurut definisi, air bersih adalah air jernih yang tidak berwarna dan tidak berbau belum tentu aman untuk dikonsumsi. Persyaratan kualitas air minum (air yang aman dikonsumsi langsung) diatur dalam Peraturan
1 n
1 n
Menteri Kesehatan No. 492/MENKES/Per/IV/2010 (Menteri Kesehatan RI, 2010). Dalam peraturan tersebut disebutkan bahwa air minum harus memenuhi persyaratan fisik, kimia dan mikrobiologi. Pada penelitian ini bahan pencemar yang dianalisis adalah logam kadmium (Cd) dan parameter airnya adalah bakteri E Coli dan Koliform.
Hasil awal uji bakteri dan logam yang terkandung pada air sumur berdasarkan pemeriksaan yang telah dilakukan di Baristand Industri Samarinda dapat dilihat pada tabel 6.
Tabel 6. Data hasil pemeriksaan awal air sumur
No Parameter Hasil Kadar maksimum yang diperbolehkan
Keterangan
1 E Coli 10 0 TMS
2 Total Koliform 30 0 TMS
3 Kadmium (Cd) 0,1 0,003 TMS
Standar menurut PERMENKES NO. 492/MENKES/Per/IV/2010 Keterangan: MS (Memenuhi Syarat), TMS (Tidak Memenuhi Syarat)
Berdasarkan tabel di atas dapat diketahui bahwa air bersih yang diuji mengandung logam kadmium (Cd) dan bakteri Escherichia Coli dan Koliform. Kandungan adanya logam kadmium (Cd), bakteri E.Coli dan Koliform di dalam makanan/minuman menunjukan kemungkinan adanya mikroba yang bersifat enteropatogenik dan toksigenik yang berbahaya bagi kesehatan. Bakteri E.Coli dan Koliform dalam jumlah tertentu dapat menjadi indikator suatu kondisi yang bahaya dan adanya kontaminasi bakteri patogen (Balia dkk, 2011).
RO (Reverse Osmosis) dengan menggunakan filter keramik berbahan campuran lempung dan andisol diharapkan dapat menghilangkan 90-99% dari patogen dan kandungan logam yang ditemukan dalam air. Metode Reverse Osmosis (RO) adalah teknik penjernihan air dengan membran reverse osmosis yang mempunyai ukuran pemfilteran sebesar 0.0001 mikron, yang akan berfungsi menurunkan Total Dissolved Solids (TDS) dalam air. Membran ini terbuat dari bahan semi permeable dan mampu menyaring kandungan logam, virus dan bakteri dalam air (Endarko dkk, 2013). Selain itu ditambahkan dengan filter keramik
berbahan campuran lempung dan andisol pada reserve osmosis. Li and Lee (2009) menjelaskan bahwa sifat-sifat istimewa membran keramik berpori, seperti kestabilan terhadap suhu tinggi, kekuatan mekanis dan mudah dalam hal regenerasi. Bahan-bahan untuk membuat filter keramik dapat bervariasi namun sebagai bahan utamanya adalah tanah liat karena kemampuannya untuk dibentuk dan tahan pada suhu tinggi.
Hasil uji bakteri dan logam yang terkandung pada air sumur sesudah melalui teknologi penjernih air sistem reserve osmosis dengan menggunakan filter keramik dapat dilihat pada tabel 7.
Tabel 7. Data hasil pemeriksaan air sumur melalui teknologi penjernih air
No Parameter Hasil Kadar maksimum yang diperbolehkan
Keterangan
1 E Coli 0 0 MS
2 Total Koliform 0 0 MS
3 Kadmium (Cd) <0,001 0,003 MS
Standar menurut PERMENKES NO. 492/MENKES/Per/IV/2010 Keterangan: MS (Memenuhi Syarat), TMS (Tidak Memenuhi Syarat)
Dari hasil yang ditunjukan di atas, terlihat bahwa air bersih hasil pengolahan melalui teknologi penjernih air sistem reserve osmosis dengan menggunakan filter keramik telah memenuhi standard air minum PERMENKES. Setelah mengalami perlakuan kandungan logam kadmium (Cd), bakteri E.Coli dan Koliform mengalami penurunan menjadi 0 sesuai dengan kadar maksimum yang telah ditentukan. Hal ini menunjukkan bahwa teknologi penjernih air sistem reserve osmosis menggunakan filter keramik mempunyai keefektifan dalam menurunkan kadar logam kadmium (Cd) dan bakteri patogen dalam air sumur. Filter keramik mampu menurunkan berbagai bahan pencemar fisik, kimia dan biologi sehingga diperoleh air bersih yang dapat ditoleransi untuk air minum. Hartopo (2014) menyatakan bahwa filter keramik efektif dalam menurunkan kadar ion logam Mn dalam air dengan tingkat keefektifan sebesar 98,9%.
Penelitian ini, penyerapan ion logam kadmium (Cd) terhadap lempung dan tanah andisol dibuktikan pada larutan model melalui metode batch dengan
persentase 97,9%, hal ini dikarenakan air sumur tidak mengandung ion logam kadmium (Cd). Partikel tanah lempung memilki kemampuan untuk mengembang apabila kontak dengan air serta memilki kapasitas pertukaran ion yang tinggi sehingga mampu menahan kation pada partikelnya dalam jumlah besar (Bhatacharya and Gupta, 2006; Zhao et al., 2011; Grasi et. al., 2012). Selain itu, adanya partikel tanah andisol yang mempunyai porositas, luas permukaan dan daya tukar kation yang tinggi (Pranoto et al., 2013; Heraldy, dkk., 2004; Munir, 1996) menyebabkan kemampuan menurunkan ion logam kadmium (Cd) meningkat.
Osmosis merupakan proses perpindahan air dari larutan yang konsentrasinya rendah menuju larutan yang konsentrasinya tinggi dikarenakan adanya tekanan osmosis. Proses perpindahan ini melalui membran semipermeabel, dimana proses perpindahan air akan berhenti setelah konsentrasi kedua larutan sama. RO membutuhkan tekanan hidrostatik lebih besar daripada perbedaan tekanan osmotiknya sehingga air bisa mengalir dari larutan yang konsentrasinya lebih tinggi melalui membran semipermeabel. Sistem RO umumnya terdiri dari 4 proses, yaitu :
1. Pengolahan Awal (pretreatment)
Air umpan terlebih dahulu diolah agar sesuai dengan kondisi membran dengan menghilangkan padatan tersuspensi, menyesuaikan pH operasi dan menambahkan inhibitor untuk control scaling yang disebabkan konstituen-konstituen seperti kalsium sulfat.
2. Pemberian Tekanan
Air umpan yang sudah diolah dinaikkan tekanannya dengan pompa sampai tekanan operasi yang diinginkan agar sesuai dengan membran dan kadar garam air umpan.
3. Separasi Membran
Membran semipermeabel menghambat jalannya air umpan yang melewatinya. Air hasil keluaran dari membran berupa air bersih yang disebut permeate, dan yang tertahan pada membran disebut concentrate. Namun, karena
tidak ada membran yang dapat bekerja 100% sempurna, maka ada sebagian kecil garam yang masih dapat melewati membran.
4. Stabilisasi
Air hasil keluaran membran (air produk) biasanya disesuaikan pHnya terlebih dahulu sebelum ditransfer ke sistem distribusi.