ABSTRAK
Telah dilakukan penelitian mengenai aktivitas antibakteri dari ekstrak daun dan getah Jarak Tintir (Jatropha multifida) terhadap pertumbuhan S. aureus secara in vitro. Luka yang berdarah dapat menyebabkan infeksi oleh S. Aureus. Daun dan getah Jarak Tintir memiliki potensi sebagai obat tradisional untuk menyembuhkan luka. Penelitian ini dilakukan untuk mengetahui aktivitas antibakteri ekstrak daun dan getah Jarak Tintir terhadap pertumbuhan S. Aureus dan nilai Minimum Inhibitory Concentration (MIC). Aktivitas antibakteri dilihat dari terbentuknya zona hambat pada perlakuan. Metode yang digunakan untuk uji aktivitas antibakteri yaitu metode Kirby-Bauer. Metode yang digunakan untuk uji MIC adalah metode dilusi padat. Dalam penelitian ini dilakukan tiga kali pengulangan. Konsentrasi ekstrak daun dan getah yang digunakan adalah 5%, 10%, 25%, 50%, dan 100%. Kontrol positif digunakan povidone iodine 10%. Terdapat aktivitas antibakteri pada ekstrak daun dan getah yang ditunjukkan dari terbentuknya zona bening di sekitar paper disc. Diameter zona hambat terkecil pada ekstrak daun adalah konsentrasi 5% diameter 4 mm, sedangkan pada getah 10% diameter 2,33. Diameter terbesar pada ekstrak daun dan getah pada konsentrasi 100% dengan diameter berturut-turut 7,67 mm dan 20,33 mm. Tidak terdapat perbedaan signifikan antara ekstrak daun dan getah dalam menghambat pertumbuhan bakteri. Nilai Minimum Inhibitory Concentration tidak didapatkan karena konsentrasi terlalu rendah dan getah tidak tercampur rata dengan media kultur. Nilai Minimum Bactericidal Concentration tidak ditemukan karena aktivitas antibakteri hanya bersifat bakteriostatik atau hanya bersifat menghambat.
ABSTRACT
An antibacterial activity research of extract leaves and saps Tintir (Jatropha multifida) on Staphylococcus aureus with in vitro was carried out. Wounds that bleed can make innfection disesase by S. Aureus. The potential of leave ang saps as a traditional medicine that usually used for heal the wounds. This research aimed to know about antibacterial activities of leave extract and saps Jarak Tintir towards growing of S. Aureus and minimun inhibitory concentration (MIC). Antibacterial activity looks from inbition zone formation. The method used in this research of activity of antibaceterial is Kirby-Baur method. The Method that used for MIC is solid dilution method. In this research conducted three times repetition. The concentration of leaves extract and saps used in this research ranges from 5%, 10%, 25%, 50%, dan 100%. Positive control used povidone iodine 10%. The presence of antibacterial activity in the leaves extract and sap are shown of the clear zone around the paper disc. Inhibition zone diameter of the smallest in leaves extract is 5% and the diameter is 4 mm then in the sap is 10% and 2,33mm. The largest diameter in 100% , leaves extract 7,67 mm and sap 20,33 mm. Minimum Inhibitory Concentration value is not obtained because the concentration used is too low and sap is not blended with the medium culture. Minimum Bactericidal Concentration value is not founded because the antibacterial activity just have a bacteriostatic or only be inhibited.
UJI AKTIVITAS ANTIBAKTERI EKSTRAK JARAK TINTIR (Jatropha multifida L.) TERHADAP PERTUMBUHAN
Staphylococcus aureus SECARA IN VITRO.
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Pendidikan
Program Studi Pendidikan Biologi
Oleh :
Cicilia Maryani NIM : 091434017
PROGRAM STUDI PENDIDIKAN BIOLOGI JURUSAN PENDIDIKAN MATEMATIKA DAN ILMU
PENGETAHUAN ALAM
FAKULTAS KEGURUAN DAN ILMU PENGETAHUAN UNIVERSITAS SANATA DHARMA
i
UJI AKTIVITAS ANTIBAKTERI EKSTRAK JARAK TINTIR (Jatropha multifida L.) TERHADAP PERTUMBUHAN
Staphylococcus aureus SECARA IN VITRO.
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Pendidikan
Program Studi Pendidikan Biologi
Oleh :
Cicilia Maryani NIM : 091434017
PROGRAM STUDI PENDIDIKAN BIOLOGI JURUSAN PENDIDIKAN MATEMATIKA DAN ILMU
PENGETAHUAN ALAM
FAKULTAS KEGURUAN DAN ILMU PENGETAHUAN UNIVERSITAS SANATA DHARMA
iv
H AL AM AN P ER S EM B AH AN
Syukur kepada
Y esus K ristus, Bunda M aria Untuk Limpahan
K asihN ya Y ang T iada H enti, M emberikan
K emurahan Bagiku Untuk K esempatan
M enyelesaikan K uliah I ni.
Dengan Penuh Syukur K upersembahkan Buah Usaha I ni Untuk....
K edua Orang T uaku
Adikku
Dan
Orang T erkasih slalu mendampingi di saat senang dan susah.
v MOTTO
Ad Maior em Dei Gl or iam
S eor ang s ahabat menar u h k as i h
s et i ap w ak t u dan menj adi s eor ang
s au dar a dal am k es u k ar an. A ms al
17 : 7
viii ABSTRAK
Telah dilakukan penelitian mengenai aktivitas antibakteri dari ekstrak daun dan getah Jarak Tintir (Jatropha multifida) terhadap pertumbuhan S. aureus secara in vitro. Luka yang berdarah dapat menyebabkan infeksi oleh S. Aureus. Daun dan getah Jarak Tintir memiliki potensi sebagai obat tradisional untuk menyembuhkan luka. Penelitian ini dilakukan untuk mengetahui aktivitas antibakteri ekstrak daun dan getah Jarak Tintir terhadap pertumbuhan S. Aureus dan nilai Minimum Inhibitory Concentration (MIC). Aktivitas antibakteri dilihat dari terbentuknya zona hambat pada perlakuan. Metode yang digunakan untuk uji aktivitas antibakteri yaitu metode Kirby-Bauer. Metode yang digunakan untuk uji MIC adalah metode dilusi padat. Dalam penelitian ini dilakukan tiga kali pengulangan. Konsentrasi ekstrak daun dan getah yang digunakan adalah 5%, 10%, 25%, 50%, dan 100%. Kontrol positif digunakan povidone iodine 10%. Terdapat aktivitas antibakteri pada ekstrak daun dan getah yang ditunjukkan dari terbentuknya zona bening di sekitar paper disc. Diameter zona hambat terkecil pada ekstrak daun adalah konsentrasi 5% diameter 4 mm, sedangkan pada getah 10% diameter 2,33. Diameter terbesar pada ekstrak daun dan getah pada konsentrasi 100% dengan diameter berturut-turut 7,67 mm dan 20,33 mm. Tidak terdapat perbedaan signifikan antara ekstrak daun dan getah dalam menghambat pertumbuhan bakteri. Nilai Minimum Inhibitory Concentration tidak didapatkan karena konsentrasi terlalu rendah dan getah tidak tercampur rata dengan media kultur. Nilai Minimum Bactericidal Concentration tidak ditemukan karena aktivitas antibakteri hanya bersifat bakteriostatik atau hanya bersifat menghambat.
ix ABSTRACT
An antibacterial activity research of extract leaves and saps Tintir (Jatropha multifida) on Staphylococcus aureus with in vitro was carried out. Wounds that bleed can make innfection disesase by S. Aureus. The potential of leave ang saps as a traditional medicine that usually used for heal the wounds. This research aimed to know about antibacterial activities of leave extract and saps Jarak Tintir towards growing of S. Aureus and minimun inhibitory concentration (MIC). Antibacterial activity looks from inbition zone formation. The method used in this research of activity of antibaceterial is Kirby-Baur method. The Method that used for MIC is solid dilution method. In this research conducted three times repetition. The concentration of leaves extract and saps used in this research ranges from 5%, 10%, 25%, 50%, dan 100%. Positive control used povidone iodine 10%. The presence of antibacterial activity in the leaves extract and sap are shown of the clear zone around the paper disc. Inhibition zone diameter of the smallest in leaves extract is 5% and the diameter is 4 mm then in the sap is 10% and 2,33mm. The largest diameter in 100% , leaves extract 7,67 mm and sap 20,33 mm. Minimum Inhibitory Concentration value is not obtained because the concentration used is too low and sap is not blended with the medium culture. Minimum Bactericidal Concentration value is not founded because the antibacterial activity just have a bacteriostatic or only be inhibited.
x
KATA PENGANTAR
Puji dan syukur kepada Tuhan Yang Maha Esa atas berkat, kasih dan
perlindungannya, sehingga penulis dapat menyelesaikan tugas akhir ini. Skripsi
ini dapat diselesaikan dengan baik dan lancar berkat doa, bimbingan, dorongan,
bantuan dan dukungan dari berbagai pihak. Oleh karena itu, dengan segala
kerendahan hati pada kesempatan ini penulis ingin mengucapkan terima kasih
kepada pihak-pihak sebagai berikut :
1. Dr. Ir. P. Wiryono Priyotamtama, S.J., selaku dosen pembimbing skripsi yang
telah memberikan bimbingan, pengarahan, koreksi, dukungan dan motivasi
kepada penulis sehingga penulis dapat menyelesaikan studi dan skripsi dengan
lancar.
2. Drs. A. Tri Priantoro, M.For.Sc., selaku Kaprodi Program Studi Pendidikan
Biologi.
3. Dosen penguji skripsi yang telah memberikan kritik, saran dan masukan
kepada penulis.
4. Para dosen Pendidikan Biologi (Bu Nana, Bu Luisa, Pak Kristio, Romo
Sunu,Pak Tardhi, Bu Maslichah, Pak Tri) yang dengan sabar dan telaten
membimbing dan memberikan banyak pengetahuan sehingga penulis dapat
menyelesaikan studi dengan baik dan lancar.
5. Ibu Maria yang telah membantu peneliti dalam proses penelitian, memberikan
dukungan dan saran yang membangun.
6. Kepala Laboratorium Fakultas Farmasi Universitas Sanata Dharma
Yogyakarta, atas ijin yang diberikan sehingga peneliti bisa melakukan
xi
7. Kepada kedua orang tuaku Bapakku Florentinus Sukarno Sri Hadiwiyono,
Mamakku Fransicanes Ngatiyem dan Adikku Yohanes Sigit Laksono.
Terimakasih atas doa dan cinta yang tiada henti, dukungan moril dan materiil
sehingga peneliti dapat menyelesaikan skripsi dan kuliah.
8. Kepada teman-temanku angkatan 2009 yang selalu memberi warna dalam
kehidupan sehari-hari dan berbagi pengalaman bersama. Kepada Ruth lana
Monika as Mamiku, Riris, Duyung, Wiwik, Indri, Siska, Yuni, Yani, Rere,
Bundo, Rambu, Mb Triel, Junot, mb kristin, Ryka Nana, Jarot, Wisnu, Mas
Kris, Widi, Leo, Rio, Bang Eran, dan teman lain yang belum bisa disebutkan.
Terimakasih atas diinamika yang telah kita lalui.
9. Mas Vincensius Didin Maman yang selalu memberikan motivasi dan
dorongan moril dan materiil. Mas Dwi yang memberikan dukungan moril dan
materiil.
10.Terimakasih untuk teman indri dan febri farmasi, Mika, Krista, Ririn (teman
satu atap) , terimakasih untuk adik-adikku Nina, Dheni, Natri, Dikta Serta Mas
Agus Laboran.
11.Semua pihak yang tidak dapat penulis sebutkan satu persatu. Terima kasih
telah membantu penulis menyelesaikan skripsi.
Penulis menyadari masih banyak kekurangan dalam penulisan skripsi
ini. Oleh karena itu, dengan segala kerendahan hati penulis mengharapkan
kritik dan saran yang membangun untuk penulisan skripsi ini. Penulis
berharap semoga karya yang jauh dari sempurna ini dapat bermanfaat bagi
xii
Penulis,
xiii
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
HALAMAN MOTTO ... v
PERNYATAAN KEASLIAN KARYA ... vi
LEMBAR PERNYATAAN PERSETUJUANPUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIK ... vii
ABSTRAK ... viii
ABSTRACT ... xi
KATA PENGANTAR ... x
DAFTAR ISI ... xiii
DAFTAR TABEL ... xvii
DAFTAR GAMBAR ... xviii
DAFTAR LAMPIRAN ... xix
BAB I PENDAHULUAN A.Latar Belakang Masalah... 1
B. Rumusan Masalah ... 5
C. Batasan Masalah ... 6
D. Tujuan ... 6
E. Manfaat ... 7
xiv
BAB II TINJAUAN PUSTAKA
A. Antibakteri ... 8
B. Deskripsi Tanaman Jarak Tintir (Jatropha multifida L.) ... 10
1. Klasifikasi ... 10
2. Morfologi dan Fisiologi ... 11
3. Habitat ... 12
4. Manfaat ... 13
5. Kandungan Metabolit Sekunder ... 14
6. Aktivitas Antibakteri ... 15
C. Deskripsi Staphylococcus aureus ... 16
1. Klasifikasi ... 16
2. Morfologi dan Fisiologi ... 16
3. Habitat ... 18
4. Penyakit ... 19
D. Kerangka Pemikiran ... 22
BAB III METODOLOGI PENELITIAN A. Jenis Penelitian ... 23
B. Subjek dan Objek Penelitian ... 23
C. Definisi Operasional ... 23
D. Desain Penelitian... 24
1. Metode Pengujian Aktivitas Antibakteri ... 24
xv
a. Pengujian MIC (Minimum Inhibitory Concentration) ... 26
b. Pengujian MBC (Minimum Bactericidal Concentration)26 E. Variabel Penelitian ... 26
F. Populasi dan Sampel ... 27
G. Waktu dan Tempat Penelitian ... 27
H. Alat dan Bahan Penelitian ... 27
I. Langkah-langkah Penelitian ... 29
1. Tahap Persiapan ... 29
2. Tahap Pelaksanaan ... 30
a. Sterilisasi ... 30
b. Ekstraksi Daun dan Penyulingan Getah ... 30
1) Ekstraksi Daun ... 30
2) Penyulingan Getah ... 32
c. Pembuatan Media Kultur Bakteri ... 32
3. Tahap Perlakuan ... 33
a. Pengujian Aktivitas Antibakteri dengan Metode Difusi Agar Kirby-Bauer ... 33
b. Pengujian MIC atau KHM ... 34
c. Pengujian MBC atau KBM ... 35
J. Analisis Data ... 35
BAB IV HASIL PENELITIAN DAN PEMBAHASAN A. Hasil Penelitian ... 37
xvi
2. Ekstrak Daun dan Getah Jarak Tintir (Jatropha multifida L)
... 37
a. Ekstrak Daun Jarak Tintir (Jatropha multifida L)... 37
b. Getah Jarak Tintir (Jatropha multifida L) ... 38
3. Pertumbuhan Staphylococcus aureus ... 38
4. Hasil Pengukuran Aktivitas Ekstrak Daun dan Getah Jarak Tintir (JatrophamultifidaL.) Terhadap Pertumbuhan Staphylococcus aureus ... 39
5. Nilai Kadar Hambat Minimal (MIC/Minimum Inhibitory Concetration) ... 42
B. Pembahasan ... 46
1. Aktivitas Ekstrak Daun (JatrophamultifidaL.) Terhadap Pertumbuhan Staphylococcus aureus ... 46
2.MIC (Minimum Inhibitory Concentration) Ekstrak Daun... 49
3. Aktivitas Getah Jarak Tintir (JatrophamultifidaL.) Terhadap Pertumbuhan Staphylococcus aureus ... 50
4. MIC (Minimum Inhibitory Concentration) Getah ... 53
C. Kaitan Antara Hasil Penelitian dan Pendidikan...55
BAB V KESIMPULAN DAN SARAN A. Kesimpulan ... 56
B. Saran ... 57
xvii
DAFTAR TABEL
Halaman
Tabel 2.1 Faktor-faktor yang mempengaruhi pertumbuhan S.aureus ... 19 Tabel 3.1 Daftar Alat Penelitian ... 27
Tabel 3.2 Daftar Bahan Penelitian ... 30
Tabel 3.3 Volume ekstrak daun yang digunakan untuk membuat stok konsentrasi
ekstrak ... 31
Tabel 3.4 Volume getah yang digunakan untuk membuat stok konsentrasi .... 32
Tabel 4.1 Diameter zona hambat bakteri pada ekstrak daun... 39
Tabel 4.2 Diameter zona hambat bakteri pada getah ... 39
Tabel 4.3 Percobaan I HasilPenentuan MIC Ekstrak Daun danGetah Jarak Tintir
(JatrophamultifidaL.) pada pertumbuhan Staphylococcus aures ... 42 Tabel 4.4 Percobaan II Hasil Penentuan MIC Ekstrak Daun dan Getah Jarak Tintir
(JatrophamultifidaL.) pada pertumbuhan Staphylococcus aureus ... 44
xviii
DAFTAR GAMBAR
Halaman
Gambar 2.1 Tanaman Jarak Tintir ... 10
Gambar 2.2 Daun Jarak Tintir ... 11
Gambar 2.3 Bunga Jarak Tintir dan Buah Jarak Tintir Masih Muda ... 12
Gambar 2.4 Biji Jarak Tintir yang Sudah Tua ... 12
Gambar 2.5 Koloni Staphylococcus aureus ... 17
Gambar 2.6 Luka luar yang terbuka ... 20
Gambar 2.7 Impetigo ... 20
Gambar 2.8 Folikulistis ... 21
Gambar 2.9 Bisul ... 21
Gambar 4.1 Zona bening yang terukur ... 40
Gambar 4.2 Hasil Uji Aktifitas Antibakteri Kiri dengan getah, kanan dengan ekstrak daun setelah inkubasi selama 24 jam ... 40
Gambar 4.3 Kontrol Positif, Negatif dan Kontrol Media ... 40
Gambar 4.4 Media kultur pada uji MIC getah yang sudah dituang dan setelah di inkubasi ... 45
Gambar 4.5 Endapan yang terjadi pada media kultur ... 45
xix
DAFTAR LAMPIRAN
Lampiran1 Skema Kerja Uji Aktivitas Antibakteri ... ..62
Lampiran 2 Skema Kerja Uji MIC ... ..63
Lampiran 3 Skema Kerja Uji MBC ... ..64
Lampiran 4 Silabus ... ..65
Lampiran 5 Rancangan Pelaksanaan Pembelajaran (RPP) ... ..68
Lampiran 6 Hasil Data Pengukuran Zona Hambat ... ..75
Lampiran 7 Dokumentasi Penelitian ... ..76
Lampiran 8 Analisis SPSS Pada Ekstrak Daun ... ..78
a. Uji Homogenitas ... 78
b. Uji Normalitas ... 83
c. Uji Transformasi ... 94
d. Uji Non Paranetrik Kruskal-Wallius... 101 e. Uji Regresi Linier ... 102
Lampiran 9 Analisis SPSS Pada Getah ... ..104
a. Uji Homogenitas ... 104
b. Uji Normalitas ... 109
c. Uji Transformasi ... 119
1
BAB I
PENDAHULUAN
A. Latar Belakang Masalah
Salah satu tantangan yang tidak bisa dihindarkan dari hidup manusia adalah
adanya penyakit. Penyakit bisa disebabkan oleh berbagai faktor antara lain:
melemahnya kekebalan tubuh karena kelelahan, pola makan tidak sehat sehingga
virus dapat dengan mudah menginfeksi tubuh manusia, penurunan sifat / gen,
atau karena cedera dan terluka. Kemajuan jaman berjalan seiring dengan
penemuan berbagai penyakit baru dan semakin resistennya bakteri atau mikrobia
patogen lainnya, sehingga masyarakat semakin dituntut untuk bisa menemukan
obat-obatan yang mampu mencegah, memberi efek atau menyembuhkan. Upaya
pengobatan terhadap penyakit sudah ada dari Jaman dahulu. Masyarakat pada
jaman dahulu mencari atau membuat sendiri obat yang mereka perlukan baik dari
tumbuhan atau hewan. Pengetahuan tentang bahan obat tersebut mereka wariskan
secara turun temurun dan disebarkan dari mulut ke mulut. Dalam catatan sejarah
dapat diketahui bahwa fitoterapi atau terapi menggunakan tumbuhan telah dikenal
masyarakat sejak masa sebelum masehi (Gana, 2008). Tumbuh-tumbuhan menjadi
komoditas penting terkait aspek kemampuan menyembuhkan penyakit sehingga
banyak penelitian dilakukan untuk mengetahui potensi berbagai tumbuhan untuk
pengobatan.
Indonesia merupakan negara yang mempunyai keragaman jenis tumbuhan
paling besar di dunia. Hal ini tercermin dalam Gana (2008), hutan tropik
Indonesia memiliki lebih dari 30.000 jenis tumbuhan berbunga. Sementara dari
bermanfaat dilaporkan sebanyak 1306 jenis dari 153 suku sebagai tumbuhan obat.
Data ini belum termasuk tumbuhan rendah. Pada saat ini bahan alam terutama
tumbuhan obat telah digunakan oleh berbagai lapisan masyarakat dunia baik di
negara berkembang maupun negara maju. Sekitar 80% penduduk negara
berkembang masih mengandalkan pengobatan tradisional dan 85% pengobatan
tradisional dalam prakteknya menggunakan tumbuh-tumbuhan (Beswika,2009).
Jurnal Current Botany dalam currentbotany.org disampaikan bahwa secara historis tanaman telah menyediakan agen anti infeksi dengan senyawa yang sangat
efektif dalam memerangi infeksi mikroba. Disampaikan juga bahwa infeksi
merupakan penyebab utama kematian di seluruh dunia dan fitokimia yang berasal
dari tanaman berpotensi sebagai bahan pengobatan bagi penyakit menular yang
berbahaya. Selanjutnya disampaikan bahwa produk alami, baik dalam bentuk
senyawa murni atau ekstrak tanaman, membuka peluang yang tidak terbatas untuk
dijadikan obat baru karena ketersediaan kandungan kimia yang beragam.
Salah satu tumbuhan tropis Indonesia yang memiliki khasiat obat adalah Jarak
tintir (Jatropha multifida L.), yang dikenal dengan beberapa nama daerah diantaranya jarak tintir (Jawa), jarak gurita (Sunda), balacai batai (Ternate), pohon
yodium, Geloah (Gayo). Hariana (2006) menuturkan dalam kajian etnobiologi
yang dilakukan di beberapa daerah tanaman perdu ini banyak dimanfaatkan oleh
masyarakat sebagai obat luka. Namun banyak pula manfaat lain dari tumbuhan ini
seperti mengobati luka bengak, patah tulang, mencegah dan mengobati kerusakan
gigi. Khasiat dari Jarak Tintir (Jatropha multifida L.) sebagai obat herba tradisonal telah banyak diteliti secara ilmiah oleh banyak peneliti. Sari (2010)
mempunyai daya efektif antimikroba terhadap bakteri patogen Staphyloccocus aureus dan jamur Candida albicans. Hasil penelitian Isnaini (2011) menyatakan bahwa konsentrasi minimal ekstrak etanol pohon yodium yang mulai menghambat
pertumbuhan koloni bakteri Escherichia coli adalah sebesar 1 %, konsentrasi efektif ekstrak etanol pohon yodium. Penghambatan lebih efektif dibandingkan
dengan ampisilin 20%.
“Jatropha multifida L. mempunyai kemampuan untuk menyembuhkan berbagai macam penyakit atau infeksi bakteri. Hal ini terkait adanya senyawa aktif dalam (Jatropha multifida L.) yang bersifat sebagai antimikroba. Berdasarkan penelitian kandungan senyawa metabolit sekunder (fitokimia) diketahui bahwa Jarak Tintir mengandung α-amirin, kampesterol, 7 α-diol,
stigmaterol, β-sitosterol, dan HCN. Batangnya mengandung alkaloid, saponin,
flavonoid dan tanin Selain itu (Jatropha multifida L.) juga mempunyai efek farmakologis diantaranya sebagai anti inflamasi, penghambat pendarahan dan penurun panas” (Hariana, 2006:138).
Kulit merupakan bagian tubuh paling luar dan salah satu indera, yaitu indera
peraba. Indera peraba peka terhadap segala sentuhan dan efek jika sesuatu
melukai tubuh kita. Selain sebagai indera peraba kulit juga berfungsi untuk
melindungi jaringan-jaringan dan organ tubuh dalam. Tanpa kulit badan manusia
hanya dibalut oleh otot. Oleh karena itu kulit merupakan mekanisme pertahanan
yang utama dalam proses infeksi bakteri. Banyak aktivitas yang menyebabkan
bakteri atau mikroba menempel pada kulit. Kulit yang terluka akan lebih rentan
terhadap infeksi. Pada kulit yang terluka akan ada beberapa jaringan yang terluka
dan lapisan kulit terbuka. Hal ini dengan mudah memungkinkan terjadinya infeksi
mendapatkan perlakuan atau pemberian antibakteri, maka bakteri akan semakin
nyaman untuk tumbuh dalam luka tersebut. Orang menganggap bahwa kulit
terluka jika sampai berdarah akan serta merta sembuh. Namun kenyataannya tidak
selalu begitu. Tubuh memiliki mekanismenya sendiri dalam melindungi setiap
organnya. Begitu pula jika kulit terluka, sel darah putih dan plasma darah
memfagosit mikroba patogen yang masuk. Namun apabila tubuh tidak dalam
keadaan normal atau baik, luka gores atau luka berdarah akan dapat menyebabkan
infeksi, hingga kematian. Salah satu bakteri patogen yang ditemukan pada luka
adalah bakteri patogen gram-positif Staphylococcus aureus. “Staphylococcus aureus dapat mengganggu sistem imun pada tubuh manusia karena mengikat antibodi, menyerang membran sel dan menyebabkan hemolisis, serta leukolisis yang mematikan sel tubuh manusia. Selain itu penyakit yang disebabkan oleh Staphylococcus aureus adalah infeksi pada kulit seperti bisul, furonkolosis; infeksi yang lebih serius, seperti pneumonia, mastitis dan meningitis; dan infeksi pada saluran urine” (Radji, 2011:184-185). Bakteri yang tergolong resistan terhadap antibiotik disebut Multi Drug Resistant (MDR), salah satunya adalah
Staphylococcus aureus. Resistensi terhadap antibiotik menyebabkan bahaya besar bagi manusia karena infeksi yang semula mudah diobati dengan antibiotik kini
menjadi sulit atau bahkan tidak dapat lagi diobati dengan antibiotik. Bakteri ini
sudah kebal terhadap antibiotik kelas standar seperti penisilin, methicillin, dicloxacillin, nafcillin, oxacillin dan cephalosporins sehingga sulit diobati.
Menjadi fatal kalau bakteri ini mampu memakan daging otot kita. Bahkan jika
sudah menjalar menjadi lebih parah karena akan menyerang organ vital seperti
antibiotik sudah menjadi perhatian global, antibiotik terancam oleh munculnya
mikroba resisten. Penting untuk menggali kemampuan senyawa metabolit
sekunder untuk menghambat pertumbuhan Staphylococcus aureus dan mengetahui efek farmakologisnya. Oleh sebab itu penelitian tentang daya hambat
aktivitas antibakteri dari ekstrak Jarak Tintir (Jatropha multifida L.) terhadap
Staphylococcus aureus sebagai bakteri patogen pada luka di kulit perlu dilakukan. Penelitian ini menggunakan getah dan daun dari tanaman Jarak Tintir (Jatropha multifida L.).
B. Rumusan Masalah
Dari latar belakang di atas maka masalah dari penelitian ini dapat dirumuskan:
Bagaimana pengaruh ekstrak Jarak tintir (Jatropha multifida L) terhadap pertumbuhan bakteri Staphylococcus aureus secara in vitro?
Berdasarkan rumusan masalah di atas, maka dibuat pertanyaan penelitian
sebagai berikut :
1. Apakah ekstrak Jarak tintir (Jatropha multifida L) mempunyai aktivitas antibakteri terhadap pertumbuhan Staphylococcus aureus ?
2. Apakah konsentrasi ekstrak daun dan getah Jarak tintir (Jatropha multifida L.) berpengaruh terhadap zona hambat yang dihasilkan pada media kultur? 3. Berapakah nilai MIC (Minimum Inhibitory Concentration) dan MBC
(Minimum Bactericidal Concentration) dari ekstrak daun dan getah Jarak tintir (Jatropha multifida L) dalam menghambat pertumbuhan
Staphylococcus aureus?
4. Ekstrak manakah yang memiliki aktivitas antibakteri yang signifikan
C. Batasan Masalah
Batasan masalah dalam penelitian ini adalah :
1. Ekstrak yang digunakan berasal dari daun yang masih muda, berwarna hijau ,
dan getah perlu diisolasi sebelum perlakuan.
2. Parameter dalam penelitian ini adalah diameter zona hambat di sekitar kertas
cakram pada media kultur dengan satuan milimeter.
3. Metode yang digunakan untuk melihat aktivitas bakteri adalah metode difusi
Kirby-Bauer dengan menggunakan paper disc untuk membantu mengetahui zona hambat yang yang terlihat pada media dengan satuan milimeter (mm).
4. Metode yang digunakan untuk menentukan MIC (Minimum Inhibitory Concentration) adalah metode dilusi padat dengan parameter tidak tumbuhnya bakteri atau media kultur setelah di inkubasikan.
D. Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui aktivitas antibakteri dari ekstrak
daun dan getah Jarak tintir (Jatropha multifida L.) terhadap pertumbuhan
Staphylococcus aureus berdasarkan zona hambat yang didapatkan dari media kultur, konsentrasi efektif ekstrak daun dan getah Jarak tintir (Jatropha multifida L.). Penelitian ini juga bertujuan untuk mengetahui mana ekstrak daun atau getah
(Jatropha multifida L.) yang memiliki zona hambat paling lebar dan juga mengukur MIC dari ekstrak daun dan getah Jarak tintir (Jatropha multifida L.)
E. Manfaat 1. Bagi Peneliti
Manfaat penelitian ini untuk peneliti adalah menambah ilmu dan wawasan
peneliti tentang pengujian pengaruh suatu ekstrak tanaman herba terhadap suatu
bakteri patogen, membantu peneliti untuk semakin memahami tentang prosedur
uji aktivitas, dan membantu peneliti menyadari akan banyaknya potensi tanaman
herba yang masih belum tergali.
2. Bagi Masyarakat
Manfaat dari penelitian ini adalah agar masyarakat dapat menggunakan daun
dan getah Jarak Tintir sebagai obat alternatif terhadap luka agar terhindar dari
infeksi Staphylococcus aureus dan sebagai dasar pengembangan bahan-bahan obat-obatan antibakteri sebagai alternatif penyembuhan terhadap penyakit yang
disebabkan oleh bakteri patogen Staphylococcus aureus.
F. Hipotesis
Terdapat aktivitas antibakteri dan perbedaan signifikan dari ekstrak daun dan
getah Jarak tintir (Jatropha multifida L.) yang bersifat menghambat pertumbuhan
8
BAB II
TINJAUAN PUSTAKA A. Antibakteri
Menurut Aulia (2013) dalam, antibakteri adalah obat atau senyawa kimia yang
digunakan untuk membasmi bakteri, khususnya bakteri yang bersifat merugikan
manusia. Beberapa istilah yang digunakan untuk menjelaskan proses pembasmian
bakteri adalah germisid, bakterisid, bakteriostatik, antiseptik, desinfektan.
“Mekanisme kerja obat antimikroba tidak sepenuhnya dimengerti. Namun mekanisme aksi ini dapat dikelompokkan dalam empat hal utama:
a. Penghambatan terhadap sintesis dinding sel b. Penghambatan terhadap fungsi membran sel c. Penghambatan terhadap sintesis protein
d. Penghambatan terhadap sintesis asam nukleat”
(
http://kesehatan.kompasiana.com/makanan/2011/06/10/anti-bakteri-dan-mekanismenya-372060.html)
Menurut Brooks (2005) dalam Dewi (2010) antibakteri merupakan bahan atau
senyawa yang khusus digunakan untuk kelompok bakteri. Antibakteri dapat
dibedakan berdasarkan mekanisme kerjanya, yaitu antibakteri yang menghambat
pertumbuhan dinding sel, antibakteri yang mengakibatkan perubahan
permeabilitas membran sel atau menghambat pengangkutan aktif melalui
membran sel dan antibakteri yang menghambat sintesis protein serta menghambat
sintesis asam nukleat sel. Aktivitas antibakteri dibagi menjadi 2 macam yaitu
aktivitas bakteriostatik (menghambat pertumbuhan tetapi tidak membunuh
Untuk dapat diterima sebagai agen antimikroba, suatu bahan harus bisa
menghambat atau menghancurkan patogen tanpa merusak bagian yang
disembuhkan. Obat Sulfonide menghambat produksi asam folat (vitamin) pada
mereka yang membutuhkan bakteri asam para-aminobenzoic (PABA) untuk bisa
mensintesis asam folat. Karena molekul sulfominade mirip dalam bentuk molekul
PABA, bakteri mencoba untuk memetabolisme sulfonide untuk menghasilkan
asam padat. Tanpa asam folat, bakteri tidak dapat memproduksi protein esensial
tertentu dan akan mati. Beberapa mekanisme agen antibakteri membunuh atau
menghambat pertumbuhan bakteri (Burton,2004).
Menurut Davis Stout (1971) dalam Priyatmoko (2008:28) , “ketentuan kekuatan antibiotik-antibakteri sebagai berikut: daerah hambatan 20 mm atau lebih berarti berdaya hambat sangat kuat, daerah hambatan 10-20 mm berdaya hambat kuat, daerah hambatan 5-10 mm berdaya hambat sedang, dan daerah hambatan 5 mm atau kurang berdaya hambat lemah”. Faktor yang mempengaruhi ukuran daerah penghambatan, yaitu sensitivitas organisme,
medium kultur, kondisi inkubasi, dan kecepatan difusi agar. Faktor-faktor yang
mempengaruhi kecepatan difusi agar, yaitu konsentrasi mikroorganisme,
komposisi media, suhu inkubasi, dan waktu inkubasi (Schlegel dan Schmidt 1994
dalam Priyatmoko 2008 ).
Uji aktivitas antibakteri dapat dilakukan dengan metode difusi dan metode
Syarat jumlah bakteri untuk uji kepekaan/sensitivitas yaitu 106-10-8 CFU/mL
(Hermawan, 2007 dalam Dewi, 2010).
B. Deskripsi Tanaman Jarak Tintir (Jatropha multifida)
1. Klasifikasi
Gambar 2.1 : Tanaman Jarak Tintir (Jatrophamultifida L .) (Sumber : http://floridata.com)
Berikut merupakan taksonomi tanaman Jarak tintir :
Kingdom : Plantae – Plants
Subkingdom : Tracheobionta – Vascular plants Superdivision : Spermatophyta – Seed plants Division : Magnoliophyta – Flowering plants Class : Magnoliopsida – Dicotyledons Subclass : Rosidae
Order : Euphorbiales
Family : Euphorbiaceae – Spurge family Genus : Jatropha L. – nettlespurge
Species : Jatrophamultifida L. – coralbush
2. Morfologi dan Fisiologi
Jarak tintir merupakan tumbuhan tahunan , berbentuk semak, dengan akar
tunggang. Tinggi tanaman sekitar 2 meter dengan batang bulat, berkayu,
pangkalnya membesar, bergetah, dan tampak jelas bekas menempelnya daun
(Suharmiati, 2005). Jarak tintir berdaun tunggal, daunnnya tersebar, panjang
daunnya mencapai 15-20 cm, berbentuk bulat, bercangap, pertulangan daunya
menjari, ujung daunnya runcing, pangkalnya membulat, tepi daun rata dan daun
berwarna hijau.
Gambar 2.2 : Daun Jarak Tintir
(Sumber: http://www.trubus-online.co.id/blog/5773-manfaat-jarak-cina.html )
Bunga jarak tinitr merupakan bunga majemuk, berbentuk malai, bertangkai di
ujung cabang, benang sarinya berjumlah delapan, kepala sari jarak tintir berbentuk
tapal kuda, putiknya berjumlah tiga berukuran pendek, kelopak bercangap dan
Gambar 2.3 : Bunga Jarak Tintir dan Biji yang masih muda
(Sumberhttp://www.tropicalplantbook.com/garden_plants/shrubs%20flow ers/red/jatropha-multifida.htm)
Bijinya bulat, jika masih muda berwarna putih, dan setelah tua menjadi
coklat (Suharmiati 2005 ).
Gambar 2.4: Biji Jarak Tintir yang sudah tua
(Sumber :
http://www.tropicalplantbook.com/garden_plants/shrubs%20flowers/red/ja tropha-multifida.htm)
3. Habitat
Jatrophamultifida L ditanamam sebagai tanaman hias di Australia utara dan Afrika tenggara, terdapat pula di Filipina dan Srilanka terutama Pulau Jawa dan
sekitar pekarangan rumah. Haryanto (2009:230) mengungkapkan “tanaman ini dapat tumbuh di tempat yang kurang subur asalkan pH tanahnya 6-7 dan drainasenya baik, sebab akar jarak tidak tahan genangan air. Jarak merupakan perdu yang tumbuh pada ketinggian 0-800 m diatas permukaan laut, tingginya dapat mencapai 2-3 m”.
4. Manfaat
Hampir semua bagian tanaman Jarak tintir bisa dimanfaatkan, menurut Hariana
(2006:138) : biji,daun dan getahnya dapat dimanfaatkan untuk mengobati beberapa penyakit seperti berikut ini.
a. Bengkak terpukul, terkilir, tulang patah dan luka berdarah
Cuci bersih 7 helai daun segar, tumbuk hingga hancur, lalu tambahkan sedikit air sampai membentuk adonan. Oleskan pada bagian yang sakit.
b. Luka berdarah
Oleskan getah batang atau daun pada bagian luka yang baru. c. Mencegah dan mengobati kerusakan gigi
Tumbuk 1 butir biji sampai halus lalu seduh dengan 1 gelas air panas. Setelah dingin, air seduhan untuk berkumur selama 3-5 menit.
Dalam penelitian yang dilakukan oleh Syarfati dalam jurnal natural (2011)
diperoleh hasil bahwa getah jarak cina berpotensi sama dengan betadin dalam
lama waktu terbentuk keropeng pada luka baru. Begitu pula penelitian yang
dilakukan oleh Sari bahwa Jatropha multifida berdaya efektif sebagai antimikroba. Dituliskan pula oleh Sabandar dalam artikel yang berjudul A Review
of Jatropha multifida L. bahwa semua bagian pada tanaman tersebut memiliki efek pengobatan yang kuat terutama bijinya. Bijinya berguna untuk mengobati
digunakan untuk mengobati kudis dengan cara ditempelkan di atas luka dan
mengobati ulkus. Kulit kayu dan daun digunakan untuk mengobati neudermatitis,
gatal pada kulit dan eksim kulit Sedangkan di Nigeria batangnya juga digunakan
untuk perawatan gigi. Dalam trubus-online juga diungkapkan bahwa Jarak cina
menjadi andalan PT. Rumpun Sejati—perusahaan penggemukan sapi di Bogor,
Jawa Barat—untuk mengobati luka di kulit sapi. Kelebihan daun betadin, selain
murah, juga manjur dan tahan lama. Aromanya membuat lalat enggan mendekat
sehingga luka sembuh lebih cepat.
5. Kandungan Metabolit Sekunder
Senyawa metabolit adalah senyawa yang digolongkan berdasarkan
biogenesisnya, artinya berdasarkan sumber bahan baku dan jalur biosintesisnya.
Terdapat 2 jenis metabolit yaitu metabolit primer dan sekunder. Metabolit primer
(polisakarida, protein, lemak dan asam nukleat) merupakan penyusun utama
makhluk hidup, sedangkan metabolit sekunder meski tidak sangat penting bagi
eksistensi suatu makhluk hidup tetapi sering berperan menghadapi spesies-spesies
lain, misalnya zat kimia untuk pertahanan, penarik seks, feromon. Contoh dari
senyawa metabolit sekunder adalah alkaloid, saponin, triterpen dan tannin.
“Senyawa kimia tanaman yang jumlahnya paling banyak adalah senyawa kimia bermolekul kecil dari kelompok yang penyebaranya terbatas inilah yang dimaksud dengan senyawa metabolit sekunder “(Sirait, 2007:2).
Batang Jarak tintir mengandung alkaloid, saponin, flavonoid, dan tanin. Getah
daun jarak tintir berkhasiat sebagai obat luka yang masih baru (Suharmiati, 2005).
Flavonoid telah diketahui sebagai vasodilatator yang dapat memperlancar aliran
darah, tanin bersifat sebagai antiseptik yang dapat menghambat pertumbuhan
vasokontriksi pembuluh darah kapiler dan kandungan saponin dapat memicu
pembentukan kolagen, yaitu protein struktural yang berperan dalam proses
penyembuhan luka (Syarfati, 2011).
Flavonoid umumnya terdapat pada tumbuhan sebagai glikosida. Flavonoid
terdapat pada seluruh bagian tanaman, termasuk pada buah, tepung sari dan akar
(Sirait, 2007) . Mekanisme kerja flavonoid diduga mendenaturasi protein sel
bakteri dan merusak membran sel (Nishino 2009 dalam Silvikasari 2011).
“Jarak cina memiliki rasa agak pahit dan bersifat netral. Beberapa bahan kimia yang terkandung dalam jarak ini adalah α-amirin, kampesterol, 7 α-diol, stigmaterol, β-sitosterol, dan HCN. Batangnya mengandung alkaloid, saponin,
flavonoid dan tanin. Efek farmakologisnya diantaranya penurun panas, antiinflamasi, dan penghambat perdarahan “(Hariana,2006:138).
6. Aktivitas Antibakteri
Dituliskan oleh Sabandar dalam artikel yang berjudul A Review of
Jatropha multifida L., Antibakteri-Aiyelaagbe (2001) dalam Sari (2010) melaporkan aktivitas antibakteri heksana, etil asestat, kloroform dan ekstrak
etanol Jatrophamultifida L. terhadap Bacillus subtilis dan Staphyloccocus aureus.
Labaditin telah menunjukkan antibakteri terhadap bakteri gram-positif,
Streptoccocus mutans, tetapi tidak berpengaruh terhadap bakteri gram-negatif. Dari penelitian yang dilakukan Zamrodi (2011) di dapatkan bahwa zat aktif
tumbuhan anting-anting (Acalypha indica L.) dari ekstrak etanol yang positif mengandung senyawa golongan tripertepenoit dan flavonoid mempunyai aktivitas
penghambatan pada pertumbuhan Escherichia coli dan Staphylococcus aureus. Rahayu dalam penelitian yang berjudul Aktivitas Antibakteri Saponin
Mastitis Pada Sapi Perah mengungkapkan bahwa terdapat aktivitas antibakteri
terhadap Staphylococcus Aureus dari saponin isolasi Aloe Barbadensis. Hasil uji aktivitas yang dilakukan oleh Ummah (2010) terungkap bahwa senyawa tannin
pada belimbing wuluh mempunyai aktivitas antibakteri terhadap Escherichia coli
dan Staphylococcus aureus.
C. Deskripsi Staphylococcus aureus 1. Klasifikasi
Berikut merupakan taksonomi Staphylococcus aureus
Domain : Bacteria
Kerajaan : Eubacteria
Filum : Firmicutes
Kelas : Bacilli
Ordo : Bacillales
Famili : Staphylococcaceae
Genus : Staphylococcus
Spesies : S. aureus
(Sumber: http://id.wikipedia.org/wiki/Staphylococcus_aureus)
2. Morfologi dan Fisiologi.
Staphylococcus aureus adalah bakteri gram-positif berbentuk bulat, berdiameter 0,5 – 1,5 mm, tidak bergerak dan tidak berspora (Holt, 1994).
Gambar 2.5 : Koloni Staphylococcus aureus
(Sumber : http://www.bioquell.com)
“Staphylococcus bersifat anaerob fakultatif karena melakukan respirasi aerob atau fermentasi dengan hasil utama asam laktat” (Radji, 2011:180). Untuk kepentingan klinis, Staphylococcus dapat dibedakan menjadi Staphylococcus yang menghasilkan dan tidak menghasilkan koagulase. Staphylococcus penghasil koagulase adalah Staphylococcus aureus (Vandepiite, 2011). Staphylococcus aureus merupakan spesies
Staphylococcus yang merupakan katalase positif, artinya mikroorganisme tersebut menggunakan enzim katalase untuk menguraikan hidrogen
peroksida (H2O2) menjadi air dan oksigen sehingga menghasilkan
gelembung-gelembung (Sears, 2011). Sedangkan spesies lain tidak bisa
menguraikan H2O2, sehingga perbedaan spesies Staphylococcus dapat
dilihat jika dilakukan penambahan H2O2 muncul gelembung-gelembung
atau tidak. Enzim koagulase mengaktifkan protombin, menyebabkan
pembekuan darah, diuji dengan cara mencampur plasma dengan kultur
bakteri dalam sebuah tabung reaksi. Secara in vivo, Staphylococcus aureus
melepaskan koagulase yang akan menyebabkan pembentukan sawar
akan melindungi Staphylococcus aureus dari sistem imun hospes (Sears, 2011). Staphylococcus aureus dapat menggangu sistem imun pada tubuh manusia karena mengikat antibodi, menyerang membran sel dan dapat
menyebabkan hemolisis serta leukosis yang mematikan tubuh manusia
(Ahira, 2013). Staphylococcus aureus memiliki kemampuan mendeteksi jumlah sel menggunakan sinyal oligopeptida, dan memastikan jumlah
tersebut cukup untuk memproduksi dan toksik dan enzim koagulase,
enzim ini yang berperan dalam menggumpalkan fibrinogen di dalam
plasma darah sehingga Staphylococcus aureus selamat dari fagositosis dan respon antibodi tubuh kita (Ahira, 2013).
3. Habitat
Suhu optimum pertumbuhan Staphylococcus adalah 30-370C dan selalu bisa tumbuh pada kandungan 10% NaCl (Holt, 1994). Sedangkan
kisaran suhu pertumbuhan antara 15-400C, Staphylococcus aureus dapat tumbuh pada suhu 15-450C dan dalam NaCl berkonsentrasi 15% (Radji,
2011). Staphylococcus aureus merupakan bagian dari flora mikroba komensal pada hidung (40% orang dewasa sehat positif), kulit dan saluran
cerna, spesies ini menyebabkan impetigo, bisul, abses, infeksi luka, infeksi
ulkus, dan luka bakar, osteomielitis, mastitis, epiema pleura, piomiositis,
sindrom syok toksik, dan jenis-jenis infeksi piogenik lainya (Vandepiite,
2011). Di antara semua bakteri yang tidak membentuk spora,
kering pada benang, kertas kain dan dalam nanah, bakteri ini dapat hidup selama 6-14 minggu” (Radji, 2011:183).
Tabel 2.1 Faktor-faktor yang mempengaruhi pertumbuhan
Staphylococcus aureus
Atmosfer Aerobik Anaerobik hingga
aerobik
Natrium Klorida 0,4-0,5% 0-20%
Adam dan Moss (1995) dalam Anonim 2011
4. Penyakit
Berbagai jenis bakteri hidup sebagai flora normal pada kulit manusia,
sebagian besar adalah bakteri gram-positif. Staphylococcus aureus adalah jenis patogen yang dapat menimbulkan infeksi dan kelainan pada kulit.
Staphylococcus aureus menyebabkan berbagai jenis infeksi pada kulit seperti seperti bisul dan furonkolosis; seperti pneumonia, mastitis dan
meningtis; dan infeksi pada saluran urine. “Staphylococcus aureus juga menyebabkan infeksi kronis, seperti osteomielitis dan endokarditis. Staphylococcus aureus merupakan salah satu penyebab utama infeksi nosokomial akibat luka tindakan operasi dan pemakaian alat-alat perlengkapan perawatan di rumah sakit” (Radji, 2011:184-185). Dalam kondisi normal bakteri sehat dan normal, bakteri ini tidak dapat
menginfeksi karena adanya antibodi dalam tubuh, infeksi biasanya dipicu
oleh luka luar atau penetrasi bakteri melalui makanan yang tercemar.
Infeksi pada kulit atau luka luar biasanya berakibat pada penanahan, area
infeksi berwarna merah, bengkak dan terasa sakit bila disentuh (Ahira,
Infeksi Staphylococcus aureus dapat menyerang setiap bagian tubuh.
Staphylococcus aureus dapat tinggal sementara di daerah kulit basah dan dimiliki oleh 20-50% manusia. Infeksi Staphylococcus aureus biasanya terjadi pada luka terbuka atau luka potong (Radji, 2011).
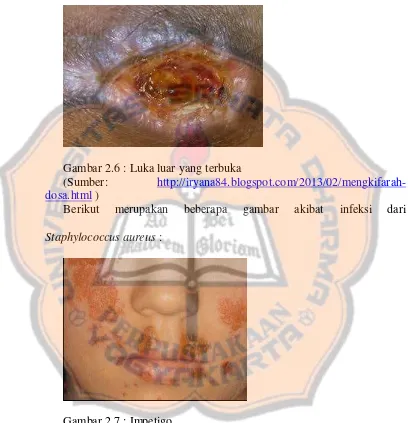
Gambar 2.6 : Luka luar yang terbuka
(Sumber: http://iryana84.blogspot.com/2013/02/mengkifarah-dosa.html )
Berikut merupakan beberapa gambar akibat infeksi dari
Staphylococcus aureus :
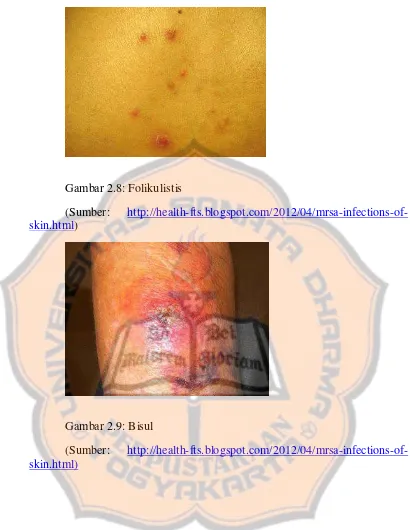
Gambar 2.7 : Impetigo
Gambar 2.8: Folikulistis
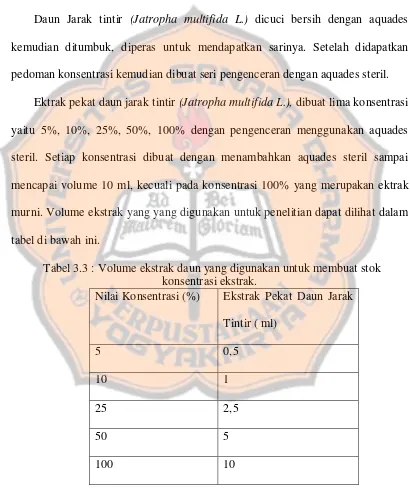
(Sumber: http://health-fts.blogspot.com/2012/04/mrsa-infections-of-skin.html)
Gambar 2.9: Bisul
D. Kerangka Pemikiran
Berdasarkan latar belakang dapat disusun kerangka pemikiran yang disajikan
pada bagan berikut ini :
Luka luar yang berdarah
Bakteri
Staphylococcus aureus
Jarak Tintir (Jatropha multifida L.)
Flavonoid, alkaloid, Saponin, Tanin
Uji aktivitas antibakteri Metode Kirby-Bauer dan
Dilusi Padat
23
BAB III
METODE PENELITIAN
A. Jenis Penelitian
Jenis dari penelitian ini adalah penelitian eksperimen. “Penelitian eksperimen adalah penelitian dimana ada perlakuan (treatment) terhadap variabel perlakuan, penelitian eksperimen dapat memberikan penjelasan tentang hubungan sebab akibat yang bisa diketahui oleh peneliti yang dimungkinkan untuk melakukan treatment terhadap objek penelitian” (Kountur, 2003:116).
B. Subjek dan Objek Penelitian
Objek penelitian adalah bakteri biakan murni Staphylococcus aureus yang diperoleh dari Fakultas Kedokteran Hewan, Universitas Gajah Mada Yogyakarta.
Subjek Penelitian adalah getah dan ekstrak daun Jarak Tintir (Jatropha multifida L.) Daun dan getah Jarak Tintir diambil di kebun tanaman obat Kampus III Universitas Sanata Dharma.
C. Definisi Operasional
Getah dari Jarak Tintir (Jatropha multifida L.) adalah getah yang didapat dari tangkai daun yang dipangkas dari batang pohonnya, getah disuling dengan
didekatkan dengan bunsen. Ekstrak daun Jarak Tintir (Jatropha multifida L.)
adalah ekstrak yang terbuat dari daun Jarak Tintir yang bagus dan tidak berlubang.
Ekstrak dibuat dengan cara ditumbuk dengan mortar, kemudian diperas sarinya
Penghambatan pertumbuhan Staphylococcus aureus dapat dilihat dari zona hambat di sekeliling paper disc yang sudah diberi getah atau ekstrak daun Jarak Tintir (Jatropha multifida L.) yang mengandung α-amirin, kampesterol, 7 α-diol,
stigmaterol, β-sitosterol, HCN, alkaloid, saponin, flavonoid dan tannin, adanya zat
tersebut yang dapat menghambat pertumbuhan bakteri. Kadar MIC dapat dilihat
dari konsentrasi terkecil perlakuan yang dapat menghambat pertumbuhan bakteri
pada media kultur dan Kadar MBC dapat dilihat dari konsentrasi perlakuan yang
tidak dapat ditumbuhi bakteri MBC didapat melalui uji penegasan streak plate.
D. Desain Penelitian
Desain dari penelitian ini menggunakan desain rancangan acak lengkap
(RAL). RAL dijadikan pilihan dalam penelitian ini karena penelitian dilakukan di
laboratorium jadi lingkungan dianggap homogen.
1. Metode Pengujian Aktivitas Antibakteri
Metode yang digunakan dalam pengujian antibakteri adalah Metode
modifikasi Kirby-Bauer. Dalam Cappuccino (2008) metode ini menggunakan
paper disc atau cakram yang disterilkan. Paper disc dengan ukuran yang sama dengan konsentrasi antibiotik yang berbeda-beda diletakkan pada media agar yang
akan bereaksi dengan bakteri yang diuji. Dari metode ini akan diketahui zona
hambat yang terlihat pada media yang mengelilingi paper disc. Untuk mengetahui kemungkinan sebab akibat antar variabel maka terdapat tujuh perlakuan yang
sebagai kontrol positif. Banyaknya pengulangan menggunakan pengulangan yang
diperoleh dari Gomes (1995) dalam (Bewiska,2009) :
8(r-1) ≥ 20
8r-8 ≥ 20
r ≥ 28/8
r ≥ 3,5
keterangan :
T : jumlah perlakuan
R : jumlah replikasi
Berdasarkan penghitungan di atas, maka jumlah pengulangan yang
dilakukan digenapkan menjadi 3 pengulangan.
2. Metode Pengujian MIC dan MBC
MIC adalah konsentrasi minimum suatu ekstrak yang diperlukan untuk
menghambat pertumbuhan bakteri, MIC atau (Minimum Inhibittory Concentration) sering disebut dengan KHM atau Kadar Hambat Minimum. MBC adalah konsentrasi minimum suatu ekstrak yang diperlukan untuk membunuh
bakteri, MBC atau (Minimum Bactericidal Concentration) sering disebut dengan KBM atau Kadar Bunuh Minimum. Pada pengujian MIC dan MBC ini
menggunakan metode dilusi padat (solid dilution test). Metode dilusi padat dalam Pratiwi (2008) dilakukan dengan cara melakukan seri pengenceran agen
a. Pengujian MIC (Minimum Inhibitory Concentration)
Membuat seri pengenceran bakteri uji, menyiapkan dan 9 tabung reaksi yang
berisi 9 ml aquades steril. Pengenceran 10-1 dibuat dengan cara mengambil 1 ml
suspensi bakteri uji yang sudah diaktifasi dan dimasukkan ke dalam tabung reaksi
yang sudah berisi 9 ml aquades steril, lalu di homogenkan dengan vortex. Untuk
pengenceran 10-2, mengambil 1 ml dari suspensi bakteri pada tabung pengenceran
10-1 tadi kemudian dimasukan ke dalam tabung reaksi lain yang juga berisi 9 ml
aquades steril, begitupun pengenceran pada seri pengencerean 10-3 sampai 10-8.
Biakan bakteri yang bisa dipakai dalam uji aktivitas adalah biakan bakteri pada
seri pengenceran 10-6 – 10-8 cfu/ml.
Inokulasi bakteri dilakukan dengan metode pour plate. Penentuan nilai MIC ditentukan dengan melihat kadar terkecil dimana konsentrasi ekstrak menghambat
pertumbuhan bakteri pada media dilusi agar padat. Hasil MIC bisa dilihat setelah
di incubator selama 24 jam dengan suhu 370C.
b.Pengujian MBC (Minimum Bactericidal Concentration)
Penentuan Nilai MBC dimulai dengan mengamati media agar pada
masing-masing konsentrasi dan memilih dua diantaranya yang terlihat paling bening atau
terlihat tidak ditumbuhi bakteri, kemudian dilakukan uji penegasan untuk
menentukan MBC, dari uji penegasan barulah didapatkan MBC.
E. Variabel Penelitian
Variabel dalam penelitian ini adalah :
1. Variabel bebas
Variabel bebas dalam penelitian ini adalah konsentrasi ekstrak daun dan
2. Variabel terikat
Variabel terikat dalam penelitian ini adalah diameter zona hambat pada
paper disc.
F. Populasi dan Sampel
Populasi dalam penelitian ini adalah tanaman Jarak tintir (Jatropha multifida L.) yang terdapat pada Kebun Tanaman Obat Kampus III Universitas Sanata Dharma dan Ngekong, Gayamharjo, Prambanan, Sleman. Sedangkan untuk
sampel dari penelitian ini adalah getah Jarak tintir (Jatropha multifida L.) dan daun Jarak tintir (Jatropha multifida L.).
G. Waktu dan Tempat Penelitian
Penelitian ini dilakukan pada bulan Juni - Juli 2013, di Laboratorim
Pendidikan Biologi, Jurusan Pendidikan Matematika dan IPA, Fakultas Keguruan
dan Ilmu Pendidikan, Universitas Sanata Dharma Yogyakarta dan Laboratorium
Fakultas Farmasi Universitas Sanata Dharma Yogyakarta .
H. Alat dan Bahan Penelitian
Peralatan yang digunakan dapat dilihat pada Tabel 3.1
Tabel 3.1 Daftar Alat Penelitian
No. Nama Alat Jumlah
1. Cawan Petri 40 buah
2. Beker Glass 1 L 1 buah
3. Paper disc 100 buah
5. Tabung Reaksi 20 buah
15. Sarung tangan Latex Secukupnya
16. Vortex 1 buah
24. Microbacterial Safety Cabinet 1 unit
25. Kertas Payung Secukupnya
33. Bunsen 3 buah
34. Perferator 1 buah
35. Kulkas 1 buah
36. Pinset 1 buah
37. Penjepit 1 buah
Bahan-bahan dalam penelitian dapat dilihat pada Tabel 3.2
No. Nama Bahan Jumlah
1. Nutrient Agar Oxoid 50 Gram
2. Aquades steril 1 Liter
3. Aquades 3 Liter
4. Daun Jarak Tintir Secukupnya
5. Getah Jarak Tintir Secukupnya
6. Ethanol 96% 1 Liter
7. Biakan murni Staphylococcus aureus
1 tabung
8. Povidone iodine 10 % 50 ml
I. Langkah-langkah Penelitian
Penelitian ini terbagi menjadi 3 tahap yaitu, tahap persiapan, tahap
pelaksanaan, tahap perlakuan.
1. Tahap Persiapan
Tahap persiapan adalah tahap inventaris alat dan bahan yang dibutuhkan
dalam penelitian. Pengumpulan bahan ekstrak dari Kebun Obat dengan cara
pengambilan daun yang dalam kondisi baik untuk digunakan dalam penelitian.
2. Tahap Pelaksanaan a. Sterilisasi
Sterilisasi dalam mikrobiologi adalah suatu proses untuk mematikan semua
organisme yang terdapat pada atau di dalam suatu benda (Hadioetomo,1985 dalam
Dewi 2010). Pratiwi (2008) menyampaikan bahwa metode sterilisasi panas
merupakan metode yang paling dapat dipercaya dan banyak digunakan. Metode
sterilisasi panas dengan uap air disebut metode sterilisasi panas basah. Sterilisasi
panas basah menggunakan temperatur di atas 1000C dilakukan dengan uap yaitu
autoklaf. Alat-alat yang akan digunakan dalam penelitian ini harus disterilkan, hal ini ditujukan agar alat-alat yang digunakan steril dari mikroba sehingga tidak
mengkontaminasi media atau kultur. Sterilisasi dilakukan pada alat-alat yang
berbahan kaca, alat-alat tersebut disterilkan dengan menggunakan autoklaf. Sterilisasi dilakukan pada tekanan 1 atm, suhu 1210C selama 15 menit. Media NA
yang akan digunakan untuk mengkulturkan bakteri juga harus dalam kondisi
steril, perlakuanya sama dengan sterilisasi alat hanya lama waktu autoklafnya
yang berbeda jika alat selama 15 menit, untuk sterilisasi media cukup dengan 10
menit. Untuk alat-alat yang tidak tahan panas dapat disterilisasi dengan
penyemprotan alkohol atau pembakaran dengan bunsen.
b. Ekstraksi Daun dan Penyulingan Getah
1) Ekstraksi Daun
Ekstraksi merupakan proses pengambilan sari yang berkhasiat atau zat tertentu
yang ada pada tanaman herbal atau hewan. Menurut Voigt (1995) ekstraksi
adalah kegiatan penarikan kandungan kimia yang dapat larut sehingga terpisah
untuk menyari diantaranya air, ester, dan campuran etanol dengan air (Voight,
1995). Ektraksi biasanya dilakukan dengan melarutkan bahan yang akan dibuat
substrat dengan pelarut tertentu. Tujuan dari dilakukannya ekstraksi adalah
mendapatkan komponen kimia yang diperoleh dari bahan.
a)Pembuatan Ekstrak Daun Jarak tintir (Jatropha multifida L.)
Daun Jarak tintir (Jatropha multifida L.) dicuci bersih dengan aquades kemudian ditumbuk, diperas untuk mendapatkan sarinya. Setelah didapatkan
pedoman konsentrasi kemudian dibuat seri pengenceran dengan aquades steril.
Ektrak pekat daun jarak tintir (Jatropha multifida L.), dibuat lima konsentrasi yaitu 5%, 10%, 25%, 50%, 100% dengan pengenceran menggunakan aquades
steril. Setiap konsentrasi dibuat dengan menambahkan aquades steril sampai
mencapai volume 10 ml, kecuali pada konsentrasi 100% yang merupakan ektrak
murni. Volume ekstrak yang yang digunakan untuk penelitian dapat dilihat dalam
tabel di bawah ini.
Tabel 3.3 : Volume ekstrak daun yang digunakan untuk membuat stok konsentrasi ekstrak.
Nilai Konsentrasi (%) Ekstrak Pekat Daun Jarak
Tintir ( ml)
5 0,5
10 1
25 2,5
50 5
2) Penyulingan Getah
Getah didapatkan dengan memotong tangkai daun dan memisahkannya dari
batang sehingga didapatkan getah Jarak tintir (Jatropha multifida L.) selain itu bisa juga dengan memotong batang yang muda dimana banyak terdapat getah.
Dalam menyuling getah diusahakan agar tidak terkontaminasi. Volume getah
yang digunakan untuk penelitian dapat dilihat dalam tabel di bawah ini.
Tabel 3.5 : Volume getah yang digunakan untuk membuat stok konsentrasi getah.
Nilai Konsentrasi (%) Getah Jarak Tintir ( ml)
5 0,5
10 1
25 2,5
50 5
100 10
c. Pembuatan Media Kultur Bakteri
“Media mempengaruhi ukuran zona melalui efeknya terhadap kecepatan pertumbuhan organisme, kecepatan difusi obat antimikroba, dan aktivitas obat. Penggunaan media harus sesuai dengan metode tersebut “(Vandepitte, 2011 :112). Media yang akan digunakan untuk mengkulturkan bakteri Staphylococcus aureus adalah media NA, sebelum sterilisasi dilakukan pengukuran pH terhadap media kultur. Bila belum sesuai pengaturan pH bisa dilakukan dengan
penambahan HCl atau NaOH. NA Oxoid dipanaskan dengan pemanas
dicampurkan pada aquades dengan perbandingan, 500 :10 yaitu untuk membuat
NA sebanyak 500 ml maka memerlukan Nutrient agar oxoid sebanyak 10 gram.
NA tidak bisa langsung digunakan melainkan harus disterilkan terlebih dahulu
dengan autoklaf. Media NA pada cawan petri yang digunakan sebagai media
kultur untuk menguji aktivitas antibakteri berisi masing-masing 10 ml. Sedangkan
media yang akan digunakan sebagai media kultur bakteri agar miring pada tabung
reaksi adalah masing-masing 5 ml. Media NA agar miring digunakan untuk
meremajakan bakteri biakan murni.
3. Tahap Perlakuan
a. Pengujian Aktivitas Antibakteri dengan Media Difusi Agar
Metode difusi agar spread plate secara aseptis digunakan untuk mengetahui aktivitas antibakteri. Media NA steril sebanyak 10 ml dalam cawan petri di
inokulum bakteri sebanyak 0,5 ml. Inokulum yang dipakai adalah inokulum pada
konsentrasi 10-8cfu/mL. Setelah inokulum dimasukkan maka inokulum diratakan
menggunakan batang L, perlakuan ini juga dilakukan dengan aseptis. Area cawan
petri dibagi menjadi 3 kuadran, yang terdiri dari kontrol negatif, kontrol positif,
dan perlakuan, hal ini dilakukan agar tidak terjadi tumpang tindih pertumbuhan
atau penghambatan bakteri. Paper disc yang sudah direndam selama 10 menit
dalam ekstrak konsentrasi tertentu dimasukan ke dalam media yang sudah
diinokulum, paper disc diambil menggunakan pinset dibiarkan sesaat sebelum
dimasukkan ke dalam cawan petri sehingga dapat berdifusi ke dalam media
sekitarnya. Selanjutnya media tersebut di inkubasikan selama 1 hari (24 jam)
dalam incubator dengan suhu 370C, setelah itu dilihat dan diukur diameter zona
hambat yang mengelilingi paper disc tersebut dengan jangka sorong. Pada suhu
370C karena pada suhu tersebut tidak mengalami perpanjangan fase lag pada
pertumbuhan bakteri dan viabilitas bakteri tidak menurun. Selama 24 jam karena
antibakteri pada pertumbuhan bakteri, biasanya terlihat lebih bening daripada
daerah sekitarnya. Ukuran zona jernih tergantung kepada kecepatan difusi
antimikroba, derajat sensitifitas, mikroorganisme dan kecepatan pertumbuhan
bakteri (Anonim, 2011). Keefektifan ekstrak dilihat dari zona hambat yang
didapat.
b. Pengujian Nilai MIC atau KHM
Ada dua macam metode dilusi yaitu metode dilusi cair dan metode dilusi
padat. Pada penelitian ini menggunakan metode dilusi padat. Konsentrasi ekstrak
daun dan getah jarak tintir adalah 5%, 10%, 25%, 50%, 100%, ditambah 1
kelompok kontrol positif, kontrol negatif, dan kontrol media. Konsentrasi minimal
yang di dapat dari uji aktivitas digunakan sebagai acuan untuk menentukan
konsentrasi yang akan digunakan dalam pengujian nilai MIC atau KHM.
Pengujian dilakukan dengan metode dilusi padat, metode ini dilakukan dengan
cara penanaman bakteri secara pourplate atau cawan tuang. Prosedur pourplate
adalah dengan mendinginkan media kultur yang sudah disterilkan dalam tabung
reaksi sampai dengan suhu 450C, kemudian dituangkan ke dalam cawan petri
yang sudah berisi mikroba uji dan sampel ekstrak (Cappuccino,2008). Media
kultur yang digunakan adalah 10 ml, sedangkan bakteri uji yang digunakan adalah
bakteri uji pada konsentrasi 10-8cfu/mL yang di vortex dahulu sebelum digunakan
sebanyak 0,5 ml sampel ekstrak sebanyak 0,5 ml. Setelah pourplate dilakukan langkah selanjutnya adalah menginkubasinya selama 24 jam dalam suhu 370C,
penentuan nilai MIC atau KHM dilihat dari konsentrasi terendah yang medianya
c. Pengujian MBC atau KBM
Metode streak dengan cottonbude steril dilakukan untuk menegaskan nilai
MBC yang diperoleh dari media yang digunakan dalam uji MIC. Metode
streakplate dilakukan dengan cara menggoreskan bakteri uji pada permukaan
media agar menggunakan jarum ose yang dibagi menjadi 3 kuadran, kerapatan
goresan pada masing-masing kuadran berbeda berturut rapatnya mulai dari
kuadran pertama hingga kuadran ketiga.
Setelah di dapatkan nilai MIC atau KHM langkah selanjutnya adalah memilih
2 konsentrasi paling besar dalam uji MIC atau KHM yang mampu menghambat
pertumbuhan bakteri , hal tersebut di tandai dengan media yang tidak ditumbuhi
oleh bakteri. Dua media paling jernih dibandingkan dengan menstreakan cotton
bud steril pada media kultur baru kemudian diinkubasi selama 24 jam dalam suhu
370C, media kultur yang tidak ditumbuhi bakteri tersebutlah yang menjadi MBC
atau KBM.
J. Analisis Data
Analisis data dalam penelitian ini dilakukan menggunakan dengan program
SPSS. Untuk mendapatkan data awal maka dilakukan uji normalitas dan uji
homogenitas. “Uji normalitas untuk mengetahui normalitas distribusi data, jika jumlah data cukup banyak dan penyebarannya tidak 100% normal, maka kesimpulan yang ditarik berkemungkinan salah” (Irianto, 2004: 273). Uji homogenitas adalah pembandingan data yang sejenis.
Untuk mengetahui adanya pengaruh ekstrak yang diuji terhadap pertumbuhan
melakukan analisa Post Hoc untuk uji Kruskal Wallis adalah Uji Mann-Whitney (Dahlan, 2009). Uji regresi linier dilakukan untuk mengetahui pengaruh
37
BAB IV
HASIL PENELITIAN DAN PEMBAHASAN
A. Hasil Penelitian
1. Identifikasi Tanaman Jarak Tintir (Jatropha multifida L.)
Diketahui ciri-ciri tanaman Jarak Tintir (Jatropha multifida L.) yaitu memiliki buah berbiji. Mula-mula berwarna hijau akan berubah menjadi
berwarna kuning selanjutnya berwarna hitam namun tidak pecah atau
merekah. Ranting tebal, gundul dan berair, panjang daun 5-15 cm dan 6-16
cm, memiliki 3-5 sudut, dan panjang tangkai daun 3,5 – 15 cm sampai 30
cm serta memiliki ujung runcing. Kelopak bunga berwarna merah,
berbentuk lonjong, panjangnya 6-7 cm dan memiliki 3 rusuk yang
membujur. Ciri-ciri tanaman Jarak Tintir (Jatropha multifida L.) yang diperoleh dari Kebun Obat Kampus III Universitas Sanata Dharma dan
Ngekong, Gayamharjo, Prambanan, Sleman yang digunakan dalam
penelitian sesuai dengan kunci determinasi Flora of Java (Backer, 1965)
2. Ekstrak Daun dan Getah Jarak Tintir (Jatropha multifida L.) a. Ekstrak Daun Jarak Tintir (Jatropha multifida L.)
Dalam pengambilan sampel memerlukan cara dan penanganan khusus
pada masing-masing bahan. Karena setiap bahan yang akan digunakan
mempunyai karakteristik dan perlakuan masing-masing. Cara pengolahan
dan pengambilan diketahui bahwa daun (Folium) diambil yang tua (bukan
daun kuning) dan daun kelima dari pucuk. Daun dipetik satu persatu