Penelitian mengenai obat baru banyak dilakukan dalam upaya pengembangan obat. Banyak tanaman asli Indonesia yang biasa digunakan dalam pengobatan herbal, berpotensi sebagai senyawa penuntun dalam upaya pengembangan obat di masa kini. Salah satunya adalah tanaman kunyit (Curcuma longa L.) yang digunakan secara luas dalam produk jamu tradisional. Rimpang kunyit diketahui memiliki kandungan aktif kurkumin yang telah banyak diteliti memiliki aktivitas sebagai antioksidan, antiinflamasi, (Majeed et al., 1995), antivirus (Mazumder et al., 1997), dan antibakteri (Kumar et al., 2001; Chattopadhyay et al., 2004).
Sampai saat ini, kurkumin telah dikembangkan menjadi berbagai senyawa analognya. Hal ini dilakukan karena absorbsi kurkumin di dalam tubuh sangat kecil pada pemberian intraperitonial (Pan et al., 1999) dan oral, sehingga efek biologis yang ditimbulkan menjadi lebih rendah. Tetrahidrokurkumin (THC) diketahui merupakan metabolit kurkumin yang memiliki aktivitas antioksidan lebih kuat dibandingkan kurkumin secara in vitro (Sugiyama et al., 1996). Berdasarkan fakta tersebut, penelitian tentang kurkumin dan metabolitnya terus dilakukan untuk memperoleh senyawa baru yang memiliki aktivitas biologis yang lebih baik.
Penelitian untuk mensintesis senyawa analog kurkumin di Fakultas Farmasi UGM telah dilakukan dan dihasilkan 3 seri molekul yang digolongkan
berdasarkan struktur cincin tengahnya yaitu Heksagamavunon (HGV), Pentagamavunon (PGV), dan Gamavuton (GVT) (Sardjiman et al., 2003). Senyawa hasil modifikasi kurkumin tersebut diantaranya adalah senyawa pentagamavunon-0 (PGV-0) dan pentagamavunon-1 (PGV-1). PGV-0 diketahui memiliki aktivitas sebagai aktivitas antioksidan yang lebih baik dibandingkan dengan kurkumin (Sardjiman et al., 1997). Studi farmakokinetika menunjukkan bahwa PGV-0 memiliki profil dalam darah yang fluktuatif, terutama pada pemberian oral (Hakim dkk., 2004), sehingga dikembangkan menjadi senyawa Tetrahidropentagamavunon-0 (THPGV-0).
Ritmaleni dan Simbara (2010) telah berhasil mensintesis senyawa THPGV-0 dengan metode hidrogenasi menggunakan katalis paladium karbon (Pd/C) 10%. THPGV-0 diketahui memiliki aktivitas antioksidan yang lebih baik dibandingkan dengan PGV-0 (Simbara, 2009). Metode yang sama digunakan oleh Andhini (2012) untuk mereduksi senyawa PGV-1 menjadi THPGV-1. Penelitian mengenai aktivitas antioksidan senyawa THPGV-1 juga telah dilakukan, dan diketahui bahwa senyawa THPGV-1 memiliki aktivitas antioksidan yang lebih baik dibandingkan dengan PGV-1 (Utama, 2012).
Sampai saat ini, penelitian terus dilakukan untuk mendapatkan analog metabolit kurkumin. Dari seri heksagamavunon (HGV) telah berhasil disintesis senyawa tetrahidroheksagamavunon-5 (THHGV-5) (Wibowo, 2013), dan tetrahidroheksagamavunon-7 (THHGV-7) (Praditya, 2014), sedangkan dari seri gamavuton (GVT) yaitu senyawa 1,5-bis-(4'-triflorometilfenil)-pentan-3-on (THC7) (Abimantranahita, 2014).
Pengembangan lebih lanjut dilakukan pada senyawa pentagamavunon-5 (PGV-5). PGV-5 memiliki kemiripan struktur dengan senyawa HGV-5. Dengan analogi tersebut, maka besar kemungkinan PGV-5 dapat direduksi menjadi tetrahidropentagamavunon-5 (THPGV-5) melalui reaksi hidrogenasi dengan katalis paladium karbon serta diprediksi mampu memberikan aktivitas antioksidan yang lebih baik dibandingkan PGV-5.
B. Rumusan Masalah
1. Apakah senyawa THPGV-5 dapat disintesis dari starting material PGV-5 melalui reaksi hidrogenasi dengan katalis paladium karbon? 2. Apakah senyawa THPGV-5 memiliki aktivitas sebagai antioksidan
yang lebih baik dibandingkan senyawa PGV-5 jika diuji dengan metode daya tangkap radikal DPPH dan daya reduksi ion feri ?
C. Pentingnya Penelitian Diusulkan
Penelitian ini bermanfaat untuk pengembangan senyawa analog kurkumin yang aman, stabil, memiliki aktivitas biologis yang lebih baik dan spesifik dibandingkan kurkumin itu sendiri, serta untuk mendapatkan senyawa antioksidan baru dari analog kurkumin.
D. Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui apakah senyawa Tetrahidropentagamavunon-5 (THPGV-5) dapat disintesis dari starting material Pentagamavunon-5 (PGV-5) melalui reaksi hidrogenasi (reduksi) dengan menggunakan katalis paladium karbon (Pd/C) dalam pelarut metanol. Penelitian
ini juga bertujuan untuk mengetahui aktivitas antioksidan senyawa Tetrahidropentagamavunon-5 (THPGV-5) hasil sintesis.
E. Tinjauan Pustaka
1. Hidrogenasi dengan Katalis Paladium Karbon
Katalis paladium merupakan salah satu katalis logam yang sering digunakan dalam reaksi reduksi. Katalis paladium karbon telah banyak digunakan pada industri manufaktur kefarmasian sebagai katalis hidrogenasi pada berbagai macam reaksi. Pada dasarnya katalis ini terdiri dari karbon aktif berukuran 200 mesh yang diimpregnasi dengan larutan garam paladium yang kemudian tereduksi menjadi bentuk logam (Chaston and Sercombe, 1961). Kandungan paladium di dalam karbon tersedia dalam berbagai konsentrasi. Salah satu konsentrasi yang biasa digunakan adalah paladium dalam karbon 10%. Katalis paladium karbon 10% telah banyak digunakan dalam sintesis berbagai macam senyawa, beberapa contohnya adalah sintesis THPGV-0 yang merupakan analog metabolit kurkumin (Ritmaleni dan Simbara, 2010)
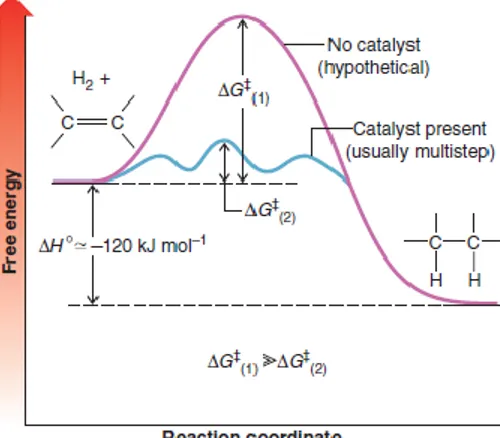
Hidrogenasi adalah suatu reaksi kimia dengan menambahkan atom hidrogen ke dalam suatu senyawa tertentu. Hidrogen yang ditambahkan dapat mereduksi ikatan rangkap dua maupun ikatan rangkap tiga dalam suatu senyawa hidrokarbon. Reaksi hidrogenasi umumnya mempunyai energi aktivasi yang tinggi. Hidrogenasi alkena tidak dapat dilakukan pada suhu kamar tanpa adanya katalis, tetapi dengan adanya katalis logam dapat dilakukan pada suhu kamar. Katalis menyediakan cara baru hidrogenasi dengan energi aktivasi yang lebih rendah seperti terlihat pada gambar 1 (Solomons and Fryhle, 2011).
Gambar 1. Diagram energi bebas dari hidrogenasi alkena pada keberadaan katalis dan reaksi hipotetik tanpa adanya katalis (Solomons and Fryhle, 2011)
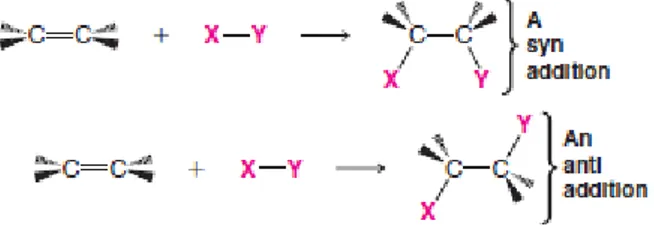
Katalis yang sangat umum digunakan untuk hidrogenasi adalah paladium, nikel, rodium, dan rutenium yang ternyata membantu mengadsorbsi molekul hidrogen pada permukaannya. Reaksi antara hidrogen dengan katalis logam terjadi dimana elektron tak berpasangan dari permukaan logam berikatan dengan elektron hidrogen, dan mengikat hidrogen di permukaan. Penggabungan antara alkena dengan permukaan yang mengadsorbsi hidrogen menyebabkan adsorbsi alkena terjadi dengan baik. Tahapan transfer atom hidrogen terjadi, dan menghasilkan alkana sebelum molekul organik meninggalkan permukaan katalis. Konsekuensinya, kedua atom hidrogen ditambahkan dari sisi yang sama dari molekul yang disebut adisi sin (syn addition ). Sebaliknya, jika penambahan hidrogen dalam posisi yang berlawanan disebut anti adisi (gambar 3) (Solomons and Fryhle, 2011).
Gambar 2. Mekanisme hidrogenasi alkena dengan katalis logam
(a) adsorbsi hidrogen; (b) adsorbsi alkena; (c,d) transfer atom hidrogen pada permukaan alkena (Solomons and Fryhle, 2011)
Gambar 3. Syn addition dan anti addition (Solomons and Fryhle, 2011)
2. Hidrogenasi Kurkumin dan Turunannya
Kurkumin merupakan senyawa yang tidak larut dalam air, tetapi larut dalam pelarut organik. Stabilitas kurkumin berada pada pH di bawah 6,5 dan kurkumin terdekomposisi pada pH netral hingga pH basa. Oleh karena itu kurkumin menjadi stabil pada saluran pencernaan dimana pH disana berada pada kisaran di bawah 6,5(Wang et al., 1997).
14
Gambar 4. Struktur Senyawa Kurkumin
Penelitian mengenai biotransformasi kurkumin telah dilakukan. Dari penelitian tersebut, diketahui bahwa salah satu metabolit kurkumin adalah
Tetrahidrokurkumin (THC). THC berhasil disintesis melalui reduksi hidrogenasi kurkumin menggunakan katalis PtO2 (Pan et al., 1999).
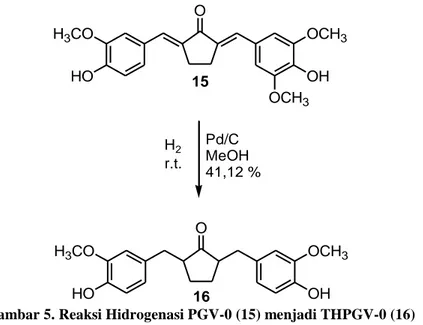
Tetrahidropentagamavunon-0 (THPGV-0) merupakan salah satu analog dari THC (metabolit kurkumin). Sintesis senyawa THPGV-0 telah dilakukan dengan menggunakan berbagai macam katalis (Ritmaleni et al., 2013).
O OCH3 OH OCH3 HO H3CO O OCH3 OH HO H3CO Pd/C MeOH 41,12 % H2 r.t. 15 16
Gambar 5. Reaksi Hidrogenasi PGV-0 (15) menjadi THPGV-0 (16)
Proses hidrogenasi PGV-0 tidak hanya membentuk THPGV-0 tapi juga membentuk 3 produk samping yang telah berhasil diidentifikasi (Ritmaleni et al., 2013). Penelitian lebih lanjut telah dilakukan di Fakultas Farmasi UGM dan berhasil melakukan sintesis analog metabolit kurkumin menggunakan metode hidrogenasi dengan katalis paladium karbon 10%. Keberhasilan dari metode tersebut, terangkum dalam tabel I.
Tabel I. Daftar senyawa hasil hidrogenasi dengan katalis paladium/karbon Senyawa Starting material Rendemen Jarak
Lebur Sumber THPGV-0 PGV-0 24,52 %. 122,2-123,4ºC (Ritmaleni dan Simbara, 2010) THPGV-1 PGV-1 18 % 139,8-142,6ºC (Andhini, 2012) THHGV-5 HGV-5 23,03 %. 139,1-139,8ºC (Wibowo, 2013) THHGV-7 HGV-7 19,21 %. 161,3-162,1ºC (Praditya, 2013) 1,5-bis-(4'-triflorometilfenil) -pentan-3-on (THC7) 1,5-bis-(4'- triflorometilfenil)- penta-1,4-dien-3-on (C7) 27,53 % 166,8-168,5°C (Abimantranahita, 2014) 3. Pentagamavunon-5 (PGV-5)
Pentagamavunon-5 (PGV-5) atau 2,6-bis-(4'-hidroksi-3',5' dimetoksi-benzilidin)-siklopentanon merupakan senyawa analog kurkumin lainnya yang telah disintesis dari senyawa 4-hidroksi-3,5-dimetoksibenzaldehid. PGV-5 dengan rumus molekul C23H24O7 memiliki jarak lebur sebesar 226-227 ºC. PGV-5
merupakan salah satu senyawa yang memiliki aktivitas antioksidan dari turunan siklopentanon (Sardjiman et al., 1997). Struktur senyawa PGV-5 terlihat seperti pada gambar 6.
17
4. Kromatografi Lapis Tipis (KLT)
KLT merupakan metode yang telah banyak digunakan dalam analisis kualitatif dan kuantitatif. Kromatografi berarti metode analisis dimana fase gerak melewati fase diam dalam sebuah sistem, dimana senyawa dipisahkan dari komponennya. KLT dikenal sebagai kromatografi dengan fase diam berada pada sebuah lempeng tipis. Kondisi yang harus dipenuhi dalam KLT yaitu senyawa atau campuran yang akan dianalisis harus larut pada solven atau tercampur pada solven/pelarut. Salah satu contoh penggunaan KLT dalam analisis yaitu pada deteksi bioautografi yang merupakan metode deteksi mikroba yang digabungkan dengan teknik kromatografi planar. Metode ini didasarkan pada struktur antimikroba atau antifungi yang berada pada senyawa yang dianalisis (Choma and Grzelak, 2010).
Kromatografi lapis tipis juga telah dikembangkan dalam pemisahan dan determinasi produk alam dalam campuran yang kompleks dalam produk tanaman. Untuk kontrol kualitas produk herbal, KLT merupakan teknik yang paling disarankan untuk identifikasi material kasar. Kemudian KLT merupakan metode penting untuk analisis kualitatif dari produk tumbuhan karena memiliki beberapa keuntungan, yaitu sampel dapat dianalisis secara simultan dan cepat, serta dapat diaplikasikan teknik pemisahan dan prosedur deteksi senyawa (Mohammad, et al.,2010). Wang et al. (2012), melaporkan bahwa banyak penggunaan teknik KLT dalam analisis kualitatif maupun kuantitatif antioksidan, dan DPPH merupakan salah satu reagen yang sering digunakan untuk tujuan tersebut. Pada tahap
skrining antioksidan, KLT bioautografi merupakan metode pilihan karena terdapat beberapa keuntungan yaitu fleksibel dan sederhana (Wang et al., 2012).
5. Kromatografi Kolom
Salah satu teknik kromatografi konvensional yang masih digunakan untuk memisahkan campuran senyawa adalah teknik kromatografi kolom. Beberapa contoh penggunaan kromatografi kolom pada tahap isolasi senyawa yaitu pada isolasi senyawa analog metabolit kurkumin, seperti THPGV-0, THHGV-5, dan THHGV-7. Senyawa THPGV-0 dan THHGV-5 mampu diisolasi dari hasil sintesis yang berupa crude product dengan kromatografi kolom pada fase gerak kloroform: etil aetat (5:1) (Simbara, 2010; Wibowo, 2013). Isolasi senyawa THHGV-7 dari crude product dilakukan dengan menggunakan metode Kromatografi Kolom yang memiliki fase diam silika pro-kromatografi kolom ukuran 200-500 μm dan fase gerak campuran pelarut n-heksana:diklorometana (5:3) (Praditya, 2014).
6. Jarak Lebur
Jarak lebur merupakan salah satu parameter kemurnian suatu senyawa organik berwujud padat dan dapat digunakan juga sebagai parameter identifikasi suatu senyawa. Senyawa murni memiliki jarak lebur yang sempit yaitu 1-2 °C (Sharp and Rowley, 1989). Senyawa yang tidak murni atau mengandung pengotor di dalamnya memiliki titik lebur lebih rendah atau lebih tinggi dari senyawa dalam bentuk murninya, dan memiliki jarak lebur yang lebih besar.
7. Spektroskopi
Spektroskopi adalah ilmu yang mempelajari interaksi antara energi dengan materi. Ketika energi diaplikasikan terhadap suatu zat, maka bisa diabsorbsi (diserap), diemisikan, karena terdapat perubahan kimia, atau ditransmisikan. Teknik spektroskopi banyak digunakan di dalam analisis kualitatif maupun kuantitatif suatu senyawa.
a. Spektroskopi UV-Visibel
Spektroskopi UV-Visibel merupakan salah satu teknik yang sering digunakan dalam analisis kefarmasian. Dalam spektroskopi UV-Visibel dilakukan perhitungan jumlah radiasi ultraviolet atau visibel yang berhasil diabsorbsi oleh suatu senyawa di dalam larutan. Instrumen yang digunakan untuk menghitung rasio, atau fungsi rasio intensitas dari dua buah beam dari sinar pada daerah UV-Visibel yang disebut dengan Spektrofotometer UV-Visibel.
Tahun 2010, Theivarasu telah mengembangkan metode spektroskopi UV dalam analisis carvedilol dalam formulasi farmasetis. Analisis ini dilakukan pada panjang gelombang 241 nm. Metode ini telah berhasil divalidasi dan diaplikasikan untuk determinasi cardevilol dalam tablet dan diketahui tidak ada gangguan dari eksipien tablet pada panjang gelombang terpilih. Sehingga dikatakan metode ini bersifat akurat, selektif, sensitif, presisi dan reprodusibel (Theivarasu et al., 2010). Naveed et al., (2014) menggunakan teknik spektroskopi UV untuk penetapan konsentrasi furosemid (obat diuretik). Penetapan konsentrasi didasarkan pada serapan maksimal furosemid yaitu pada panjang gelombang 243 nm menggunakan pelarut air. Penelitian tersebut bertujuan untuk mengembangkan
metode spektroskopi UV menjadi lebih sederhana, ekonomis, akurat, dan sensitif (Naveed et al., 2014). Bukan hanya itu, spektroskopi UV juga digunakan dalam analisis ketokonazol dalam sediaan oral (Naveed and Jaweed, 2014).
b. Spektroskopi Inframerah
Spektroskopi inframerah merupakan metode spektroskopi yang memanfaatkan vibrasi dari suatu molekul yang tereksitasi tersebut dan menghasilkan suatu spektrum inframerah. Spektrum inframerah dapat menyediakan informasi spesifik dari gugus fungsional yang mengalami vibrasi. Instrumen yang digunakan untuk mengukur resapan adalah spektrometer inframerah. Radiasi inframerah yang digunakan untuk analisis instrumental adalah radiasi pada rentang bilangan gelombang 4000-650 cm-1. Sinyal yang terukur dapat diukur pada berbagai panjang gelombang. Salah satu metode yang sering digunakan dalam analisis kefarmasian adalah menggunakan FTIR (Fourier Transform Infrared). Dalam penelitian yang dilakukan Prasad et al., (2012) disebutkan bahwa FTIR merupakan metode yang mudah, cepat dan reprodusibel, serta waktu yang singkat dibanding dengan metode yang lain (Prasad et al., 2012). Dalam bidang klinis, Sankari et al. (2010) telah melakukan penelitian untuk mendeteksi keberadaan IgA, IgG, dan IgM dalam sampel serum darah normal dan myeloma menggunakan teknik FTIR, sehingga teknik ini dapat digunakan sebagai alat diagnosis pada sampel cairan biologis manusia (Sankari et al., 2010). Teknik yang sama digunakan Rohman dkk. (2013) dalam determinasi kuantitatif simetikon di dalam suspensi antasida dan tablet kunyah. Dalam penelitiannya dikatakan bahwa teknik spektroskopi FTIR telah berhasil divalidasi dan
dikembangkan dengan parameter linearitas, sensitivitas, akurasi, dan presisi (Rohman dkk., 2013). Teknik FTIR juga digunakan oleh Prasad et al., (2012) untuk analisis kuantitatif domperidon dalam formulasi tablet. Metode ini didasarkan pada perhitungan puncak gugus karbonil pada 1717 cm-1 serta evaluasi komponen obat yang tidak diketahui menggunakan kurva kalibrasi. Metode ini telah berhasil divalidasi untuk analisis kefarmasian dalam sediaan tablet dengan harga recovery yang tinggi (>99%) (Prasad et al.,2012).
c. Spektroskopi Massa
Spektroskopi massa secara luas telah banyak digunakan. Handelsman et al., (2013) melaporkan penggunaan teknik spektroskopi massa dalam penentuan konsentrasi steroid seksual. Menurut hasil penelitiannya disebutkan bahwa dalam penentuan konsentrasi steroid seksual, MS-based assay merupakan hal yang sangat penting untuk diiikutsertakan karena spesifisitas, dan reprodusibilitasnya (Handelsman et al., 2013) .
Untuk mengidentifikasi senyawa campuran, instrumen Spektrometer Massa dapat digabungkan dengan instrumen lain untuk pemisahan senyawa campuran, seperti Kromatografi Gas (Gas Chromatography/GC). GC juga dapat digunakan untuk melihat kemurnian suatu senyawa. Kemurnian ditunjukkan dengan hanya terdeteksi satu puncak pada kromatogram selain puncak pelarut yang digunakan. Gabungan instrumen alat ini dikenal dengan GC-MS (Gas Chromatography-Mass Spectroscopy). GC-MS merupakan alat penting untuk identifikasi dan kuantitasi dari senyawa organik volatil. Alat ini berguna untuk
determinasi dari berat molekul suatu senyawa yang tidak diketahui dalam campuran yang kompleks (Mulja dan Suharman, 1995).
8. Spektroskopi Resonansi Magnetik Inti ( Nuclear Magnetic
Resonance/NMR)
Spektroskopi NMR merupakan spektroskopi absorpsi. Suatu sampel dapat menyerap radiasi elektromagnetik pada rentang frekuensi tertentu yang tergantung dari sifat-sifat sampel. Berbeda dari spektroskopi inframerah yang berfungsi untuk mengidentifikasi gugus fungsional dari suatu senyawa organik, spektroskopi NMR dapat memberikan informasi dari suatu senyawa organik mengenai jumlah atom magnetis yang berbeda maupun memperoleh informasi mengenai sifat lingkungan langsung dari masing-masing inti atom tersebut. Informasi tersebut dapat membantu dalam identifikasi struktur suatu senyawa organik yang dipelajari (Pavia et al., 2001).
Spektroskopi NMR merupakan salah satu teknik yang paling sering digunakan untuk elusidasi struktur kimia suatu senyawa. Spektrum NMR mampu menggambarkan lingkungan kimia atom hidrogen dan karbon secara detail, dimana atom dengan lingkungan kimia yang berbeda akan muncul pada daerah yang berbeda pula secara spesifik. Selain itu pola splitting yang terdapat pada spektrum 1H-NMR mampu menggambarkan keberadaan atom tetangga yang ekuivalen. Hal ini dapat membantu untuk analisa data secara lebih meyakinkan.
Sejalan dengan semakin berkembangnya obat-obatan sintetik, teknik spektroskopi NMR menjadi andalan dalan setiap proses sintesis, dimana teknik ini merupakan teknik utama yang digunakan untuk proses elusidasi struktur senyawa
hasil sintesis. NMR juga telah dikenal untuk analisis kuantitaif untuk determinasi profil kemurnian suatu senyawa. Dalam teknologi kefarmasian, teknik ini dapat digunakan untuk meyakinkan informasi mengenai polimorfisme dari senyawa obat, konformasinya dalam tablet, dan lain sebagainya (Holzgrabe et al.,1998). Teknik spektroskopi NMR kuantitatif (qNMR) juga telah digunakan untuk validasi dan determinasi kuantitatif obat antidiabetik, Pioglitazon, dalam sediaan farmasetis. Dalam penelitian ini dikatakan bahwa teknik qNMR merupakan teknik non-destruktif dan tidak perlu adanya standar pembanding dari analit obat untuk proses kuantifikasi (Gadape and Pariks, 2011).
9. Oksidan dan Antioksidan
a. Oksidan dan Radikal Bebas
Reactive oxygen species (ROS) merupakan kelompok molekul reaktif yang dihasilkan dari metabolisme oksigen. ROS dihasilkan oleh organisme hidup sebagai hasil metabolisme seluler dan faktor lingkungan, seperti polutan atau asap rokok. ROS merupakan molekul yang reaktif dan bisa membahayakan struktur sel seperti karbohidrat, asam nukleat, lipid, dan protein serta mengganggu fungsinya. Pergeseran kesetimbangan antara oksidan dan antioksidan dikenal sebagai “oxidative stress”.
ROS endogen dihasilkan dari oksigen molekuler sebagai hasil metabolisme seluler. ROS dapat dibedakan menjadi 2 yaitu radikal bebas dan nonradikal. Molekul yang mengandung 1 atau lebih elektron tak berpasangan dan memberikan reaktivitas pada molekul disebut radikal bebas. Ketika 2 radikal bebas memberikan elektron tak berpasangan mereka, bentuk nonradikal akan
terbentuk. Tiga macam ROS yang signifikan secara fisiologis yaitu anion superoksida (O2-), radikal hidroksil (•OH), dan hidrogen peroksida (H2O2).
Selain ROS endogen, ROS juga bisa berasal dari faktor luar yang disebut ROS eksogen. ROS eksogen diantaranya: Asap rokok yang mengandung banyak oksidan dan radikal bebas seperti superoksida dan nitrit oksida, paparan ozon yang menyebabkan peroksidasi lipid, hiperoksia (kondisi dimana konsentrasi oksigen lebih dari normal), radiasi ionisasi, ion metal seperti besi, kadmium, merkuri, baja, nikel, dan arsenik yang dapat menginduksi terbentuknya radikal reaktif dan membahayakan sel (Birben et al., 2012).
b. Antioksidan
Antioksidan didefinisikan sebagai senyawa yang mampu menunda, memperlambat, atau menghambat reaksi oksidasi (Pokorny et al., 2001). Senyawa antioksidan memegang peranan penting dalam pertahanan tubuh terhadap pengaruh buruk yang disebabkan radikal bebas. Antioksidan merupakan zat kimia yang secara bertahap akan teroksidasi dengan adanya efek seperti cahaya, panas, logam peroksida atau secara langsung bereaksi dengan oksigen. Ada dua macam antioksidan, yaitu antioksidan alam dan antioksidan sintetis. Sebagai contoh α tokoferol (Vitamin E) merupakan antioksidan alam yang terdapat dalam lemak dan minyak yang diperoleh dari biji tanaman. Kurkumin adalah antioksidan alam yang lain dimana aktivitasnya lebih besar dibanding dengan α-tokoferol jika diuji dalam minyak .
Antioksidan sintetis memiliki efektivitas yang tinggi namun kurang aman bagi kesehatan sehingga penggunaannya diawasi secara ketat di berbagai negara (Pujimulyani, 2003).
Penggolongan antioksidan berdasarkan fungsinya dibedakan menjadi 5 yaitu (Purba, dan Martosupono, 2009) :
a. Antioksidan primer
Antioksidan primer berfungsi untuk mencegah terbentuknya radikal bebas baru karena antioksidan tersebut dapat merubah radikal bebas yang ada menjadi radikal yang stabil. Antioksidan ini bekerja untuk mencegah pembentukan senyawa radikal bebas baru dengan cara mengubah radikal bebas yang ada menjadi molekul yang berkurang dampak negatifnya, sebelum radikal ini sempat bereaksi. Contoh antioksidan ini adalah enzim SOD yang berfungsi sebagai pelindung hancurnya sel-sel dalam tubuh serta mencegah proses peradangan karena radikal bebas. Selenium (Se) juga berperan sebagai antioksidan.
b. Antioksidan sekunder
Antioksidan sekunder berfungsi sebagai senyawa penangkap radikal bebas serta mencegah terjadinya reaksi berantai sehingga tidak terjadi kerusakan yang lebih besar. Contoh antioksidan sekunder : Vitamin E, Vitamin C, beta karoten, likopen, bilirubin, dan albumin.
c. Antioksidan tersier
Antioksidan tersier merupakan senyawa yang memperbaiki sel-sel dan jaringan yang rusak karena serangan radikal bebas. Contoh enzim yang memperbaiki DNA pada inti sel adalah metionin sulfoksi dan reduktase. Adanya
enzim-enzim perbaikan DNA ini berguna untuk mencegah penyakit kanker dan degeneratif lainnya.
d. Oxygen scavenger
Antioksidan yang termasuk Oxygen scavenger mengikat oksigen sehingga tidak mendukung reaksi oksidasi.
e. Chelators dan seguesstrants
Chelators dan seguesstrants merupakan senyawa antioksidan yang mengikat logam yang mampu mengkatalisis reaksi oksidasi. Sebagian besar antioksidan yang digunakan dalam makanan merupakan senyawa monohidroksi dan polihidroksi fenol dengan berbagai macam subtituen pada cincinnya. Senyawa ini memiliki energi aktivasi yang rendah untuk mendonorkan hidrogen. Dengan demikian, radikal antioksidan yang dihasilkan tidak menginisiasi radikal bebas lainnya karena adanya stabilisasi dari delokalisasi elektron radikal. Propagasi dan inisiasi reaksi radikal bebas dapat dihindari atau diminimalkan dengan adanya donasi hidrogen dari antioksidan dan agen pengkelat logam. Antioksidan radikal bebas dapat pula bereaksi dengan radikal bebas lipid untuk membentuk kompleks yang stabil dan mencegahnya terjadinya kerusakan (Hamid et al.,2010).
10. Aktivitas Biologis Kurkumin dan Turunannya
Kurkumin dilaporkan memiliki aktivitas antioksidan yang poten dilihat dari struktur molekulnya (Majeed and Prakash, 2008). Pada penelitian lain, disebutkan bahwa kurkumin memiliki aktivitas penangkapan radikal DPPH. Aktivitas penangkapan radikal pada kurkumin dipengaruhi oleh adanya 2 gugus
hidroksi fenolik dan adanya gugus β-diketon. Dilihat dari strukturnya, kurkumin memiliki dua buah cincin aromatik yang masing-masing mengandung gugus hidroksi fenolik yang dihubungkan oleh suatu jembatan atau rantai pendek yang terkonjugasi dengan gugus β-diketon. Gugus hidroksi fenolik merupakan gugus yang berperan dalam penangkapan radikal pertama kali pada senyawa antioksidan fenolik. Gugus –OH juga merupakan gugus pendorong elektron yang sangat berpengaruh dalam proses penyebaran elektron atau konjugasi ke dalam cincin benzena bahkan sampai ke luar cincin benzena, yaitu sampai gugus karbonil. Kurkumin juga mempunyai gugus metoksi pada cincin aromatiknya yang bersifat sebagai pendorong elektron sehingga akan menambah kerapatan pada ikatan π yang akan mempermudah senyawa dalam menangkap radikal. Kurkumin mempunyai gugus simetri yang dapat mempermudah dalam penangkapan radikal bebas melalui kedua gugus hidroksinya. Terminasi radikal pada kurkumin dapat melalui mekanisme pembentukan dimer dengan radikal kurkumin yang lain. Radikal bebas yang terbentuk pada kurkumin tersebut dapat pula distabilkan dengan resonansi (Da’i dan Utami, 2011)
Tetrahidrokurkumin (THC) yang merupakan metabolit kurkumin, dilaporkan memiliki beberapa efek farmakologi diantaranya sebagai antiinflamasi dan antioksidan. Efek antiinflamasi dan antioksidan yang dimiliki THC merupakan suatu kombinasi yang bagus pada sediaan kosmetik sebagai anti-aging. Aktivitas antioksidan dari THC juga dapat memperlambat proses melanogenesis, sehingga dapat menjaga warna kulit tetap cerah. THC juga
mampu menghambat aksi dari enzim tirosinase yang berperan dalam proses pembentukan melanin (Majeed and Prakash, 2008).
Aktivitas biologis dari analog kurkumin telah banyak diteliti di Fakultas Farmasi Universitas Gadjah Mada, Yogyakarta. Senyawa PGV-0 diketahui memiliki aktivitas antioksidan (Sardjiman et al, 1997). Selain itu juga memiliki aktivitas antiinflamasi yang lebih baik dibandingkan dengan kurkumin. Aksi farmakologis PGV-0 sebagai antiinflamasi yaitu dengan menghambat biosintesis prostaglandin melalui jalur siklooksigenase (Nurrochmad, 1997). Meiyanto (2007) meneliti bahwa PGV-0 juga dapat menginduksi apoptosis pada sel kanker payudara T47D melalui uji immunositokimia dan western blot.
Selain PGV-0, senyawa lain yang diketahui memiliki aktivitas antioksidan adalah PGV-1, PGV-5, dan HGV-5 (Sardjiman et al., 1997).
Penelitian mengenai aktivitas biologis terus dikembangkan pada analog metabolit kurkumin, diantaranya THPGV-0 dan THPGV-1. Kedua senyawa ini dilaporkan memiliki aktivitias sebagai antibakteri (Ritmaleni et al., 2013) dan antioksidan. Simbara (2009) melakukan uji antioksidan senyawa THPGV-0 menggunakan metode penangkapan radikal DPPH dan kemampuan reduksi terhadap ion feri. Hasil penelitian menunjukkan bahwa senyawa THPGV-0 memiliki aktivitas antioksidan yang lebih baik dari PGV-0. Metode yang sama digunakan oleh Utama (2012) untuk mengetahui aktivitas antioksidan terhadap THPGV-1. Senyawa THPGV-1 diketahui memiliki aktivitas antioksidan yang lebih baik dibandingkan PGV-1 (Utama, 2012).
11. Vitamin E
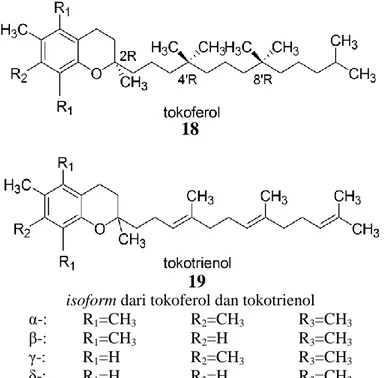
Vitamin E merupakan nama gabungan dari 8 set struktur tokoferol dan tokotrienol, yang merupakan Vitamin larut lemak dengan aktivitas antioksidan. Vitamin E dapat bertindak sebagai lipid-soluble antioksidan dengan melindungi lipoprotein dan membran yang dapat menangkap radikal bebas. Semua isoform alami dan sintetik dari Vitamin E memiliki kemampuan untuk menghambat peroksidasi lipid sebagai antioksidan “chain-breaking”. Dari kedelapan struktur, α-tokoferol banyak diteliti karena memiliki bioavailabilitas yang paling tinggi (Hamid et al.,2010).
18
19
isoform dari tokoferol dan tokotrienol α-: R1=CH3 R2=CH3 R3=CH3
β-: R1=CH3 R2=H R3=CH3
γ-: R1=H R2=CH3 R3=CH3
δ-: R1=H R2=H R3=CH3
Gambar 7. Struktur molekul Vitamin E (Hamid et al.,2010)
12. Studi Antioksidan in vitro
a. Metode Penangkapan radikal DPPH
Salah satu metode yang digunakan untuk uji antioksidan secara in-vitro adalah penggunaan DPPH (diphenylpicrylhydrazil. Molekul DPPH dikarakterisasi
sebagai radikal yang stabil karena memiliki kemampuan melakukan delokalisasi elektron dalam molekul, sehingga molekul tidak mengalami dimerisasi, seperti pada kebanyakan radikal lainnya (Molyneux, 2004). Delokalisasi juga menyebabkan terbentuknya warna ungu dari radikal DPPH yang memberikan serapan yang kuat pada panjang gelombang 517 nm. Penurunan intensitas warna ungu sebanding dengan aktivitasnya dalam penangkapan elektron, sehingga semakin kecil serapan, menunjukkan peningkatan aktivitas penangkapan radikal. Ketika larutan DPPH dicampurkan dengan molekul yang dapat menyumbangkan elektron atau hidrogen akan menjadi bentuk tereduksi dengan kehilangan warna ungunya, dan akan membentuk warna kuning dari gugus pikril (Molyneux, 2004).
20 21
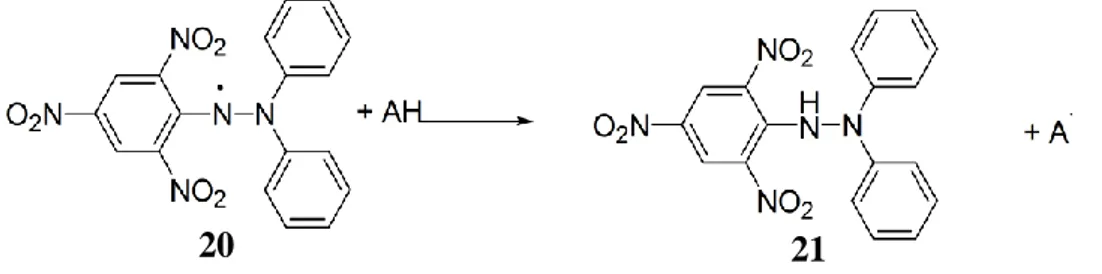
Gambar 8. Reaksi Penangkapan Radikal oleh DPPH
Parameter yang biasa digunakan untuk menginterpretasikan hasil dari uji aktivitas antioksidan dengan peredaman radikal DPPH adalah nilai efficient concentration (EC50) atau disebut nilai IC50, yakni konsentrasi yang menyebabkan
hilangnya 50% aktivitas DPPH (Molyneux, 2004).
Metode daya tangkap radikal DPPH telah digunakan secara luas untuk uji aktivitas antioksidan. Metode ini telah digunakan dalam uji aktivitas antioksidan senyawa kurkumin (Purba dan Martosupono, 2009). Beberapa contoh lainnya yaitu pada uji antioksidan larutan yang digunakan pada gigi yang telah
di-bleaching (Garcia et al, 2012). Selain itu, Anchuri (2012) juga melakukan uji antioksidan secara in-vitro dari hasil sintesis mononuklear senyawa Ruthenium (II) menggunakan metode ini.
b. Metode Daya Reduksi terhadap Ion Feri
Penentuan total kandungan antioksidan dilakukan dengan menggunakan metode FRAP (Ferric Reducing Antioxidant Power). Metode ini dapat menentukan kandungan total antioksidan dari suatu bahan berdasarkan kemampuan senyawa antioksidan mereduksi ion Fe3+ menjadi Fe2+ sehingga kekuatan antioksidan suatu senyawa dianalogikan dengan kemampuan mereduksi dari senyawa tersebut (Halvorsen et al., 2002).
Prinsip dari metode ini yaitu reduksi ion feri menjadi ion fero oleh senyawa antioksidan, yang kemudian dikopling menggunakan senyawa lain, sehingga diperoleh senyawa berwarna yang bisa dibaca absorbansinya pada daerah visibel. Sesuai dengan persamaan reaksi kimia di bawah, dimana L adalah ligand kromogenik yang menghasilkan warna (Berker, et al.,2007).
Fe(III)–L + antioksidan ↔ Fe(II)–L + oxidizedantioxidant (4)
Penelitian mengenai uji antioksidan dengan metode daya reduksi terhadap ion feri telah dilakukan oleh Wuryantoko dan Supardjan (1997) terhadap senyawa kurkumin persamaan reaksi reduksi dapat terlihat seperti pada gambar di bawah:
Kurkumin + Fe3+ Kurkumin-Fe3+ Kurkumin-Fe2+ + o-fenantrolin
Komplek o-fenantrolin-Fe2+ +
radikal kurkumin
Reaksi siklikasi kurkumin
Gambar 9. Persamaan Reaksi Reduksi Ion Feri Senyawa Kurkumin
c. Hubungan Struktur Aktivitas Antioksidan
Penelitian mengenai hubungan struktur-aktivitas senyawa fenolik telah banyak dilakukan pada aktivitas antioksidannya. Senyawa PGV-5, THPGV-5 dan Vitamin E merupakan senyawa fenolik yang mempunyai potensi besar sebagai antioksidan, karena memiliki gugus fenolik yang merupakan gugus penting dalam aktivitas antioksidan. Senyawa fenolik memiliki daya antioksidan yang lebih poten dibandingkan senyawa non-fenolik (Venkatesan et al., 2000). Selain itu disebutkan bahwa senyawa fenolik kurkumin, tetrahidrokurkumin, dan turunan lainnya menunjukkan bahwa adanya subtituen seperti metoksi yang merupakan gugus pendonor elektron pada struktur fenolik dapat meningkatkan aktivitas antioksidan karena adanya subtituen tersebut lebih memungkinkan senyawa antioksidan fenolik mendonorkan (mengabstraksikan) atom H-nya kepada suatu radikal bebas.
Pendekatan komputasi telah banyak dilakukan untuk melakukan prediksi aktivitas antioksidan berdasarkan struktur molekul. Salah satunya adalah penelitian yang dilakukan Farkas et al., (2004) yang melakukan pendekatan komputasi menggunakan teknik Partial Least Square (PLS) untuk mengetahui
hubungan struktur-aktivitas antioksidan senyawa flavonoid. Dengan pendekatan teori komputasi, efektivitas antioksidan senyawa fenolik secara umum dapat dianalisis berdasarkan parameter berikut: (a) Estimasi kekuatan ikatan O-H, yaitu berdasarkan nilai BDE (Bond Dissociation Enthalphy) atau berdasarkan struktur molekul seperti panjang ikatan dan distribusi muatan. (b) Adanya kapasitas donasi elektron molekuler yang dapat dianalisis berdasarkan nilai Potensial ionisasi (IP) atau secara teoritis setara dengan energi HOMO, dan (c) Stabilitas fenolik yang terbentuk. Lien et al., mengaplikasikan perhitungan parameter seperti panas pembentukan, energi tertinggi orbital terisi dan energi terendah orbital kosong molekul, dan jumlah gugus –OH untuk mendeskripsikan aktivitas antiradikal dari senyawa fenolik. Didukung pula oleh Amic et al., bahwa variabel indikator aktivitas antioksidan terletak pada jumlah dan posisi gugus –OH dalam senyawa.
F. Landasan Teori
Hidrogenasi senyawa analog kurkumin telah banyak dilakukan menggunakan katalis paladium karbon 10%. Salah satunya adalah senyawa PGV-1 yang berhasil direduksi menjadi senyawa THPGV-PGV-1 oleh Andhini (20PGV-12). Katalis paladium karbon mempercepat jalannya reaksi dengan menurunkan energi aktivasi. Hidrogenasi gugus α,β-tak jenuh karbonil akan menghasilkan senyawa yang memiliki gugus α,β- jenuh karbonil, mengakibatkan perubahan warna larutan yang semula kuning menjadi tidak berwarna, sehingga proses hidrogenasi dapat dikontrol secara langsung berdasarkan indikator warna. Tidak adanya ikatan karbonil α,β tidak jenuh pada senyawa THPGV-1, membuat resonansi dari karbonil menjadi lebih kecil, sehingga gugus fenoliknya memiliki densitas
elektron yang lebih besar dibandingkan dengan struktur senyawa PGV-1. Densitas elektron yang besar pada gugus fenolik ini akan membuat potensi pendonoran elektron untuk menstabilkan radikal bebas meningkat, sehingga senyawa THPGV-1 memiliki aktivitas antioksidan yang lebih tinggi dibandingkan dengan senyawa PGV-1 (Utama, 2012).
G. Hipotesis
1. Senyawa THPGV-5 dapat disintesis dari starting material PGV-5 melalui reaksi hidrogenasi dengan katalis paladium karbon.
2. Senyawa THPGV-5 memiliki aktivitas sebagai antioksidan yang lebih baik dibandingkan dengan senyawa PGV-5.