0
MODUL
BIOKIMIA PERAIRAN
Disusun oleh
Dr. Emma Rochima, SPi., MSi
Nia Kurniawati, Ir., MS
Program Studi Perikanan Fakultas Perikanan dan Ilmu Kelautan
Universitas Padjadjaran Agustus, 2016
1 MODUL 1
PENDAHULUAN DAN ORGANISASI SEL
Pendahuluan
Mata kuliah ini membahas tentang biomolekul, metabolisme sel di alam dan peranannya pada produk hasil perikanan, faktor-faktor yang mempengaruhi reaksi biokimia yang disebabkan oleh mikroba maupun enzim, kerusakan biokimiawi pada berbagai produk perikanan, prinsip-prinsip pengawetan produk perikanan serta pengendalian mikroba dan enzim
Adapun kontrak perkuliahan dapat dilihat pada Kontrak Perkuliahan.pdf
Organisasi Sel Tujuan:
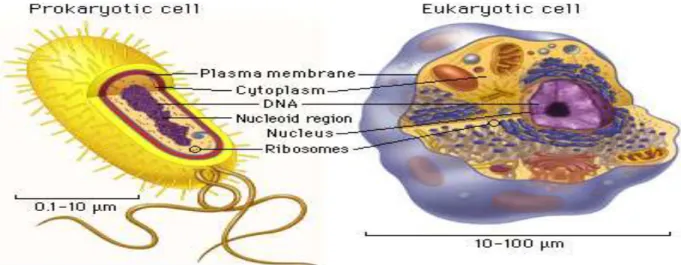
Setelah mempelajari Organisasi Sel mahasiswa mampu menjelaskan organisasi (bagian-bagian) yang terdapat pada sel prokaryotes dan eukaryotes, sifat dan fungsi bagian-bagian tersebut, serta mampu membedakan antara sel prokaryotes dengan eukaryotes.
Sel
Sel adalah bagian terkecil dari suatu organisme. Semua sel memiliki membrane sel. Lapisan tipis dari suatu jaringan yang membentengi antara sitoplasma dan lingkungan di luar sel. Membran sel berfungsi mengontrol bahan atau substansi yang masuk maupun keluar sel serta berperan melindungi sel. Beberapa struktur sel yang ada di dalam sitoplasma dinamai organel. Masing-masing organel memiliki tugas spesifik. Hampir seluruh organel dibatasi oleh membran.
2
Gambar 1: Bagian sel Inti Sel
Memiliki bentuk bulat berukuran besar di dalam sel. Membrane inti sel berperan melindungi inti sel. Inti sel terdiri dari kromatin yaitu untaian panjang yang mengapung di dalam inti sel, dan mengandung materi genetic.Adapula nucleolus yaitu bagian dari inti sel yang berukuran kecil yang juga mengapung di dalam inti sel. Nukleolus adalah tempat dimana ribosom dibuat.
3 Sitoplasma
Merupakan materi seperti gel di dalam membrane sel dan di luar inti sel yang mengandung organel-organel. Tidak seperti gelatin, sitoplasma bergerak secara konstan.
Mitokondria
Memiliki struktur melingkar, menghasilkan energy yang dibutuhkan oleh sel untuk menjalankan fungsinya. Istilah lain mitokondria sebagai rumah energi bagi sel.
Ribosom
Badan seperti biji yang menempel di bagian luar permukaan reticulum endoplasma atau sering isebut dengan bagian yang bebas mengapung di dalam sitoplasma. Bagian kecil membuat RNA, menghasilkan protein dan mengeluarkannya menuju retikulum endoplasma.
Retikulum Endoplasma
Menyambung dengan membrane inti, bagian halus dari RE (dengan atau tanpa ribosom) membentuk lipid, sedangkan bagian RE yang kasar (dengan atau tanpa ribosom) memproduksi protein.
Badan Golgi
Terlihat sepeti kumpulan karung dan tabung. Berfungsi menerima protein dan bahan baru lainnya dari RE. Mengemas protein dan melepaskannya keluar sel. Juga menyebarkan protein di dalam sel.
Lisosom
Merupakan struktur yang melingkar kecil yang mengandung enzim pencernaan yang memotong-motong bagian makanan dan mendaur ulang bagian sel yang sudah tua.
Vakuola
Bagian sel berukuran besar, bundar, terlihat seperti karung yang mengapung di dalam air dalam sitoplasma. Hampir seluruh tanaman memiliki
4
satu vakuola yang besar. Berfungsi menyimpan makanan, air dan sampah hasil metabolisme
Klasifikasi sel
• Eukariotik: organism yang mengandung satu inti sel dan organel-organel. • Prokariotik: Organisme yang kekurangan inti sel dan organel yang terikat
pada membrane. Materi genetic mengapung di dalam sitoplasma sel prokariotik.
Pada beberapa organism, sel dibedakan dalam ukuran dan struktur dan tugas yang membedakan fungsi selnya.
5 Tugas
Bandingkan sel pada hewan, tanaman dan bakteri dan buat dalam bentuk tabulasi.
Bagian Sel Tanaman Hewan Bakteri
Prokariotik dan eukariotik Membran sel Dinding sel Inti sel Klorofil Vakuola
6 Daftar Pustaka
Nelson DN &Cox MM. 2008. Lehninger: Principles Biochemistry 5th Ed. WH Freeman & Company. New York
7
MODUL 2
ASAM AMINO DAN PROTEIN
Tujuan Pembelajaran:
Mahasiswa mampu menjelaskan tentang unsur penyusun, sifat, rumus kimia, struktur , dan jenis asam amino standar, serta mengklasifikasikan asam amino standar berdasarkan rantai sisinya. Selain itu, mahasiswa mampu menjelaskan tentang pembentukan protein dari asam amino melalui ikatan peptida, urutan asam amino dalam protein, struktur protein, jenis, sifat dan fungsi protein.
Asam amino
Asam amino, peptida dan protein merupakan komponen makro yang penting dalam sistem pangan. Asam amino merupakan prekursor penyusun peptida dan protein. Struktur peptida dan protein disusun oleh deretan asam amino yang dihubungkan satu sama lain melalui ikatan kovalen yang disebut ikatan peptida. Peptida memiliki deretan asam amino yang pendek, sedangkan protein merupakan molekul yang besar dan kompleks yang disusun oleh lebih dari 100 buah residu asam amino.
Jenis peptida dan protein berbeda akan membentuk struktur kimia dan sifat fisikokimia yang berbeda pula tergantung jenis dan deretan asam amino penyusunnya. Sebagai contoh, protein yang mengandung banyak residu asam amino polar (misalnya albumin dan globulin) akan lebih larut dalam air, sebaliknya protein dengan kandungan asam amino non-polar lebih banyak (misalnya gliadin dan glutenin) akan kurang larut dalam air.
Protein merupakan molekul yang sangat penting baik dalam system biologis, kontribusinya sebagai sumber nutrisi maupun dalam mempengaruhi kualitas pangan. Dalam system bologis, protein berperan sebagai zat pengatur dan pembangun jaringan, mempunyai aktivitas biologis sebagai hormone, enzim, penghambat kerja enzim (inhibitor enzim), antibody dan lain lain. Sebagai sumber nutrisi, protein menyumbangkan energy yang sama dengan karbohidrat yaitu 4 Kkal/gram. Sedangkan dalam proses pangan, protein dapat berperan dalam mempengaruhi karakteristik produk pangan, misalnya mengentalkan,
8
membentuk gel, menstabilkan emulsi, membentuk buih, membentuk flavor dan sebagainya.
Protein dapat diperoleh dari tanaman dan hewan, misalnya kacang-kacangan, biji-bijian, ikan, unggas. Kandungan protein dalam bahan pangan bervariasi. Selain itu, protein juga dapat ditemui pada alga, khamir, dan bakteri (misalnya single cell protein).
Bab ini membahas protein dengan cakupan sebagai berikut: a. Asam amino sebagai prekursor penyusun struktur protein, yang mencakup struktur kimia, jenis, pengelompokkan, tatanama, sifat fungsional dan reaksi-reaksi kimia yang melibatkannya, b. struktur kimia peptide dan polipeptida (protein), pengelompokannya, sifat fungsionalnya dan reaksi-reaksi kimia yang melibatkannya dan c. peranan protein dalam proses pengolahan pangan.
Fungsi protein bagi tubuh antara lain sebagai pengatur, pembangun, dan menentukan aktivitas biologis (contohnya hormon, enzim dll). Sebagai enzim, protein berfungsi mengkatalisis reaksi suatu substrat A menjadi produk B. Protein pengangkut berfungsi mengikat dan membawa molekul ligan (seperti hemoglobin). Protein penyimpan contohnya ovalbumin, ferretin, kasein. Protein kontraktil yang berfungsi untuk berkontraksi, perubahan bentuk (aktin dan myosin), protein structural untuk menopang bentuk (serat kolagen dari suatu tendon), elastin dll, protein pertahanan untuk melindungi tubuh dari serangan dari luar tubuh (contoh protein antibody), fibrinogen, thrombin. Protein pengatur yang berfungsi mengatur metabolisme tubuh contohnya hormon, dan faktor transkripsi. Kebutuhan protein untuk tubuh setiap hari sebesar 1g perkilogram berat badan.
Struktur kimia
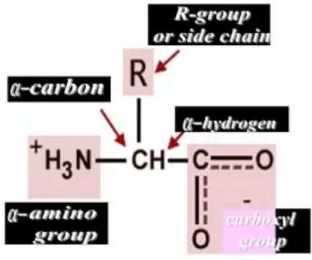
Asam amino adalah senyawa organik penyusun protein yang memiliki dua buah gugus fungsional primer, yaitu gugus amin (-NH2) dan gugus karboksil (-COOH). Kedua gugus fungsional tersebut terikat melalui ikatan kovalen pada atom karbon primer atau karbon α. Atom karbon α merupakan pusat kiral, yaitu dapat memutar sinar bidang polarisasi menuju suatu arah atau kebalikannya. Pada karbon α tersebut, terikat juga atom hydrogen (disebut juga hydrogen α) dan gugus R (rantai karbon). Struktur umum dari asam amino dapat dilihat pada Gambar di bawah ini.
9
Gambar 4. Struktur umum asam amino
Kelompok Asam amino Berdasarkan Sifat Kepolaran
a. Asam amino non-polar, mempunyai gugus samping/ residu yang memiliki gugus alifatik yaitu yang tersusun dari gugus hidrokarbon yang bersifat hidrofobik. Termasuk kelompok ini adalah: glisin, alanin, valin, leusin, metionin, isoleusin
b. Asam amino yang memiliki gugus samping berupa gugus aromatik yang tersusun dari struktur cincin aromatik atau sulfur, yaitu fenilalanin, tirosin, triptofan.
10
c. Asam amino polar karena memiliki gugus samping yang tidak bermuatan karena mengandung gugus hidroksil atau gugus amino dan bersifat hidrofilik (dapat membentuk ikatan hidrogen. Termasuk kelompok ini antara lain: serin, treonin, sistein, prolin, asparagin, glutamin
d. Asam amino yang mempunyai gugus samping bermuatan positif. Gugus samping ini mempunyai gugus amida yang dapat membentuk ion positif pada pH di bawah 7.0. Yang termasuk kelompok ini yaitu: lisin, arginin, histidin.
11
e. Asam amino memiliki gugus samping bermuatan negatif, karena terdapat gugus COOH yang dapat membentuk ion negatif pada pH di atas 7.0. Termasuk kelompok ini: asam aspartat, asam glutamat.
Adapun struktur kimia dan singkatan asam amino yang dipakai dalam literature
Asam amino Singkatan
L-Alanine Ala / A
L-Arginine Arg / R
L-Asparagine Asn / N
L-Aspartic acid Asp/ D
L-Cysteine Cys / C
L-Glutamic acid Glu / E
L-Glutamine Gln / Q Glycine Gly /G L-Histidine His / H L-Isoleucine Ile / I L-Leucine Leu / L L-Lysine Lys / K L-Methionine Met / M L-Phenylalanine Phe / F L-Proline Pro / P L-Serine Ser / S L-Threonine Thr / T L-Tryptophan Trp / W L-Tyrosine Tyr / Y L-Valine Val / V
12 SIFAT ASAM AMINO
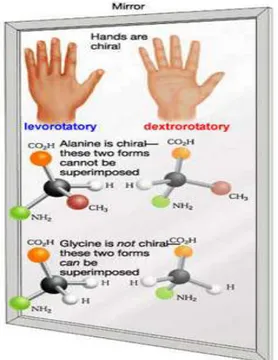
a. Isomer: Setiap asam amino (kecuali glisin) memiliki dua bentuk molekul yang sama, namun masing-masing memiliki arah perputaran atom yang berbeda dalam ruangan. Ibarat gambaran dalam cermin, molekul asam amino yang memiliki tangan kiri dan kanan yang disebut dengan chiral dan gambaran cermin disebut dengan enansiomer.
Gambar 5. Sifat Isomer Protein
b. Sifat ionisasi: Di dalam larutan, asam amino terionisasi dan dapat bersifat sebagai asam atau basa (bersifat amfoter). Dalam keadaan dipolar (zwitterion), dimana gugus amin dan karboksil berionisasi (zwitterion), asam amino memiliki kelarutan yang minimal. Selain itu asam amino memiliki titik isoelektrik yaitu suatu kondisi dimana pH pada saat molekul asam amino tersebut tidak bermuatan. Sedangkan nilai pK yaitu pH pada saat gugus amino dan karboksil 50% terionisasi dan 50% tidak terionisasi. Contoh ionisasi asam amino glisin
13
c. Beberapa asam amino dalam suatu protein memiliki muatan listrik dalam bahan yang berbeda, dan tergantung pada pH dalam media dimana protein tersebut ditemukan. Molekul protein yang disebut amfoterik, karena asam amino tersebut memiliki potensi fungsi sebagai asam maupun basa, tergantung pH. Pada titik isoelektrik, jumlah muatan positif dan negatif sama, dan pada kondisi tersebut protein memiliki kelarutan yang terendah.
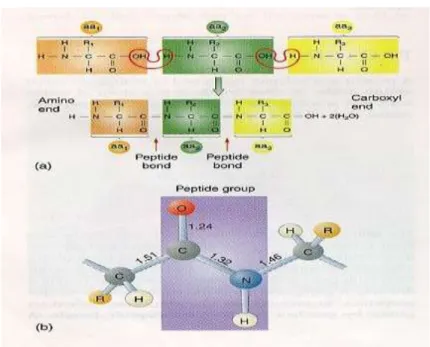
d. Polimerisasi: beberapa asam amino bergabung membentuk polimer tertentu. Ada beberapa jenis polimerisasi yaitu dipeptida, jika dua asam amino berikatan; oligopeptida jika lebih dari dua asam amino bergabung; polipeptida, jika banyak asam amino berikatan. Antar asam amino satu sama lain dihubungkan dengan dengan ikatan peptida. Ikatan peptida merupakan ikatan kovalen yang menghubungkan antara gugus amin (-NH2) pada asam amino pertama dengan gugus karboksil (-COOH) pada asam amino kedua. Pada saat terbentuk ikatan peptida, 1 molekul air dibebaskan (polimerisasi kondensasi). Ikatan peptida lebih pendek dan lebih kuat daripada ikatan C-C, tetapi lebih lemah dibanding C=C. Selain itu, ikatan peptida tidak dapat berotasi secara bebas. Berikut gambaran ikatan peptide yang menghubungkan beberapa asam amino.
Gambar 6. Ikatan peptida
Pembentukan ikatan peptide untuk membentuk struktur protein/peptide dapat dilihat dari gambar berikut ini:
14
Gambar 7. Pembentukan ikatan peptida
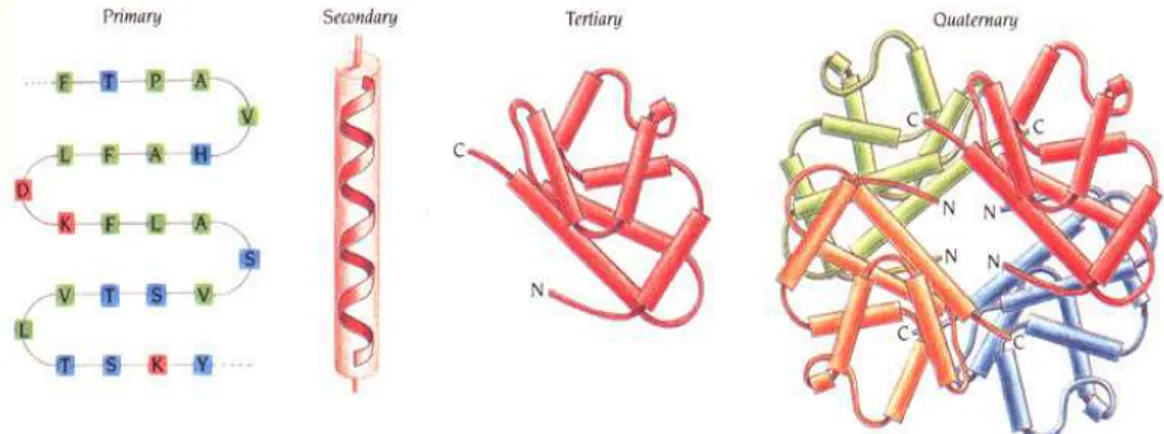
Struktur Protein
Struktur protein dibagi menjadi 4 bagian yaitu struktur primer, struktur sekunder, struktur terter dan struktur kuarterner. Struktur primer adalah merupakan sekuen linier dari asam-asam amino dari mulai ujung nitrogen sampai ke ujung karbon. Misalnya NCC-NCC-NCC-NCC-NCC-NCC-NCC-NCC. Struktur sekunder, merupakan struktur yang teratur dengan orientasi asam amino dalam ikatan peptide disebabkan karena ikatan H pada ikatan alfa heliks dan lembaran beta. Struktur tertier, merupakan struktur tiga dimensi bentuk konformasi disebabkan adanya interaksi elektrostatik lemah antar atom-atomnya. Bentuk terbanyak dari protein adalah globular (bulat). Struktur kuarterner merupakan gabungan dari dua atau lebih polipeptida atau interaksi sub-unit yang menghasilkan bentuk unik. Berikut gambaran struktur protein:
15
Gambar 8. Struktur Protein Jenis-jenis Protein
Jenis-jenis protein meliputi protein globular, protein serat, dan protein konjugasi. Protein globular merupakan protein alami yang memiliki konfigurasi struktur tertier di dalamnya. Sebagai contoh: albumin (pada telur), globulin ( pada daging, polong-polongan), histon ( pada jaringan kelenjar), dan protamin (pada sel sperma ikan). Protein serat bersifat tidak larut air dan berwujud protein yang memanjang. Sebagai contoh: kolagen, elastin (dalam daging dan ternak). Protein konjugasi yaitu protein kombinasi antara beberapa jenis seperti karbohidrat atau lipid. Contohnya glikoprotein, lipoprotein, metalloprotein, nukleoprotein, fosfoprotein.
Sifat fisiko kimiawi
Asam amino memiliki sifat fisikokimiawinya antara lain: sifat hidrasi, dimana asam amino memilki daya ikat terhadap air dan pembentuk viskositas. Selain itu, asam amino juga memiliki
Sifat kelarutan (penting untuk proses ekstraksi), sebagai pengental, pembentuk gel (penting untuk produk olahan daging dan ikan), pembentuk tekstur, koagulasi panas dan pembentuk film (seperti pada kembang tahu), dan texturized protein (pembentukan struktur serat seperti daging pada produk ekstrusi, sebagai pengemulsi, pembentuk busa (busa protein putih telur melembutkan dan mengembangkan produk cake), pembentuk adonan (protein gluten yang bersifat viskoelastis pada adonan roti dan mie) dan bersama-sama dengan gula pereduksi membentuk warna dan aroma melalui reaksi Maillard.
16
Perubahan yang mungkin terjadi selama proses pengolahan dan penyimpanan adalah:
a. Denaturasi (karena panas) yang akan menyebabkan perubahan kelarutan, sehingga mempengaruhi tekstur pada bahan pangan. b. Penyimpangan flavor yang disebabkan karena oksidasi (dikatalisis
oleh cahaya)
c. Degradasi enzimatik yang akan menyebabkan perubahan pada tekstur dan flavor (bisa menyebabkan terbentuknya flavor pahit). d. Pembekuan dapat menyebabkan protein mengalami perubahan
konformasi dan kelarutannya.
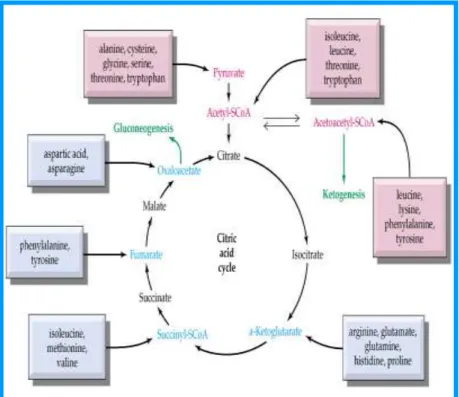
Metabolisme protein
Protein menyediakan 5-10% kebutuhan energi untuk bekerja. Sumber tenaga diperoleh melalui substrat siklus Krebs, proses glukoneogenesis melalui siklus glukosa-alanin. Siklus Krebs dapat dilihat pada Gambar di bawah ini:
17
Adapun siklus glukosa alanin tergambar seperti di bawah ini:
Gambar 10. Siklus glukosa alanin
DAFTAR PUSTAKA
Lehninger A. 1994. Dasar-dasar Biokimia Jilid 1. Thenawijaya M, penerjemah; Jakarta: Penerbit Erlangga, Terjemahan dari: Principle of Biochemistry.
18
MODUL 3
KARBOHIDRAT DAN LIPID
Kegiatan Belajar 1: Karbohidrat Tujuan:
Mahasiswa mampu menjelaskan tentang rumus kimia, struktur, sifat, dan jenis monosakrida, disakarida, oligosakarida dan polisakarida. Mahasiswa mampu menjelaskan tentang reaksi glikolisis, dan glukoneogenisis serta mampu membedakan keduanya. Mahasiswa mampu menjelaskan tentang proses metabolisme glikogen dan proses pengontrolannya
Karbohidrat
Karbohidrat atau Hidrat Arang adalah suatu zat gizi yang fungsi utamanya sebagai penghasil energi, dimana setiap gramnya menghasilkan 4 kalori. Walaupun lemak menghasilkan energi lebih besar, namun karbohidrat lebih banyak di konsumsi sehari-hari sebagai bahan makanan pokok, terutama pada negara sedang berkembang. Di negara sedang berkembang karbohidrat dikonsumsi sekitar 70-80% dari total kalori, bahkan pada daerah-daerah miskin bisa mencapai 90%. Sedangkan pada negara maju karbohidrat dikonsumsi hanya sekitar 40-60%. Hal ini disebabkan sumber bahan makanan yang mengandung karbohidrat lebih murah harganya dibandingkan sumber bahan makanan kaya lemak maupun protein.
Karbohidrat banyak ditemukan pada serealia (beras, gandum, jagung, kentang dan sebagainya), serta pada biji-bijian yang tersebar luas di alam. Karbohidrat termasuk penyusun sel karena penyusun sel terdiri dari molekul organik, yaitu molekul yang mengandung atom karbon (C), hidrogen (H), dan aksigen (O). Secara biologis, karbohidrat memiliki fungsi sebagai bahan baku sumber energi baik pada hewan, manusia dan tumbuhan.
Sumber karbohidrat nabati dalam bentuk glikogen, hanya dijumpai pada otot dan hati dan karbohidrat dalam bentuk laktosa hanya dijumpai di dalam susu. Pada tumbuh-tumbuhan, karbohidrat di bentuk dari basil reaksi CO2 dan H2O melalui proses foto sintese di dalam sel-sel tumbuh-tumbuhan yang mengandung hijau daun (klorofil). Matahari merupakan sumber dari seluruh kehidupan, tanpa matahari tanda-tanda dari kehidupan tidak akan dijumpai.
19
Manusia membutuhkan karbohidrat dalam jumlah tertentu setiap harinya. Walaupun tubuh tidak membutuhkan dalam jumlah yang khusus, kekurangan karbohidrat yang sangat parah akan menimbulkan masalah. Diperlukan sekitar 2 gram karbohidrat per Kg berat badan sehari untuk mencegah terjadinya ketosis. Secara keseluruhan tubuh harus mempertahankan keseimbangan tertentu dalam utilisasi karbohidrat, lemak dan protein sebagai sumber energi.
Fungsi Karbohidrat
Fungsi utama dari karbohidrat adalah menyediakan keperluan energi tubuh, selain itu karbohidrat juga mempunyai fungsi lain, yaitu karbohidrat diperlukan bagi kelangsungan proses metabolisme lemak. Juga karbohidrat mengadakan suatu aksi penghematan terhadap protein.
a. Karbohidrat Sebagai Sumber Energi Utama
Sel-sel tubuh membutuhkan ketersediaan energi siap pakai yang konstan (selalu ada), terutama dalam bentuk glukosa serta hasil antaranya. Lemak juga merupakan sumber energi, tetapi cadangan lemaknya tidak dapat segera dipergunakan sebagai sumber energi siap pakai. 1 gram karbohidrat menyediakan 4 kalori, dan diketahui hanya 10 gram glukosa beredar dalam darah atau 70-100 miligram glukosa per 100 ml darah. Kadar glukosa ini harus dapat dipertahankan.
b. Pengatur Metabolisme Lemak
Karbohidrat mencegah terjadinya oksidasi lemak yang tidak sempurna. Bila energi tidak cukup tersedia maka akan mengakibatkan terjadinya
peningkatan katabolisme lemak, akibatnya terjadi penumpukan/akumulasi badan-badan keton, dan terjadi keasaman pada darah (Asidosis). Dalam hal ini
karbohidrat berfungsi sebagai “fat – sparer”.
c. Penghemat Fungsi Protein (Protein Sparer)
Energi merupakan kebutuhan utama bagi tubuh, sehingga bila karbohidrat yang berasal dari makanan tidak mencukupi maka protein akan dirombak untuk menghasilkan panas dan sejumlah energi. Padahal protein mempunyai fungsi yang lebih utama yaitu sebagai zat pembangun dan
20
memperbaiki jaringan. Agar dapat dipergunakan sesuai fungsinya maka kebutuhan karbohidrat harus dipenuhi dalam susunan menu sehari-hari.
d. Karbohidrat Sebagai Sumber Energi Utama Bagi Otak dan Susunan Saraf
Otak dan susunan saraf hanya dapat mempergunakan glukosa sebagai energi, sehingga ketersediaan glukosa yang konstan harus tetap terjaga bagi kesehatan jaringan tubuh/organ tersebut. Demikian juga kekurangan glukosa dan oksigen akan menyebabkan kerusakan otak/kelainan syaraf yang tidak dapat diperbaiki.
e. Simpanan Karbohidrat Sebagai Glikogen
Tidak seperti halnya dengan simpanan lemak dalam jaringan adipose, glikogen menyediakan energi siap pakai. Lebih kurang 355 gram glikogen disimpan dalam hati dan otot, sehingga dalam tubuh orang dewasa, terdapat 365gram karbohidrat (355 gram dalam bentuk glikogen dan 10 gram dalam bentuk glukosa) jumlah ini sanggup menyediakan energi untuk melakukan aktivitas sedang selama 3 jam. Berarti ketersediaan energi dari menu sehari-hari amatlah diperlukan.
f. Pengatur Peristaltic Usus dan Pemberi Muatan Pada Sisa Makanan
Sellulosa (serat) merupakan polisakharida yang tidak dapat dicerna, tetapi mempunyai fungsi yang penting bagi kesehatan yang mengatur peristaltic usus (memungkinkan terjadinya gerakan usus yang teratur), karena serat memberi muatan/pemberat pada sisa-sisa makanan pada bagian usus besar. Hemisellulosa, agar-agar serta pectin juga memberi fungsi serupa yaitu memberi dan menyerap sejumlah air dalam kolon (bagian usus besar).
Klasifikasi Karbohidrat
Karbohidrat dapat dikelompokkan menurut jumlah unit gula, ukuran dari rantai karbon, lokasi gugus karbonil (-C=O), serta stereokimia. Berdasarkan
jumlah unit gula dalam rantai, karbohidrat digolongkan menjadi 4 golongan utama
yaitu:
1. Monosakarida (terdiri atas 1 unit gula) 2. Disakarida (terdiri atas 2 unit gula) 3. Oligosakarida (terdiri atas 3-10 unit gula)
21
4. Polisakarida (terdiri atas lebih dari 10 unit gula)
Pembentukan rantai karbohidrat menggunakan ikatan glikosida.
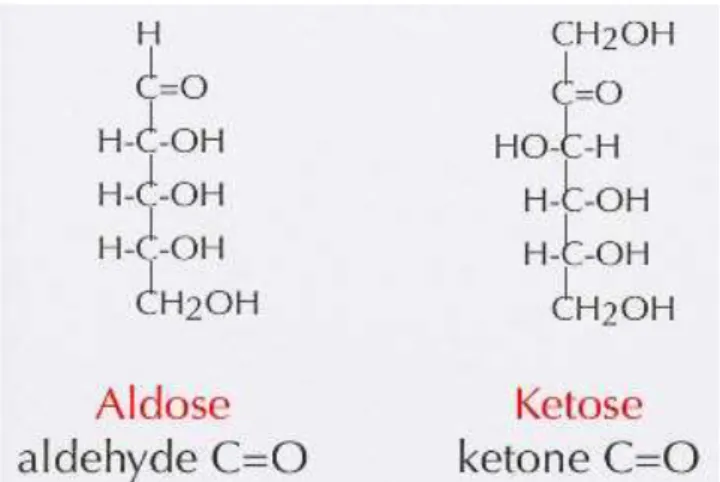
Berdasarkan lokasi gugus –C=O, monosakarida digolongkan menjadi 2 yaitu: 1. Aldosa (berupa aldehid)
2. Ketosa (berupa keton)
Gambar 11. Klasifikasi karbohidrat menurut lokasi gugus karbonil
Berdasarkan jumlah atom C pada rantai, monosakarida digolongkan menjadi: 1. Triosa (tersusun atas 3 atom C)
2. Tetrosa (tersusun atas 4 atom C) 3. Pentosa (tersusun atas 5 atom C) 4. Heksosa (tersusun atas 6 atom C) 5. Heptosa (tersusun atas 7 atom C) 6. Oktosa (tersusun atas 3 atom C)
22
Klasifikasi karbohidrat menurut jumlah atom C
Gambar 12. Contoh monosakarida
Contoh pertama di atas (sebelah kiri) menunjukkan sebuah monosakarida triosa (memiliki 3 atom C), aldosa (berstruktur aldehid/-COH) sehingga dinamakan gula aldotriosa. Sedangkan contoh kedua (sebelah kanan) menunjukkan sebuah monosakarida heksosa (memiliki 6 atom C), ketosa (berstruktur keton/R-CO-R) sehingga dinamakan gula ketoheksosa.
Berdasarkan stereokimia, monosakarida terbagi menjadi beberapa golongan. Stereokimia adalah studi mengenai susunan spasial dari molekul.
23
Salah satu bagian dari stereokimia adalah stereoisomer. Stereoisomer mengandung pengertian:
1. memiliki kesamaan order dan jenis ikatan 2. memiliki perbedaan susunan spasial 3. memiliki perbedaan properti (sifat).
Enantiomer merupakan pasangan dari stereoisomer. Dalam hal ini terdapat aturan yaitu:
1. Diberi awalan D dan L
2. Keduanya merupakan gambar cermin yang tak mungkin saling tumpang tindih
Gambar-gambar berikut memberikan penjelasan mengenai perbedaan susunan spasial dalam enatiomer.
Gambar 13. Ilustrasi untuk enantiomer (perhatikan perbedaan susunan spasial yang ada)
24
Gambar 14. Contoh enantiomer dari gula triosa (perhatikan perbedaan susunan spasial yang ada).
Struktur Karbohidrat Sederhana
Karbohidrat sederhana terdiri dari:
Monosakarida
Sebagian besar monosakarida dikenal sebagai heksosa, karena terdiri atas 6-rantai atau cincin karbon. Atom-atom hidrogen dan oksigen terikat pada rantai atau cincin ini secara terpisah atau sebagai gugus hidroksil (OH). Ada tiga jenis heksosa yang penting dalam ilmu gizi, yaitu glukods, fruktosa, dan galaktosa. Ketiga macam monosakarida ini mengandung jenis dan jumlah atom yang sama, yaitu 6 atom karbon, 12 atom hidrogen, dan 6 atom oksigen. Perbedaannya hanya terletak pada cara penyusunan atom-atom hidrogen dan oksigen di sekitar atom-atom karbon. Perbedaan dalam susunan atom inilah yang menyebabkan perbedaan dalam tingkat kemanisan, daya larut, dan sifat lain ketiga monosakarida tersebut. Monosakarida yang terdapat di alam pada umumnya terdapat dalam bentuk isomer dekstro (D). gugus hidroksil ada karbon nomor 2 terletak di sebelah kanan. Struktur kimianya dapat berupa struktur terbuka atau struktur cincin. Jenis heksosa lain yang kurang penting dalam ilmu
25
gizi adalah manosa. Monosakarida yang mempunyai lima atom karbon disebut pentosa, seperti ribosa dan arabinosa.
26 a. Glukosa
Glukosa merupakan suatu aldoheksosa, disebut juga dekstrosa karena memutar bidang polarisasi ke kanan. Glukosa merupakan komponen utama gula darah, menyusun 0,065- 0,11% darah kita. Glukosa dapat terbentuk dari hidrolisis pati, glikogen, dan maltosa. Glukosa sangat penting bagi kita karena sel tubuh kita menggunakannya langsung untuk menghasilkan energi. Glukosa dapat dioksidasi oleh zat pengoksidasi lembut seperti pereaksi Tollens sehingga sering disebut sebagai gula pereduksi.
b. Galaktosa
Galaktosa merupakan suatu aldoheksosa. Monosakarida ini jarang terdapat bebas di alam. Umumnya berikatan dengan glukosa dalam bentuk laktosa, yaitu gula yang terdapat dalam susu. Galaktosa mempunyai rasa kurang manis jika dibandingkan dengan glukosa dan kurang larut dalam air. Seperti halnya glukosa, galaktosa juga merupakan gula pereduksi.
27 c. Fruktosa
Fruktosa adalah suatu heksulosa, disebut juga levulosa karena memutar bidang polarisasi ke kiri. Merupakan satu-satunya heksulosa yang terdapat di alam. Fruktosa merupakan gula termanis, terdapat dalam madu dan buah-buahan bersama glukosa. Fruktosa dapat terbentuk dari hidrolisis suatu disakarida yang disebut sukrosa. Sama seperti glukosa, fruktosa adalah suatu gula pereduksi.
Disakarida
Disakarida adalah karbohidrat yang tersusun dari 2 molekul monosakarida, yang dihubungkan oleh ikatan glikosida. Ikatan glikosida terbentuk antara atom C 1 suatu monosakarida dengan atom O dari OH monosakarida lain. Hidrolisis 1 mol disakarida akan menghasilkan 2 mol monosakarida. Berikut ini beberapa disakarida yang banyak terdapat di alam.
a. Maltosa
Maltosa adalah suatu disakarida dan merupakan hasil dari hidrolisis parsial tepung (amilum). Maltosa tersusun dari molekul α-D-glukosa dan β-D-glukosa.
28
Dari struktur maltosa, terlihat bahwa gugus -O- sebagai penghubung antarunit yaitu menghubungkan C 1 dari α-D-glukosa dengan C 4 dari β-D-glukosa. Konfigurasi ikatan glikosida pada maltosa selalu α karena maltosa terhidrolisis oleh α-glukosidase. Satu molekul maltosa terhidrolisis menjadi dua molekul glukosa.
b. Sukrosa
Sukrosa terdapat dalam gula tebu dan gula bit. Dalam kehidupan sehari-hari sukrosa dikenal dengan gula pasir. Sukrosa tersusun oleh molekul glukosa dan fruktosa yang dihubungkan oleh ikatan 1,2 –α.
Sukrosa terhidrolisis oleh enzim invertase menghasilkan α-D-glukosa dan β-D-fruktosa. Campuran gula ini disebut gula inversi, lebih manis daripada sukrosa.
Jika kita perhatikan strukturnya, karbon anomerik (karbon karbonil dalam monosakarida) dari glukosa maupun fruktosa di dalam air tidak digunakan untuk berikatan sehingga keduanya tidak memiliki gugus hemiasetal.
Akibatnya, sukrosa dalam air tidak berada dalam kesetimbangan dengan bentuk aldehid atau keton sehingga sukrosa tidak dapat dioksidasi. Sukrosa bukan merupakan gula pereduksi.
29 c. Laktosa
Laktosa adalah komponen utama yang terdapat pada air susu ibu dan susu sapi. Laktosa tersusun dari molekul β-D-galaktosa dan α-D-glukosa yang dihubungkan oleh ikatan 1,4'-β.
Struktur laktosa
Hidrolisis dari laktosa dengan bantuan enzim galaktase yang dihasilkan dari pencernaan, akan memberikan jumlah ekivalen yang sama dari α-D-glukosa dan β-D-galaktosa. Apabila enzim ini kurang atau terganggu, bayi tidak dapat mencernakan susu. Keadaan ini dikenal dengan penyakit galaktosemia yang biasa menyerang bayi.
30 Polisakarida
Polisakarida merupakan polimer monosakarida, mengandung banyak satuan monosakarida yang dihubungkan oleh ikatan glikosida. Hidrolisis lengkap dari polisakarida akan menghasilkan monosakarida. Glikogen dan amilum merupakan polimer glukosa. Berikut beberapa polisakarida terpenting.
a. Selulosa
Selulosa merupakan polisakarida yang banyak dijumpai dalam dinding sel pelindung seperti batang, dahan, daun dari tumbuh-tumbuhan. Selulosa merupakan polimer yang berantai panjang dan tidak bercabang. Suatu molekul tunggal selulosa merupakan polimer rantai lurus dari 1,4’-β-D-glukosa. Hidrolisis selulosa dalam HCl 4% dalam air menghasilkan D-glukosa.
Struktur selulosa
Dalam sistem pencernaan manusia terdapat enzim yang dapat memecahkan ikatan α-glikosida, tetapi tidak terdapat enzim untuk memecahkan ikatan β-glikosida yang terdapat dalam selulosa sehingga manusia tidak dapat mencerna selulosa. Dalam sistem pencernaan hewan herbivora terdapat beberapa bakteri yang memiliki enzim β-glikosida sehingga hewan jenis ini dapat menghidrolisis selulosa. Contoh hewan yang memiliki bakteri tersebut adalah rayap, sehingga dapat menjadikan kayu sebagai makanan utamanya. Selulosa sering digunakan dalam pembuatan plastik. Selulosa nitrat digunakan sebagai bahan peledak, campurannya dengan kamper menghasilkan lapisan film (seluloid).
31 b. Pati / Amilum
Pati terbentuk lebih dari 500 molekul monosakarida. Merupakan polimer dari glukosa. Pati terdapat dalam umbi-umbian sebagai cadangan makanan pada tumbuhan. Jika dilarutkan dalam air panas, pati dapat dipisahkan menjadi dua fraksi utama, yaitu amilosa dan amilopektin. Perbedaan terletak pada bentuk rantai dan jumlah monomernya.
Amilosa adalah polimer linier dari α-D-glukosa yang dihubungkan dengan ikatan 1,4-α. Dalam satu molekul amilosa terdapat 250 satuan glukosa atau lebih. Amilosa membentuk senyawa kompleks berwarna biru dengan iodium. Warna ini merupakan uji untuk mengidentifikasi adanya pati.
Struktur amilosa
Molekul amilopektin lebih besar dari amilosa. Strukturnya bercabang. Rantai utama mengandung α-D-glukosa yang dihubungkan oleh ikatan 1,4'-α. Tiap molekul glukosa pada titik percabangan dihubungkan oleh ikatan 1,6'-α.
32
Struktur amilopektin
Hidrolisis lengkap pati akan menghasilkan D-glukosa. Hidrolisis dengan enzim tertentu akan menghasilkan dextrin dan maltosa.
33 Daftar Pustaka
1. Harper, Rodwell, Mayes, 1977, Review of Physiological Chemistry
2. Colby, 1992, Ringkasan Biokimia Harper, Alih Bahasa: Adji Dharma,
Jakarta, EGC
3. Wirahadikusumah, 1985, Metabolisme Energi, Karbohidrat dan Lipid,
Bandung, ITB
4. Harjasasmita, 1996, Ikhtisar Biokimia dasar B, Jakarta, FKUI
5. Toha, 2001, Biokimia, Metabolisme Biomolekul, Bandung, Alfabeta
34 Kegiatan Belajar 2: Lipid
Tujuan Pembelajaran:
Setelah mempelajari lipid, maka mahasiswa mampu menjelaskan tentang jenis, struktur, sifat, dan peranan biologis asam lemak. Juga mampu menjelaskan tentang reaksi pemecahan asam lemak menjadi asityl coA dan sintesis asam lemak dari Asetil CoA. Serta mampu menjelaskan tentang struktur, fungsi, sintesis, dan pemecahan triasilgliserol, kolesterol, dan lipoprotein
Lipid
Merupakan segolongan senyawa yang tidak larut dalam air, tapi larut dalam pelarut organik
Gambar 17. Struktur lipid Fungsi Lipid:
• Bentuk energi cadangan
• Komponen struktural membran sel • Lapisan pelindung
• Komponen permukaan sel, untuk interaksi antara sel dengan zat kimia • Proses pengangkutan melalui membran
35 Klasifikasi Lipid
► Lipid kompleks : mengandung komponen asam lemak. - asilgliserol/gliserida
- fosfogliserida - spingolipid - lilin
► Lipid sederhana : tidak mengandung asam lemak. - Terpenoid
- Steroid - Prostaglandin
Trigliserida
Triester dari asam lemak rantai panjang dan gliserol (mengandung tiga gugus OH). Trigliserida dihidrolisis oleh enzim lipase dalam usus menghasilkan asam lemak dan gliserol. Reaksi safonifikasi adalah reaksi antara trigliserol dengan basa seperti NaOH membentuk sabun .
Biosintesis trigliserida meliputi dua tahap. Tahap reaksi pertama dan kedua adalah proses asilasi gugus hidroksil dari gliserol-3-fosfat menghasilkan asam lisofosfatidat kemudian asam fosfatidat. Reaksi ini dikatalisis oleh enzim gliserolfosfat asiltransferase. Pada tahap reaksi ketiga asam fosfatidat dihidrolisis dengan enzim fosfatidat fosfatase menghasilkan diasilgliserol. Pada tahap terakhir diasilgliserol dikatalisis oleh enzim diasilgliserol asiltransferase menghasilkan triasilgliserol seperti yang tergambar di bawah ini.
36 Asam Lemak
Adalah asam karboksilat yang digunakan sebagai prekursor triasilgliserol (trigliserida). Merupakan rantai hidrokarbon lurus dengan satu gugus karboksil, umumnya merupakan karbon genap. Berdasarkan kejenuhannya asam lemak diklasifikasikan menjadi asam lemak jenuh dan asam lemak tidak jenuh (adanya ikatan rangkap). Asam lemak jenuh berwujud padat (lemak) pada suhu ruang, yang diperoleh dari lemak hewan . Asam lemak tidak jenuh berwujud cair (minyak) pada suhu ruang, yang diperoleh dari tanaman atau minyak sayuran
(vegetable oil) Konfigurasi ikatan rangkap pada asam lemak umumnya berupa
ikatan cis-
Tata nama Asam Lemak
Sesuai dengan tata nama asam karboksilat. Mis: HCOOH: asam metanoat,C18: oktadekanoat, C22: dokosanoat . Penulisan singkat asam lemak a. C 18:0 (18 atom C tanpa (0) ikatan rangkap)
b. C 18:1 ∆9 (18 atom C satu ikatan rangkap pada atom C no 9 dari gugus karboksilat)
c. C 18:2 ∆9,12 (18 atom C dua ikatan rangkap pada atom C no 9 dan 12 dari gugus
37
► Sesuai dengan tata nama asam karboksilat. Mis: HCOOH: asam metanoat,C18: oktadekanoat, C22: dokosanoat
► Penulisan singkat asam lemak
a. C 18:0 (18 atom C tanpa (0) ikatan rangkap)
b. C 18:1 ∆9 (18 atom C satu ikatan rangkap pada atom C no 9 dari gugus karboksilat)
c. C 18:2 ∆9,12 (18 atom C dua ikatan rangkap pada atom C no 9 dan 12 dari gugus karboksilat)
38 Jumlah atom karbon Jumah ikatan rangkap
Nama umum asam lemak Rumus molekul 12 14 16 18 18 18 0 0 0 0 1 2 Asam laurat Asam miristat Asam palmitat Asam stearat Asam oleat Asam linolenat CH3(CH2)10COOH CH3(CH2)12COOH CH3(CH2)14COOH CH3(CH2)16COOH CH3(CH2) 7CH=CH(CH2)7COOH CH3(CH2) 4CH=CH(CH2)2(CH2)6COOH
40 Katabolisme Asam Lemak
► Tahap pertama adalah pengaktifan asam palmitat bebas dengan asetil koenzim-A oleh enzim asil koenzim-A sintetase menghasilkan palmitoil koenzim-A.
► Tahap kedua palmitoil koenzim-A dibawa oleh karnitin dari sitoplasma ke dalam mitokondrion.
► Tahap ketiga proses dehidrogenasi palmitoil koenzim-A dengan enzim asil koenzim-A dehidrogenase menghasilkan senyawa enoil koenzim-A. ► Tahap keempat proses dehidratasi ikatan rangkap pada enoil koenzim-A
menjadi 3-hidroksipalmitoil koenzim-A oleh enzim enoil koenzim-A hidratase.
► Tahap kelima adalah dehidrogenase dengan enzim 3-hidroksiasil koenzim-A dehidrogenase pada senyawa 3-hidroksipalmitoil koenzim-A menjadi 3-ketopalmitoil koenzim-A.
► Tahap terakhir pemecahan molekul 3-ketopalmitoil koenzim-A dengan enzim asetil koenzim-A asetiltransferase menghasilkan satu molekul asetil koenzim-A dan asam lemak dlm bentuk koenzim-A nya.
asam lemak
ATP CoASH
AMP PPi
asil asam lemak koenzim-A FAD
FADH
asil asam lemak dehidrogenase enoil -CoA H2O enoil koenzim-Ahidratase 3-hidrokspalmitoil koenzim-A 3-hidroksiiasil dehidrogenase NAD H+ + NADH 3-ketopalmitoil koenzim-A asetil koenzim-A
asetil CoA asetiltransferase asil asam lemak CoA
tahap reaksi (2) sampa dg (5) diulangi sampai seuruh rantai asam lemaknya dioksidasi menjadi asetil-CoA
41 Biosintesis Asam Lemak
► Tahap pertama pembentukan malonil koenzim-A dari asetil koenzim-A.
► Tahap kedua pemanjangan rantai asam lemak sampai terbentuknya asam palmitat secara kontinu.
► Tahap ketiga pemanjangan rantai asam palmitat secara tahap demi tahap.
Gambar 18. Perbedaan Biosintesis dan Oksidasi Asam Lemak
asetil-SCoA
asetil-CoA karboksilase
HOOC
CH2CO
SCoA
ATP
ADP + Pi
CO
2malonil-CoA
7 malonil-CoA
7 malonil-CoA
ACP-SH
CoA-SH
asetil-CoA
ACP-SH
CoA-SH
asetil-S-ACP
palmitoil-S-ACP
CoA-SH
ACP-SH
palmitoil-SCoA
palmitoil-SCoA
asetil-SCoA
stearoil-SCoA
asetil-SCoA
dst
42
1. Biosintesis asam lemak terjadi dlm sitoplasma, sedangkan oksidasi asam lemak di dlm mitokondrion.
2. Biosintesis asam lemak menggunakan ACP sebagai sistem pembawanya, sedangkan oksidasi memakai CoA.
3. Biosintesis menggunakan maloni-CoA sebagai molekul pemanjang rantai, sedangkan oksidasi melepaskan asetil-CoA pd sat kali daur proses perombakannya. Biosintesis menggunakan NADPH/NADP+ sebagai sistem koenzim dlm reaksi hidrogenasi, sedangkan oksidasi memakai sistem.
Kolesterol
Terdapat di dalam semua macam jaringan hewan dan manusia. Komponen sel membran dan prekursor hormon steroid. Memiliki 27 atom karbon, 15 atom berasal dari gugus metil dan 12 dari gugus karboksil molekul asetat. Tahap reaksi biosintesis kolesterol dibagi menjadi tiga
bagian, yaitu :
1. Pembentukan asam mevalonat dari asetat. 2. Pembentukan skualin dari asam mevalonat. 3. Pembentukan kolesterol dari skualin.
Lipoprotein
Molekul terdiri dari protein dan lipid. Ada dua macam sistem lipoprotein, Yaitu :Sistem lipoprotein pengangkut, yang merupakan bagian dari plasma darah.
1. Sistem lipoprotein membran, yang merupakan pembentuk struktur membran.
Fungsi lipoprotein adalah sebagai alat pengangkut lipid antara berbagai organ, melalui darah. Lipoprotein plasma darah manusia dibagi menjadi lima golongan utama, yaitu :
1. Kilomikron: Dibentuk dalam sel epitel usus. Paling banyak mengandung lipida (terutama TG). Paling besar diameter partikel, sehingga membias sinar bila kadar tinggi serum/plasma keruh . Mengandung apoprotein ; Apo-B; Apo-C dan Apo-A. Fungsinya mengangkut : -TG dari usus ke jaringan Ekstrahepatik/jar.Lemak -Kholesterol bebas/kholesterol ester dari usus.
43
2. Lipoprotein kerapatan sangat rendah (VLDL): Dibentuk dalam sel hati, Banyak mengandung lipid (TG), Mengandung : Apo-B dan Apo-C, Fungsi, mengangkut TG Jar. Ekstrahepatik (Oksidasi), Jar. Lemak (Esterifikasi) Ditimbun , Kholesterol bebas/Ester dari hati lalu masuk ke sirkulasi darah. LPL menghidrolisis TG dari VLDL Asam lemak
3. Lipoprotein kerapatan rendah (LDL): Terbentuk dalam sirkulasi darah sebagai bentuk hasil akhir metabolisme VLDL, Paling banyak mengandung kholesterol , Mengandung : Apo-B, Akibat hidrolisis TG, proporsi protein & Lipida (kecuali TG) meningkat . Pada jaringan perifer : LDL berikatan dengan reseptor masuk dlm sel hidrolisis cholesterol ester menjadi kholesterol bebas digunakan sel yang bersangkutan 4. Lipoprotein kerapatan tinggi (HDL): Sintesis di hati dan usus, Paling
banyak mengandung protein : Apo-A dan Apo-C, Komponen lemak terutama kholesterol dan fosfolipida, sedikit TG, Mengangkut kelebihan kholesterol dari jaringan perifer dari hati lalu ekskresi
44 Daftar Pustaka
Anonim. 2009. Identifikasi Karbohidrat. http://kimia.upi.edu/utama/bahanajar / kuliah_web/2009/0606811/identifikasi%20karbohidrat.html. Diakses pada tanggal 29 September 2012. Pukul 19.30 WIB.
Anonim. 2012. Macam-Macam Karbohidrat. http://breakfast.forum-motion.net/ t1 8-macam-macam-karbohidrat. Diakses pada tanggal 29 September 2012. Pukul 19.45 WIB.
Anonim. 2012. Struktur Karbohidrat http://www.docstoc.com/docs/56921655 / Struktur-Karbohidrat. Diakses pada tanggal 29 September 2012. Pukul 19.50 WIB.
Campbell, et.at. 2000. BIOLOGI Edisi Kelima Jilid 3. Jakarta : Erlangga. Keenan et.at. 1994. Ilmu Kimia untuk Universitas. Jakarta : Erlangga.
Oxtoby, D.W., HP.Gillis, dan N.H. Nachtrieb. 2001. Prinsip-Prinsip Kimia Modern Ed-4. Alih Bahasa, Seminar Setiati Achmadi, Editor, Silvester Lemeda Sinarmata. Jakarta : Erlangga.
Lehninger A. 1994. Dasar-dasar Biokimia Jilid 1. Thenawijaya M, penerjemah; Jakarta: Penerbit Erlangga, Terjemahan dari: Principle of Biochemistry.
45
MODUL 4
VITAMIN DAN MINERAL
Kegiatan Belajar 1 : Vitamin Tujuan:
Mahasiswa mampu menjelaskan tentang jenis, struktur, sifat, peranan dan sumber vitamin dan serta senyawa antivitamin.
Vitamin
Vitamin adalah molekul organik yang di dalam tubuh mempunyai fungsi yang sangat bervariasi. Fungsi vitamin dalam metabolisme yang paling utama adalah sebagai kofaktor. Di dalam tubuh diperlukan dalam jumlah sedikit
(micronutrient). Biasanya tidak disintesis di dalam tubuh, jika dapat disintesis
jumlahnya tidak mencukupi kebutuhan tubuh, sehingga harus diperoleh dari makanan atau diet.
Pengertian vitamin adalah sekelompok senyawa organik amina yang sangat penting dan sangat dibutuhkan oleh tubuh, karena vitamin berfungsi untuk membantu pengaturan atau proses kegiatan tubuh (vitamin mempunyai peran sangat penting dalam metabolisme tubuh), karena vitamin tidak dapat dihasilkan oleh tubuh. Jika manusia, hewan dan ataupun makhluk hidup lain tanpa asupan vitamin tidak akan dapat melakukan aktivitas hidup dengan baik, kekurangan vitamin menyebabkan tubuh kita mudah terkena penyakit.
Nama vitamin sendiri berasal dari gabungan kata bahasa Latin
yaitu vita yang artinya “hidup” dan amina (amine) yang mengacu pada
suatu gugus organik yang memiliki atom nitrogen (N), karena pada
awalnya vitamin dianggap demikian. Kelak diketahui bahwa banyak
vitamin yang sama sekali tidak memiliki atom N. Dipandang dari sisi
enzimologi (ilmu tentang enzim), vitamin adalah kofaktor dalam reaksi
kimia yang dikatalisasi oleh enzim. Pada dasarnya, senyawa vitamin ini
digunakan tubuh untuk dapat bertumbuh dan berkembang secara normal
Untuk bisa mendapatkan asupan vitamin tidaklah sulit, bisa
dikatakan kebanyakan makanan yang kita konsumsi setiap hari telah
46
mengandung vitamin hanya saja mungkin kita tidak menyadari besar
kecilnya kandungan vitamin yang kita konsumsi setiap hari.
Cara kerja vitamin
Cara kerja vitamin yang larut dalam lemak dan yang larut dalam air berbeda.
Vitamin yang larut dalam lemak : Vitamin yang larut dalam lemak akan disimpan di dalam jaringan adiposa (lemak) dan di dalam hati. Vitamin ini kemudian akan dikeluarkan dan diedarkan ke seluruh tubuh saat dibutuhkan. Beberapa jenis vitamin hanya dapat disimpan beberapa hari saja di dalam tubuh, sedangkan jenis vitamin lain dapat bertahan hingga 6 bulan lamanya di dalam tubuh. Jenis vitamin yang termasuk golongan ini adalah vitamin A (antixeroftalmia), vitamin D3 (antirakhitis), dan vitamin E (tokoferol atau astisterilitas)
Vitamin yang larut dalam air : Berbeda dengan vitamin yang larut dalam lemak, jenis vitamin larut dalam air hanya dapat disimpan dalam jumlah sedikit dan biasanya akan segera hilang bersama aliran makanan. Saat suatu bahan pangan dicerna oleh tubuh, vitamin yang terlepas akan masuk ke dalam aliran darah dan beredar ke seluruh bagian tubuh. Apabila tidak dibutuhkan, vitamin ini akan segera dibuang tubuh bersama urin. Oleh karena hal inilah, tubuh membutuhkan asupan vitamin larut air secara terus-menerus. Jenis vitamin yang termasuk golongan ini adalah vitamin B komlpeks, yaitu tiamin (B1), Riboflavin (B2), peridoksin (B6), kobalamin atau antianemia (B12), niasin, folat, dan pantotenat. Di samping itu kadangkala terdapat vitamin C.
Jenis Vitamin Berdasar pada Kelarutannya
Berdasarkan kelarutannya, vitamin dapat dibedakan menjadi dua, yaitu vitamin yang larut dalam lemak (vitamin A, D, E, dan K) dan larut dalam air (vitamin B dan C). Telah disebutkan di depan bahwa tubuh kita membutuhkan sedikit vitamin. Secara umum vitamin berfungsi sebagai pengatur proses-proses kimia dalam tubuh. Agar lebih jelas, perhatikan uraian berikut.
47 Tiamin (vitamin B1): Kadar tiamin rata-rata pada daging ikan telah diketahui yaitu sekitar 0,04 mg/100g daging ikan. Struktur kimia tiamin berbobot molekul 337, dapat dilihat pada gambar dibawah.
Molekul ini tersusun dari inti pirimidin dan inti tiazol yang dihubungkan oleh jembatan metilen (-CH2-). Bagian pirimidin mempunyai kemantapan nisbi tinggi, sedangkan bagian tiazol segera terbuka di dalam larutan alkalis. Tiamin mengandung sebuah gugus amino pada lingkar pirimidin dan nitrogen kuartener yang sangat aktif pada lingkar tiazol. Lingkar tiazol juga mengandung sebuah gugus etoksi yang melakukan reaksi seperti gugus hidroksil dan penting untuk kesehatan enzim.
Riboflavin (vitamin B2): Kadar riboflavin rata-rata pada daging ikan adalah sekitar 0,07 mg/100g daging ikan. Adapun struktur kimia riboflavin dapat dilihat pada gambar berikut.
Molekul riboflavin terdiri atas struktur lingkar isoalixazin dan rantai samping gula pentose (ribosa). Riboflavin disintesis oleh semua tumbuhan hijau dan oleh kebanyakan bakteri, jamur, kapang, dan khamir.
Kelompok piridoksin (vitamin B6): Vitamin B6 bukanlah suatu zat tunggal, tetapi terdiri dari 3 senyawaan yang berkaitan, yaitu peridoksin, piridoksal, dan
48 piridoksamin. Adapun tumus struktur ketiga jenis persenyawaan ini adalah sebagai berikut:
Piridoksin disintesis oleh tumbuhan hijau daun dan mikroorganisme. Vitamin B6 ini sebagian besar terdapat dalam jaringan sebagai fosfat piridoksal dan piridoksamin. Fosfat piridoksal berfungsi sebagai koenzim dalam sejumlah reaksi kimia yang melibatkan asam-asam amino.
Sianokobalamine (vitamin B12): Vitamin B12 adalah senyawa Kristal berwarna merah tua. Vitamin ini mengandung inti porfirin dan logam berat kobalt. Bentuk koenzim B12 mempunyai sebuah gugus 5 deoksiandenosil terikat pada gugus metilen. Vitamin B12 bukanlah zat tunggal, melainkan terdiri atas beberapa senyawa yang berkaitan erat dan mempunyai kegiatan serupa. Struktur kimia vitamin B12 dapat dilihat seperti pada gambar berikut.
49 Vitamin C (asam askorbat): Kandungan vitamin C pada ikan sangat sedikit yaitu hanya rata-rata 0,33 mg/100g dengan pengecualian pada daging ikan tuna yang mencapai 0,51 mg/100g daging ikan. Rumus struktur asam L-askorbat dan L-awahidroL-askorbat dapat dilihat pada gambar berikut.
Tumbuhan dan mamalia selain manusia, kera, dan marmot dapat mensintesis asam askorbat. Asam askorbat ini meningkatkan penyerapan besi dari dalam usus. Selain itu asam askorbat ikut dalam pengangkutan atau transport elektron, dan mempercepat penyembuhan luka dengan pembentukan jaringan ikat baru.
50 Vitamin A (anti xeroftalmia): Vitamin A terbagi 2 jenis, yaitu vitamin A1 dan vitamin A2, yang dibedakan pada jumlah ikatan rangkat pada cincin pirolnya. Pada vitamin A1 hanya terdapat satu ikatan rangkap, sedangkan vitamin A2 terdapat dua ikatan rangkap. Rumus struktur vitamin A1 dan A2 bisa dilihat sebagai berikut.
Vitamin D: Vitamin D adalah suatu istilah yang digunakan untuk menyatakan sekelompok senyawa yang mirip secara kimia. Terdapat 11 sterol yang mempunyai kegiatan seperti vitamin D, antara lain vitamin D2 (kalsiferol) dan vitamin D3 (kolesterol aktif). Selain itu, di alam terdapat juga ergosterol (provitamin D2) dan 7-dehidrokolesterol (provitamin D3).
Vitamin D3 adalah bentuk vitamin yang terkandung dalam kebanyakan minyak hati ikan, merupakan bentuk yang dihasilkan oleh kegiatan sinar matahari pada 7-dehidrokolesterol dalam kulit ikan. Mekanisme pembentukan vitamin D3 bisa dilihat pada gambar berikut
.
Pada beberapa spesies seperti ikan cod, penimbunan vitamin A dan D ditemukan dalam hati. Sedangkan pada ikan herring, vitamin D ditemukan dalam kelenjar tubuh. Selanjutnya pada ikan cucut dan pari sedikit mengandung vitamin D.
Vitamin E (antisterilitas): Vitamin E terdapat dalam beberapa bentuk, yaitu alpha, beta, gamma, dan delta tokoferol. Struktur kimia umum tokoferol-tokoferol ini dilihat pada gambar berikut.
51 Vitamin E terdapat dalam konsentrasi terbesar di dalam minyak sesayuran dan yang terkaya adalah minyak kacang kedele. Selain itu, vitamin E juga terdapat di dalam minyak gandum, telur, dan hati ikan. Adapun kandungan vitamin E pada hati ikan sekitar 0,53 mg/100g hati ikan.
Senyawa Anti-Vitamin
Untuk mendukung proses metabolisme tubuh dan meningkatkan daya tahan tubuh, makhluk hidup membutuhkan asupan makanan yang banyak mengandung gizi. Memang ada sebagian zat yang sudah dapat diproduksi oleh tubuh namun sebagian besar zat gizi lainnya harus diperoleh dari makanan maupun minuman yang dikonsumsi. Namun agar kandungan gizi dapat optimal diserap oleh tubuh, harus diwaspadai adanya antivitamin yang terdapat dalam makanan.
Antivitamin adalah senyawa yang berpengaruh menghambat atau meniadakan kerja vitamin. Sifat ini disebabkan karena rumus bangun kimiawi yang hampir sama dengan vitamin, sehingga ada kompetisi antara vitamin dan anti-vitamin atau karena anti-vitamin bereaksi dengan vitamin itu. Zat ini bisa bersifat alami maupun hasil sintesis kimiawi buatan pabrik yang mengandung struktur atau komposisi kimiawi yang mirip dengan vitamin atau memang merupakan derivate dari vitamin, sehingga menimbulkan kompetisi. Keduanya bersifat saling antagonis dan saling meniadakan.
52 Defisiensi Vitamin
Memang tidak ada bahaya langsung masuknya vitamin dengan zat antagonisnya tersebut bagi tubuh secara langsung. Zat ini berbeda dengan racun atau bahan kimia lainnya yang langsung bereaksi dan dapat segera dirasakan akibatnya terhadap tubuh. Meskipun demikian, apabila hal tersebut berlangsung secara terus-menerus dan terjadi pada jenis vitamin tertentu. Hal inilah yang kemudian menyebabkan terjadinya defisiensi vitamin.
Defisiensi vitamin dapat terjadi akibat obat dan toksin yang menghambat protein pengangkut vitamin, enzim pada jalur biosintetik, atau protein pengikat koenzim. Senyawa yang menimbulkan defisiensi vitamin kadang-kadang disebut antivitamin.
Cara Kerja Anti-vitamin
Ada beberapa mekanisme kerja anti vitamin dalam tubuh. Selain berkompetisi dan saling meniadakan, ada juga zat antagonis yang menyebabkan enzim tak dapat berfungsi akibat tempat molekul vitamin dalam enzim direbut oleh zat antagonisnya. Selain itu juga ada zat antagonis yang justru bereaksi dengan vitamin membentuk zat baru yang lebih kompleks, sehingga vitamin juga tak dapat diserap oleh tubuh.
Berikut tabel vitamin dan anti - vitaminnya :
NO VITAMIN ANTI-VITAMIN
1 Vitamin A Citral
2 Vitamin D B- karotin (rumput kering)
3 Vitamin E -
4 Vitamin K Dicoumarol, warafrin
5 Tiamin Tiaminase (ikan segar, kerang, khamir);
neo-piritiamin, oxytiamin
6 Riboflavin Isoriboflavin, fenilriboflavin
7 Niasin Indol acetic acid
8 Piridoksin 4-deoksipiridoksin; 4-metoksipiridoksin
9 Biotin Avidin (putih telur mentah), lisolesitin
10 Cholin Tri-etil kolin
11 Asam Folat Aminopterin, ametoptern
12 Vit C Glucoascorbic acid
Pa da kea daa n ter te ntu ba ha n pa nga n da pa t me nga ndung s ua tu za t ya ng bisa me ngha la ngi a ktivitas s ua tu vita min da n ba hka n me r usa knya . Za t ya ng de mikia n dise but a vita min a ta u a nti-me ta bo lit untuk vita min terse but.
53 C ontoh Anti-vita min
Pa da r a ns um untuk tikus putih de nga n ka da r timin c ukup, pe na mba ha n a ntivita min be r upa piritia min, ya ng me r upa ka n for mula de nga n s tr uktur kimia ha mpir mirip de nga n tia min, ha nya sa ja pir itia min me nga ndung ke le biha n dua s ulf ur , ge ja la def is ie ns i tia min ter ja di. Ge ja la ya ng timbul te rs e but da pa t dia tasi de nga n pe na mba ha n le ve l tia min ya ng le bih tinggi. Io n- io n bis ulf it dar i pir itia min ber sifa t sa nga t mer usa k tia min de nga n c ara me meca h mo le kul tia min me nja di pir imidin da n tia zo l.
Pa da putih te lur ter da pat zat kimia a nti- vita min B6 , jika me ma ka n ini ma ka tubuh a ka n def ic it vita min ini. Pa da kuning te lur la h ter da pa t za t kimia ya ng me ne tra lka n a nti- vita min B6 itu.
Etanol adalah suatu antivitamin yang menurunkan konsentrasi hampir semua koenzim di dalam sel. Misalnya, etanol menghambat penyerapan tiamin, dan asetaldehida yang dihasilkan dari oksidasi etanol menggeser piridoksal fosfat dari tempat ikatan proteinnya, sehingga mempercepat degradasi piridoksal fosfat
C ontoh antivita min pada i kan
Ge ja la par a lis is pa da tikus ya ng dibe ri ika n me nta h. Para lisis ters e but dise ba bka n o le h s ua tu a ntivita min ya ng te r ka ndung pa da ika n me nta h ter te ntu ya ng mer usa k tia min. Antivita min te rse but ber upa e nzim tia minase , ya ng me me ca h mo le kul tia min me nja di d ua ba gia n ko mpo ne n pe nyus unnya , se hingga tida k berf ungs i la gi.
54 Kegiatan Belajar 2 : Mineral
Tujuan:
Mahasiswa mampu menjelaskan tentang mineral, struktur, sifat, peranan dan sumber mineral yang berperan dalam metabolism.
Mineral
Definisi mineral menurut pandangan nutrisi adalah suatu bahan anorganik yang dibutuhkan untuk proses kehidupan baik dalam bentuk ion atau elemen bebas. Mineral dapat diperoleh dari makanan karena tubuh tidak dapat memproduksi mineral). Elemen yang dibutuhkan tubuh terbagi 2 yaitu mikroelemen dan makro elemen. Makro elemen meliputi: sodium, potasium, klorida, magnesium, fosfor dan kalsium, sedangkan mikro elemen: besi, tembaga, zinc, yod, dan fluor.
Fungsi mineral antara lain sebagai katalisator berbagai reaksi biokimawi dalam tubuh, transmisi sinyal / pesan pada sel saraf, membantu produksi hormone, berperan dalam pencernaan dan penggunaan makanan, juga merupakan bagian dari organ vital seperti tulang, darah, gigi.
Mineral sebagai kofaktor: Banyak enzim yang mengandung ion metal (metaloenzim). Ion tersebut berfungsi mirip dengan koenzim. Fungsi dari metal tersebut dalam enzim sangat bervariasi, bisa sebagai katalis contohnya Zn. Adapula metal yang penting untuk meningkatkan efisiensi enzim, seperti ATP-Mg.
Magnesium (Mg)
Merupakan kation bivalent, cenderung berfungsi sebagai “chelator”. Lebih banyak ditemukan di intraseluler sel daripada di dalam serum darah. Mineral penting, selain Ca dan fosfor, terdapat di intraseluler sel yang sering ditemukan berikatan dengan ATP (berperan sebagai kofaktor). ATP yang berikatan dengan Mg merupakan substrat yang lebih efektif bagi enzim – enzim yang membutuhkan ATP.
Mg penting bagi manusia karena berperan dalam reaksi penghasilan energi . Pompa Na/K yang mengatur konsentrasi elektrolit di dalam sel, dikontrol oleh ATP sehingga keseimbangan elektrolit di dalam sel sangat tergantung pada Mg. Pengolahan makanan seringkali menghilangkan Mg dalam makanan.
55 Kalsium (Ca)
Merupakan mineral yang sulit diperoleh dari makanan kita sehari-hari. Berfungsi pada kontraksi otot, secondary messenger, pembentukan tulang dan otot, koagulasi darah, pemecahan glikogen dan aktivator siklus kreb. Untuk melakukan kontraksi, otot membutuhkan ATP (dalam myofibril), tapi yang menstimulasi terjadinya kontraksi adalah Ca.
Potassium (K)
Merupakan mineral esensial dan dikenal sebagai elektrolit. Fungsi tubuh dalam keadaan normal tergantung pada konsentrasi K di dalam dan luar sel. Berfungsi menjaga potensial membran sel dan sebagai kofaktor enzim. Pada membrane sel, K menjadi kation utama di dalam sel, sedangkan N sebagai kation utama di luar sel. K di dalam sel berjumlah 30 kali lebih tinggi dibanding di luar sel, sedangkan Na di luar sel sebanyak 10 X lebih tingg jika dibandingkan dengan di dalam sel. Perbedaan konsentrasi berupa gradien elektrokimiawi membran menghasilkan potensial membrane. Potensial membran penting dalam penyampaian sinyal untuk komunikasi antar sel pada sel saraf. K juga berperan sebagai kofaktor contohnya pyruvat kinase pada metabolisme karbohidrat.
Besi (Fe)
Menjalankan fungsi utamanya bersama-sama dengan protein dan tembaga membentuk hemoglobin (memindahkan O2 dari paru-paru ke jaringan yang membutuhkan). Penting pula untuk pembentukan myoglobulin (pengangkut O2 di dalam otot). Penting untuk penderita thyroidisme. Keseimbangan antara Fe, Zn dan Cu sangat penting untuk menjaga dan mencegah thyroidisme.
56 Fe terdapat dalam bentuk Ferro (Fe2+) atau Ferri (Fe3+) dimana di dalam tubuh ditemukan berasosiasi dengan protein. Di dalam tubuh tersimpan dalam jumlah besar dalam protein disebut ferritin . Dalam bentuk bebas di dalam tubuh konsentrasinya sangat rendah. Karena ion ferri tidak larut dalam air. Mungkin ion ferro toksik bagi sel karena bereaksi dengan hidrogen peroksida membentuk radikal hidroksil.
Makanan biasa mengandung ion ferri, sedangkan untuk mudah diserap tubuh harus berada dalam bentuk ion ferro. Karenanya reduksi ion ferri menjadi ion ferro membutuhkan asam askorbat (vit C) atau dengan suksinat.
Zinc (Zn)
Element essensial dalam makanan baik pada tumbuhan, hewan dan manusia. Dibutuhkan untuk pembentukan substansi genetik dalam sel dan untuk reproduksi biologis. Diperlukan juga dalam sintesis DNA dan RNA. Merupakan bagian dari ± 200 metaloenzim. Defisiensi Zn tidak spesifik karena banyaknya enzim yang membutuhkan Zn.
57 Daftar Pustaka Chiyaniezz.blogspot.com/2011/04/fungsi-vitamin-k.htmlId.wikipedia.org/wiki/vitamin(a,d,e,k) Kesehatan.kompas.com/read/2010/06/tanda.kekurangan.vitamin Ridwanaz.com/kesehatan/pengertian-vitamin-jenis-jenis-vitamin-sumber-sumber-vitamin/
Suwetja,I.K.2011.Biokimia Hasil Perikanan.Media Prima Aksara : Jakarta Anne. 2010. Senyawa Anti Vitamin.
http://www.anneahira.com/anti-vitamin.htm, diakses tanggal 13 Oktober 2012.
dr.brahm U. 1996.Biokimia kedokteran dasar. Jakarta. penerbit : EGC. http://majalahkesehatan.com/jenis-jenis-vitamin-yang-wajib-anda-ketahui,
diakses tanggal 13 Oktober 2012.
http://www.kesehatan123.com/2453/fungsi-vitamin-dan-manfaatnya, diakses tanggal 13 Oktober 2012.
Pramono, Pram. 04 Juli 2009. http://gizisehat.wordpress.com, diakses tanggal 13 Oktober 2012.
Wikipedia. Vitamin. http://id.wikipedia.org/wiki/Vitamin, diakses tanggal 13 Oktober 2012.
58
MODUL 5
ENZIM
Tujuan:
Setelah mengikuti topik enzim, mahasiswa mampu menjelaskan tentang fungsi, klasifikasi dan pengujian enzim. Selain itu mampu menjelaskan pengertian termodinamik, energi aktivasi, perubahan energi bebas, dan keseimbangan kimia dalam proses reaksi yang melibatkan enzim sebagai katalis dan kinetika enzim, juga mampu menjelaskan tentang senyawa yang dapat menghambat kerja enzim, dan mekanisme penghambatannya.
Enzim
Merupakan suatu protein yang bekerja sebagai katalis pada organisme hidup, mengatur kecepatan dimana reaksi kimia diproses dan enzim itu tidak berubah dalam proses tersebut. Proses biologis pada seluruh organisme hidup adalah reaksi kimia dan kebanyakan diatur oleh enzim, tanpa enzim banyak reaksi kimia ini tidak akan terjadi. Enzim mengkatalisa semua aspek metabolisme sel.
Enzim yang strukturnya sempurna dan aktif mengkatalisis, bersama-sama dengan koenzim atau gugus logamnya disebut holoenzim. Secara ringkas
struktur sebuah enzim yang aktif dapat dilihat pada bagan di bawah ini:
Kofaktor pada beberapa enzim dapat terikat secara lemah atau terikat secara kuat (permanent). Jika kofaktor terikat kuat dengan protein enzim dinamakan bagian prostetik. Yang berperan sebagai kofaktor umumnya adalah logam seperti yang terlihat pada Tabel di bawah ini:
59 Tidak semua enzim memiliki struktur yang lengkap terdiri dari apoenzim dan kofaktor. Contoh enzim ribonuklease pankreas hanya terdiri atas polipeptida dan tidak mengandung gugus kimiawi yang lain.
Sisi aktif enzim
Sisi aktif enzim (active site) adalah bagian dari molekul enzim tempat berikatannya substrat, untuk membentuk kompleks enzim substrat, dan selanjutnya membentuk produk akhir. Sisi aktif suatu enzim berbentuk tiga dimensi, sering berupa lekukan pada permukaan protein enzim, tempat substrat berikatan secara lemah. Substrat berikatan dengan sisi aktif suatu enzim melalui beberapa bentuk ikatan kimia yang lemah (misalnya interaksi elektrostatik, ikatan hidrogen, ikatan van der Waals, dan interaksi hidrofobik).
Koenzim Senyawa yang Dipindahkan
1.Thiamin pirofosfat
2. Flavin adenin dinukleotida (FAD)
3. Nikotinamida adenine dinukleotida (NAD) 4. Koenzim A 5. Piridoksal fosfat 6. 5’- deoksiadenosilkobalamin (koenzim B12) 7. Biositin 8. Tetrahidrofolat Aldehida Atom hidrogen Ion hidrida (H-) Gugus asil Gugus amino
Atom H dan gugus alkyl CO2
60 Setelah berikatan dengan bagian sisi aktif enzim, substrat bersama-sama enzim kemudian membentuk suatu kompleks enzim-substrat, selanjutnya terjadi proses katalisis oleh enzim untuk membentuk produk. Ketika produk sudah terbentuk enzim menjadi bebas kembali untuk selanjutnya bereaksi kembali dengan substrat.
Mekanisme kerja enzim
Dua model telah diusulkan untuk menjelaskan bagaimana enzim berikatan dengan substrat:
61 1) Model kunci – dan anak kunci yang diusulkan oleh Emil Fisher pada tahun 1894, yang menyatakan bahwa bentuk molekul substrat dengan sisi aktif enzim serupa dengan anak kunci dengan kuncinya.
2) Induced-fit model diusulkan pada tahun 1958 oleh Daniel E. Koshland, Jr. yang menyatakan bahwa terikatnya substrat menyebabkan perubahan konformasi pada bagian sisi aktif enzim.
Proses terikatnya substrat pada enzim (a) model anak kunci – kuncinya, (b) induced – fit model
Klasifikasi enzim
Banyak enzim yang telah dinamakan dengan menambahkan akhiran ase kepada nama substratnya, misalnya urease mengkatalisis hidrolisis urea, amilase menghidrolisis amilum. Tetapi banyak pula enzim yang dinamakan tidak berdasarkan nama substratnya, misalnya tripsin dan pepsin. Juga ada enzim yang dikenal dengan dua nama, misalnya amilase yang dihasilkan kelenjar ludah dinamakan pula ptialin. Karena itu, dan juga dengan terus meningkatnya jumlah enzim yang baru ditemukan, suatu dasar penggolongan enzim secara sistematis telah dikemukakan oleh persetujuan Internasional. Sistem ini menempatkan semua enzim ke dalam enam kelas utama, masing-masing dengan subkelas, berdasarkan atas jenis reaksi yang dikatalisisnya
62 Tiap-tiap enzim ditetapkan ke dalam empat tingkat nomor kelas dan diberikan suatu nama sistematik, yang mengidentifikasi reaksi yang dikatalisis. Contoh, enzim yang mengkatalisis reaksi:
ATP + D-glukosa ADP + D-glukosa – 6 – fosfat
Nama sistematik formal enzim ini adalah: fosfotransferase ATP: glukosa, yang menunjukkan bahwa enzim ini mengkatalisis pemindahan gugus fosfat dari ATP ke glukosa. Enzim ini ditempatkan ke dalam kelas 2 pada tabel 4, dan nomor klasifikasinya adalah 2.7.1.1, dengan bilangan pertama (yaitu 2) menunjukkan nama kelas (transferase), bilangan kedua (7 ) bagi subkelas (fosfotransferase) dan bilangan ketiga (1) bagi sub-sub kelas (fosfotransferase dengan gugus hidroksil sebagai penerima), dan bilangan keempat (1) bagi D-glukosa sebagai penerima gugus fosfat. Jika nama sistematiknya rumit, maka nama biasa dari enzim ini adalah heksokinase.
Sifat-Sifat Enzim
Enzim Sebagai Katalisator.
Enzim merupakan katalis yang dapat mengubah laju reaksi tanpa ikut bereaksi. Enzim bersifat khas kerjanya dan aktivitasnya dapat diatur. Tanpa kehadiran enzim, suatu reaksi itu sangat sukar terjadi, sementara dengan kehadiran enzim kecepatan reaksinya dapat meningkat sampai 107 kali. Sebagai contoh, enzim katalase yang mengandung ion besi (Fe) mampu menguraikan 5.000.000 molekul hidrogen peroksida (H2O2) permenit pada 0o C. H2O2 hanya