commit to user
i
ANALISIS GEN 16S rRNA PADA BAKTERI PENGHASIL ENZIM FITASE
TESIS
Disusun untuk memenuhi sebagian persyaratan
Guna memperoleh gelar Magister Sains
Program Studi Biosains
Oleh
Rita Wulandari
S 900809016
PROGRAM PASCA SARJANA
UNIVERSITAS SEBELAS MARET
commit to user
ii
ANALISIS GEN 16S rRNA PADA BAKTERI PENGHASIL ENZIM FITASE
TESIS
Oleh
Rita Wulandari
S 900809016
Telah disetujui oleh pembimbing
Komisi
Pembimbing Nama Tanda tangan Tanggal
Pembimbing I Prof. Dr. rer. nat. Sajidan, M.Si ……… ………..………
Pembimbing II Prof. Drs. Suranto, M.Sc, Ph.D ……… ………..
Mengetahui
Ketua Program Studi Biosains Program Pasca Sarjana
commit to user
iii
ANALISIS GEN 16S rRNA PADA BAKTERI PENGHASIL ENZIM FITASE
TESIS
Oleh
Rita Wulandari S900809016
Telah dipertahankan di depan penguji Dinyatakan telah memenuhi syarat Pada tanggal...2011
Telah disetujui oleh tim penguji
Jabatan Nama Tanda Tangan Tanggal
Ketua Prof. Dr Sugiyarto, M.Si
NIP. 19670430 199203 1 002 ...2011
Sekertaris Dr. Edwi Mahajoeno, M.Si
NIP.19601025 199702 1 001 ...2011
Anggota Penguji
Prof. Dr. rer. nat. Sajidan, M.Si NIP.19660415 199103 1 002
Prof. Drs. Suranto, MSc., PhD NIP.19570820 198503 1 004
...2011
...2011
Mengesahkan Direktur Program Pasca Sarjana
Prof. Drs. Suranto, MSc., PhD NIP.19570820 198503 1 004
Ketua Program Studi Biosain
commit to user
iv
PERNYATAAN ORISINALITAS DAN PUBLIKASI TESIS
Saya menyatakan dengan sebenar-benarnya bahwa :
1. Tesis yang berjudul : “Analisis gen 16s rRNA pada bakteri penghasil
enzim fitase” ini adalah karya penelitian saya sendiri dan tidak terdapat
karya ilmiah yang pernah diajukan oleh orang lain untuk memperoleh gelar akademik serta tidak terdapat karya atau pendapat yang pernah ditulis atau diterbitkan oleh orang lain, kecuali yang secara tertulis dikutip dalam naskah ini dan disebutkan dalam sumber kutipan dan daftar pustaka. Apabila ternyata di dalam naskah Tesis ini dapat dibuktikan terdapat unsure-unsur jiplakan, maka saya bersedia Tesis beserta gelar MAGISTER saya dibatalkan, serta diproses sesuai dengan peraturan perundang-undangan yang berlaku (UU No.20 Tahun 2003, pasal 25 ayat 2 dan pasal 70).
2. Tesis ini merupakan hak milik Prodi BIosains PPs-UNS. Publikasi sebagian atau keseluruhan isi Tesis pada jurnal atau forum ilmiah lain harus seijin Ketua Prodi Biosains PPS-UNS dan minimal satu kali publikasi menyertakan tim pembimbing sebagai author. Apabila dalam waktu sekurang-kurangnya satu semester (6 bulan sejak pengesahan Tesis) saya tidak melakukan publikasi dari sebagian atau keseluruhan Tesis ini, maka Prodi Biosains PPS-UNS berhak mempublikasikannya pada jurnal ilmiah yang diterbitkan oleh Prodi Biosains PPS-UNS dan atau media yang ditunjuk. Apabila saya melakukan pelanggaran dari ketentuan publikasi ini, maka saya bersedia mendapatkan sanksi akademik yang berlaku.
Surakarta, 20 Desember 2011 Mahasiswa,
Rita Wulandari
commit to user
v
ANALISIS GEN 16s rRNA PADA BAKTERI PENGHASIL ENZIM FITASE
Rita Wulandari, Sajidan, Suranto
Program Studi Magister Biosains, Program Pasca Sarjana Universitas Sebelas Maret Surakarta
Abstrak
Fitase merupakan enzim yang mampu melepaskan ikatan fosfat pada fitat, menghasilkan myo-inositol dan fosfat inorganik. Fitase mempunyai peran penting dalam ketersediaan nutrisi pada bahan pangan. Bakteri merupakan salah satu sumber penghasil fitase yang potensial sehingga perlu dilakukan penggalian galur bakteri penghasil fitase dari lingkungan. Tujuan dari penelitian ini adalah (1) Mengukur aktivitas fitase pada bakteri dari abu vulkanik Gunung Merapi, (2) Mengidentifikasi bakteri penghasil fitase berdasarkan gen 16S rRNA, (3) Mengkarakterisasi ekstrak fitase yang diperoleh dari bakteri penghasil fitase pada abu vulkanik Gunung Merapi.
Bakteri diisolasi dari Abu vulkanik gunung Merapi dalam media LB (Luria Bertani) dan media LB (Luria Bertani) + Na fitat 0,4%. Aktivitas fitase diukur dengan metode spektrofotometri. Sebanyak 3 isolat bakteri dengan aktivitas fitase tertinggi diidentikasi dengan marka gen 16s rRNA menggunakan primer universal. Karakterisasi ekstrak kasar fitase meliputi pH optimum, suhu optimum dan efektor logam.
Hasil penelitian diperoleh 3 isolat dengan aktivitas fitase terbesar, yaitu isolat RW Sm A, RW Sm C, dan RW Sl 5 masing-masing dengan aktivitas fitase sebesar 0,1071 U/mL, 0,1020 U/mL dan, 0,0874 U/mL. Berdasarkan analisis gen 16s rRNA ketiga isolat diketahui sebagai Bacilllus cereus RW Sm A, Bacillus aryabhattai RW Sm C dan Bacillus cereus RW Sl 5. Ekstrak kasar fitase dari ketiga isolat masing-masing mempunyai suhu optimum berturut turut; 40 oC, 60
o
C, 50 oC. pH optimum ketiga isolat berkisar antara 5-6. Aktivitas fitase isolat dihambat oleh penambahan ion Fe3+, dan Zn2+, tetapi meningkat dengan penambahan ion Ca2+.
commit to user
vi
16s rRNA GENE ANALYSIS ON PHYTASE-PRODUCING BACTERIA
Rita Wulandari, Sajidan and Suranto Biosience Program, School of Graduates
Sebelas Maret University of Surakarta
Abstract
Phytases is an enzyme that catalyzes the releasing of phosphomonoester bonds in phytate, thereby producing lower forms of myo-inositol phosphates and inorganic phosphate. Phytase has important role in animal and human nutrition availability. Bacteria is one of potential source of phytase,so more excavation for phytase-producing strains of bacteria from the environment is needed. The purposes of this study are (1) Analyzing the phytase activity bacteria from volcanic ash of Merapi mountain, (2) Identifying of phytase producing bacteria based on 16S rRNA gene, (3) Characterizing of extracted phytase from bacteria on volcanic ash of Merapi Mountain.
Bacteria were isolated from volcanic ash of Merapi Mountain in LB (Luria Bertani) medium and LB (Luria Bertani) + 0.4% Na phytate. Phytase activity measure by spectrophotometric methods. Three isolates of bacteria with the highest activity was identified with 16s rRNA gene markers using universal primer. Crude phytase extract characterization including optimum pH, optimum temperature and mineral efector.
The results should that for three isolates with the largest phytase activity, ie isolates RW Sm A, RW Sm C and RW Sl 5 with phytase activity 0.1071 U / mL, 0.1020 U / mL and, 0.0874 U / mL. Based on 16s rRNA gene analysis of three isolates known as Bacilllus cereus RW Sm A, Bacillus aryabhattai RW Sm C and Bacillus cereus RW Sl 5. Three isolated of crude phytase extractions have an optimum temperature 40 °C, 60 °C, 50 °C respectively, range of the optimum pH between 5-6.Phytase activity was inhibited by the addition of Fe3+ ions, and Zn2+, but increased with the addition of Ca2 + ion.
commit to user
vii
HALAMAN PERSEMBAHAN
Segala puji bagi Allah Tuhan semesta alam.
Karya ilmiah ini penulis persembahkan kepada,
Ibu Darmini dan bapak Sarjono tercinta, Suamiku, Muhammad Irham Mahfud tercinta,
commit to user
viii
KATA PENGANTAR
Segala puji bagi Allah Tuhan semesta alam, atas limpahan rahmat dan
hidayah-NYA penulis dapat menyelesaikan tesis yang berjudul: “Analisis gen
16s rRNA pada bakteri penghasil enzim fitase”. Tulisan ini menyajikan
bahasan tentang bakteri penghasil enzim fitase, identifikasi, dan karakteristik
enzim yang dihasilkan.
Penelitian ini mempunyai nilai penting dalam penemuan sumber enzim
fitase baru yang diisolasi dari lingkungan sehingga memperkaya sumber enzim
fitase dari mikroorganisme yang berasal dari lingkungan dan wilayah berbeda.
Adanya bakteri penghasil fitase yang diisolasi dari lingkungan vulkanik
diharapkan menambah keberagaman jenis bakteri sumber enzim fitase.
Identifikasi dan karakteristik enzim yang diperoleh selanjutnya dapat digunakan
dan dikembangkan untuk karakterisasi dalam aplikasi bioteknologi serta
pengembangan teknik rekayasa genetika untuk mendapatkan enzim yang lebih
optimal.
Kekurangan penulis dalam mengungkapkan ide, gagasan dan eksplorasi
hasil merupakan keterbatasan yang penulis miliki. Berbagai saran yang
membangun penulis harapkan untuk menambah kemanfaatan tulisan ini.
commit to user
ix
UCAPAN TERIMA KASIH
Segala puji bagi Allah Tuhan semesta alam, atas segala rahmat dan karunia yang senantiasa tercurah, sehingga penulis dapat menyelesaikan Tesis dengan judul ” Analisis gen 16s rRNA pada bakteri penghasil enzim fitase”. Penyusunan tesis ini tidak lepas dari bantuan, kerjasama dan bimbingan berbagai pihak, oleh karena itu penulis menyampaikan rasa hormat dan terima kasih yang sebesar-besarnya kepada :
1. Rektor Universitas Sebelas Maret yang telah memberikan ijin untuk mengadakan penelitian ini.
2. Prof. Drs. Suranto, M.Sc, Ph.D selaku Direktur Program Pascasarjana Universitas Sebelas Maret yang telah memberikan kesempatan yang seluas-luasnya mengikuti pendidikan pascasarjana.
3. Prof. Dr. Sugiyarto, M.Si dan Dr. Edwi Mahajoeno, M.Si selaku Pengelola Program Studi BIOSAIN yang telah membimbing dan memotivasi dalam menyelesaikan program pembelajaran.
4. Prof. Dr. rer. nat. Sajidan, M.Si selaku pembimbing pertama dan Prof. Drs. Suranto, M.Sc, Ph.D selaku pembimbing kedua yang telah berkenan memberi bimbingan sepenuhnya sampai tesis ini dapat penulis selesaikan 5. Prof. Dr. rer. nat. Sajidan, M.Si selaku ketua Tim peneliti yang telah
mensupport dana untuk rangkaian penelitian ini
6. Bapak Adi Magna Patriadi Nuhriawangsa, S.Pt., M.P, bapak Dr. sc. agr. Adi Ratriyanto, S.Pt., M.P, dan Umi Fatmawati M.Si yang telah bekerjasama dan membantu penelitian ini
7. Semua dosen Program studi Biosain yang telah memberikan ilmu, bantuan dan pengarahan
8. Seluruh staff UPT sub Laboratorium BIOLOGI Universitas Sebelas Maret yang telah berkenan mengijinkan dan membantu penulis dalam melakukan penelitian
commit to user
x
10. Seluruh staff Laboratorium Prodi P. Biologi FKIP Universitas Sebelas Maret yang telah berkenan memberi ijin penelitian bagi penulis.
11. Evi Novitasari, Suci, Lala dan mbak Tri, atas kerjasama serta bantuan selama penyelesaian penelitian, mas Rosyid dan dek Ivah, atas bantuan dalam berbagai urusan administrasi.
12. Teman-teman Biosain angkatan 2009 (Pipit, Ana, Ainun, Nina, Dodik, Zahra, Mbak Ifan, Pak Hamdin, Pak Supriyadi, Bu Yayuk, Bu Mamik, Bu Nony, Phyllis, Bundo Ria, Bundo Tiwuk, Bu Turweni, Pak Muryanto, Pak Inpurwanto, Pak Heru, Pak Amar, Pak Supono) yang telah memberikan bantuan, dukungan dan kerjasama.
13. Ibu Darmini, bapak Sarjono, yang selalu memberi restu, dan doa-doa disetiap langkah penulis, dek Arum, mas Yus, Ibu Tasmiyati, bapak Ahmad Sardi, mbak Laily, mbak Nana, mas Udin, dek Fitri, yang semakin membuat penulis bersyukur berada ditengah tengah keluarga ini.
14. Abi, Muhammad Irham Mahfud, sebagai partner sepanjang waktu yang selalu mendukung, memotivasi, mendoakan, dan juga telah membantu dalam akses berbagai jurnal selama penulisan tesis ini.
15. Semua pihak yang tidak bisa penulis sebutkan satu persatu yang telah berkontribusi dalam penyelesaian tesis ini.
Semoga segala kebaikan dibalas dengan kebaikan yang lebih baik dari Allah SWT.
commit to user
xi
DAFTAR ISI
Halaman
JUDUL i
HALAMAN PERSETUJUAN ii
HALAMAN PENGESAHAN iii
PERNYATAAN ORISINALITAS iv
ABSTRAK v
ABSTRACT vi
HALAMAN PERSEMBAHAN vii
KATA PENGANTAR viii
UCAPAN TERIMAKASIH ix
DAFTAR ISI xi
DAFTAR TABEL xiii
DAFTAR GAMBAR xv
DAFTAR LAMPIRAN xvi
BAB I PENDAHULUAN
A. Latar Belakang 1
B. Perumusan Masalah 4
C. Tujuan Penelitian 4
D. Manfaat Penelitian 4
BAB II LANDASAN TEORI
A. Tinjauan Pustaka 5
1. Ribosomal RNA 5
1.1 Gen 16s rRNA 5 1.2 Analisis gen 16s rRNA 6
2. Asam Fitat 7
2.1 Struktur Asam fitat 7 2.2 Sumber Asam fitat 8 2.3 Ketersediaan nutrisi dan dampak lingkungan 10
3. Enzim Fitase 12
3.1 Enzim 12
3.1.1 Aktivitas Enzim 12
commit to user
xii
3.2.1 Klasifikasi Enzim Fitase 16 3.2.2 Aktifitas Enzim Fitase 19 3.2.3 Sumber Enzim Fitase 20 a. Fitase Asal Mikroba 21
b. Fitase Tanaman 23 c. Fitase pada jaringan tubuh hewan 24
B. Kerangka Penelitian 26
BAB III METODE PENELITIAN
A. Tempat dan Waktu Penelitian 27
B. Alat dan Bahan Penelitian 27
C. Rancangan Penelitian 28
D. Prosedur Penelitian 28
E. Teknik Analisis Data 33
BAB IV HASIL DAN PEMBAHASAN
A. Isolasi Bakteri Fitase 35
B. Seleksi Bakteri Fitase 37
C. Karakteristik Bakteri Fitase 40
C.1. Morfologi Sel 40
C.2. Fisiologi Sel dan Ekspresi Fitase 42
D. Identifikasi Bakteri 44
E. Karakteristik Ekstrak Kasar Fitase 53
E.1. Suhu Optimum 53
E.2. pH Optimum 54
E.3. Efektor Logam 56
F. Fitase pada Bacillus 58
BAB V. KESIMPULAN DAN SARAN
A. KESIMPULAN 61
B. SARAN 61
DAFTAR PUSTAKA 63
commit to user
xiii
DAFTAR TABEL
Halaman
Tabel 1. Ribosomal RNA 5
Tabel 2. Bahan pangan dan kandungan asam fitat 9
Tabel 3. 4 kelompok fitase 20
Tabel 4. Fitase Tanaman 23
Tabel 5. Tabel Homologi Isolat RW Sm A 49
Tabel 6. Tabel Homologi Isolat RW Sm C 50
Tabel 7. Tabel Homologi Isolat RW Sl 5
50
Tabel 8. Karakteristik Enzim Fitase pada Bacillus59
Tabel L.A1. Pembuatan Kurva Standar Phosphat 69
Tabel L. A2. Aktivitas Relatif Fitase (%) 16 Isolat Bakteri 70
Tabel L. A3. Aktivitas Fitase 16 Isolat Bakteri (U/mL) 70
Tabel L. A4. Aktivitas Relatif Fitase (%) 5 Isolat Bakteri 71
Tabel L. A5. Aktivitas Fitase 5 Isolat Bakteri 71
Tabel L. A6. Absorbansi berdasarkan lama inkubasi Isolat RW Sm A 71
Tabel L. A7. Aktivitas Fitase berdasarkan lama inkubasi Isolat RW Sm A 71
Tabel L. A8. Absorbansi berdasarkan Lama Waktu Inkubasi Isolat RW Sm C 72
Tabel L. A9. Aktivitas Fitase berdasarkan Lama Waktu Inkubasi Isolat RW Sm C 72
Tabel L. A10. Absorbansi Berdasarkan Lama waktu Inkubasi Isolat RW Sl 5 72
Tabel L. A11. Aktivitas Fitase Berdasarkan Lama waktu Inkubasi Isolat RW Sl 5 73
Tabel L. A12. Absorbansi berdasarkan pH substrat pada Isolat RW Sm A 73
Tabel L. A13. Aktivitas Fitase berdasarkan pH substrat pada Isolat RW Sm A 73
Tabel L. A14. Absorbansi berdasarkan pH substrat pada Isolat RW Sm C 74
commit to user
xiv
Tabel L. A16. Absorbansi berdasarkan pH Substrat pada Isolat
RW Sl 5 74
Tabel L. A17. Aktivitas Fitase berdasarkan pH Substrat pada Isolat
RW Sl 5 75
Tabel L. A18. Absorbansi berdasarkan Suhu Inkubasi Enzim-Substrat
pada Isolat RW Sm A 75
Tabel L. A19. Aktivitas Fitase berdasarkan Suhu Inkubasi Enzim-Substrat
pada Isolat RW Sm A 75
Tabel L. A20. Absorbansi berdasarkan Suhu Inkubasi Enzim-Substrat
pada Isolat RW Sm C 76
Tabel L. A21. Aktivitas Fitase berdasarkan Suhu Inkubasi Enzim-Substrat
pada Isolat RW Sm C 76
Tabel L. A22. Absorbansi berdasarkan Suhu Inkubasi Enzim-Substrat
pada Isolat RW Sl 5 76
Tabel L. A23. Aktivitas Fitase berdasarkan Suhu Inkubasi Enzim-Substrat
pada Isolat RW Sl 5 77
Tabel L. A24. Absorbansi Isolat RW Sm A pada pH dan Suhu optimum pada berbagai durasi pemanasan (Stabilitas Suhu) 77 Tabel L. A25. Aktivitas Fitase Isolat RW Sm A pada pH dan Suhu optimum
pada berbagai durasi pemanasan (Stabilitas Suhu) 77 Tabel L. A26. Absorbansi Isolat RW Sm C pada pH dan Suhu optimum
pada berbagai durasi pemanasan (Stabilitas Suhu) 78 Tabel L. A27. Aktivitas Fitase Isolat RW Sm C pada pH dan Suhu optimum
pada berbagai durasi pemanasan (Stabilitas Suhu) 78 Tabel L. A28. Aktivitas Fitase Isolat RW Sl 5 pada pH dan Suhu optimum
pada berbagai durasi pemanasan (Stabilitas Suhu) 78 Tabel L. A29. Aktivitas Fitase Isolat RW Sl 5 pada pH dan Suhu optimum
pada berbagai durasi pemanasan (Stabilitas Suhu) 79 Tabel L. A30. Absorbansi penambahan Efektor Logam RW Sm A 79 Tabel L. A31. Absorbansi penambahan Efektor Logam RW Sm C 79 Tabel L. A32. Absorbansi penambahan Efektor Logam RW Sl 5 80 Tabel L. A33. Aktivitas Fitase dengan penambahan Efektor Logam 80
commit to user
xv
DAFTAR GAMBAR
Halaman
Gambar 1. Struktur Aktif Enzim 8
Gambar 2. Ikatan Asam fitat dengan Fe2+ dan Protein 11
Gambar 3. Struktur aktif enzim 12
Gambar 4. Pengaruh konsentrasi enzim pada aktivitas 13
Gambar 5. Pengaruh Konsentrasi substrat pada aktivitas enzim 13
Gambar 6. Pengaruh pH pada aktivitas enzim 14
Gambar 7. Pengaruh Suhu pada aktivitas enzim 14
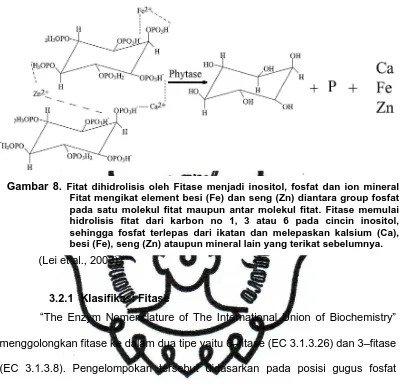
Gambar 8. Hidrolisis Fitat 16
Gambar 9. 6 – fitase (EC 3.1.3.26), fitase 3 – fitase (EC 3.1.3.8) 17 Gambar 10.Defosforilasi asam fitat oleh 3-fitase Saccaromices cerevisae.. 17
Gambar 11. Kerangka Penelitian 26
Gambar 12. Isolasi Bakteri medium cair dan padat 36
Gambar 13. Warna kuning pada reaksi vanadomolibdofosforik 38
Gambar 14. Aktivitas fitase 16 isolat bakteri 39
Gambar 15. Koloni Bakteri 40
Gambar 16. Diagram pewarnaan gram bakteri 41
Gambar 17. Perbandingan dinding sel Bakteri gram positif dan gram
Negatif 42
Gambar 18. Perbandingan fase pertumbuhan bakteri 43
Gambar 19. Elektroforesis DNA 45
Gambar 20. Elektroforegram hasil amplifikasi gen 16s rRNA 48
Gambar 21. Perbandingan urutan basa DNA 49
Gambar 22. Pohon filogenetik 52
Gambar 23. Kurva aktifitas fitase pada berbagai suhu inkubasi 54
Gambar.24a. Kurva aktivitas fitase pada berbagai pH 55
commit to user
xvi
DAFTAR LAMPIRAN
Halaman
Lampiran A. Pengukuran Aktifitas Fitase 69
Lampiran B. Pengenceran Primer 81
Lampiran C. Hasil Sekuensing isolat Bakteri 82
Lampiran D. Fasta Format sekuen DNA 83
Lampiran E. Hasil Alignment sekuen DNA 85
Lampiran F. Surat Pernyataan Kerjasama 88
Lampiran G. Jadwal kegiatan Penelitian 89
commit to user
BAB I PENDAHULUAN
A. LATAR BELAKANG
Sumber pangan makhluk hidup di alam berasal dari tumbuhan. Bahan
pangan yang berasal dari tumbuhan mengandung fosfat sebanyak 30% fosfat
bebas dan sisanya 70% terdapat dalam bentuk Fitat (Kembhavi, 2005). Asam
fitat adalah bentuk utama simpanan fosfat pada tanaman, merupakan sumber
inositol dan fosfat dalam biji tumbuhan. Asam fitat terutama terdapat pada
tanaman dari golongan serealia, biji-bijian dan polong-polongan, antara lain pada
tanaman jagung, gandum, kedelai, kacang tanah, padi dan biji bunga matahari
(Chu et al., 2000).
Asam fitat dapat menjadi sebuah komponen antinutrisi karena
kemampuannya mengikat protein dan ion mineral seperti kalsium, besi, seng,
magnesium, mangan dan copper (Chu et al, 2000). Ikatan yang kuat akan
menurunkan kelarutan, daya cerna dan penyerapan protein serta mineral (Ca,
Fe, Zn dan Mg). Komplek asam fitat bersama dengan protein enzim pencernaan
menyebabkan penurunan aktivitas enzim pencernaan.
Hidrolisis asam fitat akan sangat bermanfaat untuk meningkatkan nilai
nutrisi pada tanaman pangan. Enzim yang mengkatalis perubahan asam fitat
menjadi inositol dan fosfat inorganik adalah fitase. Ternak monogastrik seperti
babi, unggas, dan ikan tidak mampu mendegradasi asam fitat karena alat
pencernaannya sedikit menghasilkan enzim fitase. Sehingga pada hewan
monogastrik asam fitat tidak terhidrolisis dan menyebabkan ketersediaan unsur
fosfor sangat rendah dan zat makanan lain tidak dapat dimanfaatkan secara
maksimal oleh ternak. Fosfor yang tidak dicerna akan dikeluarkan melalui feces
commit to user
karena eutrofikasi yaitu terjadinya penyuburan perairan berlebihan yang akan
menyuburkan alga beracun dan menganggu ekosistem perairan.
Fitase atau mio-inositol heksakisfosfat fosfohidrolase adalah enzim yang
mengkatalis reaksi ikatan fosfodiester pada asam fitat (mio-inositol
heksakisfosfat), menghasilkan fosfat anorganik dan ester ester fosfat dari
mio-inositol yang lebih rendah. Fitase dihasilkan oleh tumbuh-tumbuhan,
mikroorganisme (bakteri, jamur, yaest) dan jaringan tubuh ternak. Fitase dapat
juga dihasilkan dari proses cloning gen Phy A dari fungi Aspergillus ficum (Ullah,
1998a), cloning gen Phy K dari bakteri Klebsiella sp. Strain ASR1 (Sajidan et al.,
2004)
Penambahan fitase pada pakan ternak dapat meningkatkan ketersediaan
fosfat, kalsium dan protein pada ternak. Beberapa penelitian tentang
penggunaan fitase dalam bentuk probiotik pada ternak telah dilakukan dengan
penggunaan bakteri penghasil fitase sebagai campuran wheat pollard pakan
ternak unggas. Diketahui campuran probiotik tersebut dapat meningkatkan
retensi protein dan mineral sehingga dapat meningkatkan pertumbuhan ayam
(Sajidan et al., 2004). Selain dimanfaatkan dalam industri pakan ternak, industri
pangan pada umumnya juga telah banyak memanfaatkan enzim fitase.
Pembuatan tepung, susu kedelai, sereal bebas fitat, pembuatan roti dan produksi
isolat protein dari tanaman menggunakan fitase dalam prosesnya.
Indonesia sebagai negara tropis mempunyai potensi keanekaragaman
bakteri yang tinggi. Karakteristik wilayah Indonesia yang mempunyai banyak
area vulkanik menambah potensi diversitas bakteri. Aktifitas bakteri fitase telah
berhasil diidentifikasi pada beberapa daerah dengan karakteristik yang berbeda,
commit to user
(Guzmanizar et al., 2009), pada ekosistem sawah, pada ladang gandum
(Shobirin, 2009), lapisan rizhosfer tanah vulkanik (Jorsquera et al., 2009).
Bakteri sebagai salah satu penghasil enzim yang potensial menjadi faktor
penting dalam produksi enzim. Oleh karena itu diperlukan usaha penggalian
galur galur bakteri penghasil fitase dari lingkungan. Pada penelitian ini dilakukan
screening mikroorganisme yang mampu menghasilkan fitase dari abu vulkanik
Gunung Merapi. Abu vulkanik yang menutup tanah dan lahan pertanian akibat
letusan Gunung Merapi pada tanggal 26 November 2010 mempunyai potensi
untuk diperoleh isolat bakteri baru sebagai penghasil enzim yang mempunyai
rentang suhu dan pH lebih lebar. Suriadikarta dkk (2010) menyebutkan adanya
kandungan fosfat pada abu vulkanik mulai dari rendah sampai tinggi. Sementara
pH abu vulkanik berkisar antara 4 – netral. Lapisan tanah vulkanik mempunyai
kandungan fosfat yang tinggi, tetapi fosfat yang tersedia sangat rendah, pada
lapisan tersebut dapat ditemukan adanya bakteri fosfat (Jorsquera., et al 2008).
Isolat bakteri yang mampu menghasilkan fitase dengan aktifitas terbesar akan
diidentifikasi berdasarkan karakter morfologi dan analisis gen 16s rRNA. Ekstrak
kasar fitase dari bakteri terpilih dikarakterisasi meliputi suhu optimum, pH
optimum, kestabilan termal dan kestabilan pH. Karakterisasi ekstrak kasar enzim
dilakukan dengan harapan akan diperoleh bakteri penghasil fitase yang dapat
commit to user
B. RUMUSAN MASALAH
Penelitian ini mempunyai rumusan masalah sebagai berikut:
1. Bagaimana aktivitas fitase pada bakteri yang berasal dari abu vulkanik
Gunung Merapi?
2. Bagaimana identitas bakteri penghasil fitase tersebut berdasarkan
metode 16S rRNA?
3. Bagaimana karakteristik ekstrak fitase yang diperoleh dari bakteri
penghasil fitase tersebut?
C. TUJUAN PENELITIAN
Penelitian ini mempunyai tujuan sebagai berikut:
1. Mengukur aktivitas fitase pada bakteri yang berasal dari abu vulkanik
Gunung Merapi
2. Mengidentifikasi bakteri penghasil fitase berdasarkan gen 16S rRNA
3. Mengkarakterisasi ekstrak fitase yang diperoleh dari bakteri penghasil
fitase pada abu vulkanik Gunung Merapi
D. MANFAAT PENELITIAN
Manfaat yang akan diperoleh dari penelitian ini antara lain:
1. Menambah keanekaragaman bakteri penghasil fitase yang berasal dari
karakteristik area yang berbeda
2. Memberi sumbangan pengetahuan terhadap biodiversitas
mikroorganisme lokal Indonesia
commit to user
BAB II
TINJAUAN PUSTAKA
A. TINJAUAN PUSTAKA
1. Ribosomal RNA
Gen rRNA mempunyai area konservatif didalam sel. Urutan basa rDNA
pada beberapa organisme sangat mirip. Gen rRNA biasa digunakan untuk
determinasi taxonomi, untuk mengetahui hubungan evolusi (filogenetik) dan
mengestimasi keberagaman bakteri. Ribosom organisme prokariotik merupakan
organ sel berukuran 70S dan terdiri dari 2 subunit besar dan kecil berukuran 30S
dan 50S, dimana huruf S menyatakan konstanta Svedberg, yaitu satuan
koefisien sentrifugasi (Tabel 1). Subunit 30S mengandung rRNA berukuran 16S
dan protein sebanyak 21 buah, sedangkan subunit 50S mengandung rRNA
berukuran 5S dan 23S, serta protein sebanyak 34 buah (Madigan dan Martinko,
2006).
Tabel 1. Ribosomal RNA
Nama Ukuran Lokasi
5s 120 Sub Unit Besar Ribosom
16s 1500 Sub Unit Kecil Ribosom
23s 2900 Sub Unit Besar Ribosom
(Stephanie, 2007)
1.2 Gen 16S rRNA
Gen 16S rRNA terletak pada DNA kromosom organisme
prokariotik yang mengkode komponen ribosom 16S rRNA yang dapat
digunakan sebagai daerah sidik jari antar spesies. Penggunaan 16s rRNA
untuk klasifikasi mikroorganisme dilakukan pertamakali oleh Carl woese,
yang mengelompokkan mikroorganisme menjadi 3 sistem utama; Archaea,
commit to user
Gen 16S rDNA digunakan untuk mempelajari identitas
organisme prokariotik dan dapat digunakan untuk mengukur perubahan
evolusi dan keterkaitan filogenetiknya (Madigan dan Martinko, 2006). Selain
16S terdapat komponen nukleotida lain yang menyusun ribosom yaitu 5S
dan 23S, namun karena ukuran 5S yang terlalu kecil dan 23S yang terlalu
besar maka dipilih 16S sebagai alat penanda sidik jari.
16S rDNA mempunyai beberapa kelebihan sebagai area sidik
jari, yaitu antara lain; gen 16S rDNA berukuran cukup besar untuk dapat
digunakan sebagai pembeda antar spesies, 16S rDNA mempunyai fungsi
konstan dalam sel, terdistribusi secara universal pada seluruh organism
prokariotik dan memiliki beberapa daerah lestari yang dapat digunakan
sebagai pembeda antar spesies. Daerah lestari pada 16S rDNA adalah
daerah yang diapit oleh dua daerah universal yang merupakan daerah yang
sama pada seluruh organism prokaroitik. Sehingga melalui daerah tersebut
dapat dirancanag sepasang primer untuk mengamplifikasi gen 16S rDNA
yang berasal dari berbagai spesies (Madigan dan Martinko, 2006).
1.3 Analisis gen 16s rRNA
Analisis gen penyandi 16S rRNA telah menjadi prosedur baku
untuk menentukan hubungan filogenetik dan menganalisis suatu ekosistem.
16S rRNA dapat digunakan sebagai penanda molekuler karena molekul ini
bersifat ubikuitus dengan fungsi yang identik pada seluruh organisme.
Molekul ini juga dapat berubah sesuai jarak evolusinya, sehingga dapat
digunakan sebagai kronometer evolusi yang baik. Molekul 16S rRNA
memiliki beberapa daerah yang memiliki urutan basa yang relatif konservatif
dan beberapa daerah urutan basanya variatif. Analisis gen penyandi 16S
commit to user
sehingga dapat dirancang suatu primer yang universal untuk seluruh
kelompok.
Indentifikasi bakteri dengan 16s rRNA dilakukan berdasarkan
perbandingan urutan basa yang konservatif. Jika urutan basa memiliki
persamaan yang tinggi maka strain dapat dimasukkan dalam satu spesies
yang sama. Sebaliknya jika derajat kesamaan urutan basa gen penyandi
16S rRNA kurang dari 97% dapat dianggap sebagai spesies baru. Data
urutan basa dari berbagai spesies mikrobia telah dikumpulkan dalam sebuah
database yang dapat diakses. Kumpulan data spesies tersebut memuat data
klasifikasi, diagnose labolatorium dan urutan basa suatu spesies. Melalui
data tersebut dapat dilakukan analisis berdasarkan persamaan urutan basa
menggunakan jarak matrik. Metode yang sering digunakan adalah Multiple
sequence Alignment (MSA), sebuah metode yang akan mengelompokkan
suatu strain berdasarkan derajat kesamaan urutan basa antar spesies (Helal
et al., 2011).
2. Asam Fitat
Asam fitat adalah bentuk simpanan fosfor dalam biji-bijian. Merupakan
garam mio-inositol asam heksafosfat, mampu membentuk kompleks dengan
bermacam-macam kation atau protein dan mempengaruhi derajat kelarutan
komponen tersebut (Piliang, 1997).
2.1 Struktur Asam fitat
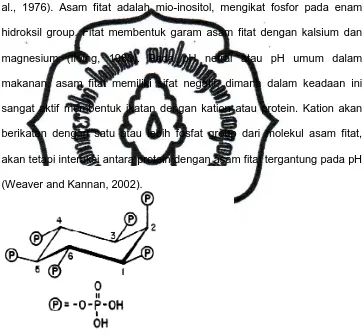
Asam fitat atau disebut sebagai Myo-inositol (1,2,3,4,5,6)
hexakisfosfate (C6H18O24P6 dan IP6). Inositol fosfat terdiri dari cincin
inositol dan sebuah kelompok fosfat (Gambar 1). Prefik Myo-
commit to user
1965 cit. Bohn et al., 2008). Asam fitat dalam bentuk fosforilase cincin
mio-inositol merupakan struktur yang kuat (Johnson, 1969). Satu molekul
fosfat mengandung dua belas proton dengan letak terpisah. Enam proton
merupakan asam sangat kuat dengan nilai pKa 5.7, 6.8 dan 7.6 dan
sisanya asam sangat lemah dengan pKa lebih besar dari 10 (Costelo et
al., 1976). Asam fitat adalah mio-inositol, mengikat fosfor pada enam
hidroksil group. Fitat membentuk garam asam fitat dengan kalsium dan
magnesium (Irving, 1980). Pada pH netral atau pH umum dalam
makanan, asam fitat memiliki sifat negatif, dimana dalam keadaan ini
sangat aktif membentuk ikatan dengan kation atau protein. Kation akan
berikatan dengan satu atau lebih fosfat group dari molekul asam fitat,
akan tetapi interaksi antara protein dengan asam fitat tergantung pada pH
(Weaver and Kannan, 2002).
Gambar 1. Struktur Asam Fitat (Graf, 1983)
2.2 Sumber Asam Fitat
Kandungan asam fitat sangat banyak terdapat dalam tumbuhan,
sel mikroorganisme dan ternak. Biji-bijian tumbuhan mengandung 60 –
90% fosfor terikat fitat dalam bentuk garam asam fitat. Asam Fitat
terdapat pada tanaman pangan seperti; jagung, gandum, kedelai, kacang
commit to user
berperan dalam proses dormansi tanaman dan perkecambahan biji
sebagai sumber ATP, berperan pada fungsi biologis penyimpanan fosfor
dan kation yang dibutuhkan untuk pertumbuhan bibit tanaman. (Chu et
al., 2000). Kebanyakan tanaman yang mengandung asam fitat
merupakan sumber pangan pada ternak maupun manusia (Tabel 2).
Barriento et al., (1994) menyatakan bahwa asam fitat dalam sereal bukan
merupakan bentuk distribusi dalam biji, akan tetapi merupakan
penghubung dalam komponen morfologi spesifik dalam biji. Dalam
biji-bijian dikotil, biji-biji-bijian yang mengandung minyak dan biji-biji-bijian legume
seperti pir, fitat tersebar didalam seluruh biji termasuk di dalam sub
selluler, dan membentuk ikatan dengan protein. Dalam tanaman komplek
fitat bersama dengan kation (K+ dan Mg2+) membentuk phityn. Phytin
tersimpan dalam protein bodi sebagai Kristal globoid. Pada padi, Kristal
globoid mengandung 67% asam fitat, 19% K, 11% Mg dan 1% Ca
(Ogawa et al., 1975 cit. Maenz et al., 2000).
Tabel 2. Bahan pangan dan kandungan Asam fitat
Tanaman Struktur % Asam fitat
Wijen Biji kering 4.71
Labu Embrio 4.08
Canola Biji kering 2.50
Bunga matahari Embrio 2.10
Mustard Biji kering 2.00
Kacang mete Embrio 1.97
Kacang-kacangan Embrio 1.80
Kacang tanah Biji 1.70
Tomat Biji 1.66
Kedelai Biji kering 1.55
Almond Embrio kering 1.42
Terung Biji 1.42
Kapri Biji kering 1.41
Pistachio Embrio 1.38
commit to user
LanjutanTanaman Struktur % Asam Fitat
Kiwi Buah segar 1.34
Kacang panjang Biji kering 1.11
Mentimun Biji tua 1.07
Sorghum Biji kering 1.06
Coklat Biji kering 1.04
Barley Biji kering 1.02
Oat Biji kering 1.02
Gandum Biji kering 1.02
Kacang polong Biji kering 1.00
(Lott et al., 2002 cit. Afinah et al., 2010)
2.3 Ketersediaan nutrisi dan dampak lingkungan
Pada tumbuhan, asam fitat berperan dalam proses dormansi
dan perkecambahan biji tanaman (Chu et al., 2000). Asam fitat juga
merupakan antioksidan dan agen anti kanker (Raboy et al., 2002). Namun
demikian, pada hewan dan manusia, asam fitat dapat menjadi komponen
antinutrisi. Asam Fitat sangat potensial mengikat protein, asam amino dan
multivalent kation atau mineral pada makanan. Ikatan tersebut
merupakan komplek yang tidak larut sehingga sulit dihidrolisis dalam
pencernakan, sukar di serap dan mempengaruhi ketersediaan nutrisi.
Asam fitat juga mengikat serat sehingga mempengaruhi kecernaan dan
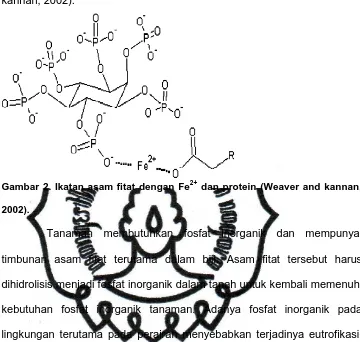
kelarutannya. Asam fitat berikatan dengan mineral penting seperti
kalsium, magnesium, cuper, besi (Fe2+, Fe3+), seng, cobalt dan mangan
(Gambar 2).
Potensi asam fitat mengikat ion mineral penting mengurangi
ketersediaan mineral dalam makanan yang mengandung asam fitat.
commit to user
komplek garam mineral-fitat penta-, hexa- yang tidak larut (Weaver and
kannan, 2002).
Gambar 2. Ikatan asam fitat dengan Fe2+ dan protein (Weaver and kannan,
2002).
Tanaman membutuhkan fosfat inorganik dan mempunyai
timbunan asam fitat terutama dalam biji. Asam fitat tersebut harus
dihidrolisis menjadi fosfat inorganik dalam tanah untuk kembali memenuhi
kebutuhan fosfat inorganik tanaman. Adanya fosfat inorganik pada
lingkungan terutama pada perairan menyebabkan terjadinya eutrofikasi,
yaitu pertumbuhan alga atau tanaman air secara berlebihan menutup
permukaan perairan, sehingga menurunkan kadar oksigen perairan dan
keseimbangan lingkungan perairan terganggu.
Pencernaan pada hewan monogastrik tidak dapat menghidrolisis
asam fitat. Asam fitat yang tidak tercerna dengan baik akan disekresikan
melalui kotoran ternak. Kotoran ternak tersebut dapat dihidrolisis oleh
mikrobia tanah dan air, sehingga ikatan fosfat pada asam fitat terlepas ke
lingkungan, mencemari sungai, danau (perairan). Menyebabkan blooming
alga, menurunkan kadar oksigen perairan, dan kematian hewan air (Shin
commit to user
3. Enzim Fitase 3.1. Enzim
Enzim merupakan katalis yang dapat mengubah laju reaksi tanpa ikut
bereaksi. Enzim bersifat khas dan bekerja secara spesifik sehingga aktifitasnya
dapat diatur. Dalam sitem biologis kecepatan kerja enzim dapat dipengaruhi oleh
kehadiran molekul lain yang dapat berperan sebagai pemicu (aktifator) atau
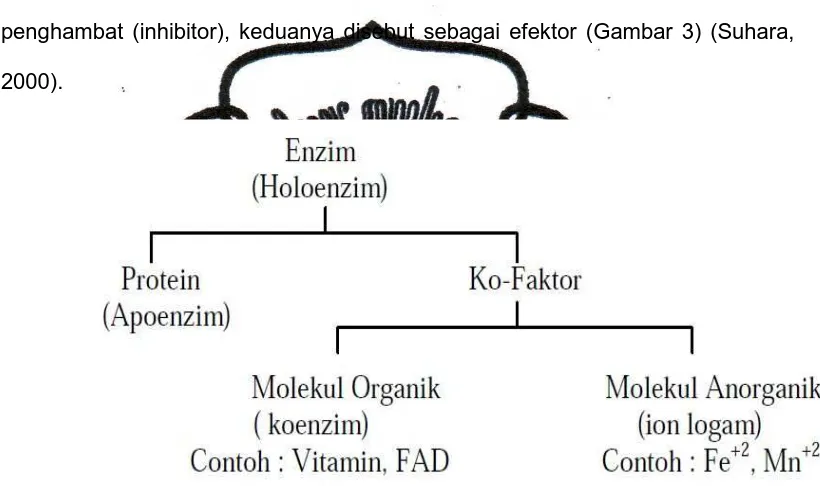
penghambat (inhibitor), keduanya disebut sebagai efektor (Gambar 3) (Suhara,
2000).
Gambar 3. Struktur aktif enzim (Suhara, 2000).
3.1.1 Aktifitas Enzim
Enzim merupakan protein yang berperan penting dalam
aktivitas biologis. Enzim sebagai katalisator reaksi mempunyai sifat
yang khas. Enzim dapat kehilangan aktivitasnya karena panas, asam
atau basa kuat, pelarut organik, dan keadaan lain yang menyebabkan
protein terdenaturasi (Girindra, 1989:91).
Selanjutnya diungkapkan oleh Suharsono (1990:124), bahwa
enzim yang aktif merupakan enzim yang mampu melakukan aktivitas
commit to user
dapat menyebabkan perubahan atau transformasi substrat sebanyak 1
mikromol per menit pada suhu dan lingkungan yang optimal selama
pengukuran aktivitas berlangsung. Satu unit aktivitas enzim (1U)
merupakan perubahan substrat 1µmol/menit.
Enzim bersifat khas dan aktif pada kondisi optimum tertentu,
sehingga aktivitasnya dipengaruhi oleh hal-hal berikut:
a. Konsentrasi Enzim
Enzim dengan derajat kemurnian yang tinggi dalam batas-batas
tertentu, menunjukkan hubungan linier antara jumlah enzim dan taraf
aktivitasnya (Gambar 4).
Gambar 4. Pengaruh konsentrasi enzim pada laju aktivitas enzim
b. Konsentrasi Substrat
Konsentrasi substrat pada taraf tertentu dapat mempengaruhi laju
aktivitas enzim dan selanjutnya laju aktivitas tidak tergantung pada
konsentrasi substrat yang ada (Gambar 5).
commit to user
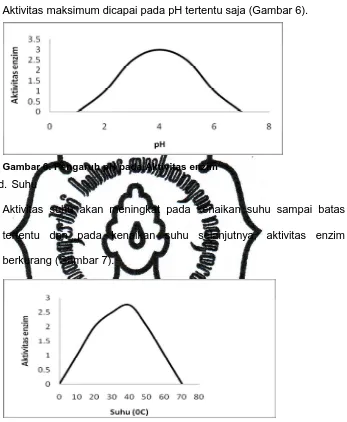
c. pH [image:30.595.165.512.129.551.2]Aktivitas maksimum dicapai pada pH tertentu saja (Gambar 6).
Gambar 6. Pengaruh pH pada Aktivitas enzim
d. Suhu
Aktivitas suhu akan meningkat pada kenaikan suhu sampai batas
tertentu dan pada kenaikan suhu selanjutnya, aktivitas enzim
berkurang (Gambar 7).
Gambar 7. Pengaruh Suhu pada aktivitas enzim
Aplikasi enzim dalam industri pakan ternak telah banyak
dilakukan dan efektifitas penggunaan enzim tersebut dipengaruhi oleh
aktifitas enzim. Enzim yang ditambahkan dalam pakan ternak
berpengaruh terhadap kecernaan pakan sehingga berdampak pada
pencernaan ternak.
Beberapa keuntungan penambahan enzim pada pakan ternak
commit to user
a. Mendegradasi antinutrisi dalam makanan yang mengganggu
proses pencernakan
b. Meningkatkan ketersediaan nutrisi dari suatu bahan pakan yang
tidak dapat terdegradasi oleh enzim pencernakan hewan ternak
c. Sebagai suplemen terhadap aktifitas pencernakan pada hewan
dalam masa pertumbuhan dan pada hewan dalam masa
penyembuhan
d. Membantu efektifitas penyerapan nutrisi sehingga mengurangi
dampak polusi kotoran ternak (Boyce et al., 2004).
3.2. Fitase
Fitase atau myo-inositol heksaisfosfat hidrolase merupakan enzim
fosfatase yang mampu mengkatalis hidrolisis pelepasan fosfat pada fitat.
Hidrolisis asam fitat sangat bermanfaat untuk meningkatkan nilai nutrisi pada
beberapa tanaman pangan (Gambar 8) (Shin et al., 2001).
Fitase adalah enzim yang dapat memutuskan ikatan phospat pada fitat,
yaitu suatu bentuk timbunan fosfat organik yang ada di alam (Jorquera et al.,
2008). Fitase aktif asal mikroba banyak ditemukan pada spesies fungi dan
aspergillus. Shieh dan Ware (1968), menyatakan bahwa hasil penyaringan pada
isolat tanah terdapat lebih dari dua ribu (2000) mikroorganisme yang mampu
menghasilkan enzim fitase. Dari isolat tersebut kebanyakan memproduksi fitase
commit to user
(Lei et al., 2003)3.2.1 Klasifikasi Fitase
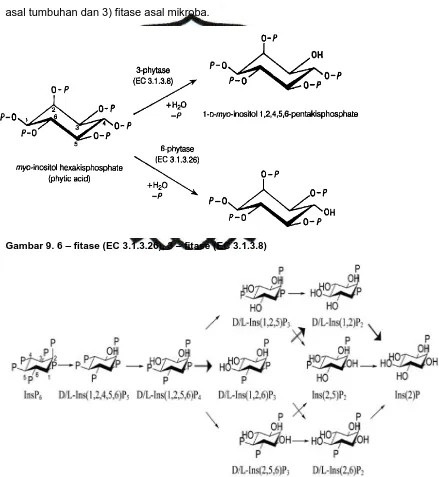
“The Enzym Nomenclature of The International Union of Biochemistry”
menggolongkan fitase ke dalam dua tipe yaitu 6–fitase (EC 3.1.3.26) dan 3–fitase
(EC 3.1.3.8). Pengelompokan tersebut didasarkan pada posisi gugus fosfat
pertama yang dihidrolisis oleh enzim. Enzim 6-fitase memulai reaksi hidrolisis
fitat dari gugus fosfat posisi L-6 atau D-4, menghasilkan produk awal L-inositol
(1,2,3,4,5)P5. Enzim 3-fitase memulai hidrolisis fitat pada gugus fosfat posisi D-3,
menghasilkan produk awal D-inositol (1,2,4,5,6)P5 (Gambar 9). Enzim 6–fitase
biasanya terdapat pada tumbuhan dan 3–fitase dijumpai pada fungi (Dvorakova,
1998).
Hidrolisis asam fitat terjadi secara berurutan mulai dari ester fosfor
mio-inositol yang lebih rendah (gambar 9), kemudian menurun sesuai dengan nomor
asam fosfat (IP5 – IP1). Enzim dalam bentuk tunggal tidak mampu melakukan
[image:32.595.114.517.112.496.2]commit to user
defosfolirase asam fitat secara penuh. Kombinasi fitase dan fosfatase non
spesifik akan meningkatkan aktivitas defosforilasi asam fitat (Maenz, 2001).
Degradasi fitat dalam saluran pencernaan unggas berhubungan dengan
aksi fitase dari satu atau tiga sumber enzim. Fitase dalam saluran pencernaan
berasal dari :1). Fitase usus yang terdapat dalam saluran pencernaan, 2) fitase
[image:33.595.108.547.234.711.2]asal tumbuhan dan 3) fitase asal mikroba.
Gambar 9. 6 – fitase (EC 3.1.3.26), 3 – fitase (EC 3.1.3.8)
commit to user
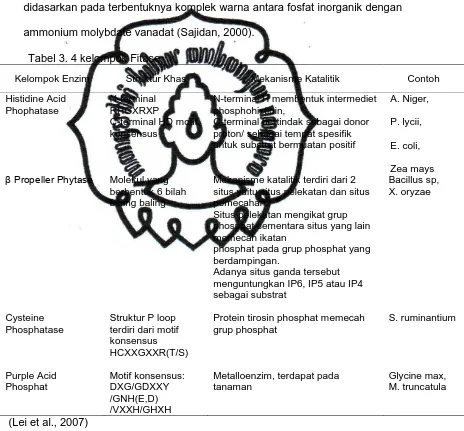
Berdasarkan mekanisme hidrolisis fitat terdapat 4 pengelompokkan
Fitase, yaitu; histidine acid phosphatase (HAP), cysteine phytase (CPhy),
purple acid phosphatase (PAP) dan -propeller phytase (BPP) (Tabel 3).
a. Histidine Acid Phophatase (HAP)
Merupakan kelompok enzim yang banyak digunakan dan dipelajari.
Enzim kelompok ini terdapat pada hewan, tumbuhan maupun mikro
organisme. Enzim ini tetap mempunyai aktivitas dalam kondisi asam.
Salah satu prokariotik yang menghasilkan HAPhy (Histidine Acid
Phophatase) adalah Escherichia coli, dari kelompok kapang antara
lain Aspergillus niger PhyA and PhyB. Aktivitas katalitik enzim terjadi
melalui 2 tahap reaksi yang menghidrolisis asam fitat menjadi
monoester fosfat. HAPhy (Histidine Acid Phophatase) banyak
digunakan dalam hidrolisis asam fitat dalam sereal dan biji-bijian
untuk pakan ternak.
b. Cysteine Phytase (CPhy)
Merupakan kelompok fitase yang ditemukan pada bakteri anaerob
dalam rumen yaitu Selomonas ruminantium (Chu et.al., 2004).
Mempunyai suhu optimum 50-55 0C dan pH optimum antara 4-5.
CPhy (Cysteine Phytase) mengkatalis reaksi defosforilasi asam fitat
menjadi myo-inositol monophosphat, aktivitas katalitiknya dihambat
oleh Fe2+, Fe3+, Hg2+, dan Zn2+.
c. Purple Acid Phosphatase (PAP)
PAP (Purple Acid Phosphatase) merupakan kelompok fitase yang
terdapat pada Burkholderia cepacia
,
dan padakedelai (Glycine max L.commit to user
ditemukan pada perkecambahan biji kedelai. GmPhy (Glycine max
phytase) mempunyai aktivitas spesifik terhadap asam fitat yang lebih
rendah dibanding aktivitas fitase dari kapang. Rendahnya aktivitas
spesifik fitase GmPhy (Glycine max Phytase) menguntungkan bagi biji
tanaman selama proses perkecambahan, dimana defosforilasi terjadi
dengan lambat dan seimbang selama perkecambahan biji. Dalam
tahap perkecambahan biji asam fitat mempunyai peran penting
sebagai sumber fosfat (Mullaney and Ullah, 2003).
d. β-Propeller Phytase (BPP)
Fitase kelompok β-Propeller Phytase (BPP) mempunyai 2 situs
pelekatan, yaitu situs untuk hidrolisis substrat dan situs untuk
mengikat substrat yang akan dihidrolisis. β-Propeller Phytase (BPP)
memutuskan ikatan 3-fosfat pada asam fitat menghasilkan inositol
3fosfat, aktivitas katalitik meningkat dengan adanya Ca (kalsium).
Adanya ikatan fitat dengan Ca (kalsium) akan membentuk
penghubung yang mendekatkan fitase dengan substrat (Shin et al.,
2001). BPP (β-Propeller Phytase) dapat digunakan sebagai tambahan
pada pakan ternak dan bermanfaat pada pertumbuhan tanaman yang
hidup pada kondisi fosfat terbatas. BPP (β-Propeller Phytase)
terdapat pada Bacillus subtilis 168PhyA, Shewanella oneidensis
PhyS, ; Xanthomonas oryzae PhyA (Lim et al., 2007).
3.2.2 Aktivitas fitase
Kebanyakan aktivitas fitase diketahui melalui warna fitat atau fosfat
inorganik yang terbentuk dari reagent setelah terjadi reaksi enzim-substrat.
Metode untuk mengetahui kuantitas fitat meliputi tahap yang kompleks;
commit to user
pencucian (Thomson, 1982 dalam Lim et al., 2007). Beberapa metode
analisis HPLC atau infrared spektrocopy merupakan teknik lain yang
digunakan (Chen, 2003). Metode yang paling mudah digunakan untuk
mengetahui aktivitas fitase adalah dengan cara menentukan fosfat inorganik
yang dilepaskan setelah terjadi reaksi enzim-substrat. Penentuan tersebut
didasarkan pada terbentuknya komplek warna antara fosfat inorganik dengan
[image:36.595.108.572.239.670.2]ammonium molybdate vanadat (Sajidan, 2000).
Tabel 3. 4 kelompok Fitase
Kelompok Enzim Struktur Khas Mekanisme Katalitik Contoh
Histidine Acid Phophatase
N-terminal RHGXRXP
C-terminal HD motif konsensus
N-terminal H membentuk intermediet phosphohistidin,
C-terminal bertindak sebagai donor proton/ sebagai tempat spesifik untuk substrat bermuatan positif
A. Niger,
P. lycii,
E. coli,
Zea mays β Propeller Phytase Molekul yang
berbentuk 6 bilah baling baling
Mekanisme katalitik terdiri dari 2 situs yaitu situs pelekatan dan situs pemecahan.
Situs pelekatan mengikat grup phosphat sementara situs yang lain memecah ikatan
phosphat pada grup phosphat yang berdampingan.
Adanya situs ganda tersebut menguntungkan IP6, IP5 atau IP4 sebagai substrat
Bacillus sp, X. oryzae
Cysteine Phosphatase
Struktur P loop terdiri dari motif konsensus HCXXGXXR(T/S)
Protein tirosin phosphat memecah grup phosphat S. ruminantium Purple Acid Phosphat Motif konsensus: DXG/GDXXY /GNH(E,D) /VXXH/GHXH
Metalloenzim, terdapat pada tanaman
Glycine max, M. truncatula
(Lei et al., 2007)
3.2.3 Sumber Fitase
Fitase terdapat di dalam tumbuh-tumbuhan mikroorganisme dan
commit to user
a. Fitase Mikrobia
Mikroorganisme penghasil fitase berasal dari bakteri misalnya
spesies pseudomonas (Irving dan Cosgrove, 1971), yeast seperti
Saccharomyces cereviceae, dan spesies aspergillus seperti
Aspergillus niger dan Aspergillus ficuum. Dvorakova (1998)
mendaftarkan 29 spesies fungi, bakteri dan yeast yang memproduksi
enzim fitase aktif. Dari 29 spesies yang terdaftar 21 memproduksi
fitase ekstraselluler dengan aktivitas paling tinggi (Volfova. et al.,
1994). Nielsen et al., (1997) menyatakan bahwa hidrolisis fitat pada
induk sapi perah dan anak terjadi di dalam saluran pencernaan.
Keadaan ini memungkinkan fitase asal mikroba akan aktif dalam
saluran pencernaan monogastrik dengan kondisi tertentu, walaupun di
dalam unggas kelihatannya hidrolisis fitat kurang penting. Selanjutnya
dinyatakan bahwa fitase asal mikroba aktif di dalam saluran
pencernaan. Mereka mengadakan penelitian dengan memberikan
penambahan alkali Esceria coli cellular, akibat perlakuan tersebut
terjadi difisiensi fosfor di dalam usus halus, selanjutnya
menambahkan campuran tepung jagung dan kacang kedelei pada
ransum dan terjadi perbaikan pada pertumbuhan dan kalsifikasi
unggas, respon ini mambuktikan akan adanya fitase atau enzim yang
serupa asal bakteri.
Enzim fitase ekstraselluler yang berasal dari mikroba stabil
pada suhu tinggi. Peningkatan suhu pada medium pereaksi dari suhu
ruang menjadi 58oC, terjadi peningkatan hidrolisis fitat oleh fitase asal
Aspergillus ficuum (Ullah et al.,1991). Peningkatan suhu dari suhu
commit to user
terdeteksi pada suhu 68oC (Ullah dan Dischinger, 1995). Suhu
optimum perlu diperhatikan untuk menjaga stabilitas enzim terutama
pada saat proses pembuatan ransum. Enzim fitase asal Asphergilus
fumigatus aktif pada kisaran pH yang luas dan suhu ekstrim 100oC
selama 20 menit atau 90oC selama 120 menit (Pasamontes et al.,
1997). Fitase Aspergillus fumigatus memiliki potensi untuk
dikembangkan secara komersial sebab pada lingkungan tersebut
akan mampu mempertahankan aktivitasnya dalam proses pelleting.
Enzim fitase yang diproduksi secara komersial adalah hasil
encoding gen pada Aspergillus niger. Produksi enzim berasal dari
Aspergillus niger var. vacuum perlu dilakukan penelitian lebih lanjut
terhadap aktivitasnya. Enzim fitase komersial asal Aspergillus niger
itu sudah digunakan sebagai pakan aditif pada hewan monogastrik di
Eropa (Wodzinski dan Ullah, 1996)
Secara umum fitase aktif pada suhu 45 sampai 60 dan
stabil pada pH tertentu. Sementara Asphergilus fumigates dapat stabil
sampai suhu 100, selama 20 menit dengan hanya kehilangan 10%
aktivitas enzim (Pasamontes et al., 1997). Fitase dari mikroba yang
berasal dari fungi, umumnya mempunyai pH optimum berkisar antara
4.5-6.0, dan aktivitas enzimnya menurun pada pH kurang dari 3.0
atau pada pH yang lebih tinggi dari 7.5. Fitase dari
commit to user
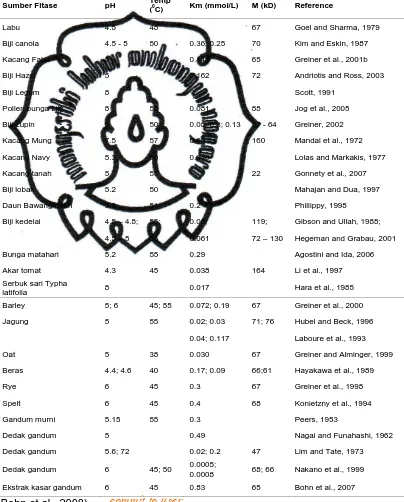
b. Fitase Tanaman
Beberapa Fitase yang ditemukan pada tanaman merupakan
jenis Histidin Acid phytase (HAP). Umumnya bahan pangan yang
[image:39.595.166.570.236.738.2]mengandung fitat juga mempunyai kandungan enzim fitase (Tabel 4).
Tabel 4. Fitase Tanaman
Sumber Fitase pH Temp
(0C) Km (mmol/L) M (kD) Reference
Labu 4.8 48 67 Goel and Sharma, 1979
Biji canola 4.5 - 5 50 0.36; 0.25 70 Kim and Eskin, 1987
Kacang Faba 5 0.148 65 Greiner et al., 2001b
Biji Hazel 5 0.162 72 Andriotis and Ross, 2003
Biji Legum 8 Scott, 1991
Pollen bunga Lily 8 55 0.081 88 Jog et al., 2005 Biji Lupin 5 50 0.08; 0.3; 0.13 57 - 64 Greiner, 2002 Kacang Mung 7.5 57 0.65 160 Mandal et al., 1972
Kacang Navy 5.3 50 0.018 Lolas and Markakis, 1977
Kacang tanah 5 55 22 Gonnety et al., 2007
Biji lobak 5.2 50 Mahajan and Dua, 1997
Daun Bawang daun 5.5 51 0.2 Phillippy, 1998
Biji kedelai 4.5 – 4.8; 55; 0.05; 119; Gibson and Ullah, 1988; 4.5 – 5 58 0.061 72 – 130 Hegeman and Grabau, 2001 Bunga matahari 5.2 55 0.29 Agostini and Ida, 2006
Akar tomat 4.3 45 0.038 164 Li et al., 1997
Serbuk sari Typha
latifolia 8 0.017 Hara et al., 1985
Barley 5; 6 45; 55 0.072; 0.19 67 Greiner et al., 2000 Jagung 5 55 0.02; 0.03 71; 76 Hubel and Beck, 1996
0.04; 0.117 Laboure et al., 1993
Oat 5 38 0.030 67 Greiner and Alminger, 1999
Beras 4.4; 4.6 40 0.17; 0.09 66;61 Hayakawa et al., 1989
Rye 6 45 0.3 67 Greiner et al., 1998
Spelt 6 45 0.4 68 Konietzny et al., 1994
Gandum murni 5.15 55 0.3 Peers, 1953
Dedak gandum 5 0.49 Nagai and Funahashi, 1962
Dedak gandum 5.6; 72 0.02; 0.2 47 Lim and Tate, 1973 Dedak gandum 6 45; 50 0.0005;
commit to user
c. Fitase pada jaringan tubuh Hewan
Beberapa fitase yang berasal dari jaringan tubuh hewan
memiliki pH optimal antara netral sampai basa. Fitase yang terdapat
pada jaringan membran intestinal vesikel unggas mempunyai pH
optimal antara 5,5-6,0. Meskipun di dalam jaringan tubuh unggas
terdapat fitase, namun tetap membutuhkan supplement fitase dari luar
tubuh untuk memenuhi kebutuhan diet unggas (Maenz, 1998).
Aktifitas fitase yang ditemukan pada rumen sapi berasal dari mikrobia
yang terdapat melimpah pada rumen (Yanke et al., 1998).
3.2.4 Prospek dan Aplikasi Enzim Fitase
Fitase biasanya digunakan sebagai supplement pada
makanan untuk meningkatkan ketersediaan P (fofat), melaui hidrolisis
fitat yang terdapat pada bahan pangan dari tumbuhan. Peningkatan
ketersediaan fosfat pada makanan dapat mengurangi kandungan
fosfat pada kotoran ternak, sehingga mengurangi melimpahnya fosfat
pada lingkungan peternakan. Fosfat inorganik (Pi) merupakan
sumberdaya yang tidak dapat diperbaharui, diperkirakan ketersediaan
fosfat di bumi akan habis dalam kurun 50 tahun. Sehingga Fitase
sangat efektif digunakan sebagai sumber natural fosfat dalam skala
global (Lei et al., 2007).
Fitase telah banyak digunakan sebagai supplement tambahan
pada makanan ternak. Diantaranya sebagai campuran wheat pollard
pakan ternak unggas. campuran probiotik tersebut dapat meningkatkan
retensi protein dan mineral sehingga dapat meningkatkan
pertumbuhan ayam (Sajidan et al., 2004). Prospek aplikasi fitase
commit to user
Kebanyakan sumber pangan berasal dari sereal dan biji bijian.
Tanaman tersebut mempunyai kandungan fitat yang tersimpan dalam
biji yaitu pada aleuron dan pada titik germinasi yang merupakan
tempat penyimpanan utama mineral dalam tanaman. Adanya fitase
yang menhidrolisis fitat, akan memperbaiki ketersediaan mineral,
protein dan nutrisi penting dalam konsumsi makanan manusia (Raboy
et al., 2002). Fitat yang berikatan dengan beberapa mineral, misalnya
besi dapat berperan sebagai antioksidan dan anti kanker. Sehingga
penggunaan fitase sebagai enzim yang bermanfaat pada ketersediaan
mineral, protein dan nutrisi dalam tubuh melalui hidrolisis fitat dengan
tetap mempertimbangkan efek positif fitat, merupakan bagian menarik
yang perlu diketahui lebih lanjut. Beberapa industri pembuatan
gandum, roti atau makanan dari bahan sereal dan biji-bijian telah
menggunakan fitase untuk mengurangi adanya fitat dalam bahan
makanan, sehingga bahan makanan menjadi lebih mudah dicerna
commit to user
B. KERANGKA PENELITIAN
Gambar 11. Diagram Kerangka Penelitian
Abu Vulkanik
Koloni dengan aktifitas Fitase tertinggi
Platting Method (Isolasi Bakteri)
Sub Kultur
Koloni Koloni Tunggal
Inokulasi pada media Screening cair
Morfologi
Molekuler (16S rRNA)
Isolasi DNA
Amplifikasi
gen 16S rRNA
Penentuan Urutan
Nukleotida
Analisis Filogenetik
Pengamatan
Koloni
Pewarnaan
Gram
Uji aktifitas Enzim
Identifikasi Bakteri Fitase
Ekstrak kasar Fitase
Karakterisasi
commit to user
BAB III
METODOLOGI
A. WAKTU DAN TEMPAT PENELITIAN
1. Waktu
Penelitian dilaksanakan bulan Desember sampai Mei 2010. Jadwal
kegiatan penelitian terlampir (Table L. G1, lampiran G).
2. Tempat
Sampel Abu vulkanik gunung Merapi Jawa Tengah diambil dari 2 tempat
yaitu; Desa Lencoh Kecamatan Selo Kabupaten Boyolali dan Cangkringan
Sleman Yogyakarta. Abu merupakan lapisan di atas tanah setebal 5 cm. Isolasi
bakteri dari sampel abu Selo Boyolali dilaksanakan di Laboratorium Mikrobiologi
FKIP Universitas Sebelas Maret Surakarta. Isolasi bakteri dari sampel abu
Cangkringan Sleman Yogyakarta dilaksanakan di LPPT Universitas Gajah Mada.
Identifikasi bakteri dilaksanakan di sub laboratorium Mikrobiologi FKIP UNS dan
sub Lab. Biologi laboratorium pusat Universitas Sebelas Maret. Karakterisasi
ekstrak kasar enzim fitase dilaksanakan di sub Lab. Biologi dan sub Lab. Kimia
laboratorium pusat Universitas Sebelas Maret. Sekuensing DNA dilaksanakan
dengan jasa komersial Laboratorium 1st base Singapura.
B. ALAT DAN BAHAN PENELITIAN
Alat dan bahan yang digunakan dalam penelitian ini antara lain:
1. Alat
Bunsen, cawan petri, tabung reaksi, gelas beker, gelas ukur, ose,
pinset, pipet, pipet mikro, tip, tabung mikro 1500 ml (eppendorf), neraca
timbang, inkubator, vortex, stirer, elektroforesis DNA, laminar air flow,
autoklaf, lampu ultraviolet, refrigerator, freezer, sentrifuge, PCR,
commit to user
2. Bahan
Aquades, dH2O filter, Master mix PCR (goTaq green Promega),
agarosa, DNA kit (Promega), etidium bromide, kristal violet, safranin.
primer forward Bact F1 (5'-GAGAGTTTGATCCTGGCCAG-3’), primer
reverse Uni B1 (5‘-CTGTTTGCTCCCCACGCTTTC-3‘). Marka DNA 1 kb
(Fermentas). Media Luria Bertani (LB), terdiri dari; 1% tripton, 1% NaCl,
0,5% yeast extract, 2% bacto agar untuk media LB padat, 0,4% Na Fitat
(Natrium Fitat) untuk media screening, Ammonium molibdate, Ammonium
metavanadate, HNO3 (asam nitrat), HCL (asam klorida).
C. RANCANGAN PENELITIAN
Penelitian ini merupakan penelitian deskriptif eksploratif. Abu vulkanik
gunung Merapi diambil dari Desa Kepuh Harjo Cangkringan Sleman Yogyakarta
dan Lencoh Selo Boyolali. Sampel Abu diambil dari lahan pertanian penduduk.
D. PROSEDUR PENELITIAN
1. Isolasi Bakteri dari sampel Abu Vulkanik
Bakteri fitase diisolasi dari abu vulkanik gunung Merapi dengan
menggunakan metode seri pengenceran (Platting Method). 1 gram abu dilarutkan
ke dalam 10 ml aquades ditambah larutan NaCl fisiologis 1%. Diambil sebanyak
1 ml dimasukkan ke dalam tabung reaksi yang berisi 9 ml larutan fisiologis
sehingga didapat pengenceran 10-2. Pengenceran dilanjutkan sampai 10-6, 10-7
dan 10-8. Masing-masing seri pengenceran diambil 10 µl dimasukkan kedalam
cawan Petri yang telah berisi media LB (Luria bertani). Kemudian diinkubasi
selama 16 jam pada suhu 37oC. Subkultur dilakukan terhadap hasil kultur
sebelumnya sehingga diperoleh koloni tunggal.
2. Seleksi bakteri Fitase
Masing masing koloni tunggal ditumbuhkan pada media LB (Luria bertani)
commit to user
Tripton : 1 yeast ekstrak : 2 NaCl. Koloni bakteri diinokulasi pada 10 mL media
cair. Diinkubasi pada suhu 37 oC selama 16 jam. Produksi ekstrak kasar enzim
fitase dilakukan dengan sentrifugasi kultur cair 4000 rpm selama 5 menit pada
suhu 4 oC. Supernatan yang dihasilkan merupakan ekstrak kasar enzim fitase.
Kemudian dilanjutkan dengan pengukuran aktivitas fitase.
3. Pengukuran Aktivitas Fitase
Pengukuran aktivitas bakteri penghasil fitase dengan metode dari Sajidan
(2002): 25 µl enzim, 125 µl susbtrat 0,4 % natrium fitat dalam 100 mM Natrium
asetat diinkubasi pada suhu 37°C selama 60 menit. Reak si dihentikan dengan
penambahan larutan STOP yang terdiri dari 2,352 g Ammonium molibdate/100
ml Aquadest sebagai larutan A, 10 g Ammonium metavanadate/100 ml Aquadest
sebagai larutan B. Larutan STOP dibuat dengan perbandingan : 1,5 volume
larutan A + 1,5 volume larutan B + 1 volume HNO3 pekat + 2 volume aquades.
Warna kuning dari fosfomolibdovanadat diukur dengan spektrofotometer pada ʎ=415 nm
4. Tahap Identifikasi
Bakteri penghasil fitase dengan aktivitas tertinggi selanjutnya dilakukan
identifikasi berdasarkan karakter morfologi dan analisis gen 16s rRNA.
a. Pewarnaan Gram dan pengamatan Koloni
Kaca objek ditetesi dengan aquades, kemudian jarum ose steril
diusapkan dalam biakan bakteri, dihomogenkan dan difiksasi diatas nyala
bunsen (± 30 cm). Usapan yang telah kering ditetesi satu tetes kristal violet
dan didiamkan selama 1 menit. Selanjutnya diteteskan satu tetes lugol dan
dibiarkan selama 30 detik. Bercak Lugol dibilas sampai warna bilasan bening
menggunakan etanol 95%. Kemudian diteteskan larutan safranin, dibiarkan
commit to user
mikroskop. Warna ungu pada sel menunjukkan Gram positif dan warna
merah menunjukkan Gram negatif.
b. Isolasi DNA Bakteri
Isolat bakteri ditumbuhkan dalam medium LB (Luria bertani), sebanyak
1 ml kultur disentrifugasi pada 12.000 rpm. Kemudian DNA diekstrak dengan
DNA kit (Promega USA) dengan langkah kerja sebagai berikut:
i. Pellet sel yang diperoleh ditambah 480 µL 50 mM EDTA dicampur
sehingga tersuspensi, kemudian ditambahkan 120 µL Lisozim 10mg/ml
dan diinkubasi pada suhu 370C selama 60 menit, kemudian di sentrifuge
12.000 rpm selama 2 menit. (Untuk bakteri gram Positif)
ii. Pellet sel ditambah 600 µL Nuclei Lysis Solution (Promega) dicampur
sehingga sel tersuspensi kembali.
iii. Inkubasi 800C selama 5 menit, kemudian didinginkan pada suhu ruang.
iv. Ditambahkan 3 µL RNAse Solution (Promega) mikro tube dibolak balik
sampai tercampur.
v. Inkubasi 370C selama 60 menit, kemudian didinginkan pada suhu ruang.
vi. Ditambahkan 200 µL Protein precipitation Solution, vortex dengan
kecepatan tinggi selama 20 detik
vii. Inkubasi dalam es selama 5 menit, kemudian sentrifuge 12.000 rpm
selama 3 menit.
viii. Supernatan dipindahkan ke dalam mikro tube baru yang telah berisi 600
µL isopropanol (mikro tube dibolak balik sehingga tercampur dan
benang-benang DNA terlihat)
ix. Sentrifuge 12.000 rpm selama 2 menit, kemudian supernatant dibuang dan
commit to user
x. Ditambahkan 600 µL 70% etanol, kemudian sentrifuge 12.000 rpm selama
2 menit
xi. Mikro tube dikering-anginkan selama 10 sampai 15 menit
xii. Ditambahkan 100 µL DNA Rehidration Solution (Promega), inkubasi pada
suhu 650C selama 60 menit.
xiii. Disimpan pada suhu 40C
Kualitas DNA diketahui melalui spektrofotometer (A260) dan
kemurnian DNA yang telah berhasil diisolasi di cek melalui elektroforesis
pada agaros gel 1%.
c. Amplifikasi DNA
Amplifikasi DNA dengan Polymerase Chain Reaction (PCR)
menggunakan universal primer (Shobirin et al., 2009) Primer Forward :
(5'GAGAGTTTGATCCTGGCCAG-3'), Primer Reverse:
(5‘CTGTTTGCTCCCCACGCTTTC-3‘). 1 mikrotube reaksi PCR berisi 25 µl
yang terdiri dari; 6, 5 µl master mix PCR go-Taq Green Promega, 2 DNA µl, 2
µl primer forward, 2 µl primer reverse, 12,5 µl dH2O filter. Siklus PCR
(Polymerase Chain Reaction) meliputi 3 tahap yaitu; denaturasi, annealing
dan ekstention. Denaturasi awal pada 94°C selama 2 menit dilanjutkan
dengan 30 siklus, denaturasi pada suhu 94°C selama 1 menit, 45 detik
annealing pada 50° C dan 1.5 menit primer ekstension pada 72°C.
Kemudian 72°C ektra ektension selama 5 menit dan terakh ir 4°C selama 1
menit.
Pita DNA dari reaksi PCR diamati dengan 1% agarosa, dengan DNA
marker 1 Kb. Setelah itu dilakukan sekuensing pada hasil PCR di
commit to user
5. Karakterisasi Ekstrak Kasar Fitase dari Isolat Terpilih
Isolate bakteri yang mempunyai aktivitas fitase paling tinggi
ditumbuhkan dalam 5 ml medium screening cair pada suhu 370C selama 16
jam. Kemudian disentrifus dengan kecepatan 4000 rpm selama 5 menit pada
suhu 40C. Supernatan yang diperoleh merupakan ekstrak kasar fitase.
Karakterisasi ekstrak kasar fitase meliputi penentuan pH optimum,
suhu optimum, efektor logam (MgCl2, ZnCl2, CaCl2, FeCl3 pada 10-3 dan 10-4
M), stabilitas pH dan stabilitas suhu.
5.1. pH optimum
pH optimum ditentukan dengan cara mengukur aktivitas enzim pada
berbagai pH substrat yaitu pada rentang 3 – 9. 0,4% Na-fitat dalam 100 mM
Na-asetat digunakan sebagai substrat di atur tingkat keasamannya sehingga
mempunyai pH 3, 4, 5, 6, 7, 8, 9.
5.2. Suhu optimum
Suhu optimum ditentukan dengan cara mengukur aktifitas enzim pada
berbagai suhu inkubasi enzim-substrat. Mulai dari suhu diruang, 370C, 400C,
500C, 600C, 700C, 800C. Ekstrak kasar enzim fitase sebanyak 25 µL
ditambahkan substrat 125 µL dan diinkubasi selama 60 menit pada berbagai
suhu yang telah ditentukan tersebut. Setelah itu ditambahkan 400 µL larutan
STOP, kemudian diukur absorbansi larutan pada ʎ = 415 nm.
Stabilitas termal enzim diketahui dengan memanaskan enzim pada
suhu optimum selama rentang waktu tertentu dan diukur aktivitasnya sampai
enzim tidak memperlihatkan aktivitas yang signifikan. Pada pengukuran
stabilitas pH dilakukan dengan cara melarutkan enzim dalam larutan buffer
commit to user
optimum selama 1 jam kemudian diukur aktifitas fitase pada tiap-tiap pH
tersebut.
5.3. Efektor Logam
Kedalam setiap larutan enzim-substrat ditambahkan 10 µL FeCl3,
MgCl2, CaCl2, dan ZnCl2 dengan konsentrasi 10-3 dan 10-4 M. Kemudian
diinkubasi pada pH dan suhu optimum selama 60 menit.
E. ANALISIS DATA
Data yang telah diperoleh kemudian dianalisis meliputi;
1. Data Pengukuran aktivitas Fitase
Nilai absorbansi yang diperoleh pada pengukuran ekstrak kasar Fitase
dianalisis jumlah kandungan fosfat anorganik (PO43-) yang terbentuk Unit/ml
dengan menggunakan persamaan regresi linier dari kurva standar P
(KH2PO4). Kurva standar fosfat dibuat dengan mengukur nilai absorbansi
larutan KH2PO4 pada berbagai konsentrasi.
Larutan KH2PO4 untuk membuat kurva standar fosfat dibuat dengan
cara melarutkan 0,38334 g KH2PO4 dalam 100 mL aquades. Kemudian
larutan tersebut diencerkan 100 kali sehingga setiap larutan mengandung
0,03834 mg KH2PO4. Seri standar dibuat dengan mengambil 0.025, 0.5,
0.075, 1, 2, 3, 4 larutan standar ditambah 6.25 mL molibdo-vanadat, dan
diencerkan sampai 25 mL. Larutan tersebut diukur absorbansinya pada ʎ =
415 nm. Nilai absorbansi larutan pada berbagai konsentrasi tersebut dihitung
korelasinya dan dibuat persamaan regresi.
2. Analisis gen 16s rRNA
Data urutan nukleotida dari hasil sekuensing gen 16s rRNA diolah
dengan program Bioedit untuk menggabungkan nukleotida menjadi satu untai
commit to user
sampel dengan urutan DNA data genbank. Analisis BLAST dilakukan secara
online di http://blast.ncbi.nlm.nih.gov/blast. Melalui analisis BLAST akan
diperoleh data homologi dari isolat bakteri terhadap data urutan nukleotida
spesies-spesies dalam genebank. Data urutan nukleotida spesies spesies
yang memiliki homologi dengan isolat dikumpulkan dalam satu file dengan
format fasta. Data-data urutan nukleotida tersebut kemudian dianalisis
Multiple sequence Alignment dengan program ClustalW2 secara online di
http://www.ebi.ac.uk/tool/msa/clust