OLIMPIADE SAINS NASIONAL 2014
CALON PESERTA
INTERNATIONAL CHEMISTRY OLYMPIAD (IChO) 2015
Mataram, Lombok
1-7 September 2014
Kimia
Teori
Waktu: 240 menit
KEMENTERIAN PENDIDIKAN DAN KEBUDAYAAN
DIREKTORAT JENDERAL PENDIDIKAN MENENGAH
DIREKTORAT PEMBINAAN SEKOLAH MENENGAH ATAS
TAHUN 2014
Hak Cipta
Petunjuk :
1. Isilah Biodata anda dengan lengkap (di lembar Jawaban) Tulis dengan huruf cetak dan jangan disingkat!
2. Ujian Teori terdiri dari 9 Soal:
Soal 1 = 19 poin Soal 2 = 20 poin Soal 3 = 25 poin Soal 4 = 23 poin Soal 5 = 20 poin Soal 6= 22 poin Soal 7 = 36 poin Soal 8 = 27 poin Soal 9 = 33 poin TOTAL Poin = 225 poin
3. Waktu yang disediakan: 240 menit (4 jam).
4. Semua jawaban harus ditulis di dalam kotak di lembar jawaban yang tersedia.
5. Diperkenankan menggunakan kalkulator yang diberikan panitia OSN. 6. Diberikan Tabel Periodik Unsur, rumus dan tetapan yang diperlukan. 7. Mulailah bekerja ketika ada tanda “MULAI” dari Pengawas.
8. Anda harus segera berhenti bekerja bila ada tanda “BERHENTI” dari Pengawas. 9. Letakkan jawaban anda di atas meja dan segera tinggalkan ruangan setelah
Tetapan dan Rumus
Bilangan Avogadro NA= 6,022 x 1023partikel.mol–1
Tetapan gas universal, R
R = 0,08205 L·atm/mol·K = 8,3145 L·kPa/mol·K
= 8,3145 x107erg/mol·K = 8,3145 J/mol·K
= 1,987 kal/mol·K = 62,364 L·torr/mol·K Tekanan gas
1 atm = 760 mmHg = 760 torr = 101,32 kPa = 101325 Pa = 1,01325 bar
1 torr = 133,322 Pa 1 bar =105Pa
1 Pa= 1 N/m2= 1 kg/(m.s2)
Massa 1 sma = 1,6605 ✕ 10-24g
Energi 1 kal = 4,182 J ; 1 J = 1 L·kPa
Kecepatan cahaya c = 3 x 108m/ detik
Tetapan Plank h =6,62606896 x10eV·sec -34J·sec = 4,13566733 x 10−15
Massa dan energi E = mc2
Persamaan gas Ideal PV= nRT
Tekanan Osmosis pada larutan = M RT
Tetapan Kesetimbangan air (Kw) pada 25oC Kw= 1,0x10-14
Tetapan kesetimbangan dan tekanan parsial
gas Kp= Kc(RT)∆n
Temperatur dan Tetapan kesetimbangan
Energi Gibbs pada temperatur konstan G H T S Isoterm reaksi kimia G = G + RT∙ln Q Hubungan tetapan kesetimbangan dan
energi Gibbs Go= -RT ln K
Potensial sel dan energi Gibbs Go= -nFEo
Tetapan Faraday F = 96500 C/mol elektron
Ampere (A) dan Coulomb (C) A =C/det
Muatan elektron 1,6022 x 10-9C
Massa elektron 0,000549 sma= 9,110 x 10-28g
Massa proton 1,007316 sma= 1,6727 x 10-24g
Massa neutron 1,008701 sma =1,6750 x 10-24g
Kecepatan cahaya 3 x 108m/s
Reaksi orde pertama: AB
Soal 1. Kandungan Kalsium Karbonat dalam Mutiara (19 poin)
Pulau Lombok terkenal dengan produksi mutiara karena banyak terdapat budidaya mutiara. Mutiara adalah suatu bahan yang keras, bulat, berkilau, yang terbentuk dalam jaringan lunak dari tiram hidup atau moluska bivalre. Mutiara dapat berwarna putih hitam, abu-abu kebiruan, kuning, oranye, merah, hijau, perak, krem, atau tidak berwarna.
Mutiara terbentuk dari ratusan dan bahkan ribuan lapisan kristal mineral aragonit (suatu CaCO3 polimorf), conchiolin (suatu jenis protein) dan air. Karena kandungan utamanya
mengandung kristal kalsium karbonat, mutiara dapat larut dalam asam cuka.
Sebanyak 1 gram mutiara dari Lombok, dilarutkan sempurna dalam 25 mL larutan asam cuka (asam asetat) 0,75 M. Pada pelarutan ini dihasilkan gas. Penambahan larutan natrium oksalat (Na2C2O4) berlebih ke dalam larutan mutiara tersebut menghasilkan
endapan putih sebanyak 1,1 gram.
a. Tentukan rumus molekul gas yang terbentuk pada pelarutan mutiara. (2)
b. Tuliskan reaksi yang terjadi pada pelarutan mutiara dalam asam asetat. (2)
c. Tuliskan reaksi yang menghasilkan endapan berwarna putih tersebut. (2)
d. Hitung persentase-massa (% massa) aragonit dalam mutiara tersebut. (4)
Dari hasil studi yang pernah dilakukan, tetapan hasil kali kelarutan aragonit dalam air laut dengan salinitas 35% pada 25°C dan tekanan 1 atm adalah 6,65 x 10−7mol2kg−2.
e. Tuliskanlah reaksi kesetimbangan kelarutan aragonit dalam air laut tersebut. (2)
f. Tentukanlah kelarutan aragonit dalam air laut (dalam satuan g/kg). (4)
g. Perkirakan pH larutan aragonit dalam air, asam atau basa, jelaskan mengapa demikian. (3)
Soal 2. Analisis Campuran Logam dalam Paduan Logam (20 poin)
Dow adalah paduan logam (alloy) yang banyak digunakan di industri logam, mengandung
logam magnesium, aluminum dan logam lainnya. Sebanyak 0,6113 g Dow dilarutkan dengan teknik tertentu untuk mencegah interferensi oleh logam lainnya. Ion aluminium dan magnesium yang terbentuk diendapkan menggunakan 8-hydroxyquinoline (HC9H6NO).
Setelah disaring dan dikeringkan, terbentuk endapan campuran Al(C9H6NO)3 dan
Mg(C9H6NO)2 yang massa totalnya adalah 7,8154 g. Campuran endapan tersebut dibakar
dan dihasilkan campuran oksida Al2O3 dan MgO yang mempunyai massa total sebanyak
1,0022 g.
a. Agar terbentuk endapan garam alumunium dan magnesium dengan 8-hydroxyquinoline secara sempurna, tentukan suasana larutan yang sebaiknya
digunakan (asam atau basa), jelaskan mengapa demikian. (3)
b. Tuliskan persamaan reaksi antara ion alumunium dan ion magnesium dengan
8-hydroxyquinoline untuk menghasilkan endapan Al(C9H6NO)3 dan Mg(C9H6NO)2
dalam suasana larutan yang sebaiknya digunakan (jawaban (a)). (4)
c. Tuliskan persamaan reaksi pembakaran Al(C9H6NO)3 dan Mg(C9H6NO)2 menjadi
oksida-oksidanya. (4)
d. Dari data yang diuraikan pada wacana di atas, hitung % massa Al dan Mg dalam paduan logam Dow tersebut. (9)
Soal 3. Senyawa Karbida dan Lampu Kereta Kuda (25 poin)
Selain senyawa organik yang jumlahnya hampir tak-berhingga, karbon juga membentuk senyawa anorganik. Salah satu contoh senyawa anorganik dari karbon adalah karbida, yaitu senyawa antara karbon dengan logam yang sangat elektropositif. Pada senyawa karbida, karbon berada sebagai anion monoatomik maupun poliatomik. Salah satu contoh karbida adalah CaC2 yang di dalamnya terdapat
anion C22 Keberadaan ion C22dibuktikan oleh reaksi CaC2dengan air yang menghasilkan
gas etuna (C2H2) seperti tertera pada Persamaan reaksi berikut:
CaC2+ 2H2O Ca(OH)2+ C2H2
a. Gambarkan struktur titik Lewis ion C22. (2)
Contoh karbida yang lain adalah magnesium karbida dengan rumus kimia Mg2C3.
b. Tentukan anion yang terdapat dalam senyawa Mg2C3. (2)
c. Gambarkan dua struktur titik Lewis yang mungkin untuk ion yang anda tuliskan pada jawaban soal b. (4)
d. Tuliskan reaksi setara Mg2C3dengan air. (3)
Padatan CaC2 bersifat kristalin dengan sel satuan (unit sel) seperti sel satuan pada kristal
NaCl.
e. Gambarkan satu unit sel CaC2. (3)
Gas etuna yang dihasilkan dari reaksi CaC2dengan air digunakan untuk bahan bakar pada
lampu kereta kuda jaman dahulu ketika lampu booglamp belum ditemukan. Diketahui kalor pembakaran standar HCo) etuna adalah 1300 kJ/mol dan entalpi pembentukan standar
Hfo) CaC2(s), H2O(l), C2H2(g) dan Ca(OH)2(s) berturut-turut adalah 63, 286, 227 dan
986 kJ/mol.
f. Jika sebuah lampu kereta kuda memerlukan 0,2 kg gas etuna per jam, hitung massa CaC2minimal yang harus tersedia dalam sebuah kereta kuda yang memiliki 2 lampu
untuk berjalan selama 3 jam pada malam hari. Asumsikan semua reaksi yang terjadi berlangsung sempurna. (4)
Soal 4. Kesetimbangan Asam-basa dalam Air (23 poin)
Suatu larutan (X) terdiri dari dua jenis asam lemah monoprotik yaitu asam asetat HOAc dengan tetapan dissosiasi asam, KHOAc = 1,8 × 10–5, dan asam formiat, HCOOH dengan
tetapan dissosiasi asam, KHCOOH = 1,8 × 10–4. Larutan X mempunyai pH = 2,38. Titrasi
100 mL larutan X memerlukan 50 mL larutan NaOH 1,00 M untuk menetralkannya. a. Tuliskan persamaan reaksi kesetimbangan disosiasi kedua asam tersebut. (2)
b. Tuliskan persamaan yang menunjukkan adanya persamaan keseimbangan konsentrasi muatan, yaitu hubungan antara konsentrasi [H] dalam larutan X dengan konsentrasi spesi-spesi ion negatif lainnya pada pH = 2,38. (3)
c. Turunkan persamaan yang mengkaitkan konsentrasi [OAc] pada kesetimbangan dengan [HOAc]awal, tetapan disosiasi asam KHOAcdan [H+]. (5)
d. Turunkan pula persamaan yang mengkaitkan konsentrasi [HCOO] pada kesetimbangan dengan [HCOOH]awal, tetapan disosiasi asam KHCOOHdan [H]. (3)
e. Dari ketiga persamaan yang diperoleh pada soal b), c) dan d) di atas dan dengan pendekatan yang sesuai, turunkan persamaan baru yang menghubungkan antara jumlah [HOAc]awaldan [HCOOH]awaldalam larutan X. (5)
f. Dengan menggunakan data reaksi netralisasi, hitunglah konsentrasi awal dari setiap asam: [HOAc]awal dan [HCOOH]awal dalam larutan X yang dinyatakan dalam mol/L
Soal 5. Kinetika Reduksi Gas NO oleh Gas H2(20 poin)
Gas NO, adalah gas pencemar yang banyak dihasilkan oleh mesin kendaraan bermotor. Reaksi reduksi gas NO oleh H2berikut ini berlangsung pada 826 ºC:
2 NO(g) + 2 H2(g) N2(g) + 2 H2O(g)
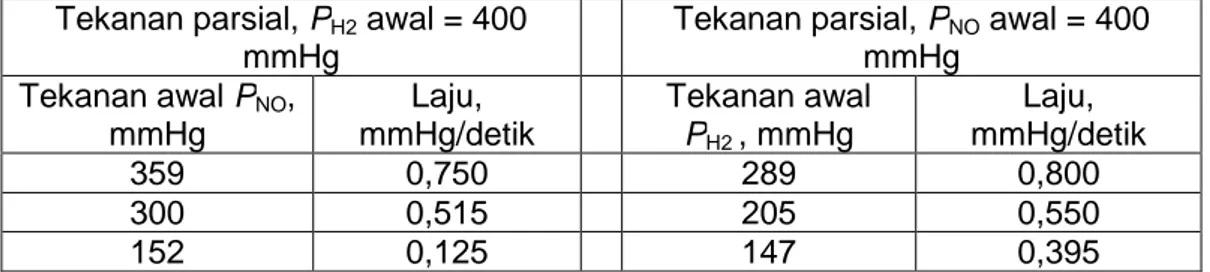
Kinetika laju reaksinya ditentukan berdasarkan metoda laju awal dengan mengukur tekanan parsial masing masing gas. Laju awal reaksi dinyatakan sebagai laju berkurangnya tekanan parsial (P) dari reaktan. Berikut ini adalah data yang diperoleh berdasarkan kondisi percobaan yang dilakukan:
Tabel Data percobaan penentuan kinetika reduksi gas NO oleh gas H2
Tekanan parsial, PH2awal = 400
mmHg
Tekanan parsial, PNOawal = 400
mmHg Tekanan awal PNO, mmHg Laju, mmHg/detik Tekanan awal PH2, mmHg Laju, mmHg/detik 359 0,750 289 0,800 300 0,515 205 0,550 152 0,125 147 0,395
a. Tentukan orde reaksi masing-masing terhadap NO dan H2. (4)
b. Tuliskan persamaan laju reduksi gas NO tersebut dan orde reaksi total. (2)
c. Hitung tetapan laju reaksi tersebut. (3)
d. Bila awalnya tekanan parsial, PH2 awal = 500 mmHg dan PNO awal = 350 mmHg,
sesudah reaksi berlangsung beberapa saat, ternyata tekanan parsial H2, PH2 turun
menjadi 350 mmHg. Hitung tekanan parsial gas NO, PNO, pada saat tersebut. (4)
Untuk reaksi reduksi tersebut, diusulkan 2 mekanisme reaksi yaitu:
Usulan Mekanisme 1, dengan 3 tahap reaksi:
i. NO + NO N2O2(kesetimbangan, cepat)
ii. N2O2+ H2H2O + N2O (lambat)
iii. N2O + H2 N2+ H2O
Usulan Mekanisme 2, dengan 2 tahap reaksi: i. 2 NO + H2 N2+ H2O2(cepat)
ii. H2O2+ H2 H2O (lambat)
e. Berdasarkan persamaan laju yang diperoleh dari percobaan tersebut:
i. Tentukan usulan mekanisme reaksi yang dapat diterima dan jelaskan mengapa demikian. (3)
Soal 6. Reaksi Redoks (22 poin)
Untuk menentukan kandungan besi dari suatu sampel air yang mengandung ion Fe3+ dan ion Fe2+, maka semua spesi ion besi harus diubah menjadi Fe3+ atau Fe2+. Data potensial reduksi standar (Eo) beberapa spesi terangkum pada Tabel di bawah ini.
Spesi Spesi E° dalam volt (V)
Fe3+ Fe2+ +0,77 Fe2+ Fe -0,41 I2 2 I- +0,54 S2O8-2 SO42- +2,01 SO42-(H+) H2SO3 +0,20 Sn4+ Sn2+ +0,15 Sn2+ Sn -0,14
a. Tuliskan spesi manakah pada Tabel di atas yang dapat mereduksi ion Fe3+menjadi Fe2+pada kondisi standar. Tuliskan persamaan reaksi yang telah disetarakan. (6)
b. Hitunglah tetapan kesetimbangan salah satu reaksi yang dituliskan pada jawaban a). (3)
Dalam air, kation Fe3+ sering dituliskan sebagai [Fe(H2O)6]3+, dapat bertindak sebagai suatu
asam dengan nilai Ka= 6,3 x103.
c. Tuliskan persamaan reaksi antara [Fe(H2O)6]3+dengan air (reaksi hidrolisis). (2)
Suatu larutan mengandung konsentrasi total ion Fe3+= 8,5x103mol/L.
d. Tentukan nilai pH dan derajat hidrolisis,. (4) (keterangan: ( = ([Fe3+]
yang mengalami hidrolisis/[Fe3+]total).
Jika diketahui suatu larutan mengandung ion Fe3+ dengan konsentrasi 3x103 mol/L dan memiliki derajat hidrolisis = 0,74 serta nilai KspFe(OH)3adalah 6,3x1038,
e. Apakah larutan tersebut dapat menghasilkan endapan Fe(OH)3? Jelaskan dengan
perhitungan. (4)
Salah satu reduktor yang biasa digunakan adalah Na2S2O5segar sebagai sumber ion SO32.
f. Jika dalam suatu larutan terdapat senyawa Fe2(SO4)3 dan Na2S2O5, maka
berdasarkan data potensial reduksi elektroda standar pada Tabel di atas, tuliskan reaksi redoks yang mungkin terjadi dalam larutan tersebut. (3)
Soal 7. Kandungan Senyawa Organik dalam Minyak Lawang (36 poin)
Pulau Lombok adalah suatu pulau yang terdapat di propinsi Nusa Tenggara Barat. Pulau ini memiliki geografis yang bervariasi sehingga memiliki keanekaragaman hayati yang tinggi, termasuk tanamannya. Salah satu tanaman yang menghasilkan komoditas penting di Lombok adalah kayu lawang [Cinnamomum culilaban (L.) J.S. Presl] seperti terlihat pada Gambar di samping ini. Tanaman ini mengandung minyak lawang yang berkhasiat sebagai obat gosok tradisional, obat rheumatik dan obat kolera. Beberapa senyawa yang terkandung dalam minyak lawang adalah: eugenol, metileugenol, safrol, dan -terpineol. Struktur senyawa-senyawa tersebut terlihat pada gambar di bawah ini.
eugenol O HO metileugenol O O safrol O O -terpineol OH
a. Tuliskan senyawa manakah yang memiliki karbon kiral dan gambar ulang struktur senyawanya kemudian beri tanda pusat karbon kiral dalam senyawa tersebut. (2)
b. Sarankan reagen dan kondisi reaksi yang memungkinkan terjadinya reaksi transformasi dari eugenol menjadi metal eugenol serta tuliskan reaksi yang terjadi.(4)
c. Gambarkan struktur produk yang ditampilkan pada skema reaksi transformasi eugenol berikut. (6)
eugenol
HNO
3(pekat)/
H
2SO
4(pekat)O
Sn, HCl
(pekat)P
H
S
O
3C
l
Q
d. Berikut adalah skema reaksi sintesis safrol dari 1,2-dihidroksi benzena (katekol) dan juga sintesis safrol dari eugenol. Gambarkan struktur senyawa organic A, B dan C dalam reaksi transformasi katekol menjadi safrol, serta tuliskan reagen dan kondisi X untuk reaksi transformasi eugenol menjadi safrol. (8)
e. Safrol menjadi bahan baku pembuatan obat psikoterapi atau psikotropika MDMA (3,4-metilendioksi-N-metilamfetamin) dengan skema reaksi berikut. Gambarkan struktur D, E dan MDMA berdasarkan skema reaksi berikut. (6)
Safrol
HBr
D
NaI
dalam heksamina
E
CH
3NH
2MDMA
f. Senyawa -terpineol dapat disintesis menurut skema reaksi berikut. Gambarkan struktur senyawa dalam setiap tahap reaksi berikut. (6)
COOCH
3F dan G
1. CH
3MgBr
2. H
+/H
2O
H dan I
g. Senyawa -terpineol dapat mengalami reaksi dehidrasi dalam H2SO4 33%
menghasilkan campuran produk dari beberapa senyawa turunan alkenanya. Gambarkan dua struktur produk dehidrasi-terpineol. (4)
OH
H2SO433%, 100oC, 1 jam
Soal 8. Etnobotani Obat Tradsional Suku Sasak Lombok (27 poin)
Obat tradisional merupakan warisan turun-temurun dari nenek moyang berakar kuat dalam budaya bangsa. Masyarakat Sasak yang tinggal di desa Senaru yang termasuk kecamatan Bayan, Kabupaten Lombok Barat, ternyata masih mempraktekan pengobatan tradisional. Dalam pengobatan tradisional mereka percaya kepada dukun kampung yang disebut dengan “Belian”. Beberapa tanaman yang sering digunakan untuk pengobatan tradisional diantaranya adalah Aistonia
scholaris (obat malaria), Voacanga foetida(Bl.)
Rolfe (sebagai agen anti bakteri), Clerodendron
paniculatum dan C. calamitosum L.(obat malaria). Clerodendron paniculatum termasuk ke
dalam keluarga Lemiaceae atau Verbenaceae yang memilki bunga kecil dan berwarna merah, serta dari hasil penelitian tanaman ini digunakan oleh masyarakat suku Sasak sebagai obat mata dan batu ginjal. Senyawa yang umum ditemukan dalam famili
Lemiaceae adalah hispudin dan asam klerodermat yang strukturnya ditampilkan di bawah
ini. O OH HO O OH H3C Hispudin O HO O O H H Asam Klerodermat a b
a. Gambarkan struktur produk yang terbentuk jika hispudin direaksikan dengan benzilklorida berlebih dalam suasana basa. (3)
b. Gambarkan struktur produk yang terbentuk jika hispudin direaksikan dengan isopropilbromida dalam katalis FeBr3. (3)
c. Hispudin termasuk ke dalam kelompok flavanon. Skema reaksi berikut adalah salah satu jalur sintesis flavanon. Gambarkan semua struktur produk dalam setiap tahap reaksi pembentukan flavanon berikut (Y, Flavanon dan W). (6)
OH
+ C6H5CHO OH- W HCl etanol
Flavanon Y
1. NaBH4dalam metanol 2. H+/H2O
d. Gambarkan mekanisme reaksi pembentukan senyawa W dalam tahap reaksi pertama dalam skema reaksi di atas. (3)
e. Gambarkan struktur produk yang terbentuk jika asam klerodermat direaksikan
dengan piperidin ( NH). (3)
f. Tentukan konfigurasi absolut (R atau S) untuk karbon kiral a dan b pada senyawa asam klerodermat. (2)
g. Gambarkan struktur produk yang terjadi jika asam klerodermat direaksikan dengan Br2 dalam CCl4 dan tuliskan apa yang teramati jika reaksi ini dilakukan di
laboratorium. (4)
h. Jika produk yang terbentuk pada soal (g) dilakukan reaksi hidrolisis dalam suasana asam, gambarkan produk yang terbentuk. (3)
Soal 9. Penentuan Struktur dari Ekstrak Kelenjar Ratu Tawon Madu (33 poin)
Tawon madu (Apis millivera) adalah serangga sosial yang hanya tertarik dengan anggota dari spesiesnya, khususnya terhadap tawon ratu. Kelenjar tawon ratu dapat mengeluarkan zat yang menjadi daya tarik bagi tawon pekerja. Senyawa X yang diekstrak dari kelenjar tawon ratu, dan setelah dianalisis ternyata mengandung karbon = 65,2 %; hidrogen = 8,75 % dan tidak mengandung unsur-unsur lain selain oksigen. Senyawa X tersebut bersifat asam, dan titrasi sebanyak 43,7 mg senyawa X membutuhkan 23,7 mL larutan NaOH
(0,0100 mol/L) untuk mencapai titik ekivalen. Senyawa X tersebut tidak mempunyai cincin benzena, dan berat molekulnya lebih kecil dari 200 g/mol.
a. Tentukan rumus molekul X, dan tuliskan gugus fungsi yang menyebabkan senyawa X bersifat asam. (8)
Untuk mengetahui senyawa X, dilakukan reaksi-reaksi berikut:
i). Senyawa X bereaksi dengan hidrogen dengan adanya logam Pt dan menghasilkan senyawa A.
ii). Reduksi selanjutnya dengan NaBH4dalam etanol menghasilkan senyawa B.
iii). Senyawa B dapat didehidrasi melalui pemanasan dalam suasana asam kuat dan menghasilkan senyawa C. Senyawa ini mengandung ikatan rangkap dua.
iv). Pada data spectrum 1H-NMR, memperlihatkan adanya gugus metil yang berikatan dengan ikatan rangkap dua.
b. Tentukan derajat ketidakjenuhan senyawa X tersebut. (3)
c. Tentukan senyawa A, B, C, dan X. (16)
Selanjutnya, reaksi ozonolisis senyawa C hanya menghasilkan senyawa asam asetat dan asam dikarboksilat HOOC-(CH2)6-COOH. Reaksi ozonolisis senyawa X itu sendiri akan
menghasilkan asam oksalat dan senyawa E yang masih mengandung gugus asam karboksilat.
d. Tuliskan nama dari isomer senyawa X. (4)