BAB 3
METODOLOGI PERCOBAAN
3.1 Alat-Alat
Alat-alat yang digunakan dalam penelitian ini adalah:
− Beaker glass 50 ml pyrex
− Beaker glass 100 ml pyrex
− Beaker glass 150 ml pyrex
− Beaker glass 200 ml pyrex
− Erlenmeyer 50 ml pyrex
− Erlenmeyer 100 ml pyrex
− Erlenmeyer 150 ml pyrex
− Erlenmeyer 250 ml pyrex
− Erlenmeyer 500 ml pyrex
− Erlenmeyer 1000 ml pyrex
− Satu set alat refluks
− Cawan petri
− Corong kaca
− Magnetic stirrer
− Hotplate ika ret basic
− Oven Memmert
− Pipet tetes
− Indikator pH-Fix 0- 14
− Thermometer 1000
− AAS
c Silber Brand
− FT-IR Bruker
− Neraca Analitik 3.2 Bahan-bahan
− Serbuk cangkang kepiting
− NaOH 3,5 %
− NaOH 50 %
− HCl 1 M
− CH3
− Larutan ninhidrin COOH 10 %
− KBr
− Aquadest
3.3 Prosedur Penelitian
3.3.1 Pembuatan reagen
3.3.1.1 Pembuatan HCl 1 M
Diukur HCl pekat 37 % sebanyak 83 ml dan diencerkan dengan aquadest dalam labu 1000 ml hingga garis tanda.
3.3.1.2 Pembuatan NaOH 3,5 %
Ditimbang NaOH pellet sebanyak 3,5 g dan dilarutkan dengan aquadest dalam labu takar 100 ml hingga garis tanda.
3.3.1.3 Pembuatan larutan NaOH 50 %
Ditimbang NaOH pellet sebanyak 50 g dan dilarutkan dengan aquadest dalam labu takar 100 ml hingga garis tanda.
3.3.1.4 Pembuatan CH3
Diukur 10 ml CH
COOH 10 %
3COOH 100 % dan diencerkan dengan aquadest dalam labu
3.3.2 Tahap isolasi kitin
Cangkang kepiting dikeringkan dan dihaluskan kemudian diayak.dalam isolasi
kitin terdiri dari 2 tahap, yaitu demineralisasi dan proteinasi.
3.3.2.1 Tahap Demineralisasi
Sebanyak 20 g cangkang kepiting dimasukkan kedalam beaker glass di
tambahkan 520 ml asam klorida (HCl) 1 M dengan perbandingan 1:26. kemudian
disaring dengan kertas saring whatman, dicuci dengan aquadest sampai pH netral
dan dikeringkan pada suhu kamar.
3.3.2.2 Tahap Deproteinasi
Sebanyak 3 g padatan dari hasil demineralisasi di masukkan dalam bejana tahan
asam dan tahan basa di lengkapi dengan pengaduk magnetik stirrer, pengangas
minyak dan termometer, di tambahkan30 ml natrium hidroksida (NaOH) 3,5%
dengan perbandingan 1:10 dan di refluks selama 30 menit pada suhu 60 oC.
kemudian disaring dengan kertas saring whatman sampai pH netral dan
dikeringkan dalam oven pada suhu 60oc selama 4 jam.
3.3.3 Tahap Deasetilasi
Sebanyak 1 g kitin di masukkan dalam bejana tahan asam dan tahan basa di
lengkapi dengan pengaduk magnetic stirrer, pengangas minyak dan termometer,
direfluks selama 30 menit pada suhu 100 oc. disaring padatan dan dicucui
sampai pH netral. kitosan basa yang dihasilkan dikeringkan dalam oven pada suhu
60oc selama 4 jam.
3.3.4 Tahap Analisa
3.3.4.1 Uji Mineral
Pada cangkang kepiting terdapat berbagai jenis mineral, tahap demineralisasi
dilakukan bertujuan untuk membuang mineral yang terdapat dalam cangkang
kepiting, dan alat yang digunakan adalah AAS.
3.3.4.2 Uji Protein
Sebanyak 1 g protein didestruksi dengan 9 g asam sulfat dan dikatalisis dengan
katalisator yang sesuai sehingga dihasilkan ammonium sulfat. Setelah
ditambahkan dengan alkali kuat, ammonium yang terbentuk didestilasi uap secara
kuantitatif kedalam larutan penyerap dan selanjutnya ditetapkan secara titrasi.
3.3.4.3 Uji Kadar Kadar Air
dalam desikator dan diulangi hingga berat konstan. Perhitungan kadar air dapat dilakukan dengan rumus sebagai berikut (Sudarmaji, 1994):
% kadar air =�−�
� 100%
Keterangan:
a : Berat kitosan awal (g)
b : Berat kitosan setelah di oven (g)
3.3.4.4Uji Kelarutan
Seberat 0,5 g masing masing kitin dan kitosan dimasukkan kedalam beaker glass, ditambahkan dengan 10 ml CH3COOH dan diaduk dengan magnetik stirrer
selama 20 menit. diamati perubahan yang terjadi, kelarutan diamati dengan membandingkan kejernihan larutan kitosan dengan kejernihan pelarutnya.
3.3.4.5 Uji Ninhidrin
Seberat 0,1 g kitosan yang diperoleh daripenelitian ditempatkan dalam suatu wadah dandisemprotkan dengan larutan ninhidrin kemudiandidiamkan selama 5 menit, diamati perubahanyang terjadi.
3.3.4.6 Penentuan Derajat Deastilasi Kitosan
Nilai absorbansi dapat dihitung dengan menggunakan rumus:
Perbandingan antara absorbansi pada A= 1.655 cm-1( serapan pita amida 1) dengan absorbansi pada A= 3450 cm-1 ( serapan gugus hidroksil ) dihitung. Untuk N-deasetilasi kitin yang sempurna (100%) diperoleh nilai
A 1655 = 1,33. Pengukuran nilai absorbansi pada puncak yang terkait,
derajat N- deasetilasi dapat dihitung dengan cara: %N−Deasetilasi = 1− �1655
�3450 � 1,33 x 100 %
A1655 : Absorbansi pada panjang gelombang 1588cm
-amida/asetamida
untuk serapan gugus
A3450 : Absorbansi pada panjang gelombang 3410cm
-hidroksil (OH)
untuk serapan gugus
3.3.4.7 Analisa Gugus fungsi pada FT-IR
komputer, buka opus 65, bersihkan tempat dan letakan sampel, masukkan sampel, dilihat hasil pada monitor.
3.4 Bagan Penelitian 3.4.1 Tahap Demineralisasi
dimasukkan kedalam beaker glass
ditambahkan 520 ml asam klorida (HCl) 1M
dengan perbandingan 1:26
disaring dengan kertas whatman
dicuci dengan aquadest
diukur pH sampai pH netral
dikeringkan pada suhu ruangan
ditimbang padatan 20 g Cangkang Kepiting
filtrat residu
3.4.2 Tahap Deproteinasi
dimasukkan dalam bejana tahan asam dan tahan basa di lengkapi
dengan pengaduk magnetik stirrer, pengangas minyak dan
termometer
ditambahkan 30 ml natrium hidroksida (NaOH) 3,5% dengan
perbandingan 1:10
direfluks selama 30 menit pada suhu 60 o
didinginkan
C
disaring padatan dengan kertas saring whatman
` dicuci dengan aquadest
diukur pH sampai pH netral
dikeringkan dalam oven pada suhu 60 0
ditimbang
C 3 g Padatan dari Hasil Demineralisasi
residu filtrat
3.4.3 Tahap Deasetilasi
ditimbang 1 g kitin
dimasukkan dalam bejana tahan asam dan tahan basa di lengkapi
dengan pengaduk magnetic stirrer, pengangas minyak dan
termometer
ditambahkan 10 ml natrium hidroksida (NaOH) 50% dengan
perbandingn 1:1
di refluks selama 30 menit pada suhu 100 o
didinginkan
c
disaring padatan kertas saring whatman
dicuci dengan aquadest
diukur pH sampai pH netral
dikeringkan dalam oven pada suhu 60 0C 1 g dari Hasil Demineralisasi
ditimbang
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil
4.1.1 Analisa FTIR
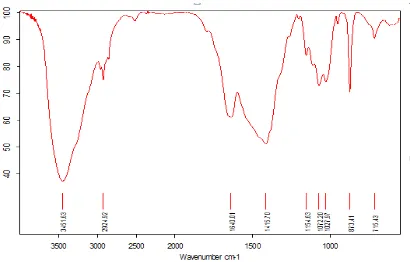
4.1.1.1 Cangkang Kepiting
Dari data spektroskopi FT-IR cangkang kepiting memberikan spektrum dengan
puncak puncak vibrasi pada daerah bilangan gelombang 3451,63 cm-1 ; 2924,92
cm-1 ; 1640,01 cm-1 ; 1415,70 cm-1 ; 1154,63 cm-1 ; 1072,20 cm-1 ; 1027,97 cm-1 ;
Gambar 4.1. Spektrum FT-IR senyawa cangkang kepiting
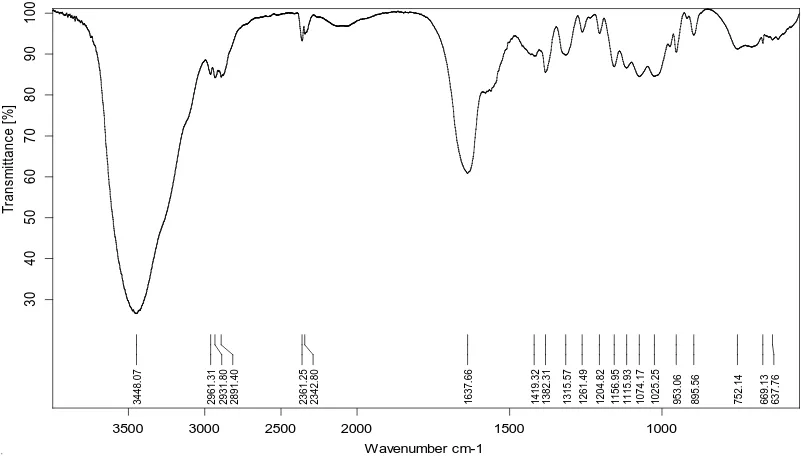
4.1.1.2 Kitin
Dari data spektroskopi FT-IR kitin yang dihasilkan dari proses deproteinasi
memberikan spektrum dengan puncak-puncak vibrasi pada daerah bilangan
gelombang 3448,07 cm-1 ; 2891,40 cm-1 ; 2361,25 cm-1 ; 1637,66 cm-1 ; 1382,31
Gambar 4.2 Spektrum FT-IR senyawa kitin
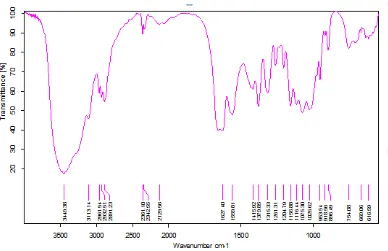
4.1.1.3 Kitosan
Gambar 4.3 Spektrum FT-IR senyawa kitosan
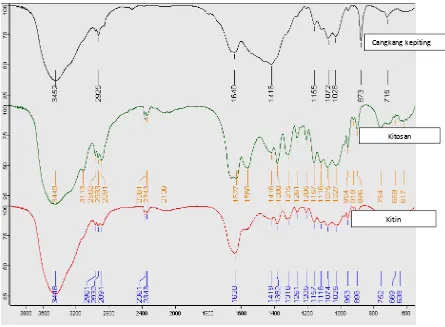
Tabel 4.1 Perbandingan kemunculan bilangan gelombang pada cangkang kepiting,kitin dan kitosan
Gugus Fungsi Bilangan Gelombang (cm-1)
Cangkang Kepiting Kitin Kitosan
-OH 3451,63 cm-1 3448,07 cm-1 3449,38 cm-1
-NH2 3451,63 cm-1 3448,07 cm-1 3449,38 cm
-C-O-C-
-1
1072,20 cm-1 1074,17 cm-1 1075,30 cm
-C=O
-1
1640,01 cm-1 1637,66 cm-1 1627,40 cm
-C-H
-1
2924,92 cm-1 2891,40 cm-1 2891,23 cm
Gambar 4.4Perbandingan kemunculan bilangan gelombang pada cangkang kepiting, kitin dan kitosan
Cangkang kepiting
Kitosan
4.1.2 Hasil Uji Mineral
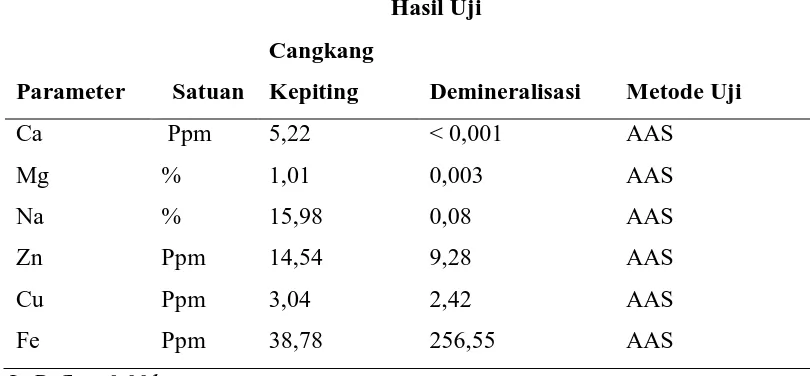
Tabel 4.2 Hasil Uji Mineral
LoD Ca= 0,001 ppm
4.1.3 Hasil Uji Protein Tabel 4.3 Hasil Uji Protein
Sampel Hasil Uji Metode UJi
Cangkang Kepiting 13,08 % SNI 01.0008.1987 Hasil Demineralisasi 43,33% SNI 01.0008.1987
Kitin 39,61 % SNI 01.0008.1987
Parameter Satuan
Hasil Uji
Metode Uji Cangkang
Kepiting Demineralisasi
Ca Ppm 5,22 < 0,001 AAS
Mg % 1,01 0,003 AAS
Na % 15,98 0,08 AAS
Zn Ppm 14,54 9,28 AAS
Cu Ppm 3,04 2,42 AAS
4.1.4 Hasil Uji Kadar Air
% kadar air =0,5−0,4662
0,5 100%
= 6,76%
Berdasarkan hasil penelitian yang telah dilakukan kadar air yang di peroleh dari kitosan adalah 6, 76 %.
4.1.5 Rendemen Cangkang Kepiting Laut Menjadi Kitosan
Dari 20 g cangkang kepiting pada tahap demineralisasi diperoleh hasil 5,0739 gr.
3 gr dari hasil demineralisasi pada tahap deproteinasi diperoleh hasil 1,8335 gr.
Rendemen % =����� ℎℎ�������� �������� ℎ jumlah bahan sebelum diolah
* Rendemen % = 5,0739
4.1.6 Hasil Uji Kelarutan
Kelarutan kitosan dan kitin dalam asam asetat 10 %.
% kelarutan = jumlah hasil yang di peroleh
����� ℎ��ℎ��������� ����� ℎ � 100 %,
% kelarutan kitosan =0,0615
0,5 � 100 % = 12,3 %,
% kelarutan kitin = 0,0085
4.1.7 Hasil Uji Ninhidrin
Hasil positif ditunjukkan dengan perubahan warna dari putih krem menjadi ungu.Kitosan yang direaksikan berubah warna menjadi violet sedangkan pada kitin tidak.
4.1.8 Derajat Deasetilasi
Derajat deasetilasi adalah prersentasi gugus asetil yang berhasil dihilangkan selama proses deproteinasi kitin, dimana kitin diberi perlakuan dengan menambahkan NaOH 50 % yang menyebabkan terhidrolisisnya gugus asetil dari gugus asetamida pada kitin. Derajat deasetilasi dapat ditentukan dari spektrum serapan spektroskopi IR dengan metode garis dasar.Puncak tertinggi dicatat dan diukur dari garis dasar yang dipilih. Perbandingan dari bilangan antara serapan pita amida ( 1655 cm-1) dengan serapan pita hidroksil (3450 cm-1
% N – Deasetilasi = = 1− A1655
Spektroskopi FT-IR mencatat penyerapan energi sebagai fungsi dari frekuensi
yang menurun dari kiri ke kanan. Energi getaran rentang untuk molekul-molekul
organik bersesuaian dengan radiasi infra merah dengan bilangan gelombang
antara 1200 – 4000 cm -1.bagian tersebut dari infra merah berguna untuk
O
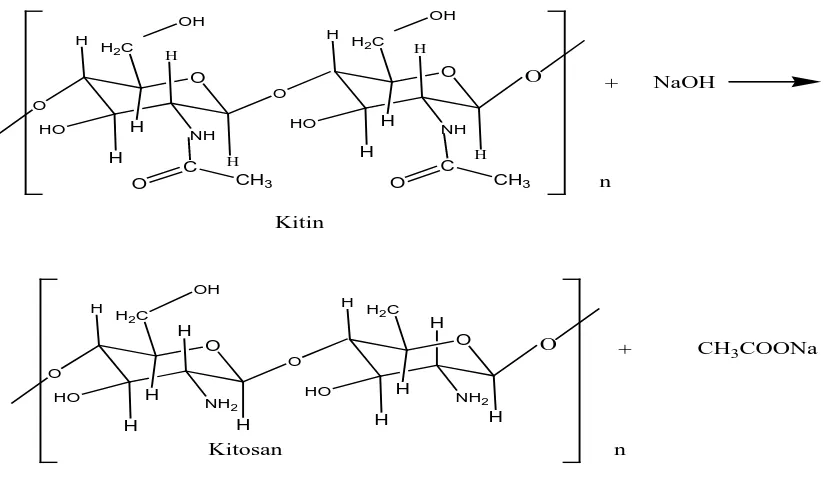
Gambar 4.4 Transformasi Kitin Menjadi Kitosan
Dari Gambar 4.4 dapat kita lihat bagaimana transformasi kitin menjadi kitosan dimana setelah penambahan NaOH 50 % terjadi pemutusan gugus asetil dengan atom nitrogen yang terdapat pada kitin sehingga menghasilkan suatu amina, untuk mengetahui struktur yang terdapat pada cangkang kepiting, kitin dan kitosan digunakan analisa FT-IR.
Pada tabel 4.1 dapat dilihat bahwa pada cangkang kepiting tidak terdapat C – N dan CH3. Analisa FT-IR juga bertujuan untuk mengetahui derajat
4.2.2 Analisa Protein dan Mineral Pada Cangkang Kepiting Sebelum dan
Sesudah Demineralisasi dan Kitin
Protein umumnya tersusun dari 20 macam asam amino, dimana asam amino
umumnya mempunyai satu gugus karboksilat dan satu gugus amina ( Riswiyanto
S. 2009). Kitin pada umumnya terikat dengan protein, mineral dan berbagai
macam pigmen (Sugita, dkk, 2009).Pada cangkang kepiting juga masih
terkandung mineral dan protein. Pada penelitian ini dilakukan analisa mineral dan
protein untuk mengetahui perbandingan kadar protein pada cangkang kepiting
yang belum diberi perlakuan, setelah didemieralisasi dan setelah dideproteinasi.
Analisa protein dengan metode kjeldahl dengan perbandingan cangkang kepiting, hasil demineralisasi dan kitin dari hasil deproteinasi secara berurutan adalah 13,08 %, 43,33 %, dan 39,61 %. Pada tahap demineralisasi terjadi peningkatan kadar protein karena sudah melalui tahap demineralisasi yang
bertujuan untuk menghilangkan kadar mineral yang terdapat pada cangkang
kepiting sehingga sebagian besar yang tertinggal adalah protein.
Pada proses deproteinasi terjadi penurunan kadar protein karena tujuan
dari deproteinasi adalah menghilangkan protein yang akan terikat secara kovalen
dengan kitin, akan terlepas dan membentuk natrium proteinat. Sedangkan pada
analisa mineral dilakukan untuk pengetahui perbandingan kadar mineral pada
cangkang kepiting dan hasil demineralisasi. Analisa mineral dari cangkang kepiting sebelum dan sesudah demineralisasi dari Kepiting dan hasil dari demineralisasi adalah Ca (5,22 % : < 0,001 ppm), Mg (1,01 % : 0,003 %), Na (15,98 % : 0,08 %), Zn (14,54 ppm : 9,28 ppm), Cu (3,04 ppm : 2,42 ppm), Fe (256,55 ppm : 38,78 ppm). Kadar logam yang dianalisa mengalami penurunan karena sudah melalui tahap demineralisasi.
4.2.3 Karakterisasi Kitin dan Kitosan
Kitosan yang di peroleh di karakterisasi untuk mengetahui mutu kitosan yang
diperoleh. Karakterisasi yang dilakukan adalah uji kadar air, kelarutan dalam
asetat 10 %, uji ninhidrin dan tekstur warna. Hasil karakterisasi pada penentuan
%. Pada hasil kelarutan antara kitosan dan kitin adalah 12,3 % dan 0,17% semakin
tinggi kelarutan semakin bagus kualitas kitosan yang diperoleh. Ninhidrin
merupakan hidrat dari triketon siklik dan jika bereaksi dengan asam amino akan
menghasilkan warna violet, Pada uji ninhidrin dalam waktu 5 menit menunjukkan
perubahan warna menjadi violet (Hart. H, 1983), pada penelitian ini dilakukan
perbandingan antara kitosan dan kitin, dalam waktu 5 menit kitosan menunjukkan
hasil berwarna violet sedangkan pada kitin tidak.Namun semakin lama berubah
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Perbandingan kadar protein pada cangkang kepiting sebelum dan sesudah demineralisasi dan kitin secara berurutan adalah 13,08 %, 43,33 %, dan 39,61 %.
2. Perbandingan kadar mineral antara cangkang kepiting sebelum dan sesudah demineralisasi secara berurutan pada Ca (5,22 % : < 0,001 ppm), Mg (1,01 % : 0,003 %), Na (15,98 % : 0,08 %), Zn (14,54 ppm : 9,28 ppm), Cu (3,04 ppm : 2,42 ppm), Fe (256,55 ppm : 38,78 ppm).
3. Dari data spektroskopi FT-IR cangkang kepiting memberikan spektrum dengan puncak puncak vibrasi pada daerah bilangan gelombang 3451,63 cm-1 ;
2924,92 cm-1 ; 1640,01 cm-1 ; 1415,70 cm-1 ; 1154,63 cm-1 ; 1072,20 cm-1 ;
1027,97 cm-1 ; 873,41 cm-1. Pada kitin yang dihasilkan dari proses deproteinasi
memberikan spektrum dengan puncak-puncak vibrasi pada daerah bilangan
gelombang 3448,07 cm-1 ; 2891,40 cm-1 ; 2361,25 cm-1 ; 1637,66 cm-1 ;
5.2 Saran
Sebaiknya pada tahap demineralisasi dari cangkang kepiting dilakukan variasi
konsentrasi HCl, pada tahap deproteinasi dan deasetilasi dilakukan variasi
konsentrasi NaOH untuk menentukan kondisi optimum dalam perubahan