i
TESIS
NILAI HOMEOSTATIC MODEL ASSESSMENT
INSULIN RESISTANCE BERKORELASI POSITIF
DENGAN JUMLAH SKIN TAG
TJOKORDA ISTRI OKA DWIPRASETIA HANDAYANI NIM 1114088102
PROGRAM PENDIDIKAN DOKTER SPESIALIS I
BAGIAN/SMF ILMU KESEHATAN KULIT DAN KELAMIN
FAKULTAS KEDOKTERAN UNUD/RS SANGLAH
DENPASAR
ii
NILAI HOMEOSTATIC MODEL ASSESSMENT
INSULIN RESISTANCE BERKORELASI POSITIF
DENGAN JUMLAH SKIN TAG
Tesis untuk Memperoleh Gelar Magister
Pada Program Magister, Program Studi Ilmu Biomedik (Combined Degree) Program Pascasarjana Universitas Udayana
TJOKORDA ISTRI OKA DWIPRASETIA HANDAYANI NIM 1114088102
PROGRAM MAGISTER
PROGRAM STUDI ILMU BIOMEDIK
PROGRAM PASCASARJANA
UNIVERSITAS UDAYANA
iii
Lembar Pengesahan
TESIS INI TELAH DISETUJUI
PADA TANGGAL JULI 2016
Pembimbing I, Pembimbing II,
Mengetahui,
Dr. dr. Made Wardhana, Sp.KK (K), FINSDV
NIP 19530811 198102 1 001
Dr. dr. IGAA Praharsini, Sp.KK, FINSDV
NIP 19630821 199003 2 001
Ketua program magister Ilmu Biomedik program Pascasarjana Fakultas Kedokteran
Universitas Udayana
Dr. dr. Gde Ngurah Indraguna Pinatih, M.Sc, Sp.GK
NIP 195805211985031002
Direktur program Pascasarjana Universitas Udayana
Prof. Dr. dr. A.A Raka Sudewi, Sp.S (K)
iv
Tesis Ini Telah Diuji pada
Tanggal Juli 2016
Panitia Penguji Tesis Berdasarkan SK Direktur Program Pascasarjana
Universitas Udayana No. ..., Tanggal ...
Ketua : Dr. dr. Made Wardhana, Sp.KK (K), FINSDV
Sekretaris : Dr. dr. IGAA Praharsini, Sp.KK, FINSDV
Anggota :
1. Prof. dr. Made Swastika Adiguna, Sp.KK (K), FINSDV, FAADV
2. Dr.dr. AAGP. Wiraguna, Sp.KK (K), FINSDV, FAADV
v
SURAT PERNYATAAN BEBAS PLAGIAT
Nama : dr. Tjokorda Istri Oka Dwiprasetia Handayani
NIM : 1114088102
Program Studi : Magister Ilmu Biomedik
Judul : Nilai Homeostatic Assesment Insulin Resistance
Berkorelasi Positif Dengan Jumlah Skin Tag
Dengan ini menyatakan bahwa karya tesis ini bebas plagiat.
Apabila di kemudian hari terbukti terdapat plagiat dalam karya ilmiah ini, maka
saya bersedia menerima sanksi sesuai peraturan Mendiknas RI No.17 tahun 2010
dan Peraturan Perundang-undangan yang berlaku.
Denpasar,
Yang membuat pernyataan,
vi
UCAPAN TERIMA KASIH
Pertama-tama perkenankanlah penulis mengucapkan terima kasih dan puji
syukur ke hadapan Tuhan Yang Maha Esa/ Ida Sang Hyang Widhi Wasa,
karena atas berkat dan rahmat-Nya tesis yang berjudul “Nilai Homeostatic Assesment Insulin Resistance Berkorelasi Positif dengan Jumlah Skin Tag”
dapat diselesaikan.
Penulis menyadari dalam pelaksanaan penelitian ini banyak mendapatkan
bimbingan, motivasi, dan bantuan lainnya dari semua pihak sehingga tugas
akhir ini dapat terlaksana dengan baik. Oleh karena itu melalui kesempatan ini
penulis sampaikan rasa terima kasih dan penghargaan yang setinggi-tingginya
kepada Rektor Universitas Udayana, Prof. Dr. dr. Ketut Suastika,
Sp.PD-KEMD dan Dekan Fakultas Kedokteran Universitas Udayana, Prof. Dr.dr.
Putu Astawa, Sp.OT, M.Kes, FICS, yang telah memberikan kesempatan dan
fasilitas kepada penulis untuk mengikuti dan menyelesaikan program
pendidikan dokter spesialis I di Fakultas Kedokteran Universitas Udayana.
Ucapan terima kasih penulis sampaikan kepada Direktur Program Pasca
Sarjana Universitas Udayana, Prof. Dr. dr. A.A. Raka Sudewi, SpS(K) dan
Ketua Program Magister Ilmu Biomedik Program Pascasarjana Universitas
Udayana Dr.dr. Gde Ngurah Indraguna Pinatih, M.Sc, SpGK serta kepada
Prof. Dr. dr. Wimpie Pangkahila, Sp.And., FAACS atas kesempatan yang
diberikan kepada penulis untuk menjadi mahasiswa Program Kekhususan
vii
Terima kasih kepada Direktur RSUP Sanglah Denpasar, dr. A.A. Sri
Saraswati, M.Kes, atas kesempatan dan fasilitas yang diberikan untuk
melanjutkan pendidikan di Bagian/SMF Ilmu Kesehatan Kulit dan Kelamin
dan melakukan penelitian di RSUP Sanglah Denpasar. Terima kasih yang
sebesar-besarnya kepada Kepala Bagian/SMF Ilmu Kesehatan Kulit dan
Kelamin Fakultas Kedokteran Universitas Udayana Prof. dr. Made Swastika
Adiguna, Sp.KK(K), FINSDV, FAADV sekaligus sebagai penguji, serta
Ketua Program Studi Pendidikan Dokter Spesialis I (KPS PPDS-I) Bagian
Ilmu Kesehatan Kulit dan Kelamin Fakultas Kedokteran Universitas
Udayana/RSUP Sanglah Denpasar sekaligus sebagai pembimbing pertama,
Dr. dr. Made Wardhana, Sp.KK(K), FINSDV yang telah memberikan
kesempatan mengikuti Program Pendidikan Ilmu Kesehatan Kulit dan
Kelamin. Terima kasih kepada Dr. dr. IGAA Praharsini, Sp.KK, FINSDV
sebagai pembimbing kedua, Dr. dr. AAGP Wiraguna, Sp.KK (K), FINSDV,
FAADV, Dr. dr. Luh Mas Rusyati, Sp.KK, FINSDV, selaku penguji, yang
telah banyak memberikan dorongan, semangat, bimbingan dan saran dalam
penyusunan karya akhir ini. Terima kasih kepada Dr. dr. Anak Agung
Wiradewi Lestari, Sp.PK , staf Laboratorium Patologi Klinik Fakultas
Kedokteran Universitas Udayana, dan staf di Laboratorium Kulit dan Kelamin
RSUP Sanglah Denpasar yang telah membantu dan memberikan sarana serta
prasarana pemeriksaan demi kelancaran tesis ini. Terima kasih yang
sebesar-besarnya kepada semua Kepala Divisi dan Staf Bagian/SMF Ilmu Kesehatan
viii
Denpasar serta seluruh tenaga paramedis dan nonmedis di Unit Rawat Jalan
dan Unit Rawat Inap yang telah membimbing, membantu dan memberikan
dukungan sehingga memungkinkan penulis menyelesaikan pendidikan.
Rasa hormat dan terimakasih yang mendalam juga penulis sampaikan
kepada kedua orang tua tercinta dr. Tjokorda Gede Oka, MS, Sp.PK dan dr. Ni
Wayan Padmi, yang telah mengasuh, membesarkan, mendidik dan mendukung
tanpa pamrih. Terimakasih juga penulis sampaikan kepada kakak tercinta
Tjokorda Oka Ekaprasetia dan Ricky Novani yang selalu memberi semangat
dan perhatian.
Terima kasih juga penulis sampaikan kepada semua teman-teman residen,
terutama dr. Desak Made Putri Pidari, dr Azhar Ramadan Nonci, dr. Midar
Madalena Alberto, dr. Herjuni Oematan, dr. Ni Made Dina Pranidya Ari, dr.
Ida Ayu Utami Dewi atas semangat dan dukungannya selama ini.
Penulis menyadari sepenuhnya bahwa karya tulis akhir ini jauh dari
sempurna, maka oleh sebab itu dengan segala kerendahan hati penulis tetap
mohon petunjuk dan saran perbaikan sehingga hasil yang tertuang dalam
karya akhir ini dapat bermanfaat bagi ilmu kedokteran dan pelayanan
kesehatan.
Denpasar, Juli 2016
Penulis
ix
ABSTRAK
NILAI HOMEOSTATIC ASSESMENT INSULIN RESISTANCE
BERKORELASI POSITIF DENGAN JUMLAH SKIN TAG
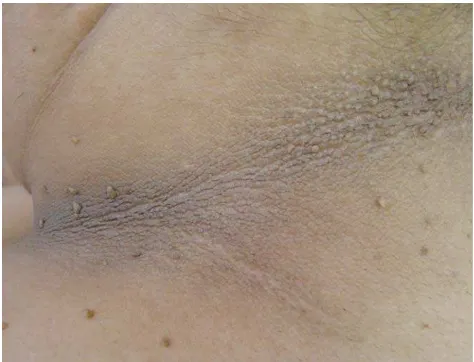
Skin tag atau akrokordon merupakan penamaan alternatif untuk menggambarkan tumor jinak yang berasal dari jaringan ikat longgar, muncul sebagai tangkai kecil dan lembut atau penonjolan yang bertangkai, sewarna dengan kulit disekitarnya, lokasi tersering adalah pada leher, aksila, dan lipatan-lipatan badan. Skin tag berhubungan dengan resistensi insulin dengan peningkatan indeks Homeostasis Model Assesment of Insulin Resistance (HOMA-IR) > 2,7 terutama pada pasien yang memiliki skin tag dengan jumlah lebih dari 5. Penelitian ini bertujuan untuk membuktikan adanya korelasi antara nilai HOMA-IR dengan jumlah lesi skin tag.
Penelitian ini adalah penelitian cross sectional yang melibatkan 48 orang penderita skin tag. Dilakukan pemeriksaan gula darah puasa dan insulin puasa untuk mendapatkan nilai HOMA-IR serta penghitungan jumlah skin tag. Pada penelitian ini didapatkan adanya korelasi positif antara nilai HOMA-IR dengan jumlah skin tag dengan nilai (r) = 0,930 dan p <0,001.
Simpulan pada penelitian ini adalah meningkatnya nilai HOMA-IR juga akan terjadi peningkatan jumlah lesi skin tag.
x
ABSTRACT
POSITIVE CORRELATIONS BETWEEN HOMEOSTATIC ASSESMENT INSULIN RESISTANCE WITH NUMBER OF SKIN TAG
Skin tag or achrocordon are the alternative name to describe benign tumor which appeared from loose connective tissue as a small soft penduculated that common site are in neck, axilae, trunk, intertriginous. Skin tag has correlation with insulin resistance and elevated index of Homeostasis Model Assesment of Insulin Resistance(HOMA-IR) > 2,7 especially for patients with skin tag number more than 5. Purpose of this study is to show there is correlation between HOMA-IR value with number of skin tag.
This is a cross sectional study involved 48 patients with skin tag. We assesed fasting blood sugar and fasting insulin to get HOMA-IR value and also count the number of skin tag.
Study result show that there is strong positive correlation between HOMA-IR value with number of skin tag with correlation coefficient (r) = 0,930 and with p <0,001. With conclusion that elevation of HOMA-IR will also increase the number of skin tag.
1
BAB I PENDAHULUAN
1.1 Latar Belakang
Kulit adalah barier utama manusia dan merupakan tempat yang paling
awal terpapar oleh lingkungan. Kulit juga dapat sebagai organ penanda dari
adanya gangguan internal tubuh. Terdapat beberapa penyakit kulit sebagai adanya
gangguan internal yang disebabkan oleh gangguan toleransi glukosa salah satunya
adalah skin tag, lesi ini juga dapat mengganggu secara kosmetik.
Gangguan toleransi glukosa dan obesitas merupakan faktor risiko tinggi
yang dapat berkembang menjadi diabetes melitus. Pada individu dengan gangguan
toleransi glukosa akan terjadi abnormalitas baik pada aksi insulin atau sekresi
insulin awal. Obesitas dan diet tinggi lemak dapat berkontribusi pada
perkembangan terjadinya resistensi insulin dan disfungsi sekresi insulin pada
individu yang rentan (Safoury, Ibrahim, 2011).
Skin tag, soft fibroma, fibroepithelial polyps, atau disebut juga akrokordon merupakan penamaan alternatif untuk menggambarkan suatu tumor jinak yang
berasal dari jaringan kolagen yang longgar serta serabut elastik, dapat berupa
tonjolan kecil, lunak dan mempunyai tangkai yang pendek di atas permukaan
kulit. Lokasi tersering adalah pada leher, aksila, dan lipatan-lipatan badan (Rasi A
2
(Thomas et al, 2012). Gambaran histologis dari skin tag umumnya ditandai dengan adanya hiperplasia epidermis yang menonjol dengan sedikit
serabut kolagen, disertai adanya hiperkeratosis, akantosis dan kadang
papilomatosis epidermis. (Weedon, 2010).
Insiden skin tag dikatakan cukup tinggi yaitu sekitar 46% dari populasi umum berdasarkan penelitian yang dilakukan di Jerman, namun secara klinis skin tag jarang mendapatkan perhatian kecuali apabila mengalami iritiasi atau nekrosis yang menyebabkan nyeri (Banik, Lubach, 1987). Pada penelitian retrospektif yang
dilakukan di bagian Ilmu Kesehatan Kulit dan kelamin RSUP Sanglah Denpasar
pada periode 2005-2008 didapatkan prevalensi skin tag sebesar 9,8% dari keseluruhan pasien dengan tumor jinak. Pada penelitian yang sama didapatkan
juga jumlah skin tag akan semakin meningkat dengan bertambahnya umur pada usia lebih dari 51 tahun. (Laksmi et al, 2010).
Patogenesis dari skin tag belum diketahui secara pasti, beberapa faktor yang dikatakan dapat sebagai pencetus adalah obesitas, penuaan, diabetes melitus
(DM), dislipidemia, resistensi insulin, poliposis kolon, infeksi human papilloma
virus (HPV), menopause, kerentanan genetik. Adanya trauma kulit yang sering
dan lama diduga merupakan faktor pencetus yang melibatkan mediator inflamasi
pada epidermis dan dermis. Ketidakseimbangan hormonal juga dapat
3
Factor (EGF) dalam α-tissue Growth Factor (TGF) mempunyai peranan dalam hal pertumbuhan skin tag (Sudy et al, 2008; Ade et al, 2010; Crook, 2012)
Rasi et al (2007) dan Sudy et al (2008) melakukan penelitian lebih lanjut mengenai skin tag dan gangguan metabolisme karbohidrat. Dalam penelitian tersebut dilaporkan bahwa pada pasien skin tag sering dijumpai gangguan metabolisme karbohidrat pada tahap yang lebih dini, yaitu keadaan korelasi
glukosa terganggu. Dalam penelitian tersebut disarankan perlunya pasien-pasien
skin tag untuk menjalani tes skrining metabolik untuk mengetahui adanya gangguan toleransi glukosa ( Rasi et al, 2007; Sudy et al, 2008)
Mekanisme patogenesis metabolik yang dapat menjelaskan korelasi antara
skin tag dan gangguan metabolisme glukosa adalah adanya resistensi insulin. Pada pasien skin tag didapati keadaan hiperinsulinemia yang bermakna dibandingkan dengan pasien yang tidak mengalami skin tag (Demir, Demir, 2002)
Keadaan resistensi insulin sendiri tidak hanya mengakibatkan gangguan
terhadap metabolisme karbohidrat, tetapi juga pada metabolisme protein dan
lemak. Situasi terjelas yang dapat menggambarkan fenomena resistensi insulin
adalah obesitas, pada obesitas didapatkan berat badan berlebih ditandai dengan
tanda gangguan metabolik seperti dislipidemia, gangguan toleransi glukosa,
hiperurisemia dan hiperinsulinemia. Hidalgo (2002) dalam penelitiannya
menyebutkan bahwa skin tag merupakan salah satu komplikasi dermatologis yang dijumpai pada pasien obesitas (Hidalgo, 2002)
4
kadar dislipidemia. Pada studi lanjut ditemukan adanya peningkatan Indeks Massa
Tubuh (IMT), kadar hormon insulin, sekresi insulin dan kadar kolesterol
dibandingkan orang yang tidak menderita skin tag. Gorpelioglu (2009) dan Sari et al (2010) melaporkan bahwa pada pasien skin tag terdapat gangguan profil lipid (Erdogan et al, 2005; Gorpelioglu et al, 2009; Sari et al, 2010)
Dari studi yang dilakukan oleh Tamega (2010) diperoleh hasil bahwa skin tag berhubungan dengan resistensi insulin didapatkan peningkatan indeks
Homeostasis Model Assesment of Insulin Resistance (HOMA-IR) > 2,7 terutama pada pasien yang memiliki skin tag dengan jumlah lebih dari 5, level insulin pada pasien dengan skin tag secara signifikan lebih tinggi daripada kontrol (P<0.01). Dapat disimpulkan bahwa nilai HOMA-IR berkorelasi positif dengan peningkatan
jumlah lesi skin tag. Mathur dan Bhargawa (1997) mendapat hasil yang berbeda, pada penelitian mereka tidak didapatkan hubungan antara resistensi insulin
dengan skin tag (Mathur et al,1997)
Berdasarkan data-data tersebut, maka disusunlah permasalahan apakah
terdapat hubungan antara nilai HOMA-IR dengan jumlah skin tag, yang pada beberapa penelitian didapatkan bahwa skin tag biasanya terjadi pada orang dengan gangguan metabolik. Peneliti ingin mengetahui apakah terdapat hubungan
peningkatan nilai HOMA-IR dengan umlah lesi skin tag di RSUP Sanglah Denpasar karena sejauh ini penelitian mengenai hal tersebut belum pernah
5
1.2 Rumusan Masalah
Apakah terdapat korelasi antara nilai HOMA-IR dengan jumlah lesi skin tag?
1.3 Tujuan Penelitian 1.3.1 Tujuan umum
Untuk mengetahui korelasi antara nilai HOMA-IR dengan skin tag.
1.3.2 Tujuan khusus
Mengetahui korelasi antara nilai HOMA-IR dengan jumlah lesi skin tag.
1.4 Manfaat Penelitian 1.4.1 Manfaat teoritis
Dapat menjelaskan peran dari resistensi insulin dalam patogenesis
terjadinya skin tag. 1.4.2 Manfaat praktis
Dengan mengetahui korelasi antara resistensi insulin melalui nilai
HOMA-IR dapat digunakan sebagai bahan pertimbangan untuk menilai seberapa besar
6
BAB II
TINJAUAN PUSTAKA
2.1Skin Tag
Skin tag atau acrochordon adalah tumor jinak kulit, yang berasal dari jaringan kolagen yang longgar serta serabut elastik, dapat berupa tonjolan kecil, lunak dan
mempunyai tangkai yang pendek di atas permukaan kulit.. Lokasi tersering adalah
pada leher, aksila, dan lipatan-lipatan badan (Rasi A et al, 2007). Lesi skin tag
paling sering dijumpai terutama pada individu yang mengalami obesitas, biasanya
mulai muncul pada dekade keempat bisa didapatkan pada usia yang lebih muda
namun sering dihubungkan dengan proses penuaan. Skin tag sering dihubungkan dengan gangguan sindrom metabolik seperti gangguan karbohidrat atau
metabolisme lipid, abnormalitas enzim hati dan hipertensi. Penyebab pasti
penyakit ini belum diketahui dengan jelas meskipun banyak faktor yang
mempengaruhi timbulnya penyakit ini. (Weedon, 2010; Thomas et al, 2012)
2.1.1 Epidemiologi
Skin tag umum dijumpai pada populasi dewasa dengan usia lebih dari 40 tahun, dan peningkatan insidennya pada orang dewasa ini mencapai umur 70
tahun. Didapatkan hubungan secara familial namun hubungan secara genetik ini
belum dapat dibuktikan hingga saat ini begitu juga hubungannya dengan etnik
tertentu. Tidak didapatkan perbedaan insiden antara pria dan wanita. Skin tag
dihubungkan dengan kehamilan, akromegali, polip intestinal asimptomatik,
7
seperti sindrom polikistik ovarium, sindrom Birt-Hogg-Dube, dan sindrom
Cowden. (Banik, Lubach, 1987; Tamega, 2010)
Berdasarkan penelitian retrospektif yang dilakukan di RSUP Sanglah Denpasar
periode tahun 2005-2009, prevalensi skin tag sebesar 9,8% dari seluruh penderita
tumor jinak kulit (Laksmi-Dewi dkk, 2010)
2.1.2 Etiologi
Etiologi dari skin tag belum diketahui secara pasti. Lebih sering terjadi pada daerah garukan dan sering berhubungan dengan beberapa kondisi, termasuk
acromegali, chron disease, aging, transplantasi organ, polip kolon, kehamilan, infeksi HPV, peningkatan jumlah sel mast, dan juga peningkatan reseptor
androgen dan estrogen serta kadar leptin. (Tamega, 2010) Skin tag juga diduga mempunyai hubungan dengan penyakit diabetes mellitus, obesitas, dislipidemia
dan resistensi insulin. (Naglaa et al, 2014)
Menurut penelitian Demir dan Demir (2001) menyimpulkan bahwa
munculnya skin tag kemungkinan merupakan suatu manifestasi klinis yang penting yang mendasari ada terjadinya gangguan metabolisme karbohidrat, oleh
karena itu setiap pasien skin tag harus dievalusi kemungkinan menderita diabetes mellitus.
Skin tag juga diduga dapat terjadi akibat faktor genetik. Faktor genetik merupakan hal yang penting untuk diteliti. Pada suatu penelitian mengatakan
setidaknya setiap dua pasien skin tag merupakan karier skin tag. Pada sindrom
8
multipel fibrofolikuloma, trichosdiscomas dan achrocordon, yang diduga mutasi terhadap suatu gen supresor yang dapat menjadi penyebab terjadinya kelainan
genetik ini. (Haimowitz JE, et al, 1997)
Adanya iritasi kulit yang sering dan lama diduga merupakan faktor
pencetus, terutama pada pasien obesitas. Ketidakseimbangan hormonal juga dapat
memudahkan untuk terjadinya skin tag, misalnya tingginya kadar estrogen dan progesterone pada saat hamil, atau terganggunya kadar growth hormone pada penderita acromegali. Para ahli mendapatkan bahwa epidermal growth factor
dalam transforming growth factor mempunyai peranan dalam hal pertumbuhan
skin tag. (Toro et al, 1999; Gaw et al, 2004; Safourry et al, 2009)
2.1.3 Patogenesis
Ada beberapa pendapat mengenai patogenesis dari skin tag. Terdapatnya beberapa teori yang menyebutkan skin tag terjadi sebagai akibat tekanan yang persisten ataupun dari gesekan yang terus menerus pada daerah permukaan kulit, terutama
pada penderita obesitas, yang menyebabkan gangguan jaringan elastik kulit.
(Safoury et al, 2011)
Rezzonico dkk, menyimpulkan bahwa individu yang mengalami skin tag
memiliki angka kejadian yang tinggi pada pasien dengan adanya pembesaran
tiroid atau terdapat nodul tiroid. Hal ini terjadi karena skin tag dan perubahan kadar tiroid berhubungan dengan tingginya kadar insulin yang bersirkulasi.
(Rezzonico et al, 2009)
9
oleh adanya gesekan yang berulang-ulang dengan pakaian yang digunakan pasien.
(Allegue et al, 2008)
Beberapa penelitian mengungkapkan peranan gangguan metabolisme
karbohidrat dan insulin serta gangguan metabolisme lipid dan hormon leptin
dalam patogenesis terjadinya skin tag. (Mathur, 1997; Dianzani et al, 1998; Erdogan et al, 2005; Erkek et al, 2008)
2.1.4 Klinis
Lesi skin tag berbentuk papul dengan konsistensi lunak, berwarna seperti kulit sampai kecoklatan, menonjol atau bertangkai di atas permukaan kulit, biasanya
timbul pada daerah fleksural atau sering mengalami gesekan seperti lipatan leher,
ketiak, lipatan paha dan perineum dengan ukuran diameter antara 1mm sampai 1
cm. (Barbato et al, 2012)
Terdapat tiga tipe gambaran klinis skin tag, yaitu: tipe papul furrowed
dengan ukuran lebar dan tingginya ± 2 mm, tipe filiformis dengan ukuran lebar 2
mm tinggi 5 mm dan yang terakhir tipe dengan bentuk paling besar atau large bag-like protuberances type sering terjadi pada tubuh bagian bawah. Tipe yang terbesar ini sering disebut tipe fibroepithelial polyp dan jarang muncul secara multipel pada satu individu. Secara eksperimental, skin tag tipe ini menunjukkan penurunan atau tidak adanya ekspresi tuberin dan/atau hamartin yang
menyebabkan terbentuknya jaringan ikat longgar dengan sedikit serabut kolagen.
10
Gambar 2.1 Skin Tag (Barbato et al, 2012)
2.1.5 Histopatologi
Gambaran histopatologi skin tag bervariasi sesuai dengan tipe klinisnya. Papul bentuk furrowed menunjukkan hiperplasia epidermal dan kadang ditemukan horn cyst formation. Lesi ini sering terdapat pada bagian leher dan kedua kelopak mata. Pada bentuk filiformis, epidermis mengalami akantosis yang minimal. Gambaran
pagetoid diskeratotik kadang ditemukan di epidermis bagian atas. Jaringan ikat
pada lesi yang bertangkai memiliki vaskularisasi yang baik, terdapat komponen
kolagen yang longgar serta serabut elastik dan kadang tampak beberapa sel lemak.
Papul fibroepitelial yang besar (bag-like lesions, polip fibroepitelial, fibrolipomas) biasanya memiliki stroma yang terdiri dari kolagen yang longgar dan inti berupa
11
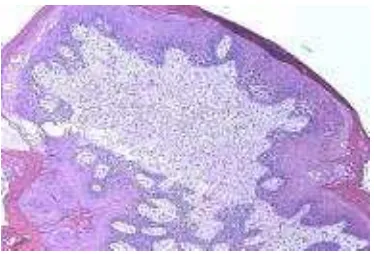
Gambar 2.2 Gambaran histopatologi skin tag. (Weedon, 2010)
2.2 Metabolisme Glukosa Dan Peranan Insulin
Karbohidrat yang masuk dalam tubuh kita akan dicerna dalam saluran
gastrointestinal untuk membentuk monosakarida yang kemudian diserap ke dalam
sirkulasi. Glukosa merupakan bentuk karbohidrat dalam sirkulasi berfungsi
sebagai bahan bakar untuk menghasilkan energi. Insulin merupakan protein yang
disintesis oleh sel beta pankreas dan merupakan hormon utama yang berperan
dalam metabolisme glukosa mengatur kadarnya dalam darah yaitu dengan cara
membawa glukosa masuk ke dalam sel melalui reseptor yang terdapat pada
membran sel. Glukosa tidak dapat masuk dan diproses ke dalam sel tanpa adanya
insulin. (Wilcox, 2005; Rasi et al, 2007; Napolitano et al, 2015)
Target utama insulin adalah adalah sel otot, liver, dan jaringan adiposa.
Kerja insulin berlawanan dengan kerja hormon stress lainnya yaitu glukagon,
adrenalin, glukokortikoid, dan growth hormone. (Rasmussen et al, 1990) 2.2.1 Proses pembentukan dan sekresi insulin
Insulin merupakan hormon yang terdiri dari rangkaian asam amino, dihasilkan
oleh sel beta kelenjar pankreas. Dalam keadaan normal, bila ada rangsangan pada
12
kebutuhan tubuh untuk keperluan regulasi glukosa darah. Secara fisiologis,
regulasi glukosa darah yang baik diatur bersama dengan hormone glukagon yang
disekresikan oleh sel alfa kelenjar pancreas. (Wilcox et al., 2005; McAuley et al., 2011)
Sintesis insulin dimulai dalam bentuk preproinsulin (precursor hormon insulin) pada retikulum endoplasma sel beta. Dengan bantuan enzim peptidase,
preproinsulin mengalami pemecahan sehingga terbentuk proinsulin, yang
kemudian membentuk dan terkumpul dalam bentuk gelembung-gelembunh
(secretory vesicles) dalam sel tersebut. Di sini, sekali lagi dengan bantuan enzim peptidase, proinsulin diurai menjadi insulin dan peptida-C (C-peptide) yang keduanya sudah siap untuk disekresikan secara bersamaan melalui membran sel.
(Wilcox et al, 2005; McAuley et al, 2011)
Mekanisme diatas diperlukan bagi berlangsungnya proses metabolisme secara
normal, karena fungsi insulin memang sangat dibutuhkan dalam proses utilisasi
glukosa yang ada dalam darah. Kadar glukosa darah yang meningkat, merupakan
komponen utama yang memberi rangsangan terhadap sel beta dalam
memproduksi insulin. Disamping glukosa, beberapa jenis asam amino dan
obat-obatan, dapat pula memiliki efek yang sama dalam rangsangan terhadap sel beta.
Mengenai bagaimana mekanisme sesungguhnya dari sintesis dan sekresi insulin
setelah adanya rangsangan tersebut, merupakan hal yang cukup rumit dan belum
sepenuhnya dapat dipahami secara jelas. (McAuley et al, 2011)
Diketahui ada beberapa tahapan dalam proses sekresi insulin, setelah adanya
13
membrane sel. Untuk dapat melewati membran sel beta dibutuhkan bantuan
senyawa lain. Glucose transporter (GLUT) adalah senyawa asam amino yang terdapat di dalam berbagai sel yang berperan dalam proses metabolisme glukosa.
Fungsinya sebagai “kendaraan” pengangkut glukosa masuk dari luar kedalam sel
jaringan tubuh. Glucose transporter 2 (GLUT 2) yang terdapat dalam sel beta misalnya, diperlukan dalam proses masuknya glukosa dari dalam darah, melewati
membran, ke dalam sel. Proses ini penting bagi tahapan selanjutnya yakni
molekul glukosa akan mengalami proses glikolisis dan fosforilasi didalam sel dan
kemudian membebaskan molekul adenosin trifosfat (ATP). Molekul ATP yang
terbentuk, dibutuhkan untuk tahap selanjutnya yakni proses mengaktifkan
penutupan K channel pada membran sel. Penutupan ini berakibat terhambatnya pengeluaran ion K dari dalam sel yang menyebabkan terjadinya tahap depolarisasi
membran sel, yang diikuti kemudian oleh tahap pembukaan Ca channel. Keadaan inilah yang memungkinkan masuknya ion Ca sehingga menyebabkan peningkatan
kadar ion Ca intrasel. Suasana ini dibutuhkan bagi proses sekresi insulin melalui
mekanisme yang cukup rumit dan belum seutuhnya dapat dijelaskan. (Rasmussen
et al, 1990; Wilcox et al, 2011)
Seperti disinggung di atas, terjadinya aktivasi penutupan K channel tidak hanya disebabkan oleh rangsangan ATP hasil proses fosforilasi glukosa intrasel,
tapi juga dapat oleh pengaruh beberapa faktor lain termasuk obat-obatan. Namun
senyawa obat-obatan tersebut, misalnya obat anti diabetes sulfonil urea, bekerja
14
disebut sulphonylurea receptor (SUR) pada membran sel beta. (Wilcox et al, 2005; McAuley et al, 2011)
2.2.2 Aktivitas insulin
Insulin mempunyai fungsi penting pada berbagai proses metabolisme dalam tubuh
terutama metabolisme karbohidrat. Hormon ini sangat krusial perannya dalam
proses utilisasi glukosa oleh hampir seluruh jaringan tubuh, terutama pada otot,
lemak, dan hepar. (Ozougwu et al, 2013)
Pada jaringan perifer seperti jaringan otot dan lemak, insulin berikatan
dengan sejenis reseptor (insulin receptor substrate = IRS) yang terdapat pada membran sel tersebut. Ikatan antara insulin dan reseptor akan menghasilkan
semacam sinyal yang berguna bagi proses regulasi atau metabolisme glukosa
didalam sel otot dan lemak, meskipun mekanisme kerja yang sesungguhnya
belum begitu jelas. Setelah berikatan, transduksi sinyal berperan dalam
meningkatkan kuantitas GLUT-4 (glucose transporter-4) dan selanjutnya juga pada mendorong penempatannya pada membran sel. Proses sintesis dan
translokasi GLUT-4 inilah yang bekerja memasukkan glukosa dari ekstra ke
intrasel untuk selanjutnya mengalami metabolisme. (Wilcox et al, 2005) Untuk
mendapatkan proses metabolisme glukosa normal, selain diperlukan mekanisme
serta dinamika sekresi yang normal, dibutuhkan pula aksi insulin yang
berlangsung normal. Rendahnya sensitivitas atau tingginya resistensi jaringan
tubuh terhadap insulin merupakan salah satu faktor etiologi terjadinya diabetes,
khususnya DM tipe 2. Baik atau buruknya regulasi glukosa darah tidak hanya
15
hepar dimana GLUT-2 berfungsi sebagai kendaraan pengangkut glukosa melewati
membrana sel kedalam sel. Dalam hal inilah jaringan hepar ikut berperan dalam
mengatur homeostasis glukosa tubuh. Peninggian kadar glukosa darah puasa,
lebih ditentukan oleh peningkatan produksi glukosa secara endogen yang berasal
dari proses glukoneogenesis dan glikogenolisis di jaringan hepar. Kedua proses
ini berlangsung secara normal pada orang sehat karena dikontrol oleh hormon
insulin. Manakala jaringan ( hepar ) resisten terhadap insulin, maka efek inhibisi
hormon tersebut terhadap mekanisme produksi glukosa endogen secara berlebihan
menjadi tidak lagi optimal. Semakin tinggi tingkat resistensi insulin, semakin
rendah kemampuan inhibisinya terhadap proses glikogenolisis dan
glukoneogenesis, dan semakin tinggi tingkat produksi glukosa dari hepar.
(McAuley et al, 2011; Ozougwu et al, 2013)
2.2.3 Efek metabolisme dari insulin
Gangguan, baik dari produksi maupun aksi insulin, menyebabkan gangguan pada
metabolisme glukosa, dengan berbagai dampak yang ditimbulkannya. Pada
dasarnya ini bermula dari hambatan dalam utilisasi glukosa yang kemudian diikuti
oleh peningkatan kadar glukosa darah. Gangguan metabolisme glukosa
disebabkan oleh dua faktor utama yakni tidak adekuatnya sekresi insulin
(defisiensi insulin) dan kurang sensitifnya jaringan tubuh terhadap insulin
(resistensi insulin), disertai oleh faktor lingkungan. (Senel E et al, 2011; Tosson et al, 2013))
Kelainan berupa disfungsi sel beta dan resistensi insulin merupakan faktor
16
bersifat progressif dan cenderung melibatkan pula gangguan metabolisme lemak
ataupun protein. Peningkatan kadar glukosa darah oleh karena utilisasi yang tidak
berlangsung sempurna pada gilirannya secara klinis sering memunculkan
abnormalitas dari kadar lipid darah. Tidak adekuatnya fase 1, yang kemudian
diikuti peningkatan kinerja fase 2 sekresi insulin, pada tahap awal belum akan
menimbulkan gangguan terhadap kadar glukosa darah. Secara klinis, barulah
pada tahap dekompensasi, dapat terdeteksi keadaan yang dinamakan Toleransi
Glukosa Terganggu yang disebut juga sebagai prediabetic state. Pada tahap ini mekanisme kompensasi sudah mulai tidak adekuat lagi, tubuh mengalami
defisiensi yang mungkin secara relatif, terjadi peningkatan kadar glukosa darah
postprandial. Dikatakan bahwa pada saat tersebut faktor resistensi insulin mulai
dominan sebagai penyebab hiperglikemia maupun berbagai kerusakan jaringan.
Semakin tingginya tingkat resistensi insulin dapat terlihat pula dari peningkatan
kadar glukosa darah puasa maupun postprandial. Sejalan dengan itu, pada hepar
semakin tinggi tingkat resistensi insulin, semakin rendah kemampuan inhibisinya
terhadap proses glikogenolisis dan glukoneogenesis, menyebabkan semakin tinggi
pula tingkat produksi glukosa dari hepar. (McAuley et al, 2001)
Hiperglikemia terjadi tidak hanya disebabkan oleh gangguan sekresi insulin
(defisiensi insulin), tapi pada saat bersamaan juga oleh rendahnya respons
jaringan tubuh terhadap insulin (resistensi insulin). Gangguan atau pengaruh
lingkungan seperti gaya hidup atau obesitas akan mempercepat progresivitas
perjalanan penyakit. Gangguan metabolisme glukosa akan berlanjut pada
17
jaringan tubuh. Rangkaian kelainan yang dilatarbelakangi oleh resistensi insulin,
selain daripada intoleransi terhadap glukosa beserta berbagai akibatnya, sering
menimbulkan kumpulan gejala yang dinamakan sindroma metabolik. (Wilcox et al, 2005; McAuley et al, 2011)
2.2.4 Resistensi insulin
Resistensi insulin merupakan gangguan metabolik akibat sel target gagal
merespon adanya insulin dengan kadar yang normal dalam sirkulasi yang pada
akhirnya terjadi hiperinsulinemia kompensata untuk mencapai respon fisiologi
yang optimal. (Sari R et al, 2010)
Diabetes mellitus terjadi ketika kemampuan sekresi insulin gagal untuk
menurunkan kadar glukosa plasma. Konsentrasi insulin secara umum meningkat
pada fase awal DM tipe 2, namun peningkatan ini tidak cukup untuk
mengkompensasi karena terjadi defek pada sel beta pankreas. Peningkatan
resitensi insulin berhubungan dengan akumulasi lemak dalam tubuh. (Shah et al, 2014)
Insulin dengan konsentrasi yang tinggi mengakibatkan terjadinya aktivasi
langsung maupun tidak langsung reseptor Insulin Growth Factor-1 (IGF-1) pada keratinosit dan fibroblast sehingga mengakibatkan terjadinya proliferasi. Reseptor
tirosin kinase lainnya seperti epidermal growth factor reseptor (EGFR) dan
fibroblast growth factor reseptor (FGFR). (Haimowitz et al, 1997)
18
terjadinya lesi ini. Proliferasi fibroblast yang terjadi pada skin tag tampaknya disebabkan oleh keadaan hiperinsulinemia melalui aktifasi reseptor IGF-1pada
permukaan sel. Skin tag berhubungan erat dengan kadar insulin saat puasa. (Banik, Lubach, 1987; Gaw, et al, 2004)
Sejak beberapa tahun terakhir, terdapat beberapa penelitian yang mencoba
mencari adanya hubungan antara skin tag dengan resistensi insulin, kadar insulin serum dan kadar IGF-1. Berdasarkan penelitian yang dilakukan Jowkar dkk,
terdapat peningkatan kadar insulin yang bermakna pada pasien dengan skin tag
dibandingkan dengan kelompok kontrol dan hal ini menyatakan adanya peran
penting insulin dan IGF-1 dalam patogenesis terjadinya skin tag. ( Safoury et al,
2009) Insulin bukan merupakan mediator satu-satunya untuk terjadinya skin tag
namun hal ini merupakan salah satu faktor yang sangat penting dalam
terbentuknya lesi ini. (Crook, 2000) Pada individu yang memiliki lesi skin tag
yang banyak penting dipertimbangkan terjadinya gangguan metabolisme
karbohidrat baik dalam bentuk manifestasi DM maupun resistensi insulin. (Naglaa
et al,2014) Rasi dkk menunjukkan bahwa pasien dengan lesi skin tag lebih dari 30 juga menderita diabetes dan IR (52%) sementara body mass index (BMI) tidak memiliki hubungan dengan jumlah lesi skin tag pada penelitian yang sama. (Mathur, Bhargawa, 1997)
Tamega dkk mengidentifikasi adanya hubungan yang independen antara
jumlah lesi skintag lebih dari 5 dengan peningkatan index HOMA-IR pada pasien
19
tag dengan BMI dan hipertrigliseridemia dan hal ini menguatkan pendapat bahwa
skin tag merupakan penanda resistensi insulin. (Tamega et al, 2010)
2.2.5 Homeostatic Model Assesment of Insulin Resistance (HOMA-IR)
Resistensi insulin merupakan suatu fenomena dimana absorbsi glukosa oleh sel
yang distimulasi oleh insulin mengalami penurunan. Sebagai respon terhadap hal
tersebut sel β pankreas terstimulasi untuk melepaskan lebih banyak insulin
sehingga terjadi peningkatan insulin secara abnormal. Hal ini selanjutnya akan
dapat menginduksi kegagalan sel β dan terjadi DM tipe 2.(Fitzgerald et al, 2014).
Homeostatic Model Assesment of Insulin Resistance (HOMA-IR) pertama kali diperkenalkan pada tahun 1985. Suatu teknik dengan metode yang
pemeriksaannya diambil dari glukosa basal dan insulin puasa. Teknik ini telah
digunakan secara luas sejak pertama kali dipublikasikan. (Wallace et al, 2004). Metode perhitungan matematika ini dikembangkan untuk aplikasinya dalam
membantu investigasi secara epidemiologi, dan digunakan untuk mengukur
resistensi insulin secara in vivo. Metode HOMA-IR ini dapat dikerjakan untuk
studi berskala besar dan dengan mengukur glukosa puasa serta insulin puasa.
(Esteghamati et al, 2010; Barbato et al, 2012). Pada suatu penelitian tentang penggunaan cut off point HOMA-IR pada pasien non diabetes oleh Geloneze et al
serta Tamega et al, berdasarkan kriteria International Diabetes Federation (IDF) didapatkan nilai cut off optimal untuk HOMA-IR pada pasien non diabetes untuk mengidentifikasi resistensi insulin dan sindrom metabolik adalah nilai >2,7
(sensitifitas 76,8% dan spesifisitas 66,7%). (Geloneze et al, 2009; Tamega et al,
20
HOMA-IR >2,5 sensitifitas >70% dan spesifisitas >60%. (Singh et al, 2013). Secara praktis resistensi insulin umumnya dihitung dengan menggunakan The Homeostasis Model Assesment of Insulin Resistance (HOMA-IR) dimana resistensi insulin = insulin puasa (mIU/L) x glukosa puasa (mmol/l)/22,5, dimana
nilai diatas 2,7 menunjukkan adanya resistensi insulin. (Barbato et al, 2012)
2.3 Insulin Growth Factor-1(IGF-1)
Insulin Growth Factor-1 (IGF-1) dan Insulin Growth Factor-2 (IGF-2) pertama kali diidentifikasi oleh Salmon dan Daughaday pada tahun 1957 namun
saat itu dinamai dengan “sulphation factor”. Pada tahun 1967, Rinderkinecht dan
Humbel mengisolasi dua substansi aktif dari serum manusia yang memiliki
kemiripan suatu proinsulin dan diberi nama Insulin Growth factor 1 dan 2. Insulin Growth Factor merupakan 70 aa polipeptida yang memiliki efek endokrin, parakrin dan autokrin. Insulin Growth Factor-1 adalah satu dari regulator utama proliferasi dan diferensiasi seluler, dimediasi oleh reseptor IGF-1 yang merupakan
famili dari tirosin kinase. (Laron., 2001; Sadagurski et al., 2006; Puche, Cortazar, 2012).
Sirkulasi IGF-1 secara umum berasal dari liver dibawah kendali GH.
Pengikatan GH pada reseptor hepatiknya merangsang ekspresi dan pelepasan
peptida IGF-1 ke sirkulasi dan memiliki afinitas yang tinggi terhadap Insulin Growth FactorBinding Protein (IGFBP) dan mempresentasikan bentuk endokrin IGF-1. Bioaktivitas IGF-1 ini diregulasi oleh enam IGFBP, insulin akan
menghambat produksi IGFBP-1 sehingga akan terjadi peningkatan
21
Insulin Growth Factor-1 adalah suatu hormon yang relevan pada masa embrio dan postnatal, walaupun utamanya diproduksi oleh liver sebenarnya setiap
jaringan mampu mensekresi IGF-1 untuk tujuan secara autokrin dan parakrin.
Sinyal autokrin dan parakrin diketahui bersifat morfogenik atau mitogenik untuk
keratinosit epidermal. IGF-1 yang diproduksi oleh keratinosit dari stratum
granulosum dan fibroblas dermal akan mengaktifkan reseptornya pada keratinosit
memfasilitasi penyebaran sel. Tidak didapatkan perbedaan bioaktivitas IGF-1
pada jenis kelamin. (Tavakkol et al, 1999; Haase et al, 2003; Vestergaard et al, 2014)
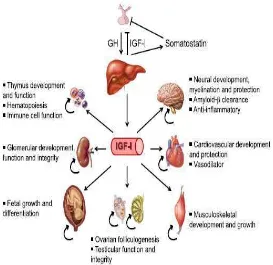
Gambar 2.3
Target dan aksis Growth Hormon dan
22
Pituritari (GH) dan liver (IGF-1) memiliki mekanisme umpan balik pada
kelenjar endokrin. IGF-1 menghambat sekresi GH pada hipotalamus melalui dua
mekanisme umpan balik, pertama menghambat ekspresi gen GH dan kedua
dengan merangsang sekresi somatostatin yang menghambat produksi GH, seperti
yang disajikan pada Gambar 2.3. Aktivasi reseptor GH di liver memicu sintesis
IGF-1 yang kemudian dilepaskan ke sirkulasi dan dapat ditemukan dalam bentuk
bebasnya yaitu IGFBP-3. (Puche,Cortazar, 2012)
2.4Resistensi Insulin Dengan Skin Tag
Sel kulit manusia memproduksi IGF dan binding proteinnya, walaupun tidak
didapatkan bukti bahwa GH diproduksi di kulit namun peptida turunannya yaitu
IGF-1 disintesis pada kulit. (Zouboulis, 2011) IGF-1 diproduksi oleh keratinosit
dari stratum granulosum dan fibroblas dermal, IGF-1 merangsang proliferasi
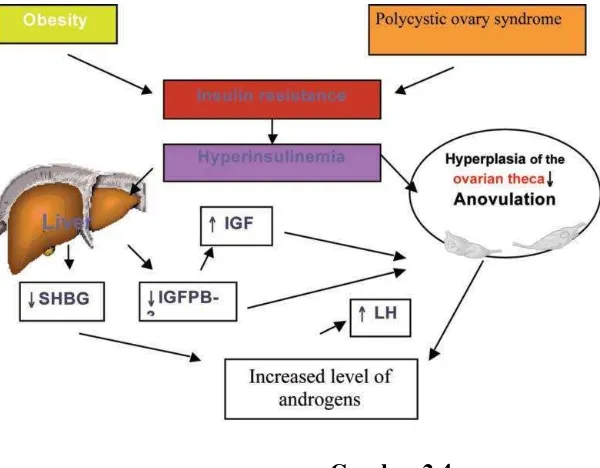
keratinosit melalui aktivasi reseptor IGF-1. (Gambar 2.4) (Barbato et al, 2012).
Gambar 2.4
23
Insulin dapat melewati dermoepidermal junction untuk mencapai
keratinosit. Pada konsentrasi yang rendah, insulin meregulasi metabolisme
karbohidrat, lipid dan protein dan dapat sebagai pemicu pertumbuhan dengan
berikatan pada reseptor insulin. Pada konsentrasi insulin yang tinggi seperti pada
kejadian resistensi insulin, maka insulin akan memicu efek pertumbuhan sel yang
berlebihan dengan berikatan pada IGF-1. Hiperinsulinemia akan merangsang
peningkatan IGF-1 pada keratinosit melalui reseptor IGF-1 mRNA yang berada di
permukaan keratinosit. Pada keratinosit, IGF-1 akan bekerja secara parakrin
dengan memediasi reseptor-reseptor respon proliferasi epitel kutaneus seperti
EGFR, FGFR membentuk akantosis, hiperkeratosis dan papilomatosis. Pada
dermal fibroblast, IGF-1 akan bekerja secara autokrin untuk berproliferasi dan
memproduksi jaringan ikat longgar yang berlebih, sehingga komponen-komponen
ini yang akan membentuk skin tag. (Bosseila et al, 2007; Tamega et al, 2010). Zaher et al (2007) mendapatkan bahwa sejumlah sitokin yang dihasilkan oleh sel mast seperti triptase, kimase, histamin, interleukin 4, dan basic FGF berperan dalam menstimulasi pertumbuhan dan proliferasi fibroblas, meningkatkan
penimbunan kolagen dan proliferasi keratinosit serta memicu hiperplasia dan
akantosis epidermis sehingga terbentuk skin tag.
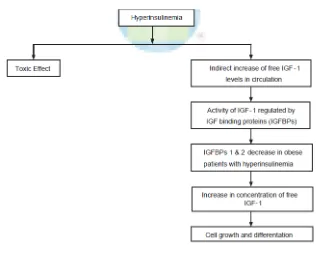
Tingginya kadar insulin dalam darah bisa berefek langsung dengan
mengaktifkan IGF-1 signaling pathway, atau secara tidak langsung dengan cara mengaktifkan level free IGF-1 pada sirkulasi. Aktivitas IGF-1 diregulasi oleh
24
Terjadi penurunan IGFBP1 dan IGFBP2 pada orang dengan hiperinsulinemia
sehingga meningkatkan perangsangan pertumbuhan dan diferensiasi sel. (Phiske,
2014)
Epidermal Growth Factor dan reseptor insulin merupakan reseptor yang memiliki aktifitas tirosin kinase sebagai salah satu faktor yang mempengaruhi
proliferasi epidermis diferensiasi sel dan metabolisme sel. Fungsi sinyal insulin
secara fisiologis membantu metabolisme glukosa, sintesis lemak dan protein,
sedangkan EGF menginduksi respon proliferasi. Selain itu insulin sendiri dapat
meningkatkan stimulasi EGF sehingga terjadi sintesis DNA dan respon
proliferasi. Ekspresi EGF yang berlebih merupakan pengaruh dari meningkatnya
insulin akibat resistensi sehingga akan meningkatkan kerja proliferasi dari EGF
ini. (Zielinski et al, 2009)
Skin tag multipel seringkali ditemukan pada orang-orang obesitas dan diabetes non-insulin dependent, abnormalitas resistensi insulin didasari pada 2 kondisi. Proliferasi fibroblas yang muncul pada skin tag lebih dikarenakan oleh adanya hiperinsulinemia melalui aktivasi reseptor insulin-like growth factor (IGF-1) yang muncul pada permukaan. Skin tag dekat hubungannya dengan level fasting insulin. (Mathur et al., 1997; Kabir, et al,. 2010; Isard, et al., 2011)
Beberapa tahun belakangan terdapat studi-studi yang berusaha
memperlihatkan hubungan antara skin tag dan resistensi insulin, dengan level serum dan level IGF-1. Jowkar et al, level insulin pada pasien skin tag jauh lebih besar daripada individu kontrol sehingga memperlihatkan pentingnya insulin pada
25
et al., 2010). Sama dengan akantosis nigrikan, insulin bukanlah satu-satunya mediator pembentukan skin tag namun merupakan yang paling penting pada pembentukan lesi ini. (Sudy et al., 2008)
Gambar 2.5
Peran IGF pada jalur sinyal pada keratinosit dan melanosit (Phiske, 2014)
Pada individu yang memiliki skin tag multipel, sangat penting untuk mencurigai kelainan metabolisme karbohidrat baik dalam bentuk resistensi insulin
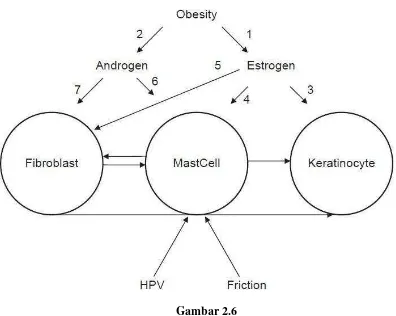
atau diabetes melitus. (Demir et al, 2002). Skin tag terkait dengan obesitas dan terjadi gangguan hormonal yaitu adanya peningkatan hormon estrogen dan
androgen (Gambar 2.6). Fungsi dari hormon ini adalah sebagai
pengaktivasi/pemecah trigliserid jaringan adiposa. Pada orang dengan obesitas
terjadi penimbunan/penumpukan jaringan adiposa dimana trigliserida yang
tersimpan mengalami penumpukan dan resistensi sehingga hormon estrogen yang
26
untuk mengekspresikan reseptor estradiol (ER α dan ER β) guna mengikat
estrogen sehingga merangsang aktivitas keratinosit dan fibroblast. Sel mast
berinteraksi dengan keratinosit dan fibroblast sehingga terbentuk skin tag.
(Safoury et al, 2010).
Gambar 2.6
Pembentukan skin tag (Safoury et al, 2010)
Resi et al memperlihatkan bahwa pasien yang memiliki lebih dari 30 lesi
memiliki risiko lebih tinggi menderita diabetes (52%) walaupun BMI tidak
27
Tidak ditemukan hubungan antara topografi dari skin tag dan metabolisme karbohidrat kecuali skin tag pada area inframamae pada wanita. (Sudy et al., 2008).
Crook melaporkan 4 pasien dengan skin tag multipel dan semua pasien mengalami peningkatan level serum trigliserida dan penurunan level HDL
kolesterol. (Crook, 2000). Skin tag multipel (lebih dari 8 lesi) lebih sensitif daripada akantosis nigrikan dalam identifikasi perubahan metabolisme
karbohidrat namun kurang spesifik. (Abbas et al, 2007). Keberadaan skin tag sebagai penanda deteksi hiperinsulinemia didasari dengan penemuan sindrom X.
(Sudy et al, 2008).
Tamega et al mengidentifikasi hubungan independen antara adanya 5 jumlah skin tag dengan peningkatan indek HOMA-IR pada pasien dermatologi. Hubungan signifikan dengan BMI dan hipertrigliserida ditemukan pada studi ini