TBP 06
Produksi PUFA dari
Aspergillus oryzae
Berbasis Onggok Dan Ampas Tahu
Dengan Variasi Konsentrasi Karbon Dan Rasio Karbon-Nitrogen
Laras Ragil Kuncoro Putri, Rita Arbianti, Tania Surya Utami, Heri Hermansyah Program Studi Teknologi Bioproses, Departemen Teknik Kimia, Fakultas Teknik,
Universitas Indonesia, Kampus UI, Depok 16424 [email protected]
Abstrak
Lemak menjadi nutrisi yang berperan penting dalam proses metabolisme. Sebanyak 60% nutrisi yang dibutuhkan untuk perkembangan otak adalah berupa lemak. Polyunsaturated Fatty Acid (PUFA) yang terdiri dari omega-3 (linoleate) dan omega-6 (linolenat), merupakan asam lemak esensial yang digunakan untuk menjaga bagian-bagian struktural dari membran sel, serta mempunyai peran penting dalam perkembangan otak. Kapang adalah salah satu
mikroorganisme oleaginous yang potensial sebagai sumber alternatif penghasil PUFA.
Peneliti menggunakan Aspergillus oryzae sebagai mikroorganisme penghasil PUFA.
Produksi single cell oil (SCO) dari mikroorganisme terhambat pada biaya operasional yang
mahal, sehingga perlu adanya pemanfaatan limbah untuk menekan biaya operasional. Oleh karena itu, dalam penelitian ini digunakan limbah industri yaitu onggok tapioka dan ampas tahu sebagai medium kultivasi. Penelitian ini dilakukan dengan melalui dua tahap kultivasi. Kultivasi tahap pertama dilakukan dengan menggunakan variasi konsentrasi karbon (2% w/w, 3% w/w, 4% w/w, 5% w/w, dan 6% w/w), sedangkan kultivasi tahap kedua dilakukan dengan menggunakan variasi rasio C/N (20:1, 30:1, 40:1, 50:1). Setiap tahap kultivasi dilakukan beberapa proses untuk memperoleh SCO antara lain yaitu, kultur medium cair, pemanenan, dan ekstraksi. Proses ekstraksi dilakukan menggunakan etanol sebagai pelarut
food grade. Hasil penelitian menunjukkan bahwa kandungan PUFA dalam lipid A. oryzae
meningkat seiring peningkatan konsentrasi karbon. Persentase PUFA tertinggi berada pada konsentrasi karbon 6% (w/w), yaitu sebesar 60,8% (w/w). Pada variasi rasio C/N, persentase
PUFA dalam lipid A. oryzae relatif menurun seiring dengan peningkatan rasio C/N.
Persentase PUFA tertinggi berada pada rasio 30:1, yaitu sebesar 56,1% (w/w).
Kata kunci: Ampas tahu, Aspergillus oryzae, onggok, Polyunsaturated Fatty Acid,Single Cell
Oil.
1.0 PENDAHULUAN
Lemak menjadi salah satu nutrisi yang berperan penting dalam proses pertumbuhan. Fungsi utama lemak adalah sebagai sumber energi (Ketaren, 1986). Kurang lebih 60% nutrisi yang dibutuhkan untuk perkembangan otak adalah berupa lemak. Lemak memiliki dua komponen dasar, yaitu asam lemak dan gliserol. Asam lemak dibedakan menjadi asam
lemak jenuh (saturated fatty acid) dan asam lemak tak jenuh (unsaturated fatty acid)
senyawa asam lemak tak jenuh. Berdasarkan letak ikatan rangkapnya, asam lemak tak
jenuh dibedakan menjadi PUFA-poly unsaturated fatty acid (omega-3, omega-6) dan MUFA-
monounsaturated fatty acid (omega-9) (Helena, 2001). PUFA yang mengandung omega-3
(linoleate) dan omega-6 (linolenate) merupakan asam lemak esensial yang tidak dapat
dibentuk sendiri oleh tubuh sehingga harus mendapatkan asupan dari luar tubuh (Sartika, 2008).
Hingga saat ini, penelitian mengenai sumber alternatif PUFA masih terus mengalami perkembangan. Sumber alternatif yang saat ini banyak diteliti adalah mikroorganisme
penghasil lipid atau yang biasa disebut dengan mikroorganisme oleaginous.Kapang
merupakan mikroorganisme oleaginous yang mudah untuk dikultivasi karena kapang dapat
hidup dalam keadaan asam dan memiliki toleransi terhadap pH yang cukup lebar, yaitu 2 - 8,5, dapat bertahan dalam kondisi dengan kadar gula ataupun garam yang tinggi (Cantrell,
1971 dalam Wassef, 1975).Dalam penelitian ini, peneliti menggunakan Aspergillus oryzae
sebagai mikroorganisme penghasil PUFA.Peneliti menggunakan limbah industri, yaitu
onggok tapioka dan ampas tahu sebagai medium fermentasi bagi Aspergillus oryzae. Variasi
yang digunakan dalam penelitian ini adalah konsentrasi karbon dan rasio C/N untuk
memperoleh konsentrasi PUFA tertinggi dari kapang.Peneliti menggunakan pelarut lipid food
grade, yaitu etanol untuk mengekstrak lipid, dan metode Gas Chromatography untuk
menganalisis kandungan PUFA.
2.0 PERCOBAAN 2.1 Alat dan Bahan
Alat yang digunakan antara lain Shaker Waterbath Memmert WNB14L4, Ultrasonic cleaner Elma S30H (2.75L), GC Shimadzu tipe 2010 dengan FID dan split injection. Bahan
yang digunakan adalah isolat Aspergillus oryzae, onggok, ampas tahu, dan medium basalt.
2.2 Variabel Penelitian
Variabel yang divariasikan dalam penelitian ini adalah konsentrasi karbon dan rasio
C/N pada medium fermentasi A. oryzae. Konsentrasi karbon yang digunakan dalam
penelitian ini adalah variasi 2% (w/w), 3% (w/w), 4% (w/w), 5% (w/w), dan 6% (w/w), dan rasio massa C/N yang digunakan dalam penelitian ini adalah 20:1, 30:1, 40:1, dan 50:1.Variabel yang diukur pada penelitian ini adalah persentase kandungan PUFA. Variabel yang dijaga tetap dalam penelitian ini adalah temperatur pada rentang 25 -30 , pH pada rentang 4,5-6,5, kecepatan agitasi 120 rpm, dan waktu inkubasi hingga memasuki fase stasioner.
Penelitian ini dilakukan dalam beberapa tahap yaitu tahap persiapan, pembuatan
stok kultur, kultur medium cair, pemanenan, ekstraksi, dan uji kandungan PUFA. 2.3 Tahap Persiapan
Persiapan yang dilakukan meliputi pembuatan tepung onggok dan tepung ampas tahu, pengujian kandungan karbon (Walkey dan Black) dan nitrogen (Kjeldahl) dalam tepung onggok dan ampas tahu, serta sterilisasi alat.
2.4 Pembuatan Stok Kultur
Perbanyakan kapang dilakukan dengan kultur yang dilakukan pada medium PDA
juga bertujuan untuk memperbanyak spora kapang yang akan digunakan pada kultur cair. Kultur pada medium PDA diinkubasi selama 3-4 hari pada suhu 25-30 .
2.4.1 Kultur Medium Cair
Kultur pada medium cair dilakukan sebanyak 2 kali, tahap yang pertama kultur medium cair dilakukan menggunakan variasi konsentrasi karbon pada konsentrasi 2% (w/w), 3% (w/w), 4% (w/w), 5% (w/w), dan 6% (w/w) dengan rasio C/N adalah 30:1. Tahap kedua kultur medium cair dilakukan menggunakan variasi rasio C:N dengan konsentrasi karbon adalah konsentrasi karbon yang memberikan berat kering biomassa
tertinggi.. Kultur medium cair dilakukanpadareaktor batch100 mL dengan menggunakan
medium onggok dan ampas tahu sebagai sumber karbon dan nitrogen, dan ditambahkan pula mikronutrien pada medium. Kultur cair ini dilakukan padasuhu25-30 ,pH4,5-6,5,kecepatan
agitasi 120rpm, dengan waktu inkubasi selama 5 hari di dalam water shaker bath.
2.5 Pemanenan
Pemanenan dimulai dari tahap penyaringan menggunakan kertas saring, kemudian dilakukan penimbangan berat basah biomass. Biomass dikeringkan dengan oven pada
suhu 70oC selama 24 jam, hingga berat konstan kemudian dilakukan penimbangan berat
kering.
2.6 Ekstraksi
Proses ekstraksi dilakukan dengan mencampur biomass dan etanol dengan perbandingan massa 1:15. Proses pemecahan dinding sel kapang dilakukan dengan
sonikasi. Proses ekstraksi lipid dilakukan selama 3 jam dengan suhu 45 (Saxena et al.,
2011), kemudian campuran disentrifugasi hingga terpisah antara biomassa dan campuran etanol-lipid. Campuran lipid dan etanol dievaporasi untuk memisahkan pelarut dari lipid dan meregenerasi pelarut. Lipid yang diperoleh berupa lipid kering atau konsentrat yang
selanjutnya diuji. Penimbangan massa lipid digunakan untuk menghitung yield lipid.
2.7 Uji Kandungan PUFA
Analisis konsentrasi PUFA dengan menggunakan GC yang ada di Balai Besar Industri Agro (BBIA), Bogor. Metode uji menggunakan GC dilakukan dengan metode GC-IUPAC 2.301
7th Edition.
3.0 HASIL DAN PEMBAHASAN 3.1 Analisis Mutu Medium Limbah
Analisis karbon dilakukan dengan menggunakan alat spektrometer UV VIS dengan panjang gelombang 651 nm. Berikut ini adalah tabel hasil analisis kandungan karbon dan nitrogen dalam limbah yang dilakukan.
Tabel 1. Analisis Kandungan Karbon dan Nitrogen Limbah
Komponen Onggok Tapioka (% w/w) Ampas Tahu (% w/w) Karbon 30,25 26,5 Nitrogen 0,2 3
B er at K e ri n g B io ma ss ( gr am)
Hasil analisis diatas menunjukkan bahwa dalam formulasi medium onggok tapioka berperan sebagai sumber utama karbon karena kandungan karbonnya lebih tinggi daripada ampas tahu, sedangkan ampas tahu berperan sebagai sumber utama nitrogen karena kandungan nitrogen ampas tahu lebih tinggi daripada onggok tapioka.
3.2 Pertumbuhan A. oryzae
Berikut ini adalah kurva pertumbuhan kapang Aspergillus oryzae yang dilakukan hingga mencapai fase stasioner.
1.8 stationer phase 1.6 1.4 1.2 1 0.8
0.6 Lag phase Log phase
0.4
0.2
0
-0.2 0 1 2 3 4 5 6 7
Hari
Gambar 1. Kurva Pertumbuhan Aspergillus Oryzae
Pertumbuhan kapang baru akan terlihat jelas ketika sudah melalui masa kultivasi 24 jam (Gandjar, 2006). Hari ke-1 hingga hari ke-4 terjadi fase eksponensial. Puncak fase eksponensial terjadi pada hari ke-5. Pertumbuhan sel pada hari ke-5 hingga hari ke-6 tidak terjadi peningkatan yang signifikan dan bahkan hampir sama berat kering biomassanya.
Oleh karena itu, pada hari ke-5 kapang dikatakan telah memasuki fase stasioner. Tung et al.,
(2004) juga melakukan kultivasi A.oryzae dalam limbah onggok tapioka dan menghasilkan
grafik pertumbuhan kapang yang memperlihatkan bahwa fase stasioner terjadi pada rentang hari ketiga hingga hari kelima. Menurut Elreesh (2013), akumulasi lipid mencapai titik maksimum pada saat pertumbuhan kapang memasuki fase stasioner, dan akan semakin menurun karena saat nutrisi telah habis terkonsumsi oleh kapang, maka lipid yang terakumulasi akan digunakan untuk proses metabolisme sel. Oleh karena itu dalam
penelitian ini proses pemanenan akan mengacu pada kurva pertumbuhan kapang A. oryzae
dan dilakukan pada fase stasioner yaitu di hari ke-5 proses fermentasi. 3.3 Pengaruh Konsentrasi Karbon terhadap Produksi PUFA
Konsentrasi sumber karbon secara alami dapat mengatur produksi lipid mikroorganisme melalui proses represi katabolik (Lopez et al., 2013). Perbedaan konsentrasi karbon mengakibatkan perbedaan pertumbuhan sel pada kapang. Variasi konsentrasi karbon yang digunakan di dalam penelitian ini, yaitu 2% (w/w), 3% (w/w), 4% (w/w), 5% (w/w), dan 6% (w/w). Pengambilan data untuk setiap variasi dilakukan sebanyak dua kali untuk lebih menambah keakuratan dari data yang diperoleh di dalam penelitian ini.Konsentrasi karbon pada medium pertumbuhan dapat mempengaruhi jumlah biomassa
dan kadar lipid. Akumulasi lipid pada mikroorganisme oleaginous terjadi dalam dua tahap,
yaitu tahap poliferasi sel dan tahap akumulasi lipid (Wynn dan Anderson, 2001 dalam Bayazit, 2014). Tahap poliferasi sel merupakan tahap perkembangan sel dengan laju maksimum yang berlangsung terus menerus sampai nutrien selain karbon terbatas, khususnya nitrogen. Karbon yang berlebih tersebut akan terus dikonsumsi oleh
B e ra t ke rin g (g) Y ie ld Li p id (% w /w )
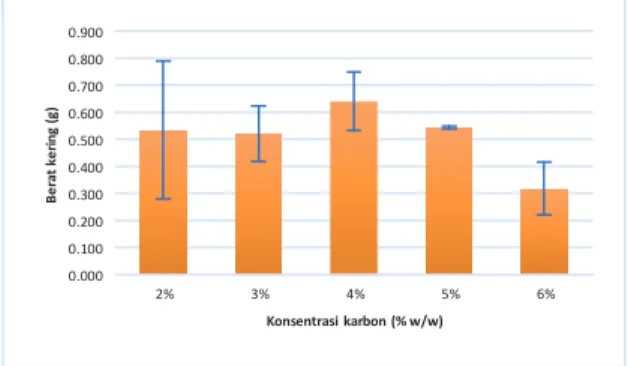
perolehan rata-rata berat kering biomassa pada setiap variasi konsentrasi karbon disajikan pada gambar di bawah ini.
0.900 0.800 0.700 0.600 0.500 0.400 0.300 0.200 0.100 0.000 2% 3% 4% 5% 6% Konsentrasi karbon (% w/w)
Gambar 2. Perolehan Rata-Rata Berat Kering Biomassa pada Variasi Konsentrasi Karbon Gambar di atas memperlihatkan perolehan jumlah berat kering biomassa relatif meningkat seiring dengan meningkatnya konsentrasi karbon hingga penambahan konsentrasi karbon 4% (w/w). Perolehan jumlah berat kering biomassa mencapai 0,64 g.
Perolehan yield lipid dengan variasi konsentrasi karbon dalam penelitian ini disajikan
pada grafik berikut ini.
14.0 12.0 10.0 8.0 6.0 4.0 2.0 0.0 2% 3% 4% 5% 6% Konsentrasi karbon
Gambar 3. Perolehan Yield Lipid pada Variasi Konsentrasi Karbon
Berdasarkan grafik di atas, maka persentase yield lipid paling besar diperoleh pada konsentrasi karbon 5% (w/w). Nilai deviasi yang diperoleh pada data konsentrasi karbon 5% (w/w) dan 6% (w/w) cukup besar dikarenakan perbedaan nilai data pertama dan data k edua pada setiap variasi cukup besar. Perbedaan ini terjadi karena perbedaan inokulum yang digunakan untuk kultur pada data pertama dan data kedua. Kualitas inokulum menjadi sebuah penentu keberhasilan dari fermentasi kapang, sehingga dapat mempengaruhi
perolehan yield lipid (Papagianni et al., 2001).
Yield lipid pada konsentrasi karbon 6% mengalami penurunan jika dibandingkan dengan konsentrasi karbon 5%. Penurunan tersebut dapat terjadi karena terjadi peningkatan
potensial osmotik pada konsentrasi substrat yang terlalu tinggi (Ahmed et al., 2006). Hal ini
menyebabkan pembentukan sel kapang menjadi tidak optimal. Jumlah biomassa yang rendah menyebabkan sedikitnya kontribusi sel untuk mensintesis lipid pada tubuhnya,
sehingga menyebabkan yield lipid menjadi rendah (Sari, 2015).
Pada konsentrasi karbon 2% (w/w) dan 3% (w/w) juga menghasilkan yield lipid yang
rendah. Perolehan yield lipid yang rendah pada konsentrasi karbon tersebut dapat terjadi
karena sebagian besar karbon yang dikonsumsi digunakan untuk proses poliferasi sel, sedangkan karbon yang digunakan dalam proses akumulasi lipid hanya terkonsumsi dalam
P ers en ta se a sam le mak t ak je nu h (% w /w)
Yield lipid tersebut lebih tinggi dibandingkan dengan yield lipid pada konsentrasi karbon 2%
(w/w) dan 3% (w/w) dan lebih rendah dibandingkan dengan konsentrasi karbon 5% (w/w) dan 6% (w/w). Nilai deviasi pada konsentrasi karbon 4% (w/w) lebih kecil jika dibandingkan dengan konsentrasi karbon 5% (w/w) dan 6% (w/w). Oleh karena itu, dengan mempertimbangkan jumlah berat kering biomassa dan nilai deviasi, konsentrasi karbon yang digunakan untuk tahap kultivasi dengan variasi rasio C/N adalah konsentrasi karbon 4% (w/w).
Lipid yang diperoleh dari proses ekstraksi kemudian dianalisis menggunakan metode
uji GC-IUPAC 2.301 7th Edition untuk mengetahui komposisi asam lemak yang ada di
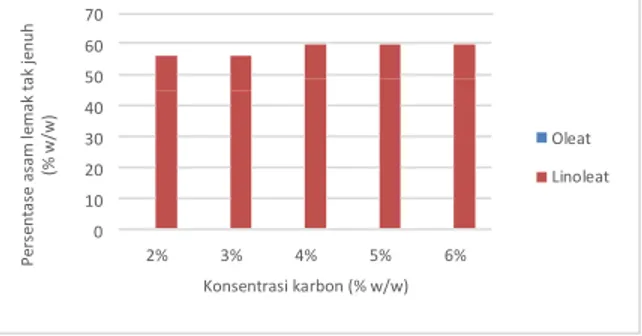
dalamnya.Persentase asam lemak tak jenuh di dalam lipid dengan variasi konsentrasi karbon meningkat seiring dengan peningkatan konsentrasi karbon.Grafik berikut ini merupakan grafik yang menyajikan persentase komposisi asam lemak tak jenuh dalam lipid dengan variasi konsentrasi karbon.
70 60 50 40 30 20 10 0 2% 3% 4% 5% 6% Konsentrasi karbon (% w/w) Oleat Linoleat
Gambar 4. Persentase Asam Lemak Tak Jenuh Lipid A. Oryzae dengan Variasi Konsentrasi Karbon
Komposisi asam lemak tak jenuh terbesar diperoleh pada konsentrasi karbon 6% (w/w) yaitu sebesar 62,79% (w/w). Pada penelitian terdahulu yang dilakukan oleh Yangmin
et al. (2015), Muniraj et al. (2013), dan Muslimah (2015), secara berurutan menghasilkan
yield asam lemak tak jenuh maksimum, yaitu 0,855 mg/100mL medium, 202,65 mg/100mL
medium, dan 12,42 mg/100mL medium. Yield asam lemak maksimum yang dihasilkan pada
penelitian ini adalah 143 mg/100 mL. Yield asam lemak tak jenuh pada penelitian ini lebih
tinggi apabila dibandingkan dengan hasil dari Yangmin et al. (2015) dan Muslimah (2015),
sedangkan jika dibandingkan dengan Muniraj et al. (2013), maka nilainya lebih rendah.
Perbedaan besar yield asam lemak tak jenuh dengan Yangmin et al. (2015) disebabkan
karena perbedaan jenis medium dan kondisi operasi kultivasi. Yangmin et al. (2015)
menggunakan medium RSM yang komposisi utamanya adalah selulosa, hemiselulosa, dan lignin, yang mana kandungan seratnya lebih sulit didegradasi oleh mikroorganisme.
Perbedaan hasil yield lipid dengan Muslimah (2015) terjadi karena perbedaan nilai
konsentrasi karbon yang digunakan dalam medium kultur. Hasil yield asam lemak tak jenuh
yang dihasilkan oleh Muniraj et al. (2013) lebih tinggi karena medium yang digunakan berupa
limbah cair kentang yang mengandung amilum sebesar 31,2% (w/w). 3.4 Pengaruh Rasio C/N terhadap Produksi PUFA
Dari empat variasi rasio yang diteliti, diketahui bahwa pada rasio 40:1 nilai rata -rata berat kering menghasilkan nilai tertinggi dengan galat < 5%. Hasil ini berbeda dengan hasil
yang didapat oleh Muslimah (2015) yang menemukan bahwa yield berat kering biomassa
kapang tertinggi didapat pada rasio C/N 30:1. Perbedaan ini dapat disebabkan karena konsentrasi karbon yang berbeda diantara kedua penelitian, dimana penelitian yang
Y ie ld Li p id (% ) B e ra t K e ri n g (g ram )
dilakukan Muslimah (2015) menggunakan konsentrasi karbon 2% (w/w) sedangkan penelitian ini menggunakan konsentrasi karbon 4% (w/w).
25.00 20.00 15.00 10.00 5.00 0.00 20 30 40 50 Rasio C/N
Gambar 5. Perolehan Berat Kering Biomassa dalam Variasi Rasio C/N
Berdasarkan Gambar 5.terlihat bahwa rata-rata berat kering sampel mula-mula meningkat hingga rasio 40:1 kemudian turun pada 50:1. Hal ini menunjukkan bahwa pada rasio yang rendah, nitrogen sangat berpengaruh pada aktivitas pertumbuhan sel seperti sintesis protein dan asam nukleat. Pada rasio yang lebih tinggi dari 40:1, nilai rata-rata berat kering menurun, hal ini dapat disebabkan karena pada konsentrasi karbon yang terlampau tinggi dibanding nitrogen, sel akan sangat cepat mengkonsumsi nitrogen dan menggunakan
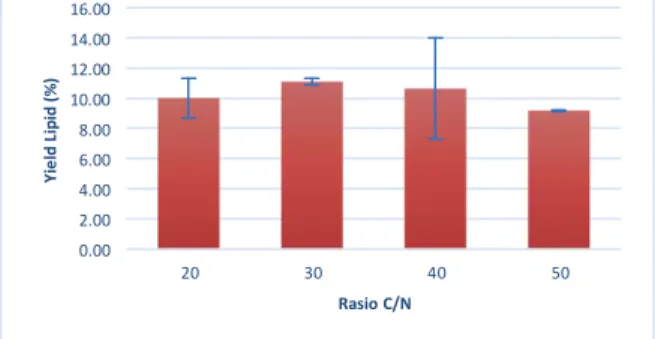
kelebihan nutriennya untuk dikonversi menjadi triasilgliserol sebagai media penyimpanan sel. 16.00 14.00 12.00 10.00 8.00 6.00 4.00 2.00 0.00 20 30 40 50 Rasio C/N
Gambar 6. Perolehan Yield Lipid Dalam Variasi Rasio C/N
Pada penelitian yang dilakukan didapatkan hasil rata-rata yield lipid terhadap berat
kering terhadap rasio C/N (duplo) dapat dilihat pada Gambar 6. Dari empat variasi rasio yang diteliti, diketahui bahwa pada rasio 30:1 nilai rata-rata berat kering menghasilkan nilai tertinggi.Hasil yang didapat dari keempat variasi relatifsama, yaitu sekitar 9% (w/w)sampai 11% (w/w). Hal ini menunjukkan bahwa pada semua rasio, penambahan atau pengurangan
rasio C/N tidak signifikan mempengaruhi perubahan total yield lipid. Hal serupa juga
ditemukan pada penelitian yang dilakukan oleh Braunwald et al. (2013), yang menunjukkan
bahwa pada peningkatan rasio C/N tidak ditemukan peningkatan total lipid yang dihasilkan. Hal ini menunjukkan bahwa nitrogen yang terdapat di dalam medium belum cukup terdeplesi untuk mengalihkan metabolisme sel ke produksi lipid.
Pada pengujian kadarpolyunsaturated fatty acid (PUFA) yang dilakukan dengan
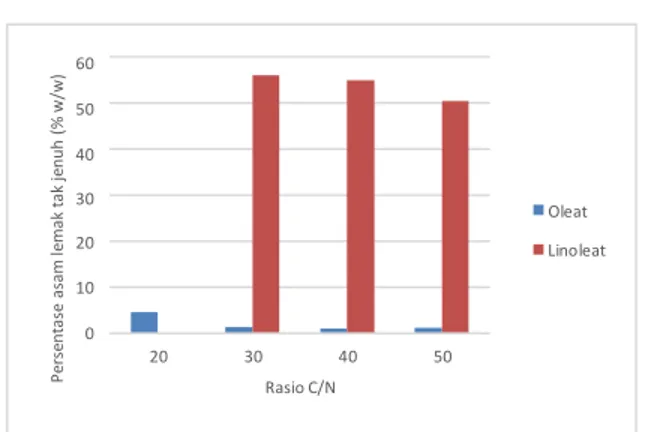
P ers en ta se a sam le mak t ak je nu h ( % w /w) 60 50 40 30 Oleat 20 Linoleat 10 0 20 30 40 50 Rasio C/N
Gambar 7. Persentase Asam Lemak Tak Jenuh Lipid A. Oryzae Dengan Variasi Rasio C/N
Pada rasio konsentrasi 30:1 menghasilkan nilai yield PUFA paling tinggi yakni
56,06%. Pada pengujian, diketahui bahwa PUFA yang dihasilkan tersusun dari asam linoleat sedangkan MUFA tersusun dari asam oleat. Pada rasio 20:1, tidak terdeteksinya PUFA dapat disebabkan oleh adanya pemutusan ikatan rangkap pada saat proses evaporasi, sehingga sebagian besar asam lemak yang terdeteksi adalah asam lemak jenuh.Berdasarkan hasil yang didapat, nilai kandungan PUFA dalam lipid yang dihasilkan pada penelitian ini tergolong sangat baik jika dibandingkan dengan beberapa penelitian serupa. Menurut Muslimah (2015), kandungan PUFA maksimum yang dihasilkan sekitar
35% sedangkan menurut Braunwald et al. (2013), kandungan PUFA maksimum yang dapat
dihasilkan adalah 31,17%. Perbedaan jumlah kandungan PUFA hasil penelitian ini dengan yang dilakukan Muslimah (2015) dapat disebabkan karena adanya perbedaan konsentrasi karbon awal yang diberikan pada medium.
4.0 KESIMPULAN
Kandungan PUFA dalam lipid yang dihasilkan oleh A. oryzae meningkat seiring
dengan peningkatan konsentrasi karbon. Kandungan PUFA terbesar diperoleh pada variasi konsentrasi karbon 6% (w/w), yaitu 60,8% (w/w) dalam bentuk asam linoleat. Kandungan
PUFA dalam lipid yang dihasilkan oleh A. oryzae menurun seiring dengan peningkatan rasio
C/N. Kandungan PUFA terbesar diperoleh pada variasi rasio karbon -nitrogen 30:1, yaitu 56,1% (w/w) dalam bentuk asam linoleat.
Daftar Pustaka
Abu-Elreesh,Gadallah dan Desouky Abd-El-Haleem, “An Effective Lipid- Producing Fungal
sp. Strain DGB1anditsusefor Biodiesel Production,” AcademicJournals,Vol.12(August,
2013),hal.34.
Ahmed,S.U.,Singh,S.K.,Pandhey,A.,Kanjilal,S.,Prasad,R.B.(2006).Effectof various process
parameters on the production of γ-linolenicacid in submerged fermentation. Food
technol. Biotechnol, 44 (2),283-287
Akpinar-Bayizit, Arzu, Tulay Ozcan, Lutfiye Yilmaz-Ersan, Fikri Basoglu, “Singlecell oil
(SCO) production by Fusarium species using cheese whey as asubstrate,”
Mljekarstvo,vol.64(2)(2014),hal.111-118.
Amaretti,A., Raimondi,S., Sala, M.,Roncaglia,L.,DeLucia,M.,Leonardi, A., Rossi,M.(2010).
Single celloils of the cold-adapted oleaginous yeast Rhodotorulaglacialis
Gandjar, Indrawati., Sjamsuridzal, Wellyzar., Oetari,Ariyanti.(2006).Mikologi: Dasar dan
terapan. Jakarta: Yayasan OborIndonesia.
Gao, Li et al. 2007. Effects of carbon concentration and carbon to nitrogen ratio on the growth and sporulation of several biocontrol fungi. Mycological Research III hal. 87 - 92.
Hall,M.J.Ratledge,C,“Lipid accumulation in anoleaginous yeast (Candida107) growing on
glucose under various conditions in aoneand two -stage continuous
culture,”App.Environment.Microb,Vol.33(1977),hal.577-584.
Jackson, Mark A. (1990). Carbon Concentration and Carbon-to-Nitrogen Ratio Influence Submerged-Culture Condition by the Potential Bioherbicide Colletotrichum truncatum NRRL 13737. American Society for Microbiology, vol. 56, No. 11.
Ketaren, S. 1986. Pengantar Teknologi Minyak dan Lemak Pangan. Jakarta: Penerbit
Universitas Indonesia.
Kirana, V. N.,Atmodjo, K., Rahardjo, B.(2014).Hubungan variasi perbandingan konsentrasi
molase:amonium nitrat terhadap pertumbuhan dan kandungan minyak
Aspergillusterreus dan Penicilliumpinophilum.JurnalBiologi.pp.1-8.
Logaraj,T.V.(2010). Studies on selectedplants and microbes withspecial reference topoly unsaturated fatty acid.Thesis.Food Microbiology Department, Universityof Mysore. Lopez,J.L.,J.A.S.Perez,J.M.F.Sevilla,F.G.A.Fernandez,E.M.Grima.Y. Christi. (2003).
Production of lovastatin by Aspergillus terreus: effect of the C:N ration.Enzyme and
Microbial Technology33: 270-27
Muniraj, Iniya Kumar, Liwen Xiao, Zhenhu Hu, Xinmin Zhan, dan Jianghong Shi, “Microbial
lipid production from potato processing waste water using oleaginous filamentous
fungi Aspergillusoryzae,”ElsevierLtd,(2013), hal.1-7.
Muslimah. 2015. Pengaruh Rasio Karbon/Nitrogen Berbasis Onggok da Ampas Tahu untuk
Produksi AA, DHA, EPA dari Aspergillus oryzae. Depok: Universitas Indonesia. Papagianni,
Maria et al. 2001. Submerged and Solid-State Phytase Fermentation by
Aspergillus niger: Effect of Agitation and Medium Viscosity on Phytase Production, Fungal Morphology and Inoculum Performance. Food Technology. Bioethanol. 39 (4) 319-326.
Papanikolaou,S,A.Dimou,S.Fakas,P.Diamantopoulou,A.Philippoussis,M. Galiotou-
Panayotou,dan G.Aggelis,“Biotechnological conversion of waste cooking olive oil into
lipid-rich bio mass using Aspergillus and Penicillium strains,” Journal of Applied
Microbiology, vol110(2013),hal 1138-1150.
Papanikolaou,S.,Panayotou,M.G.,Chevalot,I.,Komaitis,M.,Marc,I.,(2006). Influence of glucose and saturated free fatty acid mixture on citric acid and lipid production by
Yarrowialipolytica. Current Microbiology.52:134-142.
Papanikolaou.S.,Chevalot.I.,Komaitis.M.,Marc.I.,Aggelis.G.(2001)Single cell oil production by
Yarrowialipolytica growing on anindustrial derivative of animal fat in batch cultures,
Appl Microbial Biotechnol, Verlag, 58:308-312.
Ratledge, C, “Lipids. In: Biotechnology,” Weinheim, VCH, Vol. 4 (1986), hal.185-198.
Ratledge,C.&Wynn,J.P.(2002). Advances in applied microbiology Vol.51. USA: Elsevier
Science.
Ratledge,C.(2004).Fatty acid bio synthesis in microorganisms being used for singl cell oil
production. Biochimie, 86, 807-815.
Ratledge,C.Boulton,C.A,“Fats andoils. In: Comprehensive biotechnology,”
hal.983-1003.
Ratledge,C.,Wilkinson,S.G.(1988). Microbial lipid Vol.4.London: Academic Press.
Ratledge,Colin,“Fatty acid biosynthesis in microorganisms being used for Single Cell Oil
production,” Elsevier Biochimie,vol.86(2004),hal.807–815.
Ratledge,C,“Microbial lipids: Commercial realities or academic curiosities,”
AOCSPress,(1982),hal.1-15.
Sari, Firna Indrianty. 2015. Pengaruh Konsentrasi Glukosa dan Suhu Inkubasi terhadap
Produksi Monounsaturated Fatty Acid (MUFA) dan Polyunsaturated fatty Acid (PUFA)
dari Aspergillus terreus.Depok: Universitas Indonesia.
Sartika, R. A.D. (2008). Pengaruh asam lemakjenuh, tidak jenuh danasam lemak trans
terhadap kesehatan. Jurnal Kesehatan Masyarakat Nasional.2(4):154-160.
Saxena, D.K. et al.2011.Comparative Extraction of Cottonseed Oil by n-Hexane and Ethanol.
India: ARPN Journal of Engineering and Applied Science.
Sivaramakrishnan, S., Dhanya Gangadharan, Kesavan Madhavan Namphoothiri, Carlos
Richardo Soccol, dan Ashok Pandey. (2007). Alpha amylase production by
Aspergillus oryzae employing solid state fermentation. Journal of Scientific &
Industrial Research Vol. 66, August 2007, pp. 621-626.
Sumanti, Debby M, Carmencita Tjahjadi, Marleen Herudiyanto, Tati Sukarti, “Mempelajari
Mekanisme Produksi Minyak Sel Tunggal dengan Sistem
FermentasiPadatpadaMediaOnggok-AmpasTahudenganMenggunakan Kapang
Aspergillus terreus.”Jurnal teknologi dan industri pangan, vol.XVI(2005), hal.51-61.
Sumanti, Debi M, dkk. 2003. Mempelajari Mekanisme Produksi Minyak Sel Tunggal Dengan
Sistem Fermentasi Padat Pada Media Onggok-Ampas Tahu Dengan Menggunakan
Kapang Aspergillus terreus. Bandung: Universitas Padjajaran.
Tung, Truong Quy, Naoyuki Miyata, dan Keisuke Iwahori. (2004). Growth of Aspergillus
oryzae during Treatment of Cassava Starch Processing Wastewater with High
Content of Suspended Solids. Journal of Bioscience and Bioengineering. Vol. 97, No.
5, 329-335. 2004
Wassef,M.K.(1975). Fungal Lipids. Advances in lipid research,15,159-232.
Wassef,M.K.Fungal Lipids.(NewYork:Adv.LipidRes.Vol.15.Academic Press,1975).
Yangmin Gong, Jiao Liu, Mulan Jiang, ZhuoLiang, HuJin, Xiaojia Hu, Xia Wan, Chuanjiong Hu,“Improvement of Omega-3 Docosa hexaenoic Acid Production by Marine
Dinoflagellate Crypthecodiniumcohnii Using Rapeseed Meal Hydrolysate and Waste
Molassesas Feedstock,”PLoS ONE,vol.10(2015),hal1-18
Zinjarde, Smita S, “Food-related applications of Yarrowia lipolytica,” Food Chemistry,