Seroprevalensi dan Isolasi
Toxoplasma gondii
pada Ayam Kampung di Bali
(SEROPREVALENCE AND ISOLATION OF TOXOPLASMA GONDII AMONG FREE-RANGE CHICKENS IN BALI)
I Made Dwinata1, Ida Bagus Made Oka1, Nyoman Adi Suratma1, I Made Damriyasa1
1Lab Parasitologi Veteriner, 2Lab Patologi Klinik
Fakultas Kedokteran Hewan Universitas Udayana Jln Sudirman Denpasar Bali, Telepon 03610223759
ABSTRAK
Prevalensi Toxoplasma gondii pada ayam kampung merupakan indikator yang baik adanya oosista
T.gondii di lingkungan dan daging ayam merupakan salah satu sumber penularan pada manusia. Penelitian ini bertujuan untuk menentukan prevalensi dan isolasi T.gondii pada ayam kampung di Bali. Jumlah sampel ayam yang digunakan sebanyak 125 ekor ayam kampung yang berasal dari delapan kabupaten di Bali. Antibodi terhadap T.gondii diperiksa dengan metoda Modified Aglutination Test (MAT). Pada ayam yang terdeteksi adanya antibodi terhadap T gondii diambil otak serta jantungnya kemudian dilakukan isolasi parasit dengan metoda pepsin-HCl digestion. Isolat parasit tersebut kemudian diinokulasikan secara peritoneal pada mencit untuk menentukan patogenitas parasit tersebut. Secara serologi terdeteksi adanya antibodi terhadap T. gondii pada 31 ekor ayam, dengan demikian seroprevalensi toxoplasmosis pada ayam kampung di Bali sebesar 24,8%, Uji digesti dan bioassay dapat diisolasi bradisoit 17 dari 31 (55%) ayam-ayam yang positif terdeteksi adanya antibodi terhadap T. gondii (MAT ≥1:5) uji patogenitasnya pada mencit menunjukkan bahwa isolat tersebut avirulen terhadap mencit.
Kata kunci : Toxoplasma gondii, Ayam kampung
ABSTRACT
The prevalence of Toxoplasma gondii in free range chickens is a good indicator of the prevalence of T. gondii oocysts in the environment and the meat of chicken is considered one of the sources of the human infection. A study to determine the seroprevalence of T.gondii in free ranging chickens in eight regency in Bali have been undertaken. More over, attempt to isolate T gondii was also performed from the copropositive sample. Seroprevalence was detected using modified agglutination test (MAT) and isolation of T.gondii were performed from organs (heart and brain) using pepsin-HCl digestion method. Further the pathogenicity of the isolate was determined by bioassay using mice. The result showed that the seroprevalence was 24.8% (31 out of 125 chickens examined). T.gondii was found in 17 of the 31 seropositive chickens (55%) more over all isolates were a vitulent to the mice.
Key word : Toxoplasma gondii, Ayam kampung PENDAHULUAN
Infeksi Toxoplasma gondii diketahui penyebarannya di seluruh dunia pada manusia dan hewan (Dubey dan Beattie, 1988). Manusia terinfeksi secara postnatal apabila menelan sista parasit yang terkandung pada daging yang
mentah atau kurang dimasak dengan sempurna, di samping itu dapat juga terinfeksi melalui makanan atau air yang tercemar oleh oosita T. gondii, atau dari lingkungan yang tercemar oleh oosita parasit tersebut. Bangsa kucing merupa-kan induk semang terpenting dari T. gondii karena hewan tersebut akan menyebarkan atau
mencemari lingkungan dengan oosita. Kucing terinfeksi akibat makan daging inang antara yang mengandung sista T. gondii. Diketahui burung serta rodensia seperti tikus merupakan sumber penularan penting toksoplasmosis terhadap kucing.
Hasil-hasil penelitian terhadap seropreva-lensi toksoplasmosis pada manusia di berbagai daerah di Indonesia telah dilaporkan, yaitu berkisar antara 3,1%-64,0% (Chomel et al., 1993; Uga et al., 1996). Hasil penelitian beberapa peneliti menampilkan bahwa kebiasaan makan sangat menentukan terjadinya infeksi parasit tersebut. Kebiasaan makan sate yang belum masak dengan sempurna (Gandahusada, 1980), kebiasaan makan lawar di Bali (Chomel et al., 1993) dan kebiasaan makan daging organ visceral ayam yang dimasak setengah matang (Asgari et al. 2006), mendorong terjadinya infeksi.
Toksoplasmosis dilaporkan menyerang hampir semua ternak termasuk unggas. Isolasi dan karakterisasi toksoplasma pada mamalia telah banyak dilakukan. Beberapa penelitian mengarah terhadap toksoplasmosis pada ayam kampung (Dubey et al.,2005a; Dubey et al., 2005b ) dan di Iran (Asgari et al., 2006) melaporkan seroprevalensi sebesar 36,1%. Mereka tertarik melakukan penelitian karena ayam kampung tersebut mempunyai kebiasaan mencari makan di tanah sangat cocok dipakai sebagai indikator kontaminasi toksoplasmosis pada lingkungan atau tanah. Belakangan ini telah diisolasi T. gondii pada unggas, antara lain di Mesir telah diisolasi T.gondii pada ayam dan itik (Dubey et al., 2003a), di Brasil pada ayam (Dubey et al., 2003b) serta di India pada ayam (Sreekumar et al., 2003). Di Indonesia sangat sedikit laporan penelitian tentang T. gondii, bahkan pada unggas belum banyak dilaporkan. Penelitian ini merupakan pendekatan penelaahan agen penyakit T. gondii pada ayam kampung sebagai salah satu inang antara. Sampai saat ini belum pernah diisolasi T. gondii pada unggas di Indonesia. Pemahaman keragaman T. gondii pada induk semang antara (ayam kampung) akan memperluas cakrawala pengendalian penyakit tersebut secara terpadu.
Penelitian ini bertujuan mengetahui seroprevalensi T. gondii pada ayam kampung di Bali, serta patogenitas isolat parasit tersebut pada mencit.
METODE PENELITIAN Pengambilan Sampel
Ayam yang dipakai sampel penelitian adalah ayam kampung yang berumur di atas enam bulan yang dipelihara secara ekstensif. Sampel berasal dari delapan kabupaten di Bali masing masing: kabupaten Badung, Gianyar, Tabanan, Bangli, Karangasem, Kelungkung, Negara, dan Buleleng. Dari masing masing kabupaten diambil sekitar 10-20 ekor ayam yang berasal dari peternak yang berbeda. Jumlah sampel keseluruhan adalah 125 ekor. Pengambilan sampel pada masing masing kabupaten dilakukan secara bertahap. Setiap kali pengambilan sampel hanya lima ekor ayam yang dikorbankan nyawanya. Terhadap sampel tersebut dilakukan pengambilan darah, otak, dan jantung.
Pemeriksaan Serologi
Darah yang diperoleh dilakukan pemisahan serum yang kemudian dilakukan pemeriksaan serologis untuk menentukan adanya antibodi terhadap T. gondiii. Pemeriksaan serologi menggunakan metoda Modified Aglutination Test (MAT).
Metode tersebut menggunakan 96 well microplate dengan dasar cekung, serum yang diperiksa diencerkan dengan 0,2 M 2-mercaptoethanol dalam phosphat buffer saline/ PBS. Masing masing well/sumuran diisi dengan 50 μl serum sampel yang diencerkan mulai pengenceran 1:5, di samping itu dua baris sumuran diisi 50 μl diisi dengan serum kontrol positif dan negatif dengan pengenceran yang sama dengan serum sampel. Setelah penambahan serum kemudian ditambahkan 50
μl suspensi antigen pada masing masing sumuran. Microplate kemudian digoyang pelan pelan supaya antara serum dan antigen tercampur dengan baik kemudian diinkubasi. Setelah inkubasi dilakukan pembacaan hasil dengan serum kontrol sebagai pembanding. Isolasi T. gondii
Sebanyak 50 gram untuk masing masing jaringan digerus dengan blender dengan kecepatan rendah, kemudian ditambah PBS dan digerus lagi dengan kecepatan tinggi. Hasil gerusan tersebut kemudian ditambahkan larutan pepsin HCl (Dubey, 1998), setelah diinkubasi pada suhu kamar dan diputar dengan magnetic stirer selama satu jam homogenat dicuci tiga kali dengan PBS (mengandung 10
unit potassium-G penisilin dan 100 mg streptomisin dalam 100 ml). Untuk memisah-kan pepsin-HCl dilakumemisah-kan pemusingan pada 2000 rpm selama 10 menit. Supernatan dibuang dan sedimen ditambahkan PBS sampai 100 ml. Suspensi tersebut kemudian diperiksa di bawah mikroskop untuk menentukan adanya bradisoit. Bioassay pada Mencit
Suspensi dari hasil pemeriksaan metode digesti yang mengandung bradisoit T. gondii kemudian diinokulasikan pada mencit (enam mencit untuk tiap sampel positif). Sebanyak 0,5 ml suspensi yang mengandung bradisoit T. gondii diinokulasikan pada mencit secara peritoneal. Mencit diamati sampai hari ke 30 setelah infeksi. Mencit yang mati selama pengamatan dilakukan pemeriksaan eksudat dari peritoneum dan otak untuk menentukan adanya parasit T. gondii. Mencit yang bertahan hidup sampai hari ke 30 dikorbankan nyawanya dengan cara eutanasi menggunakan eter untuk isolasi T. gondii pada otak dan cairan peritoneum. Untuk menentukan patogenitas dari isolat yang didapat dilakukan dengan menghitung lethal dose (LD) 50 dan infectious dose (ID) 50 berdasarkan metode Reed dan Muench.
HASIL DAN PEMBAHASAN
Dari 125 ekor ayam kampung yang diteliti, antibodi terhadap T. gondii ditemukan pada 31 ekor. Hasil penelitian ini menunjukan seroprevalensi toksoplasmosis pada ayam kampung di Bali sebesar 24,8%. Penelitian ini pertama kali dilakukan di Bali untuk mendeteksi keberadaan toksoplasmosis pada unggas. Dibandingkan dengan seroprevalensi Toksoplasmosis pada hewan lain yang pernah diteliti di Bali, menunjukkan seroprevalensi toksoplasmosis pada ayam kampung di Bali lebih rendah bila dibandingkan dengan seroprevalensi pada babi (32%) yang pernah
dilaporkan oleh Damriyasa et al., (2001). Bila dibandingkan dengan seroprevalensi yang pernah dilaporkan oleh Dubey et al., (2008) dari Muntilan Jawa Tengah, ditemukan 24 dari 94 ayam kampung positif mengandung antibodi terhadap T. gondii dengan metode MAT. Hasil penelitian tersebut tidak jauh berbeda dengan hasil yang diperoleh pada penelitian ini. Laporan dari beberapa negara juga menunjukkan bahwa seroprevalensi toksoplasmosis bervariasi antara 18-40% yang pernah dilaporkan di India (Sreekumar et al., 2003) dan Columbia (Dubey et al., 2005). Tenter et al., 2000 melaporkan banyak faktor berpengaruh terhadap penularan toksoplasmosis seperti managemen dan standar higiene peternakan, kepadatan kucing dan kondisi lingkungan.
Titer antibodi dari ayam yang positif mengandung antibodi terhadap T. gondii bervariasi antara 1:5 sampai 1: 320, seperti disajikan pada Tabel 1.
Pada penelitian ini, uji serologi dengan MAT dimulai dengan titer yang berpengenceran rendah (1:5). Hal tersebut dilakukan karena T. gondii pernah diisolasi oleh Dubey et al., (2005) pada ayam yang mempunyai titer antibodi yang rendah. Otak dan jantung ayam yang terbukti positif mengandung antibodi terhadap T. gondii setelah dilakukan metode digesti dan selanjutnya diinokulasikan pada mencit, setelah 30 hari pascainokulasi ditemukan adanya bradisoit parasit tersebut di otak mencit yang berasal dari 17 ekor ayam. Hasil penelitian ini menunjukkan bahwa dari 31 ekor yang terdeteksi antibodi terhadap T. gondii hanya pada 17 (55%) ekor ayam dapat diisolasi T. gondii melalui inokulasi otak dan jantung ayam pada mencit. Selanjutnya hasil uji kedua metode tersebut disajikan pada Tabel 2.
Hasil yang ditunjukkan pada Tabel 2 membuktikan bahwa hampir sebagian dari ayam yang positif mengandung antibodi terhadap T. gondii, dapat diisolasi parasit tersebut melalui uji bioassay.
Tabel 1. Sebaran titer antibodi terhadap T. gondii pada ayam Titer
1:5 1:10 1: 20 1:40 1:80 1:160 1 : 320
Jumlah 7 5 3 3 7 3 3
mengarah toksoplasmosis. Hasil penelitian ini menunjukkan bahwa isolat T. gondii yang diisolasi dari ayam kampung di Bali bersifat avirulen terhadap mencit. Hasil penelitian yang sama juga dilaporkan oleh Dubey et al., (2008) yang mengemukakan bahwa isolat T. gondii yang diisolasi dari Ghana, Indonesia, Italia, Polandia, dan Vietnam bersifat avirulen terhadap mencit.
SIMPULAN
Seroprevalensi infeksi T. gondii pada ayam kampung di Bali sebesar 24,8% dan sebagian dari sampel yang positif mengandung antibodi terhadap T. gondii dapat di isolasi. Isolat T. gondii yang diisolasi dari ayam kampung di Bali bersifat avirulen terhadap mencit.
SARAN
Dari hasil penelitian ini perlu adanya penelitian secara nasional tentang prevalensi infeksi T. gondii dari berbagai hewan dan manusia di Indonesia. Adanya kajian lebih mendalam tentang kemungkinan ayam kampung sebagai sumber penularan T. gondii pada manusia.
Tabel 2. Hasil pemeriksaan serologi (MAT) dan bioassay T. gondii pada ayam MAT Total Positip negatip Positip 17 0 17 Bioassay Negatip 14 94 108 Total 31 94 125
Keterangan : MAT = Modified Aglutonation Test.
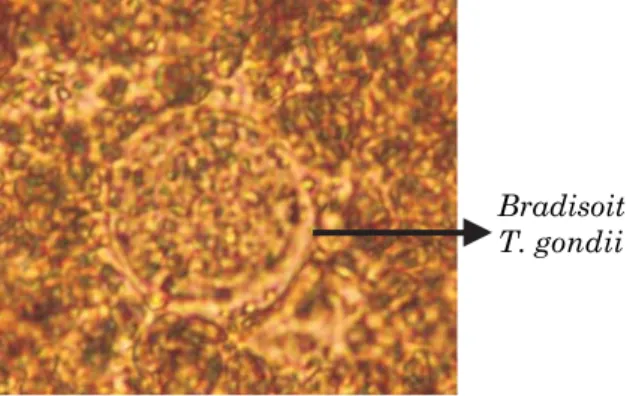
Bradisoit T. gondii
Gambar. Siste Toxoplasma gondii pada organ ayam dan mencit (400 kali)
Tabel 3.Hasil pemeriksaan bioassay terhadap T. gondii dan hubungannya dengan titer antibodi pada pemeriksaan Modified Aglutination Test (MAT)
Titer
1:2 1:5 1:10 1:20 1:40 1:80 1:160 1:320
Bio-assay positif 0 0 0 2 3 6 3 3
negatif 1 7 5 1 0 1 0 0
Total 1 7 5 3 3 7 3 3
Hal tersebut dapat disebabkan oleh pengaruh perlakuan pada saat proses digesti dengan pepsin HCl, dalam proses tersebut kemungkinan terjadi kerusakan-kerusakan pada parasit tersebut sehingga tidak berkembang setelah diinokulasikan pada mencit. Faktor lain yang dapat menyebabkan hal tersebut adalah terjadinya autolisis dari jaringan selama penyimpanan sebelum dilakukan inokulasi pada mencit. Berdasarkan data titer antibodi dan hasil bioassay menunjukkan bahwa uji bioassay positif pada ayam yang menunjukkan titer antibodi 1:20 ke atas, hasil ini selengkapnya disajikan pada Tabel 3.
Dari 14 sampel yang positif dengan pemeriksaan MAT, pada bioassay hasilnya negatif, 13 dari sampel tersebut memiliki titer di bawah 1:20, sehingga dapat disimpulkan sampel yang negatif pada uji bioassay memiliki titer di bawah 1:20. Hal tersebut senada dengan pernyataan Dubey et al., (2008), yang mengemukakan bahwa umumnya titer di bawah 1:25 merupakan hasil reaksi non spesifik. Sehingga untuk uji tapis/screening disarankan dimulai dengan titer 1:20 atau 1:25.
Dari 31 sampel yang diinokulasikan pada mencit melalui uji bioassay untuk mengetahui patogenitas dari isolat tersebut, sampai hari ke 30 tidak ada mencit yang mati atau
UCAPAN TERIMAKASIH
Penulis mengucapkan terimakasih kepada Direktorat Jendral Pendidikan Tinggi, Departemen Pendidikan Nasional , Sesuai dengan surat Perjanjian Pelaksanaan Hibah Penelitian Nomor 027/SP2H/PP/DP2M/III/2008 l atas dana yang diberikan sehingga terlaksa-nanya penelitian ini.
DAFTAR PUSTAKA
Asgari Q, Farzaneh A, Kalantari M, Akrami Mohajeri F, Moazeni M, Zarifi M, Esmaeilzadeh B , Motazedian MH . 2006. Seroprevalence of Free-Ranging Chicken Toxoplasmosis in Sub-Urban Regions of Shiraz, Iran. International Journal of Poultry Science.262-264.
Chomel BB, Karsten R, Adam C, Lambilotte C,Theis J, Goldsmith R, Koss J, Chioino C, Widjana DP , Sutisna P .1993. Serosurvey of some major zoonotic infections in children and teenagers in Bali, Indonesia. Sutheast Asian J Trop Med Public Health 24: 321-326
Damriyasa IM, Edelhofer R, Volmer R, Bauer C, Zahner H. 2001. Current seroprevalence of Toxoplasma gondii infections in sows in two regions of Germany. Abstr. Proceeding 18th Intern. Conf. WAAVP, Stresa/Italy. A2p, .8
Dubey JP. 1986. A riview of Toxoplasmosis in pigs. Vet. Paras. 19: 181-223.
Dubey JP, Beattie CP. 1988. Toxoplasmosis of animals and man. Boca Raton, FL: CRC Press.
Dubey JP. 1998. Refinement of pepsin digestion method for isolation of Toxoplasma gondii from infected tissue. Veterinary Parasitology 74, 75-77
Dubey, JP, Graham DH, Dahl E, Hilali M, El-Ghaysh A, Sreekumar C, Kwok OCH, Shen
SK, Lehman T. 2003a. Isolation and molecular characterization of Toxoplasma gondii from Chickens and ducks from Egypt. Vet. Parasitol. 114, 89-95.
Dubey JP, Navaro I T, Graham DH, Dahl E , Hilali M , Freire LB, Prudencio LB, Sreekumar C, Vianna MCB, Lehman T. 2003b. Characterization of Toxoplasma gondii isolates from free range chickens from Parana, Brazil. Vet. Parasitol. 117, 229-234. Dubey JP, Gomez-Marin JE, Bedoya A, Fabiana Lora MCB, Viaanna D Hi, Kwok OCH, Shen SK, Marcet PL, Lehmann T. 2005. Genetic and Biologic Characteristics of Toxoplasma gondii Isolates in Free –range Chickens from Columbia, South Amerika. Vet. Parasitology 134. 67-72
Dubey JP, Edelhoper R, Marcet P, Vianna MCB, Kwok OCH, Lehmann T. 2005. Genetic and Biologic Characteristics of Toxoplasma gondii Infections in Free-range Chickens from Austria. Vet. Parasitology 133. 299-306
Dubey JP, Lam Thi Thu Huong, Lowson BWL, Subekti DT, Tassi P, Cabaj W, Sundar N, Velmurugan GV, Kwok OCH, Su C. 2008. Seroprevalence and isolation of Toxoplasma gondii from free-range chicken in Ghana, Indonesia, Italy, Poland and Vietnam. J. Parasitol. 94. Pp 68-71
Gandahusada S, Endardjo S .1980. Toxoplasma antibodies in Obano, Irian Jaya, Indonesia. Sutheast Asian J Trop Med Public Health. 11: 276-279
Sreekumar C, Graham DH, Dahl E, Hilali M, Freire LB, Prudencio LB, Vianna MCB, Lehman T, Dubey JP. 2003. Genotyping of Toxoplasma gondii isolates from chickens from India. Vet. Parasitol. 118, 187-194 Tenter AM, Heckeroth AR, Weiss LM . 2000.
Toxoplasma gondii: From animal to human. Inter. J.for Parasitol., 30: 1217-5
Uga S, Ono K, Kataoka N, Hasan H. 1996. Seroepidemiologi of five major zoonotikc parasite infections in inhabitants of Sidoarjo, East Java, Indonesia. Sutheast Asian J Trop Med Public Health 27: 556-561