BAB II
TINJAUAN PUSTAKA 2.1 Air
Air merupakan salah satu dari ketiga komponen yang membentuk bumi (zat
padat, air, atmosfer). Bumi dilingkupi air sebanyak 70% sedangkan sisanya 30%
berupa daratan (dilihat dari permukaan bumi). Udara mengandung uap air
sebanyak 15% di dalam atmosfer (Gabriel, 2001).
Air memegang peranan penting dalam suatu komunitas, karena penyediaan
air merupakan suatu persyaratan penting bagi terbentuknya suatu komunitas yang
permanen. Air murni adalah berupa zat cair yang tidak mempunyai rasa, warna
dan bau yang terdiri dari atom hidrogen dan unsur oksigen dengan rumus kimia
H2O. Air bersih adalah salah satu jenis sumber daya berbasis air yang bermutu
baik dan biasa dimanfaatkan oleh manusia untuk dikonsumsi atau dalam
melakukan aktivitas mereka sehari-hari (Linsley, 1986).
Air sangat penting bagi kehidupan manusia dan fungsinya tidak dapat
digantikan dengan senyawa lain. Sesuai fungsinya, air digunakan untuk berbagai
keperluan seperti : untuk diminum, untuk sanitasi dan air untuk transportasi baik
di sungai maupun laut (Linsley, 1986).
Seiring dengan bertambahnya jumlah penduduk dan semakin meningkatnya
kesadaran akan kesehatan lingkungan, maka kebutuhan ini tidak diimbangi
dengan meningkatnya ketersediaan air bersih yang cenderung menurun, terutama
kualitas air yang memburuk. Oleh karena itu diperlukan suatu proses pengolahan
2.2 Jenis-Jenis Air Menurut Farmakope
a. Aqua Demineralisata
Aqua Demineralisata adalah air yang telah dihilangkan kation dan
anionnya (FI ed III, 1979).
b. Aqua Destillata
Aqua Destillata adalah air hasil penyulingan tidak sama dengan air
mineral, bahkan tidak ada kandungan mineralnya ( FI ed III, 1979).
c. Aqua Pro Injections
Aqua Pro Injections adalah air suling segar yang disuling kembali,
disterilkan dengan cara sterilisasi A atau C ( FI ed III, 1979).
d. Aqua Aromatika
Aqua aromatika adalah larutan jenuh minyak atsiri atau zat-zat yang
beraroma dalam air. Air aromatika harus mempunyai rasa yang menyerupai bahan
asal, bebas bau, tidak berwarna dan tidak berlendir ( FI ed III, 1979).
e. Aqua Purificata (Air Murni)
Air murni adalah air yang dimurnikan dengan proses destilasi, perlakuan
dengan menggunakan penukar ion, osmosis balik, atau proses lain yang sesuai.
Dibuat dari air yang memenuhi persyaratan air minum. Tidak mengandung zat
f. Aqua Sterile Pro Injectione (Air Steril Untuk Injeksi)
Air steril untuk injeksi adalah air untuk injeksi yang disterilkan disebut
juga aqua bidestilata dan dikemas dengan cara yang sesuai. Tidak mengandung
bahan anti mikroba atau bahan tambahan lainnya ( FI ed IV, 1995)
2.3 Sumber-Sumber Air
Kita ketahui bahwa sumber air merupakan komponen penting untuk
penyediaan air bersih karena tanpa sumber air maka suatu system penyediaan air
bersih tidak akan berfungsi. Berikut adalah 5 macam sumber air yang dapat
digunakan :
2.3.1 Air Laut
Air ini rasanya asin karena mengandung garam NaCl. Kadar garam NaCl
dalam air laut 3% dengan keadaan ini maka air laut tidak memenuhi syarat untuk
diminum (Sutrisno, 2004)
2.3.2 Air Hujan
Cara menjadikan air hujan sebagai air minum hendaknya jangan saat air
hujan baru mulai turun karena masih mengandung banyak kotoran. Air hujan juga
mempunyai sifat agresif terutama terhadapa pipa-pipa penyalur maupun bak-bak
reservoir sehingga hal ini akan mempercepat terjadinya korosi atau karatan
2.3.3 Air Permukaan
Air permukaan adalah air yang mengalir di permukaan bumi. Pada
umumnya air permukaan ini akan mendapat pengotoran selama pengalirannya,
misalnya oleh lumpur, batang kayu, daun, kotoran industry dan lainnya. Untuk
meminumnya harus melewati proses pembersihan yang sempurna (Sutrisno,
2004).
2.3.4 Air Tanah
Air tanah adalah air yang berada di bawah tanah di dalam zona jenhu
dimana tekanan hidrostatiknya sama atau lebih besar dari tekanab atmosfer
(Sutrisno, 2004)
2.3.5 Mata Air
Mata air adalah air tanah yang keluar dengan sendirinya ke permukaan
Atanah dengan hamper tidak dipengaruhi oleh musim, sedangkan kualitasnya
sama dengan air dalam (Sutrisno, 2004)
2.4 Pencemaran Air
2.4.1 Komponen Pencemaran Air
Meskipun rumus kimia air murni di lingkungan laboratorium adalah H2O
namun kenyataannya di alam, rumus tersebut seolah-olah berubah menjadi H2O +
X. Dalam hal ini, X merupakan komponen-komponen yang masuk atau
dimasukkan ke dalam badan air sehingga menyebabkan perairan menurun
berupa komponen non-biologis dan komponen biologis. Komponen non-biologis
dapat berupa pupuk/nitrogen tanaman, sampah/padatan, minyak, bahan radioaktif,
senyawa anorganik dan mineral, termasuk logam-logam berat serat komponen
anorganik sintetik seperti residu pestisida dan deterjen. Komponen biologis dapat
berupa mikroba, khususnya mikroba yang bersifat merugikan manusia dan
makhluk hidup lainnya, seperti bakteri pathogen dan bakteri pencemar (Nugroho,
2006)
2.4.2 Dampak Pencemaran Air
Pencemaran air dapat menyebabkan berkurangnya keanekaragaman atau
punahnya populasi 17athogen perairan seperti benthos, perifiton, dan plankton.
Dengan menurunnya atau punahnya 17athogen tersebut maka 17athog ekologis
perairan dapat terganggu. Apabila beban pencemaran melebihi daya dukung
lingkungannya maka kemampuan itu tidak dapat dipergunakan lagi (Nugroho,
2006)
2.5Air Minum
Air minum adalah air yang melalui proses pengolahan atau tanpa proses
pengolahan yang memenuhi syarat kesehatan dan dapat langsung diminum. Hal
inilah yang secara prinsip membedakan kualitas yang harus dimiliki antar air
bersih dan air minum. Kualitas air minum setingkat lebih tinggi daripada kualitas
air bersih ditinjau dari beberapa komponen pendukungnya. Agar air dapat
dikategorikan sebagai air minum maka dipersyaratkan harus memenuhi ketentuan
416/MENKES/PER/IX/2002, yang merupakan Standar Nasional Indonesia (SNI)
air minum (Depkes, 2010).
Dari pernyataan tersebut dapat dikatakan bahwa air bersih belum tentu dapat
diminum, karena air bersih belum tentu memenuhi 18athogen air minum yang
sehat, sedangkan air minum merupakan air yang bersih dan kualitasnya setingkat
lebih tinggi dibandingkan dengan air bersih, air minum harus sesuai dengan
parameternya yaitu parameter fisis, kimiawi, biologis maupun radiologis (Depkes,
2010).
2.5.1 Parameter Kualitas Air Minum
• Kualitas fisik yang meliputi kekeruhan, 18athogen1818e, warna, 18athoge
rasa. Kekeruhan air dapat ditimbulkan oleh adanya bahan-bahan 18athoge dan
anorganik yang terkandung di dalam air seperti lumpur dan bahan-bahan yang
berasal dari buangan. Dari segi estetika, kekeruhan di dalam air dihubungkan
dengan kemungkinan pencemaran oleh air buangan.
• Kualitas kimia yang berhubungan dengan ion-ion senyawa ataupun logam
yang membahayakan, di samping residu dari senyawa lainnya yang bersifat
racun, seperti antara lain residu pestisida. Dengan adanya senyawa-senyawa
ini kemungkinan besar bau, rasa dan warna air akan berubah, seperti yang
umum disebabkan oleh adanya perubahan pH air. Pada saat ini kelompok
logam berat seperti Hg, Ag, Pb, Cu, Zn, tidak diharapkan kehadirannya di
dalam air.
• Kualitas biologis, berhubungan dengan kehadiran mikroba 18athogen
coli) dan penghasil toksi
patogen-patogen sebagaimana analisis air mengacu pada kehadiran
mikroorganisme dalam air minum membuktikan air tersebut tercemar bahan
tinja dari manusia/hewan berdarah panas atau hasil pembusukan materi
19athoge. Hal ini berpeluang bagi mikroorganisme 19athogen, secara berkala
terdapat dalam saluran pencernaan, untuk masuk dalam air minum. Jumlahnya
lebih banyak daripada pathogen pathogen (hal ini menyebabkan lebih mudah
terdeteksi), dan. Dalam lingkungan yang dinamis, analisis biologi dapat
memberikan gambaran yang jelastentang kualitas perairan (Ardi, 2002).
2.6Water Treatment
Proses-proses utama dilakukan oleh pabrik pengolahan air yaitu pemisahan
padatan dan menghilangkan kuman. Bahan-bahan yang tidak dapat larut dapat
digolongkan menurut ukurannya dan ini mempengaruhi metoda-metoda
perawatan yang digunakan. Padatan-padatan yang besar bias terjadi secara alami,
seperti pasir, kerikil dan reruntuhan alami yang besar (daun-daun, tongkat-tongkat
dll) atau bias juga puing-puing. Partikel-partikel yang besar dapat dihilangkan
dengan cara yang sederhana atau menyaring. Bahan-bahan lebih kecil yang tidak
bias dilarutkan sebagai contoh, partikel-partikel tanah liat atau senyawa-senyawa
organic yang tidak bias dilarutkan menunjukkan suatu maslah yang penting yang
dapat member warna atau kekeruhan atau kedua-duanya kedalam air dan dapat
melindungi pathogen-patogen dari obat desinfeksi. Partikel-partikel kecil ini,
dikenal sebagai koloid-koloid. Bahan-bahan tidak larut ini berikatan satu sama
penggumpal kimia di dalam air yang mempercepat pembentukan gumpalan yang
besar dan dapat menangkap partikel-partikel yang kecil dan dapat dihilangkan
dengan pengendapan.
Beberapa bahan-bahan yang dapat larut didalam air dengan demikian akan
sedikit mempengaruhi koagulasi, proses-proses pengendapan dan filtasi.
Bahan-bahan yang dapat larut berupa organic atau anorganik, bagaimanapun grup utama
pada jenis yang dapat larut ialah anorganik. Raw water dipilih atau ditentukan
dengan mengandung konsentrasi yang rendah senyawa organik yang dapat larut
dan proses-proses treatment spesifik digunakan jika perlu untuk menghilangkan
senyawa yang dapat larut sebagai contoh superklorinasi untuk menghilangkan
senyawa rasa dan bau.
2.7Alkalinitas
Alkalinitas adalah pengukuran kapasitas air untuk mentralkan asam-asam
lemah, meskipun asam lemah atau basa lemah juga dapat sebagai penyebabnya.
Peyusun alkalinitas perairan adalah anion bikarbonat (HCO3), karbonat (CO3) dan
hidroksida (OH-). Garam dari asam lemah lain seperti: Borat (H2BO3), silikat
(HSiO3), fosfat (HPO42- dan H2PO4-), sulfida (HS-) dan ammonia (NH3) juga
membrikan kontribusi terhadap alkalinitas dalam jumlah sedikit (Santika, 1984).
Meskipun banyak komponen penyebab alkalinitas perairan, penyebab utama
dari alkalinitas tersebut adalah hidroksida, karbonat dan bikarbonat. Pada keadaan
tertentu (siang hari) adanya ganggang dan lumut air dapat menyebabkan turunnya
2.7.1 Peranan Alkalinitas
Alkalinitas berperan dalam hal-hal sebagai berikut:
a. Sistem Penyangga
Bikarbonat yang terdapat pada perairan dengan nilai alkalinitas total tinggi
berperan sebagai penyangga perairan terhadap perubahan pH yang drastis.
Jika asam ditambahkan kedalam perairan maka asam tersebut akan
digunakan untuk mengonversi karbonat menjadi bikarbonat dan
bikarbonat menjadi asam karbonat. Hal ini dapat menjadikan perairan
perairan dengan nilai alkalinitas total tinggi tidak mengalami perubahan
pH secaradrastis (Cole, 1988).
b. Bahan kimia yang digunakan dalam proses koagulasi air atau limbah
bereaksi dengan air membentuk endapan hidroksida yang tidak larut. Ion
hydrogen yang dilepaskan bereaksi dengan ion-ion penyusun alkalinitas,
sehingga alkalinitas berperan sebagai penyangga untuk mengetahui kisaran
pH yang optimum bagi penggunaan koagulan. Dalam hal ini nilai
alkalinitas sebaiknya berada pada kisaran optimumuntuk mengikat ion
hydrogen yang dilepaskan pada proses koagulasi (Cole, 1988).
c. Pelunakan air
Alkalinitas adalah paremeter kualitas air yang harus dipertimbangkan
dalam menentukan jumlah soda abu dan kapur yang diperlukan dalam
proses pelunakan dengan metode pengendapan. Pelunakan air yang
bertujuan untuk menurunkan kesadahan (Cole, 1988).
Alkalinitas merupakan parameter yang sangit penting penting termasuk
didalam pengendalian korosi. Hal itu harus diketahui disamping itu untuk
pengelompokan dala Lengelier Saturasi Indeks (Cole, 1988).
e. Limbah Industri
Banyak para agen yang mencegah pengecekan campuran limbah yang
disebabkan (hidroksida) alkalinitas untuk penerimaan air. Sebaiknya pH
alkalinitas ialah suatu factor yang penting didalam penentuan kemampuan
dari limbah untuk pengolahan secara biologi (Cole, 1988).
2.7.2 Metode Titrasi
2.7.2.1Metode Titrasi Volumetri
Alkalinitas dapat diukur dengan titrasi volumetric dengan H2SO4 didalam
satuan CaCO3 dengan menggunakan indicator warna. Dimana untuk sampel
dengan pH diatas 8,3 titrasi dilakukan dalam dua tahap. Pada tahap pertama titrasi
sampai pH 8,2 dengan phenolphthalein sebagai indicator yang ditunjukkan dari
perubahan warna merah menjadi tidak berwarna. Setelah itu titrasi dilanjutkan
dengan penambahan indicator metal orange sampai pH 4,5 (larutan menjadi tidak
berwarna). Untuk sampel yang pH nya kurang dari 8,3 hanya dilakukan titrasi satu
tahap dengan metal orange sebagai indicator sampai pH 4,5 (warna berubah dari
kuning jadi merah) (Sawyer, 1998).
Pemilihan pH 8,3 sebagai titik akhir titrasi tahap pertama ialah
berdasarkan pada titrasi alkalimetri. Nilai pH 8,3 ini untuk titrasi karbonat
menjadi bikarbonat :
Penggunaan pH 4,5 untuk titik akhir titrasi pada tahap kedua dari titrasi
sesuai dengan perkiraan untuk titik keseimbangan untuk konversi dari ion
bikarbonat menjadi asam karbonat :
HCO3- + H+ H2CO3
Dalam hal ini pada titik akhir titrasi akan tergantung pada awal konsentrasi ion
bikarbonat didalam sampel tersebut. Penggunaan ini dapat dirumuskan sebagai
berikut:
pH (bikarbonat) = 3,2 - ½ log [HCO3]
dimana HCO3- 0,01 M sesuai dengan alkalinitas 500 mg/l CaCO3 sebagai titik
kesetimbangan. Dalam hal ini asam karbonat atau karbon dioksida yang dibentuk
dari bikarbonat tidak akan hilang selama titrasi ini berlangsung (Sawyer, 1998).
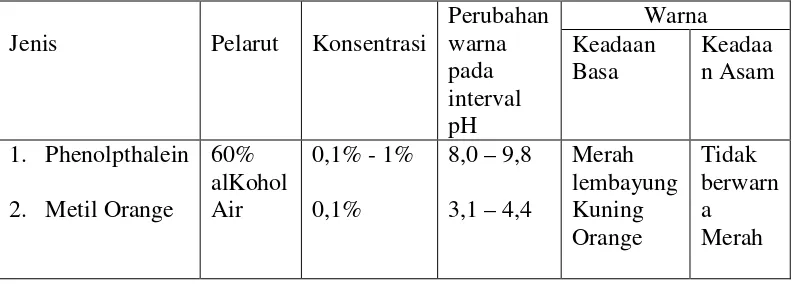
Pemilihan indikator yang sesuai:
Indikator adalah suatu zat yang warnanya berbeda-beda sesuai dengan
konsentrasi ion-hidrogen. Jika asam kuat dititrasi maka perubahan yang besar
dalam pH pada titik ekivalen cukup untuk menjangkau indicator metal orange (3,1
– 4,4) dan phenolphthalein (8,0 – 9,8)
Tabel 2.7.2.1. Indikator Untuk Titrasi Alkalinitas
Jenis Pelarut Konsentrasi
2.7.2.2Metode Potensiometri
Metode potensiometri ini menggunakan pH meter dimana dalam
mengukur pH sampel memakai elektroda yang bersih. pH meter adalah suatu
voltmeter elektronik dengan resistans input yang tinggi. (Resistans iut pH meter
yang baik adalah daerah 1012 – 1013 Ω). Baik instrument yang memakai katup
maupun memakai transitor banyak dipakai. Alat–alat ini umumnya menggunakan
listrik dari jaringan pusat (110 atau 220 V) dan mengandung rangkaian penyedia
tenaga (power supplay) sendiri berikut sebuah penyearah arus (rectifier)
(Letterman, 1999).
Instrument-instrument yang lebih kurang mengandung sebuah pengganda
(amplifier) differensial, instrument-instrument yang lebih mahal mengubah isyarat
arus searah yang digandakan dan komponen arussearah disaring dan akhirnya
isyarat yang telah digandakan diperlihatkan di atas suatu meteran yang telah
dikalibrasi dalam satuan pH (dan dalam kebanyakan kasus, juga dalam millivolt).
Jenis ketiga dari pH meter elektronik juga dikenal pada instrument mutar sebuah
potensiometer sampai sebuah galvanometer dan rangkaian potensiometer. Pada
instrument-instrumen demikian pH dibaca dari posisi tombol potensiometer
(Letterman, 1999).
Untuk titrasi dilakukan dengan asam sulfat dan pada setiap ± 0,5 ml
penambahan asam sulfat kedalam sampel secara perlahan diaduk untuk
memberikan waktu yang cukup bagi kesetimbangan elektroda. Nilai pH hasil
titrasi dibaca setelah setiap penambahan H2SO4 tersebut, atau dilakukan dengan
dan volume titran yang ditambah harus sekecil mungkin. Titrasi selesai sampai
titik lengkungan yang keduanya terlihat jelas (Santika, 1984)
Pada pengukuran pH yang secara nyata untuk mengetahui titik akhir titrasi
yang setimbang didalam penentuan alkalinitas dapat jadi semakin baik dengan
menggunakan titrasi elektrometris. Pada dasarnya kenyataannya yang paling
penting didalam air alami dimana total alkalinitas ialah suatu tambahan dari reaksi
penyebab dari garam asam lemah dengan bikarbonatnya saja. Didalam “standar
metode” hanya memegang untuk kemurnian yang diutamakan dalam larutan dan
tidak harus sesuai dengan pengelompokan untuk limbah industry atau peristiwa
air alami. Titik akhir titrasi ini ditentukan oleh:
1. Jenis indikator yang dipilih dimana warnanya berubah-ubah pada titik akhir
titrasi.
2. Perubahan nilai pH pada pH meter waktu titrasi asam – basa memperlihatkan
titik akhir titrasi/ekivalen (Santika, 1984).
2.7.3 Gangguan pada Analisa Alkalinitas
Gangguan yang dapat terjadi pada saat analisa alkalinitas serta
pencegahannya yaitu :
1. Sabun (detergen) dan Lumpur dapat mempengaruhi elektroda dan
memperlambat respon pH meter. Usahakan titrasi dilakukan dengan
perlahan untuk memberikan waktu yang cukup bagi keseimbangan pH
elektroda.
2. Amoniak, jangan dihilangkan tetapi ikut dianalisa karena merupakan
3. Karbondioksida akan mempengaruhi alkalinitas suatu sampel yang
terbuka terhadap udara. Hal ini dapat diatasi dengan melakukan
pengocokan, pengadukan dan penyaringan.
4. Pengenceran sampel tidak diperbolehkan karena air pengenceran
mempunyai alkalinitas yang berbeda.
5. Pemanasan sampel tidak diperbolehkan karena mengurangi
karbondioksida terlarut, sehingga alkalinitas berkurang pula (Santika,