LAPORAN PRAKTIKUM
KIMIA DASAR
Acara : II
Penyaringan dan Titrasi
Disusun oleh : Nama : Yunisha Febriani No. Mhs : 140801460
Hari/Tanggal : ………. Asisten : ………...……….
LABORATORIUM TEKNOBIO PANGAN
FAKULTAS TEKNOBIOLOGI
PENGESAHAN
Acara : ……
……….. ……….. ………..
Disusun oleh :
Nama
: ………...
No. Mhs
: ………...
Hari/Tanggal
: ………...
Asisten
: …………...
Pada tanggal ...
Disahkan oleh :
Asisten praktikum
KREDIT NILAI LAPORAN
III HASIL DAN PEMBAHASAN 50
I. PENDAHULUAN
A. Judul
A.1 Penyaringan A.2 Titrasi
B. Tujuan
B.1 Melatihcara menggunakan kertas saring untuk menyaring endapan hasil reaksi kimia.
B.2 Mengamati warna, bau, dan endapan yang terbentuk dari hasil penyaringan.
II. METODE
warna, bau, dan endapannya.Kertas saring dilipat menjadi ¼ lingkaran.Setelah itu, corong dibasahi dengan aquades dan kertas saring yang telah dilipat dimasukkan ke dalam corong.Cairan hasil pengenceran sebelumnya dituangkan ke dalam corong, kemudian, diaduk dengan gelas pengaduk.Setelah selesai, diamati perubahan warna, bau, dan endapannya.
B.2 Cara Kerja Titrasi
III. HASIL DAN PEMBAHASAN
Bau +++ (pekat sekali) + (kurang pekat)
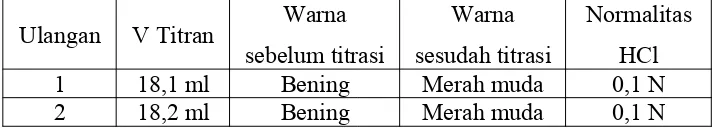
Endapan Ada Tidak 1 18,1 ml Bening Merah muda 0,1 N 2 18,2 ml Bening Merah muda 0,1 N
B. Pembahasan
B.1 Penyaringan
ukuran partikel zat-zat penyusunnya berbeda. Pori-pori alat penyaringan yang digunakan harus berukuran diantara zat-zat yang akan dipisahkan.
Kertas saring mempunyai pori-pori (lubang kecil) yang masih dapat dilalui oleh partikel-partikel air, tetapi tidak dapat dilewati oleh partikel kristal pasir. Kertas saring, berperan seperti ayakan. Air dapat melewati kertas saring karena ukuran partikelnya lebih kecil daripada pori-pori kertas saring, sedangkan pasir tertahan karena ukuran partikelnya lebih besar dari pada pori kertas saring (Fibrianto, 2008).
Sebelum penyaringan, dapat dilihat warna campuran larutan Pb asetat dan H2SO4 0,1N menjadi warna putih keruh dan berbau
menyengat (pekat sekali) dan terdapat endapan di dasar gelas beker.Dan setelah dilakukan penyaringan, dapat dilihat warna larutan berubah menjadi bening (tidak berwarna), dan baunya pun sudah tidak semenyengat (kurang pekat) seperti sebelum di saring.Dan terlihat terdapat endapan yang tadi mengendap tersaring di kertas saring.
Pencampuran antara Pb asetat dan H2SO4 encer akan
menghasilkan reasksi sebagai berikut :
Pb(CH3COOH)2 + H2SO4 PbSO4 + CH3COOH
Reaksi tersebut ternyata menghasilkan produk berupa PbSO4
(timbal sulfat) dan CH3COOH (asam asetat).Dan pada akhirnya
terjadilah endapan PbSO4 pada dasar gelas beker, dan CH3COOH yang
menyebabkan campuran larutan tersebut berbau menyengat (seperti cuka).Sebelum proses penyaringan, larutan berwarna putih keruh dan setelah disaring berwarna bening. Hal ini disebabkan karena proses penyaringan menghasilkan endapan PbSO4 yang tertahan di kertas
saring, sementara larutannya akan melewati kertas saring sehingga berwarna bening.Hasil dari percobaan sesuai dengan teori, karena terbentuk endapan hasil penyaringan berupa padatan PbSO4(tertahan di
Saat melakukan percobaan, digunakan pula corong dan gelas pengaduk.Corong digunakan untuk membantu memasukkan cairan ke dalam tempat yang bermulut sempit.Gelas pengaduk digunakan untuk mengaduk suatu campuran atau larutan kimia pada waktu melakukan reaksi kimia. Digunakan juga untuk menolong pada waktu menuangkan/mendekantir cairan dalam proses penyaringan.
B.2 Titrasi
Studi kuantitatif reaksi netralisasi asam basa yang paling mudah dilakukan adalah dengan menggunakan teknik yang dikenal sebagai titrasi. Dalam titrasi, larutan yang sudah diketahui konsentrasinya disebut larutan standar, ditambahkan secara bertahap ke larutan lain yang belum diketahui konsentrasinya sampai reaksi kimia antara dua larutan berakhir. Jika kita mengetahui volume dari larutan standar dan volume dari larutan yang belum diketahui konsentrasinya, bersama dengan konsentrasi dari larutan standar maka kita bisa menghitung konsentrasi dari larutan yang dititrasi (Chang, 2009). Ada beberapa macam jenis-jenis titrasi bergantung pada jenis reaksinya, seperti titrasi asam basa, titrasi permanganometri, titrasi argentometri, dan titrasi idiometri (Sunarya, 2007).
standarisasi larutan atau untuk memberikan informasi lain tentang komposisi suatu sampel yang sedang dianalisis (Petrucci, 2011).
Titik akhir dari titrasi dapat dicirikan dari perubahan warna indikator atau dengan perubahan drastis dari pH. pH dari reaksi campuran kedua larutan mengalami perubahan secara terus menerus selama titrasi asam basa, namun pH tiba-tiba akan berubah drastis hanya saat di dekat titik akhir. Grafik antara pH dengan volume (v) larutan titran yang ditambahkan disebut sebagai kurva titrasi (Oxtoby, 2011).
Percobaan titrasi yang dilakukan bertujuan untuk mencari normalitas dari HCl. Normalitas dari HCl yang dicari dapat ditentukan menggunakan rumus:
(V1 . N1)HCl = (V2 . N2)NaOH
V1 merupakan volume dari larutan HCl 0,1N yang ditambahkan
dengan 2 tetes PP, N1 merupakan normalitas HCl yang dicari, V2
merupakan volume rata-rata dari volume titran, dan N2 merupakan
normalitas dari NaOH. Berdasarkan percobaan, pada ulangan pertama dibutuhkan 18,1 ml larutan NaOH, sedangkan ulangan kedua dibutuhkan 18,2 ml untuk mengubah larutan HCl 0,1N dari yang berwarna bening menjadi berwarna merah muda.
Reaksi kimia yang terjadi selama proses titrasi adalah: NaOH + HCl NaCl + H2O
Reaksi titrasi dari basa kuat dengan asam kuat akan menghasilkan garam (NaCl) dan air (H2O). Saat percobaan, digunakan buret, corong, dan
IV. KESIMPULAN
Berdasarkan percobaan telah dilakukan, maka dapat ditarik kesimpulan:
A. Penyaringan
A.1 Dalam penyaringan, kertas saring digunakan sebagai media filter dilipat hingga ¼ lingkaran untuk menyaring endapan. A.2 Setelah penyaringan, warna larutan menjadi bening, baunya kurang pekat, dan tidak ada endapan karena endapan tertahan di kertas saring.
B. Titrasi
DAFTAR PUSTAKA
Arisworo, D. Yusa dan Sutresna, N. Ilmu Pengetahuan Alam (Fisika, Biologi, Kimia). Grafindo Media Utama, Bandung.
Chang, Raymond. 2009. Chemistry 10th Edition. McGraw-Hill, New York.
Fibrianto, D. N. 2008. Panduan Kimia Praktis. Pustaka Widyatama, Yogyakarta. Laboratorium Kimia Dasar FMIPA UGM. 2008. Pengenalan Alat Gelas.
http://labkd.blog.ugm.ac.id/2008/11/25/pengenalan-alat-gelas/. Diakses pada tanggal 23 September 2014.
Oxtoby, David W., Gillis, H.P. dan Camplon, Alan. 2011. Principles of Modern Chemistry. Brooks/Cole, USA.
Permanikasari, Lustika dan Andriyani, Wanti. 2009. Pemurnian Larutan Garam (Brine) dari Impuritas Ca2+ dan Mg2+ dengan Penambahan Na
2CO3 dan NaOH.
Petrucci, Ralph H., Herring, F. Geoffrey, Madura, Jeffry D. dan Bissonette, Carey.
2011. General Chemistry Principles and Modern Applications TenthEdition.Pearson Canada Inc., Toronto.
LAMPIRAN
Perhitungan normalitas HCl
Diketahui: Keterangan:
V titran ulangan ke-1 = 18,1 ml V1 = Volume larutan HCl
V titran ulangan ke-2 = 18, 2 ml V2 = Volume rata-rata NaOH
V1 = 20 ml N1 = Normalitas HCl
V2 = 18,15 ml N2 = Normalitas NaOH
N2= 0,1 N
N1= ?
Penyelesaian:
(V1 . N1)HCl = (V2 . N2)NaOH
20 ml . N1 = 18,15 ml . 0,1 N
N1 = 18,15ml .0,120ml N