EVALUASI PENGGUNAAN ASAM VALPROAT PADA PASIEN EPILEPSI PEDIATRIK DI RUMAH SAKIT BETHESDA YOGYAKARTA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Veronica Fideliawati 138114135
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
EVALUASI PENGGUNAAN ASAM VALPROAT PADA PASIEN EPILEPSI PEDIATRIK DI RUMAH SAKIT BETHESDA YOGYAKARTA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Veronica Fideliawati 138114135
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
vi
HALAMAN PERSEMBAHAN Dipersembahkan untuk Tuhan Yesus.
Bapak, Ibu, Mbak Dian, Pani. Para sahabat.
Dan semua orang yang kukasihi.
Karena masa depan itu sungguh ada dan harapanmu tidak akan hilang (Amsal 23 : 18)
vii PRAKATA
Tak terlepas dari berkat dan penyertaan Tuhan Yang Maha Esa, akhirnya naskah skripsi dengan judul “Evaluasi Penggunaan Asam Valproat Pada Pasien Epilepsi Pediatrik Di Rumah Sakit Bethesda Yogyakarta” ini bisa diselesaikan dengan baik. Selama dua semester mulai dari pembuatan proposal, penelitian, hingga terbentuknya naskah ini, penulis tidak sendirian. Karena ada yang mengatakan “Beside someone’s successful, there were thousands of people grab him on his shoulder”, maka penulis ingin mengucapkan banyak terimakasih kepada:
1. Aris Widayati, PhD., Apt. selaku Dekan Fakultas Farmasi Universitas Sanata Dharma.
2. Dr. dr. Rizaldy Pinzon, MKes, SpS. Selaku dosen pembimbing atas semua bimbingan, masukan, saran, mulai dari pencarian tema penelitian, pembuatan proposal, selama penelitian, pembuatan naskah skripsi hingga menyediakan alat dan bahan penelitian.
3. Maria Wisnu DonowatiM.Si., Apt. selaku Wakil Kepala Program Studi Apoteker Fakultas Farmasi Universitas Sanata Dharma dan juga selaku dosen penguji atas semua bantuan, saran, kritik dan masukan selama pembuatan proposal dan naskah skripsi.
4. Christianus Heru Setiawan, M.Sc., Apt.selaku dosen penguji atas semua saran, kritik dan masukan selama pembuatan proposal dan naskah skripsi.
5. Seluruh dosen Fakultas Farmasi Universitas Sanata Dharma atas segala bekal ilmu yang diberikan kepada penulis selama perkuliahan.
6. Pihak Ethical Clearance Universitas Kristen Duta Wacana yang mengeluarkan izin untuk melakukan penelitian.
7. Pihak Rumah sakit Bethesda Yogyakarta yang telah mengizinkan untuk melakukan penelitian di Poli Saraf Rumah sakit Bethesda Yogyakarta.
viii
8. Bapak, Ibu, Mbak Dian dan Pani yang selalu memberikan semangat dalam penulisan naskah skrispi.
9. Segenap teman-teman kelompok skripsi : Era, Reni, Imma, Kris, Rendra, Atika, Tiara, Santi, dan Ocha atas waktu, suka dan dukanya selama rangkaian kegiatan skripsi ini.
10. Para sahabat penulis : Bernadetta Inez Ludwinia, Fransisca Natasha, Francisca Aninda, Stephanie Affrilia , dan Athanasius Wicahyo Prihasworo atas semangat dan dukungan yang luar biasa kepada penulis.
11. Teman-teman Kos Putri Palem atas waktu dan kebersamaan selama penulis menyelesaikan naskah ini
12. Sahabat sejak SMA: Puspa, Yunita, Clara, Tika, Mbak Lita, &Rara atas “dukungannya”.
13. Teman-teman seperjuangan FSM D 2013, FKK C 2013, dan segenap teman-teman Farmasi Sanata Dharma angkatan 2013 yang luar biasa tangguh.
14. Dan kepada semua orang yang telah membantu penulis selama ini.
Tidak banyak yang bisa penulis katakan, tak lupa penulis juga memohon maaf atas ketidaksempurnaan naskah ini disana-sini, namun besar harapan penulis agar karya penelitian yang belums empurna ini bisa berkontribusi dalam dunia penelitian dan bagi masyarakat. Tuhan memberkati.
Yogyakarta, 27 Januari 2017 Penulis
ix DAFTAR ISI
HALAMAN JUDUL... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ...iv
PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI ILMIAH ... vi
PRAKATA ... vii
DAFTAR ISI ...ix
DAFTAR TABEL ...x DAFTAR LAMPIRAN ... xi ABSTRAK ... xii ABSTRACT ...xiii PENDAHULUAN ... 1 METODE PENELITIAN ... 2
HASIL DAN PEMBAHASAN ...4
KESIMPULAN ... 9
SARAN ……...9
DAFTAR PUSTAKA ... 10
LAMPIRAN ...12
x
DAFTAR TABEL
Tabel 1. Karakteristik Subjek Penelitian ... 5
Tabel 2. Kesesuaian Dosis dan Frekuensi Penggunaan ……... 6
Tabel 3. Interaksi obat anti epilepsi pada pasien epilepsi .………...7
Tabel 4. Efek Samping asam valproat pada pasien epilepsi .…………...7
xi
DAFTAR LAMPIRAN
Lampiran 1. Data Pengobatan Pasien Epilepsi...12
Lampiran 2. Parameter Evaluasi Penggunaan asam valproat...22
Lampiran 3. Perhitungan Dosis Asama Valproat...24
Lampiran 4. Ethical Clearence………..29
xii ABSTRAK
Pendahuluan :Epilepsi merupakan suatu kondisi yang ditandai dengan adanya bangkitan kejang yang berulang tanpa provokasi. Kejang epileptic merupakan akibat pelepasan aktivitas listrik otak yang berlebihan sehingga terjadi suatu fenomena abnormal yang mendadak namun transient yang meliputi perubahan kesadaran. Asam valproate dengan struktur 2-propylpentanoic acid merupakan obat anti epilepsi dengan spectrum luas. Mekanisme kerja asam valproate dalam pengobatan epilepsi adalah dengan meningkatkan inaktivasikanal Na+, sehingga menurunkan kemampuan syaraf untuk menghantarkan muatan listrik. Tujuan: mengevaluasi penggunaan obat asam valproate meliputi aspek informasi dosis, efek samping obat, dan interaksi obat pada pasien epilepsi anak di Rumah Sakit Bethesda Yogyakarta periode 2014/2016. Metode: non-eksperimental menggunakan rancangan deskriptif evaluatif dan menggunakan data retrospektif melalui data rekam medik elektronik melalui komputer. Hasil: evaluasi penggunaan obat asam valproat meliputi aspek kesesuaian dosis dan frekuensi penggunaan sebesar 15,38%, aspek interaksi obat yang muncul sebesar7,69%, aspek efek samping pengobatan yang muncul sebesar20,51%, dan untuk aspek pencapaian remisi sebanyak 56,41% kasus sudah mencapai target remisi yaitu 6 bulan bebas kejang. Kesimpulan: pola peresepan asam valproat pada pasien epilepsi pediatrik di Rumah Sakit Bethesda Yogyakata sudah rasional.
xiii ABSTRACT
Introduction: Epilepsy is a condition which is characterized by recurrent seizures without provocation. Epileptic seizures are caused by the release of excess brain electrical activity, causing a sudden abnormal phenomenon but transient involves a change of consciousness. Valproic acid with 2-propylpentanoic acid structure is a broad spectrum antiepileptic drug. Valproic acid mechanism of action in the treatment of epilepsy is by increasing the inactivation of Na+ channels, thereby reducing the ability of the nerves to conduct electrical charges. Objective: To evaluate the use of valproic acid drug includes several aspects which are dosage information, drug side effects, and drug interactions in children patients with epilepsy at Bethesda Hospital Yogyakarta on 2014/2016 period. Result: there were 15,38% cases of appropriate dose given recorded, 7,69% cases with drugs interactions were found, 20,51% cases with side effects were recorded and 56,41% cases have reached the goal of 6 months seizures-free remission. Conclusion: the prescribing pattern of valproic acid as antiepileptic drugs for pediatric patient in Bethesda Hospital Yogyakarta have been rational.
1 PENDAHULUAN
Epilepsi merupakan salah satu penyakit otak yang sering ditemukan di dunia. Epilepsi didefinisikan sebagai suatu gangguan atau terhentinya fungsi otak secara periodik yang disebabkan oleh terjadinya pelepasan muatan listrik secara berlebihan dan tidak teratur oleh sel-sel otak dengan tiba-tiba, sehingga penerimaan dan pengiriman impuls antara bagian otak dan dari otak ke bagian lain tubuh terganggu (Brodie et al, 2012).
Secara keseluruhan insiden epilepsi pada negara maju berkisar antara 40-70 kasus per 100.000 orang per tahun. Di negara berkembang, insiden berkisar antara 100-190 kasus per 100.000 orang per tahun. Prevalensi dari epilepsi bervariasi antara 5- 10 kasus per 1.000 orang (Gunawan, Winiferd, & Maja, 2013). Dari berbagai studi diperkirakan prevalensi epilepsi berkisar antara 0,5 - 4%. Rata-rata prevalensi epilepsi 8,2 per 1000 penduduk (PERDOSSI, 2011).
Prevalensi epilepsi pada bayi dan anak-anak cukup tinggi, menurun pada dewasa muda dan pertengahan, kemudian meningkat lagi pada kelompok usia lanjut (PERDOSSI,2011). Insidensi epilepsi pada anak dilaporkan dari berbagai negara dengan variasi yang luas, sekitar 4-6 per 1000 anak, tergantung pada desain penelitian dan kelompok umur populasi. Prevelansi epilepsi pada bayi dan anak-anak cukup tinggi, menurun pada dewasa muda dan pertengahan, kemudian meningkat lagi pada kelompok usia lanjut. Penderita laki-laki umumnya lebih banyak dibandingkan perempuan. Etiologi epilepsi sebagian besar bersifat idiopatik, tetapi sering juga disebabkan oleh kelainan atau lesi pada otak (Gunawan dan Stephanie, 2013)
Tujuan utama pengobatan adalah membantu orang menjadi bebas kejang tanpa efek samping obat atau perawatan lainnya. Bagi beberapa orang ini mungkin mudah untuk dicapai. Bagi orang lain mungkin cukup sulit dengan perawatan yang tersedia saat ini. Namun demikian, ada banyak kemajuan dalam pengobatan epilepsi dalam beberapa tahun terakhir sehingga orang tidak harus puas kejang lanjutan tanpa terlebih dahulu mengeksplorasi semua pilihan pengobatan yang tepat (Krumholz, et al. 2007).
Obat antiepilepsi yang secara luas digunakan di Indonesia dan merupakan obat utama yang digunakan pada anak dengan epilepsi adalah asam valproat. Asam valproat merupakan obat antiepilepsi yang bisa digunakan pada semua tipe epilepsi, terutama pada epilepsi umum yang idiopatik. Mekanisme kerja asam valproat dalam pengobatan epilepsi adalah dengan meningkatkan inaktivasi kanal Na+, sehingga menurunkan kemampuan syaraf untuk menghantarkan muatan listrik (Ikawati, 2011).
2
Perlu diperhatikan untuk beberapa peresepan obat. Penggunaan obat secara rasional adalah mensyaratkan bahwa penderita menerima obat yang sesuai dengan kebutuhan klinik, dalam dosis yang memenuhi keperluan individual sendiri, untuk periode waktu yang memadai, dan harga yang terendah bagi mereka dan komunitas mereka. Salah satu aspek penting dari pelayanan kefarmasian adalah memaksimalkan penggunaan obat rasional (Amalia dan Siregar 2003). Penggunaan obat yang tidak rasional sering dijumpai dalam praktek sehari-hari. Peresepan obat tanpa indikasi yang jelas, penentuan dosis, cara, dan lama pemberian yang keliru, serta peresepan obat yang mahal merupakan sebagian contoh dari ketidakrasionalan peresepan. Penggunaan suatu obat dikatakan tidak rasional jika kemungkinan dampak negatif yang diterima oleh pasien lebih besar dibanding manfaatnya (Kemenkes, 2011).
Pada penelitian yang pernah dilakukan sebelumnya yang berjudul evaluasi efek samping obat antiepilepsi (OAE) politerapi pada pasien epilepsi pediatrik rawat jalan di Instalasi kesehatan anak (INSKA) RSUP Dr. Sardjito Yogyakarta Periode Januari - Maret 2015 dengan metode cross sectional diperoleh hasil bahwa peresepan kombinasi OAE paling banyak adalah valproat-fenitoin. Hasil evaluasi efek samping menunjukkan efek samping yang paling banyak terjadi adalah perubahan kognitif (80,77%), diikuti oleh perubahan tingkah laku (76,92%), perubahan neurologis (57,69%), perubahan motorik (46,15%), dan perubahan berat badan (23,08%) (Iryani,2015). Maka akan dilakukan penelitian yang bertujuan mengevaluasi penggunaan asam valproat sebagai obat antiepilepsi pada pasien epilepsi anak di Rumah Sakit Bethesda Yogyakarta.
METODE PENELITIAN
Penelitian mengenai evaluasi penggunaan asam valproat pada pasien pediatrik dengan diagnosis epilepsi di Rumah Sakit Bethesda Yogyakarta ini termasuk dalam jenis penelitian non-eksperimental menggunakan rancangan deskriptif evaluatif dan menggunakan data retrospektif. Penelitian ini termasuk dalam jenis penelitian non eksperimental karena observasinya dilakukan secara apa adanya tanpa ada intervensi serta perlakuan dari peneliti terhadap subyek penelitian.
Subjek penelitian ini merupakan semua pasien rawat jalan pediatrik baik laki-laki ataupun perempuan yang terdiagnosis epilepsi di Rumah Sakit Bethesda Yogyakarta. Kriteria inklusi pada penelitian ini adalah pasien epilepsi pediatrik yang menerima resep obat asam valproat baik tunggal maupun kombinasi dan pasien terdiagnosa epilepsi yang
3
memiliki catatan rekam medik selama 2 tahun kebelakang. Sementara kriteria ekslusi pada penelitian ini adalahpasien penderita epilepsi dengan catatan medik yang tidak lengkap atau tidak bisa dikonfirmasi sebagai penunjang utama penegakan diagnosa dokter terhadap epilepsi dan pasien terdiagnosa epilepsi dengan penyakit penyerta. Besar sampel ditentukan dengan rumus berikut:
𝑛 = 𝑍𝛼
2 ∙ 𝑝(1 − 𝑝) 𝑒2 Keterangan:
𝑍2 𝛼 : Nilai Zpada derajat kemaknaan 95% : 1,96 p : Proporsi
e : Presisi
𝑛 =1,96
2∙ 0,04(1 − 0,04) 0,12 = 15
Perhitungan besar sampel minimal menggunakan proporsi 4% berdasarkan data (PERDOSSI, 2006). Dari berbagai studi diperkirakan prevalensi epilepsi berkisar antara 0,5% - 4% yang ada di Indonesia. Maka minimal sampel yang digunakan dalam penelitian adalah 15 orang.
Penelitian akan diawali dengan pengajuan permohonan izin berupa Ethical Clearance diajukan ke Komisi Etik Penelitian Kedokteran dan Kesehatan Fakultas Kedokteran Universitas Kristen Duta Wacana. Pengambilan data dilakukan dengan cara melihat rekam medik elektronik melalui komputer yang berupa kasus epilepsi pada anak. Dilihat jumlah pasien yang terdiagnosa menderita epilepsi, usia pasien, jenis kelamin pasien, berat badan pasien, pasien yang mendapat politerapi asam valproat, dosis, dan frekuensi pemberian obat.
Data diolah secara deskriptif dengan memberikan gambaran karakteristik pasien dengan diagnosis epilepsi sebagai subyek penelitian, profil penggunaan obat pasien, serta profil penggunaan obat asam valproat. Pengolahan data secara evaluatif dilakukan dengan mengevaluasi pola peresepan dan kerasionalan penggunaan asam valproat pada pasien epilepsi.
4
Data rekam medik pasien yang telah diperoleh akan diolah dengan metode statistika deskriptif dengan menghitung persentasenya. Data pasien dikelompokkan terlebih dahulu sebagai berikut:
a. Persentase pasien epilepsi yang telah menerima politerapi asam valproat berdasarkan jenis kelamin dengan menghitung jumlah pasien laki-laki dan perempun dibagi total kasus dikali 100%
b. Persentase pasien epilepsi yang telah menerima politerapi asam valproat berdasarkan dosis dan frekuensi penggunaan dengan menghitung jumlah pasien dibagi total kasus dikali 100%.
c. Persentase penggunaan politerapi asam valproat berdasarkan interaksi obat dengan menghitung jumlah obat dibagi total kasus dikali 100%.
d. Persentase penggunaan politerapi asam valproat berdasarkan efek samping obat dengan menghitung jumlah obat dibagi total kasus dikali 100%.
Selanjutnya dilakukan evaluasi kerasionalan politerapi asam valproat berdasarkan PERDOSSI 2006.
HASIL DAN PEMBAHASAN
Penelitian ini dimulai dengan penelusuran data pasien epilepsi pediatrik rawat jalan di poliklinik saraf Rumah Sakit Bethesda Yogyakarta pada periode 2014-2016. Data diambil melalui rekam medik elektronik melalui komputer.Data yang dapat tercatat sebanyak 39 kasus dengan kriteria pasien rawat jalan, pasien terdiagnosa epilepsi dengan peresepan asam valproat pertama kali pada periode 2014-2016 dan usia 3-15 tahun.
Pada anak-anak yang diketahui mengidap epilepsi, kejang bisa diprovokasi oleh kurang tidur, ataupun stress. Epilepsi dapat menyerang pada laki-laki ataupun perempuan. Secara umum diperkirakan ada 2,4 juta kasus baru setiap tahun, dan 50% kasus terjadi pada masa kanak-kanak atau remaja (WHO, 2006). Dalam hal ini perlu diperhatikan pula dosis obat yang diberikan untuk pasien epilepsi pada anak.
1. Karakteristik pasien
Salah satu faktor yang mempengaruhi epilepsi adalah jenis kelamin dan usia. Epilepsi dapat terjadi pada segala umur namun sering terjadi pada anak anak dan juga remaja. Berikut distribusi berdasarkan umur dan jenis kelamin pasien:
5
Tabel I. Karakteristik umur dan jenis kelamin pasien epilepsi pediatrik di Rumah Sakit Bethesda Yogyakarta periode 2014-2016
Selama kurun waktu 2014 sampai dengan 2016 dijumpai 39 orang anak penderita epilepsi yang berobat di poliklinik saraf Rumah Sakit Bethesda Yogyakarta. Total kasus yaitu 39 (100%) yang terdiri dari 21 (53,8%) anak perempuan dan 18 (46,2%) anak laki-laki. Sebaran usia kasus yang diteliti sesuai dengan insiden epilepsi yang berubah-ubah menurut usia,yaitu insidens tertinggi pada usia anak dini, mencapai nadirnya pada usia dewasa dini, dan naik kembali pada usia tua. Bangkitan epilepsi jarang dijumpai pada usia bulan-bulan pertama, dan lebih sering antara usia 4 bulan-4 tahun, kemudian frekuensinya menurun sampai remaja (Andayani, Taslim, & Sri, 2000)
Pada penelitian ini menunjukan bahwa pasien epilepsi pediatrik yang menerima terapi asam valproat lebih banyak perempuan 53,8% dibandingkan laki-laki 46,2%. Hasil penelitian ini juga menunjukan bahwa prevalensi pasien epilepsi anak bertambah seiring bertambahnya umur. Pada kelompok anak tertentu, serangan epilepsi mulai atau berhenti di sekitar pubertas sesuai dengan penelitian (Gunawan, & Stepahanie, 2013) yang menyatakan bahwa prevalensi epilepsi pada anak dan bayi sangat tinggi kemudian menurun pada saat dewasa muda (pubertas).
Karakteristik Jenis Kelamin
Total Pasien Laki-laki Perempuan
(18/46,2%) (21/53,8%) (39/100%) Usia (tahun)
1-5 6 15,4 5 12,8 11 28,2 6-10 6 15,4 7 17,9 13 33,3 11-15 6 15,4 9 23,1 15 38,5
6 2. Karakteristik Penggunan Asam Valproat
Asam valproat merupakan pilihan pertama untuk terapi epilepsi sesuai dengan (NICE guideline on AEDs, 2014). Obat antiepilepsi mempunyai peran dominan dalam manajemen epilepsi. Walaupun monoterapi sering digunakan sebagai pilihan pertama, seringkali politerapi sulit dihindarkan. Kesesuaian dosis untuk obat antiepilepsi itu sendiri harus diperhatikan. Interaksi obat – obat dan efek samping dari obat mungkin akan terjadi.
Tabel II. Kesesuaian dosis & frekuensi penggunaan antiepilepsi pasien epilepsi di Rumah Sakit Bethesda Yogyakarta
Dari hasil penelitian diperoleh ada sejumlah 9 (60%) dengan pemberian dosis yang tidak sesuai dikarenakan dosis yang di berikan terlalu rendah dan sejumlah 6 (40%) dengan pemberian dosis sesuai menurut guideline (PERDOSSI, 2011). Dalam kategori kesesuaian dosis ditentukan dari berat badan pasien. Sesuai dengan guideline PERDOSSI, 2011 dosis asam valproat untuk anak - anak adalah 20-40 mg/kg/hari. Dari 39 kasus yang diperoleh hanya 15 kasus yang dievaluasi berdasarkan berat badan. Kesesuian dosis saat peresepan sangatlah penting untuk tercapainya efektivitas obat. Pemberian obat dimulai dari dosis rendah dan dinaikkan bertahap sampai dosis efektif tercapai atau timbul efek samping. Kadar obat dalam darah ditentukan bila bangkitan tidak terkontrol dengan dosis efektif (IDI, 2014).
Kategori Jumlah (n = 15)
Presentase (% = 100)
Dosis sesuai 6 40
7
Tabel III. Interaksi obat antiepilepsi pada pasien epilepsi di Rumah Sakit Bethesda Yogyakarta
Kategori Jumlah
(n = 39)
Presentase (% = 100)
Ada interaksi 0 0
Tidak ada interaksi 39 100
Dalam penelitian ini tidak diperoleh interaksi antar obat antiepilepsi. Meskipun ada beberapa pasien yang menggunkan obat antiepilepsi yaitu asam valproate-fenitoin, asam valproate-lvitiracetam, dan asam valproate-clonazepam secara bersamaan namun dalam rekam medis tidak tercantum keluhan pasien sebagai inetraksi obat antiepilepsi.
Tabel IV. Efek Samping yang terjadi pada pasien epilepsi di Rumah Sakit Bethesda Yogyakarta
Kategori Jumlah
n = 39
Presentase (%=100)
Tidak ada keluhan 31 79,49
Pusing 4 10,26
Demam dan batuk 4 10,26
Tercatat dalam rekam medis dengan melihat e-RM ada 4 (10,26%) yang mengalami efek samping pusing dan 4 (10,26%) yang mengakami demam dan batuk, namun efek samping yang terjadi tidak tercantum pada guideline (PERDOSSI,2016) sebagai efek samping asam valproat. Efek sampimg yang terjadi bisa dikarenakan adanya penambahan obat lain. Sedangkan, pada 31 (79,49%) kasus pada rekam medis tercatat tidak ada keluhan dari pasien sebagai efek samping pengobatan antiepilepsi yaitu asam valproat.
3. Efektivitas obat
Menurut penelitian yang dilakukan oleh (Lingga, Lukman, & Dewa, 2016) efektivitas obat antiepilepsi (OAE) dilihat dari pencapaian remisi selama 6 bulan, karena menurut Ikatan Dokter Anak Indonesia (IDAI) rata-rata penggunaan obat antiepilepsi dapat diturunkan
8
dosisnya pada 3-6 bulan pemberian OAE. Dalam jangka waktu 3-6 bulan tersebut dapat dilihat jika 6 bulan sudah bebas kejang artinya obat efektif.
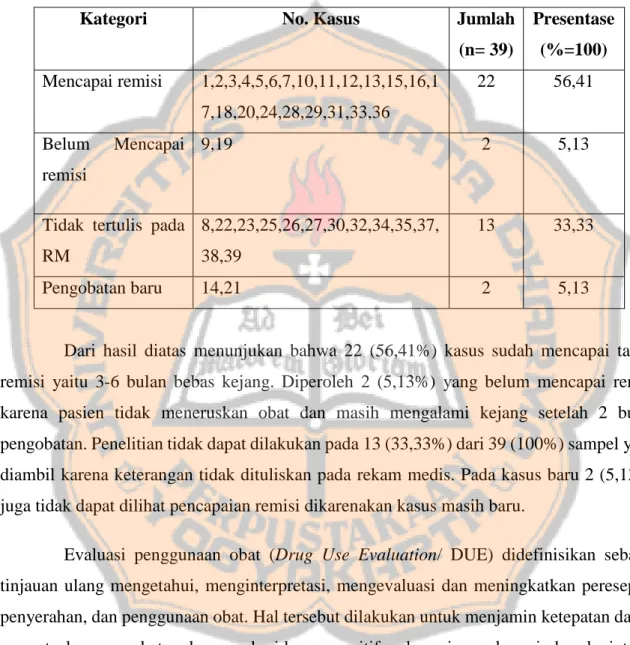
Tabel V. Efektivitas asam valproat yang diresepkan untuk pasien epilepsi pediatrik di Rumah Sakit Bethesda Yogyakarta
Kategori No. Kasus Jumlah
(n= 39) Presentase (%=100) Mencapai remisi 1,2,3,4,5,6,7,10,11,12,13,15,16,1 7,18,20,24,28,29,31,33,36 22 56,41 Belum Mencapai remisi 9,19 2 5,13
Tidak tertulis pada RM 8,22,23,25,26,27,30,32,34,35,37, 38,39 13 33,33 Pengobatan baru 14,21 2 5,13
Dari hasil diatas menunjukan bahwa 22 (56,41%) kasus sudah mencapai target remisi yaitu 3-6 bulan bebas kejang. Diperoleh 2 (5,13%) yang belum mencapai remisi karena pasien tidak meneruskan obat dan masih mengalami kejang setelah 2 bulan pengobatan. Penelitian tidak dapat dilakukan pada 13 (33,33%) dari 39 (100%) sampel yang diambil karena keterangan tidak dituliskan pada rekam medis. Pada kasus baru 2 (5,13%) juga tidak dapat dilihat pencapaian remisi dikarenakan kasus masih baru.
Evaluasi penggunaan obat (Drug Use Evaluation/ DUE) didefinisikan sebagai tinjauan ulang mengetahui, menginterpretasi, mengevaluasi dan meningkatkan peresepan, penyerahan, dan penggunaan obat. Hal tersebut dilakukan untuk menjamin ketepatan dalam memutuskan pengobatan dan memberi luaran positif pada pasien pada periode selanjutnya. Evaluasi diperlukan untuk mencegah penggunaan obat yang tidak tepat, mencegah efek samping obat, dan meningkatkan keefektifan obat (Navarro, 2009).
9 KESIMPULAN
Evaluasi penggunaan asam valproat pada pasien epilepsi anak-anak memperlihatkan bahwa pola peresepan asam valproat sebagai obat antiepilepsi sudah rasional .
SARAN
Dalam pengambilan sampel perlu diperbanyak lagi jumlah sampel yang diambil agar mengantisipasi bila ada sampel data yang tidak bisa dihitung selain itu, dilakukan penelitian dengan metode prospektif agar hasil yang diperoleh lebih akurat. Diharapkan dengan adanya penelitian lanjutan yang menggunakan data prospektif hasil evaluasi pengobatan yang dijalani pasien dapat mencapai outcome.
10
DAFTAR PUSTAKA
Amalia, L., dan Siregar, C., 2003, Farmasi Rumah Sakit: Teori dan Penerapan, Penerbit Buku Kedokteran EGC, Jakarta.
Andayani, P., Soetomenggolo, T. S., Hadinegoro, S. R. S., & Cara, B. (2000). Evaluasi Klinis Pengobatan Epilepsi dengan Karbamazepin pada Anak, 2.
Brodie, R. J., Hollebeek, L.D., Juric, B., & Ilic A., 2011, Customer Engagement Conceptual Domain, Fundamental exchange on customer value and loyalty, Journal of Business Research, 59, 449 - 456.
Carvalho, et al, 2014, Drug Interaction between Phenytoin and Valproic Acid in a Child With Refractory Epilepsy: A Case Report, Journal of Pharmacy Practice, 27 (2), 214-216.
Gunawan,D. P, Winifred, K., Maja. 2013. Gambaran Tingkat Pengetahuan Masyarakat Tentang Epilepsi Di Kelurahan Mahena Kecamatan Tahuna Kabupaten Sangihe.Bagian/SMF Neurologi Fakultas Kedokteran Universitas Sam Ratulangi Manado.
Gunawant, P. Y., & Stephanie, E. D. 2013. Karakteristik Pasien Epilepsi Di Rumah Sakit Siloam Lippo Village, Tangerang, Tahun 2013. Neurologis, Fakultas Kedokteran (Iniversitas Pelita Harapan)
Ikatan Dokter Anak Indonesia, 2016. Seputar Epilepsi Pada Anak. http://Www.Idai.Or.Id/Artikel/Seputar-Kesehatan-Anak/Seputar-Epilepsi-Pada-Anak Diakses 20 Januari 2017
Ikatan Dokter Indonesia. 2014. Panduan Praktik Klinis Bagi Dokter Di Fasilitas Pelayanan Kesehatan Primer. Jakara. PP:233 - 239
Ikawati, Z., 2011, Farmakoterapi Penyakit Sistem Saraf Pusat, Bursa Ilmu, Yogyakarta. Iryani, K. S., 2015. Evaluasi Efek Samping Obat Antiepilepsi (Oae) Politerapi Pada
Pasien Epilepsi Pediatrik Rawat Jalan Di Instalasi Kesehatan Anak (Inska) Rsup Dr. Sardjito Yogyakarta Periode Januari-Maret 2015. Fakultas Farmasi Universitas Gadjah Mada Yogyakarta
Kementrian Kesehatan Republik Indonesia. 2011. Modul Penggunaan Obat Rasional. Jakarta: Kemenkes.
11
Kementrian Kesehatan Republik Indonesia. 2014. Pedoman Penerapan Formularium Nasional. Jakarta: Kemenkes
Krumholz A, et al. 2007. Practice parameter: Evaluating an apparent unprovoked first seizure in adults (an evidence‐based review): Report of the Quality Standards Subcommittee of the American Academy of Neurology and the American Epilepsy Society. Neurology, 69(21): 1996–2007
Lingga, Lukman and Dewa, EVALUASI DOSIS ASAM VALPROAT PADA PASIEN EPILEPSI ANAK, Jurnal Manajemen dan Pelayanan Farmasi, 3 (2), 137-143. Mifsud, J., 2014. Gender differences in epilepsy: perceived or real? . Department of
Clinical Pharmacology and Therapeutics University of Malta
NICE guideline on AEDs. 2014. NICE produces guidance for the treatment and management of health conditions in England and Wales. Its guidance on epilepsy includes recommendations for the drug treatment of different types of epilepsy and seizures
Navarro, R. P. 2009. Managed Care Pharmacy Practice, Second edition, Jones and Bartlett Publisher. Massachusetts, 218, 219.
Notoatmodjo, 2010. Metode Penelitian Kesehatan. Jakarta: Rineka Cipta
PERDOSSI. 2006. Pedoman Tatalaksana Epilepsi. Airlangga University Press. Surabaya
PERDOSSI. 2016. Pedoman Tatalaksana Epilepsi. Airlangga University Press. Surabaya
WHO, 2006, Neurological Disorder: Public Health Challenges, 56 – 67, WHO Press, Geneva.
Wibowo, S. dan Gofir, A., 2006, Obat Antiepilepsi, 7-127, Pustaka Cendekia Press, Yogyakarta.
12 LAMPIRAN
Lampiran 1. Data pengobatan pasien epilepsi pediatrik di Rumah Sakit Bethesda Yogyakarta periode 2014-2016 No Tanggal Pengobatan No. RM Inisial Usia (th) L/ P BB (Kg) Peresepan Keluhan pasien 1. 16/10/2012 0198 5700 SR 15 P - Rivotril 2mg (30) 1x1 Neurodex (vitamin) tab (30) 1x1 Ikalep 250mg (tab) (30) 1x1 -06/01/2014 sudah tidak kejang, pemeriksaa n EEG membaik -22/10/2015 masih pusing 2 23/06/2015 0101 6844 DAS 12 L - Keppra 250mg tab (30) 1x50 mg Ikalep JKN 250mg tab (30) 1x 50 mg 21/07/2015 badan terasa kaku 10/03/2016 tidak kambuh 3 23/04/2013 0080 6520 KMA 10 P - Depakene 250mg/ 5ml Syr (120 ml) (1) 1x3,5 cc 17/11/2014 tidak kambuh
13 4 24/09/2013 0106 9624 AAM L - Neurotam 500mg / 5ml syr 100ml (1) 2x CTH Depakene 250mg/ 5ml syr 120ml (1) 2x2,5 CC Keppra 250mg tab (20) 2x 50 mg 29/09/2016 tidak ada keluhan & tidak kambuh 5. 22/11/2012 0195 1930 JNP 10 L - Depakene 250mg /5ml syr 120ml (2) 2x3,5 CC Peracikan obat (40) 2x1 (Keppra 250mg tab 50mg) (Ikhapen 100mg cap 50mg) 12/02/2013 tidak kambuh 09/01/2014 bebas kejang 1 tahun 05/09/2014 mulai tapering off 6. 19/05/2015 0107 3390 SJR 15 P - Riklona 2mg tab (30) 1x1 14/07/2015 kambuh kejang
14 (malam hari) Ikalep 250mg tab (30) 1x1 (pagi hari) 02/06/2016 tidak kambuh 7. 19/03/2014 0170 5160 OCPF 7 P - Depakene 250mg/5ml syr 120ml (1) 1x2,5 CC 24/06/2014 batuk dan demam 26/11/ 2015 tidak ada keluhan 21/04/2016 mulai tapering off 222/08/201 6 tidak ada keluhan 8. 19/03/2013 0102 5013 AYP M 15 P - Ikalep 250 mg tab (30) 1x1 28/03/2014 tidak ada keluhan 9. 25/11/2013 0197 5996 FTB 5 L 17,5 Depakene 250mg /5ml syr 120ml (1) 1x2,5 CC malam hari 19/08/2015 masih pusing karena tidak meneruska n obat
15 10. 11/04/2013 0198 8771 AN 11 P 32 Depakene 250mg/5ml syr 120ml (1) 2x2,5 CC Rivotril 2mg tab (20) 1x1 malam hari Racikan obat (40) 2x1 (Ikhapen 100mg cap 50mg) Keppra 250mg tab 50 mg ) 10/10/2013 tidak kambuh 23/12/2013 mulai tapering off 11. 18/09/2010 0059 6109 NAP 12 L - Depakene 250mg/ 5ml syr 120ml (1) 1x1 03/11/2014 tidak kambuh 12. 04/01/2014 0057 7087 ANN 13 P - Depakene 250mg/5ml syr 1x2,5CC 23/06/2014 mulai tapering off (sudah tidak kambuh 13. 12/07/2011 0196 8884 BA 9 L 30 Depakene 250mg 21/12/ 2014 sudah tidak
16 /5ml syr 2x2,5CC kambuh lagi 14. 12/07/2016 0204 1260 KH 4 L 13 Depakene 250mg/ 5ml syr 120 ml (2) 2x2,5 CC Keppra 250 mg tab (40) 2x50mg 22/08/2016 kontrol tanpa keluhan 15. 28/03/2015 0107 3353 FND 3 L 12 Ikalep 250mg / 5ml syr 120ml (2) 2x3,5 CC Riklona 2mg tab (30) 1x0,4mg 15/09/2015 tidak kambuh 16. 10/05/2016 0100 0442 8 NIC 5 P 17 Neurotam 500mg/5ml syr (100ml) (1) 1x5 CC Depakene 250mg/5ml syr 120ml (2) 2x2,5CC 07/11/2016 bebas kejang tapering off 17. 18/08/2011 0080 3357 HAK 12 L 85 Depakote 500mg tab (60) 1x2 14/04/2015 kontrol rutin tidak kambuh
17 Keppra 250mg tab (60) 2x1 18. 02/12/2013 0107 3706 DE 13 P - Ikalep 250mg tab (20) 1x1 malam hari 12/03/2015 pusing tapi tidak kambuh 19. 24/08/2015 0111 5473 FAF 3 L - Depakene 250mg /5ml syr 120ml 1x2,5 CC Pada bulan februari kejang 20. 08/08/2015 0111 1833 VE 12 L 42 Ikalep 250mg tab (30) 1x1 malam hari 05/03/2016 tidak ada keluhan kejang tidak kambuh 21. 19/03/2016 0203 6081 EK 6 L 10,5 Dilantin 100mg cap (40) 2x30mg Depakene 250mg /5ml syr 120ml 2x2,5 CC 05/04/2016 tidak kejang namun demam dan batuk 22. 01/10/2014 0107 1859 AMP 6 P 23,5 Depakene 250mg/5ml syr 120ml (2) 2x3CC
18 Riklona 2mg tab (30) 1x1 malam hari 23. 25/04/2014 0104 1509 KAM W 3 P 10,9 Ikhapen 100mg (40) 2x20mg Depakene 250mg/5ml 120ml syr 1x2,5CC 24. 21/01/2014 0200 6633 RPK 10 P 21 Depakene 250mg/5ml syr 120ml 1x2,5CC 19/12/2015 tidak kambuh 25. 14/06/2011 0080 7857 PPB 2 L 12,5 Depakene 250mg/5ml syr 120ml 1x2,5 CC 26. 08/08/2014 0080 8099 DGM S 6 L 20 Depakene 250mg /5ml syr 120ml 2x2,5CC 27. 11/09/2014 0097 3111 CZA 13 P - Depakene 250mg /5ml syr 120ml 1x2,5CC 28. 19/08/2014 0106 5246 DRY 13 L - Depakene 250mg/5ml 2016 sudah tidak
19 syr 120ml 1x4 CC Rivotril 2mg tab (30) 1x0,5mg malam hari kambuh lagi dan mulai tapering off 29. 05/02/2016 0108 8176 CP 15 P - Ikalep 250mg tab (50) 1x1 malam hari 29/09/2016 tidak kambuh 30. 27/03/2015 0110 7216 AKC 3 P - Depakene 250mg/5m syr 120ml 1x1,5 CC Neurotam 500mg /5ml syr 100ml 1x1,5 CC 15/04/2015 tidak kambuh 31. 30/06/2015 0111 3081 KLB 13 L - Ikalep 250mg tab (20) 1x1 siang hari Neurotam 400mg cap (20) 1x1 pagi hari 27/01/2016 tidak kambuh 32. 09/10/2015 0111 9458 XCM 9 P - Ikalep 250mg /5ml syr 17/12/2015 Tidak terjadi
20 120ml 2x2,5 CC kekambuha n 33. 24/11/2015 0203 2000 9 CPDA 11 P - Ikalep 250mg tab (30) 1x1 27/01/2016 panas dan tenggoroka n sakit 08/07/2016 tidak kejang dan tidak ada keluhan 34. 23/04/2016 0112 9499 LCG 10 P - Ikalep 250mg tab (30) 2x1 35. 25/07/2016 0113 8015 AFC 4 L - Depakene 250mg/5ml syr 120ml 1x2,5CC 06/09/2016 tidak kejang tapi kadang masih pusing 36. 11/09/2012 0104 0482 RFS 9 L - Depakene 250mg/5ml syr 120ml 2x3 CC 31/12/2013 tidak kambuh 09/11/2016 mulai tappering off 37. 27/08/2016 0200 4232 KAA 3 P 12 Depakene 250mg/5ml
21 syr 120ml 2x3,5CC 38. 06/08/2016 0113 8475 CNS 9 P - Depakene 250mg /5ml syr 120ml 1x2,5 CC 24/10/2016 tidak ada keluhan dan tidak kambuh 39. 22/07/2015 0202 7687 AR 5 P - Depakene 250mg /5ml syr 120ml 2x2,5 CC
22
Lampiran 2. Parameter Evaluasi Penggunaan Asam Valproat Pada Pasien Epilepsi Pediatrik Di Rumah Sakit Bethesda Yogyakarta.
No. Obat 1 Obat 2 0bat 3 Kesesuaian dosis
Interaksi obat
Efek samping 1 Rivotril Neurodex Ikalep - 0 1
2 keppra ikalep - 0 1
3 depakene - 0 0
4 neurotam depakene Keppra - 0 0 5 Depakene Keppra ikhapen - 0 0
6 Riklona Ikalep - 0 0
7 Depakene - 0 1
8 Ikalep - 0 0
9 Depakene 1 0 1
10 Depakene Ikhapen Keppra 0 0 0
11 Depakene - 0 0 12 Depakene - 0 0 13 Depakene 0 0 0 14 Depakene Keppra 1 0 0 15 Ikalep Riklona 1 0 0 16 Depakene Neurotam 1 0 0 17 Depakote Keppra 0 0 0 18 Ikalep - 0 1 19 Depakene - 0 0 20 Ikalep 0 0 0 21 Depakene Dilantin 1 0 1 22 Depakene Riklona 0 0 0 23 Depakene Ikhapen 0 0 0 24 Depakene 0 0 0 25 Depakene 0 0 0 26 Depakene 0 0 0 27 Depakene - 0 0 28 Depakene Ritrovil - 0 0
23 29 Ikalep - 0 0 30 Depakene Neurotam - 0 0 31 Ikalep Neurotam - 0 0 32 Ikalep - 0 0 33 Ikalep - 0 1 34 Ikalep - 0 0 35 Depakene - 0 1 36 Depakene - 0 0 37 Depakene 1 0 0 38 Depakene - 0 0 39 Depakene - 0 0 Keterangan : 1. Kesesuaian dosis
1 = sesuai dengan dosis anak PERDOSSI 2011 (15-40 mg/kg/hari) 0 = tidak sesuai dengan perhitungan Clark
2. Interaksi obat
1= ada interaksi antara obat antiepilepsi (asam valproat dan phenytoin) sesuai dengan guideline PERDOSSI 2011
0= tidak ada interaksi obat antiepilepsi sesuai dengan guideline PERDOSSI 2011 3. Efek Samping
1= terdapat efek samping 0= tidak terdapat efek samping
24 Lampiran 3. Perhitungan Dosis asam valproat
No Obat yang diberikan Usia Bb (Kg) Dosis Anak (min. ) Dosis Anak (maks.) Dosis yang diberikan Ke- sesuaia n dosis 1 Ikalep 250mg (tab) (30) 1x1 15 - 2 Ikalep JKN 250mg tab (30) 1x 50mg 12 - 3 Depakene 250mg/ 5ml Syr (120 ml) (1) 1x3,5 cc 10 - 4 Depakene 250mg/ 5ml syr 120ml (1) 2x2,5 CC 7 - 5 Depakene 250mg /5ml syr 120ml (2) 2x3,5 CC 10 - 6 Ikalep 250mg tab (30) 1x1 (pagi hari) 15 - 7 Depakene 250mg/5ml syr 120ml (1) 1x2,5 CC 7 - 8 Ikalep 250 mg tab (30) 1x1 15 -
25 9 Depakene 250mg /5ml syr 120ml (1) 1x2,5 CC 5 17,5 262,5 700 125 1 10 Depakene 250mg/5ml syr 120ml (1) 2x2,5 CC 11 32 480 1280 250 0 11 Depakene 250mg/ 5ml syr 120ml (1) 1x1 12 - 12 Depakene 250mg/5ml syr 1x2,5CC 13 - 13 Depakene 250mg /5ml syr 2x2,5CC 9 30 450 1200 250 0 14 Depakene 250mg/ 5ml syr 120 ml (2) 2x2,5 CC 4 13 195 520 250 1 15 Depakene 250mg / 5ml syr 120ml (2) 2x3,5 CC 3 12 180 480 356 1 16 Depakene 250mg/5ml syr 120ml (2) 2x2,5CC 5 17 255 680 250 1
26 17 Depakote 500mg tab (60) 1x2 12 85 1275 3400 250 0 18 Ikalep 250mg tab (20) 1x1 malam hari 13 - 19 Depakene 250mg /5ml syr 120ml 1x2,5 CC 3 - 20 Ikalep 250mg tab (30) 1x1 malam hari 12 42 630 1680 250 0 21 Depakene 250mg /5ml syr 120ml 2x2,5 CC 6 10,5 157 420 250 1 22 Depakene 250mg/5ml syr 120ml (2) 2x3CC 6 23,5 352 940 294 0 23 Depakene 250mg/5ml 120ml syr 1x2,5CC 3 10,9 163 436 125 0 24 Depakene 250mg/5ml syr 120ml 1x2,5CC 10 21 315 840 125 0 25 Depakene 250mg/5ml syr 120ml 1x2,5 CC 2 12,5 187 500 125 0
27 26 Depakene 250mg /5ml syr 120ml 2x2,5CC 6 20 300 800 250 0 27 Depakene 250mg /5ml syr 120ml 1x2,5CC 13 - 28 Depakene 250mg/5ml syr 120ml 1x4 CC 13 - 29 Ikalep 250mg tab (50) 1x1 malam hari 15 - 30 Depakene 250mg/5m syr 120ml 1x1,5 CC 3 - 31 Ikalep 250mg tab (20) 1x1 siang hari 13 - 32 Ikalep 250mg /5ml syr 120ml 2x2,5 CC 9 - 33 Ikalep 250mg tab (30) 1x1 11 - 34 Ikalep 250mg tab (30) 2x1 10 - 35 Depakene 250mg/5ml syr 120ml 1x2,5CC 4 - 36 Depakene 250mg/5ml syr 120ml 2x3 CC 9 -
28 37 Depakene 250mg/5ml syr 120ml 2x3,5CC 3 12 180 480 356 1 38 Depakene 250mg /5ml syr 120ml 1x2,5 CC 9 - 39 Depakene 250mg /5ml syr 120ml 2x2,5 CC 5 -
29
30
31
BIOGRAFI PENULIS
Penulis skripsi dengan judul “Evaluasi Penggunaan Asam Valproat Pada Pasien Epilepsi Pediatrik di Rumah Sakit Bethesda Yogyakarta” memiliki nama lengkap Veronica Fideliawati. Penulis lahir di Kotabumi, 24 Februari 1995, merupakan putri kedua dari tiga bersaudara dalam keluarga pasangan Bambang Triwahyono dan Anastasia Suwarni.Pendidikan formal yang ditempuh penulis dimulai di SD Negeri 1 Semuli Raya (2001-2007), setelah itu dilanjutkan ke SMP Xaverius Metro (2007-2010), pendidikan menengah atas di SMA Fransiskus Bandar Lampung (2010-2013). Kemudian pendidikan dilanjutkan hingga perguruan tinggi di Fakultas Farmasi Sanata Dharma Yogyakarta. Penulis kemudian melanjutkan pendidikan sarjana di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta pada tahun 2013. Semasa menempuh kuliah, penulis aktif dalam berbagai kepanitian. antara lain menjadi anggota divisi MC di TITRASI (2014), Koordinator MC di PPrtoS (2015), anggota penyiar di UKM PT. Radio Masdha Jogja (2014-2016).