6 2.1 Mentimun (Cucumis sativus)
Mentimum adalah salah satu jenis sayur-sayuran yang dikenal di hampir setiap negara. Tanaman ini berasal dari Himalaya di Asia Utara. Saat ini budidaya mentimum sudah meluas ke seluruh dunia baik daerah tropis atau subtropis. Mentimun memiliki berbagai nama daerah di Indonesia seperti timun (Jawa),
bonteng (Jawa Barat), temon atau antemon (Madura), ktimun atau antimun (Bali),
hantimun (Lampung) dan timon (Aceh) (Rukmana, 1994).
Klasifikasi botani tanaman mentimun adalah sebagai berikut: Divisi : Spermatophyta
Sub divisi : Angiospermae Kelas : Dicotyledonae Ordo : Cucurbitales Famili : Cucurbitaceae Genus : Cucumis Spesies : Cucumis sativus
Mentimun merupakan tanaman setahun yang tumbuh menjalar, dengan sistem perakaran dangkal. Batang tanaman mentimun memiliki panjang 1-3 m dengan sulur yang tidak bercabang. Daun bulat segitiga, agak berbentuk jantung, lebar 7-25 cm dan permukaan kasar karena adanya rambut-rambut di permukaan daun, panjang tangkai daun 5-15 cm. Bunga berwarna kuning berbentuk lonceng (Rubatzky dan Yamaguchi, 1999).
1.2 Penyakit Daun Kuning Pada Tanaman Mentimun Dan Virus Yang Berasosiasi
Salah satu OPT penting pada tanaman mentimun adalah virus. Ada dua tipe gejala infeksi virus pada tanaman mentimun yaitu gejala kuning dan mosaik. Gejala kuning terlihat pada helaian daun mengalami vein clearing dimulai dari daun-daun pucuk, kemudian berkembang menjadi warna kuning yang jelas, tulang daun menebal dan daun-daun menggulung ke atas dan apabila serangannya sudah lanjut (infeksi lanjut), menyebabkan daun-daunnya mengecil dan berwarna kuning terang, tanaman kerdil dan tidak berubah (De Barrow et al. 2008). Sedangkan gejala lainnya yaitu klorosis menunjukkan gejala menguning pada daun karena klorosis antara tulang daun, tulang daun dan jaringan disekitarnya tetap hijau sehingga tampak menyirip dan tidak menunjukkan adanya pemendekan internoda (Suastika et al. 2012).
Duffus (1965) melaporkan pertama kali gejala kuning atau klorosis pada mentimun oleh adanya infeksi virus dari kelompok Crinivirus. Selanjutnya, Lecoq et al. (1994) melaporkan virus dari genus Polerovirus yang menginduksi gejala klorosis atau kuning pada mentimun. Sedangkan daun kuning pada blewah dan labu di Thailand dilaporkan terinfeksi virus dari kelompok Begomovirus (Samretwanich et al. 2000). Berdasarkan laporan tersebut, gejala kuning pada daun mentimun yang ditemukan di Kecamatan Baturiti, Kabupaten Tabanan, Bali lebih mirip dengan gejala yang disebabkan oleh virus dari kelompok Crinivirus, Polerovirusdan Begomovirus.
2.2.1 Genus Polerovirus
Anggota famili Luteoviridae dapat dibedakan menjadi 3 genus, yaitu Luteovirus, Enamovirus, dan Polerovirus (King et al. 2012). Luteovirus dan Polerovirus ditularkan hanya melalui kutudaun secara persisten sirkulatif, namun tidak propagatif dalam tubuh serangga (Raccah dan Fereres 2009), sedangkan Enamovirus dapat ditularkan melalui inokulasi mekanik (King et al. 2012).
2.2.1.1 Karakter molekuler Polerovirus
Partikel virus berbentuk isometrik, beruntai tunggal ssRNA dari 5,7 kb (Mayo dan D'Arcy 1999). Virus-virus anggota famili ini mempunyai partikel berbentuk bulat berukuran diameter 25 sampai 30 nm, orientasi positif yang diekspresikan dalam 5 sampai 6 open reading frame (ORF) (D’Arcy et al. 2000). 1.2.1.2Gejala infeksi Polerovirus
Saat ini terdapat 13 spesies virus yang termasuk genus Polerovirus (Carstens dan Ball, 2009; Carstens, 2010). Setidaknya tiga spesies Polerovirus yang menginfeksi labu-labuan telah dilaporkan di Asia diantarnya Cucurbit
aphid-borne yellows virus (CABYV), Melon aphid-borne yellows virus (MABYV) dan
Suakwa aphid-borne yellows virus (SABYV) (Lecoq et al. 1992; Xiang et al. 2008
; Shang et al. 2009). Sedangkan, di Indonesia infeksi Polerovirus baru dilaporkan pada tanaman cabai (Rahayuningsih, 2013) dan wortel (Susanti, 2014) dengan spesiesnya Pepper vein yellows virus (PeVYV). Tanaman cabai yang terinfeksi Polerovirus menunjukkan gejala klorosis, lamina daun menguning, akan tetapi bagian tulang daun dan jaringan di sekitarnya tetap berwarna hijau sehingga daun terlihat seperti menjari. Klorosis merupakan peristiwa terjadinya perubahan warna
daun akibat klorofil yang dihasilkan berkurang (Bos, 1990). Bila diamati lebih lanjut terhadap tanaman yang sakit, tanaman terlihat berukuran normal, tidak mengalami penghambatan pertumbuhan, demikian juga daun-daunnya berukuran normal, serta tidak mengalami malformasi. Menurut Agrios (2005), penyakit klorosis mampu mengganggu metabolisme tanaman terutama proses fotosintesis, sehingga dapat menurunkan kualitas maupun kuantitas produksi cabai.
1.2.2 Genus Crinivirus
Crinivirus termasuk ke dalam kelompok famili Closterovirus. Closterovirus merupakan kelompok virus yang sangat beragam dan memiliki banyak spesies virus tanaman berbentuk filamen, merupakan virus RNA rantai tunggal (ssRNA viruses). Umumnya virus-virus ini menyebar melalui bantuan vektor serangga (Karasev, 2000). Closterovirus terdiri dari tiga genus, yaitu Closterovirus, Crinivirus dan Ampelovirus, yang memiliki vektor berbeda. Closterovirus disebarkan oleh Aphid, Crinivirus disebarkan oleh vektor whitefly dan Ampelovirus dengan vektor mealybug (Martelli et al. 2002).
2.2.2.1 Karakter molekuler Crinivirus
Genus Crinivirus memiliki virion lebih pendek dari 1000 nm dan memiliki dua variasi panjang, yaitu 650-850 nm dan 700-900 nm. Genomnya linier, positif sense, ssRNA dengan ukuran 15.3-19 kb, terbagi menjadi 2 molekul, dimana keduanya berfungsi untuk proses infeksi dan pemisahan pada saat pembentukan kapsid (Gambar 2.1). Ukuran CP dari anggota Crinivirus diketahui sama, berkisar antara 28-33 kDa, akan tetapi ukuran CPd bisa lebih besar, mencapai 80 kDa. RNA-1 dari Lettuce infectious yellow virus (LIYV) adalah bicitronic yang
mengkode protein yang berhubungan dengan replikasi (ORF1) dan sebuah trans peningkat akumulasi RNA-2 (ORF2) (Yeh et al. 2000). RNA-2 memiliki 7 ORF dan mengandung 5 gen yang mencirikan famili, akan tetapi hal ini berbeda dengan genus Closterovirus karena penyisipan dari gen yang sangat kecil (ORF4) pada bagian up stream dari gen CP. Semua anggota dari genus Crinivirus, ORF CPd letaknya di bagian down stream dari gen CP. Beberapa contoh virus anggota genus Crinivirus adalah LIYV, Lettuce chlorosis virus (LCV) dan Potato yellow vein virus (PYVV) (Martelli et al. 2002).
Gambar 2.1. Struktur genom dari Lettuce infectious yellows virus (LIYV), tipe spesies dari genus Crinivirus (Martelli et al. 2002)
Keterangan :
PRO: papain-like protease; MTR: methyltransferase; HEL: helicase; RdRp: RNA polymerase, HSP70: heat-shock-related protein; CP: coat protein; CPd: divergent coat protein analogue (Martelli et al. 2002).
1.2.2.2Gejala infeksi Crinivirus
Genus Crinivirus melalui salah satu spesiesnya yaitu Beet pseudo-yellows
virus (BPYV) adalah virus yang pertama kali ditemukan berasosiasi dengan gejala
kuning atau klorosis pada mentimun (Duffus, 1965). Boubourakas et al. (2006) melaporkan daun mentimun yang terinfeksi BPYV memperlihatkan gejala menguning pada daun dengan tulang daun tetap hijau dan rapuh, posisi daun yang terinfeksi biasanya berada di bagian tengah atau bawah. Gejala tersebut biasanya dikaitkan dengan kekurangan unsur hara. Saat ini BPYV dilaporkan terdapat di
seluruh dunia dan diketahui mempunyai kisaran inang luas (Wisler et al. 1998).
Virus ini dapat ditularkan secara semipersisten oleh Trialeurodes vaporariorum
(Hemiptera : Aleyrodidae) yang dikenal dengan nama kutukebul (whitefly). Selain BPYV, Cucurbit yellow stunting disorder virus (CYSDV) juga dilaporkan berasosiasi dengan penyakit klorosis atau kuning pada mentimun. Gejala infeksi CYSD mirip dengan infeksi BPYV (Lecoq et al. 1994), tetapi Cucurbit yellow
stunting disorder virus (CYSDV) ditularkan secara semipersisten oleh Bemisia
tabaci biotipe A dan B (Perring et al. 1993), dan kisaran inangnya terbatas pada
famili Cucurbitaceae. 2.2.3 Genus Begomovirus
Begomovirus merupakan salah satu genus dari famili Geminiviridae. Famili Geminiviridae adalah salah satu famili terbesar virus tanaman yang terdiri dari 209 spesies. Anggota famili Geminiviridae ditemukan di daerah tropis hingga subtropik dan menginfeksi inang dengan kisaran luas termasuk tanaman hias, pangan dan gulma (Fauquet et al. 2005). Partikel Geminiviridae berada dalam jaringan floem tanaman dan terakumulasi di dalam inti sel jaringan floem yang terinfeksi. Berdasarkan strukur genom, serangga vektor, dan kisaran tanaman inangnya, Geminiviridae dikelompokkan menjadi empat genus yaitu Topocuvirus, Curtovirus, Mastrevirus, dan Begomovirus (Hull, 2002).
Topocuvirus adalah genus Geminiviridae yang memiliki genom yang mirip dengan Curtovirus, tetapi ditularkan melalui wereng pohon Micrutalis
malleifera. Anggota Topocuvirus yaitu Tomato pseudocurly top virus (Hull,
Curtovirus merupakan salah satu dari genus Geminiviridae dengan tanaman inang dikotil, yang ditularkan oleh vektor wereng daun, dan genomnya monopartit. Anggota Curtovirus di antaranya yaitu Tobacco yellow dwarf virus
(TYDV) dengan vektor Orosius argentatus (Hemiptera: Cicadellidae) dan Beet
curly top virus (BCTV) dengan vektor Circulifer tenellus (Hemiptera:
Cicadellidae) (Hull, 2002).
Mastrevirus merupakan Geminiviridae dengan tanaman inang dari kelompok monokotil, ditularkan oleh wereng daun dan memiliki genom monopartit. Mastrevirus memiliki lebih dari 10 jenis virus yang sudah diketahui, dengan tanaman inang dari famili Graminea, yaitu Chlorosis striate mosaic virus
(CSMV), Wheat dwarf virus (WDV), Maize streak virus (MSV), dan Digitaria strak virus (DSV) (Hull, 2002).
Kelompok lain dari Geminiviridae adalah Begomovirus. Virus ini menginfeksi tanaman inang dikotil seperti tomat dan cabai yang ditularkan oleh vektor kutukebul (B. tabaci). Begomovirus memiliki genom bipartit atau
monopartit. Berdasarkan daerah asal genus tersebut anggota Begomovirus terbagi
menjadi kelompok yang berasal dari Old World (benua Eropa, Asia, Afrika) dan kelompok New World (benua Amerika). Anggota Begomovirus yang memiliki genom bipartit di antaranya African cassava mosaic virus (ACMV), Bean dwarf
mosaic virus (BDMV), Bean golden mosaic virus (BGMV), Abutilon mosaic virus
(AbMV), Cotton leaf crumple virus (CLCV), Squash leaf curl virus (SLCV),
Tomato golden mosaic virus (TGMV), Potato yellow mosaic virus (PYMV),
Indian cassava mosaic virus (ICMV), sedangkan yang memiliki genom
monopartit yaitu Tomato leaf curl virus dan Tomato yellow leaf curl virus (Navas- Castillo et al. 1999).
2.2.3.1 Karakter molekuler Begomovirus
Kelompok Begomovirus memiliki genom asam nukleat deoksiribonukleat dalam bentuk utas tunggal (single-stranded deoxyribosa nucleic acid atau ss DNA) berukuran sekitar 2,6-2,8 kb (Tsai et al. 2006). Bentuk partikel Begomovirus yaitu berbentuk sirkuler dengan partikel kembar (germinate), yang dalam keadaan tunggal umumnya berdiameter 18 - 20 nm dan sebagian besar virus ini terdapat dalam keadaan berpasangan dengan ukuran 20 x 30 nm. Protein selubung masing-masing partikel mengandung 22 kapsomer dengan lima subunit protein berukuran 30.3 kDa (masing-masing 260 asam amino). Basa nukleotida DNA-A dan DNA-B berbeda, kecuali pada daerah common region berukuran 200 nukleotida yang identik pada kedua DNA. Common region mencakup struktur
stem loop yang mengandung nonanukleotida TAATATTAC dan bersifat
conserved pada genom semua genus dari famili Geminiviridae (Hatta dan Francki,
1979).
Komponen DNA-A mengkode lima atau enam protein, yaitu semua faktor virus yang dibutuhkan untuk mengatur ekspresi gen, replikasi genom, dan penularan serangga diantara inang. DNA-B mengkode dua protein yang terlibat dalam pergerakan di dalam sel dan antar sel dalam jaringan tanaman inang. Tetapi, terdapat beberapa Begomovirus hanya memiliki genom tunggal yang mengkode enam protein dan berukuran ~3 kb. Walaupun hanya memiliki genom
tunggal, genom tersebut sama dengan komponen DNA-A dari Begomovirus bipartit dan mengandung semua informasi genetik yang cukup untuk menyebabkan infeksi sistemik dan menginduksi gejala tertentu (Rojas et al. 2005; Mansoor et al. 2006).
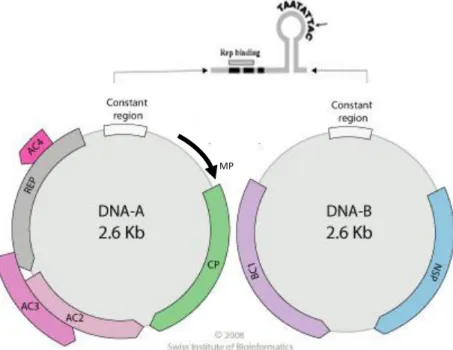
Gambar 2.2. Organisasi genom DNA-A dan DNA-B Begomovirus
Keterangan : DNA-A memiliki enam open reading frame (ORF), yaitu CP (gen AR1; protein selubung, CP) dan MP (gen AR2; protein untuk perpindahan virus, MP) pada salah satu untai; REP (gen AL1; protein replikasi, Rep); AC2 (gen AL2; protein activator transkripsi, TrAP); AC3 (gen AL3, peningkat replikasi, REn) dan AC4 (gen AL4; protein AC4) pada untai komplementer. DNA-B mengandung 2 protein pengkode ORF yang terlibat dalam perpindahan virus, yaitu NSP (gen BL1; protein selubung inti) pada salah satu untai dan BC1 (gen BL1; protein untuk perpindahan virus) pada untai komplementer (Fauquet et al. 2005; Seal et al. 2006).
Proses replikasi Begomovirus terjadi pada nukleus sel tanaman inang dengan kombinasi proses rolling circle replication dan recombination mediated
replication. Mekanisme ini membentuk DNA utas ganda intermediate dan
replicative form (RF) yang selanjutnya diubah menjadi fragmen DNA sirkuler.
DNA utas ganda intermediate di dalam sel tanaman terinfeksi menyediakan protein yang dibutuhkan untuk mengawali replikasi dan pengambilan enzim replikasi inang. Gen AC1 (Rep) berperan sebagai faktor inisiasi yang mengenali daerah pengenalan dan pembelahan atau ligasi DNA untuk memulai dan mengakhiri proses rolling circle replication. Gen C3 memfasilitasi akumulasi DNA virus dengan memodifikasi aktivitas C1 dan/atau menambah pengambilan enzim replikasi inang (Alberter et al. 2005).
2.2.3.2 Gejala infeksiBegomovirus
Begomovirus menyebabkan berbagai variasi gejala pada tanaman yang berasal dari famili berbeda. Gejala infeksi Squash leaf curl virus (SLCV) pada
Cucurbita moschata, C. pepo, dan C. maxima berupa keriting pada daun hingga kerdil. Jaringan diantara tulang daun menjadi belang dan berwarna hijau. Bunga tidak dapat berkembang atau membentuk buah, atau buah berukuran lebih kecil dan mengkerut. Virus ini menginduksi gejala mosaik hijau dengan merusak tulang daun sehingga daun menjadi berpilin (Cohen et al. 1983).
Gejala infeksi Tomato yellow leaf curl virus (TYLCV) pada tanaman tomat berupa reduksi ukuran daun, daun mengeriting, kerusakan yang berasosiasi dengan klorosis interveinal, dengan atau tanpa gejala menguning, dan tanaman kerdil secara keseluruhan. Ketika infeksi terjadi pada tahap awal pertumbuhan, tanaman menjadi kerdil, bunga yang terbentuk gugur, dan tidak dapat menghasilkan buah yang baik. Gejala yang sama juga terjadi pada Datura stramonium, Nicotiana glutinosa dan N. tabacum. Tomato yellow leaf curl virus
(TYLCV) juga menyebabkan gejala vein clearing pada tanaman Solanum nigrum
setelah masa inkubasi 23-25 hari (Al-ani et al. 2011).
Begomovirus lain yaitu Melon leaf curl virus pada tanaman selada
(Lactuca sativa) menyebabkan gejala klorosis ringan hingga parah, daun memerah
atau terbentuk bercak, dan belang hijau ketika ditularkan pada tanaman selada sehat. Gejala yang parah tampak pada tanaman kacang panjang, labu, semangka, dan zucchini yaitu berupa daun keriting dan belang (mosaik). Gejala yang lebih ringan yaitu daun keriting ringan, vein clearing, dan belang ringan tampak pada tanaman cantaloupe, melon, dan mentimun (Brown dan Nelson, 1986). Gejala lain dihasilkan oleh Tomato leaf curl virus (TLCV) pada tanaman terung berupa mosaik kuning dan belang. Penularan TLCV pada tanaman tomat menyebabkan gejala daun keriting dan menggulung ke bawah (Pratap et al. 2011).
2.3 Deteksi dan Identifikasi Virus Secara Molekuler
Deteksi virus penginduksi gejala kuning secara konvensioal dapat dilakukan melalui pengamatan gejala, uji penularan dengan vektor dan pengamatan partikel secara mikroskopik dengan mikroskop elektron. Virus kuning pada jaringan tanaman biasanya berada dalam konsentrasi rendah sampai sedang sehingga memerlukan cara deteksi yang peka seperti uji molekuler dengan teknik Polymerase Chain Reaction (PCR).
2.3.1 Polymerase Chain Reaction (PCR)
Pendekatan secara molekuler telah banyak dilakukan untuk menentukan infeksi virus kuning yang terjadi di lapang dan mengidentifikasi virus kuning secara umum. Reaksi berantai polymerase (Polymerase Chain Reaction, PCR)
adalah suatu metode enzimatis untuk melipatgandakan secara eksponensial suatu sikuen nukleotida tertentu dengan cara in vitro. Awal perkembangannya metode ini hanya digunakan untuk melipatgandakan molekul DNA. Penggunaan PCR merupakan tenik yang sangat sensitif dan spesifik untuk mendeteksi dan identifikasi patogen tanaman. Sensitifitas tersebut membuatnya dapat digunakan untuk melipatgandakan satu molekul DNA (Yuwono, 2006).
Empat komponen utama pada proses PCR adalah (1) DNA cetakan, yaitu fragmen DNA yang akan dilipatgandakan, (2) oligonukleotida primer, yaitu suatu sikuen oligonukleotida pendek (15-25 basa nukleotida) yang digunakan untuk mengawali sintesis rantai DNA, (3) deoksiribonukleotida trifosfat (dNTP), yang terdiri atas dATP, dCTP, dGTP, dTTP, dan enzim DNA polymerase, yaitu enzim yang melakukan katalisis reaksi sintesis rantai DNA. Komponen lain yang juga penting adalah senyawa buffer (Yuwono, 2006).
Reaksi pelipatgandaan suatu fragmen DNA dimulai dengan melakukan denaturasi DNA template (cetakan) sehingga rantai DNA yang berantai ganda
(double stranded) akan terpisah menjadi rantai tunggal (single stranded).
Denaturasi DNA dilakukan dengan menggunakan panas (95o C) selama 1-2 menit, kemudian suhu diturunkan menjadi 55o C sehingga primer akan “menempel” (anneling) pada cetakan yang telah terpisah menjadi rantai tunggal. Primer akan membentuk jembatan hidrogen dengan cetakan pada daerah sikuen yang komplementer dengan sikuen primer. Suhu 55o C yang digunakan untuk penempelan primer pada dasarnya merupakan kompromi (suhu bisa diturunkan atau dinaikkan). Amplifikasi akan lebih efisien jika dilakukan pada suhu yang
lebih rendah (37o C), tetapi biasanya akan terjadi mispriming yaitu penempelan primer pada tempat yang salah. Sedangkan pada suhu yang lebih tinggi (55o C), spesifisitas reaksi amplifikasi akan meningkat, tetapi secara keseluruhan efisiensinya akan menurun (Yuwono, 2006).
Primer yang digunakan dalam PCR ada dua yaitu oligonukleotida yang mempunyai sikuen yang identik dengan salah satu rantai DNA cetakan pada ujung 5’-fosfat, dan oligonikleotida yang kedua identik dengan sikuen pada ujung 3’-OH rantai DNA cetakan yang lain. Proses annealing biasanya dilakukan selama 1-2 menit. Setelah dilakukan annealing oligonukleotida primer dengan DNA cetakan, suhu inkubasi dinaikkan menjadi 72o C selama 1,5 menit. DNA polymerase pada suhu 72o C akan melakukan proses polimerasi rantai DNA yang baru berdasarkan informasi yang ada pada DNA cetakan. Setelah terjadi polimerasi, rantai DNA yang baru akan membentuk jembatan hidrogen dengan DNA cetakan. DNA rantai ganda yang terbentuk dengan adanya ikatan hidrogen antara rantai DNA cetakan dengan rantai DNA baru hasil polimerasi selanjutnya akan didenaturasi lagi dengan menaikkan suhu inkubasi menjadi 95o C. Rantai DNA yang baru tersebut selanjutnya akan berfungsi sebagai cetakan bagi reaksi polimerasi berikutnya. Rekasi-reaksi tersebut akan diulangi lagi sampai 25-30 kali (siklus) sehingga pada akhir siklus akan didapatkan molekul-molekul DNA rantai ganda yang baru hasil polimerasi dalam jumlah yang jauh lebih banyak dibandingkan dengan jumlah DNA cetakan yang digunakan (Yuwono, 2006).
2.3.2 Reverse Transcriptase Polymerase Chain Reaction (RT-PCR)
Awalnya teknik PCR hanya digunakan untuk mengamplifikasi molekul DNA dengan menggunakan DNA sebagai bahan awal yang akan digunakan sebagai cetakan. Perkembangan lebih lanjut teknik ini memungkinkan para peneliti menggunakan molekul RNA sebagai bahan awal, yaitu dengan teknik
Reverse Transcriptase Polymerase Chain Reaction (RT-PCR). Oleh karena PCR
tidak dapat dilakukan dengan menggunakan RNA sebagai cetakan maka terlebih dahulu dilakukan proses transkripsi balik (reverse transcriptase) terhadap molekul mRNA sehingga diperoleh molekul cDNA (complementary DNA). Teknik RT-PCR memerlukan enzim transcriptase balik. Enzim transcriptase balik adalah enzim DNA polymerase yang menggunakan molekul RNA sebagai cetakan untuk menyintesis molekul DNA (cDNA) yang komplementer dengan molekul RNA tersebut (Yuwono, 2006).
2.4 Analisis Filogenetika Molekuler
Analisis filogenetika molekuler merupakan proses bertahap untuk mengolah data sikuen DNA atau protein sehingga diperoleh suatu hasil yang menggambarkan estimasi mengenai hubungan evolusi suatu kelompok organisme. Paling sedikit ada tiga tahap penting dalam analisis filogenetika molekuler, yaitu
sequence alignment, rekonstruksi pohon filogenetika, dan evaluasi pohon
filogenetika dengan uji statistik (Hidayat dan Pancoro, 2006). 2.4.1 Sequences Alignment
Tujuan utama dari tahap ini adalah untuk menentukan apakah satu sikuen DNA atau protein adalah homolog dengan yang lainnya. Alignment yang
melibatkan dua sikuen yang homolog disebut pairwise alignment, sedangkan yang melibatkan banyak sikuen yang homolog disebut multiple alignment. Keberhasilan analisis filogenetika sangat tergantung kepada akurasi proses alignment (Hidayat dan Pancoro, 2006).
2.4.2 Rekonstruksi Pohon Filogenetika
Metode dalam membangun suatu pohon filogenetika dengan menggunakan karakter molekuler, sikuen DNA misalnya, dibagi menjadi empat kelompok utama, yaitu distance method (DM), likelihood method (LM), Bayesian
method (BM), dan parsimony method (PM). Prinsip DM adalah jumlah perbedaan
nukleotida antara dua sikuen DNA menunjukkan jarak evolusi yang terjadi. Jarak evolusi dihitung untuk semua pasang sikuen DNA dan sebuah pohon filogenetika direkonstruksi dari jarak atau perbedaan pasangan basa nukleotida tersebut dengan menggunakan kriteria least square, minimum evolution, neighbor joining, dan distance measure. Sebelum digunakan untuk merekonstruksi pohon filogenetika, LM telah lama digunakan untuk data frekuensi gen. Prinsip dari LM ini adalah bahwa perubahan-perubahan diantara semua basa nukleotida adalah sebanding. Masalah serius dari metode ini adalah waktu perhitungan yang lama, walaupun telah dikembangkan algoritma baru yang dianggap dapat mempercepat proses perhitungan. Untuk BM, pada dasarnya adalah sama dengan LM, hanya berbeda dalam penghitungan distribusi prior untuk membangun pohon filogenetika. Salah satu metode untuk menghitung distribusi prior adalah metode MCMC (Markov
chain Monte Carlo). Parsimony method (PM) beranggapan bahwa perubahan
asam amino yang berbeda dan berbeda dengan ketiga metode yang lain, dalam PM hanya jumlah perubahan basa nukleotida atau asam amino yang terkecil yang dapat memberikan penjelasan yang baik mengenai keseluruhan proses evolusi yang terjadi. Kemudian, topologi pohon yang dipilih sebagai yang terbaik adalah yang mengalami jumlah perubahan yang paling kecil (Hidayat dan Pancoro, 2006).
2.4.3 Evaluasi pohon filogenetika
Evaluasi pohon filogenetika berkaitan dengan uji reliabilitas dari sebuah pohon dan uji topologi antara dua atau lebih pohon yang berbeda berdasarkan set data yang sama. Banyak metode telah dikembangkan untuk menguji reliabilitas, diantaranya yaitu interior branch test (IB) dan Felsentein’s bootstrap test (FB). Prinsip IB adalah estimasi pohon dengan menguji reliabilitas setiap cabang sebelah dalam (interior branch). Sedangkan pada FB, reliabilitas diuji dengan menggunakan metode Efron’s bootstrap. Sebuah set dari site basa nukleotida dicuplik secara acak yang dilakukan secara berulang, kemudian dilakukan konsensus, sehingga hanya satu pohon filogenetika yang dihasilkan. Karena pada dasarnya pola perubahan basa nukleotida sangat rumit dan sering berubah sejalan dengan waktu evolusi, metode FB sangat baik digunakan dalam mengevaluasi pohon filogenetika (Hidayat dan Pancoro, 2006).
2.5 Program Komputer
Saat ini terdapat dua program komputer utama yang sering digunakan untuk merekonstruksi pohon filogenetika, yaitu PAUP dan MrBayes. PAUP
banyak program untuk menyelesaikan berbagai aspek dalam analisis filogenetika molekuler. Paket tersebut terdiri dari program untuk menyusun format data sikuen DNA atau protein, untuk merekonstruksi pohon filogenetika (berdasarkan metode parsimoni), dan untuk evaluasi pohon filogenetika. Perlu dicatat bahwa program PAUP dapat me-run set data selain molekuler, misalnya morfologi. Program PAUP dapat dijalankan baik dengan menggunakan komputer ber-OS (operating system) Macintosh dan Windows. Seperti program PAUP, MrBayes merupakan program multifungsi untuk merekonstruksi pohon filogenetika (berdasarkan metode Bayesian). Tetapi program ini dibuat khusus hanya untuk set data molekuler. Program MrBayes dapat diinstal pada berbagai macam OS (operating
system) komputer: Macintosh, Windows, Unix, dan Linux. Untuk memperoleh
hasil yang optimum, komputer harus memiliki speed yang tinggi dan memori penyimpan data yang besar (Hidayat dan Pancoro, 2006).