1
AKTIVITAS SITOTOKSIK Ocimum sanctum L
PADA SEL KANKER KOLON WiDr
Sari Haryanti dan Katno
Balai Besar Penelitian dan Pengembangan Tanaman Obat dan Obat Tradisional Badan Litbang Kesehatan, Kementerian Kesehatan RI sari.haryanti@gmail.com; HP. 08122646342 ABSTRAK
Ocimum sanctum L (kemangi) adalah salah satu tanaman dengan kandungan asam
ursolat. Asam ursolat merupakan senyawa kimia golongan pentasiklik triterpenoid yang terdapat pada tanaman. Beberapa penelitiaan menunjukkan bahwa asam ursolat memiliki potensi untuk dikembangkan sebagai senyawa antikanker karena kemampuannya dalam menghambat beberapa tahapan pada karsinogenesis dan didukung dengan keberadaannya yang tersebar luas pada banyak tanaman. Penelitian ini bertujuan untuk mengetahui profil KLT dan aktivitas sitotoksik in vitro ekstrak etanolik dan fraksi herba kemangi pada sel kanker kolon WiDr.
Ekstraksi dilakukan dengan maserasi menggunakan penyari etanol 96% selama 3x24 jam; maserat dikeringkan dengan rotary evaporator hingga diperoleh ekstrak kering. Identifikasi asam ursolat dengan KLT menggunakan fase diam silika gel, fase gerak kloroform‐aseton (9:1) dan penampak bercak asam sulfat 10% dalam etanol. Pengamatan dilakukan pada sinar tampak. Aktivitas sitotoksik ekstrak dan fraksinya dengan metode MTT assay untuk mendapatkan nilai IC50. Ekstrak aktif difraksinasi
berturut‐turut menggunakan heksan, kloroform, etilasetat dan air.
Profil KLT ekstrak etanol kemangi memperlihatkan adanya bercak dengan Rf dan warna yang sama dengan bercak standar asam ursolat (warna merah muda; Rf 0.65). Uji sitotoksik ekstrak etanolik memberikan nilai IC50 85 ug/ml. Berdasarkan profil KLT
keempat fraksi, hanya fraksi kloroform yang mengandung asam ursolat. Fraksi kloroform merupakan satu‐satunya fraksi yang aktif dengan nilai IC50 25 ug/ml.
Penelitian ini menunjukkan bahwa kemangi memiliki aktivitas penghambatan pertumbuhan dan menginduksi induksi kematian sel WiDr sehingga cukup potensial dikembangkan sebagai agen kemopreventif.
Kata kunci: Ocimum sanctum, fraksi, aktivitas sitotoksik, sel WiDr, kemopreventif
PENDAHULUAN
Kanker merupakan sekumpulan penyakit yang disebabkan oleh perubahan sifat normal sel yaitu sel menjadi lebih agresif, tumbuh dan membelah tanpa terkendali, karena dapat memenuhi sinyal pertumbuhannya sendiri. Sel tersebut selanjutnya memiliki kemampuan invasive (menyusup dan merusak jaringan di dekatnya) dan metastasis (menyebar ke jaringan lainnya melalui sistem pembuluh darah dan
2
limpa). Kanker berada di urutan ke dua penyebab kematian terbanyak di dunia setelah penyakit jantung. Semua organ dan bagian tubuh dapat menjadi target sel kanker. Kolon sebagai saluran terakhir pencernaan makanan juga berpotensi terkena kanker. Jumlah penderita kanker kolon berada di urutan teratas dari seluruh jenis kanker yang diderita pria dan wanita (Jemal et al., 2007). Pengembangan terapi yang komprehensif untuk mengatasi kanker kolon sangat diperlukan untuk menekan jumlah kematian penderita.
Salah satu pengembangan terapi kanker diarahkan pada terapi kombinasi antara suatu agen kemoterapi dengan senyawa kemopreventif. Salah satu pendekatan untuk menemukan senyawa kemopreventif adalah melalui eksplorasi bahan alam terutama tumbuh‐tumbuhan. Beberapa penelitian mulai diarahkan pada pengujian kombinasi bahan alam dengan agen kemoterapi untuk mengurangi terjadinya resistensi dan efek samping obat.
Bahan alam mengandung berbagai senyawa biologis yang beraksi pada sel kanker melalui mekanisme yang kompleks. Salah satu tumbuhan yang dapat dikembangkan sebagai agen kemopreventif adalah Ocimum sanctum L (kemangi). Kemangi bersifat sebagai adaptogen, di antaranya memiliki beberapa efek farmakologi seperti imunomodulator, anti‐stress, hepatoprotektif, kemopreventif, dan anti‐inflamasi. Senyawa aktif yang diketahui terdapat pada O. Sanctum L adalah flavonoids, orientin, vicenin, eugenol (1‐hydroxy‐2‐methoxy‐4‐allylbenzene), dan asam ursolat (Niture et al., 2006).
Asam ursolat diketahui memiliki aktivitas antikanker dengan menghambat peristiwa karsinogenesis, promosi kanker, induksi differensiasi sel kanker, dan angiogenesis. Aktivitas tersebut di antaranya diperantarai oleh kemampuan asam ursolat menghambat aktivasi salah satu faktor transkripsi, nuclear factor‐kappaB (NF‐κB). NF‐κB adalah salah satu protein yang meregulasi ekspresi sejumlah gen yang berperan dalam proses pembentukan kanker; termasuk gen antiapoptosis, gen yang mengatur adhesi molekul, dan gen yang mengatur siklus sel. Senyawa yang dapat menghambat aktivasi NF‐κB memiliki potensi terapetik sebagai senyawa antikanker (Shishodia et al., 2003).
Penelitian ini bertujuan untuk mengetahui profil KLT dan aktivitas sitotoksik in vitro ekstrak etanolik dan fraksi herba kemangi pada sel kanker kolon WiDr. Sel WiDr merupakan sel kanker kolon yang diambil dari jaringan epitelial seorang wanita, berupa sel adherent (melekat) dengan karakteristik antara lain resisten terhadap beberapa agen kemoterapi (Jean‐Claude et al., 1999), dan overekspresi COX‐2 (Kojima et al., 2000).
METODE PENELITIAN
Tempat dan waktu penelitian. Penelitian dilakukan di Laboratorium Parasitologi
Fakultas Kedokteran UGM.
Ekstrak etanolik dan fraksi herba kemangi (EHK). Herba kemangi diperoleh dari
3
etanol 96%. Selanjutnya ekstrak etanol cair yang didapat dikentalkan dengan rotary
evaporator, dikeringkan diatas waterbath hingga diperoleh ekstrak kering.
Fraksinasi dilakukan dengan melarutkan 10 g ekstrak aktif dalam 50 mL akuades dan dibasakan sampai pH 8 dengan penambahan amoniak, kemudian difraksinasi menggunakan heksan, kloroform, dan etil asetat menggunakan corong pisah. Fraksinasi dilakukan sebanyak 3 kali replikasi, volume penyari yang digunakan tiap kali fraksinasi adalah ± 250 mL. Hasil fraksinasi kemudian dikentalkan dengan rotary
evaporator sehingga diperoleh 4 fraksi kental, yang selanjutnya disebut fraksi
heksan, fraksi kloroform, fraksi etil asetat dan fraksi air.
Sel kanker kolon. Sel kanker kolon WiDr yang digunakan adalah koleksi
Laboratorium Parasitologi Fakultas Kedokteran Umum Universitas Gadjah Mada Yogyakarta. Kultur sel ditumbuhkan dalam media penumbuh Roswell Park Memorial
Institute (RPMI) 1640 (Gibco) yang mengandung Foetal Bovine Serum (FBS) 10% (v/v)
(Gibco), penisillin‐streptomisin 1 % (v/v) (Gibco).
Deteksi asam ursolat. Sebanyak kurang lebih 1% EHK dan 0,1% standard asam
ursolat dalam metanol ditotolkan pada lempeng KLT; kemudian dikembangkan dalam fase gerak kloroform‐aseton (9:1). Setelah batas elusi, lempeng dikeringkan dan disemprot dengan asam sulfat 10% dalam etanol hingga semua bagian lempeng terbasahi; ditunggu hingga lempeng kering. Lempeng dipanaskan dalam oven suhu 1100C selama 5 menit dan diamati pada sinar tampak. Lempeng kemudian dianalisa dengan TLC‐densitometer
Uji sitotoksik in vitro. Sejumlah 5000 sel WiDr /sumuran ditanam pada microplate 96
sumuran dan diinkubasi selama 48 jam. Setelah itu medium diganti yang baru dengan ditambahkan EHK maupun fraksi pada berbagai konsentrasi (50‐200 μg/ml) dengan co‐solvent DMSO (Sigma) dan diinkubasi pada 37ºC dalam inkubator CO2 5%
selama 48 jam. Pada akhir inkubasi, media dan ekstrak dibuang kemudian sel dicuci dengan PBS Pada masing‐masing sumuran, ditambahkan 100μl media kultur dan 10μl MTT (Sigma) 5 mg/ml. Sel diinkubasi kembali selama 4‐6 jam dalam inkubator CO2 5%, 37ºC. Reaksi MTT dihentikan dengan reagen asam isopropanol (HCl 4N
(Merck)‐isopropanol (Merck), (1:100), digoyang di atas shaker selama 10 menit. Serapan dibaca dengan ELISA reader pada panjang gelombang 595 nm.
Analisis Data. Data absorbansi pada uji sitotoksik diolah dengan regresi linier
program Excell MS Office 2007.
HASIL
Profil KLT EHK memperlihatkan adanya bercak warna merah muda pada sinar tampak dengan intensitas warna dan Rf (0,6) yang sama dengan standard asam ursolat yang digunakan.
4
Gambar 1. Profil KLT EHK (A1) dan standard asam ursolat (A2) pada pengamatan dengan sinar
tampak; B adalah profil EHK saat dianalisa dengan TLC‐densitometer
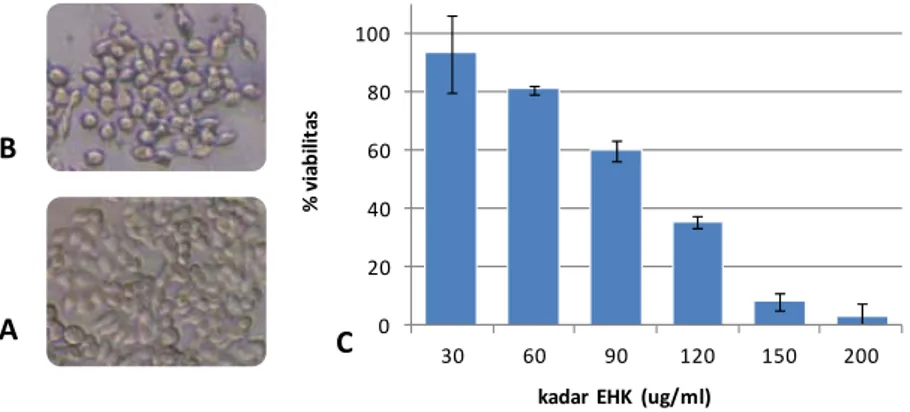
Hasil uji sitotoksik menunjukkan bahwa perlakuan EHK kadar 50‐200 µg/mL pada sel WiDr menyebabkan terjadinya perubahan morfologi dibandingkan sel tanpa perlakuan (Gambar 1). Berdasarkan morfologi serta viabilitas sel terdapat hubungan linier antara konsentrasi dan efek sitotoksik yang dihasilkan. Perubahan morfologi tersebut dimungkinkan mengarah pada kematian sel. EHK mampu menghambat pertumbuhan sel WiDr dengan IC50 sebesar 85 µg/ml.
Gambar 1. Viabilitas sel WiDr akibat perlakuan EHK. Uji dilakukan dengan menginkubasi 5x103 sel dengan EHK (50‐200 µg/mL) selama 48 jam. Terjadi perubahan morfologi pada perlakuan EHK 120 µg/mL (B) dibandingkan sel kontrol (A). Grafik C memperlihatkan adanya hubungan konsentrasi EHK terhadap persentase viabilitas sel.
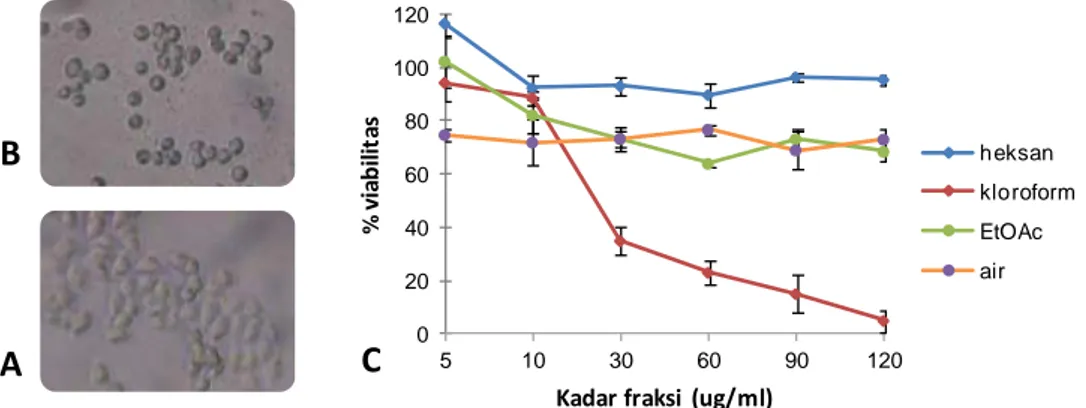
Uji sitotoksik fraksi EHK menunjukkan tidak semua fraksi memiliki aktivitas pada sel WiDr. Fraksi aktif adalah fraksi kloroform dengan IC50 25µg/mL. Profil KLT
memperlihatkan bahwa hanya fraksi kloroform yang mengandung asam ursolat. 0 20 40 60 80 100 30 60 90 120 150 200 % v iab ili tas kadar EHK (ug/ml) A B C
5
Gambar 2. Viabilitas sel WiDr akibat perlakuan fraksi EHK. Uji dilakukan dengan menginkubasi 5x103 sel dengan fraksi EHK (5‐120 µg/mL) selama 48 jam. Terjadi perubahan morfologi pada perlakuan fraksi kloroform 120 µg/mL (B) dibandingkan sel kontrol (A). Grafik C memperlihatkan hubungan konsentrasi tiap fraksi terhadap persentase viabilitas sel. PEMBAHASAN EHK memberikan hambatan pertumbuhan sel kanker kolom WIDR dengan IC50 yang
relatif kecil (85μg/ml, kurang dari 100μg/ml) sehingga cukup potensial untuk dikembangkan sebagai alternatif agen kemopreventif. Di antara keempat fraksi yang digunakan, hanya fraksi kloroform yang memiliki aktifitas penghambatan pertumbuhan sel. Berdasarkan profil KLT hanya fraksi kloroform yang memperlihatkan adanya asam ursolat. Hal tersebut menunjukkan bahwa senyawa yang bertanggung jawab terhadap aktifitas sitotoksik kemangi adalah asam ursolat. Shishodia et al., 2003, menunjukkan bahwa asam ursolat mampu menurunkan aktivitas NF‐κB melalui penghambatan IκBα kinase dan fosforilasi p65 yang berkorelasi dengan penurunan ekspresi cyclin D, COX‐2, dan MMP 9. NF‐κB berperan dalam proses kemoresistensi dengan cara aktivasi protein Myc sebagai perantara aktivasi transkripsi cyclin A dan D. Hal ini menyebabkan apoptosis terabaikan dan siklus sel terus berlanjut. Stimulasi NF‐κB dapat melalui death receptors kemudian berinteraksi dengan gen target seperti IAPs dan menghambat jalur caspase (Schimmer, 2004); atau melalui sinyal proliferasi melewati jalur Akt sehingga mengakibatkan peningkatan ekspresi protein antiapoptosis. Penelitian yang lebih mendalam perlu dilakukan untuk mengkaji peran EHK dan relevansinya dengan penghambatan aktivitas NF‐κB sehingga memberikan efek sitotoksik. KESIMPULAN Ekstrak etanolik herba kemangi (Ocimum sanctum L.) memiliki efek sitotoksik dengan nilai IC50 85µg/mL. Fraksi aktif adalah kloroform dengan nilai IC50 25µg/mL. Senyawa
yang bertanggung jawab terhadap aktifitas tersebut adalah asam ursolat. 0 20 40 60 80 100 120 5 10 30 60 90 120 % vi ab ili tas Kadar fraksi (ug/ml) heksan kloroform EtOAc air A B C
DAF Agg Che Dau Dha Jean King Koji Leig Nitu Sch She Shis FTAR PUSTA garwal, B.B. Grail in C 1: 25‐52. en, Y.H., Ch Wu, Y.C. Hedyotis ucas, H., G Chemopr Involved, 6: 429–43 armananda, Institute E., Murra Cancer J C n‐Claude, B Leyland‐J Huma Therapeu g, R.J.B., 200 ma, M., M Tanaka, M In A Colo 19(9): 122 gh, M.J., 20 Nutrition ure, SK., Ra the MGM kanker ce plants. IN immer, A.D into Clinic hata, M.F. cervical c shodia, S., Inhibits N Down‐Re D1. Cance AKA , Sethi, G., Cancer Prev ang, F.R., W ., 2005, N biflora. Pla Garcea, G. revention o and Eviden 39. , S. 2004. O for Traditio ay, T., Jiaq Clin., 57: 43 .J., Mustafa ones, B., 19 an Tumor C utics, 288 (2 00, Cancer B orisaki, T., M., 2000, L n Carcinom 25‐1231 003, Health Noteworth o, US., Srive MT repair p
ells by eth
NTERNATION D. 2004 Inh cal Practice 2005. Re cancer cells. Majumdar, Nuclear Fac gulation of er Researh. Nair, A. an vention and Wu, C.C., Ye ew Cytotox anta Med.7 , Neal, C. of Pancreati nce for the Oldenlandia onal Medici
uan Xu and 3‐66 a, A., Watso 999, Tetraze Cell Lines, T 2): 484‐489. Biology, 2nd Izuhara, K. Lipopolysacc ma Cell Line Benefits o hy, 6(1): arti enugopal K rotein: Aug hanolic and NAL JOURNA hibitor of A . Review. Ca l/Nuclear f . Review. Ca , S., Baner tor‐κBα Kin f Cyclooxyge 63, 4375‐4 6 nd Ichikawa d Therapy. en, M.H., L xic 6‐Oxyg 2: 75‐78. .P., Manso c Cancer: A Potential f and Scutel ne, Portlan d Michael on, A.J., Dam epinones ar The Journal d edition, Pe ., Uchiyama charide Inc Through Nu of Grape Se cle 5. K., 2006, Ch gmented ex aqueous e NAL OF ONCO poptosis Pr ancer Resea factor‐kapp ancer Cell In rjee, S. and nase and p6 enase 2, M 383. a H. 2006. Current Sig iaw, C.C., H enated 8,9 on, M.M., A Review o for Chemop laria Antito d, Oregon.J J.T. 2007. mian, Z., Va re Equally C l Of Pharma earson Educ a, A., Mats
reases Cycl uclear Facto eed Proanth emopreven xpression in extracts of OLOGY 29: roteins: Tra arch 64:718 a B apopt nternationa d Aggarwa 65 Phospho atrix Metal Nuclear Fa nal Transdu Huang, H.C. 9‐Hedyotisc and Berry f the Mole prevention, oxin and An Jemal, A., S Cancer Sta silescu, D., Cytotoxic to acology An cation Ltd., unari, Y., K o‐Oxygenas or‐κB Activa hocyanidin ntative strat n human ly f several In 1269‐1278 anslating Ba 83‐7190. tosis pathw l 5:10‐23. l, B.B. 200 orylation: C loproteinas ctor‐κB: A uction Ther , Kuo, Y.H. one A‐C, f y, D.P., 2 cular Pathw Pancreatol nticancer He iegel, R., W atistic 2007 Chan, T.H., o Mer+ and d Experime London. Katano, M., se‐2 Expres ation, Onco Extract (GS tegies targe mphocytes ndian medic asic Knowle ways in hu 03. Ursolic Correlation se 9, and Cy Holy rapy. and from 006, ways logy; erbs. Ward, , CA and Mer ental and ssion ogen, SPE), eting and cinal edge man acid with yclin
7
Simstein, R., Burow, M., Parker, A., Weldon, C., and Beckman, B., 2003, Apoptosis, Chemoresistance, and Breast Cancer: Insights from the WIDR Cell Model System, Exp Biol Med, 228:995–1003.
Srivastava, R.K., Sasaki, C.Y., Hardwick, J.M. and Longo, D.L. 1999. Bcl‐2‐mediated Drug Resistance: Inhibition of Apoptosis by Blocking Nuclear Factor of Activated T Lymphocytes (NFAT)‐induced fas Ligand Transcription. The Journal of
Experimental Medicine 190 (2):253‐265.
Wickenden, J.A., Clarke, M.C.H., Rossi, A.G., Rahman, I., Faux,, S.P., Donaldson, K, and MacNee, W., 2003, Cigarette Smoke Prevents Apoptosis through Inhibition of Caspase Activation and Induces Necrosis, Am. J. Respir. Cell Mol. Biol., 29:562–570.
Wyllie, A., Donahue, V., Fischer, B., Hill, D., Keesey, J., and Manzow, S., 2000, Cell