xix INTISARI
Tanaman laut alga merupakan salah satu kekayaan laut Indonesia yang sangat potensial, namun belum dimanfaatkan secara maksimal baik sebagai nutrisi makanan maupun agen biomedis. Salah satunya, alga merah Laurencia yang cukup melimpah di perairan Indonesia. Alga merah mengandung mikronutrien polifenol alga yang dikenal sebagai florotanin. Senyawa ini berupa unit-unit floroglusinol (1,3,5-trihidoksibenzena) yang berbeda dari tumbuhan terestrial.
Tujuan penelitian ini adalah mendapatkan florotanin kasar dari alga merah Laurencia papillosa (Forskal) Graville serta menetapkan kadar florotanin dalam fraksi etil asetat alga tersebut. Isolasi dilakukan menggunakan metode sokhletasi dengan pelarut metanol. Ekstrak kental yang diperoleh kemudian difraksinasi dengan kloroform, akuades, dan etil asetat untuk mendapatkan florotanin kasar.
Konsentrasi polifenol total dalam florotanin kasar ditetapkan secara spektrofotometri dengan metode Folin-Ciocalteau, menggunakan standar floroglusinol yang dibuat seri konsentrasi baku 0,5 ; 1,0 ; 2,0 ; 3,0 ; 4,0 ; 5,0 ; dan 6,0 ppm dalam pelarut aseton 75 %. Standar floroglusinol dan sampel dibaca pada panjang gelombang maksimum 750,1 nm. Konsentrasi polifenol total dalam fraksi etil asetat alga merah yang didapat adalah 10,55-11,21 mg PGE (Phloroglucinol Equivalent)/g sampel.
Kata kunci : florotanin, polifenol, alga merah Laurencia papillosa, metode Folin-Ciocalteau
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xx ABSTRACT
Seaweed algae is one of Indonesian’s sea treasures that really potential, but still haven’t been used maximally as well yet, either as food nutrition or biomedical agents. One of them is red algae Laurencia that abundant enough in Indonesian waters. The Red algae contains algae polyphenols micronutrient called phlorotannins. This compound is derived from phloroglucinol units (1,3,5-trihydoxybenzene), that is differ from terrestrial plant polyphenols.
The goals of this study is for getting crude phlorotannin from red algae
Laurencia papillosa (Forskal) Graville and determining phlorotannin concentration in ethyl acetate fractional of alga that mentioned. Isolation have been done by soxhletation method with methanol solvent. The viscous extract that was gained, than was fractionated with chloroform, aquadest and ethyl acetate to gain crude phlorotannin.
Concentration of total polyphenols in crude phlorotannin was determined by spectrophotometric with Folin-Ciocalteau method. Using phloroglucinol standard that was made in calibration series 0.5 ; 1.0 ; 2.0 ; 3.0 ; 4.0 ; 5.0 and 6.0 ppm with acetone 75 % solvent. The phloroglucinol standard and sample was scanned at 750.1 nm the maxima wavelength. Concentration of total polyphenols in ethyl acetate fractional of red algae has been investigated was 10.55-11.21 mg PGE (Phloroglucinol Equivalent)/g sample.
PENETAPAN KADAR FLOROTANIN DALAM FRAKSI ETIL ASETAT ALGA MERAH (Laurencia papillosa (Forskal) Graville) DENGAN
METODE KOLORIMETRI FOLIN CIOCALTEAU
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Ilmu Farmasi
Oleh:
Hendry Kurniawan
NIM: 048114086
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2008
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
ii
PENETAPAN KADAR FLOROTANIN DALAM FRAKSI ETIL ASETAT ALGA MERAH (Laurencia papillosa (Forskal) Graville) DENGAN
METODE KOLORIMETRI FOLIN CIOCALTEAU
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Ilmu Farmasi
Oleh:
Hendry Kurniawan
NIM: 048114086
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iii
Penelitian untuk Skripsi
PENETAPAN KADAR FLOROTANIN DALAM FRAKSI ETIL ASETAT ALGA MERAH (Laurencia papillosa (Forskal) Graville) DENGAN
METODE KOLORIMETRI FOLIN CIOCALTEAU
yang diajukan oleh :
Hendry Kurniawan
NIM: 048114086
telah disetujui oleh :
Pembimbing
Ign. Yulius Kristio Budiasmoro, M.Si. Tanggal : 12 November 2007
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
v
Roma 11:33 O, Alangkah dalamnya kekayaan, hikmat dan pengetahuan Allah! Sungguh tak terselidiki keputusan-keputusan-Nya dan sungguh tak terselami jalan-jalan-Nya!
Karya ini kupersembahkan
untuk :
Tuhan Yesus Kristus
Sahabat,
Penghibur yang tak pernah
membiarkan aku ‘down’...
Papa-Mama tercinta
Sebagai ungkapan rasa
hormat dan baktiku
Meimeiku tercinta
Sahabat-sahabatku
serta almamaterku
Segenap dosen dan
karyawan USD
Semua yang sedang
membaca skripsi ini...
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
vi
LEMBAR PERNYATAAN PERSETUJUAN
PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma :
Nama : Hendry Kurniawan
Nomor Mahasiswa : 048114086
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul :
“Penetapan Kadar Florotanin dalam Fraksi Etil Asetat Alga Merah (Laurencia papillosa (Forskal) Graville) dengan Metode Kolorimetri Folin Ciocalteau”
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, me-ngalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di Internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenarnya.
Dibuat di Yogyakarta
Pada tanggal : 25 Februari 2008
Yang menyatakan
vii
PRAKATA
Alleluia!! Terpujilah Tuhan Yang Maha Esa atas berkat kasih dan
karunia-Nya sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi
yang berjudul “Penetapan Kadar Florotanin dalam Fraksi Etil Asetat Alga
Merah (Laurencia papillosa (Forskal) Graville) dengan Metode Kolorimetri
Folin Ciocalteau”. Penelitian ini barulah langkah awal perjalanan panjang
penelitian tentang alga di bidang kosmetik dan farmasi. Skripsi ini disusun guna
memenuhi salah satu syarat untuk mendapatkan gelar Sarjana Farmasi (S. Farm.)
pada Fakultas Farmasi Universitas Sanata Dharma.
Dalam penulisan skripsi ini, penulis telah banyak mendapatkan bantuan
baik materiil, moral maupun spiritual dan dukungan yang berupa bimbingan,
dorongan, sarana maupun fasilitas dari berbagai pihak. Pada kesempatan ini,
penulis ingin menyampaikan ucapan terima kasih kepada:
1. Rita Suhadi, M. Si., Apt. selaku Dekan Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta.
2. Ign.Y. Kristio Budiasmoro,M.Si. selaku dosen pembimbing yang telah
meluangkan waktu dan tenaga untuk memberikan bimbingan dan saran
mulai dari penyusunan proposal hingga diselesaikannya skripsi ini.
3. Prof. Dr. Sudibyo Martono, M.S., Apt. dan Erna Tri Wulandari, M.Si.,
Apt. selaku dosen penguji yang telah meluangkan waktu untuk
memberikan masukan, saran selama penelitian.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
viii
4. Dra. A. Nora Iska H., M.Si., Apt. selaku dosen penanggungjawab proyek
penelitian payung dan ikut menemani selama penelitian, Abdul Rohman,
S.F., Apt. (UGM) dan Christine Patramurti, M.Si., Apt. atas segala
masukan, kepedulian saat penelitian mengalami permasalahan.
5. Dr. Sabikis, Apt. yang telah membantu menerjemahkan reaksi Folin yang
terbenam lama dalam sebuah buku tua Harry Auterhoff & Knabe.
6. Prof. Roman Przybylski (University Drive Lethbridge), Dr.
Jéssica de Matos Nunes (Universidade Federal do Rio Grande
do Sul) yang mau berbagi pengalaman riset polifenol yang luar biasa.
7. Rekan tim peneliti, “Algae crew” (Elsa, Angel, Dewi, Andri, Fani, Dipta)
yang mendukung, menyemangati selama penelitian dan penyusunan
skripsi ini.
8. Teman-teman tim peneliti Teh, Wortel, Jagung, Pulveres yang menambah
keceriaan selama di laboratorium.
9. Teman-teman FST’04, kelas B, terutama kelompok D4 (Ratna-Rizky,
Widya), “The Dream Team” (Boriz, Yusak, Peter, Rike, Fani) yang
kompak habis, dan selalu mengalami hal aneh selama praktikum.
10.Segenap staf laboran terutama di lantai IV dan kepala gudang (mas Otok)
atas masukan, bantuan, kebersamaan, dan kerjasamanya selama penelitian.
11.Teman Reef’ers, bapak gembalaku pdt. Drs. Yos Hartono, S.Th., teman
pastori: Om Edwin, Tony, Marihot, Pa Ce, mbak Yuni, kak Yetty. Serta
ix
12.Semua pihak yang tak dapat penulis sebutkan satu per satu yang telah
membantu penulis dalam menyelesaikan skripsi ini.
Akhir kata, penulis menyadari bahwa penelitian dan penyusunan skripsi
ini masih memiliki kekurangan mengingat keterbatasan penulis dalam penyusunan
skripsi ini. Oleh sebab itu, penulis mengharapkan kritik dan saran atau mungkin
ada pertanyaan dari pembaca sekalian, kirimkan ke alamat email
a_thendryk@yahoo.com. Semoga skripsi ini memberikan manfaat bagi
perkembangan ilmu pengetahuan di lingkungan akademis Universitas Sanata
Dharma, syukur-syukur di tanah air. Selamat membaca...
Yogyakarta, Februari 2008
Penulis
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
x
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis
ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah
disebutkan kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Yogyakarta, 4 Februari 2008
Penulis
xi
DAFTAR ISI
Halaman
HALAMAN JUDUL………... ii
HALAMAN PERSETUJUAN PEMBIMBING………... iii
HALAMAN PENGESAHAN………...…. iv
HALAMAN PERSEMBAHAN………...v
PRAKATA... vii
PERNYATAAN KEASLIAN KARYA ... x
DAFTAR ISI... xi
DAFTAR GAMBAR ... xv
DAFTAR TABEL... xvi
DAFTAR LAMPIRAN... xvii
INTISARI... xix
ABSTRACT... xx
BAB I. PENGANTAR ... 1
A. Latar Belakang ... 1
B. Perumusan Masalah ... 3
C. Keaslian Karya ... 3
D. Manfaat Penelitian ... 3
1. Manfaat teoritis ... 3
2. Manfaat metodologis... 4
3. Manfaat praktis ... 4
E. Tujuan Penelitian ... 4
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xii
1. Tujuan umum: ... 4
2. Tujuan khusus: ... 4
BAB II. PENELAAHAN PUSTAKA... 5
A. Alga atau Rumput Laut ... 5
B. Alga Merah ... 6
C. Kandungan kimia Laurencia sp. ... 6
D. Florotanin ... 7
E. Ekstraksi... 8
F. Spektrofotometri Visibel dan Kolorimetri ... 10
G. Metode Folin Ciocalteau ... 14
H. Validasi Metode Analisis ... 16
1. Akurasi ... 16
2. Presisi ... 16
3. Sensitivitas ... 17
4. Linearitas... 17
5. Range... 17
6. Spesifisitas ... 18
7. Detection Limit... 18
8. Quantitation Limit... 18
I. Kesalahan Dalam Metode Analisis ... 19
1. Kesalahan Sistematik (determinate errors) ... 19
2. Kesalahan Tidak Sistematik (indeterminate errors) ... 20
xiii
BAB III. METODOLOGI PENELITIAN ... 22
A. Jenis Rancangan Penelitian ... 22
B. Variabel dan Definisi Operasional ... 22
1. Variabel Penelitian ... 22
2. Definisi operasional ... 22
C. Bahan atau Materi Penelitian ... 23
D. Alat Penelitian... 23
E. Tata Cara Penelitian ... 24
1. Preparasi Sampel Alga Merah Laurenciapapillosa (Forskal) Graville.... 24
2. Penetapan Kadar Air Serbuk Alga ... 24
3. Uji Kualitatif Senyawa Fenolik... 25
4. Isolasi Florotanin Kasar ... 25
5. Optimasi Metode Kolorimetri dengan Folin-Ciocalteau... 26
a. Pembuatan larutan uji dan larutan standar ... 26
b. Penetapan Operating Time (OT)... 26
c. Penentuan Panjang Gelombang Maksimum ( maks) ... 27
6. Validasi Metode Analisis ... 27
7. Pengukuran Kadar Polifenol Total... 28
a. Perlakuan pada larutan standar floroglusinol... 28
b. Perlakuan fraksi etil asetat alga merah... 29
F. Analisis Hasil ... 30
1. Akurasi ... 30
2. Presisi ... 30
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xiv
BAB IV. HASIL DAN PEMBAHASAN ... 31
A. Pengambilan Sampel... 31
B. Preparasi Sampel Alga merah Laurenciapapillosa (Forskal) Graville ... 31
B. Hasil Uji Kualitatif... 36
1. Uji pendahuluan ... 36
2. Uji polifenol ... 37
3. Uji tanin (zat samak) ... 38
C. Isolasi Florotanin Kasar ... 38
D. Dasar Reaksi Kolorimetri dengan Folin-Ciocalteau ... 40
E. Optimasi Metode Kolorimetri dengan Folin-Ciocalteau... 44
1. Penetapan Operating Time (OT)... 44
2. Penentuan Panjang Gelombang Maksimum ( maks) ... 45
F. Hasil Validasi Metode Analisis... 48
G. Penetapan Kadar Florotanin Fraksi Etil Asetat Laurencia papillosa (Forskal) Graville ... 52
BAB V. KESIMPULAN DAN SARAN... 54
A. Kesimpulan ... 54
B. Saran... 54
DAFTAR PUSTAKA ... 55
LAMPIRAN... 59
xv
DAFTAR GAMBAR
Halaman
Gambar 1. Struktur kimia beberapa polifenol alga ... 8
Gambar 2. Rangkaian alat sokhletasi... 10
Gambar 3. Instrumentasi spektrofotometer visisbel ... 11
Gambar 4. Diagram radiasi elektromagnetik ... 12
Gambar 5. Ionisasi senyawa fenol ... 13
Gambar 6. Proses oksidasi fenol oleh enzim polifenol oksidase (PPO) ... 34
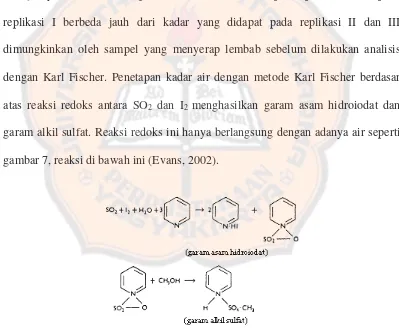
Gambar 7. Reaksi saat penetapan kadar air dengan Karl Fischer... 35
Gambar 8. Reaksi uji pendahuluan senyawa floroglusinol dan KOH ... 36
Gambar 9. Reaksi pembentukan kompleks gugus fenolik dan FeCl3... 37
Gambar 10. Reaksi redoks dalam reaksi Folin-Ciocalteau ... 42
Gambar 11. Hasil pembacaan OT floroglusinol kadar 3,0 ppmdengan pereaksi Folin Ciocalteau... 45
Gambar 12. Hasil pembacaan maks floroglusinol 3 macam kadar floroglusinol: 1,0; 3,0 dan 6,0 ppm setelah direaksikan dengan Folin Ciocalteau... 47
Gambar 13. Kurva baku hubungan kadar dan absorbansi floroglusinol setelah direaksikan dengan Folin Ciocalteau ... 51
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xvi
DAFTAR TABEL
Halaman
Tabel I. Hasil uji pendahuluan kandungan senyawa fenolik Laurencia
papillosa (Forskal) Graville ... 37
Tabel II. Hasil uji kandungan senyawa polifenol Laurencia papillosa
(Forskal) Graville ... 38
Tabel III. Data replikasi seri baku floroglusinol ... 48
Tabel IV. Hasil validasi metode Folin-Ciocalteau ... 49
Tabel V. Hasil penetapan kadar sampel florotanin kasarLaurencia
xvii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Surat Keterangan hasil identifikasi spesies alga merah ... 59
Lampiran 2. Data perhitungan kadar air dengan Karl Fischer... 61
Lampiran 3. Data penimbangan replikasi seri baku floroglusinol... 62
Lampiran 4. Contoh perhitungan seri kadar baku floroglusinol... 63
Lampiran 5. Hasil scanning maks kadar floroglusinol 1,0 ppm setelah direaksikan dengan Folin-Ciocalteau... 63
Lampiran 6. Hasil scanning maks kadar floroglusinol 3,0 ppm setelah direaksikan dengan Folin-Ciocalteau... 64
Lampiran 7. Hasil scanning maks kadar floroglusinol 6,0 ppm setelah direaksikan dengan Folin-Ciocalteau... 64
Lampiran 8. Hasil pembacaan absorbansi seri baku floroglusinol pada ketiga maks... 65
Lampiran 9. Data recovery, kesalahan sistematik dan kesalahan acak dengan metode Folin-Ciocalteau ... 65
Lampiran 10. Hasil analisis statistik regresi linear seri baku floroglusinol replikasi I... 66
Lampiran 11. Hasil analisis statistik regresi linear seri baku floroglusinol replikasi II ... 67
Lampiran 12. Hasil analisis statistik regresi linear seri baku floroglusinol replikasi III ... 67
Lampiran 13. Parameter mean recovery... 68
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xviii
Lampiran 14. Parameter CV... 69
Lampiran 15. Data penimbangan sampel fraksi etil asetat
Laurencia papillosa (Forskal) Graville... 69
Lampiran 16. Data absorbansi sampel fraksi etil asetat Laurencia papillosa
(Forskal) Graville ... 70
Lampiran 17. Contoh perhitungan kadar sampel... 70
Lampiran 18. Foto hasil uji kualitatif kandungan florotanin serbuk
alga merah Laurencia papillosa (Forskal) Graville ... 71
Lampiran 19. Foto florotanin kasardari fraksi etil asetat alga merah
Laurencia papillosa (Forskal) Graville... 72
Lampiran 20. Foto instrumen spektrofotometer UV - VIS Perkin Elmer
xix
INTISARI
Tanaman laut alga merupakan salah satu kekayaan laut Indonesia yang sangat potensial, namun belum dimanfaatkan secara maksimal baik sebagai nutrisi makanan maupun agen biomedis. Salah satunya, alga merah Laurencia yang cukup melimpah di perairan Indonesia. Alga merah mengandung mikronutrien polifenol alga yang dikenal sebagai florotanin. Senyawa ini berupa unit-unit floroglusinol (1,3,5-trihidoksibenzena) yang berbeda dari tumbuhan terestrial.
Tujuan penelitian ini adalah mendapatkan florotanin kasar dari alga merah Laurencia papillosa (Forskal) Graville serta menetapkan kadar florotanin dalam fraksi etil asetat alga tersebut. Isolasi dilakukan menggunakan metode sokhletasi dengan pelarut metanol. Ekstrak kental yang diperoleh kemudian difraksinasi dengan kloroform, akuades, dan etil asetat untuk mendapatkan florotanin kasar.
Konsentrasi polifenol total dalam florotanin kasar ditetapkan secara spektrofotometri dengan metode Folin-Ciocalteau, menggunakan standar floroglusinol yang dibuat seri konsentrasi baku 0,5 ; 1,0 ; 2,0 ; 3,0 ; 4,0 ; 5,0 ; dan 6,0 ppm dalam pelarut aseton 75 %. Standar floroglusinol dan sampel dibaca pada panjang gelombang maksimum 750,1 nm. Konsentrasi polifenol total dalam fraksi etil asetat alga merah yang didapat adalah 10,55-11,21 mg PGE (Phloroglucinol Equivalent)/g sampel.
Kata kunci : florotanin, polifenol, alga merah Laurencia papillosa, metode Folin-Ciocalteau
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
xx
ABSTRACT
Seaweed algae is one of Indonesian’s sea treasures that really potential, but still haven’t been used maximally as well yet, either as food nutrition or biomedical agents. One of them is red algae Laurencia that abundant enough in Indonesian waters. The Red algae contains algae polyphenols micronutrient called phlorotannins. This compound is derived from phloroglucinol units (1,3,5-trihydoxybenzene), that is differ from terrestrial plant polyphenols.
The goals of this study is for getting crude phlorotannin from red algae Laurencia papillosa (Forskal) Graville and determining phlorotannin concentration in ethyl acetate fractional of alga that mentioned. Isolation have been done by soxhletation method with methanol solvent. The viscous extract that was gained, than was fractionated with chloroform, aquadest and ethyl acetate to gain crude phlorotannin.
Concentration of total polyphenols in crude phlorotannin was determined by spectrophotometric with Folin-Ciocalteau method. Using phloroglucinol standard that was made in calibration series 0.5 ; 1.0 ; 2.0 ; 3.0 ; 4.0 ; 5.0 and 6.0 ppm with acetone 75 % solvent. The phloroglucinol standard and sample was scanned at 750.1 nm the maxima wavelength. Concentration of total polyphenols in ethyl acetate fractional of red algae has been investigated was 10.55-11.21 mg PGE (Phloroglucinol Equivalent)/g sample.
1
BAB I
PENGANTAR
A. Latar Belakang
Saat ini telah dikenal 8000 senyawa fenolik alam dengan struktur yang
digambarkan sebagai suatu fenol (cincin aromatik yang berikatan sedikitnya
dengan 1 gugus hidroksil) seperti asam kafeat, asam ferulat, kuersetin, apigenin,
genistein, resveratrol, asam norhidroguaiaretat, asam karnosat, silimarin, polifenol
teh, dan tanin (Svobodova et al., 2003).
Salah satu mikronutrien dari tumbuhan alga adalah polifenol yang dikenal
sebagai florotanin, merupakan senyawa polifenol yang tidak ditemukan pada
tumbuhan terestrial (Burtin, 2003). Beberapa aktivitas biologik florotanin yang
telah diteliti adalah antiproliferasi dan antioksidan (Nakamura et al., 1996; Kang
et al., 2005a; Athukorala et al., 2006; Yuan & Walsh, 2006), antiinflamasi (Shin
et al., 2006), inhibitor matriks metalloproteinase (Kim et al., 2006), sitoprotektif
terhadap stres oksidatif (Kang et al., 2005b), dan inhibitor HIV-1 reverse
transcriptase dan protease (Ahn et al., 2004).
Sebagai negara yang dikelilingi oleh lautan, Indonesia memiliki potensi
yang baik untuk mengembangkan dan memanfaatkan kekayaan lautnya terutama
alga atau rumput laut (Sulistiyowati, 1992). Alga merah cukup melimpah di
perairan Indonesia yang belum dimanfaatkan secara maksimal baik sebagai
makanan ataupun agen biomedis. Selain itu, senyawa bioaktif dari lautan yang
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
telah dieksplorasi belumlah sebanyak dari daratan yang memiliki keterbatasan
lahan tanah yang semakin sempit untuk pemukiman dan fasilitas lainnya.
Diketahui pula, tanaman alga merah telah dikembangkan jadi beberapa
produk kosmetika antioksidan karena merupakan agen pereduksi sebagaimana
halnya dengan vitamin C, sehingga perlu dilakukan investigasi tentang kandungan
aktif senyawa polifenolnya. Maka sebagai langkah awal untuk meneliti
kandungan polifenol alga merah Laurencia papillosa (Forskal) Gravilledilakukan
penelitian secara kualitatif dan kuantitatif polifenol totalnya agar dapat diketahui
kandungan senyawa florotanin Laurencia papillosa (Forskal) Graville sebenarnya
dan jika dilakukan uji penelitian lanjutan dapat diketahui besarnya potensi
aktivitasnya sebagai bioaktif yang berguna menjaga kesehatan manusia.
Penelitian mengenai estimasi kandungan polifenol total pada rumput laut
dan ekstraknya yang terhitung sebagai ekivalen floroglusinol pernah dilakukan
oleh Zhang et al. (2006) dengan metode sederhana berdasarkan reaksi kolorimetri
Folin-Ciocalteau. Metode ini memiliki keunggulan dalam hal sensitivitasnya
mengukur senyawa-senyawa yang memiliki gugus fenolik hingga tingkat part per
million (ppm), memiliki reprodusibilitas dan linearitas yang baik, sederhana,
hanya membutuhkan reagen Folin Ciocalteau sehingga metode ini masih
3
B. Perumusan Masalah
Dari uraian di atas, maka permasalahan dalam penelitian ini difokuskan
pada florotanin dalam fraksi etil asetat yang diisolasi dari alga merah Laurencia
papillosa (Forskal) Graville yang tersebar di pantai selatan Yogyakarta. Rumusan
masalah yang ada sebagai berikut :
1. Apakah florotanin berupa florotanin kasarpada fraksi etil asetat dapat diisolasi
dari alga merah Laurencia papillosa (Forskal) Graville untuk diukur dengan
metode Folin Ciocalteau?
2. Berapakah kadar florotanin dalam alga merah Laurencia papillosa (Forskal)
Graville yang diukur dengan metode Folin Ciocalteau?
C. Keaslian Karya
Sepengetahuan peneliti, penelitian tentang penetapan kadar florotanin
dalam fraksi etil asetat alga merah (Laurencia papillosa (Forskal) Graville)
dengan metode Folin-Ciocalteau belum pernah dilakukan.
D. Manfaat Penelitian
1. Manfaat teoritis
Penelitian ini diharapkan dapat memberi informasi kandungan florotanin hasil
isolasi dari alga merah (Laurencia papillosa (Forskal) Graville).
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
2. Manfaat metodologis
Penelitian ini dapat menjadi acuan tentang penggunaan metode Folin
Ciocalteau dalam penetapan kadar florotanin.
3. Manfaat praktis
Memberi informasi kepada masyarakat kandungan polifenol alga merah
(Laurencia papillosa (Forskal) Graville) yang bermanfaat bagi kesehatan
sebagai antioksidan, antikanker, sediaan kosmetik tabir surya dan manfaat lain
yang belum diteliti.
E. Tujuan Penelitian
1. Tujuan umum:
Tujuan umum penelitian ini adalah menetapkan kadar florotanin alga merah
Laurencia papillosa (Forskal) Graville.
2. Tujuan khusus:
a. Dapat mengisolasi florotanin berupa florotanin kasarpada fraksi etil asetat
alga merah Laurencia papillosa (Forskal) Graville untuk diukur dengan
metode Folin Ciocalteau.
b. Mengetahui kadar florotanin dalam alga merah Laurencia papillosa
5
BAB II
PENELAAHAN PUSTAKA
A. Alga atau Rumput Laut
Rumput laut adalah tumbuhan yang tidak dapat dibedakan antara bagian
akar, batang dan daun. Semua bagian tumbuhannya disebut thallus. Berdasarkan
ukurannya dibedakan dua golongan yaitu mikro-algae dan makro-algae (Anonim,
1979). Makroalga (alga coklat, alga hijau, dan alga merah) merupakan tumbuhan
laut yang dikonsumsi sehari-hari sebagai sayuran secara turun–menurun di Asia.
Banyak penelitian epidemiologi mengaitkan antara konsumsi alga dan manfaatnya
bagi kesehatan. Selain itu, makroalga telah banyak dieksplorasi di negara barat
sebagai sumber phycocolloid seperti alginat, karagenan, dan agar. Di sisi lain,
makroalga masih mengandung senyawa lain (makronutrien dan mikronutrien)
yang mempunyai efek protektif terhadap kesehatan yang menarik untuk diteliti
lebih lanjut. Makroalga merupakan sumber polisakarida yang tinggi (alginat dan
fucoidan dari alga coklat, karagenan dan agar dari alga merah), selain itu juga
makronutrien seperti mineral yang tinggi (yodium dari alga coklat dan kalsium),
protein dan asam amino (pikobiliprotein dari alga merah dan biru), lipid dan asam
lemak (asam linolenat dari alga hijau, asam eikosapentoat dan asam arakidonat),
dan mikronutrien (vitamin C, vitamin E, polifenol, dan karotenoid) (Burtin, 2003).
Jenis-jenis algaini umumnya tumbuh dengan baik di daerah pasang surut atau di
daerah yang selalu terendam air (subtidal) sampai batas kedalaman 200 m yang
intensitas cahaya masih dapat ditembus (Kadi, 2007).
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
B. Alga Merah
Red algae (Rhodophyta, Yunani : (rhodon) = mawar +
(phyton) = tanaman, jadi tanaman merah) adalah kelompok besar sekitar
5000-6000 spesies dari kebanyakan marine algae adalah multiselular termasuk banyak
dikenal sebagai ganggang laut (Thomas, 2002). Laurencia termasuk dalam ordo
Ceramiales dan famili Rhodomelaceae (Al Amin & Razali, 1997).
Kebanyakan coralline algae, mensekresikan kalsium karbonat dan
memainkan peran membangun batu karang (Woelkerling, 1990). Alga merah
seperti dulse (Palmaria palmata) dan nori sebagai masakan tradisional Eropa dan
Asia dan digunakan untuk produk agar, karagenan dan bahan tambahan makanan
lain (Thomas, 2002).
C. Kandungan kimia Laurencia sp.
Laurencia papillosa (Forskal) Graville mengandung polisakarida
carrageenan dan agar, dinding sel alga merah mengandung minor polisakarida
xylan (Burtin, 2003). Laurencia obtusa mengandung seskuiterpen teroksidasi
chamigrenelactone, asetogenin steroisomer neoisoprelaurefucin. Dua diterpen
terhalogenasi 15-bromoparguer-9(11)-ene-16-ol dan
15-bromoparguer-7-ene-16-ol dielusidasi dari L. nipponica. L. intricata memiliki diterpen laurenditerpenol.
Rhodomela confervoides telah dikenal sebagai sumber derivat bromofenol (Blunt
et al., 2006). Kandungan kalsium bisa setinggi 7 % dari bobot kering pada
makroalga dan bisa mencapai 34 % pada alga berkapur lithotamne. Protein alga
7
bertolakbelakang, pada alga merah dan hijau memiliki kandungan fenol yang
rendah dan protein yang tinggi. Lipid didapati hanya 1-5 % dari bobot kering alga
menunjukkan suatu poli-asam lemak tak jenuh. Selain itu terdapat pula polifenol
alga disebut florotanin (Burtin, 2003).
D. Florotanin
Polifenol alga disebut juga florotanin, berbeda dengan polifenol dari
tanaman teresterial yang berasal dari turunan asam galat dan asam ellagat,
sementara polifenol algal berasal dari unit-unit floroglusinol
(1,3,5-trihydroxybenzene) (Burtin, 2003).
Kandungan tertinggi florotanin ditemukan dalam ganggang coklat,
berkisar 5-15 % dari berat kering (Nagayama et al., 2002). Florotanin terdiri dari
molekul dengan struktur dan tingkat polimerisasi yang heterogen yaitu
phloroglucinol (2 %) dan oligomernya seperti eckol (trimer, 3 %),
phlorofucofuroeckol A (pentamer, 28 %), dieckol (heksamer, 7 %), 8,8’–bieckol
(hexamer, 7 %) dan lainnya (30 %). Florotanin dengan struktur dan tingkat
polimerisasi yang heterogen memungkinkan senyawa ini mempunyai aktivitas
biologik yang luas (Athukorala et al., 2006; Yuan & Walsh, 2006; Kang et al.,
2005a). Floroglusinol berupa kristal putih pada suhu kamar, titik lebur 218 0C,
rasa manis, tak berwarna dalam cahaya. Larut dalam 100 bagian air, 10 bagian
alkohol, 0,5 bagian piridin. Praktis larut eter, protektif terhadap cahaya (Anonim,
1989).
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
Glombitza et al. menemukan floroglusinol bebas dalam Fucus vesiculosus
dan mendeskripsikan isolasi beberapa polifloroglusinol dan dinamakan difucol,
trifucol, serta campuran dua isomerik tetrafucol. Senyawa-senyawa ini diisolasi
dan dikaraktersisasikan sebagai paracetates, yang strukturnya didapat dari data
spektrum. Dari ganggang coklat yang lain, Bifurcaria bifurcata, diisolasi sebuah
difenil eter dan dikarakterisasikan sebagai paracetate. Data spektrum
menunjukkan senyawa ini, bernama bifuhalol yang lebih lanjut diduga sebagai
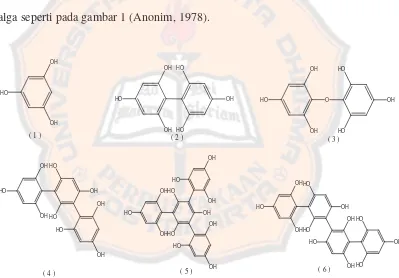
prekursor tanin phaeophyta. Contoh struktur kimia senyawa-senyawa polifenol
alga seperti pada gambar 1 (Anonim, 1978).
OH OH HO OH OH HO HO HO OH OH OH HO HO HO OH OH OH HO OH OH HO HO HO OH O OH OH HO HO HO OH OH OH HO OH OH HO OH OH HO HO HO OH OH OH HO HO HO OH
( 1 ) ( 2 )
( 3 )
( 4 ) ( 5 ) ( 6 )
Gambar 1. Struktur kimia beberapa polifenol alga : (1) Floroglusinol, (2) Difucol, (3) Bifuhalol, (4) Trifucol, (5) Isomer I Tetrafucol, (6) Isomer II Tetrafucol
E. Ekstraksi
Ekstraksi adalah kegiatan penarikan zat yang dapat larut dari bahan yang
9
penyarian adalah kecepatan difusi zat yang larut melalui lapisan batas antara
cairan penyari dengan bahan yang mengandung zat tersebut. Pada waktu
pembuatan simplisia (serbuk), beberapa sel ada yang dindingnya pecah dan ada
yang masih utuh. Proses penyarian pada sel yang dindingnya masih utuh, zat aktif
yang terlarut pada cairan penyari untuk keluar dari sel harus melewati dinding sel
(Anonim, 1986). Ekstrak adalah sediaan kering, kental atau cair dibuat dengan
menyari simplisia nabati atau hewani menurut cara yang cocok, diluar pengaruh
cahaya matahari langsung (Anonim, 1979).
Maserasi merupakan cara penyarian yang sederhana dan digunakan untuk
simplisia yang mengandung zat aktif yang mudah larut dalam cairan penyari.
Maserasi dilakukan dengan cara merendam serbuk simplisia dalam cairan penyari.
Cairan penyari akan menembus dinding sel dan masuk ke dalam rongga sel yang
mengandung zat aktif. Maserasi digunakan untuk penyarian simplisia yang
mengandung zat aktif yang mudah larut dalam cairan penyari, tidak mengandung
zat mudah mengembang dalam cairan penyari, tidak mengandung benzoin, stirak,
dan lain-lain. Keuntungan penyarian dengan maserasi adalah cara pengerjaan dan
peralatan yang digunakan sederhana dan mudah diusahakan. Kerugian maserasi
adalah pengerjaan lama, penyariannya kurang sempurna (Anonim, 1986).
Sokhletasi merupakan salah satu penyarian berkesinambungan
menghasilkan ekstrak cair yang dilanjutkan dengan proses penguapan. Serbuk
diisikan pada filter kertas berpori. Cairan penyari dalam labu dipanaskan hingga
mendidih. Uap penyari mengembun karena didinginkan oleh pendingin balik.
Embun turun melalui serbuk simplisia sambil melarutkan zat aktifnya dan kembali
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
ke labu. Cairan akan menguap kembali berulang seperti proses sebelumnya
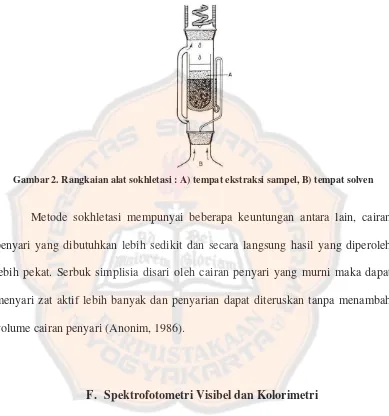
(Anonim, 1986). Rangkaian alat sokhletasi seperti gambar 2 (Evans, 2002).
Gambar 2. Rangkaian alat sokhletasi : A) tempat ekstraksi sampel, B) tempat solven
Metode sokhletasi mempunyai beberapa keuntungan antara lain, cairan
penyari yang dibutuhkan lebih sedikit dan secara langsung hasil yang diperoleh
lebih pekat. Serbuk simplisia disari oleh cairan penyari yang murni maka dapat
menyari zat aktif lebih banyak dan penyarian dapat diteruskan tanpa menambah
volume cairan penyari (Anonim, 1986).
F. Spektrofotometri Visibel dan Kolorimetri
Spektrofotometer adalah suatu instrumen yang akan memecah radiasi
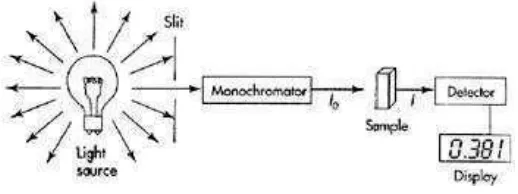
polikromatis menjadi panjang gelombang berbeda. Instrumentasi seluruh
spektrofotometer yang ada: 1) sumber radiasi kontinyu pada tertentu, 2)
monokromator untuk memilih berkas sempit dari sumber spektrum, 3) sel sampel,
4) detektor, 5) pembaca respon detektor atau recorder (Christian, 2004).
11
Gambar 3. Instrumentasi spektrofotometer visisbel
Sumber (source) untuk daerah tampak, adalah tungsten filament
incandescent lamp. Sel sampel untuk visibel dari gelas atau kuarsa (Christian,
2004). Analisis spektroskopi adalah sains untuk menetapkan berapa banyak
substansi yang ada di sampel secara akurat mengukur berapa besar cahaya yang
diabsorpsi atau diemisikan oleh atom atau molekul di dalamnya (Cairns, 2005).
Senyawa yang dapat menyerap radiasi cahaya tampak adalah senyawa
berwarna yang memiliki elektron lebih mudah dipromosikan. Spektrum serapan
elektronik ini dapat digunakan untuk analisis kuantitatif karena jumlah radiasi
elektromagnetik yang diserap ada hubungannya dengan jumlah molekul penyerap
(Silverstein & Murrill, 1991; Skoog et al., 1998), digambarkan sebagai berikut:
T = = 10 It -abc
Io (1)
A = log = abc1
T (2)
Keterangan:
T = persen transmittan
Io = intensitas radiasi yang
datang
It = intensitas radiasi yang
diteruskan
A = absorban (serapan)
a = absorbansi molar
b = tebal kuvet
c = konsentrasi analit
(Mulja & Suharman, 1995)
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
Cahaya adalah bentukan radiasi elektromagnetik, disebut demikian karena
terdiri atas komponen elektrik dan komponen magnetis yang bergelombang
bersamaan dengan arah tegak lurus dan tegak lurus terhadap arah perjalanan
radiasi melewati ruang seperti gambar 4 berikut (Cairns, 2005).
Gambar 4. Diagram radiasi elektromagnetik
Panjang gelombang saat mencapai absorbans (A) tertinggi disebut maks
dan karakteristik dari bagian kromofor (Christian, 2004). Pergeseran maks menjadi
panjang gelombang lebih panjang dikenal sebagai batokromik atau red shift
karena warna merah berada pada panjang gelombang yang panjang di akhir
spektrum visibel. Pada kasus fenol yang merupakan asam lemah, ionisasi
meningkatkan intensitas absorpsi cahaya dan posisi maks berpindah ke panjang
gelombang lebih panjang. Ini karena ionisasi dan kehilangan atom H sehingga
menghasilkan ion H+ dengan muatan negatif penuh pada oksigen (ion fenoksida),
yang dapat berinteraksi dengan cincin lebih efektif dari pasangan elektron bebas
yang ada pada molekul tak terionkan. Gambar 5 menggambarkan proses ionisasi
13
Gambar 5. Ionisasi senyawa fenol
Kolorimetri adalah suatu teknik pengukuran cahaya yang diabsorpsi oleh
zat berwarna baik warna yang terbentuk dari asalnya maupun akibat reaksi dengan
zat lain (Khopkar, 1990). Pemilihan prosedur kolorimetri untuk menentukan
substansi tergantung pada pertimbangan sebagai berikut :
1. metode kolorimetri akan memberikan hasil yang lebih akurat pada
konsentrasi rendah daripada titrimetri atau gravimetri.
2. metode kolorimetri sering digunakan pada kondisi di mana tidak ada
titrimetri atau gravimetri.
3. metode kolorimetri memiliki beberapa keuntungan dalam hal spesifisitas
(Vogel, 1978).
Kriteria untuk analisis kolorimetri yang baik adalah :
1. Menghasilkan reaksi warna yang khusus
Reaksi-reaksi yang ada sangat sedikit sekali untuk beberapa substansi
tertentu, tetapi justru memberikan warna-warna yang banyak membentuk
kelompok warna tersendiri yang hanya berhubungan dengan substansi
khusus.
2. Adanya proporsi yang sesuai antara warna dan konsentrasi
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
Untuk kolorimeter visual sangat penting bahwa intensitas warna harus
meningkat secara linier dengan konsentrasi substansi yang ditentukan.
3. Stabilitas warna
Warna yang dihasilkan harus sama untuk mendapatkan hasil yang akurat.
Hal ini menerapkan reaksi-reaksi warna yang akan dicapai secara maksimal.
Waktu untuk mencapai warna yang maksimal harus cukup lama untuk
mendapatkan pengukuran yang kurat.
4. Reprodusibel
Prosedur kolorimetri harus memberikan hasil yang reprodusibel dalam
kondisi yang spesifik.
5. Kejernihan larutan
Larutan harus bebas dari pengotor jika pembanding yang dipakai dibuat
dengan standar. Kekeruhan akan menyerap cahaya dengan baik (Vogel,
1978).
G. Metode Folin Ciocalteau
Reagen Folin-Ciocalteau tersusun atas: 100 g natrium tungstat, 25 g
natrium molibdat P, 50 mL asam fosfat P, 100 mL HCl P, 150 g lithium sulfat P,
dan beberapa tetes brom P (Anonim, 1995).
Metode Folin-Ciocalteau (Singleton & Rossi, 1965) sebagaimana
dideskripsikan oleh Waterman dan Mole (1994) telah digunakan untuk
mendeterminasikan fenol total. Metode Folin-Ciocalteau digunakan untuk
15
tidak menyediakan data senyawa fenolik tertentu dalam ekstrak. Metode
Folin-Ciocalteau berdasar atas kemampuan mereduksi gugus hidroksil fenolik dan
sangat tidak spesifik namun dapat mendeteksi semua fenol dengan sensitivitas
berbeda. Reaksi redoks dari fenolat terjadi di bawah kondisi basa mereduksi
kompleks fosfotungstat-fosfomolibdat dalam reagen menjadi suatu warna biru
(Box, 1983).
Pengujian dengan kolorimetri oksidasi/reduksi ini mengukur semua
molekul fenol tanpa ada diferensiasi antara asam gallat, monomer, dimer dan
senyawa fenolik yang lebih besar (Anonim, 2001). Paper pertama tentang metode
ini dipublikasikan pertama kali pada 1927. Singleton dan Rossi (1965)
membuktikan reprodusibilitas uji ini. Ini adalah suatu metode kuantitatif dan
sensitif, tergantung pada derajat polimerisasi: Fenolik + basa + reagen
Folin-Ciocalteau (F-C) + panas = produk berwarna biru. Absorpsi hasil reaksi polifenol
anggur dan reagen F-C pada 755 nm (Anonim, 2001).
Reagen Folin-Ciocalteau suatu agen pengoksidasi tersusun dari
heteropolifosfotungstat–molibdat (Anonim, 2001). Reagen Folin-Ciocalteau
merupakan larutan kompleks ion polimerik yang dibentuk dari asam
fosfomolibdat dan asam heteropolifosfotungstat. Reagen ini mengoksidasi fenolat
(garam alkali), sehingga mereduksi asam heteropoli menjadi suatu kompleks
Mo-W. Fenolat hanya ada pada larutan basa tetapi reagen dan produknya tidak
stabil pada kondisi basa. Reaksi tersebut menghasilkan warna biru ungu yang
dapat diukur absorbansinya dengan spektrofotometer (Jansoon, 2005).
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
H. Validasi Metode Analisis
Validasi suatu metode analisis adalah proses yang dibuat, dengan
penelitian laboratorium agar karakteristik pelaksanaan metode memenuhi
persyaratan aplikasi analisis yang diinginkan. Parameter-parameter validitas
metode analisis antara lain akurasi, presisi, linearitas, spesifisitas, range, detection
limit, dan quantitation limit (Anonim, 2005).
1. Akurasi
Akurasi adalah derajat kepercayaan antara nilai yang terukur dan nilai
sebenarnya. Nilai sebenarnya yang mutlak sangat sukar diketahui. Definisi
yang lebih mungkin mengenai akurasi adalah kesesuaian antara nilai terukur
dan nilai sebenarnya yang dapat diterima (Christian, 2004).
Akurasi dihitung sebagai persentase recovery pengujian sejumlah
analit yang diketahui jumlahnya atau sebagai perbedaan antara rata-rata dan
nilai sebenarnya yang dapat diterima (Anonim, 2005). Menurut Mulja dan
Hanwar (2003) akurasi untuk bahan baku 98-102 %, sedangkan untuk
bioanalisis rentang akurasi 80-120 % masih bisa diterima.
2. Presisi
Presisi suatu metode analisis adalah derajat kesesuaian antar hasil
percobaan individual ketika metode itu diaplikasikan secara berulang pada
sampel yang homogen (Anonim, 2005). Presisi bisa diekspresikan sebagai
standar deviasi, koefisien variasi, sebagai rentang kepercayaan nilai rata-rata
17
dinyatakan dengan nilai koefisien variasi (CV) yang < 2 % untuk kadar analit
98-102 %.
3. Sensitivitas
Sensitivitas suatu metode analisis merupakan kemampuan metode
analisis untuk memisahkan perbedaan kecil konsentrasi analit. Faktor yang
mempengaruhi sensitivitas adalah kemiringan (slope) kurva baku dan presisi.
Jika ada 2 metode analisis memiliki presisi yang sama namun salah satunya
memiliki kemiringan kurva baku yang lebih curam maka metode yang disebut
terakhir lebih sensitif, dan sebaliknya (Skoog et al., 1998).
4. Linearitas
Linearitas suatu metode analisis merupakan kemampuan (pada
rentang tertentu) untuk mendapatkan hasil uji yang secara langsung
proporsional dengan konsentrasi (jumlah) analit di dalam sampel sehingga
memberikan nilai koefisien korelasi yang lebih besar daripada nilai koefisien
korelasi pada tabel statistik (Mulja & Suharman, 1995).
5. Range
Range suatu metode analisis adalah interval antara konsentrasi
terendah sampai konsentrasi tertinggi analit yang dapat diukur secara
kuantitatif menggunakan metode analisis tertentu dan menghasilkan akurasi,
presisi, linearitas yang memadai (Anonim, 2005).
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
6. Spesifisitas
Spesifisitas didefinisikan sebagai kemampuan untuk mengukur
dengan baik komponen lain dalam analit yang mungkin ada seperti pengotor,
produk degradasi, dan komponen matriks (Anonim, 2005). Spesifisitas
merupakan karakterisitik terpenting dari suatu metode sebagai salah satu
parameter validasi yang utama (Mulja & Hanwar, 2003)
7. Detection Limit
Detection limit adalah kadar terkecil analit yang masih dapat
memberikan tanggap detektor yang tingginya 2-3 kali simpangan maksimum
dari noise (derau) garis dasar (Mulja & Hanwar, 2003). Pada kasus prosedur
analisis instrumental yang menghasilkan background noise. Menurut ICH
(International Conference on Harmonization), rasio signal-to-noise yang
dapat diterima adalah 2:1 atau 3:1 (Anonim, 2005).
8. Quantitation Limit
Quantitation limit adalah kadar terkecil analit dalam sampel yang
dapat ditetapkan dengan presisi dan akurasi yang dapat diterima pada kondisi
percobaan yang dinyatakan. Menurut ICH, rasio signal-to-noise yang dapat
19
I. Kesalahan Dalam Metode Analisis
Kesalahan dalam metode analisis sangat sukar untuk dihilangkan namun
sumber kesalahan tetap harus dibuat seminimal mungkin. Kesalahan dalam
analisis kimia dapat dikategorikan menjadi 2 kelas utama, yaitu:
1. Kesalahan Sistematik (determinate errors)
Kesalahan sistematik adalah hasil analisis yang menyimpang secara
tetap dari nilai kadar yang sebenarnya karena proses pelaksanaan prosedur
analisis, sehingga kesalahan ini disebut juga kesalahan prosedur (Mulja &
Suharman, 1995). Kesalahan sistematik dapat disebabkan oleh beberapa
faktor, antara lain:
a. Kesalahan personil dan operasi
Kesalahan ini disebabkan oleh cara pelaksanaan analisis, bukan
karena metode. Kesalahan operasi umumnya bersifat fisis (bukan khemis),
misalnya kesalahan pengamatan visual pada titik akhir titrasi, kekeliruan
cara pencucian endapan, dan sebagainya. Jadi kesalahan ini bersifat
individual dan sangat dipengaruhi oleh keterampilan analis dalam
melakukan pekerjaan analisis.
b. Kesalahan alat dan pereaksi
Kesalahan ini disebabkan oleh pereaksi yang kurang murni, alat
yang kurang valid atau pemakaian alat yang kurang tepat walaupun
alatnya sendiri baik, contohnya pengambilan volume tepat dengan pipet
ukur atau gelas ukur, penggunaan buret 50 mL (buret makro) untuk
analisis mikro, dan sebagainya.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
c. Kesalahan metode
Kesalahan ini dapat disebabkan oleh kesalahan pengambilan
sampel, kesalahan akibat reaksi kimia yang tidak sempurna, atau ikut
mengendapnya zat-zat yang tidak diinginkan (Day & Underwood, 1986).
Kesalahan sistematik dapat dihindari atau diperkecil dengan:
1). Mengkalibrasi instrumen dan melakukan koreksi secara berkala (biasanya
tiap 3 bulan atau disesuaikan dengan frekuensi pemakaian alat).
2). Memilih metode dan prosedur standar dari badan resmi.
3). Memakai bahan kimia dengan derajat untuk analisis.
4). Meningkatkan pengetahuan dan keterampilan analis.
5). Melakukan penetapan blangko atau kontrol dengan zat baku.
6). Melakukan penetapan paralel (in duplo atau in triplo).
2. Kesalahan Tidak Sistematik (indeterminate errors)
Kesalahan tidak sistematik adalah penyimpangan yang tidak tetap
dari hasil penentuan kadar dengan instrumen yang disebabkan fluktuasi dari
instrumen yang dipakai (derau). Penyebab kesalahan ini tidak dapat ditentukan
dan tidak dapat dikontrol maka kesalahan ini disebut juga kesalahan acak
(random error) (Mulja & Suharman, 1995).
J. Keterangan Empiris
Penyarian florotanin alga merah dilakukan dengan cara sokhletasi karena
hasil dengan cara maserasi didapat ekstrak yang kurang memadai. Selain itu,
21
floroglusinol. Florotanin yang ditetapkan kadarnya adalah fraksi etil asetat yang
diuapkan pelarutnya dan dianggap sebagai florotanin kasar.
Metode Folin-Ciocalteau dapat digunakan untuk menetapkan konsentrasi
gugus-gugus hidroksil fenolik dalam sampel. Metode ini tidak menyediakan data
senyawa fenolik tertentu dalam ekstrak. Metode Folin-Ciocalteau berdasar atas
kemampuan mereduksi gugus hidroksil pada fenol sehingga tidak spesifik namun
sangat sensitif untuk mendeteksi semua kandungan senyawa polifenol dalam
fraksi etil asetat alga merah yang ingin ditetapkan kadarnya, sehingga yang diukur
adalah kadar total polifenol alga yang ekivalen dengan standar floroglusinol.
Dipilih standar floroglusinol karena merupakan unit monomer florotanin.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
22
BAB III
METODOLOGI PENELITIAN
A. Jenis Rancangan Penelitian
Penelitian ini termasuk dalam penelitian deskriptif non-eksperimental
karena tidak ada intervensi atau perlakuan terhadap fenomena yang diamati.
B. Variabel dan Definisi Operasional
1. Variabel Penelitian
a. Variabel pengacau terkendali dalam penelitian ini adalah volume cairan
penyari untuk mengisolasi florotanin alga merah Laurencia papillosa
(Forskal) Graville, tempat panen alga di pantai Drini, masa panen pada
bulan Mei, komposisi reagen saat analisis.
b. Varibel pengacau tak terkendali dalam penelitian ini adalah umur alga
yang dipanen (bukan tanaman budidaya), suhu dan kelembaban ruangan
saat percobaan.
2. Definisi operasional
a. Laurencia papillosa (Forskal) Graville adalah spesies alga merah yang
diambil dari pantai Drini, Gunung Kidul, Yogyakarta pada bulan Mei.
b. Ekstrak metanol adalah hasil ekstraksi serbuk alga dengan sokhlet
23
c. Florotanin kasar adalah ekstrak kasar florotanin dari fraksi etil asetat yang
diuapkan pelarut (etil asetat) seluruhnya.
d. Kadar florotanin adalah konsentrasi polifenol total dihitung ekivalen
dengan floroglusinol (mg PGE/g sampel) yang diukur pada panjang
gelombang maksimum 750,1 nm mendekati teoritis hasil penelitian Zhang
et al. dengan metode Folin Ciocalteau.
C. Bahan atau Materi Penelitian
Bahan yang digunakan dalam penelitian adalah sebagai berikut: Alga
merah (Laurencia sp.) dari pantai Drini, Gunung Kidul, Yogyakarta diambil
tanggal 21 Mei 2007. Metanol, kloroform, etil asetat, natrium karbonat (p.a. E.
Merck, Germany), reagen Folin Ciocalteau (Sigma Chem, Co., USA.), akuades
(Fakultas Farmasi Universitas Sanata Dharma).
D. Alat Penelitian
Alat-alat yang digunakan dalam penelitian adalah sebagai berikut:
Seperangkat spektrofotometer UV-VIS Perkin Elmer Lambda 20, timbangan
elektrik BP 160 dan scaltec SBC 22 readability 0,01 mg, mesin blender, vaccum
rotary evaporator (Buchi), waterbath (Abo-tech), autoklaf, mikropipet 100-1000
l. (Acura 825, Socorex), tabung reaksi bertutup (Scott-Germany), alat-alat untuk
sokhletasi, yaitu sokhlet, labu alas bulat (Schott Duran, Germany), alat sentrifus,
corong pisah 500 mL, alat-alat gelas yang lazim digunakan untuk penelitian di
laboratorium analisis (PYREX-GERMANY)
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
E. Tata Cara Penelitian
1. Preparasi Sampel Alga Merah Laurencia papillosa (Forskal) Graville
Alga merah (Laurencia papillosa (Forskal) Graville) dikumpulkan,
dicuci dengan air mengalir dan dimasukkan dalam autoklaf selama 30 menit pada
suhu 100 0C. Selanjutnya dikeringkan dalam oven dengan suhu 80-100 0C selama
6 hari sampai dapat dihancurkan dengan kekuatan tangan, diserbuk dengan
blender, diayak dan dipilih serbuk yang lolos dengan derajat halus 20/30.
2. Penetapan Kadar Air Serbuk Alga
Penetapan kadar air serbuk alga dilakukan dengan menggunakan metode Karl
Fischer. Serbuk alga ditimbang dengan seksama 0,2 gram, kemudian ditambah 10
mL metanol, didiamkan selama 1 hari pada suhu kamar. Dilakukan pre-titrasi
pada alat, lalu dilakukan uji kebocoran sesuai prosedur perintah pada alat, hingga
didapat angka drift 10-50 pada alat. Standardisasi dilakukan dengan cara timbang
spuit berisi air, kemudian dimasukkan 1 tetes air ke dalam alat. Lalu ditimbang
kembali untuk ditentukan berat air yang dimasukkan. Kemudian dihitung
kesetaraan air. Sebanyak 1 mL metanol dimasukkan dan titrasi dengan alat
(blangko). Kemudian 1 mL sampel dimasukkan, titrasi dengan alat, hitung kadar
air dalam sampel. Kadar air dalam sampel dihitung dengan rumus:
x - blanko (10) berat yang ditimbang
x 100 %
Kadar air =
25
3. Uji Kualitatif Senyawa Fenolik
a. Uji pendahuluan
Sebanyak 1 mL filtrat alga ditambah 10 mL air, dipanaskan selama 30
menit. Larutan disaring dengan kapas. Larutan berwarna kuning sampai
merah menunjukkan adanya senyawa yang mengandung kromofor dengan
gugus hidrofilik. Jika ditambah KOH, warna larutan kuning sampai merah
menjadi lebih pekat.
b. Uji polifenol
Sebanyak 1 mL filtrat alga ditambah 3 tetes pereaksi besi (III) klorida. Jika
terjadi warna hijau-biru menunjukkan adanya polifenol.
c. Uji tanin (zat samak)
Sebanyak 1 mL filtrat alga ditambah 1 mL NaCl 2 %. Bila terjadi
suspensi (endapan) disaring melalui kertas saring. Filtrat alga ditambah 5
mL larutan gelatin 1 %. Terbentuknya endapan warna putih menunjukkan
adanya tanin.
4. Isolasi Florotanin Kasar
Serbuk alga ditimbang sebanyak 40 g. Kemudian serbuk dimasukan
ke dalam kantong khusus untuk sokhlet dan dimasukan dalam labu sokhlet.
Setelah itu diberi pelarut metanol sebanyak 2 kali sirkulasi (1 sirkulasi = 70
mL) dalam tabung sokhlet. Proses sokhletasi dilakukan sampai tetesan pelarut
jernih dengan suhu 100-120 0C. Setelah selesai, hasil sokhletasi diuapkan
pelarutnya dengan menggunakan vacuum rotary evaporator sampai volume
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
yang kecil (1/10 dari volume mula-mula) dan ditambahkan kembali pelarut
metanol hingga diperoleh 60 mL ekstrak metanol, kemudian ditambahkan 120
mL kloroform, dan 45 mL air dalam corong pisah. Corong pisah digojog
perlahan dan didiamkan hingga memisah dan membentuk 2 lapisan. Lapisan
atas dan lapisan bawah yang terbentuk dipisahkan, selanjutnya lapisan atas
diekstraksi dalam corong pisah dengan etil asetat masing-masing sebanyak
75mL. Kumpulkan fraksi etil asetat, selanjutnya diuapkan, dan diperoleh
ekstrak yang merupakan florotanin kasar.
5. Optimasi Metode Kolorimetri dengan Folin-Ciocalteau
a. Pembuatan larutan uji dan larutan standar
i. Pembuatan larutan intermediet floroglusinol
Ditimbang dengan cara seksama 0,05 g standar floroglusinol,
kemudian dilarutkan ke dalam aseton 75 % sampai volume 50,0 mL.
Buat seri konsentrasi (0,005; 0,01; 0,02; 0,03; 0,04; 0,05; dan 0,06)
ppm sebanyak 10,0 mL dengan pelarut aseton 75 %.
ii. Perlakuan fraksi etil asetat alga merah
Ditimbang dengan cara seksama 0,05 g fraksi polifenol, kemudian
dilarutkan ke dalam aseton 75 % hingga volumenya 50,0 mL.
b. Penetapan Operating Time (OT)
Pipet 0,5 mL larutan intermediet 0,03 ppm dan dimasukkan ke dalam labu
27
yang telah diencerkan dengan akuades 1:1. Didiamkan selama 2 menit,
kemudian ditambahkan 7,5 mL Na2CO3 1,9 M, dicampurkan sampai
volume 50,0 mL dengan akuades. Operating time diukur dengan
spektrofotometer visibel. Pengukuran dilakukan pada panjang gelombang
teoritis hasil reaksi floroglusinol dengan Folin Ciocalteau (750 nm).
c. Penentuan Panjang Gelombang Maksimum ( maks)
Pipet 0,5 mL larutan intermediet (0,01; 0,03; dan 0,06) ppm dan masukkan
ke dalam labu takar 50,0 mL yang mengandung 2,5 mL pereaksi fenol
Folin-Ciocalteau yang telah diencerkan dengan akuades 1:1. Didiamkan
selama 2 menit, kemudian ditambahkan 7,5 mL Na2CO3 1,9 M,
dicampurkan sampai volume 50,0 mL dengan akuades. Campuran tersebut
diinkubasi pada suhu kamar selama OT (pada 15 menit pertama dan 15
menit kedua, campuran tersebut divortex selama 30 detik). Kemudian
campuran reaksi disentrifus dengan kecepatan 4000 rpm selama 5 menit.
Kemudian ketiga larutan tersebut di-scanning pada rentang panjang
gelombang 400-900 nm dengan spektrofotometer visibel untuk melihat
panjang gelombang maksimumnya.
6. Validasi Metode Analisis
Pipet 0,5 mL untuk masing-masing larutan intermediet dan masukkan ke
dalam labu takar 50,0 mL yang mengandung 2,5 mL pereaksi fenol
Folin-Ciocalteau yang telah diencerkan dengan akuades 1:1. Didiamkan selama 2 menit,
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
kemudian ditambahkan 7,5 mL Na2CO3 1,9 M, dicampurkan sampai volume 50,0
mL dengan akuades. Campuran tersebut diinkubasi pada suhu kamar selama OT
untuk menyempurnakan reaksi sampai terbentuk warna biru (pada 15 menit
pertama dan 15 menit kedua, campuran tersebut divortex selama 30 detik).
Kemudian campuran reaksi disentrifus dengan kecepatan 4000 rpm selama 5
menit dan diukur absorbansinya pada panjang gelombang maksimum hasil
scanning ( maks) menggunakan spektrofotometer visibel. Ditentukan persamaan
kurva baku plot antara kadar baku floroglusinol dan absorbansi. Replikasi
dilakukan sebanyak 3 kali untuk dihitung recovery, kesalahan sistematik,
kesalahan acak dengan rumus sebagai berikut:
Recovery =
sebenarnya kadar
kur kadar teru
× 100 %
Kesalahan sistematik = 100 % – recovery
Kesalahan acak =
kur kadar teru rata
-rata
(SD) deviasi standar
× 100 %
7. Pengukuran Kadar Polifenol Total
a. Perlakuan pada larutan standar floroglusinol
Pipet 0,5 mL untuk masing-masing larutan intermediet dan masukkan ke
dalam labu takar 50,0 mL yang mengandung 2,5 mL pereaksi fenol
Folin-Ciocalteau yang telah diencerkan dengan akuades 1:1. Didiamkan selama
2 menit, kemudian ditambahkan 7,5 mL Na2CO3 1,9 M, dicampurkan
29
pada suhu kamar selama OT untuk menyempurnakan reaksi sampai
terbentuk warna biru (pada 15 menit pertama dan 15 menit kedua,
campuran tersebut divortex selama 30 detik). Kemudian campuran reaksi
disentrifus dengan kecepatan 4000 rpm selama 5 menit dan diukur
absorbansinya pada panjang gelombang maksimum hasil scanning ( maks)
menggunakan spektrofotometer visibel.
b. Perlakuan fraksi etil asetat alga merah
Pipet 10,0 mL larutan sampel alga merah dan dimasukkan ke dalam labu
takar 50,0 mL yang mengandung 2,5 mL pereaksi fenol Folin-Ciocalteau
yang telah diencerkan dengan akuades 1:1. Didiamkan selama 2 menit,
kemudian ditambahkan 7,5 mL Na2CO3 1,9 M, dicampurkan sampai
volume 50,0 mL dengan akuades. Campuran tersebut diinkubasi pada suhu
kamar selama OT jam untuk menyempurnakan reaksi sampai terbentuk
warna biru (pada 15 menit pertama dan 15 menit kedua, campuran tersebut
divortex selama 30 detik). Kemudian, campuran reaksi disentrifus dengan
kecepatan 4000 rpm selama 5 menit dan diukur absorbansinya pada
panjang gelombang maksimum hasil scanning ( maks) menggunakan
spektrofotometer visibel. Konsentrasi polifenol total dihitung ekivalen
dengan floroglusinol (mg PGE/g sampel). Prosedur ini dilakukan sebanyak
3 kali replikasi dengan masing-masing replikasi ditetapkan sebanyak 2 kali
dengan cara 2 kali pemipetan (duplo).
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
F. Analisis Hasil
Analisis hasil dilakukan untuk mengetahui validitas metode yang
digunakan dalam penelitian. Validitas metode dilihat dari beberapa parameter
dengan mengacu rentang nilai yang dipersyaratkan Harmita (2004), sebagai
berikut:
1. Akurasi
Akurasi dinilai berdasarkan hasil perolehan kembali (recovery) dan
kesalahan sistematik. Akurasi dikatakan baik jika nilai perolehan kembali rata-rata
(mean recovery) berada dalam rentang 80-110 % jika konsentrasi analit yang
diperiksa adalah 1 ppm (0,0001 %) dengan nilai kesalahan sistematik yang
diterima <20 % (Harmita, 2004). Recovery dan kesalahan sistematik dihitung
dengan rumus sebagai berikut:
Recovery =
sebenarnya kadar
kur kadar teru
× 100 %
Kesalahan sistematik = 100 % – recovery
2. Presisi
Penilaian presisi berdasarkan nilai kesalahan acak atau coefficient of
variation (CV). Presisi dikatakan baik jika nilai CV lebih kecil dari 4,1 % untuk
rentang recovery yang dapat diterima 85-115 % (Harmita, 2004). Kesalahan acak
diperoleh dengan rumus :
Kesalahan acak =
kur kadar teru rata
-rata
(SD) deviasi standar
31
BAB IV
HASIL DAN PEMBAHASAN
A. Pengambilan Sampel
Sampel alga merah didapat dari hasil panen petani setempat pada tanggal
21 Mei 2007 dari perairan dangkal pantai Drini, Gunung Kidul, Yogyakarta.
Secara geografis berada di wilayah samudera Indonesia, pantai selatan pulau
Jawa. Suhu perairan habitat laut alga sekitar 27-30 0C. Umur alga merah yang
dipanen tidak diketahui pasti karena bukan merupakan hasil budidaya melainkan
merupakan hasil panen langsung dari alam, meski informasi tentang perbedaan
umur, masa panen, kondisi geografis habitat alga tumbuh dan spesies alga ini
penting untuk diperhatikan karena dapat memberikan variasi kandungan polifenol
alga.
Selanjutnya jenis spesies alga merah yang didapat diidentifikasi dengan
bantuan dari pihak laboratorium Sistematika Tumbuhan (Fakultas Biologi UGM,
Yogyakarta). Hasil identifikasi, sampel alga merah termasuk dalam ordo
Ceramiales, familia Rhodomelacaeae, genus Laurencia, spesies Laurencia
papillosa (Forskal) Graville (lihat lampiran 1).
B. Preparasi Sampel Alga merah Laurencia papillosa (Forskal) Graville
Alga merah Laurencia papillosa (Forskal) Graville dikumpulkan, dicuci
dengan air tawar mengalir sebanyak dua kali untuk menghilangkan kotoran
berupa debu, pasir (silikat), material laut bukan berasal dari alga merah yang ikut
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
terbawa dan mengotori sampel alga merah. Langkah pencucian ini perlu dilakukan
dengan cermat agar pengotor tidak mengotori sampel yang ingin diteliti.
Senyawa silikat juga dapat membentuk kompleks molibdat dari reagen
Folin dalam suasana asam. Bentuk kompleks asam molibdat yang terbentuk
H6[SiMo12O40].n H2O (Auterhoff & Knabe, 1978). Setelah itu, dilakukan langkah
sortasi atau penyortiran terhadap alga yang dipanen agar materi dari jenis alga
spesies lain atau bahan organik asing tidak tercampur dengan sampel alga merah
karena alga tumbuh bersama-sama dalam satu habitat dengan alga atau rumput
laut yang berbeda spesies juga, tidak hanya dalam bentukan populasi. Sampel
yang didapat benar-benar merupakan alga merah Laurencia papillosa (Forskal)
Graville dilihat dari ciri morfologisnya. Bagian akar alga dibuang dengan pisau
atau gunting karena alga umumnya berakar pada suatu karang sehingga bagian
akarnya dibuang agar materi asing dari batu karang tidak ikut dan mengganggu
hasil analisis. Secara umum tujuan sortasi untuk meminimalkan keberadaan
materi organik asing karena materi organik maupun organic dust ini dapat
menggangu hasil analisis.
Organic dust ini dapat turut mereduksi kompleks asam dalam reagen
membentuk warna kehijauan sesuai laporan penelitian Otto Folin. Namun hal ini
tidak banyak memberi pengaruh pada hasil analisis, mengingat reagen
Folin-Ciocalteau sendiri mengandung banyak stabilizer untuk mengatasi berbagai
ketidakstabilan dari reagen termasuk karena organic dust ini, kandungan bromin
dari reagen dapat menghilangkan hasil reduksi ini, sehingga tidak lagi membentuk
33
Selain itu, pada pengamatan saat dilakukan sortasi terdapat senyawa
berupa kalsium seperti butiran kapur berwana putih yang melingkupi daerah
sekitar thallus alga, kalsium ini merupakan produk alamiah alga yakni hasil
kalsifikasi. Kalsium yang masih ada setelah dilakukan sortasi tidak akan
mengganggu analisis. Senyawa Ca ini bukanlah reduktor sehingga praktis tidak
mampu memiliki kemampuan mereduksi kompleks asam molibdat-fosfat pada
reagen Folin-Ciocalteau yang digunakan.
Setelah lolos proses sortasi maka ganggang merah diproses dalam autoklaf
selama 30 menit pada suhu 100 0C untuk mendenaturasi protein yang ada dalam
ganggang termasuk enzim polifenol oksidase atau Polyphenol Oxydase (PPO).
Efek perlakuan panas terhadap aktivitas PPO menunjukkan pemberian suhu
menyebabkan meningkatnya kecepatan reaksi antara enzim dan senyawa fenolik
sebagai substratnya. Perlakuan pada 55 0C, membuat enzim inaktif secara parsial.
PPO telah dilaporkan menjadi inaktif dengan direbus dalam air panas pada 100 0C
selama 1,5 menit (Mustapha & Ghalem, 2007).
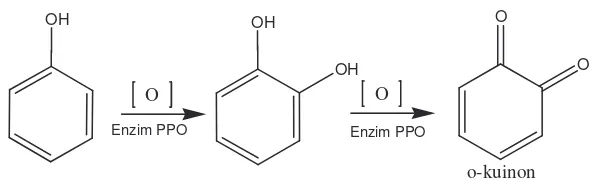
Enzim PPO ini mengkatalisis hidroksilasi dari monofenol menjadi o
-difenol. Lebih lanjut, dapat mengkatalisis oksidasi o-difenol untuk membentuk o
-kuinon. Proses polimerisasi o-kuinon ini cepat berlangsung menghasilkan pigmen
berupa senyawa polifenol. Jika enzim PPO inaktif maka proses polimerisasi fenol
tidak lagi berlangsung, membentuk polimer polifenol yang lebih panjang. Secara
sederhana digambarkan pada gambar 6 (Sullivan et al., 2003).
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
O O
o-kuinon
OH OH
O O
Enzim PPO Enzim PPO
OH
Gambar 6. Proses oksidasi fenol oleh enzim polifenol oksidase (PPO)
Hasil autoklaf dijadikan simplisia dengan cara dikeringkan dalam oven
selama beberapa hari pada suhu 90 0C, agar menjadi simplisia alga merah kering
dengan tin