Prof. Dr. Ir.
Prof. Dr. Ir. Setijo
Setijo
Bismo, DEA.
Bismo
, DEA.
DTK
DTK –
–
FTUI
FTUI
Nopember, 2014
Nopember, 2014
1 N+
V, y
1V, y
0L, x
NL, x
Skematisasi Operasi Absorpsi
Skematisasi Operasi Absorpsi
Suatu menara
sieve
-
tray
dirancang untuk proses absorpsi gas. Gas umpan memasuki kolom di
bagian bawah dengan kandungan absorptif A sebesar 1,852 %-molar. Gas umpan mengalami
pembersihan sedemikian rupa sehingga tersisa polutan A tidak lebih dari 0,088 %-molar di bagian
keluaran (puncak). Cairan absorben yang digunakan, pada awalnya mengandung 0,008 %-molar.
Sistem diketahui mengikuti Hukum HENRY dengan data seperti pada
Tabel 1
di bawah ini. Di
bagian bawah menara (
bottom
), rasio molar cairan-terhadap-gas adalah
(
)
=
1,65
b
L G
,
sedangkan di ektremitas lainnya (di puncak,
top
) adalah
(
)
=
1,71
tL G
. Pada kondisi operasi ini,
diketahui bahwa efisiensi
Murphree
dapat dianggap konstan, yaitu pada
E
MGE=
0,65
.
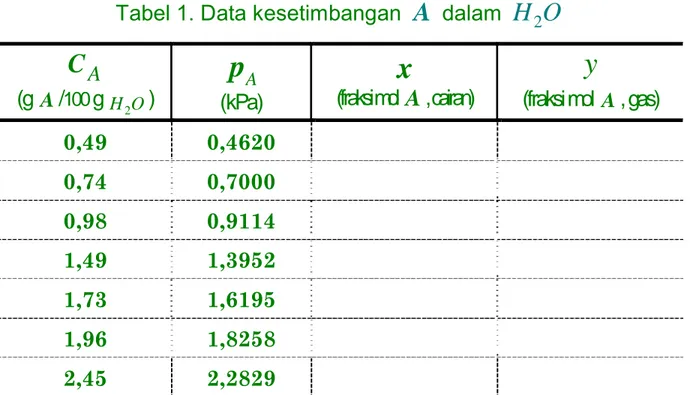
Tabel 1. Data kesetimbangan
A
dalamH O
2A
C
(g A/100 g H O2 ) Ap
(kPa)x
(fraksi mol
A
, cairan)y
(fraksi mol A, gas) 0,49 0,4620 0,74 0,7000 0,98 0,9114 1,49 1,3952 1,73 1,6195 1,96 1,8258 2,45 2,2829
Pertanyaan:
(a).
Hitunglah
y
dan
x
(lengkapi Tabel 1 di atas), sebelum
menentukan
H
′
(konstanta Henry) untuk sistem absorpsi
di atas, jika berlaku!
(b).
Hitunglah atau perkirakan jumlah talam yang diperlukan
oleh sistem ini !
(c).
Jika diinginkan kriteria diameter kolom sebesar
150
cm
(perhatikan tabel di bawah ini), maka tentukanlah tinggi
kolom yang diperlukan !
Penyesaian:
(a).
Hitunglah
y
dan
x
(lengkapi Tabel 1 di atas), sebelum menentukan
H
′
(konstanta Henry untuk sistem absorpsi di atas, jika berlaku!
Penyesaian Konstanta Henry:
Pengaluran
x
Adan
y
A(dari Tabel 1 di atas), dapat digunakan untuk
menentukan
H
′
(konstanta Henry) sebagi berikut:
Kolom Isian (Packed columns) merupakan menara kontak kontinyu
yang “secara fisik tidak memiliki tahap” seperti pada kolom talam.
Secara praktis, Kolom Isian seringkali dianalisis berdasarkan “kesetaraan”
atau “ekivalensi” tahap kesetimbangan dalam Kolom Talam, menggunakan
suatu pendekatan yang disebut “Suatu Ketinggian yang Setara dengan
Talam Teoretis atau disebut sebagai
HETP
(
Height Equivalent to a
Theoretical Plate
).
(
)
Tinggi Isian Packing
HETP
Jumlah Ekivalen dari Tahap Kesetimbangan
=
Dengan mengetahui nilai
HETP
dan
Jumlah Tahap Teoretis
“
n
” dari suatu
Menara Talam, maka dapat dihitung tinggi kolom
H
:
H
=
n HETP
Konsep
HETP
tidak memiliki basis teoretis yang kuat. Nilai
HETP
hanya dapat
dihitung berdasarkan data eksperimen atau kolom komersial dari suatu vendor.
Pada Kolom ISIAN, lebih disukai metode penentuan
Tinggi ISIAN dari pendekatan teoretis yang berbasis Koefisisen Perpindahan Massa.
Absorp
Absorp
si:
si:
Pendekatan Perpindahan Mass (HTU, NTU)
Selain variabel-variabel di atas, digunakan juga koordinat
z, yang merepresentasikan tinggi kolom.
Problem absorsi, pada umumnya adalah sebagai berikut: Suatu aliran Gas MASAM yang tercemar (oleh ABSORBEN atau ABSORPTIF) dari suatu PROSES (tertentu) ingin “dibersihkan” kandungan POLUTAN-nya.
Jika digunakan NOTASI “subskrip yang baru”, pada bagian DASAR (Bottom) dan ATAS (Top) Kolom, maka komposisi GAS dan CAIRAN yang “memasuki” dan “meninggalkan” kolom adalah:
1 1
( , )
x y
( , )
x y
2 2 L, x1 G, y1 T, pProcess
Process
G, y2 y2< yspec L, x2 z = 0 z = H x yAmplop di bagian atas yang berwarna HIJAU adalah untuk NERACA MASSA yang
diperlukan untuk (membuat) GARIS OPERASI dari Kolom Absorpsi “Packing”.
Pertama kali, diperlukan NERACA MASSA di bagian amplop atas yang berwarna HIJAU: membuat GARIS OPERASI, yang melalui titik (
x
2, y
2),(
2)
2L
y
x
x
y
G
=
−
+
1 2 m in ( , ) f L L f G G ⎛ ⎞ = ⎜ ⎟ → ∈ ⎝ ⎠1
( )
Dalam Kolom Isian ini, diperlukan juga kondisi KESETIMBANGAN:
*
y
=
mx
( )
2
Dapat dibuat Garis KESETIMBANGAN dan Garis
OPERASI ke dalam suatu diagram seperti contoh. Dari Garis OPERASI dengan KELANDAIAN “terkecil”
(minimum, yaitu: Lmin/G), didapatkan (L/G) dengan
formula berikut y* = m x y1 G Lmin G L x1 x y2 x2 y 2 2 L x + G y = L x + G y
Sebagai persamaan ketiga, diperlukan suatu “Persamaan Laju Perpindahan Massa”. Jika, dibuat porsi bagian kecil
dari kolom dimaksud, maka Neraca MASSA “sisi GAS” dalam potongan kecil tersebut adalah:
gas gas mass transfer
IN
=
OUT
+
OUT
−S adalah luas penampang dari kolom. Perlu dicatat bahwa N, G dan L semuanya didefinisikan sebagai fluksi (fluxes) bukan
sebagai laju alir molar [mol/s]:
[ ]
2 secmolar flowrate mol
G G
column tion S cm s
⎡ ⎤
= = ⎢ ⎥
⎣ ⎦
Perhitungan Tinggi ISIAN dari suatu Kolom umumnya melibatkan Koefisien Perpindahan Gas Menyeluruh atau overall gas-phase coefficient (Ky), karena cairan pada umumnya memiliki
AFINITAS yang KUAT pada zat terlarut (absorbat atau absorptif). Driving Force dari peristiwa
perpindahan ini adalah “perbedaan fraksi mol” dalam fasa gasnya (y - y*).
( )
(
)
S G y z
=
S G y z
+ Δ
z
+
N a S z
Δ
N G G L L z z+Δ z[ ]
23mass transfer surface cm
a a
volume of the column cm
⎡ ⎤ ⎢ ⎥ = = ⎢ ⎥ ⎣ ⎦ mol s ⎡ ⎤ ⎢ ⎥ ⎣ ⎦
(
*
)
[ ]
2 ymol
N
K y y
N
cm s
⎡
⎤
=
−
= ⎢
⎥
⎣
⎦
Bagilah Persamaan Laju Perpindahan Massa dengan S dan
Δ
z, didapatkant:( ) ( ) y z z y z N a G z + Δ − − = Δ Karena diinginkan suatu “perbedaan tinggi” (differential
height) dari potongan tersebut, maka berarti:
Δ
z → 0.Didefinisikan, untuk besaran N, digunakan persamaan:
Pemisahan variabel dan pengintegrasian, didapat:
dy N a G dz − =
(
*)
y dy G K a y y dz = − − ( )3(
)
2 1 0 * y H y y G dy H dz K a y y = = − −∫
∫
Mengambil term konstanta ke luar integrasi dan “menukar” batas-batas integrasi tersebut, sehingga:
Ruas KANAN dapat ditulis sebagai hasil kali:
HOG and NOG:
(
)
1 2 0*
y H y yG
dy
H
dz
K a
y
y
=
=
−
∫
∫
HOG NOG OG OG H = H NOG y G H K a =
(
)
1 2*
y OG ydy
N
y y
=
−
∫
The term HOG is called the overall Height of a Transfer Unit (HTU) based on the gas phase. Experimental data show that the HTU
varies less with G than with Kya. The smaller the HTU, the more
efficient is the contacting.
Term NOG disebut overall Number of Transfer Units (NTU) didasarkan pada fasa gas. Besaran tersebut menggambarkan perubahan menyeluruh dalam “zat terlarut” (solute) dalam fraksi mole dibagi dengan rerata fraksi mole dari “driving force”. Semakin
besar NTU, maka semakin besar diperlukan luas permukaan kontak
(extent of contacting).
Diinginkan SOLUSI dari Integral NOG, maka kita ganti y*dengan
Persamaan (2):
(
)
1 2 y OG ydy
N
y
m x
=
−
∫
Menyatukan hasilnya ke dalam persamaan untuk NOG:
1 2 2 2
1
*(
)
y OG yAdy
N
A
y
y
A y
=
−
+
−
∫
Selesaikan (1) untuk
x
, dengan diketahui A = L/(G·m): x y x2 y2A m A m
Integrasikan NOG, hasilnya:
(
)
1 2 2 21
1
*ln
y OG yA
A
y
y
A y
N
A
A
−
+
−
=
−
(
)
(
12 22)
21
1
* *ln
OGA
A
y
y
A y
N
A
A y
y
−
+
−
=
−
−
Memisahkan bagian dalam logaritma menjadi dua bagian:
Diketahui, bahwa Fraksi Absorption
α
:(
)
1 2 2 21
1
1
* *ln
OGA
A
y
y
N
A
A
A
y
y
⎛
−
−
⎞
⎜
⎟
=
+
⎜
⎟
−
⎝
−
⎠
Dengan menggunakan
α
dan melakukanbeberapa transformasi, akhirnya diperolehNOG:
1 2
1 2
*
Jumlah yang DIABSORPSI y y
Jumlah maksimum yang DIABSORPSI y y
α
= = − − 1 1ln 1 OG A A N Aα
α
− ⎛ ⎞ = ⎜ ⎟ − ⎝ − ⎠Jangan keliru antara NTU dan HTU dengan HETP dan jumlah tahap kesetimbangan teoritis n, yang
dapat dihitung dengan Persamaan KREMSER:
1
1
1
ln
ln
A
n
A
α
α
−
⎛
⎞
=
⎜
⎟
−
⎝
⎠
Pada saat Garis Operasi dan Garis keseimbangan tidak hanya lurus tetapi juga paralel, NTU = n dan HTU = HETP. Jika tidak, NTU lebih besar dari atau kurang dari n.
Tinggi KOLOM dapat dihitung dengan 2 cara: H = HOGNOG = n HETP
Perbandingan antara HTU/NTU and HETP
op. line x y eq. line op. line x y eq. line n NTU = op. line x y eq. line n NTU > NTU<n
Pada saat Garis Operasi dan Garis Keseimbangan lurus tapi tidak sejajar (NTU ≠ n), diperlukan suatu formula untuk mengubanya. Dapat ditulis: 1 ln OG A A HETP H A = − OG OG N HETP H n =
Ganti NOG dan ndengan formula yang didapatkan sebelumnya,
maka didapatkan untuk HETP:
Lakukan perhitungan yang sama untuk NOG, didapatkan:
1 ln OG A A N n A = −
Akhirnya, diinginkan menghitung koefisien perpindahan massa volumetrik menyeluru (Kya). Diketahui, bahwa:
OG OG y H G H N K a = =
Solusi untuk Kya, didapatkan: y OG
G N K a
H =
Desorpsi (Stripping):
Pendekatan Perpindahan Massa (HTU, NTU)
Sekarang kita fokus pada masalah Stripping, dengan problem
sebagai berikut: aliran cairan tercemar keluar dari suatu proses akan dipulihkan dari polutannya dalam rangka untuk membersihkan cairan tersebut.
L, x1 G, y1 T, p Process G, y2 L, x2 z = 0 z = H x y
Pertama, diperlukan Neraca Massa di sekitar “amplop hijau”, di bagian bawah kolom, yang terkait dengan Garis Operasi, melalui titik (x1, y1):
(
1)
1 ( )1 L y x x y G = − +Pada keadaan kesetimbangan:
2 * y ( ) x m = 1 1 G y + L x = L x + G y
1 2 2 1 m a k s ( . , ) L f L G f G ⎛ ⎞ = ⎜ ⎟ → ∈ ⎝ ⎠
Garis Kesetimbangan dan Garis Operasi dapat dibuat dalam suat diagram seperti di sebelah kanan ini. Dari Garis Operasi dengan kemiringan terbesar (L/G)maks, dihitung (L/G) dengan
formula berikut: y* = m x y2 max G L ⎟ ⎠ ⎞ ⎜ ⎝ ⎛ G L x2 x y1 x1 y N G G L L z z+Δ z Sebagai persamaan ketiga, kita perlukan suatu persamaan
laju perpindahan massa. Diambil irisan kecil terkait dari kolom. Neraca massa "sisi cair" dari irisan kecil tersebut:
liq liq mass transfer
IN = OUT + OUT − ( ) ( ) mol S L x z z S L x z N a S z s ⎡ ⎤ + Δ = + Δ ⎢ ⎥ ⎣ ⎦
Fluksi N melibatkan koefisien perpindahan menyeluruh
fase cair Kxdengan “driving force” (x - x*):
(
*)
x
N = K x − x
Desorpsi (Stripping):
(
*)
( )3 xdx
L K a x x
dz = −
Bagilah persamaan laju perpindahan massa dengan S
dan
Δ
z, diperoleh:Dengan
Δ
z →0, dkemudian menggunakan definisi N:Pemisahan variabel dan integrasi, menghasilkan:
2 1 0 * x H x x L dx H dz K a x x = = −
∫
∫
HOL NOLHOL adalah overall Height of a Transfer Unit (HTU) untuk fasa cair.
( ) ( ) x z z x z L N a z + Δ − = Δ
NOL adalah overall Number of Transfer Units (NTU) untuk fasa cair.
OL x L H K a =
(
)
2 1*
x OL xdx
N
x
x
=
−
∫
Desorpsi (Stripping):
Diketahui, bahwa fraction of stripping σ: 2 1 2 1 Jumlah yang didesorpsi x x Jumlah maksimum yang didesorpsi x x∗
−
= =
−
σ
Kemudian, pengertian Faktor stripping, S: S mG
L
=
Hasil integral dari NOL dapat dicari dengan cara
yang sama seperti dalam kasus absorpsi:
2 1 1 1 1 1 1ln OL S S x x N S S S x x ∗ ∗ ⎛ − − ⎞ ⎜ ⎟ = + ⋅ ⎜ ⎟ − ⎝ − ⎠
Akhirnya, setelah berbagai transformasi, didapat: 1
1ln 1 OL S S N S σ σ − ⎛ ⎞ = ⎜⎜ ⎟⎟ − ⎝ − ⎠