Tugas Kimia 2
Page 1
BAB VII
SISTEM KOLOID
INDIKATOR Menjelaskan pengelompokan campuran menjadi larutan, koloid, dan suspensi.
Mendeskripsikan perbedaan larutan, koloid, dan suspensi berdasarkan sifat campurannya, fasanya dan ukuran partikelnya.
Mendeskripsikan pembuatan koloid dapat dengan cara kondensasi, desintegrasi, dan atau gabungan dari keduanya.
Mendeskripsikan pengelompokan sifat khas koloid menjadi sifat optik dan elektrik.
Mendeskripsikan akibat hamburan cahaya terhadap sifat optik dari koloid dideskripsikan dengan jelas.
Mengamati adanya efek Tyndal dan gerak Brown melalui percobaan. Menunjukkan sifat kinetik dari koloid.
Sifat elektrik dari koloid terjadi dijelaskan sebagai akibat adanya muatan (ion-ion) yang bergerak dalam medan listrik
Mendeskripsikan elektroforesis.
Mengamati elekroforesis, koagulasi, gerak Brown, dan kesetabilan koloid dari hasil percobaan. Mendeskripsikan definisi zat terdispersi dan dan zat/medium pendispersi.
Mendeskripsikan pengelompokan koloid berdasarkan wujud zat terdispersi dan pendispersinya. Mendeskripsikan pengelompokan koloid menjadi koloid liofil dan koloid liofob.
Menjelaskan penggunaan koloid dijelaskan berdasarkan proses pembentukannya. Melakukan pengkajian pustaka mengenai penggunaan koloid.
Flashback
Ketika kelas satu, anda telah mempelajari konsep campuran/dispersi. Dispersi dapat dibedakan menjadi dispersi homogen (larutan) dan dispersi heterogen (suspensi dan koloid). Contoh dispersi adalah larutan garam (oralit) dan lumpur. Namun, tahukah anda bahwa busa, es krim, cat, asap, dan kabut juga merupakan dispersi? Dispersi yang seperti apa dan bagaimana sifatnya? Apakah seperti larutan oralit? Ataukah seperti air kopi?
A. SISTEM DISPERSI/CAMPURAN Perhatikan hal-hal berikut:
1. Apa yang terjadi bila gula dilarutkan dalam air? Bagaimana keadaan campuran yang terbentuk? Apakah partikel gula masih terlihat?
2. Apa yang terjadi bila satu sendok susu dimasukkan dalam air kemudian diaduk? Bagaimana keadaan campuran yang terbentuk? Apakah partikel susu bercampur dengan air?
3. Apa yang terjadi bila kopi dicampur dengan air kemudian diaduk? Bagaimana keadaan campuran yang terbentuk? Apakah kopi bercampur dengan air?
Apabila suatu zat dicampurkan dengan zat lain, maka akan terjadi penyebaran secara merata dari suatu zat ke dalam zat lain yang disebut sistem dispersi atau campuran. Zat yang didispersikan disebut fase terdispersi, sedangkan medium yang digunakan untuk mendispersikan disebut medium pendispersi. Contoh: susu bubuk dimasukkan ke dalam air hangat membentuk sistem dispersi, air sebagai medium pendispersi, dan susu bubuk sebagai zat terdispersi. (Analogikan dengan larutan, ada zat terlarut dan medium pelarut)
Berdasarkan ukuran partikelnya, sistem dispersi dibedakan menjadi tiga kelompok, yaitu suspensi, koloid, dan larutan.
Larutan (dispersi molekuler)
Larutan merupakan sistem dispersi yang ukuran diameter partikel zat terdispersinya sangat kecil (< 10-7
Tugas Kimia 2
Page 2
KoloidKoloid merupakan sistem dispersi yang ukuran diameter partikel zat terdispersinya 10-7 - 10-5 cm
(1 – 100 nm), secara makroskopis tampak homogen, tetapi sebenarnya heterogen (dengan mikroskop ultra dapat dibedakan antara partikel pendispersi dengan partikel terdispersi). Contoh: susu cair, asap, dan kabut.
Suspensi
Suspensi merupakan sistem dispersi yang ukuran diameter partikel zat terdispersinya relatif besar (> 10-5 cm atau > 100 nm) dan tersebar merata dalam medium pendispersinya. Pada umumnya suspensi
merupakan campuran heterogen. Contoh: pasir yang dicampur dengan air, air sungai, dan air kopi. Dalam sistem dispersi, partikel terdispersi dapat diamati dengan mikroskop biasa atau dengan mata telanjang.
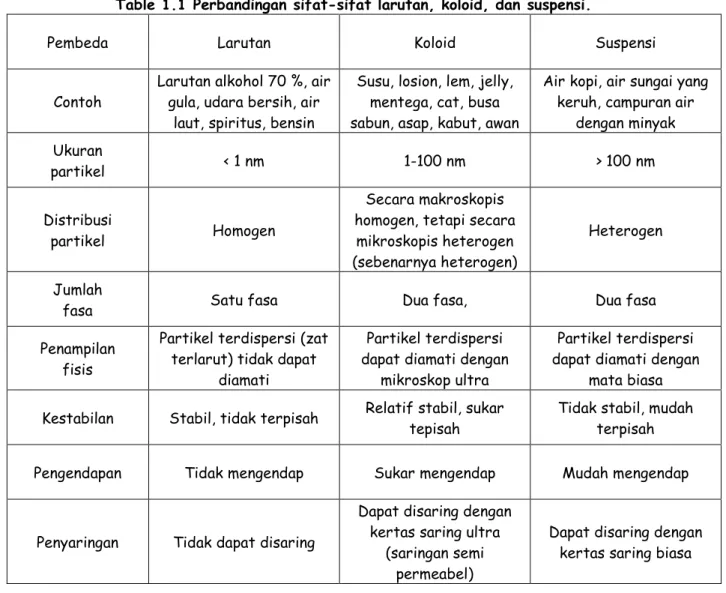
Table 1.1 Perbandingan sifat-sifat larutan, koloid, dan suspensi.
Pembeda Larutan Koloid Suspensi
Contoh
Larutan alkohol 70 %, air gula, udara bersih, air
laut, spiritus, bensin
Susu, losion, lem, jelly, mentega, cat, busa sabun, asap, kabut, awan
Air kopi, air sungai yang keruh, campuran air
dengan minyak Ukuran partikel < 1 nm 1-100 nm > 100 nm Distribusi partikel Homogen Secara makroskopis homogen, tetapi secara
mikroskopis heterogen (sebenarnya heterogen)
Heterogen Jumlah
fasa Satu fasa Dua fasa, Dua fasa
Penampilan fisis
Partikel terdispersi (zat terlarut) tidak dapat
diamati
Partikel terdispersi dapat diamati dengan
mikroskop ultra
Partikel terdispersi dapat diamati dengan
mata biasa Kestabilan Stabil, tidak terpisah Relatif stabil, sukar tepisah Tidak stabil, mudah terpisah
Pengendapan Tidak mengendap Sukar mengendap Mudah mengendap
Penyaringan Tidak dapat disaring
Dapat disaring dengan kertas saring ultra
(saringan semi permeabel)
Dapat disaring dengan kertas saring biasa B. SISTEM KOLOID
Telah dibahas bahwa asap, dan kabut merupakan koloid. Apa yang membedakan kedua zat tersebut sehingga masing-masing mempunyai sifat yang berbeda pula? Pada saat wajah anda terkena asap, wajah anda akan berdebu, sedangkan pada saat wajah anda tersapu kabut, wajah akan terasa lembab. Mengapa demikian?
Asap adalah zat padat (debu) yang terdispersi dalam udara (gas) sehingga bila terkena asap, wajah akan merasakan keberadaan debu. Kabut adalah zat cair (air) yang terdispersi dalam udara (gas) sehingga bila terkena kabut, kita akan merasakan keberadaan air (lembab). Jadi, perbedaan koloid terletak pada jenis fase terdispersi dan medium pendispersinya.
Tugas Kimia 2
Page 3
Sistem koloid dapat dibedakan menjadi 3, yaitua. Aerosol, adalah koloid yang medium pendispersinya gas.
b. Sol, yaitu koloid yang mempunyai fase terdispersi padat. Sol terdiri atas sol padat, sol (sol cair), dan sol gas (aerosol padat).
c. Emulsi, yaitu koloid yang mempunyai fase cair. Emulsi dapat dibedakan menjadi emulsi emulsi padat, emulsi cair (emulsi), dan emulsi gas (aerosol cair). Emulsi terbentuk karena pengaruh suatu pengemulsi (emulgator). Contohnya adalah sabun yang dapat mengemulsikan minyak ke dalam air. Jika campuran minyak dengan air dikocok, maka akan diperoleh suatu campuran yang segera memisah jika didiamkan. Akan tetapi, jika sebelum dikocok ditambahkan sabun atau detergen, maka diperoleh campuran yang stabil yang disebut emulsi.
d. Buih yaitu koloid yang fase terdispersinya gas, dibedakan menjadi buih padat dan buih cair (buih). e. Gel, adalah koloid setengah kaku (antara padat dan cair). Gel terbentuk dari sol yang fase/zat
terdispersinya mengadsorpsi medium pendispersinya. Contoh: agar-agar, lem kanji, selai, gelatin, gel sabun, dan gel silika. Gel dapat terbentuk dari suatu sol yang zat terdispersinya mengadsorpsi medium dispersinya, sehingga terjadi koloid yang agak padat.
Tabel 1.2 Jenis-jenis sistem koloid Fase
Terdispersi
Medium
pendispersi Nama Contoh
Padat Cair Sol Cat, lem kanji, tinta, tanah liat ,sol
emas, semir cair Padat Padat Sol padat mutiara, paduan logam (alloy), Gelas berwarna, intan hitam,
stainless steel, perunggu Padat Gas Aerosol padat Asap, debu di udara, buangan knalpot, cat semprot
Cair Gas Aerosol cair Kabut, awan, parfum, hairspray,
obat nyamuk semprot
Cair Cair Emulsi Susu, santan, mayonaisse, minyak
ikan, lotion
Cair Padat Emulsi padat Agar-agar, keju, mentega, margarin, nasi, lateks, selai, mutiara
Gas Cair Buih Busa sabun, krim kocok, putih telur
Gas Padat Buih padat Karet busa, batu apung, gabus, roti,
kerupuk C. PEMBUATAN KOLOID
Ukuran partikel koloid terletak antara partikel larutan dan susupensi, sehingga sistem partikel koloid dapat dibuat dengan pengelompokkan (agregasi) partikel larutan (cara ini disebut cara kondensasi) atau dengan menghaluskan partikel-partikel kasar dari suspensi, kemudian mendispersikannya ke dalam medium pendispersi (cara dispersi).
1. Cara Kondensasi
Dengan cara kondensasi, partikel larutan sejati (molekul atau ion) bergabung menjadi partikel koloid. Cara ini dapat dilakukan dengan reaksi-reaksi kimia, seperti reaksi redoks, hidrolisis, dan dekomposisi rangkap, atau dengan cara fisika: pengembunan uap dan pergantian pelarut.
Cara Kimia
larutan koloid suspensi
Tugas Kimia 2
Page 4
a. Reaksi Redoks (Reduksi-Oksidasi)Reaksi redoks adalah reaksi yang disertai perubahan bilangan oksidasi. Contoh 1:
Pembuatan sol belerang dari reaksi antara hidrogen sulfida (H2S) dengan belerang dioksida (SO2), yaitu
dengan mengalirkan gas H2S ke dalam larutan SO2.
2 H2S(g) + SO2(aq) ⎯⎯→ 2 H2O(l) + 3 S (koloid)
Contoh 2:
Pembuatan sol emas dari reaksi antara larutan HAuCl4 dengan larutan K2CO3 dan HCHO (formaldehida).
2 HAuCl4(aq) + 6 K2CO3(aq) + 3 HCHO(aq) ⎯⎯→ 2 Au(koloid) + 5 CO2(g) + 8 KCl(aq) + KHCO3(aq) + 2 H2O(l)
b. Reaksi Hidrolisis
Hidrolisis adalah reaksi suatu zat dengan air. Contoh:
Pembuatan sol Fe(OH)3 dari hidrolisis FeCl3. Apabila ke dalam air mendidih ditambahkan larutan FeCl3,
maka akan terbentuk sol Fe(OH)3.
FeCl3(aq) + 3 H2O(l) ⎯⎯→ Fe(OH)3 (koloid) + 3 HCl(aq)
c. Reaksi Dekomposisi Rangkap Contoh 1:
Sol As2S3 dapat dibuat dari reaksi antara larutan H3AsO3 dengan larutan H2S.
2 H3AsO3(aq) + 3 H2S(aq) ⎯⎯→ As2S3(koloid) + 6 H2O(l)
Contoh 2:
Sol AgCl dapat dibuat dengan mencampurkan larutan perak nitrat encer dengan larutan HCl encer. AgNO3(aq) + HCl(aq) ⎯⎯→ AgCl(koloid) + HNO3(aq)
Cara Fisika
d. Pengembunan uap
Uap raksa yang dialirkan melalui air dingin dapat membentuk sol raksa. e. Penggantian Pelarut
Selain dengan cara-cara kimia seperti di atas, koloid juga dapat terjadi dengan penggantian pelarut. Contoh:
Apabila larutan jenuh kalsium asetat dicampur dengan alkohol, maakan terbentuk suatu koloid berupa gel. 2. Cara Dispersi
Dengan cara dispersi, partikel kasar dipecah menjadi partikel koloid. Cara dispersi dapat dilakukan secara mekanik, peptisasi, atau dengan loncatan bunga listrik (cara busur Bredig).
a. Cara Mekanik
Menurut cara ini, butir-butir kasar digerus dengan lumping atau penggiling koloid sampai diperoleh tingkat kehalusan tertentu, kemudian diaduk dengan medium dispersi.
Contoh:
Sol belerang dapat dibuat dengan menggerus serbuk belerang bersamasama dengan suatu zat inert (seperti gula pasir), kemudian mencampur serbuk halus itu dengan air.
b. Cara Peptisasi
Peptisasi adalah cara pembuatan koloid dari butir-butir kasar atau dari suatu endapan dengan bantuan suatu zat pemeptisasi (pemecah). Zat pemeptisasi memecahkan butir-butir kasar menjadi butir-butir koloid.
Contoh:
Agar-agar dipeptisasi oleh air, nitroselulosa oleh aseton, karet oleh bensin, dan lain-lain. Endapan NiS dipeptisasi oleh H2S dan endapan Al(OH)3 oleh AlCl3.
c. Cara Busur Bredig (elektrodispersi)
Tugas Kimia 2
Page 5
Mula-mula atom-atom logam akan terlempar ke dalam air, lalu atom-atom tersebut mengalami kondensasi, sehingga membentuk partikel koloid. Jadi, cara busur ini merupakan gabungan cara dispersi dan cara kondensasi.Contoh:
Pembuatan sol emas dan sol platina. D. SIFAT-SIFAT KOLOID
Chema’s corner
Pada hari minggu yang indah dan berkabut, si chema dengan penuh semangat memacu motornya menuju rumah chemie. Tak lupa chema memakai helm dan menyalakan lampu motornya. Ketika berkas cahaya lampu motornya menembus kabut, berkas cahaya tampak jelas. Mengapa bisa demikian?
Chema menuju rumah chemie melewati hutan yang penuh pepohonan yang rindang serindang hati chema. Berkas sinar matahari yang melewati celah daun pepohonan tampak jelas. Mengapa demikian?
Bioskop saat itu akan memutar film “Si Komo”. Pada pintu ruang bioskop, tertempel sebuah peringatan ‘DILARANG MEROKOK’. Chema memberitahu chemie bahwa asap rokok dapat mengganggu pemutaran film. Mengapa bisa demikian?
Beberapa sifat khas koloid yang membedakan dengan sistem dispersi yang lain yaitu: 1. Sifat Optik (Efek Tyndall) ditemukan oleh John Tyndall
Penampilan sistem koloid pada umumnya keruh, tapi beberapa koloid tampak bening dan sukar dibedakan dengan larutan sejati. Salah satu cara yang sangat sederhana untuk mengenali koloid yaitu dengan melewatkan seberkas sinar kepada obyek yang diamati.
Larutan sejati akan meneruskan cahaya (transparan), sedangkan koloid akan menghamburkan cahaya tetapi partikel terdispersinya tidak tampak. Suspensi akan menghamburkan cahaya, tetapi partikel terdispersinya tampak. Jadi, Efek Tyndall adalah peristiwa penghamburan cahaya oleh partikel koloid. 2. Sifat Kinetik (Gerak Brown) ditemukan oleh Robert Brown
Apabila susu didiamkan untuk beberapa lama, kita tidak akan mendapatkan endapan susu. Mengapa demikian? Hal ini dikarenakan adanya gerak Brown.
Gerak Brown adalah gerak acak (gerak tak beraturan; patah-patah; zig-zag) partikel koloid dalam medium pendispersinya. Gerak Brown dapat diamati menggunakan mikroskop ultra
Pada dasarnya, partikel-partikel dalam zat selalu bergerak. Gerak Brown terjadi sebagai akibat adanya tumbukan dari molekul-molekul pendispersi terhadap partikel terdispersi, sehingga partikel terdispersi akan terlontar. Lontaran tersebut akan mengakibatkan partikel terdispersi menumbuk partikel terdispersi yang lain dan akibatnya partikel yang tertumbuk akan terlontar. Peristiwa ini terjadi terus menerus yang diakibatkan karena ukuran partikel yang terdispersi relatif besar dibandingkan medium pendispersinya. Gerak Brown dipengaruh oleh ukuran partikel dan suhu.
Dalam suspensi tidak terjadi gerak Brown, karena ukuran partikel cukup besar sehingga tumbukan yang dialaminya setimbang. Partikel zat terlarut juga mengalami gerak Brown akan tetapi tidak dapat diamati. Gerak Brown merupakan salah satu faktor yang menstabilkan koloid. Partikel-partikel koloid relatif stabil, karena partikelnya bergerak terus-menerus, maka gaya gravitasi dapat diimbangi sehingga tidak terjadi sedimentasi (pengendapan).
3. Sifat Elektrik (Muatan Koloid)
Muatan koloid merupakan salah satu sifat koloid yang terpenting. Muatan koloid juga merupakan faktor yang menstabilkan koloid, di samping gerak Brown. Semua partikel koloid mempunyai muatan sejenis (positif atau negatif). Oleh karena bermuatan sejenis maka partikel-partikel koloid saling tolak-menolak, sehingga terhindar dari pengelompokan antarsesama partikel koloid itu (jika partikel-partikel koloid saling bertumbukan dan kemudian bersatu, maka lama-kelamaan dapat terbentuk partikel yang cukup besar dan akhirnya mengendap).
Bagaimana partikel koloid memiliki muatan? Partikel koloid dapat memiliki muatan karena adanya proses adsorpsi dan proses ionisasi gugus permukaan partikel koloid. Beberapa sifat elektrik koloid antara lain:
Tugas Kimia 2
Page 6
Elektroforesis adalah pergerakan partikel koloid dalam medan listrik. Apabila ke dalam sistem koloid dimasukkan dua batang elektrode, kemudian dihubungkan dengan sumber arus searah, maka partikel koloid akan bergerak ke salah satu elektrode bergantung pada jenis muatannya. Koloid bermuatan negatif akan bergerak ke anode (elektrode positif), sedangkan koloid yang bermuatan positif bergerak ke katode (elektrode negatif). Dengan demikian, elektroforesis dapat digunakan untuk menentukan jenis muatan koloid.b. Adsorpsi
Bagaimanakah partikel koloid mendapatkan muatan listrik? Partikel koloid memiliki kemampuan menyerap ion atau muatan listrik pada permukaannya. Oleh karena itu, partikel koloid menjadi bermuatan listrik. Penyerapan pada permukaan ini disebut adsorpsi (jika penyerapan sampai ke bawah permukaan disebut absorpsi).
Adsorpsi adalah proses penyerapan suatu zat di permukaan zat lain. Sebagai contoh, penyerapan air oleh kapur tulis). Sol Fe(OH)3 dalam air mengadsorpsi ion positif sehingga bermuatan positif, sedangkan sol
As2S3 mengadsorpsi ion negatif sehingga bermuatan negatif. Contoh pemanfaatan sifat adsorpsi koloid
yaitu: proses pemurnian gula tebu, proses penyembuhan sakit perut dengan obat norit, dan proses penjernihan air minum.
c. Koagulasi
Koagulasi atau penggumpalan adalah peristiwa pengendapan partikel-partikel koloid sehingga fase terdispersi terpisah dari medium pendispersinya. Koagulasi disebabkan oleh kestabilan untuk mempertahankan partikel-partikel agar tetap tersebar dalam medium pendispersinya.
Koagulasi dapat diakukan dengan cara mekanik (misal pemanasan, pendinginan, dan pengadukan) dan dengan cara kimiawi, misal penetralan silang (pencampuran dua jenis koloid yang bermuatan berlawanan) atau penghilangan muatan elektrolisis, dan penambahan elektrolit (pengkoagulasian karet alam/lateks dengan asam asetat).
Contoh proses-proses yang memanfaatkan sifat koagulasi: proses pengolahan karet, penjernihan air dengan tawas, proses terjadinya delta pada muara, proses penggumpalan debu atau asap pabrik dengan pesawat Cottrel.
4. Koloid Pelindung
Pada beberapa proses, suatu koloid harus dipecahkan. Misalnya, koagulasi lateks. Di lain pihak, koloid perlu dijaga supaya tidak rusak. Suatu koloid dapat distabilkan dengan menambahkan koloid lain yang disebut koloid pelindung. Koloid pelindung adalah koloid yang berfungsi melindungi koloid lain supaya tidak terjadi koagulasi. Koloid pelindung ini akan membungkus partikel zat terdispersi, sehingga tidak dapat lagi mengelompok.
a. Pada pembuatan es krim digunakan gelatin untuk mencegah pembentukan kristal besar es atau gula. b. Cat dan tinta dapat bertahan lama karena menggunakan suatu koloid pelindung.
c. Kasein dalam susu melindungi minyak atau lemak dalam medium cair.
d. Lesitin merupakan pelindung yang menstabilkan butiran-butiran halus air dalam margarin. e. Larutan gom digunakan untuk melindungi partikel-partikel karbon dalam tinta gambar.
Berdasarkan interaksi antara partikel terdispersi dengan medium pendispersinya, koloid dengan medium pendispersi cair dibedakan atas koloid liofil dan koloid liofob. Koloid liofil (bahasa Yunani, lio= cairan, philia = suka) adalah koloid yang fase terdispersinya dapat menarik medium pendispersi karena gaya tarik antara partikel-partikel terdispersi dengan medium pendispersinya kuat. Koloid liofob (bahasa Yunani, lio= cairan, phobia = takut) adalah sistem koloid yang fase terdispersinya tidak dapat menarik/mengikat medium pendispersinya.
Contoh koloid liofil adalah agar-agar. Dalam air panas, agar-agar berupa sol, jika didinginkan, kembali menjadi agar-agar padat yang berbentuk gel. Sebaliknya, jika gel agar-agar dipanaskan, akan kembali menjadi sol agar-agar. Hal ini menunjukkan bahwa koloid liofil bersifat reversible (dapat balik).
Koloid liofob, contohnya sol emas, bersifat irreversibel. Jika medium pendispersi sol emas diambil, sol emas akan berubah menjadi emas padat, tetapi emas padat tidak bisa kembali menjadi sol emas meskipun ditambah medium pendispersi.
Koloid Liofil Koloid Liofob
Tugas Kimia 2
Page 7
Terdiri atas zat organik Terdiri atas zat anorganik
Stabil:
Dapat dibuat dengan konsentrasi relatif besar Sukar diendapkan dengan penambahan elekrolit
Kurang stabil:
Hanya stabil pada konsentrasi kecil
Mudah menggumpal/mengendap dengan penambahan elektrolit
Kekentalannya tinggi Kekentalannya rendah
Reversibel Irreversibel
Tidak menunjukkan gerak Brown dan efek Tyndall Gerak Brown dan efek Tyndall sangat jelas Tidak menunjukkan elektroforesis Menunjukkan peristiwa elektroforesis
Dibuat dengan cara disperse Dibuat secara kondensasi
Dapat dibuat gel Hanya beberapa yang dapat dibuat gel
E. PEMURNIAN KOLOID 1. Dialisis
Dialisis adalah cara mengurangi ion-ion pengganggu yang terdapat dalam sistem koloid denan menggunakan selaput semi permeabel. Dalam proses ini, sistem koloid dimasukkan ke dalam suatu kantong koloid, lalu kantong koloid itu dimasukkan ke dalam bejana yang berisi air mengalir. Kantong koloid terbuat dari selaput semipermiabel, yaitu selaput yang dapat melewatkan partikelpartikel kecil, seperti ion-ion atau molekul sederhana, tetapi menahan koloid. Dengan demikian, ion-ion keluar dari kantong dan hanyut bersama air. Prinsip dialisis digunakan pada proses cuci darah bagi penderita ginjal (blood dialysis).
2. Ultrafiltrasi
Pada proses ini, medium pendispersi dipaksa menembus membrane semipermeabel dengan bantuan pompa air atau pompa vakum.
F. PEMANFAATAN KOLOID
Dalam kehidupan sehari-hari, kita sering menggunakan bahan-bahan kimia berbentuk koloid. Bahan-bahan kimia tersebut dibuat oleh industri. Mengapa harus koloid? Oleh karena koloid merupakan satu-satunya cara untuk menyajikan suatu campuran dari zat-zat yang tidak saling melarutkan secara “homogen” dan stabil (pada tingkat makroskopis atau tidak mudah rusak).
Industri Kosmetik Bahan kosmetik, seperti foundation, pembersih wajah, sampo, pelembap badan, deodoran umumnya berbentuk koloid yaitu emulsi.
Industri Tekstil Pewarna tekstil berbentuk koloid karena mempunyai daya serap yang tinggi, sehingga dapat melekat pada tekstil.
Industri Farmasi Banyak obat-obatan yang dikemas dalam bentuk koloid agar stabil atau tidak mudah rusak.
Industri Sabun dan Detergen Sabun dan detergen merupakan emulgator untuk membentuk emulsi antara kotoran (minyak) dengan air, sehingga sabun dan detergen dapat membersihkan kotoran, terutama kotoran dari minyak.
Tugas Kimia 2
Page 8
1. Diketahui beberapa sistem dispersi sebagai berikut:a. Udara b. Kabut c. Susu cair d. Air kopi e. Air gula
Yang merupakan larutan adalah…. A. a dan c
B. a dan e C. b dan c D. c dan d E. c dan e
2. Partikel koloid memiliki ukuran .... A. lebih besar dari 10–3 cm
B. lebih kecil dari 10–9 cm
C. antara 10–3 cm dan 10–5 cm
D. antara 10–7 cm dan 10–9 cm
E. antara 10–5 cm dan 10–7 cm
3. Sistem koloid dapat dibuat dari suspensi dengan cara peptidasi yaitu dengan cara….
A. butir-butir kasar digerus dengan lumping atau penggiling koloid sampai diperoleh tingkat kehalusan tertentu
B. digunakan sebagai elektrode yang dicelupkan dalam medium dispersi, kemudian diberi loncatan listrik di antara kedua ujungnya
C. melakukan penggantian pelarut
D. membuat koloid dari butir-butir kasar atau dari suatu endapan dengan bantuan zat pemecah E. mengalirkan uap melalui air dingin
4. Berikut ini yang bukan merupakan cara pembuatan sistem koloid dari larutan adalah…. A. reaksi mekanik
B. reaksi redoks C. reaksi hidrolisis
D. reaksi dekomposisi rangkap E. pengembunan uap
5. Sistem koloid dapat dimurnikan dengan cara ultrafiltrasi, yaitu…. A. mengurangi ion-ion pengganggu yang terdapat dalam sistem koloid B. menggunakan gelatin untuk mencegah pembentukan kristal besar
C. medium pendispersi dipaksa menembus membran semipermeabel dengan bantuan pompa D. menggerakkan partikel koloid dalam medan listrik
E. menyaring koloid menggunakan kertas saring
6. Pemurnian sistem koloid dapat dimanfaatkan dalam proses cuci darah yaitu dialisis. Prinsip dialisis yaitu….
A. menyerap suatu zat di permukaan zat lain B. menggunakan aliran listrik dalam larutan C. elektrolisis larutan untuk memperoleh endapan
D. mengurangi ion-ion pengganggu yang terdapat dalam sistem koloid E. memberikan zat pemecah untuk menghilangkan zat penggangu
7. Salah satu sifat sistem koloid adalah sifat elektrik. Sifat elektrik sistem koloid meliputi…. A. elektroforesis
Tugas Kimia 2
Page 9
C. ultrafiltrasiD. efek Tyndall E. dialisis
8. Suatu zat setelah disaring diperoleh filtrat yang tampak jernih. Filtrat tersebut ternyata dapat menghamburkan cahaya. Dari data tersebut dapat disimpulkan bahwa….
A. filtrat merupakan larutan karena tampak jernih B. filtrat merupakan suspensi karena dapat disaring C. filtrat merupakan koloid karena menghamburkan cahaya D. zat merupakan larutan karena dapat disaring
E. zat merupakan koloid karena dapat disaring 9. Sifat kinetik sistem koloid terjadi karena….
A. adanya pergerakan partikel koloid dalam medan listrik akibat proses adsorpsi dan koagulasi B. adanya tumbukan dari molekul-molekul pendispersi terhadap partikel terdispersi
C. adanya pengendapan partikel-partikel koloid karena gaya gravitasi
D. adanya proses adsorpsi dan proses ionisasi gugus permukaan partikel koloid E. terjadi interaksi fase terdispersi koloid yang menarik medium pendispersi 10. Partikel-partikel sistem koloid memiliki muatan . Hal ini dikarenakan….
A. adanya pergerakan partikel koloid dalam medan listrik akibat proses adsorpsi dan koagulasi B. adanya tumbukan dari molekul-molekul pendispersi terhadap partikel terdispersi
C. adanya pengendapan partikel-partikel koloid karena gaya gravitasi
D. adanya proses adsorpsi dan proses ionisasi gugus permukaan partikel koloid E. terjadi interaksi fase terdispersi koloid yang menarik medium pendispersi
11. Elektroforesis dapat digunakan untuk menentukan jenis muatan koloid karena dalam medan listrik…. A. partikel koloid akan bergerak ke salah satu elektrode yang muatannya sama.
B. partikel koloid akan bergerak ke salah satu elektrode yang muatannya berlawanan
C. gugus permukaan partikel koloid akan menyerap muatan sehingga jenis muatannya dapat diketahui D. terjadi loncatan elektron sehingga mempengaruhi muatan koloid
E. terjadi pengendapan akibat gaya gravitasi
12. Gerak Brown dapat menstabilkan sistem koloid karena….
A. ukuran partikel yang terdispersi relatif kecil dibandingkan medium pendispersinya sehingga gaya gravitasi terimbangi dan tidak terjadi pengendapan
B. adanya tumbukan yang seimbang antara molekul-molekul pendispersi terhadap partikel terdispersi C. ukuran partikel cukup besar sehingga tumbukan yang dialaminya setimbang
D. tumbukan antar partikel-partikel koloid menyebabkan ukuran partikel mengecil sehingga akan melarut sempurna dan tidak mengendap
E. partikel koloid bergerak terus-menerus, gaya gravitasi dapat diimbangi sehingga tidak terjadi sedimentasi
13. Kenaikan suhu akan berpengaruh pada gerak Brown yaitu….
A. makin tinggi suhu makin cepat gerak Brown karena energi kinetik molekul medium meningkat, sehingga menghasilkan tumbukan yang lebih kuat.
B. makin tinggi suhu makin lambat gerak Brown karena energi kinetik molekul medium turun, sehingga menghasilkan tumbukan yang lebih lemah.
C. makin tinggi suhu makin cepat gerak Brown karena partikel-partikel koloid akan semakin melarut D. makin tinggi suhu makin lambat gerak Brown karena partikel-partikel koloid akan semakin melarut
sehingga tidak dapat dibedakan antara medium pendispersi dengan partikelnya.
E. tidak ada pengaruh suhu dengan gerak Brown karena gerak Brown bukan fungsi termodinamis 14. Salah satu sifat koloid yang dimanfaatkan dalam penjernihan air adalah koagulasi, yaitu ….
Tugas Kimia 2
Page 10
B. kemampuan menyerap ion atau muatan listrik pada permukaannya.C. pengendapan partikel-partikel koloid sehingga fase terdispersi terpisah dari medium pendispersinya
D. partikel koloid saling bertumbukan dan kemudian bersatu
E. terjadinya interaksi fase terdispersi koloid yang menarik medium pendispersi
15. Agar tidak rusak, ke dalam sistem koloid ditambahkan sistem koloid pelindung. Berikut ini yang bukan merupakan aplikasi sistem koloid pelindung yaitu….
A. pada pembuatan es krim digunakan gelatin untuk mencegah pembentukan kristal besar es B. kasein dalam susu melindungi minyak atau lemak dalam medium cair
C. lesitin merupakan pelindung yang menstabilkan butiran-butiran halus air dalam margarin D. larutan gom digunakan untuk melindungi partikel-partikel karbon dalam tinta gambar E. pada lateks karet ditambahkan asam cuka supaya lateks stabil
16. Asap dan kabut merupakan sistem dispersi. Perbedaan antara keduanya adalah…. A. asap merupakan aerosol cair, kabut merupakan aerosol padat
B. asap merupakan aerosol padat, kabut merupakan aerosol cair C. asap merupakan sol, kabut merupakan aerosol
D. asap merupakan aerosol, kabut merupakan sol E. asap merupakan suspensi, kabut merupakan koloid
17. Darah merupakan sistem koloid. Fase terdispersi dan medium pendispersi darah berturut-turut adalah…. A. cair, cair B. gas, cair C. cair, gas D. cair, padat E. padat, cair
18. Suatu gas yang terdispersi dalam gas bukan merupakan sistem koloid karena…. A. gas dengan gas akan bereaksi sehingga membentuk senyawa
B. gas tidak bercampur dengan gas sehingga merupakan suspensi C. campuran gas sangat labil sehingga akan segera terpisah
D. campuran gas dengan gas dapat dibedakan sehingga merupakan suspensi E. campuran gas dengan gas bersifat homogen sehingga merupakan larutan 19. Sistem koloid dengan fase terdispersi padat disebut….
A. emulsi B. buih C. gel D. sol E. aerosol
20. Sistem koloid berikut yang tidak termasuk emulsi adalah…. A. susu
B. santan C. krim kocok D. krim tangan E. losion
21. Jika campuran minyak dengan air dikocok, maka akan diperoleh suatu campuran yang segera memisah jika didiamkan. Akan tetapi, jika sebelum dikocok ditambahkan sabun atau detergen, maka diperoleh campuran yang stabil. Hal ini menunjukkan bahwa….
Tugas Kimia 2
Page 11
C. sabun merupakan koloid karena memiliki sifat adsorpsiD. koloid dapat dibuat secara hidrolisis dari suatu suspensi
E. gel dapat terbentuk dari suatu sol yang zat terdispersinya mengadsorpsi medium dispersinya 22. Sistem koloid yang partikel-partikelnya tidak menarik molekul pelarutnya disebut….
A. koloid liofob B. koloid liofil C. aerosol D. sol gel
E. koloid pelindung
23. Dibandingkan dengan sol liofil, maka sol liofob…. A. lebih mengadsorpsi mediumnya dibanding sol liofil B. lebih menunjukkan gerak Brown dan efek Tyndall C. kekentalannya lebih tinggi
D. lebih sukar diendapkan E. lebih stabil
24. Zat-zat berikut yang termasuk sol liofil yaitu…. A. detergen, kuningan, agar-agar,
B. sol belerang, agar-agar, kanji C. perunggu, kuningan, gelatin D. sabun, kanji, gelatin
E. sol logam, sol sulfida, detergen
25. Produk-produk industri banyak dipasarkan dalam bentuk sistem koloid. Hal ini karena…. A. koloid tidak membutuhkan pengawet
B. koloid memiliki sifat adsorpsi sehingga bisa menyerap air
C. koloid menunjukkan efek Tyndall sehingga tidak rusak oleh cahaya
D. koloid dapat menekan biaya produksi karena larutan membutuhkan pelarut dengan biaya tinggi E. koloid pada tingkat makroskopis bersifat homogen dan stabil
26. Mengapa gas dalam gas bukan merupakan sistem koloid?
27. Jelaskan perbedaan antara larutan, sistem koloid, dan suspensi (tiga perbedaan) 28. Jelaskan efek ukuran partikel dan suhu terhadap gerak Brown.
29. Tentukan jenis koloid, medium pendispresi, dan fase terdispersi dari: a. styrofoam