INTISARI
Obat yang beredar di masyarakat dapat dibagi menjadi obat generik dan obat dagang. Perbandingan kedua produk obat tersebut dapat ditinjau dari penelitian farmakokinetika. Penelitian ini dimaksudkan untuk membandingkan bioavailabilitas obat dagang terhadap obat generik pada kelinci putih jantan.
Penelitian ini merupakan penelitian eksperimental murni dengan rancangan eksperimental silang. Konsentrasi parasetamol dalam plasma kelinci ditentukan dengan metode kolorimetri berdasarkan metode Chafetz et al. (1971) yang telah dimodifikasi. Data kemudian diubah menjadi parameter-parameter bioavailabilitas dan dianalisis dengan ANOVA mengggunakan taraf kepercayaan 90%.
Hasil penelitian yaitu tmaks (menit) untuk tablet parasetamol generik = 24,233
± 1,193; tablet Biogesic® = 28,000 ± 4,371; tablet Pamol® = 58,467 ± 1,976. Cmaks ( g
/ml) untuk tablet parasetamol generik = 193,927 ± 38,345; tablet Biogesic® = 162,870 ± 34,831; tablet Pamol® = 156,647 ± 42,072. AUC(0-∞) ( g.menit/ml) untuk tablet
parasetamol generik = 22896,410 ± 3731,193; tablet Biogesic® = 22198,470 ± 698,045; tablet Pamol® = 25525,490 ± 7181,70. Hasil ini menunjukkan ada perbedaan tidak bermakna nilai AUC(0-∞) dan nilai Cmaks antara tablet Biogesic® dan tablet
Pamol® dengan tablet parasetamol generik. Namun, terdapat perbedaan bermakna nilai tmaks tablet Pamol® terhadap tablet parasetamol generik. Jadi, dapat disimpulkan
tablet Biogesic® bioekivalen dengan tablet generik, sedangkan tablet Pamol® bioinekivalen dengan tablet generik.
Kata kunci utama : obat generik, obat dagang, parasetamol, bioavailabilitas, bioekivalen.
ABSTRACT
Drugs can be divided into two groups, are generic drugs and brand-name drugs. The comparison of them could be found out by pharmacokinetic research. This research was aimed to compare the bioavailability of brand-name drugs to generic drugs on male white rabbits.
The research was pure cross experimental research. Paracetamol concentrations in rabbits’ plasma were determined by a colorimetric method based on modified-Chafetz et al. method (1971). The data were presented as bioavailability parameters, and were analyzed using ANOVA with 90% confidence interval.
The results showed that tmax (min) for generic paracetamol tablets = 24,233 ±
1,193; Biogesic® tablets = 28,000 ± 4,371; Pamol® tablets = 58,467 ± 1,976. Cmax ( g
/ml) for generic paracetamol tablets = 193,927 ± 38,345; Biogesic® tablets = 162,870 ± 34,831; Pamol® tablets = 156,647 ± 42,072. AUC(0-∞) ( g.min/ml) for generic
paracetamol tablets = 22896,410 ± 3731,193; Biogesic® tablets = 22198,470 ± 698,045; Pamol® tablets = 25525,490 ± 7181,70. There were insignificant differences of AUC(0-∞) and Cmaks between Biogesic® and generic tablets, and between Pamol®
and generic tablets. However, significant difference of tmaks was found out between
Pamol® and generic tablets. Therefore, we conclude that Biogesic® and generic tablets were bioequivalent, but Pamol® and generic tablets were bioinequivalent.
Keywords : generic drugs, brand-name drugs, paracetamol, bioavailability, bioequivalent.
PERBANDINGAN BIOAVAILABILITAS ANTARA TABLET BIOGESIC® DAN TABLET PAMOL® DENGAN TABLET PARASETAMOL GENERIK
PADA KELINCI PUTIH JANTAN
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh: Vincilia Indriyani NIM : 038114008
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
PERBANDINGAN BIOAVAILABILITAS ANTARA TABLET BIOGESIC® DAN TABLET PAMOL® DENGAN TABLET PARASETAMOL GENERIK
PADA KELINCI PUTIH JANTAN
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh: Vincilia Indriyani NIM : 038114008
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2007
HALAMAN PERSEMBAHAN
PRAKATA
Puji syukur kepada Tuhan Yang Maha Besar atas kasih, kuasa, mujizat, dan penyertaan-Nya yang sempurna sehingga penulis dapat menyelesaikan skripsi yang berjudul “Perbandingan Bioavailabilitas antara Tablet Biogesic® dan Tablet Pamol® dengan Tablet Parasetamol Generik pada Kelinci Putih Jantan”. Skripsi ini ditulis untuk memenuhi salah satu syarat memperoleh gelar Sarjana Farmasi (S.Farm.) pada Program Studi Farmasi di Universitas Sanata Dharma.
Penulisan skripsi ini tidak mungkin terwujud tanpa bimbingan, bantuan, dukungan, dan doa dari berbagai pihak, maka pada kesempatan ini penulis hendak mengucapkan terima kasih kepada:
1. Orang tua tercinta dan adikku, Willy, atas doa, pengertiannya, dan dukungan semangatnya yang tak pernah berhenti hingga hari ini.
2. Rita Suhadi, M. Si., Apt. selaku dekan Fakultas Farmasi Universitas Sanata Dharma dan terima kasih atas pinjaman bukunya yang sangat membantu penyelesaian skripsi ini.
3. Drs. Mulyono, Apt. selaku dosen pembimbing yang telah meluangkan waktu dan tenaga, juga atas masukan, saran, pengajaran, dukungan, dan semangat yang selalu menginspirasi dalam penyusunan skripsi ini.
4. Christine Patramurti, M. Si., Apt. selaku dosen penguji yang telah berkenan menguji dan memberikan masukan serta saran atas penulisan skripsi ini.
5. C. M Ratna Rini Nastiti, S. Si., Apt. selaku dosen penguji yang telah berkenan menguji, memberikan bimbingan, masukan dan saran yang sangat berarti dalam penyusunan skripsi ini.
6. Yosef Wijoyo, M. Si., Apt. selaku dosen yang telah berkenan memberikan masukan, dukungan dan dorongan semangat dalam pengerjaan skripsi ini.
7. Clara ”Jephi”ana Sri Widyarini, sahabat, teman praktikum, dan rekan kerja, atas persahabatan yang indah, kerja sama yang luar biasa, canda tawa, pemikiran, pengetahuan, semangat, motivasi, dan doa hingga kita bisa menyelesaikan kuliah kita, PKM dan skripsi kita bersama.
8. Mas Heru, Mas Parjiman, Mas Kayat, Mas Yuwono, Pak Mus, Pak Mukmin, Mas Wagiran, dan segenap karyawan yang telah membantu dan menyemangati.
9. Teman-teman seperjuangan di laboratorium : Fany, Essy, Surya, Galih, dan Angga atas dukungan semangat dan canda tawanya selama ini.
10.Kesukaan Bapa’s crew yaitu Ci Anita, Ci V’ri, Ci Esme, Ci Vina, Astri, Juwi, Ine, Indri, Dian, dan Christina, serta anak sel-ku Agnes, Heni, dan Jenny, atas doa, perhatian, dan kebersamaan persekutuan kita yang indah.
11.Ko Andrey, Koko Can, dan Fang-fang, sahabat-sahabat terbaik, yang selalu ada menemani hari-hariku, yang selalu mempercayaiku, mendukung dan mendoakanku.
12.Bu Ina dan Ko Dian, teman sekaligus guru musikku yang selalu memberikan semangat dan memaklumi kesibukanku dalam pengerjaan skripsi ini.
13.Adhy, Tirza, Eta, Arnie, dan teman-teman kuliah khususnya angkatan 2003 kelompok praktikum A, terima kasih atas semangat dan segala kebersamaan kita selama ini.
14.Semua pihak yang telah banyak membantu.
Atas segala bantuan yang telah diberikan selama ini, penulis mengucapkan banyak terima kasih. Penulis menyadari sepenuhnya penulisan skripsi ini tidak terlepas dari keterbatasan dan kekurangan penulis. Oleh karena itu, diharapkan kritik dan saran yang membangun demi penyempurnaan skripsi ini. Besar harapan penulis bahwa skripsi ini dapat bermanfaat bagi perbendaharaan dan perkembangan ilmu pengetahuan.
Penulis
INTISARI
Obat yang beredar di masyarakat dapat dibagi menjadi obat generik dan obat dagang. Perbandingan kedua produk obat tersebut dapat ditinjau dari penelitian farmakokinetika. Penelitian ini dimaksudkan untuk membandingkan bioavailabilitas obat dagang terhadap obat generik pada kelinci putih jantan.
Penelitian ini merupakan penelitian eksperimental murni dengan rancangan eksperimental silang. Konsentrasi parasetamol dalam plasma kelinci ditentukan dengan metode kolorimetri berdasarkan metode Chafetz et al. (1971) yang telah dimodifikasi. Data kemudian diubah menjadi parameter-parameter bioavailabilitas dan dianalisis dengan ANOVA mengggunakan taraf kepercayaan 90%.
Hasil penelitian yaitu tmaks (menit) untuk tablet parasetamol generik = 24,233
± 1,193; tablet Biogesic® = 28,000 ± 4,371; tablet Pamol® = 58,467 ± 1,976. Cmaks (μg
/ml) untuk tablet parasetamol generik = 193,927 ± 38,345; tablet Biogesic® = 162,870 ± 34,831; tablet Pamol® = 156,647 ± 42,072. AUC(0-∞) (μg.menit/ml) untuk tablet
parasetamol generik = 22896,410 ± 3731,193; tablet Biogesic® = 22198,470 ± 698,045; tablet Pamol® = 25525,490 ± 7181,70. Hasil ini menunjukkan ada perbedaan tidak bermakna nilai AUC(0-∞) dan nilai Cmaks antara tablet Biogesic® dan tablet
Pamol® dengan tablet parasetamol generik. Namun, terdapat perbedaan bermakna nilai tmaks tablet Pamol® terhadap tablet parasetamol generik. Jadi, dapat disimpulkan
tablet Biogesic® bioekivalen dengan tablet generik, sedangkan tablet Pamol® bioinekivalen dengan tablet generik.
Kata kunci utama : obat generik, obat dagang, parasetamol, bioavailabilitas, bioekivalen.
ABSTRACT
Drugs can be divided into two groups, are generic drugs and brand-name drugs. The comparison of them could be found out by pharmacokinetic research. This research was aimed to compare the bioavailability of brand-name drugs to generic drugs on male white rabbits.
The research was pure cross experimental research. Paracetamol concentrations in rabbits’ plasma were determined by a colorimetric method based on modified-Chafetz et al. method (1971). The data were presented as bioavailability parameters, and were analyzed using ANOVA with 90% confidence interval.
The results showed that tmax (min) for generic paracetamol tablets = 24,233 ±
1,193; Biogesic® tablets = 28,000 ± 4,371; Pamol® tablets = 58,467 ± 1,976. Cmax (μg
/ml) for generic paracetamol tablets = 193,927 ± 38,345; Biogesic® tablets = 162,870 ± 34,831; Pamol® tablets = 156,647 ± 42,072. AUC(0-∞) (μg.min/ml) for generic
paracetamol tablets = 22896,410 ± 3731,193; Biogesic® tablets = 22198,470 ± 698,045; Pamol® tablets = 25525,490 ± 7181,70. There were insignificant differences of AUC(0-∞) and Cmaks between Biogesic® and generic tablets, and between Pamol®
and generic tablets. However, significant difference of tmaks was found out between
Pamol® and generic tablets. Therefore, we conclude that Biogesic® and generic tablets were bioequivalent, but Pamol® and generic tablets were bioinequivalent.
Keywords : generic drugs, brand-name drugs, paracetamol, bioavailability, bioequivalent.
DAFTAR ISI
HALAMAN JUDUL ... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN ... iv
HALAMAN PERSEMBAHAN ... v
PRAKATA ... vi
PERNYATAAN KEASLIAN KARYA ... ix
INTISARI ... x
ABSTRACT ... xi
DAFTAR ISI ... xii
DAFTAR TABEL ... xvi
DARTAR GAMBAR ... xviii
DAFTAR LAMPIRAN ... xx
BAB I PENGANTAR ... 1
A. Latar Belakang ... 1
1. Perumusan masalah ... 2
2. Keaslian Penelitian... 2
3. Manfaat ... 2
B. Tujuan ... 3
1. Tujuan Umum ... 3
2. Tujuan Khusus ... 3
BAB II PENELAAHAN PUSTAKA ... 4
A. Nasib Obat di Dalam Tubuh ... 4
B. Fase Farmakokinetika ... 5
1. Absorpsi dan Bioavailabilitas ... 6
2. Distribusi ... 23
3. Biotransformasi atau metabolisme ... 23
4. Ekskresi ... 24
C. Bioekivalensi ... 25
1. Definisi ... 25
2. Studi Bioavailabilitas dan Bioekivalensi ... 26
3. Korelasi in vitro dan in vivo ... 27
D. Dasar-Dasar Farmakokinetika ... 28
1. Definisi ... 28
2. Model Farmakokinetika ... 28
3. Parameter Farmakokinetika ... 29
4. Strategi Penelitian Farmakokinetika ... 35
E. Desain Cross Over ... 37
F. Parasetamol ... 37
G. Darah ... 41
H. Kolorimetri ... 43
1. Definisi ... 43
2. Kriteria Analisis Kolorimetri ... 43
3. Metode Kolorimetri untuk Parasetamol ... 44
I. Keterangan Empiris ... 47
BAB III METODOLOGI PENELITIAN ... 48
A. Jenis dan Rancangan Penelitian ... 48
B. Variabel dan Definisi Operasional ... 48
1. Variabel Penelitian ... 48
2. Definisi Operasional ... 50
C. Bahan Penelitian ... 51
D. Alat Penelitian ... 51
E. Tata Cara Penelitian ... 51
1. Uji Pendahuluan Tablet Parasetamol ... 51
2. Pembuatan Larutan ... 53
3. Pengambilan Plasma Darah ... 55
4. Validasi Metode Analisis ... 55
5. Orientasi Dosis ... 58
6. Metode Bioanalitik Parasetamol dalam Plasma Darah ... 59
F. Analisis Hasil ... 61
1. Nilai Perolehan Kembali (Recovery), Kesalahan Sistematik, dan Kesalahan Acak ... 61
2. Pengolahan Data dengan program STRIPE ... 62
3. Analisis Data secara statistik ... 62
BAB IV HASIL DAN PEMBAHASAN ... 64
A. Uji Sifat Fisik Tablet Parasetamol ... 64
1. Uji Keseragaman Bobot ... 64
2. Uji Kekerasan ... 66
3. Uji Kerapuhan ... 66
4. Uji Waktu Hancur ... 67
5. Uji Disolusi ... 68
B. Pengambilan Plasma Darah Kelinci ... 72
C. Validasi Metode Analisis ... 73
1. Penentuan Operating Time (OT) ... 78
2. Penentuan Panjang Gelombang Maksimum Parasetamol ... 80
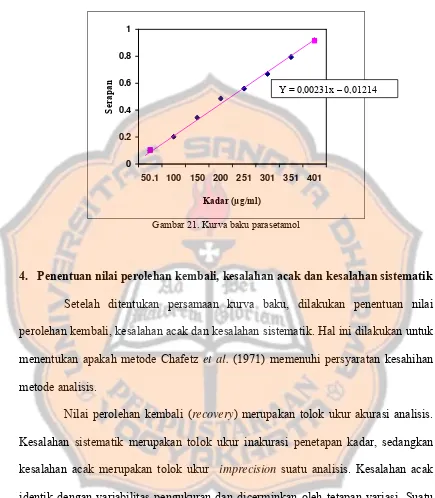
3. Pembuatan Kurva Baku ... 81
4. Penentuan Nilai Perolehan kembali, Kesalahan Sistematik, dan Kesalahan Acak ... 83
D. Orientasi Dosis dan Orientasi Waktu Pengambilan Cuplikan ... 85
E. Perbandingan Bioavailabilitas ... 87
1. Nilai tmaks ... 89
2. Cmaks ... 90
3. AUC(0-∞) ... 91
BAB V KESIMPULAN DAN SARAN ... 101
A. Kesimpulan ... 101
B. Saran ... 102
DAFTAR PUSTAKA ... 103
LAMPIRAN ... 108
BIOGRAFI PENULIS ... 142
DAFTAR TABEL
Tabel I Desain Operasional Penelitian ... 59
Tabel II Parameter-parameter Farmakokinetika beserta satuannya ... 62
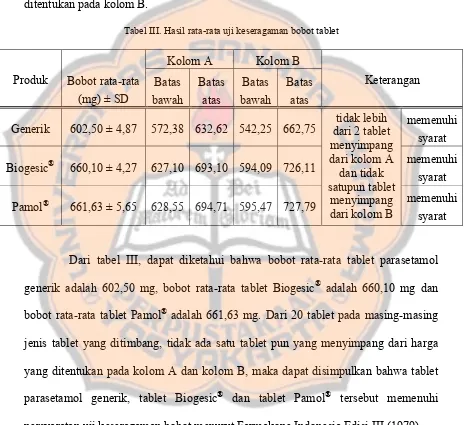
Tabel III Hasil Rata-rata Uji Keseragaman Bobot Tablet ... 65
Tabel IV Hasil Rata-rata Uji Kekerasan Tablet ... 66
Tabel V Hasil Uji Kerapuhan Tablet ... 67
Tabel VI Hasil Uji Waktu Hancur Tablet ... 68
Tabel VII Data Persamaan Kurva Baku Disolusi ... 69
Tabel VIII Hasil Uji Disolusi ... 70
Tabel IX Nilai Faktor Kemiripan (f2) ... 72
Tabel X Data Persamaan Kurva Baku ... 82
Tabel XI Nilai Perolehan Kembali, Kesalahan Sistematik, dan Kesalahan4 Acak Parasetamol di Dalam Plasma Kadar 100 µg/ml ... 84
Tabel XII Nilai Perolehan Kembali, Kesalahan Sistematik, dan Kesalahan Acak Parasetamol di Dalam Plasma Kadar 400 µg/ml ... 84
Tabel XIII Nilai Rata-Rata Parameter-Parameter Bioavailabilitas ... 87
Tabel XIV Hasil Analisis Statistik untuk tmaks ... 89
Tabel XV Hasil Analisis Statistik untuk ln Cmaks ... 90
Tabel XVI Hasil Analisis Statistik untuk AUC(0-∞) ... 92
Tabel XVII Nilai Rata-rata Geometrik Parameter-parameter Bioavailabilitas 98 Tabel XVIII Hasil Uji Keseragaman Bobot ... 108
Tabel XIX Hasil Uji Kekerasan ... 109
Tabel XX Hasil Uji Disolusi Tablet Parasetamol Generik ... 112
Tabel XXI Hasil Uji Disolusi Tablet Biogesic® ... 113
Tabel XXII Hasil Uji Disolusi Tablet Pamol® ... 114
Tabel XXIIII Perhitungan Faktor Kemiripan ... 115
Tabel XXIV Konversi Perhitungan Dosis Antar Jenis Hewan ... 118
Tabel XXV Data Tablet Parasetamol Generik 1 ... 124
Tabel XXVI Data Tablet Parasetamol Generik 2 ... 125
Tabel XXVII Data Tablet Parasetamol Generik 3 ... 126
Tabel XXVIII Data Tablet Biogesic® 1 ... 127
Tabel XXIX Data Tablet Biogesic® 2 ... 128
Tabel XXX Data Tablet Biogesic® 3 ... 129
Tabel XXXI Data Tablet Pamol®1 ... 130
Tabel XXXII Data Tablet Pamol® 2 ... 131
Tabel XXXIII Data Tablet Pamol® 3 ... 132
Tabel XXXIV Nilai Rata-rata Aritmatika Parameter-parameter Farmakokinetika ... 133
DAFTAR GAMBAR
Gambar 1 Proses Obat dalam Tubuh hingga Menimbulkan Efek ... 5
Gambar 2. Proses Farmakokinetika Obat di dalam Tubuh ... 6
Gambar 3 Proses Perjalanan Absorpsi Obat ... 7
Gambar 4 Struktur Parasetamol ... 38
Gambar 5 Metabolisme Parasetamol ... 41
Gambar 6 Reaksi Parasetamol dengan Asam Nitrat ... 45
Gambar 7 Reaksi Hidrolisis Parasetamol menjadi p-aminofenol ... 45
Gambar 8 Reaksi Pembentukan Warna ... 46
Gambar 9 Kurva Baku Disolusi ... 69
Gambar 10 Kurva Nilai Rata-rata Kumulatif Uji Disolusi ± SD ... 71
Gambar 11 Reaksi antara Asam Klorida dengan Natrium Nitrit Sehingga Membentuk ion Nitrosonium ... 74
Gambar 12 Reaksi antara Parasetamol dengan Ion Nitrosonium Membentuk 2-nitro-4-asetamidofenol ... 75
Gambar 13 Reaksi antara Asam Nitrit dengan Asam Sulfamat ... 76
Gambar 14 Reaksi antara 2-nitro-4 asetamidofenol dalam Suasana Basa Menghasilkan ion 2-nitro-4 asetamidofenolat ... 76
Gambar 15 Reaksi Menstabilkan Diri Ion 2-nitro-4 asetamidofenolat ... 77
Gambar 16 Mekanisme Reaksi Parasetamol dalam Metode Chafetz et al. ... 78
Gambar 17 Pengukuran Operating Time (OT) Larutan Parasetamol dalam Plasma Kadar 100 μg/ml ... 79
Gambar 18 Pengukuran Operating Time (OT) Larutan Parasetamol dalam Plasma Kadar 400 μg/ml ... 79
Gambar 19 Pengukuran Panjang Gelombang Maksimum Larutan Parasetamol 100 μg/ml ... 80
Gambar 20 Pengukuran Panjang Gelombang Maksimum Larutan Parasetamol 400 μg/ml ... 81
Gambar 21 Kurva Baku Parasetamol ... 83
Gambar 22 Kurva Rata-rata Kadar Parasetamol dalam Plasma versus Waktu 93
Gambar 23 Kurva Rata-rata ln Kadar Parasetamol dalam Plasma versus Waktu 93 Gambar 24 Kurva Hasil Uji Disolusi Tablet Parasetamol Generik ... 112
Gambar 25 Kurva Hasil Uji Disolusi Tablet Biogesic® ... 113
Gambar 26 Kurva Hasil Uji Disolusi Tablet Pamol® ... 114
Gambar 27 OT Larutan Parasetamol Kadar 100µg/ml ... 120
Gambar 28 OT Larutan Parasetamol Kadar 400µg/ml ... 120
Gambar 29 λmaks Larutan Parasetamol Kadar 100µg/ml ... 121
Gambar 30 λmaks Larutan Parasetamol Kadar 400µg/ml ... 121
Gambar 31 Kurva Baku Parasetamol ... 122
Gambar 32 Sertifikat Analisis Parasetamol ... 123
Gambar 33 Kurva Hubungan Kadar Tablet Parasetamol Generik vs Waktu .. 134
Gambar 34 Kurva Hubungan Kadar Tablet Biogesic®vs Waktu ... 134
Gambar 35 Kurva Hubungan Kadar Tablet Pamol®vs Waktu ... 134
Gambar 36 Kurva Hubungan ln Kadar Tablet Parasetamol Generik vs Waktu 135
Gambar 37 Kurva Hubungan ln Kadar Tablet Biogesic® vs Waktu ... 135
Gambar 38 Kurva Hubungan ln Kadar Tablet Pamol® vs Waktu ... 135
DAFTAR LAMPIRAN
Lampiran 1 Hasil Uji Keseragaman Bobot ... 108 Lampiran 2 Hasil Uji Kekerasan ... 109 Lampiran 3 Contoh Cara Perhitungan Data Disolusi ... 110 Lampiran 4 Hasil Uji Disolusi ... 112 Lampiran 5 Perhitungan Pembuatan Larutan Parasetamol untuk Kurva Baku 116 Lampiran 6 Contoh Perhitungan Pembuatan Larutan Obat ... 117 Lampiran 7 Tabel Konversi Perhitungan Dosis Antar Jenis Hewan
dan Perhitungan Orientasi Dosis ... 118 Lampiran 8 Contoh Perhitungan Volume Pemberian Larutan Parasetamol
Pada Hewan Uji ... 119 Lampiran 9 Hasil Scanning Penentuan Operating time dan Panjang
Gelombang Maksimum Parasetamol ... 120 Lampiran 10 Hasil Scanning Kurva Baku ... 122 Lampiran 11 Sertifikat Analisis Parasetamol ... 123 Lampiran 12 Hasil Pengolahan Data Dengan Program STRIPE
Untuk Tablet Parasetamol Generik ... 125 Lampiran 13 Hasil Pengolahan Data Dengan Program STRIPE
Untuk Tablet Biogesic® ... 127 Lampiran 14 Hasil Pengolahan Data Dengan Program STRIPE
Untuk Tablet Pamol® ... 130 Lampiran 15 Nilai Rata-rata Parameter-parameter Farmakokinetika ... 133 Lampiran 16 Contoh Perhitungan Nilai Rata-rata Geometrik Parameter
Bioavailabilitas ... 133 Lampiran 17 Kurva Kadar Parasetamol Dalam Plasma (Cp vs t) ... 134 Lampiran 18 Kurva ln Kadar Parasetamol Dalam Plasma (ln Cp vs t) ... 135 Lampiran 19 Hasil Pengolahan Data Secara Statistik Dengan Program SPSS 136
BAB I PENGANTAR
A. Latar Belakang
Obat tidak pernah lepas dari kehidupan masyarakat. Dewasa ini, semakin
tinggi permintaan masyarakat akan obat. Obat telah menjadi kebutuhan dalam
masyarakat. Hal tersebut memicu berkembangnya industri-industri obat sehingga obat
yang beredar di masyarakat menjadi sangat beragam. Obat dalam masyarakat dapat
dibedakan menjadi dua, yaitu obat generik dan obat bermerek dagang (trade mark).
Dalam kehidupan sehari-hari, masyarakat menggunakan kedua jenis obat tersebut.
Oleh sebab itu, obat yang beredar di dalam masyarakat harus terjamin mutu, khasiat,
dan keamanannya.
Obat generik merupakan obat jadi yang menggunakan nama zat aktif yang
terkandung di dalamnya sesuai dengan yang ditetapkan dalam Farmakope Indonesia
atau buku resmi lainnya. Obat bermerek dagang merupakan obat jadi dengan nama
dagang yang dilindungi hukum yaitu merek terdaftar. Banyaknya obat jadi dengan zat
aktif yang sama yang beredar di masyarakat baik obat generik maupun obat bermerek
dagang, menimbulkan pertanyaan apakah obat-obat tersebut adalah sama.
Perbandingan kedua jenis obat tersebut dapat ditinjau dari segi farmakokinetika.
Dalam penelitian ini, dilakukan analisis farmakokinetika yaitu dengan
melakukan studi bioavailabilitas dan bioekivalensi dengan cara membandingkan
kecepatan dan jumlah obat yang diabsorpsi dalam tubuh. Penelitian ini menggunakan
tablet Biogesic® dan tablet Pamol® selaku obat bermerek dagang yang mengandung
senyawa aktif tunggal parasetamol dengan tablet parasetamol generik sebagai
pembandingnya. Penelitian ini dilakukan pada hewan uji yaitu kelinci putih jantan.
Parasetamol dipilih sebagai obat yang akan diteliti dikarenakan parasetamol sangat
lazim digunakan dalam masyarakat baik sebagai obat flu, demam, sakit kepala, nyeri
haid, dan sebagainya.
1. Perumusan masalah
Berdasarkan latar belakang yang dipaparkan maka dapat dirumuskan
permasalahan yaitu apakah tablet Biogesic® dan tablet Pamol® memiliki
bioavailabilitas yang sama dengan tablet parasetamol generik?
2. Keaslian penelitian
Sejauh yang diketahui penulis, belum pernah dilakukan penelitian mengenai
perbandingan bioavailabilitas antara tablet Biogesic® dan tablet Pamol® dengan tablet
parasetamol generik pada kelinci putih jantan di lingkungan penelitian Universitas
Sanata Dharma dan Universitas Gadjah Mada Yogyakarta.
3. Manfaat penelitian
Penelitian mengenai perbandingan bioavailabilitas tablet parasetamol ini
memberikan informasi akan perbandingan bioavailabilitas tablet obat bermerek
dagang dan tablet obat generik yang mengandung parasetamol pada hewan uji.
B. Tujuan
Tujuan dari penelitian ini yaitu:
1. Tujuan umum :
Untuk mengetahui bioavailabilitas tablet parasetamol generik, tablet
Biogesic®, dan tablet Pamol®.
2. Tujuan khusus:
Untuk mengetahui ada tidaknya perbedaan bioavailabilitas yang bermakna
antara tablet Biogesic® dan tablet Pamol® terhadap tablet parasetamol generik, pada
BAB II
PENELAAHAN PUSTAKA
Berkaitan dengan penelitian yang berjudul “Perbandingan Bioavailabilitas Antara Tablet Biogesic® dan Tablet Pamol dengan Tablet Parasetamol Generik pada ® Kelinci Putih Jantan”, maka dilakukan studi pustaka yang akan mendukung analisis profil bioavailabilitas yang dihasilkan dari penelitian ini. Studi pustaka yang dilakukan meliputi penjelasan mengenai nasib obat di dalam tubuh, fase farmakokinetika, bioekivalensi, dasar-dasar farmakokinetika, desain cross over, parasetamol, darah, dan kolorimetri.
A. Nasib Obat di Dalam Tubuh
Disintegrasi dari bentuk sediaan
Disolusi Obat
EFEK
pemberian
Fase farmasetik
Obat tersedia untuk diabsorpsi (availabilitas farmasetik)
Obat tersedia untuk aksi (availabilitas farmakologis)
Fase farmakokinetika
Fase farmakodinamika
Dosis formulasi obat
Absorpsi, distribusi, metabolisme,
ekskresi
Interaksi obat-reseptor
Gambar 1. Proses obat dalam tubuh hingga menimbulkan efek (Bowman and Rand, 1990)
B. Fase Farmakokinetika
Tempat Aksi “Reseptor” terikat bebas
Jaringan
terikat bebas
Absorpsi Ekskresi
Sirkulasi sistemik
obat bebas
obat terikat metabolit
Biotransformasi
Distribusi
Gambar 2. Proses farmakokinetika obat di dalam tubuh (Wilkinson, 2001)
1. Absorpsi dan Bioavailabilitas
a. Definisi absorpsi dan bioavailabilitas
disintegrasi
Tablet Granul atau deagregasi agregat
Suspensi partikel halus di cairan gastrointestinal
Larutan obat dalam cairan gastrointestinal
disolusi disolusi disolusi
absorpsi
Obat dalam darah, cairan tubuh, dan jaringan
Gambar 3. Proses perjalanan absorpsi tablet (Proudfoot, 1990)
Produk obat umumnya mengalami absorpsi sistemik melalui suatu rangkaian proses, yang meliputi disintegrasi produk obat yang diikuti pelepasan obat, pelarutan obat dalam media aqueous, dan absorpsi melewati membran sel menuju sirkulasi sistemik. Di dalam proses disintegrasi obat, pelarutan, dan absorpsi, kecepatan obat mencapai sistem sirkulasi ditentukan oleh tahap yang paling lambat (rate limiting step) (Shargel, Wu-Pong and Yu, 2005).
b. Mekanisme transpor obat
membran biologis. Kebanyakan dari obat menembus membran dengan mekanisme yang disebut difusi pasif (Proudfoot, 1990). Difusi pasif menunjukkan perpindahan komponen dari fase aqueous melewati suatu membran dimana membran tersebut bersifat pasif, tenaga penggerak perpindahan tersebut hanya merupakan gradien konsentrasi komponen (Mayersohn, 2002).
Mekanisme difusi pasif dapat ditunjukkan secara matematis dengan hukum Fick :
(1)
( )
dt=
D
Δ
⎟
⎟
⎠
⎞
⎜⎜
⎝
⎛
−
→ m b g m/aq m m b g dQX
C
C
R
A
b( )
dQdtb g b→ = kecepatan obat berada di darah (b) setelah berdifusi dari cairan saluran cerna (g)
Dm = koefisien difusi obat melewati membran
Am = luas permukaan membran yang tersedia untuk proses difusi obat = koefisien partisi obat antara membran dan cairan aqueous pada saluran cerna
Rm/aq
-C = gradien konsentrasi antara konsentrasi obat di cairan saluran cerna (C
Cg b
g) dengan konsentrasi obat di dalam darah pada tempat absorpsi
(C ) b
ΔXm = ketebalan dari membran
Pada kondisi dan obat tertentu maka nilai Dm, Am, Rm/aq, dan ΔXm adalah konstan
maka dapat digantikan sebagai koefisien permeabilitas (P). (2)
( )
=P(
g −Cb)
Volume dimana obat terdistribusi dalam darah jauh lebih besar dibandingkan volume cairan saluran cerna dan karena sirkulasi darah melewati saluran gastrointestinal cepat dan terus menerus membawa obat yang terabsorpsi, maka nilai C >> Cg b. Kondisi ini yang disebut kondisi sink (Mayersohn, 2002).
(3)
( )
dt g b gdQ
C . b
→ ≅P
c. Faktor-faktor yang Mempengaruhi Absorpsi dan Bioavailabilitas Obat
Faktor-faktor yang dapat mempengaruhi bioavailabilitas suatu obat seperti tercantum di bawah ini.
1). Faktor mekanis
Faktor-faktor yang termasuk di dalamnya yaitu : a). Rute dan metode pemberian
Dosis dan aturan dosis b).
Dosis dan aturan dosis berkaitan dengan konsentrasi terapeutik yang dapat dicapai suatu obat di dalam plasma, yang berarti berhubungan dengan Cmaks dan AUC yang dihasilkan (mempengaruhi bioavailabilitas obat)
(Shargel et al., 2005).
c). Efek dari bentuk sediaan.
Faktor dari bentuk sediaan yang dapat mempengaruhi bioavailabilitas yaitu:
(1). Faktor fisikakimia bahan dalam obat meliputi sebagai berikut. Faktor yang mempengaruhi kelarutan
Absorpsi obat tergantung seberapa cepat obat larut dalam cairan gastrointestinal, sehingga faktor yang mempengaruhi kecepatan disolusi obat akan mempengaruhi bioavailabilitas obat. Kecepatan disolusi obat ditentukan dari persamaan Noyes dan Whitney (Proudfoot, 1990) :
(4)
)
C
(
D
dm
=
C
−
s h
A dt
dm/dt = kecepatan disolusi partikel obat
D = koefisien difusi larutan obat di cairan gastrointestinal A = luas permukaan efektif dari partikel obat
h = ketebalan lapisan difusi sekitar partikel obat Cs = kelarutan jenuh obat di lapisan difusi
Faktor-faktor yang mempengaruhi kelarutan obat antara lain : (a). Bentuk kristal
Polymorphism. Banyak obat dapat berada dalam lebih dari satu
bentuk kristal. Polimorfi bentuk metastable memiliki kelarutan dalam aqueous dan kecepatan disolusi yang lebih besar dibandingkan polimorfi bentuk stable.
Amorphous state. Obat dalam bentuk amorf biasanya lebih mudah larut dan lebih cepat terdisolusi daripada obat dalam bentuk kristal sehingga akan mempengaruhi bioavailabilitas.
Solvates. Obat bergabung dengan molekul dari pelarut dan membentuk bentuk kristal yang disebut solvates. Secara umum, semakin banyak solvasi maka semakin rendah kelarutan dan kecepatan disolusi obat sehingga dapat mempengaruhi bioavailabilitas obat (Proudfoot, 1990; Wagner, 1975).
(b). Asam bebas, basa bebas, bentuk garam, nilai pKa
[ ]
[ ]
pH-pKa HAA log
-=
untuk obat asam lemah (5)
[ ]
[ ]
pKa-pH BBH
log =
+
untuk obat basa lemah (6)
pH = keasaman media pKa = keasaman senyawa
-] = fraksi terion dari senyawa yang bersifat asam lemah [A
[HA] = fraksi tak terion (molekul) dari senyawa yang bersifat asam lemah
+
[BH ] = fraksi terion dari senyawa yang bersifat basa lemah
[B] = fraksi tak terion (molekul) dari senyawa yang bersifat basa lemah
(c). Kompleksasi, larutan solid, dan eutetics
(d). Surfaktan
Surfaktan dapat menghasilkan efek bervariasi pada proses disolusi dan absorpsi. Surfaktan dapat menurunkan tegangan permukaan sehingga meningkatkan kecepatan disolusi (Wagner, 1975).
Faktor yang mempengaruhi transpor obat
Faktor utama yang mempengaruhi obat dalam proses absorpsi obat menembus membran adalah koefisien partisi, banyaknya ionisasi dalam cairan biologis yang ditentukan dari nilai pKa, pH cairan medium obat terlarut, dan berat molekul atau volume (Mayersohn, 2002).
(a). Koefisien partisi
Membran biologis merupakan lapisan lipid sehingga obat yang larut dalam lemak (lipofil) lebih dapat menembus membran. Ko/w adalah
rasio kelarutan obat di dalam minyak (oil) dengan kelarutan obat di dalam air (water). Hal ini berarti obat-obat yang memiliki nilai Ko/w
lebih besar akan lebih banyak yang dapat menembus membran biologis dan dapat diabsorpsi. Peningkatan nilai Ko/w akan
meningkatkan kecepatan absorpsi (Mayersohn, 2002)
(b). Nilai pKa, pH, keberadaan muatan
akan terionisasi pada cairan biologis. Arti pentingnya ionisasi dalam proses absorpsi obat didasarkan pada observasi dimana obat dalam bentuk non ion memiliki nilai Ko/w lebih besar dibandingkan obat
dalam bentuk ion. Hal ini berarti membran bersifat permeabel terhadap bentuk non ion dari obat asam lemah dan basa lemah (Mayersohn, 2002; Proudfoot, 1990).
(c). Molal volume, difusivitas
Difusivitas berkaitan dengan berat molekular. Bentuk misel akan berdifusi lebih lambat dari fase aqueous bulk menuju ke lapisan difusi dan berdifusi lebih lambat dalam melewati lapisan difusi dibandingkan molekul obat monomerik (Wagner, 1975).
(d). Stagnant water layers / aqueous diffusion layer
(2). Faktor farmasetik dan pembuatan obat
Faktor-faktor yang termasuk di dalamnya yang mungkin menyebabkan adanya perbedaan pada parameter-parameter bioavailabilitas adalah sebagai berikut.
(a). Ukuran partikel dan luas permukaan area
Peningkatan luas permukaan area obat untuk kontak dengan cairan gastrointestinal akan meningkatkan kecepatan disolusi. Secara umum, semakin kecil ukuran partikel obat, semakin besar luas permukaan area dan semakin besar kecepatan disolusi, yang akan meningkatkan bioavailabilitas (Proudfoot, 1990; Wagner, 1975).
(b). Static electrification dari obat padat
Banyak proses farmasetik seperti blending, pencampuran, coating, dan sebagainya dapat menghasilkan static electrification dari bahan padat. Hal ini dapat menyebabkan terjadinya agregasi dan obat tidak bercampur. Agregasi dapat menurunkan luas permukaan efektif sehingga dapat menurunkan kecepatan disolusi (Wagner, 1975).
(c). Jenis bentuk sediaan
bentuk larutan di cairan gastrointestinal, maka makin banyak penghalang absorpsi obat dan akan mempengaruhi bioavailabilitas obat. Bioavailabilitas obat larutan aqueous > suspensi aqueous > kapsul > tablet tidak bersalut > tablet bersalut (Proudfoot, 1990).
(d). Jenis dan jumlah bahan tambahan (eksipien) seperti bahan pengisi, bahan pelicin, bahan pengikat, garam netral, garam asam atau garam basa, dan lain-lain
(e). Ukuran granul dan distribusi ukurannya
Dalam proses pembuatan tablet, proses granulasi merupakan proses pengikatan campuran dan mempengaruhi sifat alir. Setelah granul dibentuk menjadi tablet maka tablet akan mempertahankan integritasnya. Ukuran granul dan distribusi ukurannya penting karena mempengaruhi hancurnya tablet menjadi granul yang kemudian hancur menjadi partikel-partikel kecil, sehingga akan mempengaruhi ukuran partikel yang mempengaruhi luas permukaan dan akan menentukan bioavailabilitas obat (Wagner, 1975).
(f). Jenis dan jumlah bahan penghancur dan metode mencampurnya
Bahan penghancur biasanya merupakan bahan yang akan mengembang apabila ada air yang kemudian akan menekan tablet untuk hancur. Proses disintegrasi tablet dalam cairan aqueous pada saluran gastrointestinal merupakan salah satu rate limiting step yang menentukan bioavailabilitas obat (Wagner, 1975).
(g).Waktu pencampuran
tersebut tidak tercampur dengan baik sehingga akan mempengaruhi konsentrasi obat dalam tubuh (Wagner, 1975).
(h). Tekanan kompresi
Tekanan kompresi menentukan waktu hancur tablet dan kecepatan disolusi obat dari bentuk tablet (Wagner, 1975).
(i). Efek matrik
Untuk obat-obat yang lepas lambat maka terjadi efek matrik. Ketika obat diberikan secara oral, maka pada fase aqueous, air akan masuk ke dalam matrik yang terbuat dari polimer sintetik yang tidak terabsorpsi pada saluran gastrointestinal, kemudian obat akan terlepas dari matrik secara perlahan-lahan (Wagner, 1975).
(j). Jenis dan jumlah surfaktan
mempengaruhi enzim pemetabolisme obat atau ikatan obat dengan reseptor. Surfaktan dapat mengganggu integritas dan fungsi membran, surfaktan juga dapat mengubah waktu pengosongan lambung (Wagner, 1975; Proudfoot, 1990).
(k). Bentuk dan geometri
Bentuk dan geometri akan mempengaruhi kecepatan disolusi obat. Hal ini berhubungan dengan luas permukaan area efektif dan bentuk sediaan (Wagner, 1975).
(l). Kondisi lingkungan selama pembuatan
Kelembaban selama pembuatan dapat mempengaruhi potensi dari bentuk sediaan yang dibuat misalkan aspirin karena kondisi lembab akan terhidrolisis sehingga mempengaruhi bentuk sediaan yang dibuat (Wagner, 1975).
(m). Kondisi penyimpanan dan lama penyimpanan
2). Faktor Fisiologi
Faktor fisiologik mempengaruhi pelepasan, disolusi obat dari bentuk sediaan, absorpsi pada saluran pencernaan dan dapat mempengaruhi profil bioavailabilitas obat. Faktor-faktor tersebut yaitu :
a. Motilitas usus dan waktu transit obat dalam usus
Usus merupakan tempat utama terjadinya absorpsi obat sehingga semakin besar kecepatan transit usus maka semakin kecil waktu tinggal obat di dalam usus berarti makin kecil waktu obat kontak dengan tempat absorpsi sehingga jumlah obat yang terabsorpsi menjadi kecil (Proudfoot 1990).
b. Kecepatan pengosongan lambung
Kebanyakan obat diabsorpsi di usus halus sehingga penurunan kecepatan obat dalam bentuk larutan meninggalkan lambung, akan menurunkan kecepatan absorpsi obat dan menunda onset efek terapeutik dari obat. Selain itu, ada obat-obat yang akan mengalami degradasi akibat pH lambung dan aktivitas enzim dalam cairan lambung jika terjadi penundaan pengosongan dalam lambung sehingga akan menurunkan konsentrasi efektif obat dan mempengaruhi bioavailabilitas. Salah satu faktor yang meningkatkan kecepatan pengosongan lambung adalah rasa lapar Proudfoot, 1990).
c. Tempat absorpsi dan area permukaan yang efektif untuk absorpsi obat
villi dan mikrovilli pada usus halus sehingga kebanyakan obat akan terabsorpsi maksimum di dalam usus halus yang berarti akan menghasilkan kecepatan dan jumlah obat terabsorpsi yang maksimum (menentukan bioavailabilitas). Glycocalyx merupakan lapisan pada mikrovilli. Absorpsi obat dari lumen usus halus untuk mencapai pembuluh darah harus melewati beberapa barrier. Larutan obat untuk mencapai mikrovilli harus berdifusi menembus unstirred layer, lapisan mukus dan glycocalyx (Proudfoot, 1990).
d. Nilai pH cairan gastrointestinal, konsentrasi elektrolit
Keasaman (pH) cairan di saluran gastrointestinal bervariasi, pH cairan lambung antara 1-3,5; pH cairan usus halus antara 5-8 (pH 5-6 di duodenum dan sekitar pH 8 di ileum), pH cairan usus besar sekitar 8. Nilai pH cairan gastrointestinal akan mempengaruhi absorpsi obat. Nilai pH cairan gastrointestinal dapat menentukan absorpsi dalam berbagai cara karena kebanyakan obat merupakan asam lemah atau basa lemah, kelarutan komponen-komponen tersebut dalam air dipengaruhi pH, dan kecepatan disolusi dari bentuk sediaan terutama tablet dan kapsul juga dipengaruhi pH. Bagian obat yang terionisasi lebih larut dalam air daripada bagian obat yang tak terionisasi (Mayersohn, 2002; Shargel et al., 2005).
e. Stabilitas obat pada saluran gastrointestinal
mengalami degradasi dan mengalami metabolisme di saluran gastrointestinal, akibatnya fraksi obat yang terabsorpsi menjadi lebih kecil sehingga menurunkan bioavailabilitas obat (Proudfoot, 1990; Wagner, 1975).
f. Metabolisme hepatik
Hati merupakan tempat utama terjadinya metabolisme. First-pass effect merupakan fenomena dimana sebagian obat sebelum mencapai sirkulasi sistemik mengalami metabolisme di hati sehingga akan menurunkan jumlah obat yang terabsorpsi yang berarti menurunkan bioavailabilitas (Proudfoot, 1990)
g. Keberadaan makanan di saluran pencernaan
Mekanisme makanan dalam mempengaruhi bioavailabilitas obat yaitu dengan mengubah kecepatan pengosongan lambung, menyebabkan terjadinya stimulasi sekresi gastrointestinal, kompetisi antara komponen makanan dan obat, kompleksasi obat dengan komponen dalam makanan, meningkatkan viskositas dari isi gastrointestinal, dan dapat mengubah aliran darah ke hati (Proudfoot, 1990; Wagner, 1975).
tekanan hidrostatik dan intralumenal, kapasitas buffer, dan tonisitas (Wagner, 1975).
2. Distribusi
Setelah diabsorpsi, obat akan didistribusi ke seluruh tubuh melalui sirkulasi darah (Setiawati, Zulnida, Suyatna, 2002). Distribusi merupakan proses perpindahan obat dari sirkulasi sistemik menuju ke jaringan dan organ tubuh serta ke cairan tubuh lainnya seperti cairan interstitial dan cairan intercellular (Wilkinson, 2001).
Distribusi obat dibedakan atas 2 fase berdasarkan penyebarannya di dalam tubuh. Distribusi fase pertama berjalan dengan cepat yaitu ke organ-organ yang perfusinya cepat seperti hati, ginjal, dan otak. Distribusi fase kedua memerlukan waktu lebih lama sebelum mencapai keseimbangan konsentrasi obat di jaringan dengan yang di dalam darah, yaitu ke organ-organ yang perfusinya tidak secepat organ di atas seperti otot, visera, kulit, dan jaringan lemak (Setiawati dkk., 2002; Wilkinson, 2001).
3. Biotransformasi atau metabolisme
mengakhiri kerja obat (Setiawati dkk., 2002). Biotransformasi terjadi pada hati, saluran cerna, ginjal, dan paru-paru (Wilkinson, 2001).
Reaksi biotransformasi obat dapat dibedakan menjadi 2 fase. Reaksi fase I adalah reaksi fungsional yang mengubah obat menjadi metabolit yang lebih polar, meliputi reaksi oksidasi, reduksi, dan hidrolisis (Setiawati dkk., 2002). Reaksi fase II merupakan reaksi biosintetik (konjugasi). Reaksi ini merupakan reaksi konjugasi obat atau metabolit hasil reaksi fase pertama dengan menggunakan substrat endogen seperti asam glukuronat, sulfat, glutation, asam amino atau asetat. Konjugat yang dihasilkan akan bersifat polar, inaktif dan dengan cepat dapat diekskresi melalui urin dan feses (Setiawati dkk., 2002; Wilkinson, 2001).
4. Ekskresi
Ekskresi merupakan peristiwa pengeluaran obat dan atau metabolitnya dari dalam tubuh. Ginjal merupakan organ terpenting untuk mengekskresi obat dan metabolitnya. Obat dikeluarkan dari tubuh dalam bentuk metabolit hasil biotransformasi atau dalam bentuk asalnya. Obat atau metabolit polar diekskresi lebih cepat daripada obat larut lemak (Setiawati dkk., 2002).
C. Bioekivalensi 1. Definisi
Ekivalensi dapat didefinisikan antara lain :
a. Ekivalensi kimia menunjukkan dua atau lebih sediaan obat mengandung jumlah yang sama yang tertera pada label (kurang lebih pada rentang tertentu) (Malinowski, 2000).
b. Ekivalensi klinik terjadi ketika obat yang sama dari dua atau lebih sediaan obat menunjukkan efek in vivo yang identik yang terukur dari respon farmakologik atau dari kontrol gejala atau penyakit (Malinowski, 2000). c. Ekivalensi terapeutik menyatakan bahwa dua merek produk obat diharapkan
akan menghasilkan hasil klinik yang sama (Malinowski, 2000). Dua produk obat mempunyai ekivalensi terapeutik jika keduanya mempunyai ekivalensi farmaseutik atau merupakan alternatif farmaseutik dan pada pemberian dengan dosis molar yang sama akan menghasilkan efikasi klinik dan keamanan yang sebanding. Dengan demikian, ekivalensi / inekivalensi terapeutik seharusnya ditunjukkan dengan uji klinik (Anonim, 2004 b). Ekivalensi farmasetik
d. ditujukan pada dua produk dengan kesamaan bentuk sediaan, zat aktif dan jumlah zat aktif (Malinowski, 2000; Anonim 2004 b). e. Alternatif farmasetik jika keduanya mengandung zat aktif yang sama tetapi
berbeda dalam bentuk kimia (garam, ester, dsb.) atau bentuk sediaan atau kekuatan (Anonim, 2004 b; Chereson, 1999).
sediaan yang sama mencapai sirkulasi sistemik dengan kecepatan dan jumlah yang sama atau bisa disebut memiliki bioavailabilitas yang sama. Bioekivalensi ditunjukkan jika keduanya mempunyai ekivalensi farmasetik atau merupakan alternatif farmasetik dan pada pemberian dengan dosis molar yang sama akan menghasilkan bioavailabilitas yang sebanding sehingga efeknya akan sama, dalam hal efikasi maupun keamanan (Malinowski, 2000; Anonim, 2004 b).
2. Studi Bioavailabilitas dan Bioekivalensi
Studi bioavailabilitas dilakukan baik terhadap bahan obat aktif yang telah disetujui maupun terhadap obat dengan efek terapeutik yang belum disetujui oleh Food and Drug Administration (FDA) untuk dipasarkan. FDA dalam menyetujui
suatu produk obat untuk dipasarkan harus yakin bahwa produk obat tersebut aman dan efektif sesuai label indikasi penggunaan serta harus memenuhi seluruh standar yang digunakan dalam identitas, kekuatan, kualitas dan kemurnian (Shargel et al., 2005).
dagang (Chereson, 1999).
Bioavailabilitas dari produk obat sering menentukan efikasi terapeutik dari obat tersebut karena hal ini mempengaruhi onset, intensitas, dan durasi dari respon terapeutik obat tersebut (Chereson, 1999). Pada studi bioekivalensi, dibutuhkan suatu formulasi obat sebagai standar pembanding yang hendaknya mengandung obat aktif terapeutik dalam formulasi yang paling banyak berada dalam sistemik (yakni larutan atau suspensi), dalam jumlah sama, dan hendaknya diberikan dengan rute sama seperti formulasi yang dibandingkan (Shargel et al., 2005).
Bioekivalensi dapat dilakukan menggunakan uji in vitro jika uji in vitro memiliki korelasi yang baik dengan data bioavailabilitas secara in vivo. Selain itu, uji bioekivalensi dapat dilakukan melalui studi farmakodinamika melalui uji perbandingan klinis (Malinowski, 2000).
3. Korelasi in vitro dan in vivo
Korelasi in vitro dan in vivo yang dimaksud adalah hubungan antara karakteristik biologi obat (efek farmakodinamika atau konsentrasi obat dalam plasma) dan karakteristik fisika kimia produk obat (Shargel et al., 2005). Korelasi in vitro dan in vivo ini penting untuk diketahui agar dalam menentukan bioavailablitas suatu obat
Parameter uji in vitro yang paling dekat hubungannya dengan bioavailabilitas adalah kecepatan disolusi. Obat yang masuk ke dalam tubuh dapat diabsorpsi jika sudah dalam bentuk larutan sehingga kecepatan obat untuk larut dari bentuk sediaannya (laju disolusi) akan menentukan kecepatan dan atau jumlah obat yang terabsorpsi (Chereson, 1999).
D. Dasar-dasar Farmakokinetika 1. Definisi
Farmakokinetika adalah ilmu yang mempelajari kinetika absorpsi, distribusi dan eliminasi (terdiri dari metabolisme dan ekskresi) dari obat. Studi farmakokinetika meliputi pendekatan eksperimental dan teoritis. Aspek eksperimental dari farmakokinetika meliputi perkembangan teknik pengambilan sampel biologis, metode analisis obat dan metabolitnya, dan prosedur pengolahan data. Aspek teoritis dari farmakokinetika meliputi perkembangan model farmakokinetika yang digunakan untuk memprediksikan proses disposisi yang terjadi setelah pemberian obat. Aplikasi dari metode statistik termasuk dalam studi farmakokinetika yaitu untuk penetapan parameter farmakokinetika dan interpretasi data (Shargel, Wu-Pong, B. C. Yu, 2005).
2. Model Farmakokinetika
Model farmakokinetika digunakan untuk menginterpretasikan data-data farmakokinetika (Shargel et al., 2005).
Kompartemen dianggap sebagai sebuah jaringan atau kumpulan jaringan yang memiliki kesamaan aliran darah dan afinitas terhadap obat. Di setiap kompartemen, obat dianggap terdistribusi secara seragam. Model ini merupakan suatu sistem terbuka apabila obat dapat dieliminasi dari tubuh (Shargel et al., 2005). Kompartemen farmakokinetik ini tidak berhubungan dengan lokasi secara anatomi tubuh namun hanya parameter operasional yang diturunkan secara matematis (Mutschler, Derendorf, Schäfer-Korting, Elrod and Estes, 1995).
Model satu kompartemen menunjukkan bahwa setelah pemberian, obat terdistribusi secara langsung. Model dua atau lebih kompartemen, terjadi distribusi obat ke dalam ruang distribusi yang dapat dilewatinya dengan kecepatan berbeda-beda (Mutschler et al., 1995). Model dua kompartemen, obat dapat berpindah antara kompartemen sentral ke dan dari kompartemen perifer (jaringan). Kompartemen sentral menggambarkan plasma dan organ yang memiliki perfusi tinggi dan secara cepat seimbang dengan obat. Jumlah total obat di dalam tubuh dapat dihitung dari jumlah obat di dalam kompartemen sentral ditambah dengan obat di dalam kompartemen jaringan (Shargel et al., 2005).
3. Parameter Farmakokinetika
farmakokinetika diperoleh dari profil kinetika dari obat yang dapat diperoleh melalui kurva konsentrasi obat terhadap waktu. Konsentrasi obat dapat diukur sebagai fungsi terhadap waktu di beberapa cairan tubuh seperti darah, plasma, serum, saliva, dan urin. Konsentrasi obat dalam darah mencerminkan perubahan kinetika di sirkulasi sistemik. Untuk mendapatkan kurva konsentrasi obat terhadap waktu maka perlu dilakukan pengukuran konsentrasi obat berulangkali pada beberapa titik waktu (Mutschler et al., 1995). Parameter-parameter farmakokinetika antara lain:
a. AUC (Area under the curve)
AUC merupakan ukuran dari jumlah obat di dalam tubuh dan dapat dihitung dengan menggunakan rumus trapezoid, yaitu :
[
]
t n-1 n(
n n-1t t t
2 C C AUC n
1
-n −
+
=
) (7)
AUC = area di bawah kurva
tn = waktu pengamatan dari konsentrasi obat Cn
tn-1 = waktu pengamatan sebelumnya yang berhubungan dengan konsentrasi
obat Cn-1 (Mutschler et al., 1995).
Dalam hal ini area tersisa,
[
]
k C AUC t pn
tn =
∞ (8)
Cpn = konsentrasi dalam plasma terakhir pada tn
k = slop yang diperoleh dari bagian akhir kurva (Shargel et al., 2005).
Untuk menghitung AUC total (AUC∞) maka dilakukan ekstrapolasi bagian akhir area setelah titik terakhir yang diukur (AUCtn - ∞). Prosedur yang
digunakan disebut sahih bila bagian ekstrapolasi tersebut kira-kira di bawah 10% dari AUC total dan tidak boleh digunakan bila melebihi 20% dari AUC total (Mutschler et al., 1995).
b. Volume distribusi (Vd)
Parameter ini menunjukkan volume penyebaran obat dalam tubuh dengan kadar plasma atau serum. Vd tidak perlu menunjukkan volume
penyebaran obat yang sesungguhnya ataupun volume secara anatomik, tetapi hanya volume imajinasi dimana tubuh dianggap sebagai 1 kompartemen yang terdiri dari plasma atau serum, dan Vd menghubungkan jumlah obat dalam
tubuh dengan kadarnya dalam plasma atau serum (Setiawati, 2002). DB = Vd . C (9) p
D = jumlah obat dalam tubuh B
Tubuh dapat dianggap sebagai suatu sistem dengan volume yang konstan. Oleh karena itu, volume distribusi untuk suatu obat umumnya konstan (Shargel et al., 2005). Volume distribusi besar menunjukkan jumlah obat yang terdistribusi ke dalam jaringan besar atau terkonsentrasi di jaringan tertentu (Mutschler, et al., 1995).
c. Bersihan total (Klirens / Cl)
Klirens adalah volume plasma yang dibersihkan dari obat per satuan waktu oleh seluruh tubuh (ml/menit). Parameter ini menunjukkan kemampuan tubuh untuk mengeliminasi obat. Untuk obat dengan kinetika orde satu, Cl merupakan bilangan konstan pada kadar obat yang biasa ditemukan dalam klinik.
oral oral
IV IV
AUC F.D AUC
D
Cl= = (10)
el
d k
V
Cl= ⋅ (11)
D = Dosis
F = Fraksi obat yang terabsorpsi
Umumnya bersihan total merupakan hasil beberapa bersihan bagian bersama-sama, yang terpenting adalah bersihan ginjal (ClR) dan bersihan hati
(ClH) (Mutschler, 1991).
d. Waktu paruh eliminasi (t ) dan kecepatan eliminasi ½
Waktu paruh eliminasi adalah waktu yang diperlukan untuk turunnya kadar obat dalam plasma atau serum pada fase eliminasi (setelah fase absorpsi dan distribusi) menjadi separuhnya. Untuk obat-obat dengan kinetika orde reaksi satu, t½ ini merupakan bilangan konstan, tidak tergantung dari besarnya
dosis, interval pemberian, kadar plasma maupun cara pemberian (Setiawati, 2002).
el
el k
0,693 k
2 ln t
2
1 = = (12)
kel adalah konstanta kecepatan eliminasi.
Waktu paruh eliminasi adalah parameter farmakokinetik yang berbeda dengan waktu paruh dari efek atau waktu yang diperlukan untuk menjadikan efek farmakologi menjadi separuh dengan efek semula (Mutschler et al., 1995).
2 1
t 2 ln
kel = (13)
e. Bioavailabilitas
Parameter ini menunjukkan fraksi dari dosis obat yang mencapai peredaran darah sistemik dalam bentuk aktif (Setiawati, 2002). Faktor yang menentukan bioavailabilitas adalah kecepatan dan jumlah obat yang dilepas dari bentuk sediaannya, kecepatan dan jumlah obat yang mengalami absorpsi, dan besarnya efek lintas pertama (Mutschler et al., 1995).
Besarnya bioavailabilitas absolut dapat dihitung dengan cara sebagai berikut :
( )
% 100 AUCAUC F
i.v
x ⋅
= (14)
F = bioavailabilitas absolut AUC = AUC pemberian nonsistemik x
= AUC pemberian intravaskuler AUCiv
Dalam kasus apabila dosis dan formulasi untuk rute pemberian i.v tidak ada, maka dapat ditentukan bioavailabilitas relatif yang diperoleh dengan cara :
( )
% 100 AUCAUC F
standar x
rel= ⋅ (15)
= AUC pemberian nonsistemik AUCx
AUCstandar = AUC produk standar
Parameter untuk menggambarkan kecepatan absorpsi adalah konsentrasi obat dalam plasma maksimum (Cmaks) dan selang waktu antara
pemberian obat hingga mencapai konsentrasi maksimum dalam plasma (tmaks) (Mutschler et al., 1995).
4. Strategi Penelitian Farmakokinetika
Strategi penelitian farmakokinetika (SPF) adalah rencana yang disusun sebelum meneliti tahap farmakokinetika obat, guna memperoleh informasi tentang nasib obat dalam tubuh secara kuantitatif. Objek penelitian farmakokinetika adalah tahap farmakokinetika obat dengan parameter farmakokinetika sebagai tolok ukurnya. Parameter farmakokinetika adalah besaran yang diturunkan secara matematik dari hasil pengukuran kadar obat atau metabolitnya di dalam darah atau urin (Suryawati dan Donatus, 1998).
Tahap-tahap SPF meliputi : 1. Pemilihan rancangan uji coba. 2. Pemilihan subjek uji dan jumlahnya. 3. Pemilihan cuplikan hayati.
4. Pemilihan metode analisis penetapan kadar. Syarat-syarat metode analisis yaitu :
selektivitas adalah kemampuan metode analisis untuk membedakan suatu obat dengan metabolitnya, obat lain dan kandungan endogen cuplikan hayati.
b. sensitivitas
sensitivitas berkaitan dengan kadar terendah yang dapat diukur dengan metode analisis yang digunakan. Hal ini diperlukan karena untuk menghitung parameter farmakokinetika suatu obat diperlukan kadar obat tertinggi sampai terendah pada rentang waktu tertentu.
c. ketelitian dan ketepatan
ketelitian dan ketepatan ini akan menentukan kesahihan hasil penetapan kadar. Ketepatan (accuracy) ditunjukkan oleh kemampuan metode memberikan hasil pengukuran sedekat mungkin dengan nilai yang sesungguhnya. Ketelitian (precision) menunjukkan kedekatan hasil pengukuran berulang pada cuplikan hayati yang sama.
5. Pemilihan takaran dosis dan bentuk sediaan obat.
Takaran dosis yang diberikan harus menjamin dapat diukurnya kadar obat atau metabolitnya pada rentang waktu tertentu sehingga diperoleh data yang cukup memadai untuk analisis farmakokinetika.
6. Pemilihan lama dan banyaknya waktu pengambilan cuplikan hayati.
obat sebaiknya dilakukan setidaknya 3 kali pada tahap absorpsi, 3 kali di sekitar puncak, 3 kali pada tahap distribusi, dan 3 kali pada tahap eliminasi.
7. Analisis dan evaluasi hasil.
Langkah-langkah ini meliputi analisis sederetan kadar obat utuh atau metabolitnya dalam darah atau urin, analisis statistika dan evaluasi (Suryawati dan Donatus, 1998).
E. Desain Cross Over
Desain cross over merupakan desain blok secara acak dimana tiap blok menerima lebih dari satu formulasi obat pada waktu yang berbeda. Keuntungan dari desain cross over pada studi bioavailabilitas-bioekivalensi adalah tiap subjek bertindak sebagai kontrol sendiri, desain ini menghilangkan variasi biologik antarsubjeknya, dan dengan randomisasi yang tepat maka hal ini akan memberikan kalkulasi yang paling baik mengenai perbedaan tiap formulasi (Chow and Jen-Pei, 2000)
(> 24 jam), dapat dipertimbangkan penggunaan desain dua kelompok paralel (Anonim, 2004 b).
F. Parasetamol
Parasetamol mengandung tidak kurang dari 98,0 % dan tidak lebih dari 101,0 % C H NO8 9 2, dihitung terhadap zat anhidrat. Parasetamol berupa serbuk hablur
putih, tidak berbau, rasa sedikit pahit. Larut dalam air mendidih dan dalam NaOH 1 N, mudah larut dalam etanol. Tablet parasetamol mengandung parasetamol tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket (Anonim, 1995). Larut dalam 70 bagian air, dalam 7 bagian etanol (95 %) P, dalam 13 bagian aseton P, dalam 40 bagian gliserol P, dan dalam 9 bagian propilenglikol P, larut dalam larutan alkali hidroksida. Khasiat dan penggunaan : analgetikum, antipiretikum (Anonim, 1979).
NHCOCH3
HO
N-(4-hydroxyphenyl)acetamide
Gambar 4. Struktur Parasetamol (Anonim, 1995)
2000).
Melalui uji klinis, telah terbukti bahwa makanan dapat menurunkan tingkat absorpsi parasetamol. Pada keadaan puasa secara nyata dapat meningkatkan kecepatan absorpsi parasetamol walaupun tidak mempengaruhi jumlah total yang diabsorpsi (McGilveray and Mattok, 1972). Menurut Lacy, Armstrong, Goldman, dan Lance (2003), parasetamol cepat diabsorpsi dan hampir sempurna, namun apabila parasetamol dikonsumsi diikuti dengan makanan berkarbohidrat tinggi akan terjadi penundaan absorpsi yang berarti menunjukkan penurunan kecepatan absorpsi. Menurut Proudfoot (1990), makanan akan menurunkan laju pengosongan lambung sehingga akan menunda onset parasetamol.
Onset dari parasetamol relatif cepat, yaitu kurang dari 1 jam, sedangkan durasinya sekitar 4 – 6 jam. Parasetamol memiliki tmax 0,5 – 2 jam. Obat ini tersebar
ke seluruh cairan tubuh. Availabilitas oral parasetamol adalah 88 ± 15% (Benet, 1992). Dalam plasma, 20 – 50% parasetamol akan terikat oleh protein plasma (Anonim, 2004 a ; Lacy et al., 2003). Volume distribusi dari parasetamol adalah 0,94 L/kg (Melmon and Morelli, 1992) atau pada manusia 70 kg, volume distribusinya sekitar 67 ± 8 L (Benet, 1992).
(Kadar Efek Minimum) parasetamol adalah bila kadar parasetamol dalam darah adalah sebesar 10µg/ml hingga 20 µg/ml, sedangkan nilai KTM (Kadar Toksik Minimum) parasetamol adalah bila kadar parasetamol dalam plasma lebih besar dari 300 µg/mL (Benet, 1992).
Parasetamol akan dimetabolisme oleh enzim mikrosom hati. Sebagian parasetamol (80%) dikonjugasi dengan asam glukuronat dan sebagian kecil lainnya dengan asam sulfat. Selain itu, parasetamol juga dapat mengalami hidroksilasi. Metabolit hasil hidroksilasi ini, dapat menimbulkan methemoglobinemia dan hemolisis eritrosit (Wilmana, 2002). Klirens parasetamol adalah 250 ml/menit sampai 450 ml/menit. Klirens parasetamol akan turun apabila terjadi disfungsi hati. Klirens akan meningkat bila terjadi hipertiroidsm (Melmon and Morelli, 1992).
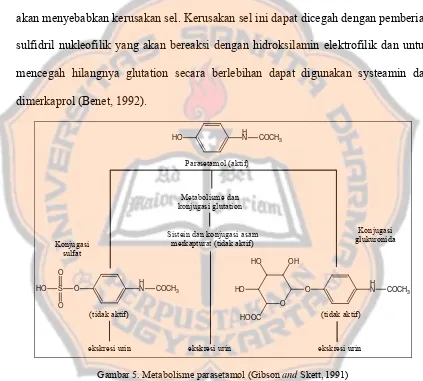
Parasetamol mengalami metabolisme fase kedua yang menghasilkan inaktivasi farmakologis dari obat induk. Seperti yang terlihat pada gambar 5, parasetamol mengalami konjugasi glutation, glukuronida, dan konjugasi sulfat, dan sebagai hasilnya konjugasi fase kedua tidak aktif secara farmakologis (Gibson and Skett, 1991).
Hidroksilamin akan bereaksi nonenzimatik dengan glutation dan kemudian akan didetoksifikasi. Namun, karena jumlah glutation di hati terbatas maka apabila parasetamol dikonsumsi berlebihan maka hidroksilamin yang mungkin terbentuk akan bereaksi dengan makromolekul dan merusak struktur dan fungsinya sehingga akan menyebabkan kerusakan sel. Kerusakan sel ini dapat dicegah dengan pemberian sulfidril nukleofilik yang akan bereaksi dengan hidroksilamin elektrofilik dan untuk mencegah hilangnya glutation secara berlebihan dapat digunakan systeamin dan dimerkaprol (Benet, 1992).
HO HN COCH3
O HN COCH3
S O
O
HO O HN COCH3
O OH HO
HO
HOOC Parasetamol (aktif)
Konjugasi sulfat
Konjugasi glukuronida
(tidak aktif) (tidak aktif)
Metabolisme dan konjugasi glutation
Sistein dan konjugasi asam merkapturat (tidak aktif)
ekskresi urin ekskresi urin ekskresi urin
Gambar 5. Metabolisme parasetamol (Gibson and Skett, 1991)
menghilangkan atau mengurangi nyeri ringan sampai sedang. Parasetamol menurunkan suhu tubuh dengan mekanisme yang diduga juga berdasarkan efek sentral seperti salisilat (Wilmana, 2003).
G. Darah
Darah terdiri atas unsur-unsur padat, yaitu eritrosit, leukosit serta trombosit yang tersuspensi di dalam suatu media cair yakni plasma. Pada darah normal, jumlah plasma mencapai 55% dari volume darah. Konsentrasi total protein dalam plasma manusia kurang lebih 77,5 g/dL, dan membentuk bagian utama unsur-unsur padat plasma.
Begitu darah membeku (mengalami koagulasi), fase cair yang tertinggal dinamakan serum. Serum sudah tidak lagi mengandung faktor-faktor pembekuan (termasuk fibrinogen) (Murray, Granner, Mayes, and Rodwell, 1990). Plasma dihasilkan dari melakukan sentrifugasi pada darah dan ditambahkan ke dalamnya bahan antikoagulan Chamberlain, 1995).
mencakup protein sederhana tetapi juga protein terkonjugasi seperti glikoprotein serta berbagai tipe lipoprotein (Murray et al., 1990). Sebanyak 55% dari jumlah protein total tersebut adalah albumin (Montgomery, Conway, Spector, 1993).
Sering terdapat afinitas yang kuat antara protein dengan obat, dan penghilangan protein secara langsung dengan ultrafiltrasi atau dialisis dapat juga menghilangkan fraksi yang besar dari obat. Di sisi lain, pengukuran obat secara langsung, hanya mengukur obat yang bebas, bukan keseluruhan obat yang ada. Oleh sebab itu, permasalahan yang dihadapi adalah bagaimana menghancurkan ikatan antara protein dengan obat dan memperoleh keseluruhan obat untuk dianalisis (Chamberlain, 1995).
Metode paling sederhana dan paling tua adalah dengan mengendapkan protein dan memperoleh filtratnya. Protein didenaturasi dan ikatannya dengan obat dihancurkan sehingga obat seluruhnya terlepas di dalam filtrat. Reagen asam yang paling terkenal untuk denaturasi protein ini adalah asam trikloroasetat dan asam tungstat (Chamberlain, 1995).
H. Kolorimetri 1. Definisi
senyawa tidak berwarna menjadi zat berwarna dan penentuan fotometrinya dilakukan dalam daerah sinar tampak (400-800 nm) (Roth and Blascke, 1981).
2. Kriteria analisis kolorimetri
Kriteria untuk analisis kolorimetri yang baik adalah : a. Menghasilkan reaksi warna yang khusus
Reaksi-reaksi yang ada sangat sedikit sekali untuk beberapa substansi tertentu, tetapi justru memberikan warna-warna yang banyak membentuk kelompok warna tersendiri yang hanya berhubungan dengan substansi khusus.
b. Adanya proporsi yang sesuai antara warna dan konsentrasi
Untuk kolorimetri visual sangat penting bahwa intensitas warna harus meningkat secara linear dengan konsentrasi dari substansi yang ditentukan. c. Stabilitas warna
Warna yang dihasilkan harus sama untuk mendapatkan hasil yang akurat. Hal ini menerapkan reaksi-reaksi dari warna yang akan dicapai secara maksimal. Waktu untuk mencapai warna yang maksimal harus cukup lama untuk mendapatkan pengukuran yang akurat.
d. Reprodusibel
Prosedur kolorimetri harus memberikan hasil yang reprodusibel dalam kondisi yang spesifik.
e. Kejernihan larutan
dengan standar. Kekeruhan akan menyerap cahaya dengan baik (Bassett, Denney, Jeffrey, and Mendham, 1991).
3. Metode kolorimetri untuk parasetamol
Ada beberapa macam cara yang dapat digunakan pada metode kolorimetri untuk parasetamol, yaitu:
a. Cara asam nitrat
Parasetamol yang dilarutkan dengan metanol dan ditambah larutan asam nitrat akan menghasilkan warna kuning kemerahan (Connors et al., 1986).
NHCOCH3
OH
HNO3
NHCOCH3
OH
NO2
Gambar 6. Reaksi parasetamol dengan asam nitrat (Connors et al., 1986)
b. Cara hidrolisis menjadi p-aminofenol
NHCOCH3
OH
H+/ H2O
OH NH2
+ CH3COOH
parasetamol p-aminofenol asam asetat
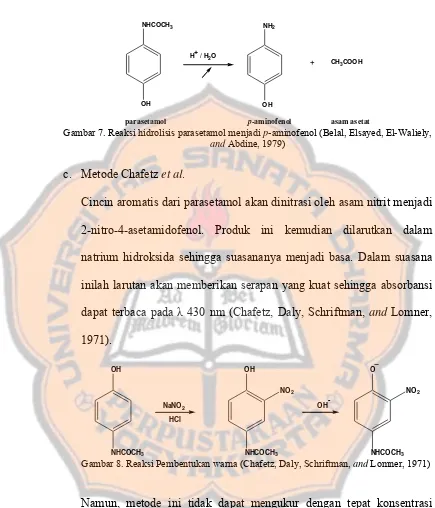
Gambar 7. Reaksi hidrolisis parasetamol menjadi p-aminofenol (Belal, Elsayed, El-Waliely, and Abdine, 1979)
c. Metode Chafetz et al.
Cincin aromatis dari parasetamol akan dinitrasi oleh asam nitrit menjadi 2-nitro-4-asetamidofenol. Produk ini kemudian dilarutkan dalam natrium hidroksida sehingga suasananya menjadi basa. Dalam suasana inilah larutan akan memberikan serapan yang kuat sehingga absorbansi dapat terbaca pada λ 430 nm (Chafetz, Daly, Schriftman, and Lomner, 1971).
NHCOCH3
OH
NaNO2 HCl
OH
NHCOCH3
NO2
OH
-O
NHCOCH3
NO2
Gambar 8. Reaksi Pembentukan warna (Chafetz, Daly, Schriftman, and Lomner, 1971)
Namun, metode ini tidak dapat mengukur dengan tepat konsentrasi parasetamol dalam plasma di bawah 50 µg/ml sehingga pada konsentrasi tersebut biasanya digunakan metode kromatografi (Widdop, 1986).
dipengaruhi oleh salisilat (Chamberlain, 1995). Asam salisilat akan memberikan reaksi yang mirip dengan parasetamol, tetapi di dalam plasma asam salisilat baru akan memberikan intensitas warna yang mirip dengan 20 µg/ml parasetamol jika kadar asam salisilat di dalam plasma 1000 µg/ml. Sampel yang terkontaminasi oleh heparin yang mengandung kresol sebagai pengawet dapat memberikan hasil yang semu sebesar 200 µg/ml (Widdop, 1986).
I. Keterangan empiris
BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian perbandingan bioavailabilitas antara tablet Biogesic® dan tablet Pamol® dengan tablet parasetamol (generik) pada kelinci putih jantan termasuk ke dalam jenis penelitian eksperimental murni, rancangan eksperimental silang.
B. Variabel Penelitian dan Definisi Operasional
1. Variabel penelitian
a. Variabel utama
1). Variabel bebas
Variabel bebas dalam penelitian ini adalah 3 jenis tablet parasetamol yaitu tablet parasetamol generik, tablet Biogesic®, dan tablet Pamol®.
2). Variabel tergantung
Variabel tergantung merupakan hasil pengamatan penelitian ini, berupa parameter-parameter bioavailabilitas, yaitu :
a). AUC0-∞ adalah area di bawah kurva kadar obat dalam plasma terhadap
waktu dari waktu 0 sampai waktu tidak terhingga.
b). Cmax adalah kadar puncak obat dalam plasma yang teramati.
c). tmax adalah waktu sejak pemberian obat sampai dicapai Cmax.
a). ka adalah tetapan laju absorpsi.
b). AUC(0-t) merupakan area di bawah kurva kadar obat dalam plasma
terhadap waktu dari waktu ke-0 sampai waktu terakhir kadar obat diukur.
c). Vd (volume distribusi) adalah volume penyebaran obat dalam tubuh. d). Cl (klirens) adalah volume darah yang dapat dibersihkan dari obat per
satuan waktu.
e). t½ adalah waktu paruh obat dalam plasma. f). kel adalah tetapan laju eliminasi
b. Variabel pengacau
1). Variabel pengacau yang dapat dikendalikan, yaitu :
a). galur spesies hewan uji dikendalikan dengan galur lokal.
b). jenis kelamin hewan uji dikendalikan dengan jenis kelamin jantan. c). umur hewan uji dikendalikan dengan 2-3 bulan.
d). berat badan hewan uji dikendalikan dengan 1,7-2 kg.
e). status hewan uji sebelum perlakuan adalah dengan dipuasakan terhadap makanan dan minuman selama 18 jam sebelum perlakuan. 2). Variabel pengacau yang tidak dapat dikendalikan yaitu keadaan patologis
2. Definisi operasional
Definisi operasional pada penelitian ini yaitu :
a. Bioavailabilitas adalah persentase dan kecepatan zat aktif dalam suatu produk obat yang mencapai / tersedia dalam sirkulasi sistemik dalam bentuk utuh / aktif setelah pemberian produk obat tersebut
b. Bioekivalensi adalah perbandingan bioavailabilitas dari dua atau lebih produk obat.
c. Dua produk obat dikatakan bioekivalen jika :
0,8 < R T AUC geometrik rata -rata nilai AUC geometrik rata -rata nilai < 1,25 0,8 < R maks T maks ) C ( geometrik rata -rata nilai ) C ( geometrik rata -rata nilai < 1,25 0,8 < R maks T maks t geometrik rata -rata nilai t geometrik rata -rata nilai < 1,25
T = obat yang diuji
R = obat yang dijadikan sebagai pembanding
d. Obat generik adalah obat jadi dengan nama resmi yang ditetapkan dalam Farmakope Indonesia untuk zat berkhasiat yang dikandungnya
C. Bahan Penelitian
Asam trikloroasetat kualitas proanalisis (E. Merck, Darmstadt, Germany), larutan asam klorida pekat kualitas proanalisis (E. Merck, Darmstadt, Germany), natrium nitrit kualitas proanalisis (E. Merck, Darmstadt, Germany), asam sulfamat kualitas proanalisis (Sigma), natrium hidroksida kualitas proanalisis (E. Merck, Darmstadt, Germany), pa