PEMURNIAN PARSIAL LAKASE DARI ISOLAT KAPANG
TANDAN KOSONG KELAPA SAWIT
DAN UJI AKTIVITASNYA TERHADAP SUBSTRAT ALAM
SKRIPSI
RADITA YUNIAR ARIZANDY
PROGRAM STUDI S-1 KIMIA DEPARTEMEN KIMIA
FAKULTAS SAINS DAN TEKNOLOGI UNIVERSITAS AIRLANGGA
SURABAYA 2012
ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
PEMURNIAN PARSIAL LAKASE DARI ISOLAT KAPANG
TANDAN KOSONG KELAPA SAWIT
DAN UJI AKTIVITASNYA TERHADAP SUBSTRAT ALAM
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains Bidang Kimia pada Fakultas Sains dan Teknologi
OLEH
RADITA YUNIAR ARIZANDY NIM: 080810050
Tanggal lulus: 7 Agustus 2012
Disetujui Oleh
Pembimbing I,
Prof. Dr. Ni Nyoman Tri Puspaningsih NIP: 19630515 198701 2 001
Pembimbing II,
Dr. Ni’matuzahroh NIP: 19680105 199203 2 003 ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
LEMBAR PENGESAHAN NASKAH SKRIPSI
Judul : Pemurnian Parsial Lakase Dari Isolat Kapang Tandan Kosong Kelapa Sawit Dan Uji Aktivitasnya Terhadap Substrat Alam
Penyusun : Radita Yuniar Arizandy
NIM : 080810050
Tanggal Ujian : 7 Agustus 2012
Disetujui oleh :
Pembimbing I,
Prof. Dr. Ni Nyoman Tri Puspaningsih NIP: 19630515 198701 2 001
Pembimbing II,
Dr. Ni’matuzahroh NIP: 19680105 199203 2 003
Mengetahui : Ketua Departemen Kimia Fakultas Sains dan Teknologi
Universitas Airlangga
Dr. Alfinda Novi Kristanti, DEA NIP. 19671115 199102 2 001 ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
PEDOMAN PENGGUNAAN SKRIPSI
Skripsi ini tidak dipublikasikan, namun tersedia di perpustakaan dalam lingkungan Universitas Airlangga, diperkenankan untuk dipakai sebagai referensi kepustakaan, tetapi pengutipan harus seizin penyusun dan harus menyebutkan sumbernya sesuai kebiasaan ilmiah.
Dokumen skripsi ini merupakan hak milik Universitas Airlangga ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
i
KATA PENGANTAR
Segala puji syukur kepada Allah SWT atas segala limpahan berkat dan rahmat-Nya sehingga penyusun dapat menyelesaikan skripsi dengan judul “Pemurnian Parsial Lakase dengan Isolat Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap Substrat Alam”. Skripsi ini dibuat sebagai salah satu syarat untuk memperoleh gelar sarjana sains dalam bidang kimia Fakultas Sains dan Teknologi Universitas Airlangga.
Dalam kesempatan ini penyusun mengucapkan terima kasih yang sebesar-besarnya kepada semua pihak yang memberikan bantuan dan dukungan terutama kepada :
1. Prof.Dr. Ni Nyoman Tri Puspaningsih, M.Si selaku dosen pembimbing I yang selalu memberikan masukan dan meluangkan waktu bagi penulis untuk berkonsultasi.
2. Dr. Ni’matuzahroh selaku dosen pembimbing II yang selalu memberikan masukan dan meluangkan waktu bagi penulis untuk berkonsultasi.
3. Dr. Afaf Baktir M.S selaku dosen wali yang selalu memberikan kelancaran dalam proses penyusunan skripsi.
4. Seluruh dosen Departemen Kimia Universitas Airlangga atas ilmu yang telah diberikan.
5. Orang tua, seluruh keluarga, dan orang terkasih yang telah memberikan dukungan dan motivasi serta kasih sayang selama ini.
6. Teman – teman biokimia, Nadya Aisya’ dan Siska Winda Aryani atas dukungan, motivasi, dan bantuan dalam penyusunan skripsi.
7. Teman-teman angkatan 2008 Departemen Kimia Universitas Airlangga dan semua pihak yang telah membantu penulis.
Dalam penyusunan skripsi ini, penyusun menyadari bahwa masih terdapat banyak kekurangan dalam penyusunan skripsi ini, oleh karena itu penyusun sangat mengharapkan kritik dan saran yang bersifat membangun untuk kesempurnaan penulisan skripsi ini. Semoga skripsi ini dapat bermanfaat bagi semua pihak.
Surabaya, 28 Juli 2012 Penyusun,
Radita Yuniar Arizandy ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
ii Ucapan terima kasih diberikan kepada:
1. Allah SWT, atas rahmat dan hidayah yang diberikan selama proses
pembuatan skripsi hingga akhir.
2. Prof. Dr. Ni Nyoman Tri Puspaningsih, M.Si, selaku dosen
pembimbing I yang senantiasa sabar dan meluangkan waktu untuk
berkonsultasi dan membimbing serta memberi masukan bagi penulis .
3. Dr. Ni’matuzahroh, selaku dosen pembimbing II yang senantiasa
sabar dan meluangkan waktu untuk berkonsultasi, membimbing, dan
memotivasi penulis hingga naskah skripsi terselesaikan.
4. Dr. Afaf Baktir M.S, selaku dosen wali yang selalu memberikan
kelancaran dalam proses penyusunan skripsi.
5. Seluruh dosen Departemen Kimia Universitas Airlangga, atas ilmu
yang telah diberikan.
6. Mbak Anita, atas bantuan, saran, dan semangat yang diberikan
kepada penulis ketika penulis dilanda galau skripsi
4. Mama, papa, dan adik, atas doa, dukungan, kasih sayang, motivasi,
dan cinta yang selalu mengalir di saat penulis merasa jenuh. Kalian
merupakan inspirasi dan motivasi utama dalam penyelesaian naskah
skripsi.
5. Keluarga besar H. M. Djamhari, terima kasih atas dukungan dan doa
serta semangat yang selalu diberikan kepada penulis.
6. M. Nasrul Aziz, atas dukungan, doa, saran, motivasi, dan bantuan
yang tidak pernah berhenti kepada penulis sampai naskah skripsi
terselesaikan.
7. Biokimblast, terutama Siska dan Nadya yang selalu kompak dan
saling menghibur saat penulis merasa jenuh dan galau.
8. Luki, Oox, Julie, Aci, Adel, Aya, Bela, yang selalu bisa menjadi
tempat curhat, gosip, dan galau ketika penulis berada di titik jenuh.
Kalian adalah keluarga terindah.
ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
iii
9. Keluarga besar kimia 2008, atas berbagai bantuan dan informasi yang
dibagikan kepada penulis.
10. Keluarga besar philadevil, pipit, amel, sintia, yuni, mbak tria, mbak
retty, mbak indah, mbak ima, mbak tika atas dukungan dan doa bagi
penulis.
11. Pak damam dan mbak yuli, atas bantuan yang diberikan bagi penulis
dalam proses penyelesaian naskah skripsi.
12. Seluruh pihak yang membantu terselesainya naskah skripsi penulis
yang belum disebutkan satu per satu, terima kasih atas doa, bantuan,
dan dukungan yang telah diberikan.
Terima kasih atas dukungan, doa, motivasi, dan bantuan yang selalu
diberikan kepada penulis hingga naskah skripsi terselesaikan. Tak
henti – hentinya ucapan terima kasih diberikan kepada semua pihak
yang terkait.
Penulis,
Radita Yuniar Arizandy ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
iv
Radita Yuniar Arizandy, 2012, Pemurnian Parsial Lakase dari Isolat Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap Substrat Alam. Skripsi dibawah bimbingan Prof. Dr. Ni Nyoman Tri Puspaningsih, M.Si dan Dr. Ni’matuzahroh. Departemen Kimia Fakultas Sains dan Teknologi Universitas Airlangga.
ABSTRAK
Enzim lakase merupakan enzim yang mengkatalis pendegradasi lignin. Degradasi lignin dapat dilakukan secara optimum apabila enzim lakase memiliki aktivitas tinggi. Penelitian terdahulu telah berhasil mengisolasi dan mengkarakterisasi enzim lakase dari kapang A, B, C, dan D. Penelitian ini bertujuan untuk melakukan uji aktivitas enzim lakase dari kapang A, B, C, dan D, melakukan pemurnian parsial dengan garam ammonium sulfat untuk mengetahui tingkat kemurnian enzim lakase apabila dibandingkan dengan ekstrak kasar, dan mengamati profil permukaan substrat alam akibat perlakuan enzim dengan aktivitas tertinggi dengan menggunakan SEM (Scanning Microscope Electron). Penelitian ini diawali dengan menguji aktivitas enzim lakase dari kapang A, B, C, dan D didapatkan aktivitas sebesar 1,4 U/mL, 1,54 U/mL, 1,33 U/mL, dan 1,26 U/mL. Hasil pemurnian parsial enzim lakase dari masing – masing isolat dengan garam ammonium sulfat melalui proses dialisis untuk penghilangan garam yang terendapkan. Tingkat kemurnian enzim lakase dari kapang A, B, C, dan D masing – masing adalah sebesar 1,547 kali, 1,769 kali, 1,996 kali, dan 3,044 kali dari aktivitas ekstrak kasar. Profil permukaan substrat alam setelah diberi perlakuan enzim menjadi rusak, berongga, dan pecah akibat enzim lakase yang mengkatalis degradasi lignin.
Kata kunci: enzim lakase, lignin, pemurnian parsial, dialisis, Scanning Microscope Elektron
ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
v
Radita Yuniar Arizandy, 2012, Partial Purification of Laccase from Empty Palm Fruit Bunches Isolate and Determination of Natural Substrates Activity. The Script is Under Guidance of Prof. Dr. Ni Nyoman Tri P, M.Si and Dr. Ni’matuzahroh, Department Of Chemistry, Faculty of Sciences and Technology. Airlangga University, Surabaya.
ABSTRACT
Laccase is enzyme which catalyze the degradation of lignin. Degradation of lignin can be done optimally when the laccase has high activity. Previous research has succeeded isolated and characterize the laccase of the fungus A, B, C, and D. This study aimed to determine the activity of laccase from fungus A, B, C, and D, also the partial purification with ammonium sulfate salts to determine the purity levels of the laccase when compared with the crude extract, and observe the natural substrate surface profile due the activity of highest enzyme treatment by using SEM (Scanning Electron Microscope). This study begins by examining the activity of the enzyme laccase from fungus A, B, C, and D obtained by the activity of 1.4 U/mL, 1.54 U/mL, 1.33 U/mL, and 1.26 U/mL. The results of partial purification of laccase from each of isolates with ammonium sulfate salt through the dialysis process for removal precipitated salt. The purity level of the laccase from fungus A, B, C, and D respectively are 1.547 times, 1.769 times, 1.996 times and 3.044 times compared to the activity of crude extract. Surface profile of natural substrate that has been treated by enzyme is damaged, hollow, and broken by laccase that catalyze the degradation of lignin.
Keyword: laccase enzyme, lignin, partial purrification, dialisys, Scanning Microscope Electron
ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
vi
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
vii
3.3.2.1.2 Media PDA agar miring ... 27
3.3.2.1.3 Persiapan substrat alam ... 27
3.3.2.2 Media cair... 28
3.3.3 Persiapan tabung selofan ... 28
3.3.4 Peremajaan kapang... 28
3.3.5 Pembuatan larutan ... 29
3.3.5.1 Larutan buffer universal ... 29
3.3.5.2 Pembuatan larutan substrat ABTS ... 30
3.3.5.2.1 Pembuatan larutan asam asetat (CH3COOH) 0,2 M .... 30
3.3.5.2.2 Pembuatan larutan natrium asetat (CH3COONa) 0,2 M ... 30
3.3.5.2.3 Pembuatan buffer sodium asetat pH 4,5 ... 30
3.3.5.2.4 Pembuatan larutan substrat ABTS 0,4 mM... 30
3.6 Produksi Enzim Lakase ... 31
3.7 Uji Aktivitas Enzim Lakase ... 31
3.8 Penentuan Kadar Protein Lakase ... 32
3.9 Pemurnian Enzim Lakase ... 33
3.9.1 Pengendapan enzim lakase dengan amonium sulfat ... 34
3.9.2 Dialisis lakase ... 35
3.10 Hidrolisis Jerami Padi dan Tongkol Jagung dengan Enzim Lakase 35
3.11 Analisis Perubahan Struktur Lignin Jerami Padi dan Tongkol Jagung dengan Menggunakan SEM ... 36
BAB IV HASIL DAN PEMBAHASAN ... 37
4.1 Peremajaan Isolat Kapang Tandan Kosong Kelapa Sawit ... 37
4.2 Hasil Produksi Enzim Lakase ... 38
4.3 Hasil Uji Aktivitas Enzim Lakase Terhadap Substrat ABTS ... 39
4.4 Hasil Uji Kadar Protein ... 42
4.5 Hasil Pemurnian Enzim Lakase dari Keempat Isolat Tandan Kosong Kelapa Sawit ... 42
4.5.1 Hasil pengendapan enzim lakase dengan amonium sulfat ... 42
4.5.2 Hasil dialisis enzim lakase ... 46
4.6 Analisis Profil Permukaan Jerami Padi dan Tongkol Jagung Dengan Menggunakan SEM ... 49
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
viii
DAFTAR TABEL
Nomor Judul Tabel Halaman 3 Komposisi buffer universal ... 29 4 Pemurnian parsial enzim lakase ... 48
ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
ix
2.5 Pengaruh konsentrasi enzim terhadap laju reaksi ... 15
2.6 Pengaruh konsentrasi substrat terhadap laju reaksi ... 15
2.7 Pengaruh temperatur terhadap laju reaksi ... 16
2.8 Pengaruh pH terhadap laju reaksi ... 17
2.9 Representasi pita sinar-X dari struktur kristal lakase III dari Trametes versicolor (PDB code 1KYA) ... 17
2.10 Lignin, selulase, dan hemiselulase pada jaringan tumbuhan ... 18
2.11 Prekursor penyusun lignin ... 18
2.12 Struktur 3D lignin ... 19
2.13 Struktur lignin ... 19
2.14 Tabel kemurnian protein ... 21
2.15 Proses dialisis ... 23
4.1 Keempat isolat kapang tandan kosong kelapa sawit hasil peremajaan 37 4.2 Reaksi Asam 2,2’-azinobis-di-(3-ethylbenzthiazolinesulphonat) (ABTS) ... 39
4.3 Kurva hubungan perubahan absorbansi radikal kation dengan waktu kapang A ... 40
4.4 Kurva hubungan perubahan absorbansi radikal kation dengan waktu kapang B ... 40
4.5 Kurva hubungan perubahan absorbansi radikal kation dengan waktu kapang C ... 41
4.6 Kurva hubungan perubahan absorbansi radikal kation dengan waktu kapang D ... 41
4.7 Kurva kejenuhan amonium sulfat terhadap aktivitas enzim lakase dari kapang A ... 44
ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
x
4.8 Kurva kejenuhan amonium sulfat terhadap aktivitas enzim lakase
dari kapang B ... 44
4.9 Kurva kejenuhan amonium sulfat terhadap aktivitas enzim lakase dari kapang C ... 45
4.10 Kurva kejenuhan amonium sulfat terhadap aktivitas enzim lakase dari kapang D ... 45
4.11 Penampang atas jerami padi perbesaran 500x ... 50
4.12 Penampang atas jerami padi perbesaran 1000x ... 51
4.13 Penampang melintang jerami padi perbesaran 2000x ... 52
4.14 Penampang atas tongkol jagung perbesaran 1000x ... 52
4.15 Penampang atas tongkol jagung perbesaran 2000x ... 53
4.16 Penampang melintang tongkol jagung perbesaran 2000x ... 54 ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
xi
DAFTAR LAMPIRAN
Nomor Judul Lampiran
1 Gambar hasil penelitian
2 Penentuan aktivitas enzim lakase dengan substrat ABTS 3 Pembuatan kurva standar BSA
4 Penentuan kadar protein enzim
5 Data optimasi kejenuhan pengendapan ammonium sulfat 6 Perhitungan tabel kemurnian
7 Gambar sampel SEM
ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
1 BAB I PENDAHULUAN
1.1Latar Belakang Masalah
Lakase merupakan enzim ekstraseluler yang menggunakan senyawa
oksigen untuk menjalankan reaksi oksidasi berbagai senyawa aromatik dan
non-aromatik (Thurston, C.F, 1994). Enzim lakase merupakan enzim yang dapat
mendegradasi lignin pada tumbuhan berserat. Enzim pendegradasi lignin sering
dihasilkan oleh jamur pelapuk putih (white rot fungi). Kemampuan jamur pelapuk
putih dalam mendegradasi lignin disebabkan oleh aktivitas ekstraselular
ligninolitik. Dalam bidang industri, enzim lakase sangat diperlukan peranannya,
seperti pada industri pemutihan pulp dan industri bioetanol. Industri bioetanol ini
memanfaatkan selulosa dan hemiselulosa dalam produksi etanol. Pemanfaatan ini
sering terhambat karena adanya kompleks lignin yang berasosiasi dengan selulosa
dan hemiselulosa, sehingga diperlukan proses delignifikasi agar selulosa dan
hemiselulosa terlepas dari komplek lignin, dan depolimerisasi untuk mendapatkan
gula bebas dan fermentasi gula heksosa dan pentosa untuk mendapatkan produksi
bioetanol (Trisanti, 2009).
Kelapa sawit (Elaeis quineensis Jaco) dari famili Arecaceae merupakan
salah satu sumber minyak nabati, dan merupakan primadona bagi komoditi
perkebunan. Pengembangan perkebunan kelapa sawit di Indonesia berjalan sangat
pesat. Pada tahun 1968, luas areal baru 120.000 ha dan menjadi 5,16 juta ha pada
tahun 2005 dan pada tahun 2006 diproyeksikan mencapai 6,046 juta ha. ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
2
Pengelolaan produksi kelapa sawit yang sebelumnya hanya perkebunan
besar, saat ini telah mencakup perkebunan rakyat (PR) dan perkebunan besar
swasta (PBS). Pada tahun 2005, luas areal PR sekitar 2,202 juta ha (40,44%),
PBN 630.000 ha (11,58%) dan PBS 2,61 juta ha (47,98%). Sumatera
mendominasi ketiga jenis perkebunan, sedangkan Kalimantan dan Sulawesi
menjadi lokasi pengembangan perkebunan swasta dan perkebunan rakyat (Warta
Penelitian, 2007) . Di propinsi Bengkulu, sampai dengan tahun 2005 memiliki
luas tanaman perkebunan rakyat kelapa sawit sebesar 90,898 ha, dengan rincian
yaitu tanaman muda 40,475 ha, tanaman produktif 50,192 ha dan tanaman tua atau
rusak 231 ha (Anonim, 2006). Saat ini, peningkatan perkebunan besar maupun
rakyat semakin bertambah luas. Menurut Dinas Perkebunan Propinsi Bengkulu
(2007) di Propinsi Bengkulu terdapat 11 pabrik pengolahan kelapa sawit dengan
kapasitas produksi 30 – 60 ton/jam sehingga berpotensi menghasilkan limbah
yang dapat dipergunakan sebagai bahan baku pembuatan pulp dan kertas dari
tandan kosong .
Tandan kosong kelapa sawit merupakan limbah yang cukup melimpah
keberadaannya. Komponen utama limbah pada kelapa sawit adalah selulosa,
hemiselulosa dan lignin, sehingga limbah ini disebut sebagai limbah lignoselulosa
(Darnoko, 1993). Beberapa kapang yang tumbuh pada tanaman berkayu
dilaporkan mampu mendegradasi lignin dalam kayu. Kapang – kapang tersebut
terbukti memiliki aktivitas enzim lakase (Arora, D.S et al., 2000).
Indonesia menghasilkan limbah lignoselulosa dari pertanian (tongkol
jagung, kulit pisang dan jerami padi) yang sangat melimpah yaitu sekitar 200 juta
ton per tahun (Berita Resmi Statistik, 2006). Komponen utama lignoselulosa yang ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
3
terdiri atas selulosa, hemiselulosa dan lignin. Dengan tingginya kadar lignin yang
terkandung dalam limbah tersebut, diharapkan keberadaan enzim lakase mampu
mendegradasi kompleks lignin yang terkandung dalam limbah tersebut. Substrat
limbah pertanian yang akan digunakan pada penelitian ini adalah tongkol jagung
dan jerami padi.
Penggunaan enzim untuk proses pengolahan limbah lignoselulosa masih
belum banyak dilakukan. Kebanyakan industri – industri lebih memilih untuk
melakukan pengolahan limbah dengan menggunakan zat kimia yang harganya
jauh lebih murah, namun hasilnya kebanyakan masih kurang memenuhi standar.
Hal ini akan lebih efektif apabila enzim lakase diproduksi untuk mendegradasi
lignin, yang kemudian dapat dimanfaatkan untuk keperluan penting lainnya.
Tingginya harga substrat mempengaruhi produksi enzim lakase. Enzim lakase
dapat diproduksi melalui limbah – limbah yang memiliki serat, limbah – limbah
berkayu, dan juga limbah lignoselulosa lainnya. Substrat dari enzim lakase ini
dapat menggunakan salah satu limbah lignoselulosa yang ada di Indonesia.
Pemanfaatan produk pertanian yang tidak berguna diharapkan dapat menekan
biaya produksi enzim lakase. Diharapkan limbah pertanian di Indonesia dapat
dioptimalkan pemanfaatannya.
Kapang merupakan organisme multiseluler yang dapat hidup melekat pada
substrat yang sesuai. Substrat yang baik, mampu mengembangbiakkan kapang
dalam jumlah yang besar. Jamur basidiomisetes merupakan kelompok utama
pendegradasi lignoselulosa. Walaupun beberapa bakteri diketahui dapat
mendegradasi lignin, tetapi bakteri yang mampu mendegradasi lignin secara
kompleks belum pernah dilaporkan. Jamur pelapuk kayu menghasilkan enzim - ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
4
enzim pendegradasi lignoselulosa seperti golongan selulase, ligninase, dan
hemiselulase. Jamur pelapuk kayu digolongkan ke dalam jamur pelapuk putih dan
jamur pelapuk cokelat, yang masing - masing memiliki metabolisme degradatif
yang berbeda. Jamur pelapuk putih mampu mendegradasi seluruh komponen
material lignoselulosa termasuk lignin, sedang jamur pelapuk cokelat lebih
cenderung mendegradasi bagian selulosa dan hemiselulosa tetapi tidak lignin
(Munir, 2006). Penelitian ini menggunakan tandan kosong kelapa sawit untuk
mengisolasi kapang penghasil enzim lakase berdasarkan penelitian sebelumnya
yang dilakukan oleh Dewi (2010), yang berhasil mengisolasi empat kapang
Aspergillus sp. yang dapat menghasilkan enzim lakase.
Pada penelitian yang dilakukan oleh Dewi (2010) telah berhasil
mengisolasi empat kapang yang belum diketahui spesiesnya pada tandan kosong
kelapa sawit yang dapat menghasilkan enzim lakase. Keempat isolat kapang
tersebut telah dikarakteristik dan uji aktivitasnya. Dapat disimpulkan bahwa
keempat isolat kapang tandan kosong kelapa sawit tersebut memiliki aktivitas
enzim lakase yang hampir sama. Penelitian lanjutan akan dilakukan dengan
tahapan pemekatan dan pemurnian parsial enzim lakase dengan menggunakan
amonium sulfat. Pada proses ini enzim akan beragregat dan mengendap, sehingga
kompleks enzim yang murni akan mengendap bersama garam amonium sulfat,
proses ini dinamakan ‘salting out’. Tahapan selanjutnya adalah melakukan proses
dialisis untuk menghilangkan garam amonium sulfat. Tingkat kemurnian suatu
enzim diketahui dari aktivitas spesifik enzim tersebut, semakin tinggi aktivitas
spesifik suatu enzim maka enzim akan semakin murni. Selain itu juga dapat
diketahui berdasarkan kelipatan pemurnian enzim yang diperoleh. Hal ini dapat ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
5
diketahui dengan cara membagi aktivitas spesifik enzim hasil pemurnian dengan
aktivitas spesifik awal ekstrak kasar enzim (Minch, 1989).
Pada penelitian yang dilakukan sebelumnya oleh Aminah (2011) tentang
isolasi dan karakterisasi enzim selulase dari kapang Aspergillus sp.(1), disebutkan
bahwa salah satu isolat kapang penghasil enzim selulase memiliki aktivitas
terhadap substrat alam (tongkol jagung dan jerami padi). Namun, aktivitasnya
masih rendah, sehingga dalam penelitian akan digunakan enzim lakase untuk
mendegradasi lignin pada substrat tongkol jagung dan jerami padi yang
merupakan limbah pertanian terbanyak di Indonesia. Diharapkan enzim lakase
dari isolat kapang tandan kosong kelapa sawit mampu mengurangi kandungan
lignin dalam substrat alam, dan memudahkan proses hidrolisis substrat alam oleh
selulase.
1.2 Rumusan Masalah
Berdasarkan latar belakang masalah yang telah diuraikan di atas, dapat
dirumuskan suatu masalah penelitian sebagai berikut:
1. Berapakah aktivitas ekstrak kasar enzim lakase dari keempat isolat tandan
kosong kelapa sawit terhadap ABTS?
2. Berapakah tingkat kemurnian enzim lakase dari keempat spesies isolat kapang
tandan kosong kelapa sawit hasil presipitasi garam amonium sulfat apabila
dibandingkan dengan ekstrak kasarnya?
3. Bagaimanakah profil permukaan dari substrat alam yang telah diberi
perlakuan enzim lakase dengan aktivitas tertinggi menggunakan analisis
SEM?
ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
6
1.3Tujuan Penelitian
1. Menentukan aktivitas ekstrak kasar enzim lakase dari keempat isolat kapang
tandan kosong kelapa sawit penelitian Dewi (2010) terhadap substrat ABTS.
2. Menentukan tingkat kemurnian enzim lakase dari keempat spesies isolat
kapang tandan kosong kelapa sawit hasil presipitasi garam amonium sulfat
apabila dibandingkan dengan ekstrak kasarnya.
3. Mengetahui profil permukaan dari substrat alam (tongkol jagung dan jerami
padi) yang telah diberi perlakuan enzim lakase dengan aktivitas tertinggi
menggunakan analisis SEM.
1.4Manfaat Penelitian
Penelitian ini bermanfaat dalam industri pengolahan limbah tongkol
jagung dan jerami padi serta limbah lignoselulosa yang lain agar dapat digunakan
kembali sebagai bahan baku atau produk lain.
ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
7 BAB II
TINJAUAN PUSTAKA
2.1 Kapang (Fungi)
Kapang merupakan cendawan eukariotik, bersifat multiseluler, dapat
bereproduksi secara aseksual dan seksual, berbentuk filamen (seperti benang),
merupakan mikroorganisme aerob dan bersifat heterotrof. Kapang dapat
berkembang biak secara aseksual dan seksual. Berkembang biak secara aseksual
dengan cara pembelahan sel, penguncupan, atau pembentukan spora. Sedangkan
berkembangbiak secara seksual dapat dengan cara peleburan nucleus dari dua sel
induknya. Kapang dapat bertahan dengan keadaan alam yang tidak
menguntungkan dengan cara membentuk spora yang berdinding tebal (Pelczardan
Chan, 2005). Kapang tidak dapat melakukan fotosintesis sehingga untuk
memenuhi kebutuhan energinya, kapang memproduksi enzim ekstraseluler
(Wainwright, 1992). Beberapa kapang yang dapat hidup pada bahan yang
mengandung lignoselulosa yang tinggi akan mengeluarkan enzim yang dapat
mendegradasi bahan tersebut sebagai nutrisinya (Herliyana et al., 2008).
2.1.1 White Rot Fungi
Fungi pelapuk putih merupakan kelompok fungi yang memiliki
kemampuan pendegradasi lignin paling tinggi. Degradasi lignin dalam kayu
menyebabkan terbentuknya kantung – kantung yang berwarna putih, sehingga
fungi ini disebut sebagai fungi pelapuk putih. Fungi ini melakukan dekomposisi
lignin sehingga dapat mencapai selulosa dan hemiselulosa (Pérez, 2002). ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
8
Gambar 2.1 Fungi pelapuk putih
2.2 Enzim
Enzim merupakan suatu biokatalis dalam sistem biologi yang bekerja
secara spesifik. Bekerja dengan urut – urutan yang teratur, enzim mengkatalisis
ratusan reaksi bertahap yang menguraikan molekul nutrien, reaksi yang meyimpan
dan mengubah energi kimiawi, dan yang membuat makromolekul sel dari
prekursor sederhana (Lehninger, 2007). Fungsi dari enzim adalah meningkatkan
kecepatan reaksi dengan cara menyediakan suatu jalur reaksi yang baru melalui
transisinya. Enzim bekerja untuk menurunkan energi aktivasi, sehingga reaksi
lebih mudah dicapai daripada reaksi tanpa katalis. Enzim dapat mempercepat
reaksi 103 sampai 106 kali lebih cepat dibandingkan tanpa menggunakan katalis.
Reaksi enzimatis hanya bekerja pada pH dan suhu tertentu serta dapat
menunjukkan kekhususan stereoisomerik. Keunggulan enzim sebagai
biokatalisator antara lain daya katalitiknya yang tinggi, spesifitas tinggi, dapat
bekerja pada kondisi suhu da pH yang tidak ekstrim, aktivitas katalitik beberapa ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
9
enzim dapat dikendalikan dan diproduksi, sehingga memudahkan penyediaannya
(Stryer, 2002).
Reaksi katalitik oleh enzim pada umumnya bersifat cepat membentuk
reaksi kesetimbangan tanpa disertai reaksi samping, bekerja dalam larutan encer,
berlangsung pada suhu rendah dan kondisi netral (Ottaway et al., 1984).
Berdasarkan biosintesisnya, ada dua macam enzim yaitu enzim konstitutif
dan enzim induktif. Enzim konstitutif adalah enzim yang selalu tersedia di dalam
sel mikroba dalam jumlah yang relatif konstan. Sedangkan enzim induktif adalah
enzim yang berada di dalam sel dengan jumlah yang tidak tetap, tergantung pada
keberadaan induser. Jumlah enzim dapat bertambah sampai ribuan kali bahkan
lebih apabila di dalam medium terdapat substrat yang berperan sebagai induser,
terutama apabila substrat penginduksi merupakan satu – satunya sumber karbon
(Stryer, 2002).
2.2.1 Struktur enzim
Struktur enzim terdiri dari struktur primer, sekunder, tersier, dan kuartener.
Struktur primer terdiri dari urutan asam amino dari protein. Urutan, macam, dan
jumlah asam amino yang membentuk rantai polipeptida adalah struktur primer
protein. Struktur sekunder adalah tingkat struktur organisasi pada protein yang
menjelaskan pelipatan rantai polipeptida menjadi motif struktural alfa-helix dan
beta sheet yang disebabkan adanya ikatan hidrogen pada tulang punggung
polipeptida (Kendrew, 1994).
Struktur tersier protein merupakan bentuk yang paling stabil, karena
ditunjang oleh berbagai jenis ikatan yang menstabilkan struktur tersier protein.
Jenis ikatan tersebut antara lain : ikatan hidrogen yang terdapat di antara gugus R ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
10
residu asam amino rantai samping yang berdekatan, ikatan ion di antara gugus R
yang berlawanan, interaksi hidrofobik dari gugus R asam amino hidrofobik dan
ikatan kovalen berupa ikatan disulfida dari residu sistein (Ottoway et al., 1984).
Struktur tersier disebabkan oleh interaksi rantai samping polipeptida, membentuk
konformasi tiga dimensi protein secara keseluruhan (Kendrew, 1994).
Struktur kuartener terbentuk karena adanya interaksi beberapa rantai
polipeptida membentuk oligomer. Oligomer berinteraksi kembali melalui ikatan
ionik, ikatan van der waals, dan ikatan hidrofobik (Bodanzky, 1998).
2.2.2 Klasifikasi Enzim
Berdasarkan Nelson dan Michael, 2003, enzim diklasifikasikan menjadi
enam kelas berdasarkan tipe reaksi yang dikatalisnya yaitu sebagai berikut.
1. Oksidoreduktase merupakan golongan enzim yang dapat mengkatalis
pemisahan dan penambahkan elektron atau hidrogen.
2. Transferase merupakan golongan enzim yang mengkatalis pemindahan
gugus senyawa kimia.
3. Hidrolase merupakan golongan enzim yang dapat memutus ikatan kimia
dengan penambahan air.
4. Liase merupakan golongan enzim yang membentuk ikatan rangkap dengan
melepas satu gugus kimia. Golongan enzim ini memutuskan berbagai
ikatan kimia selain melalui hidrolisis dan oksidasi.
5. Isomerase merupakan golongan enzim yang mengkatalis perubahan pada
isomer.
6. Ligase merupakan golongan enzim yang menggabungkan dua molekul
yang disertai dengan hidrolisis ATP.
ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
11
2.2.3 Kekhususan Enzim
Substrat harus memiliki hubungan tertentu terhadap bentuk dan sifat kimia
sisi aktif enzim agar bisa terjadi suatu ikatan. Enzim bersifat spesifik terhadap
suatu reaksi. Menurut Price dan Lewis (2006), kekhususan enzim terhadap reaksi
dapat bersifat :
1. Kekhususan sterik merupakan kekhususan absolut, dimana golongan enzim
bekerja berdasarkan stereokimia struktur molekul dari substratnya. Dari dua
senyawa yang enansiomer, enzim hanya bereaksi dengan salah satunya.
2. Kekhususan reaksi dimana terdapat dua golongan enzim yang bekerja
berdasarkan substrat-substrat yang memiliki gugus fungsional sejenis yang
bekerja berdasarkan jenis reaksinya yaitu :
1)Kekhususan relatif, apabila suatu enzim bekerja terhadap substrat yang
memiliki gugus fungsional sejenis.
2)Kekhususan absolut, apabila suatu enzim bekerja terhadap satu substrat
saja.
2.2.4 Mekanisme kerja enzim
Mekanisme katalisis enzim merupakan reaksi yang melibatkan gugus
fungsi residu asam amino yang terdapat pada sisi aktif enzim. Sebagai katalis
biologi, enzim mempercepat reaksi dengan cara menciptakan suatu keadaan
transisi terstabilisasi melalui pembentukan kompleks enzim-substrat yang
mempunyai energi aktivasi lebih rendah. Energi aktivasi merupakan energi
tertinggi yang harus dicapai agar suatu reaksi dapat terjadi. Dengan lebih
rendahnya energi aktivasi maka berarti lebih banyak molekul yang dapat
mencapainya sehingga reaksi berjalan lebih cepat. ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
12
Sebelum melakukan fungsi katalitiknya, enzim terlebih dahulu membentuk
ikatan dengan substrat, digambarkan dengan persamaan sebagai berikut :
Gambar 2.2 Reaksi enzimatis
Langkah pertama dalam proses katalisis adalah pembentukan kompleks enzim
substrat. Substrat diikat pada daerah yang dinamakan sisi aktif enzim. Reaksi
kimia yang terjadi dalam kompleks enzim substrat tersebut dapat dilanjutkan
dengan pelepasan produk dan enzim.
Mekanisme katalisis enzim merupakan reaksi-reaksi yang melibatkan
gugus-gugus fungsi dari residu asam amino yang terdapat pada sisi aktif enzim.
Sisi aktif enzim adalah tempat pengikatan substrat yang mengandung residu asam
amino sebagai gugus katalitiknya. Dan secara langsung terlibat dalam pembuatan
serta pemutusan ikatan selama proses katalisis. Ciri – ciri umum sisi aktif enzim
yaitu lokasi sisi aktif enzim merupakan bagian kecil dari keseluruhan molekul
enzim, hanya residu yang ada pada sisi aktif enzim yang terlibat pada proses
katalisis dan melakukan kontak dengan substratnya; Sisi aktif enzim memiliki
struktur tiga dimensi yang dibentuk oleh gugus – gugus asam amino yang
berbeda; Pengikatan substrat dengan enzim dipengaruhi oleh adanya gaya tarik –
menarik yang lemah. Interaksi reversible biomolekul dapat berlangsung karena
adanya ikatan elektrostatik, ikatan hidrogen, gaya van der waals, dan interaksi
hidrofobik; Sisi aktif enzim berbentuk kantung atau celah. Hal ini mempengaruhi
perlindungan terhadap sisi aktif tersebut; Proses pengikatan substrat pada enzim ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
13
membentuk kompleks enzim-substrat merupakan tahap awal berlangsungnya
katalis enzimatik (Puspaningsih, 2004).
Ikatan yang terjadi antara enzim dan substrat merupakan ikatan yang
lemah, seperti ikatan elektrostatik, ikatan hidrogen, gaya – gaya van der waals,
ataupun interaksi hidrofobik. Interaksi yang terjadi antara molekul enzim dan
substrat melibatkan gugusan reaktif atau gugus pengikat ( binding group ) dari
enzim maupun substrat, dan enzim hanya dapat mengikat substrat yang memiliki
gugusan – gugusan reaktif yang sama. Proses katalitik melibatkan sejumlah
gugusan – gugusan reaktif lain yang disebut gugusan katalitik ( catalytic group ).
Enzim hanya dapat mengikat substrat yang memiliki gugus reaktif yang sama
(Stryer et al., 2002). Model interaksi enzim substrat dibedakan menjadi :
1. Model Lock and Key (lubang dan anak kunci) : dikemukakan oleh Emil
Fischer pada tahun 1890. Dalam model Fischer, tempat katalitik dianggap
terbentuk terlebih dahulu agar sesuai dengan substratnya (Stryer et al., 2002).
Pada model ini, spesifitas pengikatan tergantung pada ketepatan pengaturan
atom-atom pada sisi aktif. Substrat dapat terikat pada enzim bila mempunyai
ukuran atau bentuk yang sesuai dengan sisi aktif enzim (Gambar 2.5). Dapat
disimpulkan bahwa satu enzim hanya dapat berikatan pada satu model substrat
yang memiliki sisi aktif yang sesuai dengan enzim. Meskipun dalam model ini
termasuk dalam model cetakan yang kaku, namun dapat dipakai untuk
memahami sifat – sifat tertentu dari enzim. ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
14
Gambar 2.3 Interaksi substrat dan enzim model Lock and Key (Stryer et al., 2002)
2. Model Induced Fit : dikemukakan oleh Daniel G. Koshland pada tahun 1958.
Koshland mengemukakan bahwa ukuran atau bentuk sisi aktif enzim dapat
mengalami modifikasi oleh adanya pengikatan substrat (Gambar 2.6). Pada
model ini, sisi aktif enzim diasumsikan cocok dengan substratnya sesaat
setelah enzim mengikat substrat. Jadi substrat dianggap mampu menginduksi
perubahan bentuk dalam sisi aktif enzim. Perubahan ini menempatkan residu
asam amino pada sisi aktif enzim yang memungkinkan terjadinya pengikatan
substrat selama proses katalisis. Enzim menunjukkan fleksibilitasnya dalam
berikatan dengan substrat (Stryer et al., 2002).
Gambar 2.4 Interaksi substrat dan enzim model induced fit (Stryer et al., 2002)
2.2.5 Aktivitas enzim
Faktor-faktor yang mempengaruhi aktivitas enzim adalah : konsentrasi
enzim, konsentrasi substrat, temperatur dan pH. ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
15
2.2.5.1 Konsentrasi enzim
Kecepatan reaksi suatu enzim dipengaruhi oleh konsentrasi enzim.
Banyaknya substrat yang diubah menjadi produk sebanding dengan tinggi
konsentrasi enzim yang digunakan (Gambar 2.5). Semakin tinggi konsentrasi
enzim maka laju reaksi berjalan lebih cepat selama konsentrasi enzim jauh lebih
sedikit dibanding substrat (Stryer et al., 2002).
Gambar 2.5 Pengaruh konsentrasi enzim terhadap laju reaksi
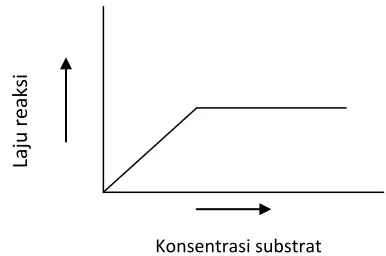
2.2.5.2 Konsentrasi substrat
Apabila konsentrasi substrat semakin tinggi maka laju reaksi akan semakin
cepat. Namun bila konsentrasi diperbesar lagi maka tidak terjadi penambahan laju
reaksi. (Gambar 2.6). Hal tersebut disebabkan karena enzim telah jenuh dengan
substrat. Pada konsentrasi substrat yang menghasilkan laju reaksi maksimal,
penambahan konsentrasi substrat lebih lanjut tidak akan merubah laju reaksi
(Stryer et al., 2002).
Gambar 2.6 Pengaruh konsentrasi substrat terhadap laju reaksi
Laj
u reaksi
Konsentrasi substrat
Laju
reaks
i
Konsentrasi enzim ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
16
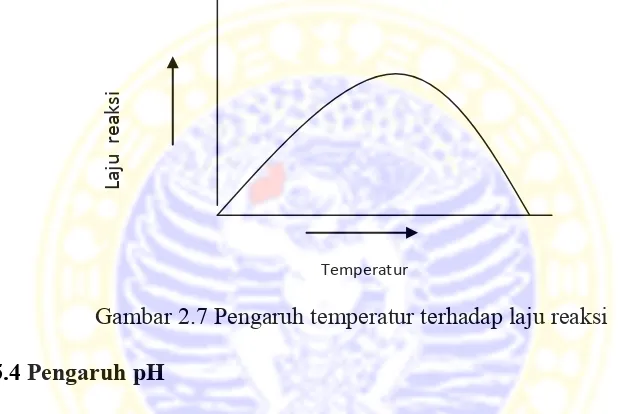
2.2.5.3 Pengaruh temperatur
Semakin tinggi temperatur maka laju reaksi berjalan makin cepat. Hal
tersebut disebabkan karena atom – atom yang terdapat dalam molekul enzim
memiliki energi yang tinggi, sehingga energi pengaktifan akan tercapai. Akan
tetapi apabila temperatur dinaikkan lebih tinggi maka laju reaksi akan menurun,
dapat dilihat gambar 2.7. Hal tersebut dikarenakan enzim mengalami denaturasi
sehingga enzim kehilangan aktivitasnya (Stryer et al., 2002).
Gambar 2.7 Pengaruh temperatur terhadap laju reaksi
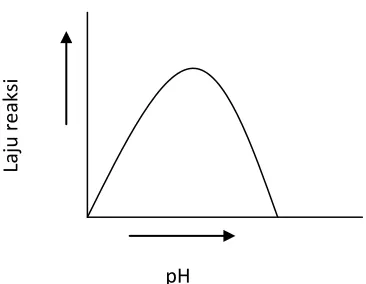
2.2.5.4 Pengaruh pH
Enzim memiliki muatan positif atau negatif pada suatu pH tertentu. Hal ini
dikarenakan enzim dapat bersifat basa, netral, atau asam tergantung rantai
samping susunan proteinnya. Pada pH tertentu enzim dapat beraktivitas
maksimum (pH optimum). pH optimum tergantung pada masing-masing enzim
karena setiap enzim memiliki pH optimum yang spesifik yang bergantung pada
konsentrasi substrat. Apabila pH semakin jauh dari titik pH optimum maka laju
reaksi dari enzim akan rendah. Pada gambar ditunjukkan kurva pH optimum
(Gambar 2.8) (Stryer et al., 2002).
Temperatur
Laj
u
reaksi
ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
17
Gambar 2.8 Pengaruh pH terhadap laju reaksi
2.3 Enzim Lakase
Lakase adalah sekelompok enzim yang dihasilkan oleh jamur pelapuk
putih (white rot fungi) secara ekstraseluler (Schmidt, 2006). Nama lakase berasal
dari fakta bahwa ekstrak pertama yang mampu untuk mengoksidasi fenol dengan
oksigen atmosfir, diisolasi dari Rhus vernicifera, suatu pohon yang berasal dari
Jepang yang menghasilkan lak (Paolo, 1992). Salah satu substrat dari enzim
lakase adalah ABTS (asam 2,2’-azinobis-2-ethyl-benzthiazolin-6-sulfonat) dapat
berperan sebagai mediator yang memungkinkan oksidasi komponen non fenolik
yang tidak dapat dioksidasi oleh lakase sendiri (Wells A, et al., 2006). Enzim
lakase mampu mendegradasi lignin pada tumbuhan. Enzim pendegradasi lignin
(lignolitik) terdiri dari lakase (polifenol oksidase), lignin peroksidase (Li-P) dan
mangan peroksidase (Mn-P). Ketiganya merupakan multi enzim ekstraseluler
yang berperan dalam proses depolimerisasi lignin (Anindyawati, 2009).
Gambar 2.9 Representasi pita sinar-X dari struktur kristal lakase III dari Trametes versicolor (PDB code 1KYA) (Oxford, 2007).
pH
Laj
u reaksi
ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
18
2.4 Lignin
Lignin merupakan bahan penguat yang terdapat bersama – sama selulosa
di dinding sel tumbuhan (Robinson, 1995). Lignin membentuk matriks yang
mengelilingi selulosa dan hemiselulosa, penyedia kekuatan pohon dan pelindung
dari biodegradasi (Fadillah, dkk, 2008).
Gambar 2.10 Lignin, selulase, dan hemiselulase pada jaringan tumbuhan
Lignin tergolong dalam bagian utama dari dinding sel tanaman yang
merupakan polimer terbanyak setelah selulosa. Secara kimia, lignin sebenarnya
merupakan polimer yang mengandung satuan sejenis koniferil alkohol. Karena
struktur kimianya kompleks, lignin sangat sulit didegradasi dan hanya beberapa
jenis mikrobia tertentu saja yang mampu mendegradasi senyawa ini (Erni, et al,
2003).
Ketiga prekursor penyusun lignin adalah conyferyl alcohol, p-coumaryl
alcohol, dan synapyl alcohol (Pearl,1967) :
Gambar 2.11 Prekursor penyusun lignin 1) p-coumaryl alcohol, 2) conyferyl alcohol, 3) synapyl alcohol
ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
19
Gambar 2.12 Struktur 3D lignin
Gambar 2.13 Struktur lignin
2.5 Substrat Alam
Keberadaan lignin dalam limbah lignoselulosa seringkali menjadi
penghambat pemanfaatan limbah lignoselulosa, terutama limbah pertanian.
Tongkol jagung dan jerami padi merupakan limbah pertanian yang sangat ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
20
melimpah keberadaannya. Limbah – limbah tersebut memiliki komposisi antara
lain:
1) Komposisi serat tongkol jagung adalah 23,74% lignin, 65,96% selulosa,
dan 10,82% hemiselulosa (Meryandini et al., 2009).
2) Menurut Davendra (1982) dalam Meryandini et al., (2009), jerami padi
terdiri atas 33% selulosa, 26% hemiselulosa, 7% lignin serta 13% silika.
2.6 Pemurnian Enzim
Pemurnian enzim dilakukan untuk mendapatkan suatu enzim yang bebas
dari pengotor. Tujuan dari pemurnian enzim ini adalah untuk memisahkan dan
memurnikan enzim secara parsial enzim lakase dari protein – protein lain yang
terdapat dalam ekstrak kasar enzim. Tahap – tahap pemurnian enzim tergantung
dari tujuan akhir, apakah untuk tujuan komersial atau tujuan riset (Harris et al.,
1989). Enzim yang dimurnikan secara parsial masih dapat digunakan untuk tujuan
komersial, sedang enzim murni atau hampir murni dikehendaki untuk tujuan riset
atau dalam produk analitik.
Langkah awal dalam pemurnian enzim adalah preparasi ekstrak kasar yang
mengandung protein menjadi bentuk yang dapat dilarutkan. Teknik isolasi protein
tersebut tergantung dari lokasi protein yang akan diisolasi, yaitu protein
intraseluler atau protein ekstraseluler. Tahapan isolasi protein intraseluler diawali
dengan mencuci jaringan atau sel dengan buffer salin yang bertujuan untuk
menghilangkan pengotor atau bahan ekstraseluler. Selanjutnya dilakukan lisis sel
untuk memecah atau membuka sel menggunakan mortar atau pestle, homogenizer,
sonicator, tissue grinder, cell disruptor, blender hingga menghasilkan homogenat.
Kemudian, sentrifugasi homogenat tersebut sampai membentuk supernatan dan ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
21
pelet sel. Supernatan merupakan ekstrak kasar yang mengandung protein yang
diinginkan, sedangkan pelet sel mengandung protein membran. Jika protein yang
diinginkan berasosiasi dengan membran, maka isolasi protein dilakukan dengan
mengisolasi organel dan ditangani dengan deterjen atau didisrupsi (Harris et al.,
1989). Untuk tahapan isolasi protein ekstraseluler dilakukan dengan cara
sentrifugasi cairan sel atau medium kultur menghasilkan supernatan dan pelet sel.
Supernatan merupakan ekstrak kasar, sedangkan pelet sel mengandung sel dan
komponen non protein. Pemurnian enzim dilakukan berdasarkan sifat kelarutan,
ukuran, dan muatan afinitas pengikatan spesifik dari enzim itu sendiri. Tabel
kemurnian enzim terdapat pada gambar 2.14.
Gambar 2.14 Tabel kemurnian protein (Scopes, 1994)
2.6.1 Pemekatan enzim
Menurut Harris et al., 1989, pemekatan enzim merupakan tahap awal dari
prosedur pemurnian enzim sebelum tahap pemurnian berikutnya atau dapat pula
digunakan untuk keperluan analisis enzim. Ada dua tahap pemekatan enzim, yaitu
dengan menggunakan metode analitik dan metode preparatif. Untuk metode
preparatif dilakukan dengan metode fraksinasi garam, fraksinasi pelarut organik, ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
22
fraksinasi dengan menggunakan polimer organik, ultrafiltrasi, liofilisasi, dan
dialisis (Bollag dan Edelstein, 1991). Metode fraksinasi enzim yang biasa
dilakukan yaitu fraksinasi garam ammonium sulfat dan pelarut organik aseton.
Untuk metode analitik, menggunakan fraksinasi asam (asam trikloroasetat),
fraksinasi organik (aseton atau etanol), dan imunopresipitasi yang dapat
menyebabkan denaturasi protein. Dalam metode ini aktivitas enzim tidak menjadi
prioritas.
Prinsip dari fraksinasi garam berdasarkan pada kelarutan protein yang
berinteraksi polar dengan molekul air, interaksi ionik protein dengan garam, dan
daya tolak menolak protein yang bermuatan sama. Kelarutan protein pada pH dan
suhu tertentu berpengaruh pada meningkatnya kenaikan konsentrasi garam
(salting in). Kenaikan kelarutan protein menyebabkan meningkatnya kekuatan ion
larutan. Pada penambahan garam pada konsentrasi tertentu menyebabkan
kelarutan protein akan menurun (salting out). Molekul air yang berikatan dengan
garam – garam semakin banyak menyebabkan penarikan selubung air yang
mengelilingi permukaan protein. Peristiwa yang seperti ini akan mengakibatkan
protein akan saling berinteraksi, beragregasi, dan mengendap (Harris et al., 1989),
(Scopes, 1994). Ammonium sulfat merupakan garam yang paling sering
digunakan untuk mengendapkan protein karena memiliki kelarutan yang tinggi
dalam air, relatif tidak mahal, dan dapat mempertahankan kestabilan protein di
dalam larutan amonium sulfat (2M-3M) selama bertahun – tahun (Scopes, 1994).
Tahap pemekatan enzim selanjutnya adalah dialisis. Garam berlebih yang
terdapat dalam larutan enzim yang telah difraksinasi dengan ammonium sulfat
dapat dihilangkan dengan cara dialisis, diafiltrasi, dan filtrasi gel. Dalam tahap ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
23
dialisis, protein ditempatkan dalam sebuah tabung selofan (membran
semipermeabel) yang ujung – ujungnya diikat. Kemudian tabung tersebut
direndam dengan larutan buffer tertentu. Molekul yang berukuran kecil akan
keluar dari membran, sedang molekul yang memiliki ukuran lebih besar akan
tertahan di dalam tabung selofan. Larutan buffer yang digunakan untuk merendam
tabung selofan diganti setiap kali larutan buffer akan jenuh, agar proses dialisis
berjalan dengan baik.
Gambar 2.15 Proses dialisis ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
24 BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Biokimia, Fakultas Sains dan
Teknologi Universitas Airlangga dan Laboratorium Sentral, Fakultas Matematika
dan Ilmu Pengetahuan Alam Universitas Negeri Malang. Penelitian dimulai dari
bulan Februari 2012 sampai dengan Juli 2012.
3.2 Sampel, Bahan, dan Alat Penelitian
3.2.1 Sampel penelitian
Sampel yang digunakan adalah keempat isolat kapang dari tandan kosong
kelapa sawit yang menjadi koleksi Laboratorium Biokimia, Departemen Kimia,
Fakultas Sains dan Teknologi Universitas Airlangga.
3.2.2 Bahan penelitian
Bahan yang digunakan dalam penelitian ini adalah kentang, agar – agar,
dextrose, pewarna non-phenol ABTS (Asam
2,2’azinobisdi-3-ethylbenzthiazolinesulphonat), Asam Asetat Glacial, Yeast Extract, Malt Extract,
Asam Sitrat, Natrium Fosfat Dibasis, Kalium Hidroksida, Kalsium Fosfat,
Natrium Asetat, Ammonium sulfat, Etanol 96%, Larutan Asam Fosfat 85%, dan
akuades.
ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
25
3.2.3 Alat penelitian
Alat – alat yang digunakan dalam penelitian ini adalah labu Erlenmeyer
100 dan 250 mL, pipet mikro, autoklaf (Ogawa Seiki, CO, LTD. Osk 6508),
sentrifuge dingin (Beckman model TJ-R), shaker incubator (Heidolph Unimax
1010, Inkubator 1000), waterbath (Sanyo Rikogakukikai), oven (Isotemp* oven
model 655F), freezer, lemari es (Sharp matric), spektrofotometer UV-VIS
(Shimadzu UV-1700), timbangan analitik (OHAUS), laminar air flow cabinet
(Kottermann), pH meter (Metrohm 744), tabung Eppendorf, tabung selofan, SEM
(Scanning Electron Microscopy) (FEL tipe Inspect-S50) milik laboratorium
bersama Fakultas MIPA Universitas Negeri Malang, dan alat – alat gelas yang
biasa digunakan di laboratorium.
ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
26
3.3 Prosedur Kerja
3.3.1 Diagram alir penelitian
Peremajaan Keempat Spesies Kapang TKKS (Tandan Kosong Kelapa Sawit)
Produksi Enzim Lakase dari Keempat Spesies Isolat Kapang TKKS
Uji Aktivitas Spesifik Keempat Enzim Lakase dengan ABTS
Pemurnian Parsial Enzim Lakase dengan Variasi Kejenuhan
Amonium Sulfat
Penentuan Tingkat Kemurnian Keempat Enzim Lakase
Uji Aktivitas Spesifik Keempat Enzim Lakase yang Telah Dipekatkan dengan
Amonium Sulfat terhadap ABTS
Menentukan Kadar Protein dengan Metode Bradford
Uji Aktivitas Enzim Lakase Terpilih dengan Substrat Alam
(Tongkol Jagung dan Jerami Padi) dengan Analisis SEM Menentukan Enzim Lakase yang
Memiliki Aktivitas Tertinggi
ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
27
3.3.2 Pembuatan media
3.3.2.1 Media padat
3.3.2.1.1 Media PDA
Kentang 20 g dikupas, dibersihkan kemudian diiris tipis. Irisan kentang
tersebut direbus dalam 80 mL aquades sampai kentang menjadi lunak. Air rebusan
kentang disaring dalam gelas Beaker sehingga diperoleh suspensi bening
kemudian endapannya dibuang. Suspensi bening dipindahkan dalam tabung
Erlenmeyer 250 mL dan ditambahkan akuades hingga volume akhir 100 mL,
kemudian ditambahkan dextrose dan agar batangan masing-masing 1,5 g.
Campuran bahan dipanaskan di atas kompor listrik hingga semua bahan terlarut
sempurna. Setelah bahan larut sempurna, tabung Erlenmeyer ditutup rapat dengan
kapas selanjutnya dilapisi dengan aluminium foil. Media disterilkan dengan
autoclave pada tekanan 1 atm, temperatur 121oC selama 15-20 menit.
3.3.2.1.2 Media PDA agar miring
Potato Dextrose Agar (PDA) dituang ke dalam tabung reaksi masing –
masing 6 mL. Kemudian mulut tabung ditutup dengan kapas dan dilapisi
aluminium foil. Tabung reaksi berisi PDA disterilkan dalam autoclave suhu
121°C selama 20 menit. Setelah steril dimiringkan dan ditunggu sampai memadat.
3.3.2.1.3 Persiapan substrat alam
Jerami padi dan tongkol jagung dikeringkan terlebih dahulu pada
temperatur 70 oC dalam oven hingga beratnya konstan. Masing-masing substrat ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
28
dipotong – potong ± 1 cm untuk analisis SEM. Substrat disterilisasi dengan
autoclave untuk menghindari kontaminasi.
3.3.2.2 Media cair
Media cair yang digunakan adalah media GMY (Glucose Malt Yeast).
Media cair ini berfungsi sebagai media pertumbuhan. Komposisi dari media GMY
adalah 4 gr Glukosa, 4 gr Yeast Extract, dan 10 gr Malt Extract. Campuran
dilarutkan dalam akuades, kemudian diatur hingga pH mencapai 7,2 dengan
KOH 0,2 N. Selanjutnya, ditambah akuades sampai volume nya 1000 mL. Media
ini disterilkan dalam autoclave suhu 121°C selama 20 menit.
3.3.3 Persiapan tabung selofan
Menyiapkan tabung selofan yang akan didialisis. Tabung selofan yang
telah disiapkan dididihkan selama 30 menit dalam larutan EDTA (dalam suasana
basa), kemudian dibilas dengan akuades. Salah satu ujung dari selofan diikat
sehingga enzim dapat dimasukkan untuk proses dialisis
3.3.4 Peremajaan kapang
Media padat yang telah disterilkan digunakan untuk meremajakan kapang.
Proses peremajaan kapang dilakukan secara aseptik di laminar air flow cabinet.
Dalam ruang laminar air flow, disiapkan bunsen, isolat kapang terdahulu, ose, dan
alkohol. Dalam media PDA agar miring yang baru digoreskan 1 ose isolat kapang
setelah itu ditutup dengan kapas yang telah disterilkan kemudian dilapisi
aluminium foil dan diinkubasi pada temperatur 37oC selama 5 hari. ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
29
3.3.5 Pembuatan larutan
3.3.5.1 Larutan buffer universal
Larutan stok A, asam sitrat (C6H8O7) 0,1 M dibuat dengan cara
menimbang 1,921 gram asam sitrat lalu dilarutkan dalam aquades dan diencerkan
dalam labu ukur 100 mL hingga tanda batas. Larutan stok B, natrium fosfat
dibasis (Na2HPO4.7H2O) 0,2 M dibuat dengan cara menimbang 5,365 gram lalu
dilarutkan dalam aquades dan diencerkan dalam labu ukur 100 mL hingga tanda
batas. Larutan buffer universal pH 3-8 dibuat dengan cara mencampurkan larutan
A dan B dengan komposisi larutan yang sesuai kemudian diencerkan dalam
aquades sampai volume campuran tepat 100 mL.
A (mL) B (mL) pH
79,45 20,55 3
61,45 38,55 4
48,50 51,50 5
36,85 63,15 6
17,65 82,35 7
2,75 97,25 8
Tabel 1. Komposisi buffer universal ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
30
3.3.5.2 Pembuatan larutan substrat ABTS
3.3.5.2.1 Pembuatan larutan asam asetat (CH3COOH) 0,2 M
Larutan Asam Asetat 0,2 M dibuat dengan cara mengencerkan asam asetat
glasial 17,487437 M. Sebanyak 1,14 mL asam asetat glasial dimasukkan ke dalam
labu ukur 100 mL kemudian diencerkan dengan akuades sampai tanda batas dan
dikocok sampai homogen.
3.3.5.2.2 Pembuatan larutan natrium asetat (CH3COONa) 0.2 M
Larutan natrium asetat 0,2 M dibuat dengan cara menimbang 1,6406 gr
natrium asetat. Natrium asetat tersebut dilarutkan dalam akuades dengan
menggunakan beaker glass, lalu dipindahkan ke dalam labu ukur 10 mL, dan
diencerkan dengan akuades sampai tanda batas dan dikocok sampai homogen.
3.3.5.2.3 Pembuatan buffer sodium asetat pH 4,5
Larutan buffer sodium Asetat pH 4,5 dibuat dengan mencampurkan
larutan asam asetat dan natrium asetat. Sebanyak 30,5 mL larutan asam asetat
0,2 M 19,5 mL larutan natrium asetat 0,2 M dimasukkan dalam labu ukur 100 mL
kemudian ditambahkan akuades sampai tanda batas dan dikocok sampai
homogen. Larutan tersebut diukur pHnya sampai menunjukkan pH 4,5.
3.3.5.2.4 Pembuatan larutan substrat ABTS 0,4 mM
Larutan substrat ABTS dibuat dengan cara menimbang 0,011 gr ABTS.
ABTS tersebut dilarutkan dalam buffer sodium asetat pH 4,5 dengan
menggunakan akuades. Selanjutnya larutan tersebut dipindah ke dalam labu ukur ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
31
50 mL secara kuantitatif. Larutan diencerkan dengan buffer sodium asetat sampai
tanda batas dan dikocok sampai homogen.
3.6 Produksi Enzim Lakase
Kapang yang telah tumbuh di media PDA, dibuat inokulum dengan cara
melarutkan konidia atau spora dengan akuades steril. Inokulum ini dimasukkan
sebanyak 200µL ke dalam media cair GMY yang diberi penambahan larutan
CuSO4 0,05 mM. Media GMY yang mengandung inokulum ini diinkubasi selama
waktu terbaik pada masing – masing kapang pada suhu ruang dan digojog dengan
kecepatan 150 rpm. Pada waktu terbaik masing – masing kapang, media GMY
yang telah diinkubasi dan digojog, disentrifugasi dengan kecepatan 3300 rpm, 4°C
selama 2 menit. Supernatan yang terbentuk pada media setelah disentrifugasi
inilah yang disebut enzim lakase.
3.7 Uji Aktivitas Enzim Lakase
Uji aktivitas enzim lakase dilakukan berdasarkan metode Bourbonnais dan
Paice (1990). Prinsip uji ini adalah sebagai berikut : pewarna non-phenol Asam
2,2’-azinobis-di-(3-ethylbenzthiazolinesulphonate) (ABTS), dioksidasi oleh
lakase menjadi radikal kation (ABTS) yang lebih stabil. Konsentrasi radikal
kation yang berwarna biru kehijauan (dibaca pada panjang gelombang 420 nm)
berkolerasi dengan aktivitas lakase.
Pengukuran aktivitas lakase dilakukan dengan menggunakan kondisi
optimum hasil penelitian Dewi (2010). Pengukuran tersebut dilakukan dengan
cara sebagai berikut : Larutan 0,4 mM ABTS dalam buffer natrium asetat (pH 4,5)
sebanyak 1160 µL dimasukkan ke dalam kuvet 1,5 mL, kemudian ditambahkan ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
32
40 µL enzim dan dikocok agar tercampur homogen. Kemudian absorbansi radikal
kation diamati pada panjang gelombang 420 nm (
ε
mM = 36 mM-1 cm-1) selamalima menit menggunakan spektrofotometer UV-VIS. Perubahan absorbansi
radikal kation ini diamati setiap menit. Aktivitas lakase dinyatakan sebagai
International Unit (IU) per liter, dengan 1 IU didefinisikan sebagai jumLah enzim
yang dapat mengoksidasi 1 µmol ABTS tiap menit. Aktivitas lakase ditentukan
dengan menggunakan persamaan sebagai berikut:
Dengan :
V = volume total reaksi (mL)
v = volume enzim (mL)
ε
=
extinction coefficient ABTS pada 420 nm = 36 mM-1 cm-1d = Light path of cuvette (cm)
∆A.min-1 = perubahan absorbansi tiap menit pada 420 nm
3.8 Penentuan Kadar Protein Lakase
Metode yang digunakan dalam menentukan kadar protein pada penelitian
ini adalah metode Bradford (1976) dengan menggunakan standar Bovine Serum
Albumin (BSA). Langkah awal yang dilakukan adalah menyiapkan reagen
Bradford yang terdiri dari 50 mg Coomassie brilliant blue G-250 yang dilarutkan
dalam 25 mL etanol 96%, kemudian ditambahkan 50 mL asam fosfat 85% dan
diencerkan dengan akuades sampai volume 500 mL. Analisis sampel dilakukan
dengan cara memasukkan 10 µL sampel dalam tabung Eppendorf kemudian ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap
33
ditambahkan akuades sampai volume 100 µL lalu ditambahkan reagen Bradford.
Blanko yang digunakan terdiri dari 100 µL akuades dan 1 µL reagen Bradford.
Setelah itu, larutan dihomogenkan dengan vortex, kemudian absorbansi dibaca
dengan menggunakan spektrofotometer pada panjang gelombang 595 nm.
Standar BSA dibuat pada kisaran 100 – 500 µg/mL dari stok BSA dengan
kadar 1 mg/mL. Dari stok tersebut dilakukan pengenceran dengan akuades untuk
memperoleh konsentrasi yang diinginkan. Blanko yang digunakan adalah 100 µL
akuades dan 1 mL reagen Bradford. Selanjutnya absorbansi dibaca dengan
menggunakan spektrofotometer dengan panjang gelombang 595 nm.
3.9 Pemurnian Enzim
Ekstrak kasar enzim lakase dari isolat kapang TKKS dipresipitasi dengan
amonium sulfat dengan tingkat kejenuhan tertentu. Tabel kejenuhan amonium
sulfat yang digunakan adalah berdasarkan tabel Scopes (1994).
Setelah dipresipitasi dengan amonium sulfat kemudian dilakukan
sentrifugasi pada kecepatan 6000 rpm, selama 20 menit pada suhu 4°C. Endapan
enzim dilarutkan dalam buffer tertentu dengan pH optimumnya masing – masing,
kemudian didialisis. Dialisis dilakukan dengan cara memasukkan larutan enzim
lakase tersebut ke dalam tabung selofan. Tabung selofan yang berisi enzim lakase
direndam dalam larutan buffer dengan konsentrasi yang lebih rendah dengan pH
optimumnya masing – masing sambil diaduk dengan pengaduk magnetik dan
diletakkan dalam ruangan bersuhu tertentu.
ADLN Perpustakaan Universitas Airlangga
Skripsi Pemurnian Parsial Lakase dari Isolat
Kapang Tandan Kosong Kelapa Sawit dan Uji Aktivitasnya Terhadap