LAPORAN SKRIPSI – TK 091383
Sintesa dan Karakterisasi Partikel Nanokomposit ZnO-Silika sebagai Fotokatalis dengan Metode Sonikasi
Oleh:
Mohammad Rahmatullah
NRP. 2309100097
Septono Sanny Putro
NRP. 2311106012
DosenPembimbing:
Prof. Dr. Ir. SugengWinardi, M. Eng
NIP. 195209161980031002
Dr.Widiyastuti, ST. MT
NIP. 197503062002122002
JURUSAN TEKNIK KIMIA
FAKULTAS TEKNOLOGI INDUSTRI
INSTITUT TEKNOLOGI SEPULUH NOPEMBER
LAPORAN SKRIPSI – TK 091383
Synthesis and Characterisation ZnO-Silica Nanocomposites as Photocatalyst with Sonication Method
Mohammad Rahmatullah
NRP. 2309100097
Septono Sanny Putro
NRP. 2311106012
Advisors:
Prof. Dr. Ir. SugengWinardi, M. Eng
NIP. 195209161980031002
Dr.Widiyastuti, ST. MT
NIP. 197503062002122002
CHEMICAL ENGINEERING DEPARTMENT
FACULTY OF INDUSTRIAL TECHNOLOGY
SEPULUH NOPEMBER INSTITUTE OF TECHNOLOGY
Sintesa dan Karakterisasi Partikel Nanokomposit ZnO-Silika sebagai Fotokatalis dengan Metode Sonikasi
Nama : Mohammad Rahmatullah (2309 100097)
Septono Sanny Putro (2311 106012)
Jurusan : Teknik Kimia FTI-ITS
Pembimbing : Prof. Dr. Ir Sugeng Winardi, M Eng Dr. Widiyastuti, ST. MT
ABSTRAK
Sintesis nanokomposit ZnO-Silika dibuat dengan mengaplikasikan continuous and pulse mode ultrasonication
untuk membuat sol ZnO dan pertukaran resin kation untuk menghasilkan sol silika dari water glass. Penelitian ini bertujuan untuk mengetahui kondisi operasi yang sesuai untuk membentuk campuran sol ZnO-silika pada berbagai macam variasi konsentrasi campuran sol dan dialirkan gas nitrogen pada reaktor. Sol ZnO dibuat dengan sonikasi pada suhu 70 oC dengan melarutkan 0,2 M Zn(NO3)2 ke dalam aquadest. Teteskan sedikit
demi sedikit 20 mL NH4OH 25% kedalam larutan hingga
terbentuk endapan. Tambahkan 10 tetes NH4OH 25% untuk
menjernihkan larutan tersebut. Untuk mencegah pertumbuhan partikel ZnO ditambahkan dalam sol silika yang terbuat dari
waterglass yang telah dilarutkan kedalam aquadest pada temperatur 60oC dan dilewatkan kedalam resin kation anion. Partikel nanokomposit ZnO-Silika dihasilkan dengan metode Sonikasi. Morfologi, kristalinitas, gugus fungsi dan sifat optis dari nanokomposit ZnO-Silika masing-masing dianalisa dengan menggunakan SEM (Scanning Electron Micrograph), XRD ( X-ray Diffraction), Fourier Transform Infra Red (FTIR), dan Spektrofotometer UV-Vis.
Snynthesis and characterisation ZnO-Silica Nanocomposites as Photocatalyst with Sonication Method
Name of Student : Mohammad Rahmatullah(2309 100097) Septono Sanny Putro (2311 106012)
Major : Chemical Engineering FTI-ITS
Teacher of Advisor : Prof. Dr. Ir Sugeng Winardi, M Eng Dr. Widiyastuti, ST. MT
ABSTRACT
Synthesis of ZnO-silica nanocomposites was made applying continuous and pulse mode ultrasonication for producing ZnO sol, dip-coating for film preparation and cation resin column for producing silica sol from water glass. The aim of the research is to find out the optimum operation condition to produce ZnO-Silica sol under variation of mixed-sol concentration and added flowrate of Nitrogen gases. ZnO solution is prepared by using sonication method by initially dissolving 0,2 M Zn(NO3)2 in distilled water. 20 mL of 25%
NH4OH is added drop by drop till mild precipitation occured and
the 10 drops of 25% NH4OH were added to make the solution
clear. ZnO solution is then mixed with silica sol from waterglass which is prepared by dissolving it in distilled water at 60oC and then contacting it in cation-anion resin column. This intend to trap ZnO in order to prevent the particles growth. The powder of ZnO-silica nanocomposites is obtained by using Sonication method. Morphology, crystallinity, functional groups and optical properties of ZnO-Silica nanocomposites are analyzed by SEM (Scanning Electron Micrograph), XRD (X-ray Diffraction), Fourier Transform Infra Red (FTIR), and Spektrofotometer UV-Vis.
KATA PENGANTAR
Penulis mengucapkan Alhamdulillah. puji syukur kehadirat Allah SWT. yang selalu melimpahkan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan Laporan Skripsi “Sintesa dan Karakterisasi Partikel Nanokomposit ZnO-Silika Sebagai Fotokatalis dengan Metode Sonikasi” tepat pada waktunya. Laporan ini merupakan syarat kelulusan bagi mahasiswa tahap sarjana di Jurusan Teknik Kimia FTI-ITS Surabaya. Penulis menyadari laporan ini tidak akan selesai tanpa bantuan dari berbagai pihak. Pada kesempatan ini penulis ingin mengucapkan terima kasih kepada :
1. Bapak Dr. Ir. Tri Widjaja. M.T. selaku Ketua Jurusan Teknik Kimia. Fakultas Teknologi Industri. Institut Teknologi Sepuluh Nopember Surabaya
2. Bapak Prof. Ir. Sugeng Winardi. M.T. selaku Dosen Pembimbing dan Kepala Laboratorium Mekanika Fluida dan Pencampuran. atas bimbingan dan saran yang diberikan. 3. Ibu Dr. Widiyastuti. ST. MT. selaku Dosen pembimbing atas
bimbingan dan motivasi yang telah diberikan.
4. Bapak Dr. Tantular Nurtono. ST. M.T. selaku Dosen Laboratorium Mekanika Fluida dan Pencampuran atas saran dan motivasi yang diberikan.
5. Ibu Dr. Siti Machmudah. ST. M.T. selaku Dosen Dosen Laboratorium Mekanika Fluida dan Pencampuran atas saran dan motivasi yang diberikan.
6. Dosen-dosen Teknik Kimia FTI-ITS yang telah memberikan ilmunya kepada penulis
7. Kedua Orang Tua kami atas doa, perhatian, dan kasih sayang yang selalu tercurah selama ini.
Kami menyadari laporan ini tidak luput dari kekurangan. maka kami mengharap saran dan kritik demi kesempurnaan laporan ini sehingga dapat bermanfaat bagi pembaca.
Surabaya, Juli 2014
DAFTAR ISI
ABSTRAK i
KATA PENGANTAR iii
DAFTAR ISI v
DAFTAR GAMBAR vii
DAFTAR TABEL viii
BAB 1 PENDAHULUAN
1.1 Latar Belakang 1-1
1.2 Perumusan Masalah 1-3
1.3 Batasan Penelitian 1-4
1.4 Tujuan Penelitian 1-4
1.5 Manfaat Penelitian 1-4
BAB 2 TINJAUAN PUSTAKA
2.1 Karakteristik Zinc Oxide (ZnO) 2-1
2.2 Karakteristik Silika 2-1
2.3 Metode Pembuatan Partikel Nanometer 2-2
2.3.1 Ultrasonikasi 2-2
2.4 Peralatan untuk Analisa Partikel 2-3 2.4.1 Scanning Electromagnetic Microscope (SEM) 2-3 2.4.2 X-Ray Diffraction (XRD) 2-4 2.4.3 Fourier Transform Infra Red (FTIR) 2-5
2.4.4 Spektrofotometer 2-6
2.5 Penelitian Terdahulu 2-6
BAB 3 METODOLOGI
3.1.1 Bahan yang Digunakan 3-1 3.1.2 Peralatan yang Digunakan 3-1
3.2 Tahap Pembuatan 3-2
3.2.1 Pembuatan Partikel ZnO murni dengan 3-2 Metode Sonikasi
3.2.2 Pembuatan Sol Silika dari Waterglass 3-4 3.2.3 Pembuatan Partikel ZnO-Silika 3-6
3.4 Tahap Analisa 3-9
3.5 Variabel yang Dikerjakan 3-11
3.6 Uji Katalitik 3-12
BAB 4 HASIL PENELITIAN DAN PEMBAHASAN
4.1 Mekanisme Reaksi 4-1
4.1.1 Pembuatan Sol ZnO 4-1
4.1.2 Pembuatan Sol Silika 4-2
4.2 Hasil Analisa 4-3
BAB 5 KESIMPULAN DAN SARAN
5.1 Kesimpulan 5-1
5.2 Saran 5-1
DAFTAR TABEL
Tabel 3.5 Variabel yang dikerjakan 3-9
DAFTAR GAMBAR
Gambar 3.1 Skema tahapan pembuatan partikel ZnO murni 3-3 Gambar 3.2 Skema pembuatan partikel ZnO murni 3-4 Gambar 3.3 Skema tahapan pembuatan sol silika 3-5 Gambar 3.4 Skema pembuatan sol silika 3-6 Gambar 3.5 Skema tahapan pembuatan ZnO-silika 3-7 Gambar 3.6 Skema proses pembentukan partikel 3-8
ZnO-silika
Gambar 3.7 Skema uji katalitik dengan menggunakan 3-12 methylen blue
Gambar 4.1 Hasil Analisa SEM (A) continous mode 1 jam 4-4 (B) continous mode 1,5 jam (C) continous
mode 2 jam (D) continous mode 2,5 jam
Gambar 4.2 Hasil Analisa XRD (A) continous mode 1 jam 4-5 (B) continous mode 1,5 jam (C) continous
mode 2 jam (D) continous mode 2,5 jam
Gambar 4.3 Hasil Analisa SEM (A) continous mode 4-6 2,5 jam (B) pulse 3:1 mode 2,5 jam
Gambar 4.4 Hasil Analisa XRD (A) continous mode 4-7 2,5 jam (B) pulse 3:1 2,5 jam
Gambar 4.5 Hasil Analisa SEM partikel ZnO-Silika 4-8 (A) continous mode 1 jam penambahan
silika menit ke 15 (B) continous mode 1 jam penambahan silika menit ke 45
Gambar 4.6 Hasil Analisa XRD partikel ZnO-Silika 4-9 (A) continous mode 1 jam penambahan
mode 1 jam penambahan silika menit ke 45
Gambar 4.7 Hasil analisa XRD partikel silica 4-11 Gambar 4.8 Hasil Analisa FTIR partikel ZnO murni 4-12
Continous mode 1 jam; Continous mode 1,5 jam; Continous mode 2 jam; Continous mode 2,5 jam
Gambar 4.9 Hasil Analisa FTIR partikel ZnO-silika 4-13 Continous mode 1 jam penambahan silika
menit ke 15; Continous mode 1 jam penambahan silika menit ke 30; Continous mode 1 jam
penambahan silika menit ke 45
DAFTAR NOTASI
NOTASI KETERANGAN SATUAN
m Massa zat (sol, precursor) gr M Beratmolekulpartikel gr/mol
v Volume L
ρ Density gr/L
λ Panjanggelombang cm-1
DAFTAR PUSTAKA
Alias, S.S., Ismail, A.B., & Mohamad, A.A. (2010): Effect of pH on ZnO Nanoparticle Properties Synthesized by Sol-Gel Centrifugation, Journal of Alloys and Compounds. 499:231-237
Balkis, Ratna dan Setyawan, H. (2009): Sintesa Silika Berpori dengan Metode Dual Templating dan Waterglass, Journal Nanosains dan Nanoteknologi. 13-18
Chandra, A., & Andreas, Y. (2007): Sintesa Partikel Silika Berpori Dengan Penambahan Gelatin Sebagai Template Dalam Spray Dryer. Skripsi, Institut Teknologi Sepuluh November. Surabaya
Chang, H., Park, J.H., & Jang, H.D., (2008): Flame Synthesis of Silica Nanoparticles by Adopting Two-Fluid Nozzle Spray. Colloids and Surfaces A: Physicochem. Eng. Aspects, 313–314, 140–144
Day, Jr, R. A., Underwood, A. L. (1989): Analisis Kimia Kuantitatif. Erlangga. Jakarta
Dodd, A.C., McKinley, A.J., Saunders, M. & Tsuzuki, T. (2005):
Effect of Particle size on the Photocatalytic Activity of nanoparticulate Zinc Oxide. Journal of Nanoparticle Research. 8: 43-51
Dong, L., dkk. (2005): Preparation of ZnO colloids by aggregation of the nanocrystal subunits, Journal of Colloid and Interface Science. 283:380-384
Ernawati, L. dan Faridah, L. (2001): Preparasi Film ZnO-Silika Nanokomposit Dengan Metode So-gel. Skripsi. Institut Teknologi Sepuluh November. Surabaya
Hendra., R. (2008): Pembuatan Karbon Aktif. Universitas Indonesia. Jakarta.
Surface A: Physicochemical and Engineering Aspects. 74(1):13
Marczak, R., dkk. (2010): Optimum Between Purification And Colloidal Stability Of Zno Nanoparticles. Advanced Powder Technology. 21:41-49
Rosa, S.E., Shobih, Lesmana, T.H., (2009): Pembuatan Film Oksida Konduktif Transparan ZnO:Al Menggunakan Metoda Screen Printing. Journal Elektronika, No. 1 Vol 9 Sahu, Dojalisa., dkk. (2010): Probing The Surface States in Nano ZnO Powder Synthesized by Sonication Method: Photo and Thermo-luminescence Studies. Journal of Luminescence. 130:1371-1378
Winardi, S., Kusdianto & Widiyastuti. (2011): Preparasi Film ZnO-Silika Nanokomposit Dengan Metode Sol-gel.
Dalam Prosoding Seminar Nasional Teknik Kimia Kejuangan. ISSN. 1693 - 4393
RIWAYAT PENULIS
Mohammad Rahmatullah lahir di Pamekasan, 03 April 1991. Penulis menempuh pendidikan formal di SDN Bugih 5 Pamekasan Tahun 1997 – 2003, melanjutkan di SMPN 1 Pamekasan Tahun 2003 – 2006, dan SMAN 1 Galis Pamekasan Tahun 2006 – 2009. Penulis menempuh kuliah di Institut Teknologi Sepuluh Nopember Surabaya Jurusan Teknik Kimia Tahun 2009-2015. Penulis pernah menempuh kerja praktek di PT. SIER Surabaya pada tahun 2014. Di akhir masa studi, penulis memilih Laboratorium Mekanika Fluida dan Pencampuran untuk pengerjaan Tugas Akhir. Kami di bawah bimbingan Prof. Dr.Ir. Sugeng Winardi, M.Eng dan Dr. Widiyastuti, ST., MT. Penulis berhasil menyelesaikan tugas akhir Pra Desain Pabrik Gula Rafinasi.
DATA PRIBADI
Nama : Mohammad Rahmatullah
Alamat : Jl. Nyalabu Indah G-6 Pamekasan No. Telepon : 085732662515
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Saat ini ketersediaan cadangan bahan bakar fosil untuk energi di dunia semakin menipis dan harganya semakin meningkat. Untuk itu perlu dikembangakan suatu teknologi yang menciptakan sumber energi alternatif baru. Sumber energi alternatif ini harus yang mempunyai efisiensi yang tinggi dan ramah terhadap lingkungan sekitar. Penggunaan semikonduktor fotokatalisis dapat mengubah H2O menjadi Hidrogen dan
Oksigen dengan imputan sinar UV bertenaga rendah, dimana Hidrogen dapat menjadi energi alternatif pengganti yang ramah lingkungan. Akan tetapi dalam pengaplikasian fotokatalisis lebih mudah dilakukan dalam kegiatan sehari - hari, yakni sebagai pengolah air atau udara, serta kemampuannya membuat permukaan bahan menjadi tetap bersih.
Bahan semikonduktor fotokatalisis seperti Cadmium Sulfide (CdS), Titanium Dioxide (TiO2) dan dioksida zirkonium
(ZrO2) seringkali mempunyai efek berbahaya pada tubuh manusia
dan lingkungan, karena itu perlu adanya bahan alternatif yang lebih efisien dan ramah lingkungan. ZnO memiliki potensi sebagai bahan fotokatalisis yang setara dengan Titanium Dioxide (TiO2) untuk mendegradasi senyawa organik yg terkandung
dalam air dengan bantuan sinar UV. TiO2 dan ZnO yang paling banyak digunakan fotokatalis semikonduktor karena fotosensitifitas mereka tinggi, stabilitas fotokimia, band gap yang besar, daya oksidasi yang kuat dan sifat non - toksik. Penelitian baru-baru ini menyoroti ZnO menunjukkan aktivitas lebih baik daripada TiO2 dalam fotodegradasi beberapa pewarna dalam larutan air, karena indeks bias yang dimiliki ZnO lebih rendah dan bersifat transparan sehingga dapat menyerap lebih banyak sinar UV yaitu UVA dan UVB sedangkan TiO2 hanya menyerap
Nanopartikel fotokatalisis dapat diproduksi dengan berbagai metode, menurut Park (2007) diantaranya, sintesis plasma, wet-phase processing, presipitasi kimia, sol-gel processing, pengolahan mekanik, sintesis mechanicochemical, high-energy ball milling, chemical vapour deposition dan ablasi laser, sedangkan metode untuk sintesis nanopartikel menurut (Rosa dkk, 2009) co-precipitation, ultrasound irradiation, elektrokimia, dan sintesis hidrotermal. Dari beberapa metode diatas metide sol-gel merupakan metode yang paling sering digunakan, karena metode ini menghasilkan homogenitas dan sifat optik yang baik, pengontrolan komposisi yang mudah, pengolahan pada suhu rendah dan biaya peralatan yang murah (Alias dkk, 2010). Sedangkan kekurangan dari metode ini adalah waktu yang digunakan cukup lama (Iva & Paulina, 2012). Sebagai alternatifnya metode yang bisa digunakan adalah metode sonikasi. Metode sonikasi merupakan metode top down, metode ini merupakan pembuatan struktur nano dengan memperkecil material yang besar (Greiner, 2009).
Dojalisa dkk, (2010), telah berhasil menghasilkan partikel ZnO dengan menggunakan metode sonikasi. Prosesnya dengan cara menggunakan gelombang ultrasonik dengan rentang frekuensi 20 kHz-10 MHz yang ditembakkan ke dalam medium cair untuk menghasilkan cavitation bubble yang dapat membuat partikel memiliki diameter dalam skala nano. Namun dalam penelitian yang dilakukan hanya sampai tahap pembuatan larutan ZnO.
Silika merupakan bahan baku utama yang dapat diperoleh dari bahan sintesis seperti silika fumed, TEOS (Tetroethylorthosilicate) dan TMOS (Tetramethylorosilicate) (Dong dkk, 2005). Bahan silika diatas sangat terbatas dan mahal sehingga untuk mengatasi hal tersebut diperlukan alternatif lain untuk mencari sumber silika dari bahan yang murah dan ramah lingkungan seperti waterglass (Balkis & Setyawan, 2009).
Pembuatan koloid nanopartikel silika dari waterglass
dkk, 1993) dengan cara melewatkan melalui resin penukar kation dan anion dengan tujuan untuk menghilangkan impuritis dalam bentuk baik anion maupun kation. Pada penelitian sebelumnya (Lusi & Farida, 2010) telah mencoba membuat silika dari
waterglass namun silika yang dihasilkan berbentuk gel ketika konsentrasi silika > 50% mol campuran. Bila yang diinginkan material dalam bentuk partikel maka terbentuknya gel harus dihindari karena dalam aplikasinya ZnO yang digunakan sebagai bahan fotokatalisis adalah dalam bentuk partikel dengan ukuran antara 1-405 µm..Berdasarkan penelitian sebelumnya yang dilakukan Maula dan Ruliawati (2011) dalam sintesa partikel nanokomposit ZnO-silika dengan metode kombinasi sol-gel dan
flame spray pyrolysis, dihasilkan partikel yang kurang seragam, penelitian yang dilakukan oleh (Wahyu & Siska, 2012) dengan mensintesa partikel nanokomposit ZnO-silika dengan metode kombinasi sol-gel dan spray drying, namun partikel ZnO tidak terbentuk. Sedangkan penelitian yang dilakukan (Putri & Hakim, 2014) dengan mensintesa partikel nanokomposit ZnO-silika dengan metode sonikasi partikel yang dihasilkan masih belum seragam namun sudah tidak terbentuk gel.
1.2 Perumusan Masalah
Dengan meninjau penelitian terdahulu dimana metode yang digunakan untuk pembuatan partikel nano komposit berasal dari ZnO yang menggunakan metode sol-gel dengan pelarut aquadest dalam pelaksanaanya masih terdapat kekurangan mendispersikan ZnO ke dalam sol silika sehingga sol yang tebentuk morfologi dari ZnO Silika masih belum seragam dan masih terdapat impurities.
1.3 Batasan Masalah
Pembuatan sol ZnO berdasarkan metode sonikasi yang dilakukan oleh (Dojalisa dkk, 2009) dan pembuatan sol silika berdasarkan (Liu dkk, 1993) dengan pengaturan pH dan konsentrasi. Untuk mendapatkan partikel komposit ZnO-silika digunakan metode ultrasonikasi pada kondisi tertutup dengan mengalirkan gas nitrogen.
1.4 Tujuan Penelitian
Mengetahui pengaruh ratio konsentrasi, waktu, mode pulse dan continuous, serta penambahan aliran gas nitrogen terhadap karakteristik nanokomposit ZnO-Silika sebagai bahan fotokatalis.
1.5 Manfaat Penelitian
BAB 2
TINJAUAN PUSTAKA
2.1 Karakteristik Zinc Oxide (ZnO)
Zinc oxide merupakan senyawa inorganic dengan rumus molekul ZnO, berbentuk serbuk putih, tidak larut dalam air, dan secara luas digunakan sebagai zat adiktif pada kebanyakan material dan produk seperti plastik, keramik, kaca, semen, pelumas dan baterai. ZnO merupakan salah satu bahan yang dapat digunakan sebagai fotokatalis dari bahan lainnya seperti titanium dioksida (TiO2), oksida timah (SnO2), dioksida zirkonium
(ZrO2), kadmium sulfida (CdS), dan semikonduktor oksida
belerang lainnya. Dalam aplikasi tersebut, ZnO lebih unggul TiO2
karena penyerapan yang lebih luas dari sinar UV (ZnO menyerap baik UVA dan UVB sedangkan TiO2 hanya menyerap UVA) dan
indeks bias yang lebih rendah. (Dodd dkk, 2006)
2.2 Karakteristik Silika
Silika merupakan senyawa oksida logam yang banyak terdapat di alam, namun keberadaannya di alam tidak dalam kondisi bebas melainkan terikat dengan senyawa lain baik secara fisik maupun kimia. Silika banyak digunakan di industri karena sifat dan morfologinya yang unik, meliputi luas permukaan dan volume porinya yang besar, dan kemampuan untuk menyerap berbagai zat seperti air, oli dan bahan radioaktif (Chandra dan Andreas, 2007).
Sol silika atau yang disebut juga silicic acid hydrosol
dibentuk dari dispersi partikel SiO2 koloid dalam air. Secara
2.3 Metode Pembuatan Partikel Nanometer
Pada penelitian ini metode yang digunakan untuk pembuatan partikel yaitu metode sonikasi.
2.3.1 Ultrasonikasi
Sonikasi merupakan suatu proses pengubahan sinyal listrik menjadi getaran mekanis yang dapat diarahkan menuju suatu zat yang dilakukan untuk memecahkan ikatan antar molekul atau untuk merusak sel. Getaran yang dihasilkan dapat memecah bagian molekul dan merusak sel. Bagian utama dari sonikator adalah generator listrik ultrasonik. Alat ini menghasilkan sinyal (sekitar 20 KHz) yang menghidupkan transduktor. Transduktor kemudian mengkonversi sinyal elektrik degan menggunakan kristal piezoelectric, yaitu kristal yang dapat merespon listrik dengan menghasilkan getaran mekanis. Getaran tesebut dijaga oleh sonikator hingga melewati probe. Probe sonikator berperan dalam menyampaikan getaran pada cairan yang disonikasi. Pergerakan probe yang terjadi dengan cepat menghasilkan efek kavitasi yang terjadi ketika terbentuk gelembung-gelembung mikroskopis dalam larutan akibat adanya getaran. Pembentukan dan penghancuran gelembung tersebut menghasilkan gelombang getaran berenergi tinggi yang dapat merusak sel.
2.4 Peralatan untuk Analisa Partikel
2.4.1 Scanning Electromagnetic Microscope (SEM)
digunakan dalam analisa SEM bersama dengan spectrum yang terbuat dari karakteristik sinar-X. Karena intensitas sinyal BSE sangat terkait dengan nomor atom (Z) dari sampel, BSE dapat memberikan informasi tentang distribusi unsure-unsur yang berbeda dalam sampel. Karakteristik sinar-X ini digunakan untuk mengisi shell dan melepas energi. Karakteristik sinar-X ini digunakan untuk mengidentifikasi dan mengukur komposisi kelimpahan elemen dalam sampel.
2.4.2 X-Ray Diffraction (XRD)
X-ray Diffraction adalah teknik analisis yang cepat terutama digunakan untuk identifikasi fase dari bahan kristal dan dapat memberikan informasi tentang dimensi sel satuan.Max von Laue, pada tahun 1912, menemukan bahwa zat kristal bertindak sebagai tiga dimensi kisi-kisi difraksi untuk panjang gelombang sinar X. Difraksi sinar- X sekarang menjadi teknik umum untuk studi struktur kristal dan jarak atom. Difraksi sinar-X didasarkan pada interferensi konstruktif dari monokromatik sinar-X dan sampel kristal.
Sinar-X dihasilkan oleh tabung sinar katoda, disaring untuk menghasilkan radiasi monokromatik, collimated untuk berkonsentrasi, dan diarahkan ke sampel. Interaksi sinar dengan sampel menghasilkan interferensi konstruktif ketika kondisi memenuhi hukum Bragg. Hukum ini berkaitan dengan panjang gelombang radiasi elektromagnetik untuk sudut difraksi kisi dan jarak dalam sampel kristal. Difraksi sinar-X kemudian terdeteksi, diproses dan dihitung. Konversi puncak difraksi dengan jarak d
memungkinkan identifikasi mineral karena mineral masing-masing memiliki satu set unik jarak d. Biasanya, hal ini dicapai dengan perbandingan jarak d dengan pola referensi standar.
bahan target dengan elektron. Ketika elektron memiliki energy yang cukup untuk mengeluarkan electron shell dalam diri bahan target, karakteristik spectrum sinar-X dihasilkan. Spektrum ini terdiri dari beberapa komponen Kα yang paling umum dan Kβ.
Kα terdiri dari Kα1danKα2. Kα1 memiliki panjang gelombang lebih pendek dan dua kali intensitas sebagai Kα2.
Sebuah catatan detector dan proses pada sinyal sinar-X terjadi yang kemudian mengubah sinyal menjadi tarif hitungan yang kemudian dikeluarkan melalui perangkat seperti printer atau monitor computer. X-ray Diffraction paling banyak digunakan untuk identifikasi bahan kristalin seperti mineral dan senyawa anorganik. (www. serc.carleton.edu)
2.4.3 Fourier Transform Infra Red (FTIR)
2.4.4 Spektrofotometer
Spektrofotometer sangat berhubungan dengan pengukuran jauhnya pengabsorbansian energi cahaya oleh suatu sistem kimia sebagai fungsi panjang gelombang dengan absorban maksimum dari suatu unsur atau senyawa. Konsentrasi unsur atau senyawa dapat dihitung dengan menggunakan kurva standar yang diukur pada panjang gelombang absorban tersebut, yaitu panjang gelombang yang diperoleh dari hasil nilai absorbansi yang tertinggi. Spektrum absorban selain bergantung pada sifat dasar kimia, juga bergantung pada faktor-faktor lain. Larutan pembanding dalam spektrofotometri pada umumnya adalah pelarut murni atau suatu larutan blanko yang mengandung sedikit zat yang akan ditetapkan atau tidak sama sekali. Prinsip kerja spektrofotometer adalah bila cahaya (monokromatik maupun campuran) jatuh pada suatu medium homogen, sebagian dari sinar masuk akan dipantulkan, sebagian diserap dalam medium itu, dan sisanya diteruskan. Nilai yang keluar dari cahaya yang diteruskan dinyatakan dalam nilai absorbansi karena memiliki hubungan dengan konsentrasi sampel. (Day & Underwood, 1989).
2.5 Penelitian Terdahulu
Abdullah (2004) meneliti trapping ZnO dengan matriks silika dengan menggunakan prekursor TEOS (tetraethoxysilane) sebagai sumber silika dan metode spray drying untuk menghasilkan partikel ZnO-Silika dengan menggunakan nitrogen sebagai gas pembawa ke furnace. Liu dkk, (1991) membuat sol nanopartikel silika dari waterglass pada kondisi asam dan basa dengan cara melewatkan melalui resin penukar kation dan anion untuk menghilangkan impuritis dalam bentuk baik anion maupun kation. Putri dan Hakim, (2014) mensintesa partikel nanokomposit ZnO-silika dengan metode kombinasi sonikasi,
BAB 3
METODOLOGI
Pada bab ini terdiri dari beberapa tahap meliputi tahap persiapan, tahap pembuatan dan tahap analisa. Pada tahap persiapan bahan yang digunakan terdiri dari bahan kimia sebagai reaktan maupun bahan-bahan kimia lain sebagai bahan pendukung dan alat-alat yang digunakan ketika penelitian berlangsung.
3.1 Tahap Persiapan : 3.1.1 Bahan yang digunakan:
1. Kristal Zn(NO3)24H2O p.a 98,5% (E. Merck, D-1600
Darmstadt, Germany)
2. Larutan NH4OH25% (Merck Darmstadt, Germany)
3. Larutan Ethanol Analytical Reagent (AR) 99,8% (PT Smart Indonesia)
4. Waterglass NaO 8 %, SiO2 27% (Merck KGaA 64271
Darmstadt, Germany)
5. Kristal KOH (Merck KGBA 64271 Darmstadt, Germany) 6. Gas Nitrogen
7. Resin kation 8. Aquadest
3.1.2 Peralatan yang digunakan:
1. Flowmeter (Koflok model RK 1200) berfungsi pengukur laju alir gas N2
2. Ultrasonik (Sonics Vibra Cell) berfungsi mengubah sinyal listrik menjadi getaran mekanis yang dapat diarahkan menuju suatu zat yang dilakukan untuk memecahkan ikatan antar molekul atau untuk merusak sel sehingga terbentuk partikel dengan ukuran nano
4. Pompa peristaltik micro tube pump (Eyela Tokyo Rikakikai, MP-3N) berfungsi memompa sol silika ke dalam reaktor
5. Pendingin refluks berfungsi untuk mendinginkan uap proses sonifikasi sintesa partikel
6. Drying oven (OneMed, model 101-0) berfungsi untuk mengeringkan partikel.
7. Watertrap berfungsi untuk mengabsorpsi gas yang keluar dari reaktor
8. Stirrer hot plate berfungsi untuk memanaskan aquadest 9. Centrifuge (OneMed, model 0508-1) berfungsi untuk
memisahkan partikel dengan larutannya
10. Dry Cabinet (Krisbow) berfungsi sebagai tempat penyimpanan partikel dalam kondisi kelembaban yang stabil
11. Neraca Analitik (Ohaus Adventurer Pro) berfungsi untuk menimbang bahan.
3.2 Tahap Pembuatan
Pada tahap persiapan terbagi menjadi dua tahapan, yaitu tahap pembuatan partikel ZnO murni dan tahap pembuatan sol silika dengan melewatkan resin kation.
3.2.1 Pembuatan partikel ZnO murni dengan metode sonikasi
Metode sonikasi merupakan salah satu metode yang paling mudah dalam pembuatan partikel ZnO murni. Sejumlah 5,308 gram zinc nitrat dilarutkan dalam 100 mL aquadest. Kemudian ditambahkan 20 mL NH4OH 25% ke dalam larutan zink nitrat
hingga tebentuk endapan dan mengeruh. Selanjutnya ditambahkan 10 tetes NH4OH 25% ke dalam larutan untuk
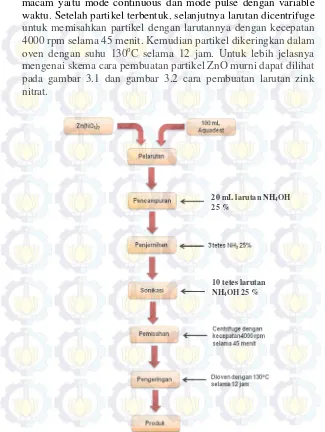
macam yaitu mode continuous dan mode pulse dengan variable waktu. Setelah partikel terbentuk, selanjutnya larutan dicentrifuge untuk memisahkan partikel dengan larutannya dengan kecepatan 4000 rpm selama 45 menit. Kemudian partikel dikeringkan dalam oven dengan suhu 130oC selama 12 jam. Untuk lebih jelasnya mengenai skema cara pembuatan partikel ZnO murni dapat dilihat pada gambar 3.1 dan gambar 3.2 cara pembuatan larutan zink nitrat.
Gambar 3.1 Skema tahapan pembuatan partikel ZnO murni
20 mL larutan NH4OH
25 %
Gambar pembuatan larutan zink nitrat
Gambar 3.2 Skema pembuatan larutan [Zn(NH3)4](NO3)2
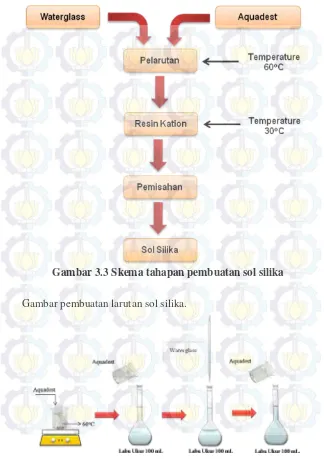
3.2.2 Pembuatan sol silika dari waterglass
Pembuatan sol silika dilakukan dengan cara melarutkan
waterglass dalam 100 mL aquadest yang terlebih dahulu dipanaskan hingga suhu 60oC kemudian larutan didiamkan hingga temperatur turun menjadi 30oC. Selanjutnya larutan waterglass
Gambar 3.3 Skema tahapan pembuatan sol silika
Gambar 3.4 Skema pembuatan sol silika
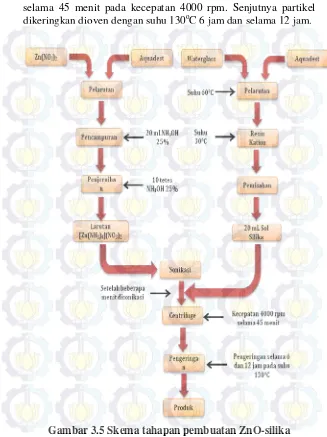
3.2.3 Pembuatan partikel ZnO-silika
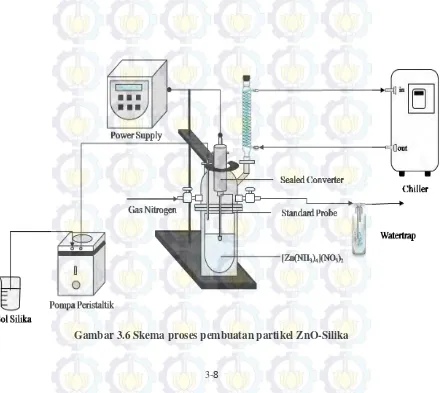
Pembentukan partikel ZnO-silika dengan menggunakan sonikasi dalam kondisi tertutup dengan dialirkan gas nitrogen dengan beberapa variable yang diantaranya mode ultrasonik continous atau pulse pada saat sintesa berlangsung serta waktu sonifikasi. Konsentrasi silika juga menjadi variable pada penelitian ini, besar kecilnya konsentrasi silika mempengaruhi sifat dari partikel ZnO-silika yang dihasilkan.
Pada tahap ini partikel ZnO-Silika dihasilkan dengan metode Sonikasi dengan tahap-tahap prosesnya seperti yang dijelaskan pada gambar 3.5. Mula-mula larutan Zink Nitrat 0,2 M sebesar 5,308 gram yang sudah dilarutkan dalam 100 mL aquadest lalu ditambahkan 20 mL larutan NH4OH 25% dan 10
tetes larutan NH4OH 25%, kemudian dimasukan kedalam reaktor,
selama 45 menit pada kecepatan 4000 rpm. Senjutnya partikel dikeringkan dioven dengan suhu 130oC 6 jam dan selama 12 jam.
3.4 Tahap Analisa
Partikel yang dihasilkan melalui metode sonifikasi dapat diamati menggunakan SEM (Scanning Electron Micrograph) Zeiss Evo MA LS series, Cambridge, England untuk analisa morfologi, XRD (X-ray Diffraction) (Philips, 30 mA, X-Ray 40 kv, Netherland) untuk analisa kemurnian dan derajat kristal, Fourier-transform Infra Red (FTIR) (Shimadsu, Resolution 8 (cm-1)) untuk menentukan gugus fungsi, dan uji katalis dengan menggunakan Spektrofotometer UV-Vis (Termo scientific) untuk mengetahui sifat optikal.
3.5 Variabel yang dikerjakan
Run
Pengeringan Mode
3.6 Uji Katalitik
Setelah didapatkan partikel ZnO murni maupun ZnO-silika dengan beberapa variabel yang berbeda dari hasil penelitian, kemudian partikel-partikel tersebut dilakukan uji katalitik dengan cara larutan methylen blue dengan konsentrasi 0,00001M sebanyak 50 mL dengan menambahkan partiekl ZnO murni atau ZnO-silika yang kemudian dipaparkan ke sinar matahari selama waktu tertentu. Tujuannya adalah untuk mengetahui sejauh mana partikel yang diperoleh dari hasil penelitian dapat mendegradasi warna dari methylen blue dan seberapa besar pengaruh waktu dalam pemaparannya. Berikut adalah gambar skema uji katalitik dengan methylen blue.
Gambar 3.7 Skema uji katalitik dengan menggunakan methylen blue
Keterangan:
1. Methylen Blue yang digunakan konsentrasinya 0,00001 M sebanyak 50 mL.
2. ZnO-silika dan ZnO murni yang digunakan sebesar 0,07 gram (70 mg)
BAB 4
HASIL PENELITIAN DAN PEMBAHASAN
Nanokomposit adalah kombinasi dari satu atau lebih komponen yang terpisah dan salah satu komponennya adalah skala nanometer. Tujuan pembuatan nanokomposit adalah untuk menghasilkan sifat yang terbaik dari tiap komponen. Dalam nanokomposit, nanopartikel bertindak sebagai filler dalam sebuah matriks. Nanokomposit merupakan material yang dibuat dengan menyisipkan nanopartikel (filler) dalam sebuah sampel material makroskopik (matriks). Nanokomposit dihasilkan dari pencampuran dalam sejumlah fase yang berbeda. Pencampuran ini dapat menghasilkan sifat baru yang tidak ditemui pada masing-masing material asal. Nanokomposit memperlihatkan sifat-sifat baru yang lebih unggul dibandingkan dengan material asal (Abdullah, 2009).
Salah satu cara untuk menghentikan pertumbuhan ukuran
partikel ZnO adalah men-trap partikel tersebut dalam matriks
padatan. Dan sebagai material padat dipilih silika yang berfungsi
sebagai pen-trap partikel ZnO agar tidak teragglomerasi. Dalam
proses trapping yang perlu diperhatikan adalah waktu dan
mekanisme proses trapping. Proses trapping harus berlangsung
dalam waktu singkat dan disertai dengan pengadukan hal ini dimaksudkan agar tidak terjadi sebaran ukuran partikel selama
proses trapping. Distribusi ukuran partikel menyempit setelah sol
ZnO di-trap ke matrik silika (Dong et al., 2005).
4.1 Mekanisme Reaksi 4.1.1 Pembentukan sol ZnO
Sintesa serbuk ZnO nano dapat dibuat dengan menggunakan sonikator dengan mode continous dan mode pulse. Dalam metode ini 0,2 M Zinc Nitrat dilarutkan dalam 10 mL
setetes hingga terjadi endapan dan ditambahkan 10 t etes NH3
untuk membuat larutan menjadi bening. Panas yang ditimbulkan selama proses sonikasi, terjadi pelepasan ammonia dari larutan
yang mengakibatkan peruraian Zn(NH3)42+ kompleks. Berikut
reaksi pembentukan partikel ZnO:
Zn(NO3)2 + 2NH4OH + H2O Zn(OH)2 + 2NH4NO3 + dihasilkan dari proses sonikasi. PH larutan diukur saat awal dan pada akhir experiment. Pada kedua kondisi atau mode, pH titik awal adalah 10,4, tapi pH turun ke 9,6 setelah akhir continous mode dan pH 8,4 untuk pulse mode ketika akhir proses.
Partikel yang diperoleh dari metode sonikasi dicuci 2-3 kali dengan aquadest dan alkohol dari centrifuge. Endapan atau partikel dikumpulkan dalam cawan petri dan dikeringkan dalam
oven pada suhu 130oC selama semalam (Sahu et al, 2010)
4.1.2 Pembentukan sol Silika
Sol silika atau yang disebut juga silicic acid hydrosol
dibentuk dari dispersi partikel SiO2 koloid dalam air. Sumber
SiO2 didapat dari waterglass.Silicic acid terbentuk dengan cara
melewatkan waterglass ke dalam resin kation. Didalam penelitian
ini pembuatan sol silika 0,1 M dibuat dengan melarutkan 1,6532 ml waterglass kedalam aquadest 100 ml pada temperatur 60 oC. Aktivasi resin kation menggunakan larutan HCl 2 N. Setelah
diaktivasi resin dibilas dengan aquadest sebelum dikontakkan
dari klorin. Didalam resin kation terjadi pertukaran ion Na+ dari
larutan dengan ion H+.
Proses dapat dijelaskan dengan reaksi berikut :
Na2SiO3 + H2O + 2H+ → Si(OH)4 + 2Na+
Dalam pembuatan sol silika yang perlu diperhatikan adalah pH sol yang terbentuk. Sol silika dikatakan stabil saat pH≈1-3 dan pH≈7. Selanjutnya dalam penelitian ini untuk membuat sol silika yang stabil, sol silika yang terbentuk (pH≈4) kemudian ditambahkan KOH 0,1 M hingga sol silika (pH≈7).
Penelitian ini menggunakan ultrasonikator untuk mempercepat proses sintesis ZnO. Ada dua mode yang digunakan saat penelitian berlangsung yaitu continous mode dan pulse mode. Variable waktu yang digunakan pada penelitian ini adalah 1 jam, 1,5 jam 2 j am, dan 2,5 jam. Sedangkan untuk pulse mode pada penelitian ini adalah pulse 3:1 yaitu on = 3 detik, off = 1 detik dan untuk continous mode adalah ultrasonikator akan menyala setiap detiknya hingga berhenti menurut seting waktu yang telah ditentukan. Ultrasonikator yang digunakan memiliki spesifikasi operasi 500 W, frekuensi 20 kHz, amplitude 60% dan suhu
ultrasonikator 70oC.
4.2 Hasil Analisa
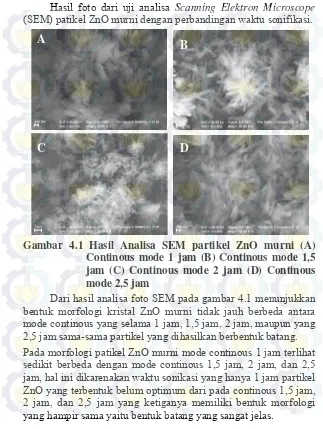
Hasil foto dari uji analisa Scanning Elektron Microscope (SEM) patikel ZnO murni dengan perbandingan waktu sonifikasi.
Gambar 4.1 Hasil Analisa SEM partikel ZnO murni (A) Continous mode 1 jam (B) Continous mode 1,5 jam (C) Continous mode 2 jam (D) Continous mode 2,5 jam
Dari hasil analisa foto SEM pada gambar 4.1 menunjukkan bentuk morfologi kristal ZnO murni tidak jauh berbeda antara mode continous yang selama 1 jam, 1,5 jam, 2 jam, maupun yang 2,5 jam sama-sama partikel yang dihasilkan berbentuk batang. Pada morfologi patikel ZnO murni mode continous 1 jam terlihat sedikit berbeda dengan mode continous 1,5 jam, 2 jam, dan 2,5 jam, hal ini dikarenakan waktu sonikasi yang hanya 1 jam partikel ZnO yang terbentuk belum optimum dari pada continous 1,5 jam, 2 jam, dan 2,5 jam yang ketiganya memiliki bentuk morfologi yang hampir sama yaitu bentuk batang yang sangat jelas.
A
B
C
)
Hasil uji analisa X-Ray Diffraction (XRD) partikel ZnO murni dengan perbandingan waktu sonifikasi dengan mode continuous
Berdasarkan hasil analisa XRD, pada gambar 4.2 menunjukkan bahwa semua partikel yang dihasilkan dari mode continous selama 1 jam, 1,5 jam, 2 jam dan 2,5 jam menunjukan partikel ZnO murni. Dapat dibuktikan dengan menbandingkan Joint Committee on Powder Diffraction Standards (JCPDS) 36-1451. Puncak peak yang dihasilkan oleh partikel dengan mode continous selama 1 j am, 1,5 jam, 2 j am dan 2,5 j am mengikuti orientasi dengan JCPDS 36-1451, hanya saja terjadi pelebaran dibawah peak bila dibandingkan dengan JCPDS 36-1451. Semakin lama proses pembuatan partikel, maka partikel tersebut memiliki kualitas kristal wurtzite sangat baik hal ini terlihat dari puncaknya yang tajam, pelebaran dibawah puncak peak yang tidak begitu lebar.
Hasil foto dari uji analisa Scanning Elektron Microscope
(SEM) perbandingan antara mode continous dengan mode pulse 3:1
Gambar 4.3 Hasil Analisa SEM partikel ZnO murni (A) continous mode 2,5 jam (B) pulse 3:1 mode 2,5 jam
Gambar 4.3 menunjukkan bentuk morfologi kristal ZnO murni dari mode continous yang selama 2,5 jam dengan mode pulse 3:1 selama 2,5 j am. Terlihat kedua mode sama-sama menghasilkan partikel yang berbentuk batang, hanya saja pada mode continous lebih menyebar partikelnya dan lebih kecil kristalnya dari pada yang mode pulse yang cendrung menyatu lebih besar kristalnya. Mode pulse 3:1 merupakan mode
ultrasonik on = 3 d etik dan off = 1 d etik yang artinya selama proses sonikasi berlangsung ultasonikator mengeluarkan gelombang energi selama 3 detik dan 1 detik berhenti. Selama 1 detik sonikator berhenti mengeluarkan gelombang energi, pada saat itu partikel ZnO mengalami penyatuan atau saling mengikat kembali sehingga bentuk kristal dari partikel ZnO menjadi lebih besar.
Hasil uji analisa X-Ray Diffraction (XRD) partikel ZnO
murni perbandingan antara mode continous dengan mode pulse 3:1
Pada gambar 4.4 dari hasil analisa XRD menunjukkan bahwa partikel yang dihasilkan dari mode continous selama 2,5 jam dengan mode pulse 3:1 selam 2,5 jam juga menunjukan partikel memiliki kekristalan ZnO murni yang tinggi. Dapat
dibuktikan dengan menbandingkan Joint Committee on Powder
Diffraction Standards (JCPDS) 36-1451. Puncak peak yang dihasilkan oleh partikel dengan mode continous selama 2,5 j am dan mode pulse 3:1 selama 2,5 jam sama-sama berorientasi dengan JCPDS 36-1451
Hasil foto dari uji analisa Scanning Elektron Microscope
(SEM) partikel ZnO-Silika dengan perbandingan waktu penambahan sol silika ke dalam ZnO
Gambar 4.5 Hasil Analisa SEM partikel ZnO-silika (A) Continous mode 1 jam penambahan silika menit ke 15; (B) Continous mode 1 jam penambahan silika menit ke 45
Dari hasil uji analisa SEM pada gambar 4.5 memperlihatkan bahwa pada partikel ZnO-silika mode continous 1 jam dengan penambahan silika pada menit ke 15 t erlihat berbentuk gumpalan dari pada mode continous 1 jam dengan penambahan silika pada menit ke 45. Saat menit ke 15, sintesa ZnO belum terjadi sehingga ketika ditambahkan silika pembentukan ZnO menjadi terhambat oleh adanya silika. Sedangkan pada mode continous 1 jam dengan penambahan silika pada menit ke 45, sebagian ZnO sudah terbentuk sehingga jika
lihat morfologi kristalnya lebih kecil dari pada yang penambahan silika yang menit ke 15.
Hasil uji analisa X-Ray Diffraction (XRD) partikel
ZnO-Silika dengan perbandingan waktu penambahan sol silika ke dalam ZnO
Dari hasil XRD pada gambar 4.6 partikel ZnO-Silika pada mode continous 1 jam dengan penambahan silika menit ke 45 menunjukkan kristal ZnO lebih terlihat dari pada partikel ZnO-Silika mode continous 1 jam dengan penambahan silika menit ke
15 dan menit ke 30. Bila dibandingkan dengan Joint Committee
on Powder Diffraction Standards (JCPDS 36-1451) partikel ZnO-silika yang dihasilkan dari penambahan ZnO-silika menit ke 45 lebih mengorientasi ke JCPDS 36-1451 dari pada penambahan silika ke menit 15 maupun ke menit 30. P artikel yang dihasilkan dari penambahan silika menit ke 45 juga memiliki ke miripan dengan hasil XRD ZnO murni. Pada penambahan silika ke menit 45, proses pembentukan ZnO sudah terjadi sehingga silika yang sifatnya mengikat tidak menghambat laju pembentukan ZnO. Sedangkan pada penambahan silika ke menit 15 dan ke menit 30, pembentukan ZnO belum maksimal sehingga laju sintesa ZnO terhambat oleh adanya silika.
Pada pembuatan partikel ZnO-silika dari hasil XRD pada gambar 4.6 tidak terlihat peak dari krital silika yang terlihat hanya kristal dari ZnO murni saja. Kristal silika terbentuk atau terjadi
kalsinasi pada suhu 750oC, kurang dari suhu 750oC kristal silika
belum terbentuk dan masih berupa amorf. Jika dianalisa dengan XRD peak dari silika tidak terlihat karena pada proses pembuatan
ZnO-silika suhu yang digunakan hanya 70oC saja.
Partikel nanokomposit Zinc Silika dikalsinasi pada
500oC menunjukkan pola XRD mirip dengan sampel yang tidak
dikalsinasi yaitu sesuai dengan silika amorf. Sementara pola XRD
sampel dikalsinasi pada 750oC menunjukkan struktur kristal
10 15 20 25 30 35 40 45 50 55 60
Int
ens
ity
[a
.u]
2θ
Suhu 600oC Suhu 400o
C
Gambar 4.7 Hasil analisa XRD partikel silika
Gambar 4.7 menampilkan hasil analisa XRD untuk partikel
silika yang dihasilkan dengan suhu 600oC dan suhu 400oC.
Hasilnya menunjukan dari silika murni adalah amorf. Difraksi
puncak silika sekitar 2θ = 22o dapat dinyatakan untuk silika dalam
Hasil uji analisa Fourier-transform Infra Red ( FTIR) partikel ZnO murni dengan perbandingan waktu sonifikasi dengan mode continuous
4000 3500 3000 2500 2000 1500 1000 500
λ [cm-1
Gambar 4.8 Hasil Analisa FTIR partikel ZnO murni Continous mode 1 jam; Continous mode 1,5 jam; Continous mode 2 jam; Continous mode 2,5 jam
Zn
Mode continuous 1 jam Mode continuous 1,5 jam Mode continuous 2 jam
N=
N
Mode continuous 2,5 jam
Dari hasil FTIR pada gambar 4.8 untuk ZnO murni terlihat setiap lembah memiliki bentuk yang hampir sama baik variabel 1 jam, 1,5 jam 2 jam maupun 2,5 jam. Lamanya sonikasi pada pembuatan ZnO tidak mempengaruhi gugus fungsi dari partikel ZnO murni yang diperoleh.
Hasil uji analisa Fourier-transform Infra Red (F TIR) partikel ZnO-silika Continous mode 1 j am penambahan silika menit ke 15; Continous mode 1 jam penambahan silika menit ke 30; Continous mode 1 jam penambahan silika menit ke 45.
4000 3500 3000 2500 2000 1500 1000 500
λ [cm-1]
Gambar 4.9 Hasil Analisa FTIR partikel ZnO-silika Continous mode 1 jam penambahan silika menit ke 15; Continous mode 1 jam penambahan silika
menit ke 30; Continous mode 1 jam penambahan silika menit ke 45
Dari hasil analisa uji FTIR pada ambar 4.9 terlihat pada
range pita serapan antara 980-1190 cm-1 merupakan pita serapan
dari gugus fungsi Si-O-Si pada ZnO-silika yang ditambahankan ke menit 15 terlihat lembah dari gugus fungsi Si-O-Si yang jelas. Hal ini dikarenakan pada saat menit ke 15 sintesa ZnO belum terbentuk sehingga silika yang ditambahkan belum terkomposit dengan ZnO. Sedangkan pada ZnO-silika yang penambahan menit ke 30, lembah dari gugus fungsi Si-O-Si mulai mengecil sebab pada menit ke 30 sintesa ZnO sudah mulai terjadi meskipun belum maksimal kristal ZnO yang dihasilkan. Untuk pembuatan ZnO-silika yang penambahan silika pada menit ke 45, l embah dari gugus fungsi Si-O-Si mulai mengecil hal ini dikarenakan pada menit ke 45 pada pembuatan ZnO sudah terbentuk partikel ZnO sehingga silika yang ditambahkan sebagian sudah terkomposit dengn partikel ZnO.
Uji katalitik Methylen Blue tanpa katalis dengan pemaparan sinar matahari
Uji katalitik Methylen Blue untuk partikel nanokomposit ZnO-Silika dengan mode continuous 1 jam konsentrasi silika 0,1 M dibawah pemaparan sinar matahari
Gambar 4.11 Uji katalitik Methylen Blue + ZnO-Silika Uji katalitik Methylen Blue untuk partikel nanokomposit ZnO murni dengan mode continuous 1,5 jam dibawah pemaparan sinar matahari
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian dan pembahasan yang telah dikemukakan pada bab sebelumnya, maka dapat diambil kesimpulan sebagai berikut:
1. Partikel ZnO murni dapat dibuat dengan metode sonifikasi dengan mereaksikan ZnO(NO3)2 dalam aquadest dan
larutan ammonium hidroksida 25%.
2. Bentuk partikel yang dihasilkan dari sintesa ZnO murni dari ZnO(NO3)2 dengan mode continous maupun mode
pulse yaitu berbentuk batang.
3. Besar kecilnya morfologi partikel ZnO murni dipengaruhi oleh lamanya waktu pembuatan partikel terlihat pada hasil analisa SEM.
4. Waktu penambahan silika pada ZnO mempengaruhi bentuk morfologi dari partikel maupun kekristalan ZnO pada partikel ZnO-Silika yang dihasilkan.
5. ZnO-silika dapat mendegradasi warna dari methylen blue setelah dilakukan uji katalitik dengan pemaparan sinar matahari.
6. Lamanya waktu pemaparan sinar matahari pada uji katalitik mempengaruhi besarnya penurunan warna dari methylen blue.
7. Dari uji katalitik penurunan warna methylen blue yang paling besar adalah partikel ZnO murni bila dibandingkan dengan partikel ZnO-silika.
5.2 Saran
yang kurang optimal. Untuk menguranginya maka disarankan penelitian selanjutnya:
1. Memperbaiki kinerja alat dari eksperimen dengan mengkondisikan temperature pada ultrasonikator dengan menggunakan pendingin jaket.
2. Pembuatan partikel ZnO-Silika untuk penelitian selanjutnya mencoba menggunakan metode spray drayer sehingga diharapkan dapat menghasilkan partikel dengan karakterisasi yang berbeda dari sebelumnya.
3. Pembuatan ZnO-Silika nanokomposit dengan metode sonikasi sebaiknya dilakukan dengan variabel yang lebih bervariasi sehingga akan diperoleh hasil yang lebih baik. 4. Untuk penelitian selanjutnya, uji katalitik sebaiknya
LAMPIRAN
1. Pembuatan sol ZnO
Bahan yang digunakan:
• Bahan yang digunakan ini antara lain:Kristal Zn(NO3)2
• Larutan NH3
• Larutan Aquadest
Menentukan massa Zn(NO3)2 0,2 M yang dibutuhkan dalam
100 ml Aquadest:
𝑔𝑔𝑔𝑔= 𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑔𝑔
2. Pembuatan sol Silika
Bahan yang digunakan :
• Sodium Silicate MerckKGaA 64271 Darmstadt Germany 27%
• Aquadest
Menentukan volume Sodium Silicate 0,1 M yang dibutuhkan dalam100 ml aquadest :
𝑔𝑔𝑔𝑔= 𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑀𝑔𝑔
= 0,1 𝑀𝑀𝑀𝑀𝑀𝑀
= 0,6 𝑔𝑔𝑔𝑔
3. Pembuatanlarutan HCl 2 N
Bahan yang digunakan:
• HCL p.a
1 liter = 1,19 kg
Kandungan 37-38 %, diambil 37 %
• Aquadest
4. Pembuatan larutan KOH 0,1 M
Bahan yang digunakan :
• KOH Merck KGaA Darmstadt Germany 98%
• Aquadest
Menentukan massa KOH 0,1 M yang dibutuhkan dalam100 ml aquadest:
5. Data hasil uji katalitik
5.1 Tabel uji katalitik methylen blue tanpa katalis
750 0.047 0.047 0.047 0.043 0.044
5.2 Tabel uji katalitik methylen blue + ZnO murni
784 0.039 0.039 0.037 0.046 0.041
5.3 Tabel uji katalitik methylen blue + ZnO-Silika
760 0.011 0.025 0.028 0.026 0.027
762 0.011 0.025 0.029 0.025 0.027
764 0.011 0.025 0.029 0.024 0.028
766 0.011 0.025 0.028 0.025 0.027
768 0.01 0.026 0.028 0.025 0.027
770 0.012 0.025 0.028 0.024 0.027
772 0.012 0.025 0.028 0.024 0.026
774 0.011 0.025 0.029 0.024 0.026
776 0.011 0.026 0.028 0.024 0.027
778 0.011 0.025 0.028 0.025 0.027
780 0.01 0.026 0.027 0.024 0.028
782 0.009 0.025 0.028 0.024 0.027
784 0.01 0.024 0.029 0.025 0.026
786 0.011 0.025 0.027 0.024 0.028
788 0.01 0.025 0.028 0.024 0.026
790 0.011 0.025 0.028 0.024 0.027
792 0.011 0.025 0.028 0.024 0.027
794 0.012 0.024 0.027 0.023 0.026
796 0.011 0.024 0.027 0.024 0.027
798 0.012 0.024 0.027 0.024 0.026


2](https://thumb-ap.123doks.com/thumbv2/123dok/1815732.2100403/30.420.49.373.91.512/gambar-skema-pembuatan-larutan-zn-nh-no.webp)