PENETAPAN KADAR CAMPURAN PARASETAMOL,
PROPIFENAZON DAN KAFEIN DARI SEDIAAN
TABLET DENGAN METODE KROMATOGRAFI
LAPIS TIPIS (KLT) DENSITOMETRI
SKRIPSI
OLEH:
NERDY
NIM . 071501032
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENETAPAN KADAR CAMPURAN PARASETAMOL,
PROPIFENAZON DAN KAFEIN DARI SEDIAAN
TABLET DENGAN METODE KROMATOGRAFI
LAPIS TIPIS (KLT) DENSITOMETRI
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk
Mencapai Gelar Sarjana Farmasi pada
Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
NERDY
NIM . 071501032
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PENETAPAN KADAR CAMPURAN PARASETAMOL, PROPIFENAZON DAN KAFEIN DARI SEDIAAN TABLET DENGAN METODE
KROMATOGRAFI LAPIS TIPIS (KLT) DENSITOMETRI OLEH:
NERDY NIM 071501032
Dipertahankan di hadapan Panitia Penguji Fakultas Farmasi
Universitas Sumatera Utara Pada tanggal: Januari 2011
Pembimbing I, Panitia Penguji,
(Prof. Dr. rer. nat. Effendy De Lux Putra, SU., Apt.) (Dr. Ginda Haro, M.Sc., Apt.)
NIP . 195306191983031001 NIP . 195108161980031002
Pembimbing II,
(Prof. Dr. rer. nat. Effendy De Lux Putra, SU., Apt.) NIP . 195306191983031001
(Drs. Muchlisyam, M.Si., Apt.) NIP . 195006221980021001
(Dra. Salbiah, M.Si., Apt.) NIP . 194810031987012001
(Drs. Fathur Rahman Harun, M.Si., Apt.) NIP . 195201041980031002
Medan, Januari 2011 Fakultas Farmasi Universitas Sumatera Utara
Dekan,
KATA PENGANTAR
Puji dan syukur ke hadirat Tuhan Yang Maha Esa yang telah melimpahkan rahmat, hidayah dan kemudahan kepada penulis sehingga dapat menyelesaikan penelitian dan penyusunan skripsi yang berjudul “PENETAPAN KADAR CAMPURAN PARASETAMOL, PROPIFENAZON DAN KAFEIN DARI SEDIAAN TABLET DENGAN METODE KROMATOGRAFI LAPIS TIPIS (KLT) DENSITOMETRI” sebagai salah satu syarat untuk mencapai gelar Sarjana Farmasi di Fakultas Farmasi Universitas Sumatera Utara.
Kromatografi Lapis Tipis (KLT) Densitometri merupakan metode yang dapat digunakan untuk penetapan kadar campuran senyawa kimia. Tujuan penelitian ini adalah untuk menetapkan kadar campuran parasetamol, propifenazon dan kafein dalam tablet. Kombinasi obat ini digunakan untuk
penanganan rasa nyeri (analgetika). Hendaknya hasil penelitian ini menjadi masukan kepada industri obat tentang penetapan kadar campuran parasetamol, propifenazon dan kafein dalam tablet secara Kromatografi Lapis Tipis (KLT) Densitometri.
Pada kesempatan ini penulis menyampaikan rasa hormat dan terima kasih yang sebesar – besarnya kepada Bapak Prof. Dr. rer. nat. Effendy De Lux Putra, SU., Apt. dan Bapak Drs. Muchlisyam, M.Si., Apt. yang telah membimbing dengan penuh kesabaran, tulus dan ikhlas selama penelitian dan penulisan skripsi ini berlangsung. Ucapan terima kasih juga disampaikan kepada Dekan Fakultas Farmasi Universitas Sumatera Utara, Prof. Dr. Sumadio Hadisahputra, Apt. yang telah memberikan bantuan dan fasilitas selama masa pendidikan.
Penulis juga tidak lupa mengucapkan terima kasih dan penghargaan yang tulus kepada kedua orang tua dan abang penulis yang tercinta atas doa, dorongan dan pengorbanan baik moril maupun materil dalam penyelesaian skripsi ini.
Medan, Januari 2011 Penulis,
PENETAPAN KADAR CAMPURAN PARASETAMOL,
PROPIFENAZON DAN KAFEIN DARI SEDIAAN
TABLET DENGAN METODE KROMATOGRAFI
LAPIS TIPIS (KLT) DENSITOMETRI
ABSTRAKObat dalam bentuk kombinasi sering digunakan untuk mengobati berbagai penyakit, termasuk diantaranya rasa nyeri dan demam. Kombinasi Parasetamol, Propifenazon dan Kafein merupakan kombinasi untuk penanganan rasa nyeri (analgetika) dan demam (antipiretika) yang terdiri dari derivat para amino fenol Parasetamol, derivat pirazolinon Propifenazon dan derivat xantin Kafein. Kombinasi dua atau lebih analgetika sering kali digunakan, karena terjadi efek potensiasi.
Analisis campuran Parasetamol, Propifenazon dan Kafein dari sediaan tablet secara simultan dapat dilakukan dengan metode Kromatografi Lapis Tipis Densitometri. Pendeteksian dengan menggunakan detektor Ultra Violet/Visible pada panjang gelombang 260 nm dengan terlebih dahulu dilakukan pemisahan dengan Kromatografi Lapis Tipis (KLT) fase diam Silika Gel 60 F254 (E.Merck) dan fase gerak kloroform : aseton : amonium hidroksida 25% (8 : 2 : 0,1). Harga Rf yang diperoleh untuk Parasetamol, Propifenazon dan Kafein secara berturut-turut adalah 0,27; 0,74 dan 0,51.
Penentuan linieritas kurva kalibrasi, untuk Parasetamol dengan koefisien korelasi, r = 0,9999 dan persamaan regresi, y = 1647,0932x + 311,1138; dan untuk Propifenazon dengan koefisien korelasi, r = 0,9999 dan persamaan regresi, y = 830,9619x + 76,4238; serta untuk Kafein dengan koefisien korelasi, r = 0,9999 dan persamaan regresi, y = 906,7000x + 24,8893. Hasil penetapan kadar tablet campuran Parasetamol, Propifenazon dan Kafein yang dianalisis memenuhi persyaratan untuk tablet secara umum yakni mengandung tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket.
Uji akurasi diperoleh % perolehan kembali rata - rata untuk Parasetamol, Propifenazon dan Kafein secara berturut - turut adalah 100,2112%; 100,5551% dan 100,0251%. Untuk uji presisi diperoleh nilai RSD untuk Parasetamol, Propifenazon dan Kafein secara berturut - turut adalah 0,3767%; 0,2740% dan 0,4942%. Batas deteksi untuk Parasetamol, Propifenazon dan Kafein berturut – turut adalah 0,8023 μg; 0,3854 μg dan 0,1134 μg, sedangkan batas kuantitasi untuk Parasetamol, Propifenazon dan Kafein berturut – turut adalah 2,4312 μg; 1,1680 μg dan 0,3438 μg. Maka dari hasil yang diperoleh ini dapat disimpulkan bahwa metode yang digunakan dalam penelitian ini mempunyai akurasi dan presisi yang memenuhi syarat.
DETERMINATION OF MIXTURE OF
PARACETAMOL, PROPYPHENAZONE AND
CAFFEINE FROM TABLETS WITH THIN LAYER
CHROMATOGRAPHY (TLC) DENSITOMETRY
METHOD
ABSTRACT
Drug in combination is often used to treat various illnesses, including pain and fever. Combination of Paracetamol, Propyphenazone and Caffeine is a combination for the treatment of pain (analgesic) and fever (antipiretic) consisting of the amino phenol derivatives Paracetamol, pirazolinon derivatives Propyphenazone and xanthine derivatives Caffeine. The combination of two or more analgesic often used, because there was potentiation effect.
Analysis of a mixture of Paracetamol, Propyphenazone and Caffeine of tablets can be performed with Thin Layer Chromatography (TLC) Densitometry method. Detection using the Ultra Violet / Visible detector at a wavelength of 260 nm by first separated by Thin Layer Chromatography (TLC) stationary phase Silica Gel 60 F254 (E. Merck) and mobile phase chloroform : acetone : ammonium hydroxide 25% (8: 2: 0,1). Rf value obtained for Paracetamol, Propyphenazone and Caffeine respectively are 0,27; 0,74 and 0,51.
Determination linearity by calibration curves, for Paracetamol with correlation coefficient, r = 0,9999 and regression equation, y = 1647,0932x + 311,1138; and to Propyphenazone with correlation coefficient, r = 0,9999 and regression equation, y = 830,9619x + 76,4238; as well as to Caffeine with a correlation coefficient, r = 0,9999 and regression equation, y = 906,7000x + 24,8893. Results tablets determination of tablets mixture Paracetamol, Propyphenazone and Caffeine were analyzed meet the requirements for general tablets which contain not less than 90,0% and not more than 110% of the amount indicated on the label.
Accuracy test obtained average % recovery for Paracetamol, Propyphenazone and Caffeine respectively also is 100,2112%; 100,5551% and 100,0251%. For precision test obtained RSD values for Paracetamol, Propyphenazone and Caffeine respectively were of 0,3767%; 0,2740% and 0,4942%. Limits of detection for Paracetamol, Propyphenazone and Caffeine respectively were of 0,8023 μg; 0,3854 μg and 0,1134 μg, while the limit of quantitation for Paracetamol, Propyphenazone and Caffeine respectively were of 2,4312 μg; 1,1680 μg and 0,3438 μg. So from the results obtained it can be concluded that the method used in this study have accuracy and precision are eligible.
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... v
ABSTRACT ... vi
DAFTAR ISI ... vii
DAFTAR TABEL ... x
DAFTAR GAMBAR ... xi
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 2
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
BAB III METODOLOGI PENELITIAN ... 15
3.1 Alat ... 15
3.2 Bahan ... 15
3.3 Pengambilan Sampel ... 16
3.4 Prosedur Penelitian... 16
3.4.1 Penyiapan Bahan ... 16
3.4.1.1 Pembuatan fase gerak Kloroform : Aseton : Amonium Hidroksida 25% (8:2:0,1) ... 16
3.4.1.2 Pelarut ... 16
3.4.1.3 Pembuatan Larutan Induk Baku Parasetamol ... 16
3.4.1.4 Pembuatan Larutan Induk Baku Propifenazon ... 16
3.4.1.5 Pembuatan Larutan Induk Baku Kafein ... 17
3.4.2.1 Identifikasi Baku Parasetamol, Propifenazon dan
Kafein dengan Spektrofotometer InfraMerah ... 17
3.4.2.2 Penentuan Panjang Gelombang Optimum ... 17
3.4.2.3 Penyiapan Plat Kromatografi Lapis Tipis (KLT) 18 3.4.2.4 Penyiapan Alat Automatic Development Chamber ... 18
3.4.2.5 Penyiapan Alat Densitometer ... 18
3.4.2.6 Analisa Kualitatif ... 19
3.4.2.7 Analisa Kuantitatif ... 19
3.4.2.7.1 Penentuan Linieritas Kurva Kalibrasi Parasetamol, Propifenazon dan Kafein 19
3.4.2.7.2 Penetapan Kadar Parasetamol, Propifenazon dan Kafein dalam Sampel ... 19
3.4.2.7 Analisa Secara Statistik... 20
3.4.3 Metode Validasi ... 21
3.4.3.1 Akurasi (Kecermatan) ... 21
3.4.3.2 Presisi (Keseksamaan) ... 22
3.4.3.3 Batas Deteksi dan Batas Kuantitasi ... 22
BAB IV HASIL DAN PEMBAHASAN ... 24
4.1 Identifikasi Baku Parasetamol, Propifenazon dan Kafein dengan Spektrofotometer InfraMerah ... 24
4.2 Penentuan Panjang Gelombang Optimum... 30
4.3 Analisa Kualitatif Parasetamol, Propifenazon dan Kafein dengan Menggunakan Kromatografi Lapis Tipis (KLT) Densitometri ... 34
4.4 Penentuan Linearitas Kurva Kalibrasi... 37
4.4.1 Penentuan Linearitas Kurva Kalibrasi Parasetamol ... 37
4.4.2 Penentuan Linearitas Kurva Kalibrasi Propifenazon ... 38
4.4.2 Penentuan Linearitas Kurva Kalibrasi Kafein ... 39
4.5 Penetapan Kadar Sampel ... 40
4.6 Hasil Uji Validasi ... 41
BAB V KESIMPULAN DAN SARAN ... 45
5.1 Kesimpulan ... 45
PENETAPAN KADAR CAMPURAN PARASETAMOL,
PROPIFENAZON DAN KAFEIN DARI SEDIAAN
TABLET DENGAN METODE KROMATOGRAFI
LAPIS TIPIS (KLT) DENSITOMETRI
ABSTRAKObat dalam bentuk kombinasi sering digunakan untuk mengobati berbagai penyakit, termasuk diantaranya rasa nyeri dan demam. Kombinasi Parasetamol, Propifenazon dan Kafein merupakan kombinasi untuk penanganan rasa nyeri (analgetika) dan demam (antipiretika) yang terdiri dari derivat para amino fenol Parasetamol, derivat pirazolinon Propifenazon dan derivat xantin Kafein. Kombinasi dua atau lebih analgetika sering kali digunakan, karena terjadi efek potensiasi.
Analisis campuran Parasetamol, Propifenazon dan Kafein dari sediaan tablet secara simultan dapat dilakukan dengan metode Kromatografi Lapis Tipis Densitometri. Pendeteksian dengan menggunakan detektor Ultra Violet/Visible pada panjang gelombang 260 nm dengan terlebih dahulu dilakukan pemisahan dengan Kromatografi Lapis Tipis (KLT) fase diam Silika Gel 60 F254 (E.Merck) dan fase gerak kloroform : aseton : amonium hidroksida 25% (8 : 2 : 0,1). Harga Rf yang diperoleh untuk Parasetamol, Propifenazon dan Kafein secara berturut-turut adalah 0,27; 0,74 dan 0,51.
Penentuan linieritas kurva kalibrasi, untuk Parasetamol dengan koefisien korelasi, r = 0,9999 dan persamaan regresi, y = 1647,0932x + 311,1138; dan untuk Propifenazon dengan koefisien korelasi, r = 0,9999 dan persamaan regresi, y = 830,9619x + 76,4238; serta untuk Kafein dengan koefisien korelasi, r = 0,9999 dan persamaan regresi, y = 906,7000x + 24,8893. Hasil penetapan kadar tablet campuran Parasetamol, Propifenazon dan Kafein yang dianalisis memenuhi persyaratan untuk tablet secara umum yakni mengandung tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket.
Uji akurasi diperoleh % perolehan kembali rata - rata untuk Parasetamol, Propifenazon dan Kafein secara berturut - turut adalah 100,2112%; 100,5551% dan 100,0251%. Untuk uji presisi diperoleh nilai RSD untuk Parasetamol, Propifenazon dan Kafein secara berturut - turut adalah 0,3767%; 0,2740% dan 0,4942%. Batas deteksi untuk Parasetamol, Propifenazon dan Kafein berturut – turut adalah 0,8023 μg; 0,3854 μg dan 0,1134 μg, sedangkan batas kuantitasi untuk Parasetamol, Propifenazon dan Kafein berturut – turut adalah 2,4312 μg; 1,1680 μg dan 0,3438 μg. Maka dari hasil yang diperoleh ini dapat disimpulkan bahwa metode yang digunakan dalam penelitian ini mempunyai akurasi dan presisi yang memenuhi syarat.
DETERMINATION OF MIXTURE OF
PARACETAMOL, PROPYPHENAZONE AND
CAFFEINE FROM TABLETS WITH THIN LAYER
CHROMATOGRAPHY (TLC) DENSITOMETRY
METHOD
ABSTRACT
Drug in combination is often used to treat various illnesses, including pain and fever. Combination of Paracetamol, Propyphenazone and Caffeine is a combination for the treatment of pain (analgesic) and fever (antipiretic) consisting of the amino phenol derivatives Paracetamol, pirazolinon derivatives Propyphenazone and xanthine derivatives Caffeine. The combination of two or more analgesic often used, because there was potentiation effect.
Analysis of a mixture of Paracetamol, Propyphenazone and Caffeine of tablets can be performed with Thin Layer Chromatography (TLC) Densitometry method. Detection using the Ultra Violet / Visible detector at a wavelength of 260 nm by first separated by Thin Layer Chromatography (TLC) stationary phase Silica Gel 60 F254 (E. Merck) and mobile phase chloroform : acetone : ammonium hydroxide 25% (8: 2: 0,1). Rf value obtained for Paracetamol, Propyphenazone and Caffeine respectively are 0,27; 0,74 and 0,51.
Determination linearity by calibration curves, for Paracetamol with correlation coefficient, r = 0,9999 and regression equation, y = 1647,0932x + 311,1138; and to Propyphenazone with correlation coefficient, r = 0,9999 and regression equation, y = 830,9619x + 76,4238; as well as to Caffeine with a correlation coefficient, r = 0,9999 and regression equation, y = 906,7000x + 24,8893. Results tablets determination of tablets mixture Paracetamol, Propyphenazone and Caffeine were analyzed meet the requirements for general tablets which contain not less than 90,0% and not more than 110% of the amount indicated on the label.
Accuracy test obtained average % recovery for Paracetamol, Propyphenazone and Caffeine respectively also is 100,2112%; 100,5551% and 100,0251%. For precision test obtained RSD values for Paracetamol, Propyphenazone and Caffeine respectively were of 0,3767%; 0,2740% and 0,4942%. Limits of detection for Paracetamol, Propyphenazone and Caffeine respectively were of 0,8023 μg; 0,3854 μg and 0,1134 μg, while the limit of quantitation for Paracetamol, Propyphenazone and Caffeine respectively were of 2,4312 μg; 1,1680 μg and 0,3438 μg. So from the results obtained it can be concluded that the method used in this study have accuracy and precision are eligible.
BAB I PENDAHULUAN
1.1 Latar belakang
Parasetamol dan Propifenazon merupakan obat yang secara luas digunakan
dalam penanganan rasa nyeri (analgetika) dan demam (antipiretika). Kafein sering
dikombinasikan dengan Parasetamol dan Propifenazon untuk memperkuat efek
analgetikanya melalui mekanisme vasokonstriktif guna untuk mengobati nyeri
kepala. Karena terjadi efek potensiasi, maka dosis masing – masing komponennya
diturunkan sehingga efek samping dapat dikurangi (Tan & Rahardja, 2007).
Banyak sekali keuntungan penggunaan Kromatografi Lapis Tipis (KLT)
dan salah satu keuntungan utamanya adalah mampu memisahkan beberapa sampel
secara bersamaan, yang lebih menguntungkan dibandingkan Kromatografi Cair
Kinerja Tinggi (KCKT) (Watson, 2009).
Densitometri merupakan metode analisis instrumental yang didasarkan
pada interaksi radiasi elektromagnetik dengan analit yang merupakan bercak pada
Kromatografi Lapis Tipis (KLT). Densitometri dimaksudkan untuk analisis
kuantitatif analit dengan kadar kecil, yang sebelumnya dilakukan pemisahan
dengan Kromatografi Lapis Tipis (KLT) (Rohman, 2009).
Menurut Undang – Undang Republik Indonesia Nomor : 36 Tahun 2009
Tentang Kesehatan Pasal 105 Ayat 1 bahwa sediaan farmasi yang berupa obat dan
bahan baku obat harus memenuhi syarat Farmakope Indonesia atau buku standar
Berdasarkan hal tersebut diatas, penulis tertarik untuk melakukan
penetapan kadar campuran Parasetamol, Propifenazon dan Kafein dari sediaan
tablet yang beredar di pasaran menggunakan densitometer yang sebelumnya
dilakukan pemisahan menggunakan Kromatografi Lapis Tipis (KLT) dengan fase
diam Silika Gel 60 F254 (E.Merck) dan fase gerak kloroform : aseton : amonium
hidroksida 25% (8 : 2 : 0,1) (Dimitrovska, et al., 1993). Hasil yang diperoleh
dibandingkan dengan persyaratan kadar untuk tablet secara umum yakni
mengandung tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah
yang tertera pada etiket.
Untuk menguji validitas dari metode ini dilakukan pengujian antara lain
uji akurasi dengan parameter % perolehan kembali, uji presisi dengan parameter
simpangan baku relatif (RSD) dan batas deteksi serta batas kuantiasi (Rohman,
2009).
1.2 Perumusan Masalah
1. Apakah hasil penetapan kadar dari tablet yang mengandung campuran
Parasetamol, Propifenazon dan Kafein secara simultan dengan metode
Kromatografi Lapis Tipis (KLT) Densitometri memenuhi persyaratan
kadar untuk tablet secara umum?
2. Apakah metode Kromatografi Lapis Tipis (KLT) Densitometri yang
digunakan untuk penetapan kadar campuran Parasetamol, Propifenazon
dan Kafein dari sediaan tablet secara simultan dapat memenuhi
1.3 Hipotesis
1. Hasil penetapan kadar dari tablet yang mengandung campuran
Parasetamol, Propifenazon dan Kafein secara simultan dengan metode
Kromatografi Lapis Tipis (KLT) Densitometri memenuhi persyaratan
kadar untuk tablet secara umum.
2. Metode Kromatografi Lapis Tipis (KLT) Densitometri yang digunakan
untuk penetapan kadar campuran Parasetamol, Propifenazon dan Kafein
dari sediaan tablet secara simultan dapat memenuhi persyaratan uji
validasi.
1.4 Tujuan Penelitian
1. Mengetahui kesesuaian kadar tablet yang mengandung campuran
Parasetamol, Propifenazon dan Kafein yang ditentukan secara simultan
dengan metode Kromatografi Lapis Tipis (KLT) Densitometri terhadap
persyaratan kadar untuk tablet secara umum.
2. Menentukan validitas metode Kromatografi Lapis Tipis (KLT)
Densitometri yang digunakan untuk penetapan kadar campuran
Parasetamol, Propifenazon dan Kafein dari sediaan tablet secara simultan.
1.5 Manfaat Penelitian
Diharapkan metode Kromatografi Lapis Tipis (KLT) Densitometri dapat
digunakan sebagai metode alternatif pada industri farmasi dan BPOM untuk
penetapan kadar campuran Parasetamol, Propifenazon dan Kafein dari sediaan
BAB II
TINJAUAN PUSTAKA
3.1Parasetamol, Propifenazon dan Kafein
Parasetamol dan Propifenazon merupakan obat yang secara luas digunakan
dalam penanganan rasa nyeri (analgetika) dan demam (antipiretika). Kafein sering
dikombinasikan dengan Parasetamol dan Propifenazon untuk memperkuat efek
analgetikanya melalui mekanisme vasokonstriktif guna untuk mengobati nyeri
kepala. Karena terjadi efek potensiasi, maka dosis masing – masing komponennya
diturunkan sehingga efek samping dapat dikurangi (Tan & Rahardja, 2007).
Efek samping yang paling umum dari penggunaan analgetika adalah
gangguan lambung (Salisilat, Obat Analgetik Non Steroid dan Derivat
Pirazolinon), kerusakan darah (Parasetamol, Salisilat dan Derivat Antranilat),
kerusakan hati dan ginjal (Parasetamol dan Derivat Antranilat) dan juga reaksi
alergi kulit. Efek samping ini terjadi pada penggunaan dalam jangka waktu yang
lama atau penggunaan dalam dosis yang tinggi. Oleh karena itu penggunaan
analgetika secara kontinu tidak dianjurkan (Tan & Rahardja, 2007).
3.1.1 Parasetamol
Parasetamol memiliki rumus molekul C8H9NO2 dengan berat molekul
151,16. Pemeriannya berupa serbuk hablur, putih, tidak berbau dan rasa sedikit
pahit. Senyawa ini larut dalam air mendidih, dan dalam natrium hidroksida 1 N,
mudah larut dalam etanol (Depkes RI, 1995).
Parasetamol memiliki khasiat analgetis antipiretis tanpa aktivitas
dianggap sebagai zat penghilang rasa nyeri (analgetika) yang paling aman. Efek
analgetisnya dapat diperkuat oleh Kafein hingga 50%. Dalam hati zat ini
diuraikan menjadi metabolit toksis sebagai konjugat glukoronida sulfida. Pada
dosis tinggi mengakibatkan nekrosis hati yang tidak reversibel. Dosis yang
berlebihan (Overdose) dapat menimbulkan mual dan muntah (Tan & Rahardja,
2007).
Gambar 1. Rumus Bangun Parasetamol 3.1.2 Propifenazon
Propifenazon memiliki rumus molekul C14H18N2O dengan berat molekul
230,3. Pemeriannya berupa kristal putih atau serbuk kristal putih. Senyawa ini
sangat mudah larut dalam etanol dan kloroform, larut dalam eter, larut dalam 400
bagian air (Moffat, et al., 2004).
Propifenazon tidak memiliki khasiat anti radang, memiliki waktu paruh
( ) 90 menit dan memiliki resiko agranulositosis yang lebih rendah
dibandingkan induknya fenazon. Umumnya dalam bentuk kombinasi dengan
Gambar 2. Rumus Bangun Propifenazon 3.1.3 Kafein
Kafein memiliki rumus molekul C8H10N4O2 dengan berat molekul 194,19
(Kafein Anhidrat), 212,21 (Kafein Monohidrat). Pemeriannya berupa serbuk putih
atau bentuk jarum mengkilat putih, biasanya menggumpal, tidak berbau, rasa
pahit. Larutan bersifat netral terhadap kertas lakmus. Senyawa ini agak sukar larut
dalam air, dalam etanol, mudah larut dalam klororform, sukar larut dalam eter
(Depkes RI, 1995).
Gambar 3. Rumus Bangun Kafein 3.2 Kromatografi Lapis Tipis (KLT)
Kromatografi Lapis Tipis (KLT) bersama – sama dengan berbagai macam
variasinya pada umumnya dirujuk sebagai kromatografi planar. Pada kromatografi
lapis tipis, fase diamnya berupa lapisan yang seragam (uniform) pada permukaan
bidang datar yang didukung oleh lempeng kaca, plat aluminium atau plat plastik.
Meskipun demikian kromatografi planar ini dapat dikatakan sebagai bentuk
Banyak tahapan pada prosedur Kromatografi Lapis Tipis yang telah dapat
diinstrumentasikan, dengan tujuan mengurangi pekerjaan, menghasilkan data
yang mempunyai tingkat reprodusibilitas dan kuantitasi, serta dapat ditangani
dengan sistem data yang modern (Miller, 2005).
3.2.1 Penjerap (Fase Diam)
Penjerap yang paling sering digunakan pada Kromatografi Lapis Tipis
adalah silika gel dan serbuk selulosa, sementara mekanisme sorpsi – desorpsi
(suatu mekanisme perpindahan solut dari fase diam ke fase gerak atau sebaliknya)
yang utama pada Kromatografi Lapis Tipis adalah partisi dan adsorbsi (Rohman,
2009).
Jarak migrasi senyawa pada plat silika gel tergantung pada polaritasnya.
Senyawa yang paling polar bergerak naik dengan jarak paling dekat dari titik awal
penotolan, sedangkan senyawa dengan polaritas paling kecil bergerak paling jauh
dari titik awal penotolan tersebut. Silika gel merupakan penjerap polar yang
paling sering digunakan, meskipun demikian silika gel juga banyak dijumpai
dalam bentuk yang termodifikasi (Watson, 2009).
Untuk membantu visualisasi maka selama proses pembuatan plat
Kromatografi Lapis Tipis ditambahkan zat yang berfluorosensi. Secara umum plat
Kromatografi Lapis Tipis yang telah didesain dengan penambahan zat yang
berfluorosensi dapat diamati dibawah sinar ultraviolet. Sebagian besar analit akan
tampil sebagai bercak yang berwarna gelap dengan dasar yang dapat
berfluorosensi. Sebelum digunakan plat Kromatografi Lapis Tipis biasanya
diaktifkan dengan pemanasan pada suhu diatas 100OC selama kurang lebih
pada plat Kromatografi Lapis Tipis (KLT). Plat Kromatografi Lapis Tipis (KLT)
yang telah kering biasanya disimpan dalam desikator untuk menjaga agar tetap
kering dan bersih (Miller, 2005).
Gambar 4. Permukaan Silika Gel
3.2.2 Fase Gerak
Fase gerak pada Kromatografi Lapis Tipis (KLT) dipilih dari pustaka,
sistem yang paling sederhana adalah dengan menggunakan campuran 2 pelarut
organik sehingga pemisahan dapat terjadi secara optimal. Pada saat pemilihan fase
gerak, maka fase gerak harus mempunyai kemurnian yang sangat tinggi karena
Kromatografi Lapis Tipis (KLT) merupakan teknik pemisahan yang sangat
sensitif. Daya elusi dari fase gerak yang dipilih harus dapat memberikan harga Rf
analit diantara 0,2 – 0,8 guna untuk memaksimalkan pemisahan. Untuk pemisahan
dengan menggunakan Kromatografi Lapis Tipis (KLT), maka polaritas fase gerak
akan menentukan nilai Rf dari analit (Rohman, 2009).
Semakin polar suatu pelarut atau campuran pelarut maka akan semakin
jauh pelarut tersebut menggerakkan senyawa polar naik dari titik awal penotolan.
yang nyata dalam jarak migrasi dengan peningkatan polaritas pada fase gerak
(Watson, 2009).
3.2.3 Aplikasi Sampel (Penotolan Sampel)
Untuk tujuan kuantitasi, tidak hanya harus menjaga area sampel yang
kecil, tetapi volume sampel yang diaplikasikan kepada plat harus diketahui secara
akurat. Penotol sampel secara mekanik dapat diperoleh secara komersil dan dapat
menotolkan sejumlah tertentu sampel secara akurat pada posisi yang telah
ditentukan (Miller, 2005).
3.2.4 Pengembangan
Pengembangan pelarut biasanya dilakukan dengan cara menaik
(ascending), yang mana ujung lempeng dicelupkan ke dalam pelarut pengembang.
Untuk menghasilkan reprodusibilitas kromatografi yang baik, wadah fase gerak
harus dijenuhkan dengan uap fase gerak (Rohman, 2009).
Plat dicelupkan dalam fase gerak yang dipilih kira – kira 0,5 cm. Bejana
diusahakan jangan sampai bocor. Untuk meyakinkan bahwa bejana kromatografi
telah jenuh, maka dinding dalam bejana dapat dilapisi dengan lembaran kertas
saring yang ujungnya direndam dalam fase gerak (Sastrohamidjojo, 1985).
3.2.5 Deteksi
Bercak pemisahan pada Kromatografi Lapis Tipis umumya merupakan
bercak yang tidak berwarna. Untuk penentuannya dilakukan secara kimia maupun
fisika. Cara kimia yang biasanya digunakan adalah dengan mereaksikan bercak
dengan suatu pereaksi melalui cara penyemprotan sehingga bercak akan tampak
secara jelas. Cara fisika yang digunakan untuk menampakkan bercak adalah
berfluorosensi, maka akan membuat bercak terlihat lebih jelas. Jika senyawa tidak
dapat berfluorosensi maka fase diam yang akan ditambahkan zat yang dapat
berfluorosensi, dengan demikian bercak akan kelihatan gelap karena menyerap
sinar ultraviolet sedangkan latar belakangnya akan terlihat berflourosensi.
Cara kimiawi mendeteksi bercak anatara lainnya:
• Menyemprot lempeng Kromatografi Lapis Tipis dengan reagen yang kromogenik
yang akan bereaksi secara kimia dengan seluruh solut yang mengandung gugus
fungsional tertentu sehingga bercak menjadi berwarna. Kadang – kadang
dipanaskan terlebih dahulu untuk mempercepat reaksi pembentukan warna dan
meningkatkan intensitas warna bercak.
• Melakukan scanning pada permukaan lempeng dengan densitometer, suatu
instrumen yang dapat mengukur intensitas radiasi yang direfleksikan dari
pernukaan lempeng ketika disinari dengan lampu ultraviolet atau lampu sinar
tampak. Solut – solut yang mampu menyerap radiasi sinar akan dicatat sebagai
puncak (peak) dalam pencatat (recorder) (Rohman, 2009).
3.2.6 Densitometri
Densitometri merupakan metode analisis instrumental yang mendasarkan
pada interaksi radiasi elektromagnetik dengan analit yang merupakan bercak pada
plat Kromatografi Lapis Tipis. Densitometri lebih dititikberatkan untuk analisis
kuantitatif analit – analit, yang mana diperlukan pemisahan terlebih dahulu
dengan Kromatografi Lapis Tipis. Untuk mengevaluasi bercak hasil Kromatografi
Lapis Tipis secara densitometri, bercak di-scanning dengan sumber sinar dalam
bentuk celah (slit). Sinar yang dipantulkan diukur dengan sensor cahaya
daerah yang mengandung bercak dihubungkan dengan banyaknya analit yang ada
melalui kurva kalibrasi yang telah disiapkan.
3.3 Validasi Metode
Validasi metode adalah suatu proses yang menunjukkan bahwa prosedur
analitik telah sesuai dengan penggunaan yang dikehendaki. Proses validasi
metode untuk prosedur analitik dimulai dengan pengumpulan data validasi oleh
pelaksana guna mendukung prosedur analitiknya (Bliesner, 2006). Validasi
merupakan persyaratan mendasar yang diperlukan untuk menjamin kualitas dan
reabilitas hasil dari semua aplikasi analitik (Ermer, 2005). Hasil validasi metode
dapat digunakan untuk memutuskan kualitas, reabilitas dan konsistensi dari hasil
analitik (Huber, 2007). Adapun karakteristik dalam validasi metode menurut USP
(United States Pharmacopeia) XXX yaitu akurasi / kecermatan, presisi /
keseksamaan, spesifisitas, batas deteksi, batas kuantitasi, linieritas, rentang dan
kekuatan / ketahanan.
3.3.1 Akurasi (Kecermatan)
Akurasi/kecermatan adalah kedekatan antara nilai hasil uji yang diperoleh
lewat metode analitik dengan nilai sebenarnya. Akurasi dinyatakan dalam persen
perolehan kembali (% recovery) Akurasi dapat ditentukan dengan dua metode,
yakni placebo recovery dan standard addition method. Pada
spiked-placebo recovery atau metode simulasi, analit murni ditambahkan (spiked) ke
dalam campuran bahan pembawa sediaan farmasi, lalu campuran tersebut
dianalisis dan jumlah analit hasil analisis dibandingkan dengan jumlah analit
maka sejumlah analit yang telah diketahui konsentrasinya dapat ditambahkan
langsung ke dalam sediaan farmasi otentik. Metode ini dinamakan standard
addition method atau metode penambahan baku. (USP XXX, 2007; Ermer, 2005;
Harmita, 2004).
3.3.2 Presisi (Keseksamaan)
Presisi/keseksamaan adalah ukuran keterulangan metode analitik,
termasuk di antaranya kemampuan instrumen dalam memberikan hasil analitik
yang reprodusibel. Berdasarkan rekomendasi ICH (the International Conference
on the Harmonisation), karakteristik presisi dilakukan pada 3 tingkatan, yakni
keterulangan (repeatability), presisi antara (intermediate precision) dan
reprodusibilitas (reproducibility). Keterulangan dilakukan dengan cara
menganalisis sampel yang sama oleh analis yang sama menggunakan instrumen
yang sama dalam periode waktu singkat. Presisi antara dikerjakan oleh analis
yang berbeda. Sedangkan reprodusibilitas dikerjakan oleh analis yang berbeda dan
di laboratorium yang berbeda (USP XXX, 2007; Épshtein, 2004).
3.3.3 Spesifisitas
Spesifisitas adalah kemampuan untuk mengukur analit yang dituju secara
tepat dan spesifik dengan adanya komponen lain dalam matriks sampel seperti
ketidakmurnian, produk degradatif dan komponen matriks. Secara umum,
spesifisitas dapat ditunjukkan oleh pendekatan secara langsung maupun tidak
langsung. Pendekatan langsung dapat ditunjukkan oleh minimalnya gangguan
oleh senyawa lain terhadap hasil analisis misalnya mendapatkan hasil yang sama
dengan atau tanpa senyawa pengganggu, resolusi kromatografik yang bagus dan
pengamatan karakteristik akurasi dari metode tersebut. Bila akurasi metode telah
dapat diterima (acceptable) dan valid, maka metode tersebut otomatis telah masuk
kriteria sebagai metode yang spesifik (Ermer, 2005).
3.3.4 Batas Deteksi dan Batas Kuantitasi
Batas deteksi adalah konsentrasi analit terendah dalam sampel yang masih
dapat dideteksi, meskipun tidak selalu dapat dikuantifikasi. Sedangkan batas
kuantitasi adalah konsentrasi analit terendah dalam sampel yang dapat ditentukan
dengan presisi dan akurasi yang dapat diterima pada kondisi operasional metode
yang digunakan (USP XXX, 2007).
Menurut ICH, batas deteksi dan batas kuantitasi dapat ditentukan dengan 2
metode yakni metode non-instrumental visual dan metode perhitungan. Metode
non-instrumental visual digunakan dalam analisis kromatografi lapis tipis dan
metode titrimetri. Sementara itu, metode perhitungan banyak digunakan dalam
analisis menggunakan instrumental (Rohman & Gandjar, 2007).
3.3.5 Linearitas
Linieritas adalah kemampuan suatu metode untuk memperoleh hasil uji
yang secara langsung proposional dengan konsentrasi analit pada kisaran yang
diberikan. Linieritas dapat ditentukan secara langsung dengan pengukuran analit
atau sampel yang di-spiked pada konsentrasi sekurang-kurangnya lima titik
konsentrasi yang mencakup seluruh rentang konsentrasi kerja (Ermer, 2005).
Berdasarkan rekomendasi ICH, linieritas dalam prakteknya diperkirakan pertama
kali secara visual dari penampilan kurva plot luas area/tinggi puncak dengan
Research, US FDA) merekomendasikan bahwa kriteria linieritasnya pada tingkat
koefisien korelasi tidak lebih kecil dari 0,999 (Épshtein, 2004).
3.3.6 Rentang
Rentang adalah konsentrasi terendah dan tertinggi yang mana suatu
metode analitik menunjukkan akurasi, presisi dan linieritas yang cukup. Rentang
harus mencakup sekurang-kurangnya rentang hasil analisis yang diperlukan atau
diharapkan dalam penelitian atau konsentrasi target uji (Ermer, 2005). Rentang
suatu prosedur dapat divalidasi lewat pembuktian bahwa prosedur analitik
tersebut mampu memberikan presisi, akurasi dan linieritas yang dapat diterima
ketika digunakan untuk menganalisis sampel (USP XXX, 2007; USP Convention,
2006).
3.3.7 Kekuatan (Ketahanan)
Kekuatan/ketahanan dievaluasi dengan melakukan perubahan parameter
dalam melakukan metode analitik seperti persentase kandungan pelarut organik
dalam fase gerak, jumlah zat tambahan (garam, pereaksi pasangan ion, dan
lainlain) dalam fase gerak, pH larutan dapar, waktu pengekstraksian analit,
komposisi pengekstraksi dan perbandingan konsentrasi fase gerak (Épshtein,
BAB III
METODOLOGI PENELITIAN
Penelitian ini merupakan penelitian eksperimental, yang dilakukan di
Laboratorium Kimia Farmasi Kuantitatif dan Laboratorium Penelitian, Fakultas
Farmasi, Universitas Sumatera Utara, Medan. Pada bulan Mei sampai Agustus
tahun 2010.
3.1 Alat
Alat yang digunakan dalam penelitian meliputi alat Kromatografi Lapis
Tipis (KLT) (Camag), Spektrofotometer InfraMerah (Shimadzu),
Spektrofotometer UltraViolet/Visible Double Beam (Shimadzu), Neraca Analitik
(Mettler Toledo), plat Kromatografi Lapis Tipis (KLT) Silika Gel 60 F254
(E.Merck), serta alat gelas lainnya.
3.2 Bahan
Bahan-bahan yang digunakan jika tidak dinyatakan lain adalah berkualitas
proanalisis produksi E.Merck yaitu metanol, aseton, kloroform, amonium
hidroksida 25%, Parasetamol BPFI (PPOM Jakarta), Kafein BPFI (PPOM
Jakarta), Baku Parasetamol (PT. Kimia Farma), Baku Propifenazon (PT.
Konimex) dan Baku Kafein (PT. Kimia Farma), tablet Saridon® (P.T. Bayer
3.3 Pengambilan Sampel
Pengambilan sampel dilakukan secara purposif yaitu tanpa
membandingkan satu tempat dengan tempat yang lain. Sampel yang digunakan
adalah tablet Saridon® (P.T. Bayer Indonesia) dan tablet Bodrex Migra® (P.T.
Tempo Scan Pacific Tbk.).
3.4 Prosedur Penelitian 3.4.1 Penyiapan Bahan
3.4.1.1 Pembuatan fase gerak Kloroform : Aseton : Amonium hidroksida 25% (8:2:0,1)
Sebanyak 400 ml kloroform dicampur dengan 100 ml aseton kemudian
diaduk hingga tercampur merata. Selanjutnya ditambahkan 5 ml amonium
hidroksida 25% dan diaduk hingga tercampur merata.
3.4.1.2 Pelarut
Pelarut yang dipakai dalam penelitian adalah metanol dengan kualitas
proanalisis.
3.4.1.3 Pembuatan Larutan Induk Baku Parasetamol
Ditimbang seksama sejumlah 100 mg Parasetamol BPFI, dimasukkan ke
dalam labu tentukur 10 ml, dilarutkan dan diencerkan dengan metanol hingga
garis tanda sehingga diperoleh larutan dengan konsentrasi 10000 μg/ml.
3.4.1.4 Pembuatan Larutan Induk Baku Propifenazon
Ditimbang seksama sejumlah 100 mg Baku Propifenazon, dimasukkan ke
dalam labu tentukur 10 ml, dilarutkan dan diencerkan dengan metanol hingga
3.4.1.5 Pembuatan Larutan Induk Baku Kafein
Ditimbang seksama sejumlah 100 mg Kafein BPFI, dimasukkan ke dalam
labu tentukur 10 ml, dilarutkan dan diencerkan dengan metanol hingga garis tanda
sehingga diperoleh larutan dengan konsentrasi 10000 μg/ml.
3.4.2 Prosedur Analisis
3.4.2.2 Identifikasi Baku Parasetamol, Propifenazon dan Kafein dengan Spektrofotometer InfraMerah
Uji identifikasi dilakukan dengan menggunakan spektrofotometer
InfraMerah (Fourier Transform Infra Red), yaitu dengan cara : menimbang
masing – masing Parasetamol BPFI, Baku Parasetamol, Baku Propifenazon,
Kafein BPFI dan Baku Kafein masing – masing zat ditimbang 2 mg dan Kalium
Bromida 200 mg. Kemudian dimasukkan ke dalam lumpang, digerus hingga
homogen yang selanjutnya dianalisa pada rentang bilangan gelombang 4000 – 500
cm-1 dan direkam spektrum InfraMerah. Spektrum InfraMerah baku pabrik yang
diperoleh dibandingkan dengan spektrum InfraMerah BPFI dan spektrum
InfraMerah dari literatur.
3.4.2.2 Penentuan Panjang Gelombang Optimum dengan Spektrofotometer UltraViolet/Visible
Panjang gelombang analisis ditentukan dengan cara membuat spektrum
serapan UltraViolet dari Parasetamol BPFI dengan konsentrasi 5 μg/ml, Baku Propifenazon dengan konsentrasi 10 μg/ml dan Kafein BPFI dengan konsentrasi 9 μg/ml menggunakan spektrofotometer UltraViolet/Visible pada rentang panjang
gelombang 200 – 400 nm. Kemudian ketiga spektrum serapan UltraViolet yang
diperoleh dibuat tumpang tindih untuk mengetahui pada panjang gelombang
3.4.2.3 Penyiapan Plat Kromatografi Lapis Tipis (KLT)
Plat Kromatografi Lapis Tipis (KLT) yang berukuran 20 cm × 20 cm
diaktifkan dengan dipanaskan pada suhu 110OC selama 30 menit dalam oven.
Dipotong hingga diperoleh ukuran 10 cm × 20 cm dan siap ditotolkan zat dengan
jarak 1 cm dari tepi bawah dan 1 cm dari tepi samping kiri untuk penotolan
pertama serta jarak antar penotolan adalah 1 cm.
3.4.2.4 Penyiapan Alat Automatic Development Chamber
Alat dihidupkan, kemudian pada masing – masing wadah penampungan
fase gerak yang digunakan untuk menjenuhkan chamber dan yang digunakan
untuk mengelusi dimasukkan sebanyak 20 ml fase gerak kloroform : aseton :
amonium hidroksida 25% (8 : 2 : 0,1). Alat dijalankan dan masing – masing fase
gerak masuk ke dalam chamber secara otomatis. Chamber dijenuhkan selama 30
menit dan ditandai dengan plat penjenuh (saturation plate) yang telah terbasahi
sempurna oleh fase gerak. Kemudian dimasukkan plat Kromatografi Lapis Tipis
(KLT) yang telah ditotolkan sampel, diprekondisikan selama 30 menit,
decelupkan dan dielusi sampai 1 cm dari tepi atas dan 1 cm dari tepi samping kiri
untuk pengelusian pertama serta jarak antar pengelusian adalah 1 cm. Plat
Kromatografi Lapis Tipis (KLT) diangkat, dikeringkan selama 30 menit dan
selanjutnya dikeluarkan dari chamber.
3.4.2.5 Penyiapan Alat Densitometer
Alat dihidupkan dan diatur panjang gelombang deteksi dengan detektor
(KLT) yang telah dielusi ke dalam alat densitometer dan direkam densitogram
sesuai dengan jarak bercak dari hasil pengelusian.
3.4.2.6 Analisa Kualitatif Campuran Parasetamol, Propifenazon dan Kafein dengan Menggunakan Kromatografi Lapis Tipis (KLT) Densitometri
Analisa kualitatif campuran Parasetamol, Propifenazon dan Kafein dari
sampel tablet dilakukan dengan membandingkan harga Rf masing – masing
komponen yang terdapat di dalam sampel tablet dengan harga Rf campuran
Parasetamol BPFI, Baku Propifenazon dan Kafein BPFI.
3.4.2.7 Analisa Kuantitatif
3.4.2.7.1 Penentuan Linieritas Kurva Kalibrasi Parasetamol, Propifenazon dan Kafein
Larutan induk baku Parasetamol, Propifenazon dan Kafein masing –
masing dipipet 5 ml, 3 ml dan 1 ml, dimasukkan ke dalam labu tentukur 10 ml,
lalu diencerkan dengan metanol sampai garis tanda sehingga menghasilkan
larutan dengan konsentrasi Parasetamol, Propifenazon dan Kafein 5000 μg/ml,
3000 μg/ml dan 1000 μg/ml. Lalu ditotolkan sebanyak 3 μl, 4 μl, 5 μl, 6 μl, 7 μl dan 8 μl pada plat Kromatografi Lapis Tipis (KLT). Kemudian dielusi dalam
chamber yang telah dijenuhkan dengan fase gerak, selanjutnya dideteksi dengan
densitometer pada panjang gelombang 260 nm. Direkam densitogram dan dibuat
kurva kalibrasi antara jumlah zat terhadap luas puncak, lalu dihitung persamaan
regresi dan koefisien korelasi.
3.4.2.7.2 Penetapan Kadar Campuran Parasetamol, Propifenazon dan Kafein dalam Sampel Tablet
Tablet sebanyak 20 buah ditimbang dan digerus hingga homogen.
Propifenazon), dimasukkan ke dalam labu tentukur 50 ml, dilarutkan dan
diencerkan dengan metanol sampai garis tanda. Dikocok, lalu disaring (beberapa
ml filtrat pertama dibuang). Ditotolkan sebanyak 5 μl pada plat Kromatografi
Lapis Tipis (KLT). Kemudian dielusi dalam chamber yang telah dijenuhkan
dengan fase gerak, selanjutnya dideteksi dengan densitometer pada panjang
gelombang 260 nm. Direkam densitogram dan dicatat luas puncak. Kadarnya
dihitung dengan mensubstitusikan luas puncak ke dalam persamaan regresi (y =
ax + b) yang diperoleh dari kurva kalibrasi.
3.5.2.8 Analisa Secara Statistik
Menurut Épshtein, 2004 analisis data hasil perhitungan kadar campuran
Parasetamol, Propifenazon dan Kafein dari sampel tablet secara statistik dapat
menggunakan uji t. Rumus yang digunakan adalah:
Data diterima jika pada interval kepercayaan
99,5% dengan nilai α = 0,005.
Keterangan:
= standard deviation/simpangan baku
= kadar dalam satu perlakuan
= kadar rata-rata dalam satu sampel
= jumlah perlakuan
Untuk menghitung kadar campuran Parasetamol, Propifenazon dan Kafein
yang sebenarnya dalam sampel tablet secara statistik digunakan rumus:
Keterangan:
= kadar rata-rata dalam satu sampel
= harga t tabel sesuai dengan derajat kepercayaan
= standard deviation/simpangan baku
= jumlah perlakuan.
3.4.3 Validasi Metode
3.4.3.1 Akurasi (Kecermatan)
Menurut Harmita, 2004 kecermatan dinyatakan dalam % perolehan
kembali (% recovery) analit yang ditambahkan. Kecermatan dapat dilakukan
dengan metode penambahan baku (standard addition method). Metode
penambahan baku dapat dilakukan dengan pengukuran % perolehan kembali pada
3 rentang spesifik yakni 80%, 100% dan 120%. Dimana pada masing - masing
rentang spesifik digunakan 70% sampel (analit) yang dianalisis dan 30% baku
yang akan ditambahkan. Kemudian campuran sampel (analit) dan baku dianalisis
dengan prosedur yang sama seperti pada sampel. % perolehan kembali dapat
dihitung dengan menggunakan rumus sebagai berikut:
Keterangan:
= konsentrasi total sampel yang diperoleh dari pengukuran
= konsentrasi sampel sebenarnya
3.4.3.2 Presisi (Keseksamaan)
Menurut Rohman, 2009 presisi dinyatakan dengan standard
deviation/simpangan baku (SD) atau relative standard deviation/simpangan baku
relatif (RSD) dari serangkaian data. Nilai RSD dirumuskan dengan:
Keterangan:
= relative standard deviation/simpangan baku relatif
= standard deviation/simpangan baku serangkaian data
= rata – rata data
3.4.3.3 Batas Deteksi dan Batas Kuantitasi
Menurut Miller, 2005 batas deteksi (limit of detection/LOD) dan batas
kuantitasi (limit of quantitation/LOQ) dapat dihitung dengan menggunakan rumus
sebagai berikut:
Keterangan:
= limit of detection/batas deteksi
= limit of quantitation/batas kuantitasi
= residual standard deviation/standar deviasi residual
= slope dari kurva kalibrasi
Keterangan:
= respon pada konsentrasi
= respon yang dihitung dari regresi pada konsentrasi
BAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Baku Parasetamol, Propifenazon dan Kafein dengan Spektrofotometer InfraMerah
Identifikasi Baku Parasetamol, Propifenazon dan Kafein dilakukan dengan
menggunakan spektrofotometer InfraMerah (Fourier Transform Infra Red) pada
rentang bilangan gelombang 4000 – 500 cm-1. Spektrum InfraMerah baku pabrik
yang diperoleh dibandingkan dengan spektrum InfraMerah BPFI dan spektrum
InfraMerah dari literatur. Spektrum InfraMerah Baku Parasetamol, Propifenazon
dan Kafein dapat dilihat pada Gambar 1, Gambar 4 dan Gambar 5 dibawah ini.
Spektrum InfraMerah Parasetamol dan Kafein BPFI dapat dilihat pada Gambar
[image:35.595.115.512.456.716.2]2, dan Gambar 6 dibawah ini. Spektrum InfraMerah Parasetamol dan Kafein dari literatur dapat dilihat pada Gambar 3, dan Gambar 7 dibawah ini.
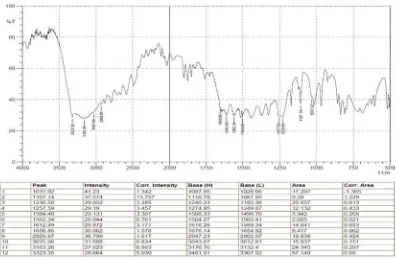
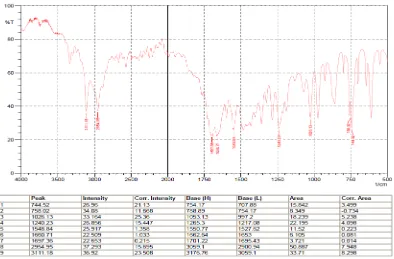
Gambar 2. Spektrum InfraMerah Parasetamol BPFI
[image:36.595.123.505.391.641.2]Tabel 1. Hasil Identifikasi Sidik Jari dari Parasetamol Data Moffat, et al 1227
cm-1 1263 cm-1 1506 cm-1 1565 cm-1 1612 cm-1 1657 cm-1 Data Parasetamol BPFI 1228,66 cm-1 1257,59 cm-1 1506,41 cm-1 1562,34 cm-1 1610,56 cm-1 1656,85 cm-1 Data Baku Parasetamol 1230,58 cm-1 1257,59 cm-1 1504,48 cm-1 1562,34 cm-1 1612,49 cm-1 1656,85 cm-1
Dari hasil pengukuran diperoleh bentuk spektrum InfraMerah Baku
Parasetamol yang hampir sama dengan bentuk spektrum InfraMerah Parasetamol
BPFI dan bentuk spektrum InfraMerah Parasetamol yang terdapat pada literatur.
Pada identifikasi sidik jari diperoleh bilangan gelombang Baku Parasetamol yang
hampir sama dengan bilangan gelombang Parasetamol BPFI dan bilangan
gelombang Parasetamol yang terdapat pada literatur (Moffat, et al., 2004).
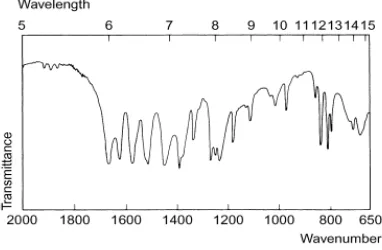
Tabel 2. Hasil Identifikasi Gugus Fungsi dan Ikatan dari Parasetamol Gugus fungsi dan ikatan Literatur Baku Parasetamol
C−H Aromatis 3020 – 3100 cm-1 3035,96 cm-1
C═C 1650 – 1670 cm-1 1656,85 cm-1
Benzen 1500 dan 1600 cm-1 1506,41 dan 1610,56 cm-1 C−H Alifatis 2850 – 2960 cm-1 2929,87 cm-1
O−H 3100 cm-1 3163,26 cm-1
C−O 1050 – 1150 cm-1 1107,14 cm-1
N−H 3310 – 3500 cm-1 3325,28 cm-1
C−N 1030 dan 1230 cm-1 1031,92 dan 1228,66 cm-1
C═O 1700 cm-1 1656,85 cm-1
Jika dilihat pada Tabel 2 gugus O−H tidak muncul pada bilangan
gelombang 3400 – 3640 cm-1, melainkan muncul pada bilangan gelombang 3100
cm-1. Hal ini terjadi karena adanya interaksi antar molekul. Pada identifikasi
gugus fungsi dan ikatan, diperoleh bilangan gelombang Baku Parasetamol yang
hampir sama dengan bilangan gelombang Parasetamol yang terdapat pada
bahwa baku yang diidentifikasi adalah Parasetamol (McMurry, 1993; Silverstein,
[image:38.595.120.507.141.398.2]et al., 1984).
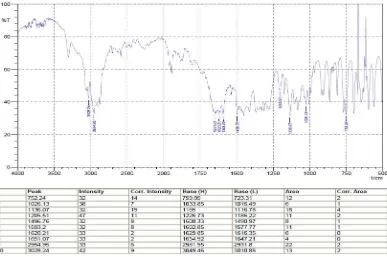
Gambar 4. Spektrum InfraMerah Baku Propifenazon Tabel 3. Hasil Identifikasi Sidik Jari dari Propifenazon
Data Moffat, et al 750 cm-1 1131 cm-1 1500 cm-1 1590 cm-1 1618 cm-1 1650 cm-1 Data Baku Propifenazon 752,24 cm-1 1136,07 cm-1 1496,76 cm-1 1593,20 cm-1 1620,21 cm-1 1651,07 cm-1
Dari hasil pengukuran diperoleh bentuk spektrum InfraMerah Baku
Propifenazon yang hampir sama dengan bentuk spektrum InfraMerah
Propifenazon yang terdapat pada literatur. Pada identifikasi sidik jari diperoleh
bilangan gelombang Baku Propifenazon yang hampir sama dengan bilangan
Tabel 4. Hasil Identifikasi Gugus Fungsi dan Ikatan dari Propifenazon Gugus fungsi dan ikatan Literatur Baku Parasetamol
C−H Aromatis 3020 – 3100 cm-1 3028,24 cm-1
C═C 1650 – 1670 cm-1 1651,07 cm-1
Benzen 1500 dan 1600 cm-1 1496,76 dan 1593,2 cm-1 C−H Alifatis 2850 – 2960 cm-1 2954,95 cm-1
C−N 1030 dan 1230 cm-1 1026,13 dan 1205,51 cm-1
C═O 1700 cm-1 1651,07 cm-1
Pada identifikasi gugus fungsi dan ikatan, diperoleh bilangan gelombang
Baku Propifenazon yang hampir sama dengan bilangan gelombang Propifenazon
yang terdapat pada literatur. Dari data spektrum InfraMerah yang diperoleh dapat
diambil kesimpulan bahwa baku yang diidentifikasi adalah Propifenazon
(McMurry, 1993; Silverstein, et al., 1984).
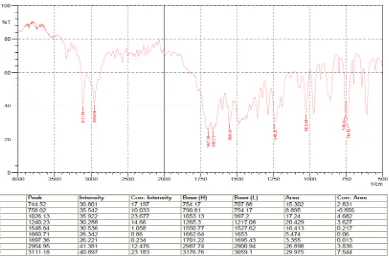
Gambar 6. Spektrum InfraMerah Kafein BPFI
[image:40.595.122.505.394.636.2]Tabel 5. Hasil Identifikasi Sidik Jari dari Kafein Data Moffat, et al 747
cm-1 760 cm-1 1242 cm-1 1548 cm-1 1658 cm-1 1698 cm-1
Data Kafein BPFI 744,52 cm-1 758,02 cm-1 1240,23 cm-1 1548,84 cm-1 1660,71 cm-1 1697,36 cm-1
Data Baku Kafein 744,52 cm-1 758,02 cm-1 1240,23 cm-1 1548,84 cm-1 1660,71 cm-1 1697,36 cm-1
Dari hasil pengukuran diperoleh bentuk spektrum InfraMerah Baku Kafein
yang hampir sama dengan bentuk spektrum InfraMerah Kafein BPFI dan bentuk
spektrum InfraMerah Kafein yang terdapat pada literatur. Pada identifikasi sidik
jari diperoleh bilangan gelombang Baku Kafein yang hampir sama dengan
bilangan gelombang Kafein BPFI dan bilangan gelombang Kafein yang terdapat
[image:41.595.107.514.94.185.2]pada literatur (Moffat, et al., 2004).
Tabel 6. Hasil Identifikasi Gugus Fungsi dan Ikatan dari Kafein
Gugus fungsi dan ikatan Literatur Baku Parasetamol C−H Aromatis 3020 – 3100 cm-1 3111,18 cm-1
C═C 1650 – 1670 cm-1 1660,71 cm-1
C−H Alifatis 2850 – 2960 cm-1 2954,95 cm-1 C−N 1030 dan 1230 cm-1 1026,13 dan 1240,23 cm-1
C═O 1700 cm-1 1697,36 cm-1
Pada identifikasi gugus fungsi dan ikatan, diperoleh bilangan gelombang
Baku Kafein yang hampir sama dengan bilangan gelombang Kafein yang terdapat
pada literatur. Dari data spektrum InfraMerah yang diperoleh dapat diambil
kesimpulan bahwa baku yang diidentifikasi adalah Kafein (McMurry, 1993;
Silverstein, et al., 1984).
Kadar campuran Parasetamol, Propifenazon dan Kafein dalam sampel
tablet ditentukan dengan Kromatografi Lapis Tipis (KLT) Densitometri. Untuk
mendapatkan hasil yang baik, terlebih dahulu ditentukan panjang gelombang
analisis yang optimum.
Panjang gelombang analisis ditentukan dengan cara membuat spektrum
serapan UltraViolet dari Parasetamol BPFI dengan konsentrasi 5 μg/ml, Baku
Propifenazon dengan konsentrasi 10 μg/ml dan Kafein BPFI dengan konsentrasi 9 μg/ml menggunakan spektrofotometer UltraViolet/Visible pada rentang panjang
gelombang 200 – 400 nm. Kemudian ketiga spektrum serapan UltraViolet yang
diperoleh dibuat tumpang tindih untuk mengetahui pada panjang gelombang
berapa ketiganya memberikan serapan optimum. Spektrum serapan UltraViolet
dari Parasetamol BPFI, Baku Propifenazon dan Kafein BPFI dapat dilihat pada
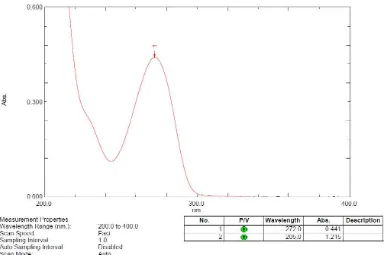
[image:42.595.112.498.440.728.2]Gambar 8, Gambar 9 dan Gambar 10 dibawah ini.
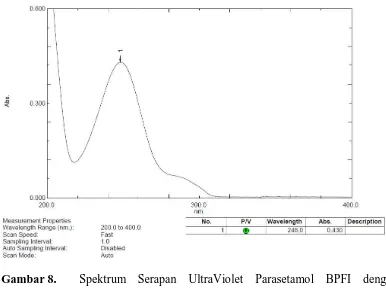
Dari hasil pengukuran diperoleh bentuk spektrum serapan UltraViolet
Parasetamol BPFI yang hampir sama dengan bentuk spektrum serapan UltraViolet
Parasetamol yang terdapat pada literatur. Absorbsi maksimum Parasetamol BPFI
dalam metanol dijumpai pada panjang gelombang 248 nm dan absorbsi
maksimum Parasetamol yang terdapat pada literatur di dalam metanol dijumpai
pada panjang gelombang 247 nm dengan 850 dan Ɛ 12850 ( Dibbern, et al.,
[image:43.595.115.501.277.536.2]2002).
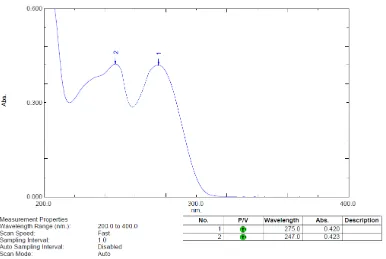
Gambar 9. Spektrum Serapan UltraViolet Baku Propifenazon dengan Konsentrasi 10 μg/ml
Dari hasil pengukuran diperoleh bentuk spektrum serapan UltraViolet
Baku Propifenazon yang hampir sama dengan bentuk spektrum serapan
UltraViolet Propifenazon yang terdapat pada literatur. Absorbsi maksimum Baku
Propifenazon dalam metanol dijumpai pada panjang gelombang 275 nm dan 247
metanol dijumpai pada panjang gelombang 275 nm dan 246 nm dengan 420
[image:44.595.115.499.139.394.2]dan 425 serta Ɛ 9670 dan 9790 (Dibbern, et al., 2002).
Gambar 10. Spektrum Serapan UltraViolet Kafein BPFI dengan Konsentrasi 9 μg/ml
Dari hasil pengukuran diperoleh bentuk spektrum serapan UltraViolet
Kafein BPFI yang hampir sama dengan bentuk spektrum serapan UltraViolet
Kafein yang terdapat pada literatur. Absorbsi maksimum Kafein BPFI dalam
metanol dijumpai pada panjang gelombang 272 nm dan absorbsi maksimum
Kafein yang terdapat pada literatur di dalam metanol dijumpai pada panjang
gelombang 273 nm dengan 875 dan Ɛ 9220 (Dibbern, et al., 2002).
Hasil tumpang tindih ketiga spektrum serapan dapat dilihat pada Gambar
Gambar 11. Hasil Tumpang Tindih Spektrum Serapan UltraViolet Parasetamol BPFI dengan Konsentrasi 5,0 μg/ml, Baku Propifenazon dengan Konsentrasi 10,0 μg/ml dan Kafein BPFI dengan Konsentrasi 9,0 μg/ml Disertai Panjang Gelombang Optimum
Dari hasil tumpang tindih spektrum serapan UltraViolet Parasetamol
BPFI, Baku Propifenazon dan Kafein BPFI diperoleh panjang gelombang yang
memberikan serapan optimal untuk ketiganya yaitu pada 260 nm.
4.3 Analisa Kualitatif Campuran Parasetamol, Propifenazon dan Kafein dengan Menggunakan Kromatografi Lapis Tipis (KLT) Densitometri
Hasil analisa kualitatif campuran Parasetamol, Propifenazon dan Kafein
dari sampel tablet dilakukan dengan membandingkan harga Rf masing – masing
komponen yang terdapat di dalam sampel tablet dengan harga Rf campuran
Parasetamol BPFI, Baku Propifenazon dan Kafein BPFI, maka diperoleh harga Rf
yang sama. Dimana harga Rf 0,27 untuk Parasetamol dan Parasetamol BPFI, 0,74
untuk Propifenazon dan Baku Propifenazon serta 0,51 untuk Kafein dan Kafein
BPFI. Densitogram hasil pengelusian campuran Parasetamol BPFI, Baku Parasetamol BPFI
Baku Propifenazon
Propifenazon, Kafein BPFI dan densitogram hasil pengelusian sampel tablet dapat
dilihat pada Gambar 12, Gambar 13 dan Gambar 14 dibawah ini.
Mekanisme pemisahan campuran Parasetamol, Propifenazon dan Kafein
menggunakan Kromatografi Lapis Tipis (KLT) fase diam Silika Gel 60 F254
(E.Merck) dan fase gerak kloroform : aseton : amonium hidroksida 25% (8 : 2 :
0,1) yaitu berdasarkan sifat kepolaran dari ketiga komponen ini. Polaritas
Parasetamol > Kafein > Propifenazon. Sehingga harga Rf Propifenazon > Kafein >
Parasetamol. Hal ini terjadi karena fase diam yang digunakan bersifat polar, maka
terjadi interaksi yang lebih kuat antara fase diam dengan senyawa polar
dibandingkan interaksi antara fase diam dengan senyawa non polar. Senyawa
dengan polaritas paling tinggi bergerak naik dengan jarak paling dekat dari titik
awal penotolan, sedangkan senyawa dengan polaritas paling rendah bergerak naik
[image:46.595.115.509.453.704.2]dengan jarak paling jauh dari titik awal penotolan tersebut (Watson, 2009).
Gambar 13. Densitogram Hasil Pengelusian Sampel Tablet Saridon® (P.T. Bayer Indonesia)
Gambar 14. Densitogram Hasil Pengelusian Sampel Tablet Bodrex Migra® (P.T. Tempo Scan Pacific Tbk.)
Harga Rf yang sama antara sampel tablet dengan harga Rf campuran
[image:47.595.117.508.406.652.2]sampel yang digunakan dalam penelitian ini mengandung campuran Parasetamol,
Propifenazon dan Kafein.
4.4 Penentuan Linearitas Kurva Kalibrasi
4.4.1 Penentuan Linearitas Kurva Kalibrasi Parasetamol
Hasil uji linearitas kurva kalibrasi Parasetamol BPFI yang dilakukan pada
rentang jumlah zat 0,0000 μg hingga 40,1600 μg diperoleh hubungan yang linier antara jumlah zat terhadap luas area, dengan koefisien korelasi, r = 0,9999 dan
persamaan regresi, y = 1647,0932x + 311,1138. Kurva kalibrasi Parasetamol BPFI
[image:48.595.114.511.372.549.2]dapat dilihat pada Gambar 15 dibawah ini.
Tabel 7. Data Hasil Pendeteksian Parasetamol BPFI yang Diperoleh dari Alat Densitometer pada Panjang Gelombang 260 nm untuk Kurva Kalibrasi
Nomor X (Jumlah Zat / µg) Y (Area / A)
1 0,0000 0,0000
2 15,0600 25909,0167
3 20,0800 33205,8167
4 25,1000 41506,2167
5 30,1200 49805,6833
6 35,1400 58103,7500
Gambar 15. Kurva Kalibrasi Parasetamol BPFI Jumlah Zat Terhadap Luas Puncak
4.4.2 Penentuan Linearitas Kurva Kalibrasi Propifenazon
Hasil uji linearitas kurva kalibrasi Baku Propifenazon yang dilakukan pada
rentang jumlah zat 0,0000 μg hingga 23,9040 μg diperoleh hubungan yang linier
antara jumlah zat terhadap luas area, dengan koefisien korelasi, r = 0,9999 dan
persamaan regresi, y = 830,9619x + 76,4238. Kurva kalibrasi Baku Propifenazon
dapat dilihat pada Gambar 16 dibawah ini.
Tabel 8. Data Hasil Pendeteksian Baku Propifenazon yang Diperoleh dari Alat Densitometer pada Panjang Gelombang 260 nm untuk Kurva Kalibrasi
Nomor X (Jumlah Zat / µg) Y (Area / A)
1 0,0000 0,0000
2 8,9640 7717,5667
3 11,9520 9962,4833
4 14,9400 12459,2167
5 17,9280 14947,2833
6 20,9160 17437,1833
[image:49.595.111.511.579.746.2]Gambar 16. Kurva kalibrasi Baku Propifenazon Jumlah Zat Terhadap Luas Puncak
4.4.3 Penentuan Linearitas Kurva Kalibrasi Kafein
Hasil uji linearitas kurva kalibrasi Kafein BPFI yang dilakukan pada
rentang jumlah zat 0,0000 μg hingga 8,1040 μg diperoleh hubungan yang linier
antara jumlah zat terhadap luas area, dengan koefisien korelasi, r = 0,9999 dan
persamaan regresi, y = 906,7000x + 24,8893. Kurva kalibrasi Kafein BPFI dapat
Tabel 9. Data Hasil Pendeteksian Kafein BPFI yang Diperoleh dari Alat Densitometer pada Panjang Gelombang 260 nm untuk Kurva Kalibrasi
Nomor X (Jumlah Zat / µg) Y (Area / A)
1 0,0000 0,0000
2 3,0390 2841,7667
3 4,0520 3688,6833
4 5,0650 4605,6167
5 6,0780 5522,3500
6 7,0910 6449,0000
7 8,1040 7376,8833
Gambar 17. Kurva kalibrasi Kafein BPFI Jumlah Zat Terhadap Luas Puncak Harga koefisien korelasi yang diperoleh untuk kurva kalibrasi Parasetamol
BPFI, Baku Propifenazon dan Kafein BPFI adalah 0,9999. Harga koefisien
korelasi ini dapat diterima karena koefisien korelasi ini telah memenuhi
persyaratan yakni lebih besar dari 0,995 (Moffat, et al., 2004).
Perhitungan jumlah zat dalam pembuatan kurva kalibrasi pada Lampiran
BPFI, Baku Propifenazon, dan Kafein BPFI pada berbagai rentang jumlah zat
dapat dilihat pada Lampiran 5 Halaman 40 dan Lampiran 6 Halaman 44.
Perhitungan persamaan regresi dan linearitas kurva kalibrasi Parasetamol BPFI,
Baku Propifenazon dan Kafein BPFI dapat dilihat pada Lampiran 7 Halaman
46.
4.5 Penetapan Kadar Campuran Parasetamol, Propifenazon dan Kafein dalam Sampel Tablet
Hasil penetapan kadar campuran Parasetamol, Propifenazon dan Kafein
dari sampel tablet yang ditentukan secara simultan dengan Kromatografi Lapis
Tipis (KLT) Densitometri, dilakukan dengan mensubtitusikan luas puncak ke
dalam persamaan regresi (y = ax + b). Data hasil perhitungan kadar setelah
dilakukan uji statistik dapat dilihat pada Tabel 10 dibawah ini. Densitogram hasil
pendeteksian sampel tablet Saridon® (P.T. Bayer Indonesia) dan sampel tablet
Bodrex Migra® (P.T. Tempo Scan Pacific Tbk.) dapat dilihat pada Lampiran 9
Halaman 51 dan Lampiran 11 Halaman 58.
Tabel 10. Data Hasil Perhitungan Kadar Setelah Dilakukan Uji Statistik
No Tablet Parasetamol Propifenazon Kafein
1 Saridon
®
(P.T. Bayer Indonesia)
97,0484% ± 0,3324% 94,4508% ± 0,1425% 98,3786% ± 0,1935% 2
Bodrex Migra® (P.T. Tempo Scan Pacific
Tbk.) 97,6157% ± 0,0475% 102,4931% ± 0,1557% 105,7689% ± 0,2680%
Dari tabel diatas dapat dilihat bahwa kedua tablet yang dianalisis
memenuhi persyaratan untuk tablet secara umum yakni mengandung tidak kurang
dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket.
[image:52.595.109.518.514.634.2]Parasetamol, Propifenazon dan Kafein yang sebenarnya dari sampel tablet dan
data hasil pengolahan data dari sampel tablet Saridon® (P.T. Bayer Indonesia)dan
tablet Bodrex Migra® (P.T. Tempo Scan Pacific Tbk.) dapat dilihat pada
Lampiran 10 Halaman 54, Lampiran 12 Halaman 61 dan Lampiran 13 Halaman 65.
4.6 Validasi Metode
Pada penelitian ini dilakukan uji validasi metode, dengan metode
penambahan bahan baku (standard addition method) kedalam sampel. Uji ini
meliputi uji akurasi dengan parameter % perolehan kembali (% recovery) dan uji
presisi dengan parameter simpangan baku relatif (relative standard
deviation/RSD).
Uji akurasi dan uji presisi dilakukan pada rentang spesifik 80%, 100%,
120%, masing – masing dengan 6 kali replikasi. Setiap rentang spesifik
mengandung 70% sampel dan 30% baku. Data hasil pengujian % perolehan
kembali dan simpangan baku relatif dari tablet Saridon® (P.T. Bayer Indonesia)
dengan metode penambahan bahan baku dapat dilihat pada Tabel 11 di bawah ini.
Densitogram hasil pengelusian campuran Parasetamol, Propifenazon, dan Kafein
pada uji validasi dapat dilihat pada Lampiran 14 Halaman 67. Perhitungan
penimbangan % perolehan kembali dapat dilihat pada Lampiran 15 Halaman 69
Tabel 11. Data Hasil % Perolehan Kembali Campuran Parasetamol, Propifenazon dan Kafein dengan Metode Penambahan Baku pada Rentang Spesifik 80%, 100% dan 120%
No. Rentang Spesifik
Luas Area Perolehan Kembali
Parase-tamol
Propi-fenazon Kafein
Parase-tamol
Propi-fenazon Kafein 1
80%
32644,1 9683,9 3615,4 99,8638% 100,6871% 99,5905% 2 32647,3 9681,8 3619,6 99,8960% 100,6166% 99,9750% 3 32649,6 9686,2 3616,5 99,9192% 100,7643% 99,6912% 4 32644,9 9687,6 3618,3 99,8718% 100,8112% 99,8560% 5 32640,0 9681,5 3619,1 99,8224% 100,6066% 99,9292% 6 32646,2 9688,4 3616,6 99,8849% 100,8381% 99,7003% 7
100%
40630,0 12053,2 4514,0 100,0444% 100,7598% 100,6406% 8 40628,4 12056,4 4512,4 100,0315% 100,8457% 100,5234% 9 40629,8 12051,4 4511,3 100,0428% 100,7115% 100,4429% 10 40628,1 12050,0 4519,0 100,0291% 100,6739% 101,0069% 11 40628,7 12055,7 4518,0 100,0339% 100,8269% 100,9336% 12 40629,1 12051,7 4510,6 100,0371% 100,7195% 100,3916% 13
120%
48876,5 14446,7 5405,9 100,7037% 100,1608% 99,7028% 14 48876,9 14446,6 5405,4 100,7064% 100,1586% 99,6723% 15 48884,1 14449,1 5402,3 100,7548% 100,2145% 99,4831% 16 48882,7 14449,9 5403,5 100,7454% 100,2324% 99,5563% 17 48878,2 14447,4 5405,2 100,7152% 100,1765% 99,6601% 18 48875,9 14447,9 5405,8 100,6997% 100,1877% 99,6967%
Perolehan Kembali Rata - Rata 100,2112% 100,5551% 100,0251%
Standar Deviasi 0,3775% 0,2755% 0,4943%
Relatif Standar Deviasi 0,3767% 0,2740% 0,4942%
Pada uji akurasi diperoleh % perolehan kembali rata - rata untuk
Parasetamol, Propifenazon dan Kafein secara berturut - turut adalah 100,2112%,
100,5551% dan 100,0251%. Data hasil % perolehan kembali dan contoh
perhitungan % perolehan kembali dapat dilihat pada Lampiran 18 Halaman 84
dan Lampiran 19 Halaman 87. Nilai % perolehan kembali yang diizinkan adalah
diantara 98% - 102% (Harmita, 2004).
Untuk uji presisi diperoleh nilai RSD rata – rata untuk Parasetamol,
[image:54.595.87.543.108.514.2]0,4942%. Perhitungan analisis data statistik % perolehan kembali dapat dilihat
pada Lampiran 17 Halaman 81. Simpangan baku relatif yang diperoleh telah
memenuhi syarat presisi untuk validasi prosedur analitik karena lebih kecil dari
2% (Ermer, 2005).
Batas deteksi dan batas kuantitasi dihitung dari persamaan regresi yang
diperoleh dalam kurva kalibrasi (Ermer and Burgess, 2005). Batas deteksi untuk
Parasetamol, Propifenazon dan Kafein berturut – turut adalah 0,8023 μg, 0,3854 μg dan 0,1134 μg, sedangkan batas kuantitasi untuk Parasetamol, Propifenazon
dan Kafein berturut – turut adalah 2,4312 μg, 1,1680 μg dan 0,3438 μg. Perhitungan Batas Deteksi dan Batas Kuantitasi Parasetamol BPFI, Baku
Propifenazon dan Kafein BPFI dapat dilihat pada Lampiran 8 Halaman 49.
Maka dari hasil yang diperoleh ini dapat disimpulkan bahwa metode yang
digunakan dalam penelitian ini mempunyai akurasi dan presisi yang memenuhi
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Penetapan kadar sediaan tablet yang mengandung campuran Parasetamol,
Propifenazon dan Kafein secara simultan dengan densitometer pada panjang
gelombang 260 nm dapat dilakukan dengan terlebih dahulu dilakukan pemisahan
dengan Kromatografi Lapis Tipis (KLT) fase diam Silika Gel 60 F254 (E.Merck)
dan fase gerak kloroform : aseton : amonium hidroksida 25% (8 : 2 : 0,1). Kadar
campuran Parasetamol, Propifenazon dan Kafein yang dianalisis dari sediaan
tablet yang ditentukan memenuhi persyaratan kadar untuk tablet secara umum
yakni mengandung tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari
jumlah yang tertera pada etiket. Hasil uji validasi metode Kromatografi Lapis
Tipis (KLT) Densitometri pada penetapan kadar campuran Parasetamol,
Propifenazon dan Kafein dalam tablet secara simultan memberikan hasil akurasi
dan presisi yang memenuhi persyaratan. Dengan demikian metode ini dapat
digunakan untuk penetapan kadar campuran Parasetamol, Propifenazon dan
Kafein dalam sediaan tablet.
5.2 Saran
Disarankan agar dilakukan penelitian penetapan kadar campuran
Parasetamol, Propifenazon dan Kafein dalam sediaan tablet dengan metode lain
DAFTAR PUSTAKA
Bliesner, D.M. (2006). Validating Chromatographic Methods A Practical Guide. New Jersey: John Wiley and Sons, Inc.. Page 1.
Depkes RI. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan RI. Hal. 254, 649.
Dibbern, H.W., Müller, R.M., dan Wirbitzki, E. (2002). UV and IR Spectra. Germany: Cantor Verlag/Aulendorf. Pages 301, 1392, 1386.
Dimitrovska, A., Jolevska, S.T., Nancovska, A., dan Ilievska, M. (1993). Determination of Propyphenazone, Paracetamol, Caffeine and Codeine Phosphate With Thin Layer Chromatography. Bulletin of the Chemists and
Technologists of Macedonia. Vol. 14. 1st November: 39 – 41.
Ermer, J. (2005). Analytical Validation within the Pharmaceutical Environment. In: J. Ermer and J.H. McB. Miller (eds). Method Validat