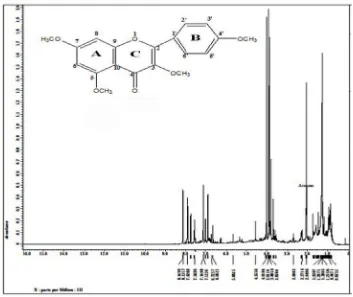
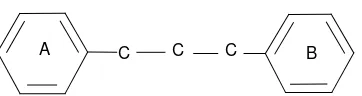ISOLASI SENYAWA FLAVONOIDADARI KULIT BATANG
TUMBUHAN PETAI CINA ( Leucaena glauca L.)
SKRIPSI
MARLINTON SINAGA
070802020
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
ISOLASI SENYAWA FLAVONOIDA DARI KULIT BATANG
TUMBUHAN PETAI CINA ( Leucaena glauca L.)
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
MARLINTON SINAGA 070802020
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : ISOLASI SENYAWA FLAVONOIDA DARI
KULIT BATANG TUMBUHAN PETAI CINA (Leucaena glauca L.)
Kategori : SKRIPSI
Nama : MARLINTON SINAGA
Nomor Induk Mahasiswa : 070802020
Program Studi : SARJANA (S1) KIMIA
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM UNIVERSITAS SUMATERA UTARA
Disetujui di Medan, Juni 2012
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Drs. Johannes Simorangkir, MSi Drs. Philipus H Siregar, MSi
NIP. 1953 0714 1980 03004 NIP. 1958 0504 1986 011002
Diketahui/Disetujui oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
ISOLASI SENYAWA FLAVONOIDA DARI KULIT BATANG TUMBUHAN PETAI CINA (Leucaena glauca L.)
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juni 2012
PENGHARGAAN
Segala puji serta ucapan syukur saya panjatkan pada Tuhan Yesus Kristus, karena melalui berkat dan penyertaannya penulis dapat menyelesaikan penelitian dan penulisan skripsi ini dalam waktu yang ditetapkan.
ABSTRAK
Isolasi senyawa flavonoida yang terkandung di dalam kulit batang tumbuhan petai cina (Leucaena glauca L.) dilakukan dengan ekstraksi maserasi dengan metanol. Fraksi metanol diuapkan lalu dilarutkan kembali dengan etil asetat kemudian dipekatkan dan diuapkan. Fraksi etil asetat dilarutkan dengan metanol dan diekstraksi partisi dengan n-heksana. Lapisan metanol dipisahkan dengan kolom kromatografi dengan fasa diam silika gel dan berturut-turut dengan fasa gerak campuran n-heksana : etil asetat 90:10 v/v, 80:20 v/v , 70:30 v/v, 60:40 v/v. Senyawa murni yang diperoleh dari hasil isolasi berbentuk kristal jarum, berwarna kuning muda, massa=12mg, Rf=0,65, dan titik lebur=143-145oC. Kristal tersebut juga bereaksi positif terhadap pereaksi-pereaksi senyawa flavonoida. Hasil identifikasi Spektroskopi UV-Visible, FT-IR, dan 1
H-NMR menunjukkan bahwa kristal merupakan senyawa golongan flavonoida yaitu flavon.
. .
THE ISOLATION OF FLAVONOID FROM THE BARK OF PETAI CINA ( Leucaena glauca L. )
ABSTRACT
DAFTAR ISI
Daftar Lampiran ix
Daftar Gambar x
1.6. Metodologi Penelitian 3
Bab 2 Tinjauan Pustaka 5
2.1. Tumbuhan Petai Cina 5
2.1.1. Morfologi Tumbuhan Petai Cina 5
2.1.2. Sistematika Tumbuhan Petai Cina 6
2.1.3. Manfaat Tumbuhan Petai Cina 6
2.1.4. Efek Farmakologis dan Hasil Penelitian 6
2.1.5. Kandungan Kimia Petai Cina 7
2.2. Senyawa Organik Bahan Alam 7
2.3. Senyawa Flavonoida 8
2.3.1. Struktur Dasar Senyawa Flavonoida 10
2.3.2. Klasifikasi Senyawa Flavonoida 10
2.3.3. Sifat Kelarutan Flavonoida 16
2.3.4. Biosintesa Flavonoida 16
2.4. Teknik Pemisahan 18
2.4.1.Ekstraksi 18
2.4.2. Kromatografi 18
2.4.1.1. Kromatografi Lapis Tipis 19
2.4.1.2. Kromatografi Kolom 20
2.4.1.3. Harga Rf (Retardation Factor) 21
2.5.3. Kristalisasi 21
2.5.4. Rekristalisasi 22
2.5. Teknik Spektroskopi 22
2.5.1. Spektrofotometri Ultra-Violet 22
Bab 3 Bahan dan Metode Penelitian 27
3.1. Alat-Alat 27
3.2. Bahan 28
3.3. Prosedur Penelitian 28
3.3.1. Penyediaan Sampel 28
3.3.2. Uji Pendahuluan terhadap Ekstrak Petai Cina 28
3.3.2.1. Skrining Fitokimia 29
3.3.3. Prosedur Memperoleh Ekstrak Pekat Lapisan Metanol 29 dari Petai Cina (L.glauca L.)
3.3.4.. Analisis Kromatografi Lapis Tipis 30 3.3.5. Isolasi Senyawa Flavonoida dengan Kromatografi Kolom 30
3.3.6. Pemurnian (Rekristalisasi) 31 3.3.7. Uji Kemurnian Hasil Isolasi dengan Kromatografi Lapis Tipis 32
(KLT)
3.3.8. Penentuan Titik Lebur 32
3.3.9. Identifikasi Senyawa Hasil Isolasi 32 3.3.9.1. Identifikasi dengan Spektrofotometer UV-Visible 32 3.3.9.2. Identifikasi dengan Spektrometer Resonansi Magnetik Inti Proton(1
3.3.9.3. Identifikasi dengan Spektrofotometer
H-NMR) 33
Infra Merah (FT-IR) 33
3.4. Bagan Skrining Fitokimia 34
DAFTAR LAMPIRAN
Halaman
Lampiran A. Determinasi Tumbuhan Petai Cina 46
(L.glauca L.)
Lampiran B. Gambar Tumbuhan Petai Cina 47
(L.glauca L.)
Lampiran C. Kromatogram Lapisan Tipis Ekstrak Pekat Lapisan Metanol 48 Kulit Batang Tumbuhan Petai Cina (L.glauca L.)
Lampiran D. Kromatografi Lapis Tipis Senyawa Hasil Isolasi Melalui 49 Penampakan Noda Dengan Penambahan Pereaksi
Lampiran E. Spektrum UV-Visible beberapa senyawa beberapa flavonoida 50 Lampiran F. Ekspansi Spektrum 1
Lampiran G. Ekspansi spektrum
H-NMR Senyawa Hasil Isolasi 51 1
Lampiran H. Spektrum
H-NMR senyawa hasil isolasi 52 1
DAFTAR GAMBAR
Halaman
Gambar 1. Kerangka Dasar Senyawa Flavonoida 10
Gambar 2. Biosintesa hubungan antara jenis monomer Flavonoida dari alur
Asetat-malonat dan alur sikimat 17
Gambar 3. Spektrum UV-Visible Senyawa Hasil Isolasi 37
Gambar 4. Spektrum FT-IR Senyawa Hasil Isolasi 38
DAFTAR TABEL
Halaman
ABSTRAK
Isolasi senyawa flavonoida yang terkandung di dalam kulit batang tumbuhan petai cina (Leucaena glauca L.) dilakukan dengan ekstraksi maserasi dengan metanol. Fraksi metanol diuapkan lalu dilarutkan kembali dengan etil asetat kemudian dipekatkan dan diuapkan. Fraksi etil asetat dilarutkan dengan metanol dan diekstraksi partisi dengan n-heksana. Lapisan metanol dipisahkan dengan kolom kromatografi dengan fasa diam silika gel dan berturut-turut dengan fasa gerak campuran n-heksana : etil asetat 90:10 v/v, 80:20 v/v , 70:30 v/v, 60:40 v/v. Senyawa murni yang diperoleh dari hasil isolasi berbentuk kristal jarum, berwarna kuning muda, massa=12mg, Rf=0,65, dan titik lebur=143-145oC. Kristal tersebut juga bereaksi positif terhadap pereaksi-pereaksi senyawa flavonoida. Hasil identifikasi Spektroskopi UV-Visible, FT-IR, dan 1
H-NMR menunjukkan bahwa kristal merupakan senyawa golongan flavonoida yaitu flavon.
. .
THE ISOLATION OF FLAVONOID FROM THE BARK OF PETAI CINA ( Leucaena glauca L. )
ABSTRACT
BAB I
PENDAHULUAN
1.1 Latar Belakang
Flavonoida merupakan kandungan khas tumbuhan hijau dengan mengecualikan alga
dan hornwort. Flavonoida sebenarnya terdapat pada semua bagian tumbuhan termasuk
daun, akar, kulit, tepung sari, nectar, bunga, buah buni, dan biji. Hanya sedikit saja
catatan yang melaporkan adanya flavonoida pada hewan , misalnya dalam kelenjar
bau berang – berang, sekresi lebah, dan di dalam sayap kupu – kupu, itupun dengan
anggapan bahwa flavonoida tersebut berasal dari tumbuhan yang dijadikan makanan
hewan dan tidak dibiosintesis di dalam tubuh mereka. Menurut perkiraan , kira – kira
2 % dari seluruh karbon yang difotosintesis oleh tumbuhan diubah menjadi
flavonoida. Sebagian besar tannin pun berasal dari flavonoida. Jadi, flavonoida
terdapat dalam semua tumbuhan hijau sehingga pastilah ditemukan pula pada setiap
ekstrak tumbuhan ( Markham, 1988 ).
Keanekaragaman tumbuhan di Indonesia merupakan salah satu kekayaan alam
yang perlu dilestarikan mengingat peranan dan khasiat tumbuhan dapat memberikan
manfaat bagi kesehatan masyarakat. Tumbuh – tumbuhan merupakan salah satu
sumber senyawa bahan alam hayati yang memegang peranan penting dalam
pemanfaatan zat kimia berkhasiat. Didukung oleh penelitian ilmiah secara fungsional
tidak lagi dipandang sebagai bahan konsumsi maupun penghias, tetapi sebagai
tanaman obat yang multifungsi. Penggunaan senyawa bahan alam sebagai obat bukan
hal baru, sejak manusia ada dipermukaan bumi, mencoba mengobati berbagai macam
penyakit yang di deritanya menggunakan senyawa bahan alam secara turun temurun
secara tradisional dapat dipergunakan sebagai obat ( racikan sederhana ) karena
memiliki khasiat yang menyembuhkan serta komposisi kimia yang dimilikinya.
Salah satu tumbuhan berkhasiat yang sering digunakan sebagai sumber obat
adalah tumbuhan petai cina (Leucaena glauca L.). Bagian yang digunakan sebagai
obat adalah daun, akar, biji, dan seluruh bagian tanaman. Keseluruhan tanaman ini
dapat digunakan sebagai sumber bahan obat-obatan tradisional (Dalimartha, 2000).
Dari penelitian terdahulu diketahui bahwa pada batang petai cina terdapat
senyawa tannin (Suttie, 2002 ), dan pada daunnya dilakukan analisa Karotenoid (
Wina dan Susana, 1993 ), Penelitian (Wahyuni, 2006) menunjukkan bahwa infusa
daun petai cina dengan konsentrasi 40% mempunyai efek antiinflamasi pada tikus
jantan galur Wistar yang diinduksi dengan 0,1 ml karagenin 1% dengan nilai AUC
(ml.Jam) sebesar 0,24 ( Fauziyah, 2008 ).
Dari uraian diatas, peneliti tertarik melakukan penelitian terhadap kulit batang
tumbuhan petai cina tersebut, khususnya mengenai senyawa flavonoida yang
terkandung di dalamnya. Metode yang digunakan adalah dengan mengekstraksi kulit
batang dengan metanol, kemudian dilakukan analisa KLT dan kolom kromatografi.
Selanjutnya komponen atau senyawa murni yang diperoleh ditentukan strukturnya
berdasarkan hasil analisis Spektrofotometri Infra Merah
(FT-IR), Spektrometri Resonansi Magnetik Inti Proton (1H-NMR), Spektrofotometri
UV-Visible, dan penentuan titik lebur.
1.2 Permasalahan
Permasalahan dalam penelitian ini adalah golongan flavonoida apa yang terdapat
1.3Tujuan Penelitian
Mengisolasi senyawa flavonoida dari kulit batang tumbuhan petai Cina (L. glauca L.)
dan menentukan strukturnya.
1.4 Manfaat Penelitian
Hasil dari penelitian ini diharapkan dapat memberikan sumber informasi ilmiah pada
bidang kimia bahan alam hayati dan farmasi dalam pengembangan ilmu kimia
flavonoida di dalam kulit batang tumbuhan petai Cina
(
L. glaucaL.).1.5 Lokasi Penelitian
1. Lokasi Pengambilan Sampel
Sampel yang digunakan diperoleh dari Sabulan, Kecamatan Sitio – tio. Kabupaten
Samosir. Sumatera Utara.
2. Lokasi Penelitian
Penelitian dilakukan di laboratorium Kimia Bahan Alam FMIPA, Universitas
Sumatera Utara.
3. Lokasi Identifikasi Kristal Hasil Iisolasi
Analisis Spektrofotometri Inframerah (FT-IR), Spektrofotometri UV-Visible, dan
Spektrofotometri Resonansi Magnetik Inti Proton (1H-NMR) dilakukan di Pusat
Penelitian Kimia - LIPI, Kawasan PUSPIPTEK Serpong, Tangerang.
1.6 Metodologi Penelitian
Dalam penelitian ini, isolasi senyawa flavonoida dilakukan terhadap kulit batang
Tahap awal dilakukan uji skrining fitokimia untuk senyawa flavonoida, yaitu dengan
menggunakan pereaksi FeCl3 5%, NaOH 10%, Mg-HCl dan H2SO4(p). Selanjutnya
dilakukan isolasi terhadap sampel melalui beberapa tahap yaitu ekstraksi maserasi,
ekstraksi partisi, analisis kromatografi lapis tipis, analisis kromatografi kolom,
rekristalisasi dan analisis kristal hasil isolasi. Untuk analisis kristal hasil isolasi
dilakukan melalui analisis kromatografi lapis tipis, pengukuran titik lebur dan
identifikasi dengan menggunakan Spektrofotometer UV-Visible , Spektrofotometer
Infra Merah (FT-IR), dan Spektrofotometer Resonansi Magnetik Inti Proton (1
BAB 2
TINJAUAN PUSTAKA
2.1 Tumbuhan Petai Cina
Petai cina berasal dari Amerika tropis, tersebar di daerah tropik dan ditemukan pada
ketinggian antara 1-1.500 m dpl. Petai cina akan berbuah lebih baik jika terkena
langsung dengan sinar matahari. Tanaman ini dapat tumbuh di segala macam tanah,
asalkan jangan di tanah lempung yang pekat dan tergenang air.
2.1.1 Morfologi Tumbuhan Petai Cina
Petai cina merupakan perdu ataupun pohon kecil dengan tinggi 2-10 m, memiliki
batang pohon keras dan berukuran tidak besar serta batang bulat silindris dan bagian
ujung berambut rapat. Daun majemuk terurai dalam tangkai, menyirip genap ganda
dua sempurna, anak daun kecil-kecil terdiri dari 5-20 pasang, bentuknya lanset, ujung
runcing, tepi rata, panjang 6-21 mm dan lebar 2-5 mm. Bunga majemuk terangkai
dalam karangan berbentuk bongkol yang bertangkai panjang dan berwarna putih
kekuningan atau sering disebut cengkaruk. Buahnya mirip buah petai ( parkia speciosa
) tetapi ukurannya jauh lebih kecil dan berpenampang lebih tipis, termasuk buah
polong yang berisi biji – biji kecil dengan jumlah cukup banyak, pipih, dan tipis
bertangkai pendek, panjang 10-18 cm, lebar 2 cm dan diantara biji ada sekat. Biji
terdiri dari 15-30 butir, letak melintang, bentuk bulat telur sungsang, panjang 8 mm,
lebar 5 mm, berwarna coklat kehijauan atau coklat tua dan licin mengkilap.
Petai cina dipakai untuk pupuk hijau dan sering ditanam sebagai tanaman
pagar sedangkan daun muda, tunas bunga, dan polong bisa dimakan sebagai lalap
mentah ataupun dimasak terlebih dahulu. Perbanyakan selain dengan penyebaran biji
2.1.2 Sistematika Tumbuhan Petai Cina
Sistematika tumbuhan petai cina adalah sebagai berikut :
Kingdom : Plantae
Divisi : Spermatophyta
Class : Dicotyledoneae
Ordo : fabales
Famili : Mimosaceae
Genus : Leucaena
Spesies : Leucaena glauca L.
Nama umum tumbuhan adalah petai Cina. Tumbuhan ini dikenal masyarakat
Indonesia dengan nama daerah yaitu : pete cina , pete selong (Sumatera), pete selong (
Sunda ), lamtoro, peutey, selamtara, pelending, kamalandingan, (Jawa), kalandingan
(Madura). Sinonim Leucaena glauca L. adalah Leucaena leucocephala ( Lmk ) De
Wit. Nama asing petai cina Yin he huan (C), wild tamarind (L) dan nama simplisia
petai cina adalah semen leucaenae glaucae ( biji lamtoro ) (Yuniarti, 2008 ).
2.1.3 Manfaat Tumbuhan Petai Cina
(
L. glauca L.)Biji, daun, dan seluruh bagian tanaman dapat digunakan untuk mengobati beberapa
penyakit. Diantaranya adalah kencing manis ( diabetes melitus), patah tulang,
cacingan, bisul, terlambat haid, radang ginjal ( nephritis ) dan susah tidur ( Dalimarta,
2000).
2.1.4 Efek Farmakologis dan Hasil Penelitian
Efek farmakologis Petai cina diantaranya adalah menyembuhkan luka luar, abses paru,
meluruhkan urine ( diuretik ), melancarkan darah, dan anti anti-inflamasi (Dalimartha,
2.1.5 Kandungan Kimia Petai Cina
Biji mengandung mimosin, leukanin, leukanol, dan protein. Daun mengandung
alkaloid, saponin, flavonoida, tanin, protein, lemak, kalsium, fosfor, besi, serta
vitamin ( A, B, C ) (Dalimartha, 2000).
2.2 Senyawa Organik Bahan Alam
Senyawa organik bahan alam dapat diklasifikasikan berdasarkan sifat-sifat kimia yang
dimilikinya. Ada empat cara klasifikasi yang diusulkan, yaitu:
1. Klasifikasi Berdasarkan Struktur Kimiawi
Klasifikasi ini berdasarkan pada kerangka molekuler dari senyawa yang
bersangkutan. Menurut sistem ini, ada 4 kelas yaitu:
a. Senyawa alifatik rantai terbuka atau lemak dan minyak.
Contoh: asam-asam lemak, gula, dan asam-asam amino pada umumnya
b. Senyawa alisiklik atau sikloalifatik
Contoh: terpenoida, steroida, dan beberapa alkaloida
c. Senyawa aromatik atau benzenoid
Contohnya: golongan fenolat dan golongan kuinon
d. Senyawa heterosiklik
Contoh: alkaloida, flavonoida, golongan basa asam inti
2. Klasifikasi Berdasarkan Sifat Fisiologik
Setelah penelitian yang lebih mendalam dilakukan terhadap morfin (1806), penisilin
(1939) dan prostaglandin (1963), maka perhatian para ahli sering ditujukan kepada
isolasi dan penentuan fungsi fisiologis dari senyawa organik bahan alam tertentu.
Hampir separoh dari obat-obatan yang digunakan sehari-hari merupakan bahan alam,
misalnya alkaloida dan antibiotik, atau golongan-golongan sintetik. Oleh karena itu,
senyawa organik bahan alam dapat juga diklasifikasikan segi aktivitas fisiologik dari
3. Klasifikasi Berdasarkan Taksonomi
Pengklasifikasian ini didasarkan pada penyelidikan morfologi komparatif dari
tumbuh-tumbuhan yaitu taksonomi tumbuhan.
4. Klasifikasi Berdasarkan Biogenesis
Semua konstituen tumbuhan dan binatang dibiosintesis dalam organisme melalui
reaksi-reaksi yang dibantu oleh enzim tertentu. (istilah “biosintesis” dan “biogenesis”
mempunyai arti yang sama: pembentukan bahan alam oleh organisme hidup.
2.3 Senyawa Flavonoida
Istilah flavonoida diberikan pada suatu golongan besar senyawa yang berasal dari
kelompok senyawa yang paling umum, yaitu senyawa flavon, suatu jembatan oksigen
terdapat diantara cincin A dalam kedudukan orto, dan atom karbon benzil yang
terletak disebelah cincin B. Senyawa heterosoklik ini, pada tingkat oksidasi yang
berbeda terdapat dalam kebanyakan tumbuhan. Flavon adalah bentuk yang
mempunyai cincin C dengan tingkat oksidasi paling rendah dan dianggap sebagai
struktur induk dalam nomenklatur kelompok senyawa-senyawa ini (Manitto, 1981).
Senyawa-senyawa flavonoida adalah senyawa-senyawa polifenol yang
mempunyai 15 atom karbon, terdiri dari dua cincin benzena yang dihubungkan
menjadi satu oleh rantai linier yang terdiri dari tiga atom karbon. Senyawa-senyawa
flavonoida adalah senyawa 1,3 diaril propana, senyawa isoflavonoida adalah senyawa
1,2 diaril propana, sedangkan senyawa-senyawa neoflavonoida adalah 1,1 diaril
propana.
Sekitar 2% dari seluruh karbon yang difotosintesis oleh tumbuhan (atau
kira-kira 1x109 ton/tahun) diubah menjadi flavonoida atau senyawa yang berkaitan
dengannya. Sebagian besar tanin pun berasal dari flavonoida. Jadi flavonoida
merupakan salah satu golongan fenol alam yang terbesar. Senyawa flavonoida
sebenarnya terdapat pada semua bagian tumbuhan termasuk daun, akar, kayu, kulit,
tumbuh-tumbuhan, kecuali alga. Namun ada juga flavonoida yng terdapat pada
hewan, misalnya dalam kelenjar bau berang-berang dan sekresi lebah. Dalam sayap
kupu – kupu dengan anggapan bahwa flavonoida berasal dari tumbuh-tumbuhan yang
menjadi makanan hewan tersebut dan tidak dibiosintesis di dalam tubuh mereka.
Penyebaran jenis flavonoida pada golongan tumbuhan yang tersebar yaitu
angiospermae, klorofita, fungi, briofita (Markham, 1988).
Flavonoida merupakan senyawa 15-karbon yang umumnya tersebar di seluruh
dunia tumbuhan. Lebih dari 2000 flavonoid yang berasal dari tumbuhan telah
diidentifikasi. Kerangka dasar flavonoida biasanya diubah sedemikian rupa sehingga
terdapat lebih banyak ikatan rangkap, menyebabkan senyawa itu menyerap cahaya
tampak, dan ini membuatnya berwarna.
Ada tiga kelompok flavonoida yang amat menarik perhatian dalam fisiologi
tumbuhan, yaitu antosianin, flavonol, dan flavon. Antosianin (dari bahasa Yunani
anthos, bunga dan kyanos, biru-tua) adalah pigmen berwarna yang umunya terdapat di
bunga berwarna merah, ungu, dan biru. Pigmen ini juga terdapat di berbagai bagian
tumbuhan lain, misalnya buah tertentu, batang, daun, dan bahkan akar. Sering
flavonoida terikat di sel epidermis. Warna sebagian besar buah dan banyak bunga
adalah akibat dari antosianin, walaupun beberapa warna tumbuhan lainnya, seperti
buah tomat dan beberapa bunga kuning, karena karotenoid. Warna cerah daun musim
gugur disebabkan terutama oleh timbunan antosianin pada hari cerah dan dingin,
walaupun karotenoid kuning atau jingga merupakan pigmen terbesar di daun musim
gugur pada beberapa spesies.
Antosianin umumnya tidak terdapat di lumut hati, ganggang, dan tumbuhan
tingkat rendah lainnya, walaupun beberapa antosianin dan flavonoida ada di lumut
tertentu. Antosianin jarang ditemui di gimnospermae, walaupun gimnospermae
mengandung jenis lain dari flavonoida. Beberapa macam antosianin terdapat di
tumbuhan tingkat tinggi, dan sering lebih dari satu macam terdapat di bunga tertentu
atau organ lain. Mereka dijumpai dalam bentuk glikosida, biasanya mengandung satu
tengah, atau pada gugus hidroksil di posisi 5 cincin A. Bila gula dihilangkan, maka
bagian sisa molekul, yang masih berwarna, dinamakan antosianidin (Salisbury, 1995).
2.3.1 Struktur Dasar Senyawa Flavonoida
Senyawa flavonoida adalah senyawa yang mengandung C15 terdiri atas dua inti
fenolat yang dihubungkan dengan tiga satuan karbon. Struktur dasar flavonoida dapat
digambarkan sebagai berikut :
C C C
A B
Gambar 1. Kerangka dasar senyawa flavonoida (Sastrohamidjojo,
1996).
2.3.2 Klasifikasi Senyawa Flavonoida
Flavonoida mengandung sistem aromatik yang terkonjugasi sehingga menunjukkan
pita serapan kuat pada daerah spektrum sinar ultraviolet dan spektrum sinar tampak,
umumnya dalam tumbuhan terikat pada gula yang disebut dengan glikosida
(Harborne, 1996). Dalam tumbuhan, flavonoida terdapat dalam berbagai struktur.
Keragaman ini disebabkan oleh perbedaan tahap modifikasi lanjutan dari struktur
dasar flavonoida tersebut, antara lain :
1. Flavonoida O-glikosida, satu gugus hidroksil flavonoida (atau lebih) terikat
pada satu gula (lebih) dengan ikatan hemiasetal yang tak tahan asam. Pengaruh
glikosilasi menyebabkan flavonoida menjadi kurang reaktif dan lebih mudah
larut dalam air. Glukosa merupakan gula yang paling umum terlibat dan gula
lain yang sering juga terdapat adalah galaktosa, ramnosa, xilosa, dan
arabinosa. Gula lain yang kadang-kadang ditemukan adalah alosa, manosa,
2. Flavonoida C-glikosida, gula terikat pada atom karbon flavonoida dan dalam
hal ini gula tersebut terikat langsung pada inti benzena dengan suatu ikatan
karbon-karbon yang tahan asam. Glikosida yang demikian disebut C-glikosida.
Jenis gula yang terlibat ternyata jauh lebih sedikit ketimbang jenis gula pada
O-glukosa, biasanya dari jenis glukosa yang paling umum, dan juga galaktosa,
ramnosa, xilosa, dan arabinosa.
3. Flavonoida sulfat, senyawa ini mengandung satu ion sulfat, atau lebih, yang
terikata pada hidroksil fenol atau gula. Senyawa ini sebenarnya bisulfat karena
terdapat sebagai garam, yaitu flavon-O-SO3
4. Biflavonoida, yaitu flavonoida dimer. Flavonoida yang biasanya terlibat adalah
flavon dan flavanon yang secara biosintesis mempunyai pola oksigenasi yang
sederhana 5,7,4’ dan ikatan antar flavonoida berupa ikatan-ikatan karbon atau
kadang-kadang eter. Monomer flavonoida yang digabungkan menjadi
biflavonoida dapat berjenis sama atau berbeda, dan letak ikatannya
berbeda-beda. Biflavonoida jarang ditemukan sebagai glikosida, dan penyebarannya
terbatas, terdapat terutama pada gimnospermae.
K. Banyak yang berupa glikosida
bisulfat, bagian bisulfat terikat pada hidroksil fenol yang mana saja yang masih
bebas atau pada gula.
5. Aglikon flavonoida yang aktif-optik, sejumlah aglikon flavonoida mempunyai
atom karbon asimetrik dan dengan demikian menunjukkan keaktifan optik
(yaitu memutar cahaya terpolarisasi-datar). Yang termasuk dalam golongan
flavonoida ini adalah flavanon, dihidroflavonol, katekin, rotenoid, dan lain-lain
(Markham, 1988).
Menurut Robinson (1995), flavonoida dapat dikelompokkan berdasarkan
keragaman pada rantai C3 yaitu :
1. Flavonol
Flavonol paling sering terdapat sebagai glikosida, biasanya 3-glikosida, dan aglikon
flavonol yang umum yaitu kamferol, kuersetin, dan mirisetin yang berkhasiat sebagai
antioksidan dan antiimflamasi. Flavonol lain yang terdapat di alam bebas kebanyakan
basa dioksidasi oleh udara tetapi tidak begitu cepat sehingga penggunaan basa pada
pengerjaannya masih dapat dilakukan.
O O
OH
flavonol
2. Flavon
Flavon berbeda dengan flavonol dimana pada flavon tidak terdapat gugusan
3-hidroksi. Hal ini mempunyai serapan UV-nya, gerakan kromatografi, serta reaksi
warnanya. Flavon terdapat juga sebagai glikosidanya lebih sedikit daripada jenis
glikosida pada flavonol. Flavon yang paling umum dijumpai adalah apigenin dan
luteolin. Luteolin merupakan zat warna yang pertama kali dipakai di Eropa. Jenis yang
paling umum adalah 7-glukosida dan terdapat juga flavon yang terikat pada gula
melalui ikatan karbon-karbon. Contohnya luteolin 8-C-glikosida. Flavon dianggap
sebagai induk dalam nomenklatur kelompok senyawa flavonoida.
O O
flavon
3. Isoflavon
Isoflavon merupakan isomer flavon, tetapi jumlahnya sangat sedikit dan sebagai
fitoaleksin yaitu senyawa pelindung yang terbentuk dalam tumbuhan sebagai
pertahanan terhadap serangan penyakit. Isoflavon sukar dicirikan karena reaksinya
tidak khas dengan pereaksi warna manapun. Beberapa isoflavon (misalnya daidzein)
kebanyakan yang lain tampak sebagai bercak lembayung yang pudar dengan amonia
berubah menjadi coklat.
O O
isoflavon
4. Flavanon
Flavanon terdistribusi luas di alam. Flavanon terdapat di dalam kayu, daun dan bunga.
Flavanon glikosida merupakan konstituen utama dari tanaman genus prenus dan buah
jeruk ; dua glikosida yang paling lazim adalah neringenin dan hesperitin, terdapat
dalam buah anggur dan jeruk.
O O
flavanon
5. Flavanonol
Senyawa ini berkhasiat sebagai antioksidan dan hanya terdapat sedikit sekali jika
dibandingkan dengan flavonoida lain. Sebagian besar senyawa ini diabaikan karena
konsentrasinya rendah dan tidak berwarna.
O O
OH
6. Katekin
Katekin terdapat pada seluruh dunia tumbuhan, terutama pada tumbuhan berkayu.
Senyawa ini mudah diperoleh dalam jumlah besar dari ekstrak kental Uncaria gambir
dan daun teh kering yang mengandung kira-kira 30% senyawa ini. Katekin berkhasiat
sebagai antioksidan.
Leukoantosianidin merupakan senyawa tan warna, terutama terdapat pada tumbuhan
berkayu. Senyawa ini jarang terdapat sebagai glikosida, contohnya melaksidin,
apiferol.
Antosianin merupakan pewarna yang paling penting dan paling tersebar luas dalam
tumbuhan. Pigmen yng berwarna kuat dan larut dalam air ini adalah penyebab hampir
semua warna merah jambu, merah marak , ungu, dan biru dalam daun, bunga, dan
buah pada tumbuhan tinggi. Secara kimia semua antosianin merupakan turunan suatu
struktur aromatik tunggal yaitu sianidin, dan semuanya terbentuk dari pigmen sianidin
ini dengan penambahan atau pengurangan gugus hidroksil atau dengan metilasi atau
O
OH
Antosianin
9.Khalkon
Khalkon adalah pigmen fenol kuning yang berwarna coklat kuat dengan sinar UV bila
dikromatografi kertas. Aglikon khalkon dapat dibedakan dari glikosidanya, karena
hanya pigmen dalam bentuk glikosida yang dapat bergerak pada kromatografi kertas
dalam pengembang air. (Harborne, 1996).
O
kalkon
10. Auron
Auron berupa pigmen kuning emas yang terdapat dalam bunga tertentu dan briofita.
Dalam larutan basa senyawa ini berwarna merah ros dan tampak pada kromatografi
kertas berupa bercak kuning, dengan sinar ultraviolet warna kuning kuat berubah
menjadi merah jingga bila diberi uap amonia. (Robinson, 1995).
HC
O
O
2.3.3 Sifat Kelarutan Flavonoida
Aglikon flavonoida adalah polifenol dan karena itu mempunyai sifat kimia senyawa
fenol, yaitu bersifat agak asam sehingga dapat larut dalam basa. Tetapi harus diingat,
bila dibiarkan dalam larutan basa, dan disamping itu terdapat oksigen, banyak yang
akan terurai. Karena mempunyai sejumlah gugus hidroksil, atau suatu gula, flavonoida
merupakan senyawa polar, maka umumnya flavonoida cukup larut dalam pelarut polar
seperti etanol (EtOH), metanol (MeOH), butanol (BuOH), aseton, dimetilsulfoksida
(DMSO), dimetilformamida (DMF), air dan lain-lain. Adanya gula yang terikat pada
flavonoida (bentuk yang umum ditemukan) cenderung menyebabkan flavonoida lebih
mudah larut dalam air dan dengan demikian campuran pelarut yang disebut diatas
dengan air merupakan pelarut yang lebih baik untuk glikosida. Sebaliknya, aglikon
yang kurang polar seperti isoflavon, flavanon dan flavon serta flavonol yang
termetoksilasi cenderung lebih mudah larut dalam pelarut seperti eter dan kloroform.
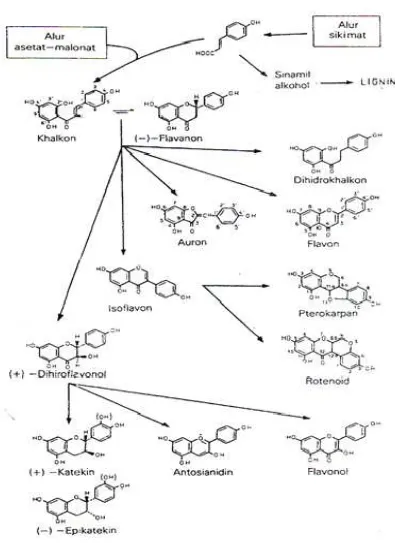
2.3.4. Biosintesa Flavonoida
Semua varian flavonoida saling berkaitan karena alur biosintesis yang sama, yang
memasukkan prazat dari alur sikimat dan alur asetat malonat, flavonoida pertama
dihasilkan segera setelah alur itu betemu. Flavonoida yang dianggap pertama kali
terbentuk pada biosintesis adalah Khalkon dan semua bentuk lain yang diturunkan
darinya melalui berbagai alur. Modifikasi flavonoida lebih lanjut terjadi pada berbagai
tahap dan manghasilkan : penambahan atau pengurangan hidroksilasi, metilasi gugus
hidroksil atau inti flavonoida, isoprenilasi gugus hidroksil atau inti flavonoida,
metilenasi gugus orto-dihidroksil, dimerisasi ( pembentukan biflavonoida ),
pembentukan bisulfate dan glikolisasi gugus hidroksil ( pembentukan flavonoida
2.4 Teknik Pemisahan
Tujuan dari teknik pemisahan adalah untuk memisahkan komponen yang akan
ditentukan berada dalam keadaan murni, tidak tercampur dengan
komponen-komponen lainnya. Ada 2 jenis teknik pemisahan:
1. Pemisahan kimia adalah suatu teknik pemisahan yang berdasarkan adanya
perbedaan yang besar dari sifat-sifat fisika komponen dalam campuran yang
akan dipisahkan.
2. Pemisahan fisika adalah suatu teknik pemisahan yang didasarkan pada
perbedaan-perbedaan kecil dari sifat-sifat fisik antara senyawa-senyawa yang
termasuk dalam suatu golongan (Muldja, 1995).
2.4.1 Ekstraksi
Ekstraksi dapat dilakukan dengan metoda maserasi, sokletasi, dan perkolasi. Sebelum
ekstraksi dilakukan, biasanya serbuk tumbuhan dikeringkan lalu dihaluskan dengan
derajat kehalusan tertentu, kemudian diekstraksi dengan salah satu cara di atas.
Ekstraksi dengan metoda sokletasi dapat dilakukan secara bertingkat dengan berbagai
pelarut berdasarkan kepolarannya, misalnya n-heksana, eter, benzena, kloroform, etil
asetat, etanol, metanol, dan air.
Ekstraksi dianggap selesai bila tetesan terakhir memberikan reaksi negatif
terhadap senyawa yang diekstraksi. Untuk mendapatkan larutan ekstrak yang pekat
biasanya pelarut ekstrak diuapkan dengan menggunakan alat rotari evaporator
(Harborne, 1996).
2.4.2 Kromatografi
Kromatografi merupakan suatu cara pemisahan fisik dengan unsur-unsur yang akan
dipisahkan terdistribusikan antara dua fasa, satu dari fasa-fasa ini membentuk lapisan
stasioner denagn luas permukaan yang besar dan yang lainnya merupakan cairan yang
Cara-cara kromatografi dapat digolongkan sesuai dengan sifat – sifat dari fasa
diam, yang dapat berupa zat padat atau zat cair. Jika fasa diam berupa zat padat
disebut kromatografi serapan, jika berupa zat cair disebut kromatografi partisi. Karena
fasa gerak dapat berupa zat cair atau gas maka ada empat macam sistem kromatografi
yaitu:
1) Fasa gerak cair–fasa diam padat (kromatografi serapan):
a.kromatografi lapis tipis
b.kromatografi penukar ion
2) Fasa gerak gas–fasa diam padat, yakni kromatografi gas padat
3) Fasa gerak cair–fasa diam cair (kromatografi partisi), yakni kromatografi
kertas.
4) Fasa gerak gas–fasa diam zat cair, yakni :
a. kromatografi gas–cair
b. kromatografi kolom kapiler
Semua pemisahan dengan kromatografi tergantung pada kenyataan bahwa senyawa –
senyawa yang dipisahkan terdistribusi diantara fasa gerak dan fasa diam dalam
perbandingan yang sangat berbeda – beda dari satu senyawa terhadap senyawa yang
lain (Sastrohamidjojo, 1991).
2.4.2.1 Kromatografi Lapis Tipis
Kromatografi Lapis Tipis pada plat berlapis yang berukuran lebih besar, biasanya
5x20 cm, 10x20 cm, atau 20x20 cm. Biasanya memerlukan waktu pengembangan 30
menit sampai satu jam. Pada hakikatnya KLT melibatkan dua fase yaitu fase diam
atau sifat lapisan, dan fase gerak atau campuran pelarut pengembang. Fase diam dapat
berupa serbuk halus yang berfungsi sebagai permukaan penyerap atau penyangga
untuk lapisan zat cair. Fase gerak dapat berupa hampir segala macam pelarut atau
campuran pelarut (Sudjadi, 1986).
Pemisahan senyawa dengan Kromatografi Lapis Tipis seperti senyawa organik
alam dan senyawa organik sintetik dapat dilakukan dalam beberapa menit dengan alat
yang harganya tidak terlalu mahal. Jumlah cuplikan beberapa mikrogram atau
pelarut dan jumlah cuplikan yang sedikit. Kromatografi Lapis Tipis (KLT) merupakan
salah satu metode pemisahan yang cukup sederhana
yaitu dengan menggunakan plat kaca yang dilapisi silika gel dengan menggunakan
pelarut tertentu (Gritter,1991).
Nilai utama Kromatografi Lapis Tipis pada penelitian senyawa flavonoida
ialah sebagai cara analisis cepat yang memerlukan bahan sangat sedikit. Menurut
Markham, Kromatografi Lapis Tipis terutama berguna untuk tujuan berikut:
1. Mencari pelarut untuk kromatografi kolom
2. Analisis fraksi yang diperoleh dari kromatografi kolom
3. Identifikasi flavonoida secara ko-kromatografi.
4. Isolasi flavonoida murni skala kecil
5. Penyerap dan pengembang yang digunakan umumnya sama dengan penyerap
dan pengembang pada kromatografi kolom dan kromatografi kertas (Markham,
1988).
2.4.2.2 Kromatografi Kolom
Kromatografi cair yang dilakukan dalam kolom besar merupakan metode
kromatografi terbaik untuk pemisahan dalam jumlah besar (lebih dari 1 g). Pada
kromatografi kolom, campuran yang akan dipisahkan diletakkan berupa pita pada
bagian atas kolom penyerap yang berada dalam tabung kaca, tabung logam, dan
tabung plastik. Pelarut atau fasa gerak dibiarkan mengalir melalui kolom karena
aliran yang disebabkan oleh gaya berat atau didorong dengan tekanan. Pita senyawa
linarut bergerak melalui kolom dengan laju yang berbeda, memisah, dan dikumpulkan
berupa fraksi ketika keluar dari atas kolom (Gritter, 1991).
Dengan menggunakan cara ini, skala isolasi flavonoida dapat ditingkatkan
hampir ke skala industri. Pada dasarnya, cara ini meliputi penempatan campuran
flavonoida (berupa larutan) diatas kolom yang berisi serbuk penyerap (seperti
memakai pelarut yang cocok. Kolom hanya berupa tabung kaca yang dilengkapi
dengan keran pada salah satu ujung (Markham, 1988).
2.4.2.3 Harga Rf (Reterdation Factor)
Mengidentifikasi noda-noda dalam lapisan tipis lazim menggunakan harga Rf yang
diidentifikasikan sebagai perbandingan antara jarak perambatan suatu zat dengan
jarak perambatan pelarut yang dihitung dari titik penotolan pelarut zat. Jarak yang
ditempuh oleh tiap bercak dari titik penotolan diukur dari pusat bercak. Untuk
mengidentifikasi suatu senyawa, maka harga Rf senyawa tersebut dapat dibandingkan
dengan harga Rf senyawa pembanding.
Jarak perambatan bercak dari titik penotolan
Rf =
Jarak perambatan pelarut dari titik penotolan (Sastrohamidjojo, 1991).
2.4.3 Kristalisasi
Kristalisasi adalah pengendapan kristal dari larutan yang terbuat dari bahan tertentu.
Selama proses pembentukan kristal, molekul akan cenderung menjadi melekat kristal
tumbuh terdiri dari jenis yang sama molekul karena cocok dalam kisi kristal untuk
molekul struktur yang sama daripada molekul yang lain. Jika proses kristalisasi
diperbolehkan untuk terjadi dalam mendekati – kondisi kesetimbangan, preferensi
molekul untuk deposit pada permukaan terdiri dari molekul seperti akan menyebebkan
peningkatan dalam kemurnian bahan kristal. Sehingga proses rekristalisasi adalah
salah satu metode yang paling penting tersedia bagi ahli kimia untuk pemurnian
padatan. Prosedur tambahan dapat dimasukkan kedalam proses kristalisasi untuk
menghilangkan pengotor. Termasuk filtrasi untuk menghilangkan pengotor yang
2.4.4 Rekristalisasi
Kristal yang diperoleh dari kolom dilarutkan kembali dengan EtOAc, diaduk hingga
semua kristal larut sempurna. Kemudian ditambahkan n – heksana secara perlahan –
lahan hingga pembentukan kembali senyawa yang lebih murni dari sebelumnya dan
jatuh di dasar wadah. Didekantasi larutan bagian atas wadah. Lalu diuapkan sisa
pelarut dari amorf hingga diperoleh kristal yang benar – benar bebas dari pelarut
(Jacobs,T.L, 1974).
2.5 Teknik Spektroskopi
Teknik spektroskopi adalah salah satu teknik analisis kimia–fisika yang mengamati
tentang interaksi atom atau molekul dengan radiasi elektromagnetik. Ada dua macam
instrumen pada teknik spektroskopi yaitu spektrometer dan spektrofotometer.
Instrumen yang memakai monokromator celah tetap pada bidang fokus disebut
sebagai spektrometer. Apabila spektrometer tersebut dilengkapi dengan detektor yang
bersifat fotoelektrik maka disebut spektrofotometer (Muldja, 1955).
Informasi Spektroskopi Inframerah menunjukkan tipe – tipe dari adanya gugus
fungsi dalam satu molekul dan Resonansi Magnetik Inti yang memberikan informasi
tentang bilangan dari setiap tipe dari atom hidrogen dan juga memberikan informasi
yang menyatakan tentang lingkungan dari setiap tipe dari atom hidrogen.
Kombinasinya dan data yang ada kadang – kadang menentukan struktur yang lengkap
dari molekul yang tidak diketahui (Pavia, 1979).
2.5.1 Spektrofotometri Ultra Violet
Serapan molekul di dalam derah ultra violet dan terlihat dari spektrum bergantung
pada struktur ultra elektronik dari molekul. Penyerapan sejumlah energi,
Spektrum Flavonoida biasanya ditentukan dalam larutan dengan pelarut
Metanol (MeOH) atau Etanol (EtOH). Spektrum khas terdiri atas dua maksima pada
rentang 240-285 nm (pita II) dan 300-550 nm (pita I). Kedudukan yang tepat dan
kekuatan nisbi maksima tersebut memberikan informasi yang berharga mengenai sifat
flavonoida dan pola oksigenasinya. Ciri khas spektrum tersebut ialah kekuatan nisbi
yang rendah pada pita I dalam dihidroflavon, dihidroflavonol, dan isoflavon serta
kedudukan pita I pada spektrum khalkon, auron dan antosianin yang terdapat pada
panjang gelombang yang tinggi.
Ciri spektrum golongan flavonoida utama dapat ditunjukkan sebagai berikut :
λ maksimum
2.5.2 Spektrofotometri Infra Merah (FT-IR)
Spektrum inframerah suatu molekul adalah hasil transisi antara tingkat energi getaran
yang berlainan. Pancaran inframerah yang kerapatannya kurang dari 100 cm -1
Penyerapan ini tercantum, namun spektrum getaran terlihat bukan sebagai
garis – garis melainkan berupa pita – pita. Hal ini disebabkan perubahan energi
getaran tunggal selalu disertai sejumlah perubahan energi putaran (Silverstein, 1986).
Dalam molekul sederhana beratom dua atau beratom tiga tidak sukar untuk
menentukan jumlah dan jenis vibrasinya dan menghubungkan vibrasi-vibrasi tersebut
dengan energi serapan. Tetapi untuk molekul-molekul beratom banyak, analisis
jumlah dan jenis vibrasi itu menjadi sukar sekali atau tidak mungkin sama sekali,
karena bukan saja disebabkan besarnya jumlah pusat – pusat vibrasi, melainkan
karena juga harus diperhitungkan terjadinya saling mempengaruhi (inter-aksi)
beberapa pusat vibrasi.
Vibrasi molekul dapat dibagi dalam dua golongan , yaitu vibrasi regang dan
vibrasi lentur.
1. Vibrasi regang
Di sini terjadi terus menerus perubahan jarak antara dua atom di didalam suatu
molekul. Vibrasi regang ini ada dua macam yaitu vibrasi regang simetris dan tak
simetri.
2.Vibrasi lentur
Di sini terjadi perubahan sudut antara dua ikatan kimia. Ada empat macam vibrasi
lentur yaitu vibrasi lentur dalam bidang yang dapat berupa vibrasi scissoring atau
vibrasi rocking dan vibrasi keluar bidang yang dapat berupa waging atau berupa
twisting (Noerdin, 1985).
2.5.3 Spektrometri Resonansi Magnetik Inti Proton (1H-NMR)
Spektrometri Resonansi Magnetik Inti (Nuclear Magnetic Resonance, NMR)
merupakan alat yang berguna pada penentuan struktur molekul organik. Teknik ini
memberikan informasi mengenai berbagai jenis atom hidrogen dalam molekul..
jumlah atom hidrogen dalam setiap lingkungan dan struktur gugusan yang berdekatan
dengan setiap atom hidroge (Cresswell, 1982).
Spektrometri Resonansi Magnetik Inti (Nuclear Magnetic Resonance, NMR)
pada umumnya digunakan untuk :
1. Menentukan jumlah proton yang memiliki lingkungan kimia yang sama pada
suatu senyawa organik.
2. Mengetahui informasi mengenai struktur suatu senyawa organic (Dachriyanus,
2004)
Pergeseran kimia adalah pengukuran medan dalam keadaan bebas. Semua
proton-proton dalam satu molekul yang ada dalam lingkungan kimia yang serupa
kadang-kadang menunjukkan pergeseran kimia yang sama. Setiap senyawa
memberikan penaikan menjadi puncak absorbsi tunggal dalam spektrum NMR. Di
dalam medan magnet, perputaran elektron-elektron valensi dari proton menghasilkan
medan magnet yang melawan medan magnet yang digunakan. Hingga setiap proton
dalam molekul dilindungi dari medan magnet yang digunakan dan bahwa besarnya
perlindungan ini tergantung pada kerapatan elektron yang mengelilinginya. Makin
besar kerapatan elektron yang mengelilingi inti, maka makin besar pula medan yang
dihasilkan yang melawan medan yang digunakan (Bernasconi,1995).
Senyawa yang paling lazim dan paling berguna dipakai sebagai acuan adalah
tetrametilsilana (TMS). Beberapa keuntungan dari pemakaian standar internal TMS
yaitu :
1. TMS mempunyai 12 proton yang setara sehingga akan memberikan
spektrum puncak tunggal yang kuat.
CH3
CH3 Si CH3
2. TMS merupakan cairan yang mudah menguap, dapat ditambahkan
kedalam larutan sampel dalam pelarut CDCl3 atau CCl4 (Silverstein,
1986).
Pada spektrometri RMI integrasi sangat penting. Harga integrasi menunjukkan
daerah atau luas puncak dari tiap – tiap proton . Sedangkan luas daerah atau luas
puncak tersebut sesuai dengan jumlah proton. Dengan demikian perbandingan tiap
integrasi proton sama dengan perbandingan jumlah proton dalam molekul
BAB 3
7. Kolom kromatografi Pyrex
8. Tabung reaksi Pyrex
9. Plat tetes
10.Rotari evaporator Büchi R-114
11.Statif dan klem
12.Lampu UV 254 nm/ 356 nm UVGL 58
13.Batang pengaduk
14.Alat Pengukur Titik Lebur Fisher
15.Neraca analitis Mettler AE 200
16.Pipet tetes
17.Penangas air Büchi B-480
18.Botol vial
19.Bejana Kromatografi Lapis Tipis
20.Spektrofotometer FT-IR Shimadzu
21.Spektrometer 1
22.Spektrofotometer UV-Visible
3.2 Bahan-Bahan
1. Kulit batang tumbuhan petai cina (L. glauca L.)
2. Metanol (Me-OH) Teknis
3. N-heksana Teknis
4. Etil asetat (EtOAc) Teknis
5. Aquadest
Sampel yang diteliti adalah kulit batang tumbuhan petai cina yang diperoleh dari
daerah
Sabulan, Kecamatan Sitio – tio, Kabupaten Samosir, Sumareta Utara. Kulit batang
tumbuhan
petai cina dikeringkan di udara terbuka, lalu dihaluskan sampai diperoleh serbuk kulit
batang
tumbuhan petai cina sebanyak 3000 g.
- Skrining fitokimia
3.3.2.1 Skrining Fitokimia
Untuk mengetahui adanya senyawa flavonoida pada kulit batang tumbuhan petai cina,
maka dilakukan uji pendahuluan secara kualitatif sebagai berikut :
Prosedur :
- Dimasukkan ± 10 gram serbuk kulit batang petai cina (L. glauca L.) yang telah
dikeringkan dan dipotong-potong kecil ke dalam erlenmeyer
- Ditambahkan metanol ± 100 ml
- Didiamkan
- Disaring
- Dibagi ekstrak metanol ke dalam 4 tabung reaksi
- Ditambahkan masing-masing pereaksi
a. Tabung I : dengan FeCl3
b. Tabung II : dengan H
5% menghasilkan larutan berwarna hitam
2SO4(p)
c. Tabung III : dengan Mg-HCl menghasilkan larutan berwarna merah muda menghasilkan larutan orange kekuningan
d. Tabung IV : dengan NaOH 10% menghasilkan larutan berwarna biru violet
3.3.3 Prosedur Memperoleh Ekstrak Pekat Lapisan Metanol dari Kulit Batang
Tumbuhan Petai Cina (L. glauca L.)
Serbuk kulit batang tumbuhan petai cina ditimbang sebanyak 3000 g, kemudian
dimaserasi dengan metanol sebanyak ± 10L sampai semua sampel terendam dan
dibiarkan selama ± 3 hari. Maserat ditampung dan dipekatkan dengan menggunakan
alat rotarievaporator sehingga diperoleh ekstrak pekat metanol. Kemudian diuapkan
hingga semua pelarut metanol menguap. Lalu dilakukan pemblokan tannin dengan
cara melarutkan fraksi metanol dengan etil asetat, dan disaring. Filtrat kemudian
dirotarievaporator lalu diuapkan hingga semua pelarut etil asetat menguap. Lalu fraksi
etil asetat dilarutkan dengan metanol dan dipartisi berulang-ulang dengan n-heksana.
rotarievaporator dan diuapkan sehingga diperoleh ekstrak pekat lapisan metanol
sebanyak 6,55 g.
3.3.4 Analisis Kromatografi Lapis Tipis (KLT)
Analisis Kromatografi Lapis Tipis dilakukan terhadap ekstrak metanol dengan
menggunakan fasa diam silika gel 60F254 Merck. Analisis ini dimaksudkan untuk
mencari pelarut yang sesuai didalam analisis kromatografi kolom. Pelarut yang
digunakan adalah campuran pelarut n-heksana : etil asetat. Fasa gerak yang digunakan
adalah campuran n-heksana : etil asetat dengan perbandingan (90:10 ; 80:20 ; 70:30 ;
60:40 v/v.
Prosedur:
Dimasukkan 10 ml larutan fase gerak n-heksana : etil asetat (90:10)v/v ke dalam
bejana kromatografi, kemudian dijenuhkan. Ditotolkan ekstrak pekat metanol pada
plat KLT yang telah diaktifkan. Dimasukkan plat ke dalam bejana yang telah berisi
pelarut yang telah dijenuhkan, lalu ditutup dan dielusi. Plat yang telah dielusi
dikeluarkan dari bejana, lalu dikeringkan dan difiksasi dengan pereaksi FeCl3 5%.
Diamati warna bercak yang timbul dan dihitung harga Rf yang diperoleh. Perlakuan
yang sama dilakukan untuk perbandingan pelarut n-heksana : etil asetat dengan
perbandingan (80:20)v/v; (70:30)v/v; dan (60:40)v/v.
Dari hasil analisis KLT menunjukkan bahwa di dalam kulit batang tumbuhan
petai cina terkandung senyawa flavonoida. Hasil pemisahan yang baik diberikan pada
fase gerak n-heksana : etil asetat (60:40)v/v (LAMPIRAN C).
3.3.5 Isolasi Senyawa Flavonoida dengan Kromatografi Kolom
ASTM dan fasa gerak yaitu n-heksana 100%, campuran pelarut n-heksana : etil asetat
dengan perbandingan (90:10) v/v, (80 : 20) v/v, (70:30)v/v, dan (60:40) v/v.
Prosedur :
Dirangkai alat kolom kromatografi. Terlebih dahulu dibuburkan silika gel 40 (70-230
mesh) ASTM dengan menggunakan n-heksana, diaduk hingga homogen lalu
dimasukkan ke dalam kolom kromatografi. Kemudian dielusi dengan menggunakan
n-heksan 100% hingga silika gel padat dan homogen. Dimasukkan 6,55 g ekstrak
metanol kulit batang petai cina ke dalam kolom kromatografi yang telah berisi bubur
silika gel, lalu ditambahkan fasa gerak n-heksana : etil asetat (90:10)v/v secara
perlahan-lahan, dan diatur sehingga aliran fasa yang keluar dari kolom sama
banyaknya dengan penambahan fasa gerak dari atas. Ditingkatkan kepolaran dengan
menambahkan fasa gerak n – heksana : etil asetat dengan perbandingan (80:20)v/v,
(70:30)v/v, dan (60:40)v/v. Hasil yang diperoleh ditampung dalam botol vial setiap 12
ml , lalu di KLT dan digabung fraksi dengan harga Rf yang sama lalu diuji dengan
FeCl3 5%. Kemudian diuapkan sampai terbentuk kristal.
3.3.6 Pemurnian
Senyawa yang diperoleh dari hasil isolasi kromatografi kolom harus dimurnikan.
Prosedur :
Kristal yang diperoleh dilarutkan kembali dengan etil asetat, diaduk hingga semua
kristal larut sempurna. Kemudian ditambahkan n – heksana secara perlahan–lahan
hingga terjadi pengendapan zat-zat pengotor di dasar wadah. Kemudian didekantasi
larutan bagian atas wadah, lalu diuapkan sisa pelarut dari kristal hingga diperoleh
3.3.7 Uji Kemurnian Hasil Isolasi dengan Kromatografi Lapis Tipis (KLT)
Uji kemurnian kristal dilakukan dengan kromatografi lapis tipis dengan menggunakan
fasa diam silika gel 60 F254 dengan fasa gerak n-heksana : etil asetat (60:40) v/v.
Prosedur :
Dimasukkan 10 ml larutan fasa gerak ke dalam bejana kromatografi, lalu dijenuhkan.
Ditotolkan kristal yang sebelumnya dilarutkan dengan etil asetat pada plat KLT.
Dimasukkan plat KLT tersebut ke dalam bejana kromatografi yang telah jenuh.
Setelah pelarut fasa gerak merembes sampai batas tanda, plat KLT dikeluarkan dari
bejana, dikeringkan, dan difiksasi dengan menggunakan pereaksi FeCl3 5% dalam
metanol menghasilkan bercak berwarna hitam yang menunjukkan adanya senyawa
flavonoida.
3.3.8 Penentuan Titik Lebur
Kristal hasil isolasi yang telah murni dimasukkan ke dalam alat pengukur titik lebur,
diatur suhu. Lalu diamati suhu sampai kristal melebur.
3.3.9 Identifikasi Senyawa Hasil Isolasi
3.3.9.1 Identifikasi dengan Spektrofotometer UV-Visible
Analisis dengan alat Spektrofotometer UV-Visible diperoleh dari Laboratorium Pusat
Penelitian Kimia - LIPI, Kawasan PUSPIPTEK Serpong, Tangerang dengan
3.3.9.2. Identifikasi dengan Spektrometer Resonansi Magnetik Inti Proton (1
H-NMR)
Analisis dengan alat Spektrometer 1H-NMR diperoleh dari Laboratorium Pusat
Penelitian Kimia - LIPI, Kawasan PUSPIPTEK Serpong, Tangerang dengan
menggunakan aseton sebagai pelarut.
3.3.9.3 Identifikasi dengan Spektrofotometer Inframerah (FT-IR)
Analisis dengan alat Spektrofotometer FT-IR diperoleh dari Laboratorium Pusat
3.4 Bagan Skrining Fitokimia
10 g serbuk kulit batang tumbuhan petai Cina
(
L. glauca L.
)
diekstraksi maserasi dengan metanol
disaring
dipekatkan
dibagi ke dalam 4 tabung reaksi
Tabung I
Larutan hitam
Larutan biru violet
Larutan merah muda
Larutan orange kekuningan
3.5 Bagan Penelitian
3000 g serbuk kulit batang tumbuhan
petai cina (L.glauca L.)
didiamkan selama 3 hari diulangi sebanyak 3 kali
Ekstrak metanol Residu
dimaserasi dengan metanol sebanyak 10 L
diskrining fitokimia
diuji KLT untuk mengetahui sistem eluen yang sesuai pada kromatografi kolom dikromatografi kolom dengan fase diam silika gel 60 GF (0,063-0,200 mm dan
fase gerak kln-heksan : etil asetat dengan perbandingan (90:10 ; 80:20 ; 70:30 ; 60:40 v/v ditampung tiap fraksi sebanyak 12 mL dalam botol vial
diuji KLT untuk mengetahui harga Rf digabung fraksi dengan harga Rf yang sama
diuapkan hingga semua etil asetat menguap dilarutkan dengan metanol
diekstraksi partisi dengan n-heksana sampai bening
Hasil Analisis diskrining fitokimia
Lapisan n-heksana (tidak dilanjutkan) Lapisan metanol
diuapkan hingga semua metanol menguap dilarutkan dengan etil asetat
disaring
dipekatkan dengan rotarievaporator
Fraksi 1-19
90 : 10 Fraksi 20-130
80 : 20
Hasil negatif Hasil negatif Hasil negatif Hasil negatif
ditentukan nilai Rf nya diuapkan
Tidak dilanjutkan Tidak dilanjutkan Tidak dilanjutkan Kristal Kuning
direkristalisasi di KLT ditimbang massa diuji titik lebur
dianalisis spektrofo-tometer
UV-Visible, FT-IR, 1H-NMR
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
Hasil skrining fitokimia terhadap ekstrak metanol dari kulit batang tumbuhan petai
cina (L. glauca L.) menunjukkan bahwa sampel positif terhadap pereaksi – pereaksi
flavonoida. Dimana pereaksi-pereaksinya adalah :
1. H2SO4 (p)
2. NaOH 10% memberikan warna biru violet memberikan warna orange kekuningan
3. FeCl3
4. Mg-HCl memberikan warna merah muda 5% memberikan warna hitam
Hasil isolasi senyawa flavonoida dari kulit batang tumbuhan petai cina
diperoleh dengan menggunakan fase gerak n-heksana : etil asetat (60:40)v/v, berwarna
kuning, berbentuk kristal, massa = 12 mg, positif terhadap pereaksi flavonoida, Rf =
0,65.
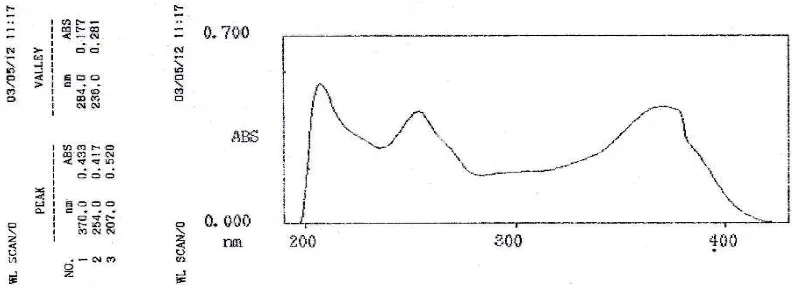
Dari hasil analisis spektrofotometer UV_Visible (Gambar 3. Spektrum
UV-Visible Senyawa Hasil Isolasi) memberikan 2 pita serapan panjang gelombang
Gambar 3. Spektrum UV-Visible Senyawa Hasil Isolasi
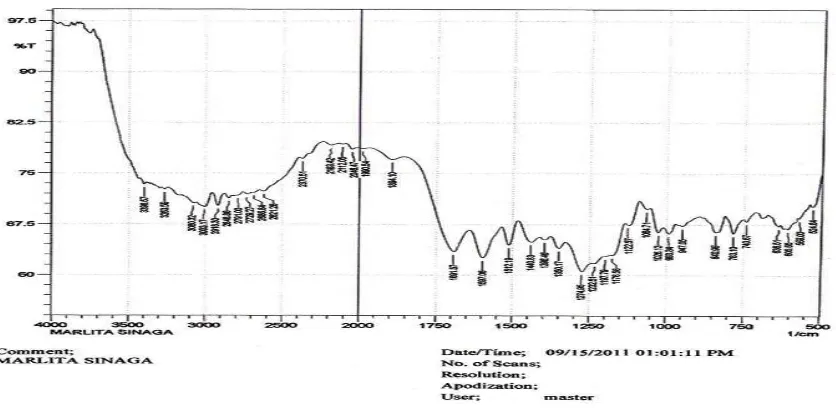
Hasil analisis Spektrofotometer FT-IR ( Gambar 4. Spektrum FT-IR Senyawa
Hasil Isolasi) menghasilkan pita–pita serapan pada daerah bilangan gelombang
sebagai berikut :
1. Pada bilangan gelombang 3080,17 - 3003 cm-1
2. Pada bilangan gelombang 2918,30 – 2848,86 cm
puncak melebar menunjukkan
adanya vibrasi ulur –CH aromatik
-1
3. Pada bilangan gelombang 1691,57 cm
puncak tajam menunjukkan
adanya vibrasi ulur –CH alifatik
-1
4. Pada bilangan gelombang 1597,06 – 1512,19 cm
puncak tajam menunjukkan adanya
vibrasi regang ikatan rangkap C=O dari keton
-1
puncak tajam menunjukkan
adanya serapan ikatan rangkap dari C=C regang, dan pada bilangan
gelombang 783,10 cm-1
5. Pada bilangan gelombang 1440,83 - 1350,17 cm
menunjukkan adanya C=C ulur dari sistim aromatik.
-1
puncak sedang
menunjukkan adanya vibrasi ulur dari –CH
6. Pada bilangan gelombang 1274,95 cm 3 -1
7. Pada bilangan gelombang 840,96 cm
puncak sedang menunjukkan adanya
vibrasi ulur C-O-C
-1
puncak sedang menunjukkan adanya
Gambar 4. Spektrum FT-IR Senyawa Hasil Isolasi
Hasil analisis Spektroskopi Resonansi Magnetik Inti Proton (H1-NMR)
senyawa hasil isolasi dengan menggunakan pelarut aseton-d6
1. Pergeseran kimia pada daerah δ= 3,8954 – 4,0186 ppm dengan puncak singlet
menunjukkan proton dari substituen –O-CH
dan TMS sebagai
standar yang memberikan signal – signal pergeseran kimia pada daerah sebagai
berikut :
2. Pergeseran kimia pada daerah δ= 6,9034 – 6,9099 ppm dengan puncak doblet
menunjukkan proton dari H
3
3. Pergeseran kimia pada daerah δ= 7,1226 – 7,1408 ppm dengan puncak doblet
menunjukkan proton-proton dari H 8
4. Pergeseran kimia pada daerah δ= 7,9035 – 7,9203 ppm dengan puncak doblet
menunjukkan proton-proton C-CH=CH-C pada posisi H 6
3’ dan H
5. Pergeseran kimia pada daerah δ= 8,1317 – 8,1499 ppm dengan puncak doblet
menunjukkan proton-proton C-CH=CH-C pada posisi H
5’
Gambar 5. Spektrum 1H-NMR Senyawa Hasil Isolasi
4.2 Pembahasan
Dari hasil kromatografi lapis tipis, diketahui bahwa perbandingan pelarut yang baik
untuk mengisolasi senyawa flavonoida dari kulit batang tumbuhan petai cina adalah
n-heksana : etil asetat (60:40)v/v yang menunjukkan pemisahan yang lebih baik dari
noda yang dihasilkan. Hal ini juga dibuktikan dengan analisis KLT yang menunjukkan
hanya satu noda tunggal pada kristal.
Seperti yang telah diketahui bahwa flavonoida merupakan senyawa turunan
dari fenolik dimana strukturnya dibentuk dari cincin aromatik A dan cincin aromatik
B yang dihubungkan oleh cincin C yang terdiri dari gugus fungsi karbonil dan gugus
fungsi eter. Untuk mengetahui adanya gugus fungsi dari senyawa flavonoida ini maka
diperlukan analisa spektroskopi FT-IR, sedangkan untuk menentukan golongan dari
bentuk peak dan posisi pada ppm dari protonnya diperlukan analisa spektroskopi 1
H-NMR.
Berdasarkan Spektrum UV-Visible dengan pelarut metanol dari senyawa
flavonoida yang diisolasi, memberikan 2 pita serapan panjang gelombang yaitu pita I
dengan λ=370 nm dan pita II dengan λ=254 nm. Menurut literatur (Markham,1988) ada dua kemungkinan penggolongan dari flavonoida ini yaitu flavon dan
flavonol.Yang membedakan ke dua penggolongan ini adalah letak -OH pada posisi
C3. Melihat pembanding dari Markham tersebut, senyawa hasil isolasi ini memang
lebih dominan ke flavonol akan tetapi jika dilihat dari spektrum 1H-NMR tidak
ditemukan adanya peak -OH dengan kata lain -OH tersubstitusi dan didukung juga
oleh spektrum FT-IR tidak ditemukan peak untuk -OH sehingga senyawa hasil isolasi
yang diperoleh digolongkan pada flavonoida jenis flavon.
Dari spektrum FT-IR menunjukkan adanya vibrasi gugus C=O pada frekuensi
1691,57 cm-1, adanya vibrasi gugus C-O-C pada frekuensi 1274,95 cm-1. Ini
membuktikan bahwa ada cincin C yang menghubungkan cincin A dan cincin B pada
senyawa hasil isolasi. Untuk senyawa aromatik terlihat adanya vibrasi gugus C=C
pada frekuensi 1597,06-1512,19 cm-1, adanya vibrasi C-H aromatik pada frekuensi
3080,17-3003 cm-1.
Dari spektrum 1H-NMR menunjukkan adanya senyawa aromatik terdapat pada
peak 6-8 ppm (Mabry, 1970). Dari data 1
1. Pergeseran kimia pada daerah δ = 6,9034-7,1408 ppm dengan
puncak doblet menunjukkan proton cincin A (Lampiran F. dan
Lampiran H.2.)
H-NMR pada senyawa hasil isolasi
ditunjukkan :
2. Pergeseran kimia pada daerah δ = 7,9035- 8,1499 ppm dengan
puncak doblet menunjukkan proton cincin B (Lampiran F. dan
Lampiran H.1.)
3. Pergeseran kimia pada daerah δ = 3,8954 – 4,0186 ppm dengan
Letak O-CH3 kami duga berada pada cincin A diposisi C5, C7 , berada pada
cincin B diposisi 4’ dan kami menduga bahwa –OH pada C5 tidak ada karena peak 1
H-NMR dari OH pada 12 ppm tidak muncul. Posisi doblet dari cincin A yaitu kopling (
penggandengan ) pada H6 dan H8,sedangkan posisi doblet pada cincin B yaitu kopling
pada H3’ dan H5’ serta kopling pada H2’ dan H6’(Mabry, 1970). Kemudian kami
menduga –O-CH3 pada cincin C berada diposisi C3 karena pada spektrum 1H-NMR
sama sekali tidak ada spektrum yang menunjukkan proton C3.
Jadi dari data spektrum UV-Visible, FT-IR dan 1
O
H-NMR kami menduga kemungkinan
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Hasil isolasi yang diperoleh dari 3000 g kulit batang tumbuhan petai cina (
L.glauca. L. ) merupakan Kristal berwarna kuning, diperoleh sebanyak 12 mg,
Rf = 0,65.
2. Berdasarkan hasil skrining fitokimia flavonoida terhadap Kristal hasil isolasi
dari kulit batang tumbuhan petai cina ( L.glauca. L. ), menunjukkan hasil yang
positif mengandung senyawa flavonoida.
3. Hasil analisis dengan skrining fitokimia pereaksi – pereaksi flavonoida,
Spektrofotometri UV-Visible,Infra Merah (FT – IR) dan Resonansi Magnetik
Inti Proton (1H-NMR) menunjukkan bahwa kristal hasil isolasi dari kulit
batang tumbuhan petai cina (L.glauca. L. ) adalah senyawa flavonoida jenis
flavon.
5.2 Saran
Perlu dilakukan analisis Spektroskopi Massa, 13C-NMR agar diperoleh data –
data yang lebih mendukung untuk menentukan struktur senyawa flavonoida yang
DAFTAR PUSTAKA
Bernasconi, G. 1995. Teknologi Kimia. Jilid 2. Edisi Pertama. Jakarta : PT. Pradaya
Paramita.
Cresswell, C.J., dkk. 1982. Analisis Spektrum Senyawa Organik. Edisi Kedua. Bandung : Penerbit ITB.
Dachriyanus. 2004. Analisis Struktur Senyawa Organik Secara Spektroskopi. Padang : Andalas University Press.
Dalimartha, S. 200. Atlas Tumbuhan Obat di Indonesia. Jakarta : Trubus Agriwidya.
Fauziyah, N. 2008. Efek Antiinflamasi Ekstrak Etanol Daun Petai Cina (Leucaena glauca, Benth) pada Tikus Putih Jantan Galur Wistar. Universitas Muhammadiyah Surakarta : Surakarta.
Gritter, R.J.1991. Pengantar Kromatografi. Terbitan ke-2. Terjemahan Kokasih Padmawinata. Bandung : Penerbit ITB.
Harborne, J.B. 1987. Metoda Fitokimia, Penuntun Cara Modern Menganalisa Tumbuhan. Terbitan ke-2 . Terjemahan Kokasih Padmawinata dan Iwang Soediro. Bandung : Penerbit ITB.
Manitto, P. 1992. Biosintesis Produk Alami. Cetakan Pertama. Terjemahan Koensoemardiyah. Semarang : Penerbit IKIP Press.
Mabry, T.J., dkk. 1970. The Systematic Identification of Flavonoids. New York : Springer Verlag.
Markham, K.R. 1988. Cara Mengidentifikasi Flavonoida. Terjemahan Kokasih Pradmawinata. Bandung : ITB Press.
Muldja, M.H. 1995. Analisis Instrumental. Cetakan Pertama. Surabaya : Universitas Airlangga Press.
Noerdin, D. 1985. Elusidasi Struktur Senyawa Organik dengan Cara Spektroskopi Ultra Lembayung dan Inframerah. Edisi Pertama. Bandung : Penerbit Angkasa.
Pasto, D.J. 1992. Experiment and Techniquein Organic Chemistry. New Jersey : Prantice Hall, Inc.
Pavia, L.D. 1979. Introduction to Spectroscopy a Guide for Students of Organic Chemistry. Philladelphia : Saunders College.
Salisbury, F.B. 1995. Fisiologi Tumbuhan. Edisi Ke-4. Jilid 2. Bandung : Penerbit
ITB.
Sastrohamidjojo, H. 1985. Kromatografi. Edisi Pertama. Cetakan Pertama Yogyakarta : Penerbit Liberty.
Sastrohamidjojo, H. 1996. Sintesis Bahan Alam. Yogyakarta : Penerbit Gadjah Mada University Press.
Silverstein, R. M. 1986. Penyidikan Spektrometrik Senyawa Organik. Terjemahan A. J. Hatomo dan Anny Viktor Purba. Edisi ke-4. Jakarta : Penerbit Erlangga.
Sudjadi. 1986. Metode Pemisahan. Yogyakarta : Penerbit Kanisius.
Tobing, R. L. 1989. Kimia Bahan Alam. Departemen Pendidikan dan Kebudayaan. Direktorat Jenderal Pendidikan Tinggi. Jakarta : Proyek Pembangunan Lembaga Pendidikan Tenaga Kependidikan.
Underwood, A.L. 1981. Analisa Kimia Kuantitatif. Edisi ke-4. Jakarta : Erlangga.
Wina, E., dkk. 1993. Analisis Kuantitatif Karotenoid dari Daun Lamtoro sebagai Pakan Ayam. Proceedings Semnas Kimia dan Pembangunan. Himpunan Kimia Bandung. Hlm 193 - 203
LAMPIRAN C . Kromatogram Lapisan Tipis Ekstrak Pekat Lapisan Metanol Kulit Batang Petai Cina (L. glauca L.)
Keterangan :
Fasa diam :
Kieselgel 60 F
E : Ekstrak Pekat Lapisan Metanol Kulit Batang petai Cina
254
(Leucaena glauca L.)
I : Fasa gerak n-heksana : etil asetat (90:10 v/v) II : Fasa gerak n-heksana : etil asetat (80:20 v/v) III : Fasa gerak n-heksana : etil asetat (70:30 v/v) IV : Fasa gerak n-heksana : etil asetat (60:40 v/v)
I II III IV
E E E E
No. Fasa Gerak Jumlah Noda Rf
1. n-heksana : etil asetat (90 : 10 v/v) 0 0 2. n-heksana : etil asetat (80 : 20 v/v) 0 0
3. n-heksana : etil asetat (70 : 30 v/v) 2
0,19 0,32
4. n-heksana : etilasetat (60 : 40 v/v) 3
LAMPIRAN D. Hasil Kromatografi Lapis Tipis Senyawa Hasil Isolasi Melalui Penampakan Noda Dengan Pereaksi
I II
F F
Keterangan :
Fase diam : Silika gel 60 F
F : Senyawa hasil isolasi 254
I : FeCl3
II : NaOH 10% (berwarna biru violet) 5% (berwarna hitam)
Data harga Rf dari bercak noda :
No. Penampakan bercak Pereaksi Warna Noda Rf
1. I FeCl3 5% Hitam 0,65
LAMPIRAN E. Spektrum UV-Visible Senyawa Pembanding Flavonoida ( Markham,
LAMPIRAN H. Spektrum 1
1. Spektrum NMR of 3,4’,5,6,7,8-Hexamethoxyflavone in CDCl
H-NMR Senyawa Pembanding Flavonoida ( Mabry,
1970 )
3