AKTIVITAS ANTIOKSIDAN EKSTRAK UMBI BENGKOANG
PADA BERBAGAI UMUR PANEN DENGAN METODE DPPH
(
2,2-diphenyl-1-picrylhydrazyl
)
SKRIPSI
Oleh:
JUNI ANNIDA LINTANG
090305037/ILMU DAN TEKNOLOGI PANGAN
PROGRAM STUDI ILMU DAN TEKNOLOGI PANGAN
FAKULTAS PERTANIAN
AKTIVITAS ANTIOKSIDAN EKSTRAK UMBI BENGKOANG
PADA BERBAGAI UMUR PANEN DENGAN METODE DPPH
(
2,2-diphenyl-1-picrylhydrazyl
)
SKRIPSI
Oleh:
JUNI ANNIDA LINTANG
090305037/ILMU DAN TEKNOLOGI PANGAN
Skripsi sebagai salah satu syarat untuk memperoleh gelar sarjana di Fakultas Pertanian
Universitas Sumatera Utara
PROGRAM STUDI ILMU DAN TEKNOLOGI PANGAN
FAKULTAS PERTANIAN
Judul Skripsi : Aktivitas Antioksidan Ekstrak Umbi Bengkoang pada Berbagai Umur Panen dengan Metode DPPH
(2,2-diphenyl-1-picrylhydrazyl) Nama : Juni Annida Lintang
NIM : 090305037
Program Studi : Ilmu dan Teknologi Pangan
Disetujui Oleh, Komisi Pembimbing
Dr. Ir. Herla Rusmarilin, MP Linda Masniary Lubis, STP, M.Si Ketua Anggota
Mengetahui:
Dr. Ir. Herla Rusmarilin, MP Ketua Program Studi
ABSTRAK
Juni Annida Lintang. Aktivitas Antioksidan Ekstrak Umbi Bengkoang pada Berbagai Umur Panen dengan Metode DPPH (2,2-diphenyl-1-picrylhydrazyl), dibimbing oleh Herla Rusmarilin dan Linda Masniary Lubis.
Bengkoang merupakan Famili Fabaceae yang potensial sebagai sumber antioksidan karena kaya akan flavonoid dan fitoestrogen. Penelitian dilakukan dalam tiga tahap. Tahap I: Pembuatan tepung bengkoang dengan satu faktor, yaitu: umur panen (U): (3, 4, dan 5 bulan). Tahap II: Pembuatan ekstrak metanolik bengkoang dengan satu faktor, yaitu: umur panen (U): (3,4, dan 5 bulan). Tahap III: Uji aktivitas antioksidan ekstrak metanolik fraksi eter/air dengan 2 faktor, yaitu: konsentrasi (K): (10, 20, 40, 80, 160 ppm) dan umur panen (U): (3, 4, dan 5 bulan).
Hasil penelitian menunjukkan umur panen berpengaruh berbeda sangat nyata terhadap komposisi proksimat tepung bengkoang dan rendemen ekstrak metanolik yang dihasilkan. Kadar air, kadar abu, dan kadar lemak cenderung menurun dengan meningkatnya umur panen. Sedangkan kadar serat kasar cenderung meningkat. Kadar protein tepung bengkoang dan rendemen ekstrak metanolik maksimum pada umur 4 bulan dan cenderung menurun pada umur 5 bulan. Interaksi konsentrasi ekstrak dan umur panen berpengaruh berbeda sangat nyata terhadap aktivitas antioksidan. Antioksidan fraksi eter cenderung meningkat sedangkan antioksidan fraksi air cenderung menurun dengan meningkatnya umur panen. Antioksidan ekstrak metanolik bengkoang tergolong kuat karena IC50 fraksi eter/air kurang dari 100ppm.
Kata kunci : Antioksidan, DPPH, fraksi eter, fraksi air
ABSTRACT
Juni Annida Lintang. Antioxidant Activity of Jicama Roots (Bengkoang) in
Several Harvesting Age Using DPPH Method (2,2-diphenyl-1-picrylhydrazyl), supervised
by Herla Rusmarilin and Linda MasniaryLubis.
Jicama or yam bean is Fabaceae Family which is potential as a source of antioxidants as it is rich in flavonoid and phytoestrogen. The research was performed in three stages. Stage I: Making of jicama flour with one factor (harvesting age (U): (3, 4, and 5 months). Stage II: Making of jicama methanolic extract with one factor (harvesting age (U): (3, 4, and 5 months). Stage III: Estimating the antioxidant activity of ether/water fractions of methanolic extract with two factors i.e: concentration (K): (10, 20, 40, 80, 160 ppm) and harvesting age (U): (3,4, and 5 months).
The results showed that the harvesting age had highly significant effect on proximate composition of jicama flour and yield of methanolic extract. Moisture content, ash content, and fat content tended to decrease with increasing harvesting age. Meanwhile, crude fiber content tended to increase. The protein content of jicama flour and yield of methanolic extract were maximum at 4 month harvest and tended to decrease at 5 months. The interaction of concentration and harvesting age had highly significant effect on antioxidant activity. The antioxidant of ether fraction tended to increase, but the antioxidant of the water fraction tended to decrease with increasing the harvesting age. The antioxidant of jicama methanolic extract is categorized as a strong antioxidant because the IC50 ether/water fractions were less than 100 ppm.
RIWAYAT HIDUP
Penulis dilahirkan di Medan 08 Juni 1991. Penulis merupakan anak ke-2 dari 3 bersaudara dari Ayahanda Hamsir Lintang dan Ibunda Suasa M. Nur Lubis. Penulis lulus SNMPTN (Seleksi Nasional Masuk Perguruan Tinggi Negeri) tahun 2009 di Program Studi Ilmu dan Teknologi Pangan, Fakultas Pertanian, Universitas Sumatera Utara. Sebelum menjadi mahasiswa, penulis menempuh pendidikan formal di SD Negeri 060834 Medan (1997-2003), SMP Negeri 1 Medan (2003-2006), dan SMA Negeri 4 Medan (2006-2009).
Selama menjadi mahasiswa, penulis memiliki pengalaman berorganisasi di (1) BKM Al-Mukhlisin FP USU sebagai Sekretaris Divisi DIKLAT (2009-2010), Bendahara Divisi Ukhuwah Islamiyah (2010-2011), dan staf Divisi Kaderisasi (2011-2012); (2) IMITP FP USU sebagai staf divisi kewirausahaan (2010-2011), (3) KAMMI Komisariat Nusantara USU sebagai Bendahara Umum (2010-2011); dan (4) HMPPI (Himpunan Mahasiswa Peduli Pangan Indonesia) sebagai Koordinator Regional Sumatera (2011-2013).
KATA PENGANTAR
Puji dan syukur penulis ucapkan kepada Allah SWT atas limpahan berkah dan nikmat-Nya yang telah memelihara dan memberi kesehatan serta kemudahan kepada penulis, sehingga skripsi ini dapat selesai. Judul penelitian pada skripsi ini adalah “Aktivitas Antioksidan Ekstrak Umbi Bengkoang pada Berbagai Umur Panen dengan Metode DPPH (2,2-diphenyl-1-picrylhydrazyl)”.
Selama menyelesaikan skripsi, penulis banyak mendapat bantuan dan bimbingan dari berbagai pihak. Oleh karena itu, penulis mengucapkan terima kasih kepada :
1. Kedua orangtua tercinta Ayahanda H. Lintang dan Ibunda Suasa M. Nur Lubis atas kasih sayang, didikan, dan dukungan yang selama ini diberikan. Semoga Allah selalu memberkahi hidup keduanya. Aamiin.
2. Ibu Dr. Ir. Herla Rusmarilin, MP. selaku ketua komisi pembimbing yang begitu banyak memberikan inspirasi, mengajarkan banyak ilmu, membantu dalam teknis penelitian dan penulisan skripsi.
3. Ibu Linda Masniary Lubis STP, M.Si sebagai anggota komisi pembimbing yang telah sabar dan bersedia meluangkan waktu, tenaga, dan pikiran untuk membimbing dan mengarahkan selama penyusunan skripsi ini.
4. Bapak Prof. Dr. Ir. Zulkifli Lubis, M.App.Sc dan Ibu Mimi Nurminah, STP, M.Si yang telah bersedia menguji penulis dalam ujian meja hijau.
6. Kakak Ara Ridanti Lintang dan Adik Ahmad Muhaisin Lintang atas segala perhatian, dukungan, dan bantuannya.
7. Teman-temanku Food Techno09 alias ITP09 yang banyak memberikan pengalaman berharga. Teman-temanku di BKM Al-Mukhlisin, KAMMI, HMPPI (BPP, BPR, Bapes) dan HMPPI Regional I Sumatera (UGP, Unsyiah, USU, Unand, UR, Unja, dan Unsri), dan promotor SingkongDay, ukhuwah yang begitu indah kawan takkan dilupa, insya Allah.
8. Kakak/abang senior dan adik-adik junior ITP USU
9. Asisten LTP angkatan 2009, 2010, dan semua anak magang LTP angkatan 2011.
DAFTAR ISI
Kegunaan Penelitian ... 6
Hipotesis Penelitian ... 6
TINJAUAN PUSTAKA ... 7
METODE PENELITIAN ... 22
Waktu dan Tempat Penelitian ... 22
Bahan Penelitian ... 22
Alat Penelitian ... 22
Metode Penelitian ... 23
Model Rancangan ... 24 Pelaksanaa Pembuatan tepung bengkoang ... 25
Pembuatan ekstrak metanolik bengkoang ... 26
Pembuatan larutan ekstrak metanolik fraksi eter / air ... 26
Pengamatan dan Pengukuran Data ... 26
Kadar air ... 27
Kadar abu ... 27
Kadar serat kasar ... 27
Kadar lemak ... 29
Rendemen ... 29
Uji aktivitas antioksidan fraksi eter dan air ... 30
HASIL DAN PEMBAHASAN ... 34
Tahap I: Pembuatan Tepung Bengkoang ... 34
Kadar air (%bk) ... 35
Kadar abu (%bk) ... 36
Kadar lemak (%bk) ... 38
Kadar protein (%bk) ... 39
Kadar serat kasar (%bk) ... 41
Tahap II: Pembuatan Ekstrak Metanolik Bengkoang ... 43
Rendemen (%) ... 43
Tahap III: Uji Aktivitas Antioksidan Ekstrak Metanolik Fraksi Eter/Air ... 46
Pengaruh interaksi antara umur panen umbi bengkoang dengan konsentrasi ekstrak metanolik fraksi eter terhadap aktivitas antioksidan (% peredaman DPPH) ... 50
Pengaruh interaksi antara umur panen umbi bengkoang dengan konsentrasi ekstrak metanolik fraksi air terhadap aktivitas antioksidan (% peredaman DPPH) ... 52
Nilai IC50 hasil pengujianaktivitas antioksidan (ppm) ... 54
KESIMPULAN DAN SARAN ... 60
Kesimpulan ... 60
Saran ... 61
DAFTAR PUSTAKA ... 62
DAFTAR TABEL
No. Hal
1. Komposisi zat gizi umbi bengkoang ... 9
2. Komposisi zat gizi umbi dan tepung bengkoang ... 11
3. Komposisi kimia tepung bengkoang umur panen 3 bulan, 4 bulan, dan 5 bulan ... 34
4. Rendemen ekstrak metanolik ... 43
5. Rendemen ekstrak metanolik fraksi eter ... 45
6. Rendemen ekstrak metanolik fraksi air ... 45
7. Aktivitas antioksidan ekstrak metanolik fraksi eter dan fraksi air ... 47
8. Uji LSR efek utama interaksi antara konsentrasi ekstrak metanolik fraksi eter terhadap aktivitas antioksidan (% peredaman DPPH) ... 51
9. Uji LSR efek utama interaksi antara konsentrasi ekstrak metanolik fraksi eter terhadap aktivitas antioksidan (% peredaman DPPH) ... 53
DAFTAR GAMBAR
No. Hal
1. Ilustrasi tanaman bengkoang ... 7
2. Struktur kimia flavonoid ... 14
3. Struktur kimia radikal bebas DPPH ... 20
4. Reaksi Penangkapan atom H dari antioksidan oleh DPPH ... 20
5. Skema pembuatan tepung bengkoang ... 31
6. Skema pembuatan ekstrak metanolik bengkoang ... 32
7. Skema uji aktivitas antioksidan ekstrak metanolik fraksi eter/air ... 33
8. Hubungan antara umur panen umbi bengkoang dengan kadar air (%bk) ... 35
9. Hubungan antara umur panen umbi bengkoang dengan kadar abu (%bk) ... 37
10. Hubungan antara umur panen umbi bengkoang dengan kadar lemak (%bk) ... 38
11. Hubungan antara umur panen umbi bengkoang dengan kadar protein (%bk) ... 40
12. Hubungan antara umur panen umbi bengkoang dengan kadar serat kasar (%bk) ... 42
13. Hubungan antara umur panen umbi bengkoang dengan rendemen ekstrak metanolik (%) ... 44
14. Struktur kimia katekin ... 48
15. Struktur kimia daidzein ... 48
16. Struktur kimia daidzein-7-O-β-glucopiranose ... 49
17. Struktur kimia (8,9)-Furanyl-pterocarpan-3-ol ... 49
18. Struktur kimia 5-hydroxy-daidzein-7-O- β-glucopiranose ... 49
20. Struktur kimia 2-butoxy-2,5-bis(hydroxymethyl)-tetrahydrofurane-
3,4-diol ... 49
21. Hubungan interaksi antara konsentrasi ekstrak metanolik fraksi eter dengan umur panen umbi bengkoang terhadap aktivitas antioksidan fraksi eter (%) ... 51
22. Hubungan interaksi antara konsentrasi ekstrak metanolik fraksi air dengan umur panen umbi bengkoang terhadap aktivitas antioksidan fraksi air (%) ... 53
23. Struktur DPPH radikal dan DPPH nonradikal ... 55
24. Nilai IC50 Aktivitas antioksidan penangkal radikal bebas DPPH ... 56
25. Struktur kimia BHT (Butylated Hydroxy Toluene) ... 57
DAFTAR LAMPIRAN
No. Hal 1. Daftar analisis sidik ragam kadar air tepung bengkoang dan uji
LSR efek utama pengaruh umur panen terhadap kadar air ... 66 2. Daftar analisis sidik ragam kadar abu tepung bengkoang dan uji
LSR efek utama pengaruh umur panen terhadap kadar abu ... 67 3. Daftar analisis sidik ragam kadar abu tepung bengkoang dan uji
LSR efek utama pengaruh umur panen terhadap kadar lemak ... 68 4. Daftar analisis sidik ragam kadar abu tepung bengkoang dan uji
LSR efek utama pengaruh umur panen terhadap kadar protein ... 69 5. Daftar analisis sidik ragam kadar abu tepung bengkoang dan uji
LSR efek utama pengaruh umur panen terhadap kadar serat kasar ... 70 6. Daftar analisis sidik ragam rendemen ekstrak metanolik dan uji
LSR efek utama pengaruh umur panen terhadap rendemen ekstrak
metanolik bengkoang ... 71 7. Daftar analisis sidik ragam rendemen ekstrak metanolik fraksi eter ... 72 8. Daftar analisis sidik ragam rendemen ekstrak metanolik fraksi air ... 73 9. Daftar analisis sidik ragam aktivitas antioksidan ekstrak metanolik
fraksi eter umbi bengkoang dan uji LSR efek utama pengaruh konsentrasi ekstrak dengan umur panen terhadap aktivitas
antioksidan ... 74 10. Daftar analisis sidik ragam aktivitas antioksidan ekstrak metanolik
fraksi air umbi bengkoang dan uji LSR efek utama pengaruh konsentrasi ekstrak dengan umur panen terhadap aktivitas
antioksidan ... 76 11. Daftar analisis sidik rgam IC50 berbagai senyawa uji dan Uji LSR
ABSTRAK
Juni Annida Lintang. Aktivitas Antioksidan Ekstrak Umbi Bengkoang pada Berbagai Umur Panen dengan Metode DPPH (2,2-diphenyl-1-picrylhydrazyl), dibimbing oleh Herla Rusmarilin dan Linda Masniary Lubis.
Bengkoang merupakan Famili Fabaceae yang potensial sebagai sumber antioksidan karena kaya akan flavonoid dan fitoestrogen. Penelitian dilakukan dalam tiga tahap. Tahap I: Pembuatan tepung bengkoang dengan satu faktor, yaitu: umur panen (U): (3, 4, dan 5 bulan). Tahap II: Pembuatan ekstrak metanolik bengkoang dengan satu faktor, yaitu: umur panen (U): (3,4, dan 5 bulan). Tahap III: Uji aktivitas antioksidan ekstrak metanolik fraksi eter/air dengan 2 faktor, yaitu: konsentrasi (K): (10, 20, 40, 80, 160 ppm) dan umur panen (U): (3, 4, dan 5 bulan).
Hasil penelitian menunjukkan umur panen berpengaruh berbeda sangat nyata terhadap komposisi proksimat tepung bengkoang dan rendemen ekstrak metanolik yang dihasilkan. Kadar air, kadar abu, dan kadar lemak cenderung menurun dengan meningkatnya umur panen. Sedangkan kadar serat kasar cenderung meningkat. Kadar protein tepung bengkoang dan rendemen ekstrak metanolik maksimum pada umur 4 bulan dan cenderung menurun pada umur 5 bulan. Interaksi konsentrasi ekstrak dan umur panen berpengaruh berbeda sangat nyata terhadap aktivitas antioksidan. Antioksidan fraksi eter cenderung meningkat sedangkan antioksidan fraksi air cenderung menurun dengan meningkatnya umur panen. Antioksidan ekstrak metanolik bengkoang tergolong kuat karena IC50 fraksi eter/air kurang dari 100ppm.
Kata kunci : Antioksidan, DPPH, fraksi eter, fraksi air
ABSTRACT
Juni Annida Lintang. Antioxidant Activity of Jicama Roots (Bengkoang) in
Several Harvesting Age Using DPPH Method (2,2-diphenyl-1-picrylhydrazyl), supervised
by Herla Rusmarilin and Linda MasniaryLubis.
Jicama or yam bean is Fabaceae Family which is potential as a source of antioxidants as it is rich in flavonoid and phytoestrogen. The research was performed in three stages. Stage I: Making of jicama flour with one factor (harvesting age (U): (3, 4, and 5 months). Stage II: Making of jicama methanolic extract with one factor (harvesting age (U): (3, 4, and 5 months). Stage III: Estimating the antioxidant activity of ether/water fractions of methanolic extract with two factors i.e: concentration (K): (10, 20, 40, 80, 160 ppm) and harvesting age (U): (3,4, and 5 months).
The results showed that the harvesting age had highly significant effect on proximate composition of jicama flour and yield of methanolic extract. Moisture content, ash content, and fat content tended to decrease with increasing harvesting age. Meanwhile, crude fiber content tended to increase. The protein content of jicama flour and yield of methanolic extract were maximum at 4 month harvest and tended to decrease at 5 months. The interaction of concentration and harvesting age had highly significant effect on antioxidant activity. The antioxidant of ether fraction tended to increase, but the antioxidant of the water fraction tended to decrease with increasing the harvesting age. The antioxidant of jicama methanolic extract is categorized as a strong antioxidant because the IC50 ether/water fractions were less than 100 ppm.
PENDAHULUAN
Latar Belakang
Perubahan radikal pada kehidupan manusia yang semakin modern berdampak pada tingkat kesehatan yang semakin menurun dan menimbulkan penyakit-penyakit baru penyebab kematian terbesar di dunia. Penyebab kematian terbesar di dunia kebanyakan merupakan penyakit degeneratif utama seperti CVD (Cardio Vascular Disease), kanker, dan diabetes.
Dari data Riset Kesehatan Dasar diketahui lebih dari 1/3 kematian di dunia disebabkan oleh CVD yang meliputi penyakit jantung koroner dan stroke. Penyakit jantung dan stroke merupakan penyebab kematian utama di negara maju dan negara berkembang. Data Global Cancer Statistic menunjukkan prevalensi penderita kanker di Indonesia mencapai 4,3 tiap 1000 orang. Prevalensi Diabetes Mellitus (DM) sebesar 366 juta jiwa penduduk dunia dan 80% penderitanya merupakan penduduk negara berkembang (International Diabetes Federation, 2012) dan saat ini DM merupakan penyebab kematian terbesar ke-2 penduduk perkotaan usia 45-54 tahun (Kementrian Kesehatan, 2012).
Penyakit degeneratif dapat dicegah dengan diet pangan fungsional (Marsono, 2013). Pangan fungsional diyakini memiliki kandungan zat gizi dan non-gizi yang bermanfaat bagi kesehatan. Konsensus tahun 1996 pada The First International Conference on East-West Perspective on Functional Food
mengeluarkan definisi pangan fungsional sebagai pangan yang karena komponen bioaktifnya memberikan manfaat kesehatan. Menurut Badan POM definisi pangan fungsional merupakan pangan yang secara alami atau telah melalui pengolahan mengandung senyawa-senyawa yang berdasar kajian ilmiah telah terbukti memberikan fungsi fisiologis tertentu yang bermanfaat bagi kesehatan dan dikonsumsi layaknya makanan/minuman bukan seperti suplemen.
Antioksidan digolongkan sebagai salah satu komponen pangan fungsional menurut Badan POM. Kementrian kesehatan Jepang juga memasukkan antioksidan dan fitokimia ke dalam 12 bahan yang terbukti bermanfaat bagi kesehatan. Antioksidan dibutuhkan tubuh untuk menyumbangkan satu buah elektron kepada radikal bebas, sehingga tubuh terlindung dari kerusakan oksidatif.
mengonsumsi komponen fitokimia seperti senyawa fenolik (flavonoid, asam, fenolik, tannin, dan lignan) yang banyak terdapat pada tanaman.
Keanekaragaman hayati Indonesia menempati posisi ke-2 teratas setelah Brazil. Oleh sebab itu, negara ini kaya akan berbagai tanaman pangan yang diduga banyak mengandung berbagai komponen bioaktif yang dapat digunakan sebagai pangan fungsional dalam menghambat berbagai penyakit degeneratif. Indonesia dengan keadaan suhu, iklim, kelembaban, dan intensitas matahari yang tinggi menyebabkan tanaman dapat menghasilkan metabolit sekunder seperti: antibakteri, antibiotik, maupun antioksidan sebagai bentuk pertahanan diri terhadap lingkungan. Metabolit sekunder ini dapat menghambat berbagai jenis penyakit degeneratif (Murakami et al., 1996), sehingga memberikan peluang bagi Indonesia untuk mengembangkan pengobatan natural dari bahan-bahan yang mengandung komponen bioaktif tersebut dalam mengimbangi harga obat sintetik yang terus membumbung tinggi.
Suzuki (1998) dalam Astawan (2009) melaporkan bahwa tingkat kematian akibat jantung koroner, kanker payudara, kanker rahim, dan aterosklerosis relatif rendah karena asupan makanan asal kedelai seperti tahu, natto, misso, dan susu kedelai yang relatif tinggi. Hal tersebut diduga karena peran isoflavon kedelai memiliki aktivitas biologis sebagai fitoestrogen, antioksidan, dan antimutagen.
Selain kedelai, tanaman yang terkenal karena kandungan isoflavonnya adalah bengkoang. Bengkoang tergolong familia Fabaceae. Familia leguminocea
dan fabaceae telah banyak dilaporkan mengandung fitoestrogen dan sangat memungkinkan banyak mengandung flavonoid, sehingga bengkoang diduga merupakan sumber antioksidan potensial serta dapat digunakan untuk mengobati penyakit yang berhubungan dengan kekurangan hormon estrogen. Namun secara historis, bengkoang belum digunakan untuk menyeimbangkan hormon dan mengontrol kesuburan. Bengkoang sejak lama telah digunakan sebagai tabir surya pemutih dan penyegar kulit (Lukitaningsih, 2010).
Beberapa penelitian mengenai antioksidan umbi bengkoang menunjukkan hasil yang berbeda-beda. Jumlah antioksidan yang berbeda dapat dihubungkan dengan ekstraksi dan jenis pelarut yang digunakan. Antioksidan yang terkandung di dalam umbi bengkoang dapat diekstrak mengggunakan berbagai pelarut, seperti: air, metanol, dan aseton. Penelitian Huerta (2005) menunjukkan total antioksidan status umbi bengkoang tertinggi terdapat pada umbi bengkoang yang diekstrak dengan pelarut metanol. Selain jenis pelarut, umur panen umbi diduga dapat mempengaruhi jumlah antioksidan dan kandungan kimia umbi bengkoang.
Untuk menentukan aktivitas antioksidan, proses pertama yang dilakukan adalah mengekstrak senyawa antioksidan dari bahan. Ekstraksi berfungsi untuk mendapatkan senyawa yang homogen, sehingga tidak lagi mengandung senyawa lain yang tidak memiliki aktivitas antioksidan. Salah satu metode penentuan aktivitas antioksidan adalah DPPH. Radikal bebas DPPH (2,2-diphenyl-1 -picrylhydrazyl) merupakan radikal stabil, pengukurannya mudah dan akurat. Metode DPPH memberikan informasi reaktivitas senyawa uji dalam mereduksi radikal bebas DPPH. Reaktivitas DPPH dengan senyawa uji ditunjukkan dengan perubahan warna ungu menjadi kuning lemah dan dibaca absorbansinya pada panjang gelombang 517 nm (Kuncahyo dan Sunardi, 2007).
Berdasarkan uraian di atas, bengkoang diduga mengandung banyak senyawa antioksidan yang diharapkan dapat mencegah penyakit degeneratif.
Untuk membuktikan hal tersebut maka penelitian dengan judul “Aktivitas Antioksidan Ekstrak Umbi Bengkoang pada Berbagai Umur
Tujuan Penelitian
Untuk mengetahui pengaruh umur panen umbi bengkoang terhadap komposisi kimia proksimat tepung bengkoang dan rendemen ekstrak metanolik yang dihasilkan. Dari penelitian ini juga dapat diketahui metode ekstraksi senyawa antioksidan yang menghasilkan aktivitas kuat, serta untuk mengetahui pengaruh umur panen umbi bengkoang dan konsentrasi ekstrak metanolik fraksi eter/air terhadap aktivitas antioksidan yang dinyatakan dengan nilai IC50 (Inhibition Concentration 50%)
Kegunaan Penelitian
Hasil penelitian dapat menjadi acuan bagi petani dan masyarakat untuk menentukan umur panen bengkoang sesuai karakterisktik dan tujuan pemanfaatannya. Penelitian ini diharapkan dapat digunakan secara ilmiah oleh semua pihak terkait, sehingga masyarakat dapat lebih mengetahui dan memahami manfaat umbi bengkoang dan fungsi utama antioksidannya dalam melindungi tubuh dari kerusakan oksidatif yang berakibat pada gangguan kesehatan seperti kanker, penyakit jantung, disfungsi immune, katarak, dan DM (Diabetes Mellitus).
Hipotesis Penelitian
TINJAUAN PUSTAKA
Bengkoang
Klasifikasi botani bengkoang menurut Lukitaningsih (2009) adalah sebagai berikut.
Kingdom : Plantae
Divisio : Magnoliophyta Kelas : Magnoliopsida Ordo : Fabales
Famili : Fabaceae Genus : Pachyrhizus Spesies : P. erosus
Nama Binomial : Pachyrhizus erosus (L) Urb
Bengkoang digolongkan dalam suku polong-polongan (Fabaceae) karena menghasilkan buah berbentuk polong (garis pipih) dan berambut halus yang berbiji 4-9 butir. Daun bengkoang berbentuk majemuk menyirip, beranak daun tiga, dan memiliki bunga dengan warna kelopak putih kebiruan. Bengkoang memiliki batang yang menjalar, membelit, dan berambut halus ke arah bawah (Lestarianto, 2013). Ilustrasi tanaman bengkoang dapat dilihat pada Gambar 1.
Bagian biji dan daun bengkoang tidak dapat dimakan karena mengandung rotenon yaitu racun pembunuh serangga dan ikan (Lestarianto, 2010). Bagian tanaman bengkoang yang dapat dimakan adalah umbi. Umbi bengkoang berbentuk bulat dan berwarna putih dengan kulit luar yang kuning pucat dan tipis. Bentuk umbi bengkoang dapat dibedakan menjadi 2, yaitu: bulat pipih dan bulat panjang. Bentuk bengkoang bulat pipih lebih berasa manis, air yang lebih banyak, kulitnya tipis, dan tidak banyak serat. Sedangkan bentuk bengkoang bulat panjang rasanya tawar, lebih berserat, berwarna agak kekuningan, dan memiliki kulit yang tebal (Astawan, 2009).
Bengkoang dibudidayakan di daerah dataran rendah. Biasanya ditanam di sela-sela tanaman cabai dan lada. Akarnya yang mampu bersimbiosis dengan Rhizobium bersifat menguntungkan karena dapat menambat nitrogen. Panjang akar mencapai 2 m, sedangkan panjang tanaman dapat mencapai 4-5 m. Tanaman bengkoang membentuk umbi akar (cormus) yang bisa mencapai bobot 5 kg (Astawan, 2009).
bengkoang di Indonesia terdapat di pulau Jawa, Madura, Sumatera (Sumatera Barat di Padang, dan Sumatera Utara di daerah Binjai).
Kadar air umbi bengkoang yang tinggi bersifat menyegarkan dan dapat menggantikan cairan tubuh. Umbi bengkoang juga kaya mineral seperti fosfor, zat besi, dan kalsium. Komposisi zat gizi umbi bengkoang dapat dilihat pada Tabel 1. Tabel 1. Komposisi zat gizi umbi bengkoang
Zat Gizi Dasar Kadar per 100g Persentase RDA(%) Energi (Kkal) 38,000 2,00
Keterangan: RDA: Recommended Dietary Allowances
Bengkoang juga merupakan diet rendah kalori (35-39 kkal dalam 100g). Umbi bengkoang mengandung asam askorbat dalam jumlah yang cukup besar. Asam-asam amino yang terdapat pada umbi bengkoang antara lain: asam aspartat, asam glutamat, glisin, histidin, arginin, treonin, alanin, prolin, tyrosin, valin,
metionin, isoleusin, leusin, fenilalanin, serin, sistein, dan lisin (Noman, et al., 2007).
Bengkoang memiliki rasa yang manis, oleh karena itu bengkoang biasanya dikonsumsi segar atau diolah minimal menjadi rujak, manisan, asinan, salad, koktail, serta campuran dalam pembuatan tekwan. Rasa manis pada bengkoang dihasilkan oleh inulin yang tergolong serat pangan (oligosakarida). Inulin tidak dapat langsung dipecah menjadi gula, diperlukan enzim inulase untuk pemecahannya, sehingga di dalam usus akan difermentasi. Sifat prebiotik inulin menyebabkan inulin sangat cocok menggantikan gula pada orang diabetes maupun yang sedang berdiet kalori rendah (Rudrappa, 2009).
Selain menjadi makanan, umbi putih bengkoang juga telah lama digunakan dalam berbagai kosmetik seperti masker wajah untuk tabir surya, memutihkan, dan menyegarkan kulit serta bahan dasar obat kanker, diabetes, dan nyeri perut (Lukitaningsih, 2010). Saat ini bengkoang sudah banyak dipasarkan dalam bentuk bubuk atau pasta untuk masker kulit (Astawan, 2009). Olahan bengkoang dalam bentuk bubuk/tepung dapat meningkatkan nilai ekonomis, memperpanjang masa simpan, dan diversifikasi produk olahan bengkoang.
ton/hektar, maka tiap hektar akan menghasilkan pati sebanyak 1,05 – 3,85 ton pati dan 0,21 – 0,77 ton protein (Hasani dan Karuniawan 2010). Komposisi kimia tepung bengkoang dapat dilihat pada Tabel 2.
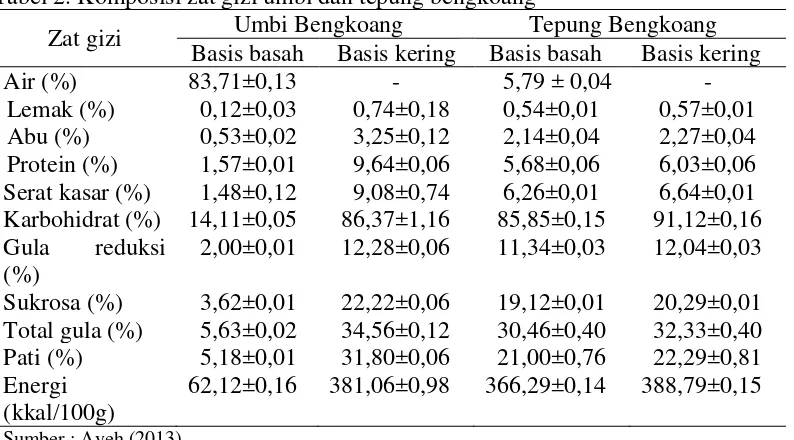
Tabel 2. Komposisi zat gizi umbi dan tepung bengkoang
Zat gizi Umbi Bengkoang Tepung Bengkoang Basis basah Basis kering Basis basah Basis kering Air (%) 83,71±0,13 - 5,79 ± 0,04 -
62,12±0,16 381,06±0,98 366,29±0,14 388,79±0,15
Sumber : Ayeh (2013)
Bengkoang merupakan Famili Fabaceae. Fabaceae dan Leguminoceae
Beberapa penelitian telah dilakukan terhadap tanaman bengkoang dan hasilnya sangat bermanfaat bagi kesehatan. Salah satunya, pemberian ekstrak bengkoang dapat meningkatkan proliferasi sel kelenjar payudara pada konsentrasi 75 mg/ml maksimum 125 mg/ml. Ekstrak bengkoang menekan atropi rahim tikus terovaktomi dengan mengoreksi kekurangan hormon estrogen, bersinergi dengan estrogen endogen melindungi organ yang dipelihara. Konsumsi ekstrak bengkoang juga dapat meningkatkan densitas tulang femur tikus terovaktomi, sehingga bengkoang mencegah osteoporosis (Lukitaningsih, 2010).
Antioksidan
Senyawa yang mampu memberikan satu atom hidrogen pada radikal bebas adalah antioksidan. Kemampuan antioksidan menghambat oksidasi akibat radikal bebas dapat melindungi sel dari kerusakan dan mencegah timbulnya penyakit akibat kerusakan sel dan jaringan. Antioksidan bukan hanya dapat mencegah kerusakan oksidatif pada tubuh manusia, tetapi juga dapat mencegah kerusakan pada bahan makanan. Berdasarkan sumbernya, antioksidan dibedakan menjadi 2, yaitu: antioksidan alami dan antioksidan sintetis (Wikipedia, 2011).
Antioksidan alami terbagi atas antioksidan vitamin dan enzim. Antioksidan vitamin seperti tokoferol (vitamin E), vitamin C, dan karotenoid lebih dikenal dibanding antioksidan enzim: superoksida dismutase (SOD), katalase, glutation peroksidase, dan antioksidan lain yang dapat meredam radikal bebas. Secara alami radikal bebas dihasilkan dalam metabolisme tubuh (endogen) yang berasal dari autoksidasi, oksidasi enzimatik dan respiratory burst. Begitu juga dengan antioksidannya yang dihasilkan di dalam tubuh. Tetapi perubahan radikal pada kehidupan manusia menyebabkan banyaknya radikal bebas eksogen yang dapat masuk ke tubuh seperti dari polusi udara, radiasi UV, sinar-X, pestisida, asap rokok, dan konsumsi makanan yang mengandung peroksida lipid (Judarwanto, 2013).
Ketidakseimbangan jumlah radikal bebas dan antioksidan di dalam tubuh menyebabkan terjadinya stress oksidatif. Oleh karena itu dibutuhkan antioksidan eksogen untuk menyeimbangkan jumlah antioksidan dengan radikal bebas dan mencegah kerusakan oksidatif (Setiawan dan Suhartono, 2005).
Antioksidan sintetik yang banyak digunakan adalah BHT (Butylated Hydroxy Toluene), BHA (Butylated Hydroxy Anysole), PG (Propil Galat), TBHQ
(Tert-Butyl Hydroxyl Quinon), NDGA (Nordihidroguairetic Acid), dan
α-tokoferol. Antioksidan sintetik dapat berbahaya bagi kesehatan, misalnya BHA dan BHT yang dapat menyebabkan pembengkakan organ hati (Gordon et al., 2001 dalam Prakasa, 2010).
antioksidan dan dengan dosis tinggi yang dapat berisiko. Jika ditinjau dari mekanisme kerjanya, antioksidan terbagi atas: antioksidan primer, sekunder, dan tersier. Antioksidan primer dapat mengubah radikal bebas menjadi bentuk yang stabil, memutus reaksi berantai, sehingga mencegah pembentukan radikal bebas baru. Antioksidan primer biasa merupakan antioksidan enzim seperti: SOD (Super Oksida Dismutase), katalase, dan glutation peroksidase. Antioksidan sekunder memiliki kemampuan mengurangi laju awal reaksi berantai. Yang tergolong antioksidan sekunder adalah antioksidan vitamin, antara lain: vitamin C, E, dan β -karoten. Sedangkan antioksidan tersier mampu memperbaiki kerusakan sel dan jaringan akibat oksidasi oleh radikal bebas. Contohnya enzim metionin sulfooksida reduktase mampu memperbaiki kerusakan DNA (Wikipedia, 2011). Flavonoid
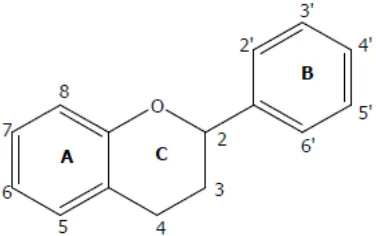
Komponen antioksidan dapat dihasilkan tanaman berupa senyawa fenolik (flavonoid, asam, fenolik, tannin, dan lignan). Komponen fenolik terbukti mampu menangkal radikal bebas. Senyawa flavonoid telah teridentifikasi dalam bengkoang. Struktur kimia flavonoid (Gambar 2) memiliki inti flavon terdiri dari 15 atom C dengan 3 cincin (C6-C3-C6) (Lukitaningsih, 2009).
Terdapat tujuh jenis senyawa utama flavonoid, yaitu: flavon, isoflavon, flavonol, flavanon, antosianin, katekin, dan khalkon. Khalkon merupakan flavonoid yang memiliki 2 gugus fenol yang terhubung dengan 3 atom karbon. Turunan dari struktur khalkon yang berisi 3 cincin dapat membentuk struktur flavanon. Dari bentuk flavanon inilah jenis-jenis flavonoid lainnya dihasilkan, termasuk isoflavon, flavonol, flavanol, dan flavon (Lukitaningsih, 2009).
Isoflavon diklasifikasikan sebagai fitoestrogen. Diduga struktur kimia isoflavon mirip dengan hormon estrogen dan obat osteoporosis sintetis ipriflavon. Estrogen dan ipriflavon dapat melindungi densitas mineral tulang pada wanita pasca menopause, menghambat kerusakan, dan sekaligus menstimulasi pembentukan tulang. Struktur kimianya yang mirip dengan hormon estrogen (fitoestrogen) membuat senyawa ini berperan penting dalam penyembuhan penyakit yang disebabkan oleh hormon, seperti kanker payudara, ovarium, prostat, dan sindrom post menopose. Daidzein dan geinistein juga berperan menurunkan kolesterol (Lukitaningsih, 2010).
Isoflavon yang merupakan bagian dari flavonoid dapat berperan sebagai antioksidan, sehingga berguna untuk mencegah: (1) kerusakan oksidatif membran sel, (2) aterosklerosis akibat teroksidasinya LDL (kolesterol jahat), (3) penyakit jantung koroner, (4) penyakit kardiovaskuler, dan (5) kerusakan oksidatif DNA. Selain itu, daya antioksidan isoflavon juga berguna untuk memberi efek antiproliferatif dan menghambat pertumbuhan sel melanoma (salah satu pemicu kanker) (Astawan, 2009).
menurunkan kadar kolesterol total maupun low density lipoprotein (LDL), serta meningkatkan kolesterol baik high density lipoprotein (HDL), (3) menurunkan tekanan darah sistolik dan diastolik, (4) bersifat antimutagenesis (mencegah mutasi gen), serta (5) mencegah osteoporosis pada wanita pasca menopause. Penyakit kronis pasca menopause menyebabkan wanita banyak menggunakan hormon estrogen sebagai terapi. Beberapa penelitian menunjukkan terapi tersebut dalam waktu lama menyebabkan risiko kanker terutama payudara dan rahim. Alternatifnya dapat menggunakan isoflavon karena antioksidan ini memiliki struktur yang hampir sama dengan hormon estrogen dan kemampuannya berikatan dengan reseptor estrogen di dalam sel (Lukitaningsih, 2010).
Radikal Bebas
Radikal bebas dapat berasal dari dalam (endogen) dan luar tubuh (eksogen). Radikal endogen berasal dari autooksidasi, oksidasi enzimatik, dan
respiratory burst, sedangkan radikal eksogen dapat bersumber dari asap rokok, polusi udara, radiasi UV, sinar-X, dan pestisida. Radikal bebas dapat terbentuk dari hasil samping proses oksidasi atau pembakaran seperti saat bernafas maupun dari olahraga yang berlebihan, dan saat terjadi peradangan dalam tubuh. Pada saat infeksi atau peradangan dalam tubuh, radikal berfungsi untuk membunuh mikrooganisme penyebab infeksi. Namun, paparan radiasi dari luar tubuh dalam jumlah yang berlebihan dan secara terus-menerus akan menyebabkan kerusakan sel, mengurangi adaptasi sel terhadap lingkungan yang dapat menimbulkan penyakit, serta mengakibatkan kematian pada sel (Judarwanto, 2013).
Radikal bebas dan spesies oksigen reaktif (ROS) merupakan kondisi patologik dari penyakit tertentu seperti terjadinya inflamasi, gangguan metabolik, penuaan sel, aterosklerosis, dan karsinogen (Suryanto dan Wehantouw, 2009). Inflamasi adalah proses yang diperantarai sintesis prostaglandin dengan katalis sikooksigenase. Pada proses ini dihasilkan zat antara berupa radikal bebas (Lautan, 1997). ROS meliputi radikal hidroksil (*OH), radikal anion superoksida (O2*-), hidrogen peroksida (H2O2), dan singlet oksigen (1O2). Radikal bebas dan ROS menyebabkan kerusakan pada komponen biologi seperti protein, DNA, dan lipid (Suryanto dan Wehantouw, 2009).
tubuh. Radikal bebas dapat merusak DNA bila terbentuk di sekitar DNA seperti pada radiasi biologis. Jika radikal bebas mengambil elektron dari sel tubuh maka struktur DNA akan berubah, sehingga terjadi mutasi gen. Jika mutasi berlangsung tahunan maka akan terbentuk sel kanker. Pada umumnya semua jaringan di dalam tubuh dapat menangkal radikal bebas menggunakan enzim khusus dari dalam jaringan tersebut. Namun, seiring dengan pertambahan usia manusia secara alami tubuh mengalami degradasi dan kemunduran, sehingga tidak lagi mampu menangkal radikal bebas yang masuk ke dalam tubuh maka dibutuhkan antioksidan eksogen sebagai penangkal radikal bebas (Judarwanto, 2013).
Ekstraksi
Ekstraksi adalah salah satu tahap terpenting dalam proses analisis. Ekstraksi merupakan cara pemisahan komponen dari campurannya dengan cara penarikan komponen yang dapat larut, sehingga terpisah dari komponen yang tidak dapat larut. Teknik ekstraksi bergantung pada tekstur, kandungan air bahan, dan jenis senyawa yang akan diekstrak atau diisolasi (Harborne 1987 dalam Sundari 2008). Metode ekstraksi menggunakan pelarut terbagi 2, yaitu: cara panas dan cara dingin. Ekstraksi cara panas seperti refluks, digesti, soxhletasi, infus, dan dekok menggunakan suhu di atas suhu kamar. Sedangkan metode ekstraksi cara dingin menggunakan suhu kamar. Ekstraksi cara dingin terdiri dari perkolasi dan maserasi (Hamdani, 2013).
karena prosesnya merendam sampel dalam pelarut dan dilakukan pengadukan bila perlu. Prinsipnya menggunakan gerak kinetik pelarut yang dapat menembus jaringan bahan, sehingga komponen yang diinginkan dapat larut dalam pelarut. Kelebihan maserasi adalah sederhana dan tidak memerlukan peralatan spesifik (Hamdani, 2013dan Yulanda, 2007 dalam Winata, 2011).
Tahap awal ekstraksi adalah dengan menghaluskan jaringan tanaman yang akan diekstrak (memperkecil ukuran partikel bahan) dengan tujuan memperbesar luas permukaannya, sehingga lebih banyak komponen metabolit yang diekstrak. Sebelum diekstrak, bahan harus dikeringkan untuk mempertahankan kandungan metabolit dalam tanaman yang telah dipotong, sehingga metabolisme tanaman atau bahan tersebut terhenti (Mursito, 2002 dalam Winata, 2011).
Metode DPPH
Metode yang akhir-akhir ini popoler digunakan untuk menentukan aktivitas antioksidan adalah DPPH. DPPH atau 2,2-diphenyl-1-picrylhydrazyl
Gambar 3. Struktur kimia radikal bebas DPPH (Molyneux, 2004)
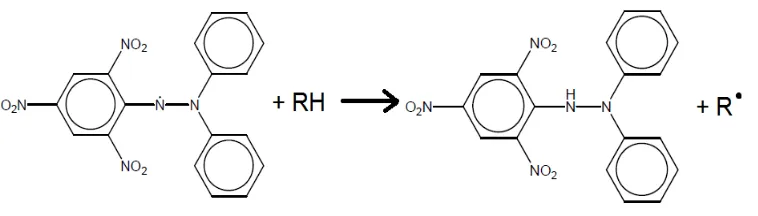
Prinsip pengukuran aktivitas antioksidan metode DPPH adalah dengan penangkapan atom H dari senyawa antioksidan bahan uji oleh radikal bebas DPPH. Reaksi penangkapan atom H dari antioksidan oleh DPPH dapat dilihat pada Gambar 4. Dalam Gambar 4, antioksidan disimbolkan sebagai RH, sedangkan R• merupakan antioksidan yang telah kehilangan atom hidrogennya.
Gambar 4. Reaksi Penangkapan atom H dari antioksidan oleh DPPH (Winata, 2011)
METODE PENELITIAN
Waktu dan Tempat Penelitian
Penelitian dilaksanakan pada bulan Juli hingga Desember tahun 2013 di Laboratorium Teknologi Pangan, Laboratorium Analisa Kimia Bahan Pangan, dan Laboratorium Sentral Fakultas Pertanian Universitas Sumatera Utara.
Bahan Penelitian
Bahan utama adalah umbi bengkoang varietas gajah dengan umur panen tiga, empat, dan lima bulan. Umbi bengkoang diperoleh dari perkebunan warga di daerah Tanah Merah kota Binjai, Sumatera Utara. Bahan-bahan kimia (reagensia) yang digunakan adalah BHT dan vitamin C sebagai kontrol positif, radikal bebas DPPH (2,2-diphenyl-1-picrylhydrazyl) untuk uji aktivitas antioksidan, n-hexan, metanol, dietil eter, dan akuades untuk ekstraksi senyawa antioksidan serta bahan-bahan untuk analisis proksimat umbi bengkoang seperti NaOH, H2SO4 pekat, K2SO4, dan CuSO4.
Alat Penelitian
Pembuatan tepung bengkuang menggunakan oven, blender, dan saringan komersil. Alat untuk ekstraksi senyawa antioksidan meliputi reciprocal mixer
(Denley), erlenmeyer, corong kaca, kertas saring (Whatman No. 41), waterbath, dan corong pisah. Untuk analisis proksimat meliputi neraca analitik (Sartorius), oven (Memmert), tanur, tabung kjeldahl, soxhlet, pendingin balik, labu didih, dan
Metode Penelitian (Bangun, 2001)
Kegiatan yang dilakukan dalam penelitian ini terdiri dari tiga tahap, yaitu : a. Tahap 1: Pembuatan tepung bengkoang. Tahap 1 pada penelitian ini
menggunakan Rancangan Acak Lengkap (RAL) nonfaktorial, yaitu: umur panen umbi bengkoang (U) yang terdiri dari 3 taraf, yaitu :
U1 = 3 bulan U2 = 4 bulan U3 = 5 bulan
Setiap perlakuan dibuat dalam 3 kali ulangan
b. Tahap 2: Pembuatan ekstrak metanolik bengkoang. Tahap 2 pada penelitian ini menggunakan Rancangan Acak Lengkap (RAL) nonfaktorial, yaitu: umur panen umbi bengkoang (U) yang terdiri dari 3 taraf, yaitu :
U1 = 3 bulan U2 = 4 bulan U3 = 5 bulan
Setiap perlakuan dibuat dalam 3 kali ulangan
c. Tahap 3: Uji aktivitas antioksidan ekstrak metanolik bengkoang fraksi eter/air. Pada tahap 3, penelitian menggunakan Rancangan Acak Lengkap (RAL) dengan dua faktor, yaitu:
Faktor I : Konsentrasi ekstrak metanolik fraksi eter/air (K) yang terdiri dari 5 taraf, yaitu :
K4 = Konsentrasi 80 ppm K5 = Konsentrasi 160 ppm
Faktor II : Umur panen umbi bengkoang (U) yang terdiri dari 3 taraf, yaitu : U1 = 3 bulan
U2 = 4 bulan U3 = 5 bulan
Semua perlakuan dibuat ulangan sebanyak 3 kali. Model Rancangan (Bangun, 1991)
Penelitian ini dilakukan dengan tiga tahap, yaitu : Tahap 1 : Pembuatan tepung bengkoang
Tahap 2: Pembuatan ekstrak metanolik bengkoang
Penelitian tahap 1 dan 2 menggunakan model Rancangan Acak Lengkap (RAL) nonfaktorial dengan model sebagai berikut:
Ŷij = µ +αi + εij dimana:
Ŷij : Hasil pengamatan dari faktor U pada taraf ke-i dalam ulangan ke-j µ : Efek nilai tengah
αi : Efek perlakuan ke-i
εij : Efek galat perlakuan ke i dengan ulangan ke j
Ŷijk= µ + αi+ βj+ (αβ)ij+ εijk
dimana:
Ŷijk : Hasil pengamatan dari faktor K pada taraf ke-i dan faktor U pada taraf ke-j dalam ulangan ke-k
µ : Efek nilai tengah
αi : Efek faktor K pada taraf ke-i
βj : Efek faktor U pada taraf ke-j
(αβ)ij : Efek interaksi faktor K pada taraf ke-i dan faktor U pada taraf ke-j
εijk : Efek galat dari faktor K pada taraf ke-i dan faktor U pada taraf ke-j dalam ulangan ke-k
Apabila hasil yang diperoleh berbeda nyata maupun sangat nyata maka uji dilanjutkan dengan uji beda rataan dengan menggunakan uji LSR (Least Significant Range).
Pelaksanaan Penelitian
Pembuatan tepung bengkoang (Rusmarilin, 2003)
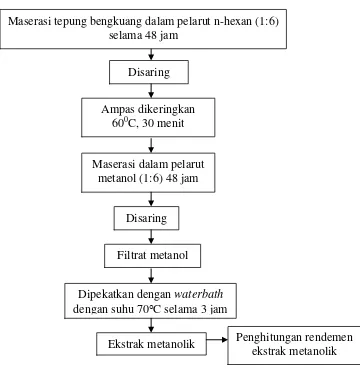
Pembuatan ekstrak metanolik bengkoang (Kuncahyo dan Sunardi, 2007) Ekstraksi tepung bengkoang dilakukan untuk memperoleh ekstrak metanolik. Sebanyak 25 g tepung bengkoang dimaserasi dalam pelarut hexan 150 ml (maserasi 48 jam), disaring, dan ampasnya dikeringkan dalam oven dengan suhu 60°C selama 30 menit. Ampas yang telah kering, direndam dalam pelarut metanol sebanyak 150 ml (maserasi 48 jam), dan disaring untuk mendapatkan filtrat metanol. Filtrat atau ekstrak metanol dipekatkan menjadi ekstrak kental metanolik dalam waterbath selama 3 jam dengan suhu 70°C dan dihitung rendemen ekstrak metanolik bengkoang. Skema pembuatan ekstrak metanolik bengkoang dapat dilihat pada Gambar 6.
Pembuatan larutan ekstrak metanolik fraksi eter/air (Kuncahyo dan Sunardi, 2007)
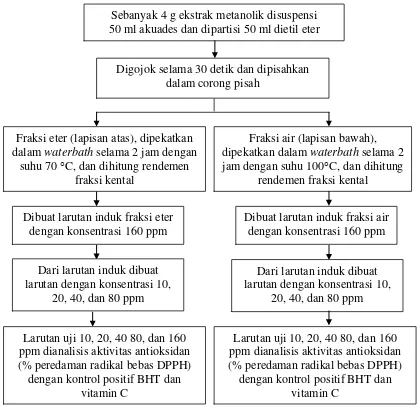
Sebanyak 4 g ekstrak kental metanolik disuspensi dengan 50 ml akuades dan dipartisi dengan 50 ml dietil eter. Digojok selama 30 detik, dan dibiarkan memisah akibat adanya perbedaan massa jenis antara fraksi eter (lapisan atas) dan fraksi air (lapisan bawah). Fraksi eter/air masing-masing dipekatkan dalam
waterbath selama 2 jam dengan suhu 70°C untuk fraksi eter dan 100°C untuk fraksi air. Ekstrak metanolik fraksi eter/air dilarutkan dalam metanol dan dibuat larutan dengan konsentrasi 10 ppm, 20 ppm, 40 ppm, 80 ppm, dan 160 ppm. Skema pembuatan larutan ekstrak metanolik fraksi eter/air tersaji pada Gambar 7.
Pengamatan dan Pengukuran Data
serat kasar. Ekstrak metanolik bengkoang dan ekstak metanolik fraksi eter/air dihitung rendemen dan diukur absorbansi peredaman radikal bebas DPPH pada ekstrak metanolik fraksi eter/air berbagai konsentrasi dan umur panen.
Kadar air, metode oven (SNI 01–2891–1992)
Ditimbang sampel sebanyak 1-2 gram pada botol timbang yang telah diketahui bobotnya. Kemudian dikeringkan dalam oven dengan suhu 105°C selama 3 jam. Didinginkan dalam desikator dan ditimbang, diulangi beberapa kali hingga diperoleh bobot yang tetap. Prinsipnya dengan menghitung jumlah air yang menguap saat dipanaskan dalam oven dan dianggap kadar air yang ada pada bahan. Perhitungannya adalah sebagai berikut :
Kehilangan bobot setelah dikeringkan (g)
Kadar air (% bk) = x 100% Bobot bahan setelah dikeringkan (g)
Kadar abu (Sudarmadji, et al., 1996)
Penentuan kadar abu cara kering, dengan mengoksidasikan semua zat dalam bahan pada suhu tinggi 500-6000C. Sampel ditimbang sebanyak 5 g, dimasukkan dalam cawan porselen dan dibakar dalam tanur. Kemudian zat yang tersisa di dalam cawan pengabuan ditimbang. Perbandingan bobot zat sisa (abu) dengan bobot awal sampel (5 g) dinyatakan dalam (%) sebagai kadar abu.
Bobot abu (g)
Kadar abu (%) = x 100% Bobot sampel awal (g)
Kadar serat kasar (Sudarmadji, et al., 1996)
Menentukan banyaknya zat-zat yang tidak larut asam dan basa encer dengan kondisi tertentu. Langkah analisis meliputi penghilangan lemak dan
dan suhu mendidih. Residu yang diperoleh merupakan serat kasar yang mengandung 97% lignin, selulosa, dan senyawa lain yang belum teridentifikasi.
Bobot residu (g)
Kadar serat kasar (%) = x 100%
Kadar protein, cara makro kjeldahl (AOAC, 1995)
Ditimbang sampel yang telah dihaluskan sebanyak 0,2 g, dimasukkan ke dalam labu kjeldahl 30 ml selanjutnya ditambahkan 1,5 ml H2SO4 pekat dan 2 g katalis (CuSO4 dan K2SO4), dan dididihkan selama 2 jam atau sampai berwarna hijau kebiruan. Labu beserta isinya didinginkan, kemudian isinya dipindahkan ke dalam alat destilasi dan ditambahkan 15 ml larutan NaOH 40%. Kemudian dibilas dengan akuades. Erlenmeyer 250 ml berisi H2SO4 0,025 N dan 2–4 tetes indikator mengsel (campuran metil merah 0,02% dalam alkohol dan metil biru 0,02% dalam alkohol dengan perbandingan 2:1) diletakkan di bawah kondensor. Ujung tabung kondensor harus terendam dalam labu berisi campuran larutan H2SO4 dengan mengsel, kemudian dilakukan destilasi hingga destilat mencapai 125 ml. Ujung kondensor kemudian dibilas dengan sedikit air destilat dan ditampung dalam erlenmeyer lalu dititrasi dengan NaOH 0,02 N sampai terjadi perubahan warna ungu menjadi hijau. Penetapan blanko dilakukan dengan cara yang sama.
(A-B) x N x 0,014 x 5,18
Kadar protein = x 100% Bobot Sampel (g)
A = ml NaOH untuk tittrasi blanko B = ml NaOH untuk titrasi sampel N = Normalitas NaOH
Kadar lemak, metode soxhlet (AOAC, 1995)
Dipanaskan labu alas datar 250 ml di dalam oven pada suhu 105oC hingga didapat bobot tetap kemudian sampel ditimbang sebanyak 5 gram lalu dimasukkan ke dalam kertas saring. Kertas saring yang berisi sampel diekstrak dengan 130 ml hexan dengan menggunakan soxhlet selama 5 jam dan labu lemak dipisahkan dari alat pengekstraksi lalu diuapkan. Labu dikeringkan dalam oven 60oC dan ditimbang sampai bobot tetap. Kemudian dihitung kadar lemak sampel dengan rumus :
Bobot akhir labu lemak (g) - Bobot awal labu lemak (g) Kadar lemak (%) = x 100%
Bobot sampel (g) Rendemen (Kuncahyo dan Sunardi, 2007)
Tepung bengkoang 25 g dilarutkan dan direndam (maserasi) dalam pelarut non polar (hexan) 150 ml selama 48 jam. Dilakukan penyaringan, ampas dikeringkan hingga tidak berbau hexan. Residu dilarutkan dalam metanol (maserasi 48 jam) kemudian disaring dan filtrat dipekatkan untuk mendapatkan ekstrak kental metanolik. Ekstrak kental metanolik dihitung rendemennya dengan rumus berikut.
Bobot ekstrak metanolik pekat (g)
Rendemen (%)= x 100% Bobot tepung bengkoang (g)
Bobot ekstrak metanolik pekat fraksi eter/air (g)
Rendemen (%)= x 100% 4 (g)
Uji aktivitas antioksidan fraksi eter dan air (Kuncahyo dan Sunardi, 2007) Fraksi air dan eter berbagai umur panen masing-masing dibuat larutan induk dengan konsentrasi 160 ppm. Dari larutan induk dibuat larutan dengan konsentrasi 10 ppm, 20 ppm, 40 ppm, dan 80 ppm. Larutan uji (10 ppm, 20 ppm, 40 ppm, 80 ppm, dan 160 ppm) masing-masing sebanyak 4 ml, ditambahkan radikal bebas DPPH 0,1 mM sebanyak 1 ml dimasukkan ke dalam vial dan dikocok. Didiamkan pada suhu kamar selama 30 menit, kemudian dibaca serapan aktivitasnya pada panjang gelombang 517 nm. Blanko yang digunakan adalah 4 ml metanol dan 1 ml DPPH 0,1 mM. Kontrol positif sebagai pembanding digunakan antioksidan sinetetis BHT dan vitamin C. Nilai absorbansi (Abs.) yang diperoleh menunjukkan aktivitas antioksidan senyawa uji (% peredaman). Nilai IC50 masing-masing dihitung dengan persamaan regresi.
Gambar 5. Skema pembuatan tepung bengkoang Tepung bengkoang
Diayak dengan ayakan komersil Irisan kering diblender hingga menjadi tepung
Disusun di atas Loyang dan keringkan dalam oven suhu 500C selama 48 jam (sampai kering)
Diiris tipis
Disortasi, trimming, dan dan dicuci
Analisis proksimat -Penentuan kadar air -Penentuan kadar abu -Penentuan kadar lemak -Penentuan kadar protein
Penentuan kadar serat kasar Bengkoang
Umur Panen (U) U1 = 3 bulan U2 = 4 bulan U3 = 5 bulan
Gambar 6. Skema pembuatan ekstrak metanolik bengkoang Maserasi dalam pelarut
metanol (1:6) 48 jam Ampas dikeringkan
600C, 30 menit
Disaring Disaring
Maserasi tepung bengkuang dalam pelarut n-hexan (1:6) selama 48 jam
Filtrat metanol
Dipekatkan dengan waterbath
dengan suhu 70°C selama 3 jam
Gambar 7. Skema pembuatan larutan ekstrak metanolik fraksi eter/air Sebanyak 4 g ekstrak metanolik disuspensi 50 ml akuades dan dipartisi 50 ml dietil eter
Digojok selama 30 detik dan dipisahkan dalam corong pisah
Fraksi eter (lapisan atas), dipekatkan dalam waterbath selama 2 jam dengan
suhu 70 °C, dan dihitung rendemen fraksi kental
Fraksi air (lapisan bawah), dipekatkan dalam waterbath selama 2 jam dengan suhu 100°C, dan dihitung
rendemen fraksi kental
Dibuat larutan induk fraksi air dengan konsentrasi 160 ppm Dibuat larutan induk fraksi eter
dengan konsentrasi 160 ppm
Larutan uji 10, 20, 40 80, dan 160 ppm dianalisis aktivitas antioksidan (% peredaman radikal bebas DPPH)
dengan kontrol positif BHT dan vitamin C
Larutan uji 10, 20, 40 80, dan 160 ppm dianalisis aktivitas antioksidan (% peredaman radikal bebas DPPH)
dengan kontrol positif BHT dan vitamin C
Dari larutan induk dibuat larutan dengan konsentrasi 10,
20, 40, dan 80 ppm
Dari larutan induk dibuat larutan dengan konsentrasi 10,
HASIL DAN PEMBAHASAN
Tahap I: Pembuatan Tepung Bengkoang
Pembuatan tepung bengkoang menggunakan umbi bengkoang varietas gajah yang dipanen pada umur 3 bulan, 4 bulan, dan 5 bulan setelah ditanam. Umbi bengkoang yang telah disortasi dan dikupas kulitnya, kemudian diiris tipis untuk selanjutnya dikeringkan dalam oven dengan suhu 500C selama 48 jam. Setelah kering, umbi dihaluskan hingga menjadi tepung. Proses pengeringan dan penepungan dilakukan untuk mengurangi kadar air bahan. Kandungan air yang tinggi akan menghambat proses pemekatan karena titik didih air lebih tinggi daripada pelarut yang digunakan. Penepungan bertujuan untuk memperbesar luas permukaan bahan dengan ukuran partikel yang seragam, sehingga ekstraksi komponen pada tahap selanjutnya akan menjadi optimum.
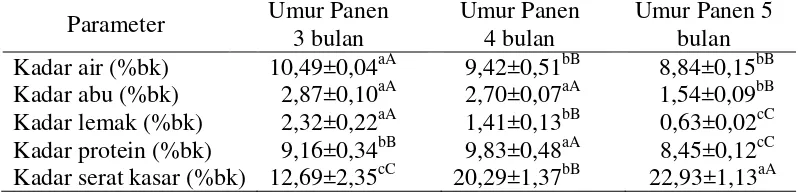
Hasil analisis proksimat tepung bengkoang dapat dilihat pada Tabel 3. Dari hasil penelitian yang dilakukan, diperoleh komposisi kimia tepung bengkoang yang memberikan pengaruh berbeda sangat nyata (P<0,01) terhadap kadar air, kadar abu, kadar lemak, kadar protein, dan kadar serat kasar.
Tabel 3. Komposisi kimia tepung bengkoang umur panen 3 bulan, 4 bulan, dan Kadar serat kasar (%bk) 12,69±2,35cC 20,29±1,37bB 22,93±1,13aA
Keterangan: -nAngka yang diikuti huruf kecil yang berbeda dalam baris yang sama menunjukkan berbeda nyata pada taraf 5% dan huruf besar pada taraf 1%
Kadar air (%bk)
Dari Tabel 3 diketahui bahwa perbedaan umur panen umbi bengkoang memberikan pengaruh berbeda sangat nyata (P<0,01) terhadap kadar air tepung bengkoang. Kadar air tepung bengkoang yang dipanen pada umur 3 bulan (U1) berbeda sangat nyata terhadap umur panen 4 bulan (U2) dan 5 bulan (U3). U2 berbeda sangat nyata terhadap U3. Semakin tinggi umur panen umbi bengkoang maka kadar air tepung bengkoang yang dihasilkan cenderung semakin rendah, seperti yang terlihat pada Gambar 8.
Gambar 8. Hubungan antara umur panen umbi bengkoang dengan kadar air (%bk)
Kadar air tepung bengkoang tertinggi terdapat pada umbi bengkoang umur panen 3 bulan (U1), yaitu sebesar 10,49% sedangkan kadar air terendah terdapat pada umbi bengkoang yang dipanen pada umur 5 bulan (U3), yaitu sebesar 8,84%. Kadar air tepung bengkoang belum diatur dalam SNI, sehingga tepung bengkoang belum memiliki nilai standar proksimat seperti kadar air, kadar abu, kadar protein, dan kadar lemaknya. Namun, jika dibandingkan dengan kadar air dari beberapa jenis tepung seperti tepung terigu dengan kadar air maksimum 14,5%; tepung
ketan 12%; tepung sagu 13%; dan tepung beras 11% maka kadar air tepung bengkoang 8,84-10,49% memenuhi standar beberapa jenis tepung tersebut.
Perbedaan kadar air tepung bengkoang umur panen 3, 4, dan 5 bulan dikarenakan selama masa tanam, terjadi proses pertumbuhan yang ditandai dengan pembesaran umbi secara terus-menerus. Ketika umbi mulai membesar maka tudung akar tidak lagi berfungsi menyerap unsur hara dan air, tetapi terus-menerus menimbun cadangan makanan atau pati (Rubatzky dan Yamaguchi, 1998 dalam Nurdjanah et al., 2007), sehingga umbi mengalami pertambahan jumlah pati, pembesaran ukuran granula pati, dan pertambahan berbagai komponen nonpati (Susilawati, et al., 2008) yang menyebabkan terjadinya peningkatan bobot kering umbi. Hal inilah yang menyebabkan semakin tua umur panen umbi kandungan airnya cenderung semakin rendah. Penurunan kadar air seiring dengan meningkatnya umur panen juga terjadi pada umbi kentang (Kusdibyo dan Asandhi, 2004), rimpang garut (Maulani, et al., 2012), dan ubi kayu (Susilawati et al., 2008).
Kadar abu (%bk)
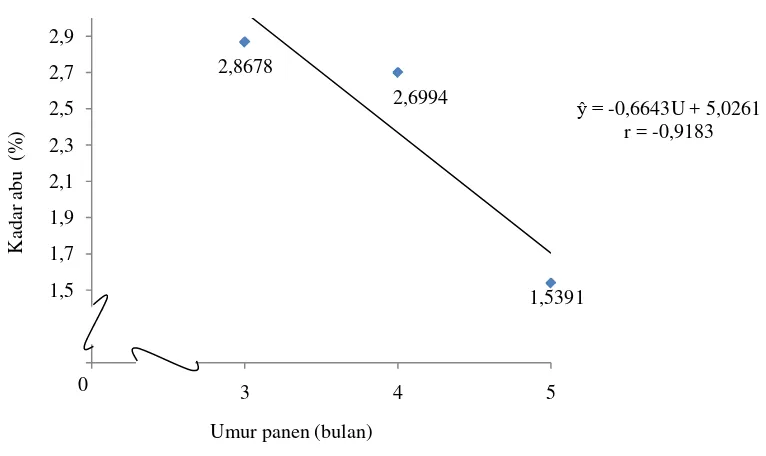
Gambar 9. Hubungan antara umur panen umbi bengkoang dengan kadar abu (%bk)
Dari Gambar 9 dapat dilihat bahwa kadar abu tepung bengkoang cenderung menurun dengan meningkatnya umur panen umbi bengkoang. Kadar abu tepung bengkoang tertinggi terdapat umur panen 3 bulan, yaitu sebesar 2,87%. Pada umur panen 4 bulan, kadar abu turun menjadi 2,67%. Kadar abu tepung bengkoang terendah terdapat pada umur panen 5 bulan, yaitu sebesar 1,54%.
Abu merupakan zat anorganik atau zat sisa yang tidak terbakar sampai bebas atom karbon. Zat anorganik ini terdiri dari unsur-unsur mineral. Kandungan mineral dalam umbi akan semakin menurun seiring dengan lamanya umbi di dalam tanah (Maulani, et al., 2012). Mineral-mineral merupakan kofaktor enzim. Seperti magnesium (Mg) yang dilaporkan Rudrappa (2009) terdapat dalam umbi bengkoang merupakan kofaktor bagi sekitar 300 enzim. Dalam setiap biosintetis terutama untuk menghasilkan metabolit sekunder pada tanaman, sangat banyak melibatkan enzim (Manitto, 1992). Hal inilah yang menyebabkan kadar abu
tepung bengkoang mengalami penurunan dengan semakin lamanya umur panen umbi bengkoang. Kadar abu beberapa jenis tepung menurut Standar Nasional Indonesia, maksimun pada kisaran 0,5-1%, seperti pada terigu maksimum 0,5%, tepung beras 1%, sagu 0,6%, dan ketan 1%. Jika dilihat dari SNI beberapa tepung maka kadar abu tepung bengkoang jauh lebih tinggi.
Kadar lemak (%bk)
Dari Tabel 3 dapat dilihat bahwa perbedaan umur panen umbi bengkoang memberikan pengaruh berbeda sangat nyata (P<0,01) terhadap kadar lemak tepung bengkoang. Kadar lemak U1 berbeda sangat nyata terhadap U2 dan U3. Kadar lemak U2 berbeda sangat nyata terhadap U3.Hubungan antara umur panen dengan kadar lemak tepung bengkoang dapat dilihat pada Gambar 10.
Gambar 10. Hubungan antara umur panen umbi bengkoang dengan kadar lemak (%bk)
Dari Gambar 10 dapat dilihat bahwa kadar lemak tepung bengkoang cenderung menurun dengan meningkatnya umur panen umbi bengkoang. Kadar lemak tepung bengkoang tertinggi sebesar 2,32% terdapat pada U1, sedangkan terendah terdapat pada pelakuan U3 sebesar 0,63%. Jika dibandingkan dengan hasil penelitian Ayeh (2013) yang menyebutkan bahwa kadar lemak tepung
bengkoang sebesar 0,57+0,01% maka hasil ini mendekati kadar lemak dari umbi bengkoang yang dipanen 5 bulan setelah tanam (U3).
Adanya penurunan kadar lemak selama peningkatan umur panen diduga disebabkan mulai terjadinya degradasi komponen lipid pada bengkoang selama pematangan umbi di dalam tanah. Umbi bengkoang yang tua (umur panen 5 bulan) mulai memiliki bau langu seperti beany flavor pada kedelai, tetapi tidak setajam bau langu pada kedelai.
Beany flavor merupakan indikasi terjadinya reaksi yang dikatalisis oleh enzim lipoksigenase. Bau langu ini dihasilkan oleh senyawa keton dan aldehid terutama hexanal dan heptanal dari hasil oksidasi komponen lemak (FAO, 2009). Diduga asam lemak terkandung dalam umbi bengkoang terutama asam lemak tidak jenuh trilinolein telah dioksidasi oleh onzim lipoksigenase, sehingga menghasilkan aroma langu (beany flavor).
Asam lemak yang terdapat dalam umbi bengkoang diantaranya asam palmitat dan asam trilinolein. Asam lemak terutama yang tidak jenuh (trilinolein) dapat mencegah penyakit kardiovaskuler karena mampu menurunkan LDL dalam plasma darah. Diduga kemampuan menurunkan LDL dalam darah ini dikaitkan dengan kemampuannya sebagai antioksidan yang sangat baik. Trilinolein merupakan antioksidan yang paling kuat diantara senyawa lain yang terdapat dalam umbi bengkoang (Lukitaningsih, 2009).
Kadar protein (%bk)
bengkoang. Hubungan perlakuan umur panen umbi bengkoang dengan kadar protein tersaji pada Gambar 11.
Gambar 11. Hubungan perlakuan umur panen umbi bengkoang dengan kadar protein (%bk)
Dari Gambar 11 dapat diketahui bahwa kadar protein meningkat sampai pada umur panen 4 bulan dan cenderung menurun pada umur panen 5 bulan. Kadar protein tertinggi terdapat pada tepung bengkoang yang dipanen pada umur 4 bulan (U2), yaitu sebesar 9,83% dan terendah pada umur 5 bulan (U3), yaitu sebesar 8,46%. Kadar protein yang relatif tinggi menunjukkan bahwa tepung bengkoang potensial digunakan sebagai sumber protein nabati.
Bengkoang gajah biasanya dipanen pada umur 4 bulan. Pada umur ini umbi bengkoang telah dianggap matang dan memiliki bobot yang besar. Jika panen ditunda hingga umur 5 bulan maka batang umbi akan terlihat mulai menghitam dan mengering artinya bengkoang mulai masuk pada tahap pelayuan. Pada proses pematangan menurut Arief (2012), organisasi dalam sel mulai terganggu dan memicu reaksi hidrolisis berbagai substrat yang melibatkan
enzim. Hasil dari hidrolisis klorofil, pati, pektin, dan tannin akan membentuk etilen, pigmen, flavor, enzim, dan polipeptida. Akibat terbentuknya enzim-enzim dan polipeptida maka kandungan protein dalam umbi akan meningkat seperti yang ditunjukkan dalam Gambar 11. Kadar protein tepung umbi bengkoang meningkat pada umur panen 4 bulan, namun mulai mengalami penurunan pada umur panen 5 bulan. Menurunnya kadar protein merupakan ciri dari terjadinya pelayuan. Pelayuan merupakan hasil dari perubahan-perubahan di dalam sel seperti penipisan dinding dinding sel, terjadi degradasi mitokondria, klorofil berkurang, kandungan protein menurun, kegiatan pernafasan dan fotosintesis menurun dan sifat permeabilitas membran sel juga berubah (Arief, 2012).
Kadar serat kasar (%bk)
Gambar 12. Hubungan perlakuan umur panen dengan kadar serat kasar (%) Dari Gambar 12 dapat dilihat bahwa semakin tinggi umur panen umbi bengkoang maka kadar serat kasar tepung bengkoang yang dihasilkan cenderung semakin tinggi. Tepung bengkoang dari umbi yang dipanen pada umur 3 bulan memiliki kadar serat terendah yaitu sebesar 12,69% sedangkan pada umur 5 bulan kadar serat meningkat jauh mencapai 22,93%.
Umbi bengkoang yang dipanen pada umur 5 bulan memiliki tekstur yang lebih berserat dibandingkan bengkoang yang lebih muda (umur panen 3 dan 4 bulan). Hal ini disebabkan terbentuknya jaringan selulosa yang lebih banyak pada umbi yang sudah tua (Maulani, et al., 2012). Pada pengamatan fisik umbi bengkoang U3 memiliki ukuran dan bobot umbi yang paling besar dibanding U1 dan U2. Begitu juga dengan kulit luar yang lebih tebal dan daging umbi yang memiliki tekstur lebih berserat. Selama peningkatan umur panen terjadi peningkatan komponen nonpati seperti serat dan lignin yang menyebabkan tekstur lebih keras dan berkayu (Nurdjanah et al., 2007) akibat terbentuknya polisakarida yang berfungsi sebagai penguat tekstur (Winarno, 2004).
Tahap II: Pembuatan Ekstrak Metanolik Bengkoang
Tepung bengkoang umur panen 3 bulan, 4 bulan, dan 5 bulan masing-masing sebanyak 25 g dilarutkan dalam n-hexan, residu diekstrak menggunakan pelarut metanol untuk mendapatkan ekstrak metanolik. Ekstrak metanolik yang diperoleh kemudian dipekatkan hingga diperoleh ekstrak metanolik yang kental. Rendemen (%)
Ekstrak kental metanolik yang diperoleh, ditimbang beratnya dan dilakukan penghitungan rendemen pada semua perlakuan umur panen. Rendemen ekstrak metanolik dapat dilihat pada Tabel 4.
Tabel 4. Rendemen ekstrak metanolik Perlakuan Berat
Keterangan : notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% dan berbeda sangat nyata pada taraf 1%.
Gambar 13. Hubungan umur panen umbi bengkoang dengan rendemen ekstrak metanolik (%)
Dari Gambar 13 dapat dilihat bahwa rendemen ekstrak metanolik meningkat pada umur panen 4 bulan dan cenderung menurun pada umur 5 bulan. Rendemen terendah terdapat pada perlakuan U1 (umur panen 3 bulan) dan tertinggi pada U2 (umur panen 4 bulan). Diduga pada umur panen 4 bulan, tanaman bengkoang banyak membentuk metabolit sekunder, sehingga mengandung komponen bioaktif yang lebih banyak dibanding pada umur panen 3 bulan, sedangkan pada umur panen 5 bulan umbi bengkoang sudah mulai mengalami proses pelayuan yang mengakibatkan pembentukan metabolit sekunder dalam tanaman menjadi berkurang.
Ekstrak metanolik yang telah diperoleh selanjutnya disuspensi dengan 50 ml akuades dan dipartisi dengan 50 ml dietil eter. Larutan dipisahkan dalam corong pisah menjadi dua fraksi, yaitu larutan bagian atas (fraksi eter) dan bagian bawah (fraksi air). Fraksi eter dan fraksi air masing-masing dipekatkan, ditimbang bobotnya, dan dilakukan penghitungan rendemen. Rendemen fraksi eter dan air dapat dilihat pada Tabel 5 dan Tabel 6.
Tabel 5. Rendemen ekstrak metanolik fraksi eter Perlakuan Berat ekstrak
metanolik (g)
Dari Tabel 5 diketahui rendemen tertinggi fraksi eter terdapat pada perlakuan umur panen 4 bulan, yaitu sebesar 0,76%, sedangkan rendemen terendah pada umur panen 3 bulan yaitu sebesar 0,563%. Dari Lampiran 7 diketahui bahwa umur panen memberikan pengaruh berbeda tidak nyata terhadap rendemen ekstrak metanolik fraksi eter.
Tabel 6. Rendemen ekstrak metanolik fraksi air Perlakuan Berat ekstrak
Dari Tabel 6 dapat dilihat bahwa rendemen tertinggi dari fraksi air terdapat pada perlakuan umur panen 4 bulan, yaitu sebesar 92,54% dan terendah pada umur panen 3 bulan yaitu sebesar 83,01%. Dari Lampiran 8 diketahui bahwa pengaruh umur panen umbi bengkoang memberikan pengaruh berbeda tidak nyata terhadap rendemen ekstrak metanolik fraksi air.
Rendemen tertinggi pada fraksi eter dan fraksi air terdapat pada perlakuan umur panen 4 bulan. Hal ini dikarenakan rendemen ekstrak metanolik tertinggi dihasilkan dari perlakuan umur panen 4 bulan. Rendemen fraksi air yang jauh lebih tinggi daripada fraksi eter, menunjukkan bahwa senyawa polar dalam ekstrak metanolik bengkoang lebih banyak daripada senyawa yang bersifat semipolar yang terlarut dalam fraksi eter.
Tahap III: Uji Aktivitas Antioksidan Ekstrak Metanolik Bengkoang Fraksi Eter/Air
Tabel 7. Aktivitas antioksidan ekstrak metanolik fraksi eter dan fraksi air
Aktivitas antioksidan (% Peredaman DPPH)
Fraksi Eter Fraksi Air
I II III
Rata-Dari Tabel 7 diketahui bahwa ekstrak metanolik umbi bengkoang fraksi eter dan fraksi air memiliki aktivitas antioksidan yang dinyatakan dengan % peredaman radikal DPPH. Senyawa antioksidan yang terkandung dalam umbi bengkoang salah satunya merupakan golongan senyawa fenolik. Cantwell et al
(2002) melaporkan komponen fenolik ekstrak metanol umbi bengkoang mirip dengan spektra UV dari senyawa katekin, tetapi tidak ditemukan senyawa katekin tunggal dalam ekstrak metanol yang dipisah menggunakan HPLC (High Performance Liquid Chromatography).
Gambar 14. Struktur kimia katekin (Lukitaningsih, 2009)
Flavonoid memiliki sekitar 9000 jenis struktur senyawa yang telah diidentifikasi. Flavonoid sebagai satu dari senyawa alami yang paling beragam dan tersebar luas mungkin merupakan senyawa fenol alami yang paling penting. Senyawa ini memiliki spektrum yang luas dalam aktivitas biologi dan kimia termasuk dalam penghambatan radikal bebas. Kelompok utama flavonoid adalah flavon, isoflavon, flavonol, flavanon, antosianin, katekin, dan khalkon (Lukitaningsih, 2009).
Berbeda dengan Cantwell (2002) yang menduga komponen fenolik dalam ekstrak umbi bengkoang adalah katekin, Lukitaningsih (2009) dalam penelitiannya telah mengidentifikasi senyawa isoflavonoid di dalam ekstrak umbi bengkoang. Senyawa tersebut antara lain daidzein, daidzein-7-O-β-glucopiranose,
(8,9)-Furanyl-pterocarpan-3-ol, 5-gydroxy-daidzein-7-O- β-glucopiranose,
4-2(2-(Furane-2-yl)ethyl-2-methyl-2,5-dihydrofurane-3-carbaldehyde, dan 2-butoxy-2,5-bis(hydroxymethyl)-tetrahydrofurane-3,4-diol. Struktur senyawa-senyawa tersebut dapat dilihat pada Gambar 15, Gambar 16, Gambar 17, Gambar 18, Gambar 19, dan Gambar 20.
Gambar 16. Struktur kimia daidzein-7-O-β-glucopiranose (Lukitaningsih, 2009)
Gambar 17. Struktur kimia (8,9)-Furanyl-pterocarpan-3-ol (Lukitaningsih, 2009)
Gambar 18. Struktur kimia 5-hydroxy-daidzein-7-O- β-glucopiranose (Lukitaningsih, 2009)
Gambar 19. Struktur kimia 4-2(2-(Furane-2-yl)ethyl-2-methyl-2,5-dihydrofurane- 3-carbaldehyde (Lukitaningsih, 2009)
Berdasarkan kelarutannya dalam air, flavonoid terbagi atas struktur aglikon dan glukosida. Di alam, flavonoid terbanyak ditemukan dalam bentuk
7-O-glukosida. Namun senyawa ini tidak ditemukan dalam ekstrak umbi
bengkoang. Diantara komponen isoflavonoid yang teridentifikasi dalam ekstrak umbi bengkoang, 4-(2-(furane-2-yl)-2-methyl-2,5-dihydrofurane-3-carbaldehyde
adalah senyawa yang memiliki aktivitas antioksidan tertinggi.
Lukitaningsih (2009) menyatakan aktivitas antioksidan ekstrak umbi bengkoang tertinggi dihasilkan pada ekstrak umbi bengkoang menggunakan pelarut etil asetat, sedangkan senyawa yang memiliki aktivitas antioksidan tertinggi dari ekstrak umbi bengkoang adalah senyawa trilinolein, kemudian diikuti oleh 4-(2-(furane-2-yl)-2-methyl-2,5-dihydrofurane-3-carbaldehyde, daidzein-7-O-ßglucopyranose, dan 2-butoxy-2,5-bis(hydroxymethyl)-tetrahydrofurane-3,4-diol. Senyawa trilinolein mengandung banyak gugus karbonil serta ikatan rangkap C=C, hal inilah yang menyebabkan trilinolein memiliki aktivitas antioksidan yang tinggi. Sedangkan golongan senyawa isoflavon seperti daidzein dan daidzein-7-O-ßglucopyranose mengandung gugus fenol yang dapat memberikan atom H pada radikal bebas.
Pengaruh interaksi antara umur panen umbi bengkoang dengan konsentrasi ekstrak metanolik fraksi eter terhadap aktivitas antioksidan (% peredaman DPPH)
DPPH) dapat dilihat pada Tabel 8. Hubungan interaksi antara konsentrasi ekstrak metanolik fraksi eter dengan umur panen umbi bengkoang terhadap aktivitas antioksidan dapat dilihat pada Gambar 21.
Tabel 8. Uji LSR efek utama interaksi antara konsentrasi ekstrak metanolik fraksi eter terhadap aktivitas antioksidan (% peredaman DPPH)
Jarak LSR Perlakuan Rataan
Keterangan : notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% dan berbeda sangat nyata pada taraf 1%.
Gambar 21. Hubungan interaksi antara konsentrasi ekstrak metanolik fraksi
eter dengan umur panen umbi bengkoang terhadap aktivitas antioksidan fraksi eter (%)