Lampiran 2. Gambar tumbuhan jambu mete
Lampiran 3. Gambar daun segar dan simplisia dari daun jambu mete (Anacardium occidentale L)
Daun jambu mete segar(Anacardium occidentale L)
Lampiran 4.Bagan pembuatan ekstrak dan fraksinasi
Dimasukkan kedalam wadah
Ditambahkan etanol80% sampai serbuk terendam sempurna
Direndam selama 5 hari terlindung dari cahaya, sambil sesekali diaduk
Disaring
Dimaserasi kembali dengan pelarut etanol 80%
Dipekatkan dengan rotary evaporator Dikeringkan dengan freeze dryer
Ditambah sedikit etanol
Dimasukkan ke dalam corong pisah Ditambah akuades Serbuk simplisia daun jambu mete
Maserat Ampas
Maserat Ampas
Ekstrak etanol
Fraksi n-heksan Sisa
Fraksi n-heksan
Fraksi kloroform Sisa
Fraksi kloroform
Fraksi etilasetat Sisa
Lampiran 5. Bagan pengujian aktivitas antibakteri
Diambil 1 ose
Disuspensikan ke dalam 10 ml NB
Diukur kekeruhan pada panjang gelombang 580 nm sampai diperoleh transmitan 25 %
Dimasukkan 0,1 ml inokulum ke dalam cawan petri
Ditambahkan 20 ml media nutrient agar ke dalam cawan petri
Dihomogenkan dan dibiarkan memadat
Ditanamkan silinder logam Dimasukkan 0,1 ml ekstrak dengan berbagai konsentrasi Diinkubasi pada suhu 36-37ºC selama 18-24 jam
Diukur diameter daerah hamabatan di sekitar silinder logam
Stok kultur
Inokulum bakteri
Media padat
Lampiran 6. Hasil pengukuran diameter daerah hambat ekstrak etanol daun jambu mete terhadap pertumbuhan bakteriStaphylococcus epidermidis
Konsentrasi Ekstrak
etanol (mg/ml)
Diameter daerah hambatan (mm) D1
Lampiran 7. Hasil pengukuran diameter daerah hambat ekstrak etanol daun jambu mete terhadap pertumbuhan bakteri Streptococcus mutans
Konsentrasi Ekstrak
etanol (mg/ml)
Diameter daerah hambatan (mm) D1
Lampiran 8. Hasil pengukuran diameter daerah hambat ekstrak etanol daunjambu mete terhadap pertumbuhan bakteri Staphylococcus aureus
Konsentrasi Ekstrak
etanol (mg/ml)
Diameter daerah hambatan (mm) D1
Lampiran 9. Hasil pengukuran diameter daerah hambat ekstrak etanol daun jambu mete terhadap pertumbuhan bakteri Escherichia coli
Konsentrasi Ekstrak
etanol (mg/ml)
Diameter daerah hambatan (mm) D1
Lampiran 10. Hasil pengukuran diameter daerah hambat fraksi etilasetat daunjambu mete terhadap pertumbuhan bakteri Staphylococcus epidermidis
Konsentrasi Fraksi etilasetat
(mg/ml)
Diameter daerah hambatan (mm) D1
Lampiran 11. Hasil pengukuran diameter daerah hambat fraksi etilasetat daunjambu mete terhadap pertumbuhan bakteri Streptococcus mutans
Konsentrasi Fraksi etilasetat
(mg/ml)
Diameter daerah hambatan (mm) D1
Lampiran 12. Hasil pengukuran diameter daerah hambat fraksi etilasetat daun jambu mete terhadap pertumbuhan bakteri Staphylococcus aureus
Konsentrasi Fraksi etilasetat
(mg/ml)
Diameter daerah hambatan (mm) D1
Lampiran 13. Hasil pengukuran diameter daerah hambat fraksi etilasetat daun jambu mete terhadap pertumbuhan bakteri Escherichia coli
Konsentrasi Fraksi etilasetat
(mg/ml)
Diameter daerah hambatan (mm) D1
Lampiran16. Hasil uji aktivitas antibakteri ekstrak etanol daun jambu mete terhadap bakteri Staphylococcus aureus
Lampiran 19. Hasil uji aktivitas antibakteri fraksi n-heksan daun jambu mete terhadap bakteri Streptococcus mutans
DAFTAR PUSTAKA
Abulude, F.O., Ogunkoya, M.O., and Adebote, V.T. (2009). Phytochemical and antibacterial investigations of crude extracts Of Leaves and stem barks Of Anacardium occidentale. Continental J. Biological Sciences 2: 12-19. Anonimous. (1982). The Oxoid Manual of Culture Media, Ingredient and other
Laboratory Service, edisi ke-5. Basingstoke-England. Halaman 32, 64. Ayepola, O.O and Ishola, R.O. (2009). Evaluation Of Antimicrobial activity Of
Anacardium occidentale Linn. Advances in Medical and Dental Sciences. 3(1): 1-3.
Brooks, G.F., Jawetz, Melnick., and Adleberg’s. (2001). Mikrobiologi KedokteranEdisi I. Jakarta: Salemba Medika. Halaman 286
Cseke, L.J., Ara, K., Kaufman, P.B., Setzer, W.N.,and Brielmann, H.L. (2006). The Chemical Components ol Plants. New York: Taylor&Francis CRC. Halaman 22, 25
Dahake, A.P., Vishal D.Joshi., and Arun B.Joshi. (2009). Antimicrobial Screening of Different Extract of Anacardium occidentale Linn. Leaves. International Journal of ChemTech Research. 1(4): 856-858.
Dalimartha. (2000). Atlas Tumbuhan Obat Indonesia. Jakarta: Trubus Agriwidya. Halaman 80.
Depkes RI. (1995), Materia Medika Indonesia Jilid IV.Jakarta: Departemen Kesehatan Republik Indonesia. Halaman 43-51.
Depkes RI. (2008). Farmakope Herbal Indonesia Edisi I. Jakarta: Departemen Kesehatan Republik Indonesia. Halaman 36.
Ditjen POM. (1979). Farmakope Indonesia. Edisi III. Jakarta: Depkes RI.Halaman 9.
DitjenPOM.(1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan RI. Halaman 891-898, 1154.
Ditjen POM. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Depkes RI. Halaman 1, 10-11
Duke, James A., Mary Jo B.G., and Andrea, R.O. (2009). Medicinal Plants of Latin America. New York: CRC Press. Halaman 37.
Farnsworth, N.R. (1966). Biologycal and Phytochemical Screening of Plants.Journal of Pharmaceutical Science. 55(3): 262-264.
Harborne, J.B. (1987). Metode Fitokimia. Penerjemah: Kosasih Padmawinata dan Iwang Soediro. Bandung: Penerbit ITB. Halaman 147
Hardv, S.P. (2002). Human Microbiology. New York: Taylor&Francis Inc. Halaman 3-5
Hawley, L.B. (2001). Intisari Mikrobiologi dan Penyakit Infeksi. Jakarta: Penerbit Hipokrates. Halaman 46-47, 72-73
Heinrich. (2009). Farmakognosi dan Fitoterapi. Jakarta: Penerbit Buku Kedokteran EGC. Halaman 82, 85, 103
Igbinosa, O.O., Igbinosa, E.O., and Aiyegoro, O.A. (2009). Antimicrobial Activity and Phytochemical Screening of Stem Bark Extracts From Jatropha curcas (Linn). 3(2): 58-62.
Irianto, K. (2007). Mikrobiologi. Bandung: CV Yrama Widya. Halaman 10-12 Jayalakshmi, B., Raveesha, K.A., and Amruthesh, K.N. (2011). Phytochemical
Investigations and Antibacterial Plants Against Pathogenic Bacteria. Journal Of Applied Pharmaceutical Science. 01(05): 124-128
Jawetz, E. (2001). Mikrobiologi Kedokteran. Penerjemah: Mudi Hardi, E., dkk. Surabaya: Penerbit Salemba Medika. Halaman 318, 372
Kumala dan Oktora, R. (2006). Pemanfaatan Obat Tradisional Dengan Pertimbangan Manfaat dan Keamanannya.Majalah Ilmu Kefarmasian. 3(1): 1-7.
Lay, B.W. (1994). Analisis Mikroba di Laboratorium. Jakarta: PT. Raja Grafindo Persada. Halaman 109.
Majumbar, S.H., Chakraborthy, G.S., and Kulkarni, K.S. (2008). Medicinal Potentials of Semecarpus Anacardium Nut. Journal of Herbal Medicine and Toxicology. 2(2): 9-13.
Markham, K.R. (1982). Technique of Flavonoid Identification. Terjemahan K. Padmawinata. (1988). Cara Mengidentifikasi Flavonoid. Bandung: ITB press. Halaman 1.
Masaki, H.,and Isao Kubo. (1991). Antibacterial Agents from The Cashew Anacardium occidentale (Anacardiaceae) Nut Shell Oil. Journal Of Agricultural Food Chemistry. 39: 418-421.
Pratiwi, S.T. (2008). Mikrobiologi Farmasi. Jakarta: Erlangga. Halaman 23, 111-117
Robinson, T. (1995). Kandungan Organik Tumbuhan Tinggi. Edisi keenam. Bandung: Penerbit ITB. Halaman 52, 191, 193
Saleem, M., Mamona, N., and Young, S.L. (2009) Antimicrobial Natural Products: An Update On Future Antibiotic drug Candidates. 27: 238-254. Sherley. (2008). Taksonomi Koleksi Tanaman Obat Kebun Tanaman Obat
Citeureup. Jakarta: BPOM RI. Halaman 8
Vijayakumar and Kalaichelvan, P.T. (2011). Antioxidant And Antimicrobial Activity Using Different Extracts of Anacardium Occidentale L.International Journal of Applied Biology And Pharmaceutical Technology. 2(3): 436-443.
Watimena. (1991). Farmakodinamik dan Terapi Antibiotik. Yogyakarta: Universitas Gadjah Mada Press. Halaman 60-61
WHO. (2000). General Guidlines for Methodologies on Research and Evaluation of Traditional Medicine. Geneva: World Health Organization. Halaman 1.
BAB III
METODE PENELITIAN
Metode penelitian yang dilakukan adalah metode eksperimental, meliputi penyiapan bahan, skrining fitokimia, dan pembuatan ekstrak. Pengujian aktivitas antibakteri dengan metode difusi agar menggunakan silinder logam. Parameter yang dilihat adalah besarnya diameter hambat pertumbuhan mikroba.
3.1 Alat
Alat yang digunakan dalam penelitian ini adalah alat–alat gelas, autoklaf (Fisons), blender (Philips), bola karet, desikator, freeze dryer (Modulio), inkubator (Fiber Scientific), jangka sorong, jarum ose, kamera digital (Canon), kompor (Sharp), Laminar Air Flow Cabinet (Astec HLF 1200L), lemari pendingin (Toshiba), neraca listrik (Mettler AE 200), pinset, pipet mikro (Eppendorf),rotary evaporator (Haake D), silinder logam, dan spektrofotometri visibel (Dynamic).
3.2 Bahan
serbuk magnesium, serbuk zinkum, timbal (II) asetat, dan toluena. Nutrient agar, Staphylococcusepidermidis (ATCC 6918), Streptococcus mutans(ATCC 25175), Staphylococcus aureus(ATCC 6538)dan Escherichia coli(ATCC 25922).
3.3 Pengumpulan Bahan Tumbuhan
Pengumpulan bahan tumbuhan dilakukan secara purposif yaitu tanpa membandingkan dengan tumbuhan yang sama dari daerah lain. Sampel yang digunakan adalah daun jambu mete (Anacardium occidentale) yang masih segar, yang diambil dari Desa Muliorejo, Kecamatan Sunggal, Kabupaten Deli Serdang, Propinsi Sumatera Utara.
3.3.1 Identifikasi tumbuhan
Identifikasi sampel dilakukan diHerbarium Medanense, Universitas Sumatera Utara. Hasil identifikasi tumbuhan dapat dilihat pada Lampiran 1, halaman 43 dan gambar tumbuhan dapat dilihat pada Lampiran 2, halaman 44. 3.3.2 Pengeringan simplisia
Daun jambu mete yang telah dikumpulkan sebanyak 2,5 kg dicuci bersih dengan air mengalir, kemudian ditiriskan lalu ditimbang, selanjutnya bahan dikeringkan dengan cara diangin-anginkan di udara terbuka terlindung dari sinar matahari langsung, setelah kering diserbuk dan disimpan dalam kantung plastik ditempat yang terlindung dari sinar matahari.
3.4 Pembuatan Pereaksi
hidroksida 2N dan timbal (II) asetat 0,4 M. Liebermann-Bouchard menurut Harborne (1987). Pereaksi Dragendorff menurut Zweig dan Sherma (1987).
3.4.1 Pereaksi asam klorida 2 N
Sebanyak 16,67 ml asam klorida pekat dilarutkan dalam air suling hingga volume 100 ml.
3.4.2 Pereaksi asam sulfat 2 N
Sebanyak 5,4 ml asam sulfat pekat dilarutkan dalam air suling hingga volume 100 ml.
3.4.3 Pereaksi besi (III) klorida 1%
Sebanyak 1 g besi (III)klorida dilarutkan dalam air suling hingga 100 ml. 3.4.4 Pereaksi Bouchardat
Sebanyak 4 g kalium iodida, dilarutkan dalam sedikit air suling kemudian ditambahkan 2 g iodium, setelah semuanya larut ditambahkan air suling hingga 100 ml.
3.4.5 Pereaksi Dragendorff
Sebanyak 0,85 g bismut (III) nitrat ditimbang, kemudian dilarutkan dalam 100 ml asam asetat glasial ditambahkan 40 ml air suling. Pada wadah lain ditimbang 8 g kalium iodida lalu dilarutkan dalam 20 ml air suling, lalu campurkan kedua larutan sama banyak. Kemudian ditambahkan 20 ml asam asetat glasial dan diencerkan dengan air suling hingga 100 ml.
3.4.6 Pereaksi Liebermann-Burchard
3.4.7 Pereaksi Mayer
Sebanyak 1,35 g raksa (II) klorida dilarutkan dalam 60 ml air suling. Pada wadah lain sebanyak 5 g kalium iodida dilarutkan dalam 10 ml air lalu campurkan keduanya dan ditambahkan air suling hingga 100 ml.
3.4.8Pereaksi molish
Sebanyak 3 g alfa-naftol ditimbang, kemudian dilarutkan dalam asam nitrat 0,5 N hingga volume 100 ml.
3.4.9 Pereaksi natrium hidroksida 2 N
Sebanyak 8,002 g kristal natrium hidroksida dilarutkan dalam air suling hingga 100 ml.
3.4.10 Pereaksi timbal (III) asetat 0,4 M
Sebanyak 15,17 g timbal (II) asetat dilarutkan dalam air bebas karbondioksida hingga 100 ml.
3.5 Skrining Fitokimia 3.5.1 Pemeriksaan alkaloida
Sebanyak 0,5 g serbuk simplisia ditambahkan 1 ml asam klorida 2 N dan 9 ml air suling, dipanaskan di atas penangas air selama 2 menit, didinginkan dan disaring. Filtrat dipakai untuk uji alkaloida sebagai berikut:
a. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes larutan pereaksi Mayer akan terbentuk endapan berwarna putih atau kuning.
c. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes larutan pereaksi Dragendorff, akan terbentuk endapan merah atau jingga.
Alkaloida positif jika terjadi endapan atau kekeruhan paling sedikit dua dari tiga percobaan diatas membrikan hasil positif. Pada penambahan pereaksi Mayer terbentuk endapan berwarna putih atau kuning. Pada penambahan peeaksi Bouchardat terbentuk endapan berwarna coklat (Depkes, 1989). 3.5.2 Pemeriksaan antrakinon
Sebanyak 0,2 g serbuk simplisia ditambah 5 ml asam sulfat 2 N, dipanaskan sebentar, setelah dingin ditambahkan 10 ml benzen, dikocok dengan 2 ml natrium hidroksida 2 N, didiamkan. Lapisan air berwarna merah dan lapisan benzen tidak berwarna menunjukkan adanya antrakinon (Depkes,1989).
3.5.3 Pemeriksaan tanin
Sebanyak 0,5 g serbuk simplisia disari dengan 10 ml air suling lalu disaring, filtratnya diencerkan dengan air sampai tidak berwarna. Larutan diambil 2 ml dan ditambahkan 1-2 tetes pereaksi besi (III) klorida 1%. Jika terjadi warna biru atau kehitaman menunjukkan adanya tanin (Depkes, 1989).
3.5.4 Pemeriksaan flavonoida
3.5.5 Pemeriksaan glikosida
Sebanyak 3 g serbuk simplisia disari dengan 30 ml campuran etanol 96 dengan air (7:3) direfluks selama 10 menit, didinginkan dan disaring. Filtrat diambil 20 ml kemudian ditambahkan 25 ml air suling dan 25 ml timbal (II) asetat 0,4 M, dikocok, didiamkan selama 5 menit lalu disaring. Filtrat disari dengan 20 ml campuran kloroform dan isopropanol (3:2), dilakukan berulang sebanyak 3 kali. Kumpulan sari air diuapkan pada suhu tidak lebih dari 50ºC. Sisanya dilarutkan dalam 2 ml metanol. Larutan sisa digunakan untuk percobaan:
Sebanyak 0,1 ml larutan percobaan dimasukkan dalam tabung reaksi dan diuapkan diatas penangas air. Pada sisa ditambahkan 2 ml air dan 5 tetes pereaksi Molish. Secara perlahan-lahan ditambahkan 2 ml asam sulfat pekat melalui dinding tabung, terbentuk cincin warna ungu pada batas antara kedua cairan menunjukkan adanya ikatan gula (Depkes, 1995).
3.5.6 Pemeriksaan steroida/triterpenoida
Sebanyak 1 g serbuk simplisia dimaserasi dengan 20 ml eter selama 2 jam, disaring, filtrat diuapkan dalam cawan penguap, pada sisanya ditambahkan 20 tetes asam asetat anhidrida dan 1 tetes asam sulfat pekat (pereaksi Liebermann-Burchard). Apabila terbentuk warna ungu atau merah yang berubah menjadi biru hijau menunjukkan adanya steroida/triterpenoida (Harborne, 1987).
3.5.7 Pemeriksaan saponin
setinggi 1-10cm dan tidak hilang dengan penambahan 1 tetes asam klorida 2 N menunjukkan adanya saponin (Depkes, 1995).
3.6 Pembuatan Ekstrak Etanol Daun Jambu Mete
Pembuatan ekstrak dilakukan dengan cara maserasi menggunakan pelarut etanol 80% (Depkes,2008). Sebanyak 500 g serbuk simplisia daun jambu mete dimaserasi dengan pelarut etanol 80% sampai seluruh serbuk terendam, ditutup dan dibiarkan selama 5 hari terlindung dari cahaya, sambil sesekali diaduk. Campuran tersebut diserkai setelah 5 hari, kemudian ampasnya dicuci dengan etanol, filtrat dimasukkan dalam bejana dan disimpan di tempat yang terlindung dari cahaya selama 2 hari, kemudian dienap tuangkan (Depkes, 1979). Seluruh maserat digabung dan dipekatkan dengan bantuan alat rotary evaporator pada temperatur tidak lebih dari 40ºC sampai diperoleh ekstrak kental, kemudian dikeringkan dengan freeze dryer. Bagan pembuatan ekstrak dan fraksinasi dapat dilihat pada Lampiran 4, halaman 46.
3.7 Pembuatan Fraksi n-Heksan, Kloroform Dan Etilasetat Daun Jambu Mete
etilasetat 50 ml, kemudian dilakukan pemisahan sesuai dengan prosedur fraksinasi diatas sampai diperoleh fraksi etilasetat yang jernih.Hasil fraksinasi n-heksan, kloroform dan etilasetat masing-masing di rotary evaporator selanjutnya di freeze dryer hingga diperoleh ekstrak kental fraksi n-heksan, fraksi kloroform dan fraksi etilasetat.
3.8 Sterilisasi Alat
Alat-alat yang digunakan dalam uji aktivitas antimikroba ini, disterilkan terlebih dahulu sebelum dipakai. Alat-alat gelas disterilkan didalam oven pada suhu 170ºC selama 1 jam. Media disterilkan di autoklaf pada suhu 121ºC selama 15 menit. Jarum ose dan pinset dipijar dengan lampu bunsen (Lay, 1994).
3.9Pembuatan Media
3.9.1 Media nutrient agar (NA)
Komposisi: Lab-lemco powder 1 g
Yeast extract 2 g
peptone 5 g
sodium chloride 5 g
Agar 15 g
Cara pembuatan:
3.9.2 Media nutrien broth (NB)
Komposisi : Lab-lemco powder 1 g
Yeast extract 2 g
peptone 5 g
sodium chloride 5 g
Cara pembuatan:
Sebanyak 13 g serbuk Nutrient Broth (NB) yang sudah jadi ditimbang, dilarutkan dalam air suling steril sedikit demi sedikit kemudian volumenya dicukupkan hingga 1 L dengan bantuan pemanasan sampai semua bahan larut sempurna, kemudian disterilkan di autoklaf pada suhu 121oC selama 15 menit (Oxoid, 1982).
3.10 Pembuatan Agar Miring
Ke dalam tabung reaksi steril dimasukkan 3 ml media nutrient agar steril, didiamkan pada temperatur kamar sampai sediaan membeku pada posisi miring kira-kira 45º. Kemudian disimpan dalam lemari pendingin (Lay, 1994).
3.11 Pembuatan Stok Kultur Bakteri
3.12Penyiapan Inokulum Bakteri
Koloni bakteri Staphylococcusepidermidis, Streptococcus mutans, Staphylococcus aureus dan Escherichia coli, diambil dari stok kultur dengan jarum ose steril lalu disuspensikan dalam tabung reaksi yang berisi 10 ml larutan Nutrient Brooth, diaduk homogen, lalu diinkubasikan dalam inkubator 37ºC selama 3 jam dan diukur pada panjang gelombang 580 nm dengan menggunakan alat spektrofotometri visibel sampai diperoleh transmitan 25 % (Depkes, 1995).
3.13 Pembuatan Larutan Uji (Ekstrak Etanol, Fraksi n-Heksan, Fraksi Kloroform Dan Fraksi Etilasetat) Dengan Berbagai Konsentrasi
Ekstrak etanol ditimbang 5 g dilarutkan dengan menggunakan pelarut DMSO (Dimetil sulfoksida) hingga 10 ml maka konsentrasi ekstrak adalah 500 mg/ml kemudian dibuat pengenceran selanjutnya sampai diperoleh ekstrak dengan konsentrasi 400 mg/ml; 350 mg/ml; 300 mg/ml; 250 mg/ml; 200 mg/ml; 150 mg/ml; 100 mg/ml; 50 mg/ml; 25 mg/ml; 10 mg/ml; 5 mg/ml. Dilakukan prosedur yang sama terhadap fraksi n-heksan, fraksi kloroform dan fraksi etilasetat.
3.14 Uji Aktivitas Antibakteri Ekstrak Etanol, Fraksi n-heksan, Fraksi Kloroform dan Fraksi Etilasetat daun Jambu Mete Dengan Metode Difusi Agar
BAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Tumbuhan
Identifikasi tumbuhan yang digunakan dilakukan di Herbarium Medanense, Universitas Sumatera Utara, hasilnya adalah daun jambu mete (Anacardium occidentale L.), familia Anacardiaceae.
4.2 Hasil Skrining Fitokimia
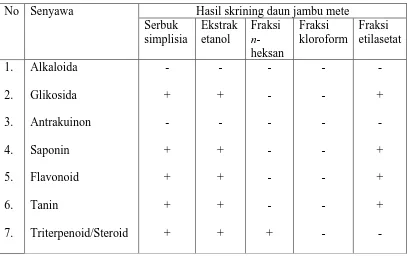
Hasil skrining fitokimia serbuk simplisia, ekstrak etanol, fraksi n-heksan, fraksi kloroform, dan fraksi etilasetat dari daun jambu mete menunjukkan adanya alkaloid, glikosida, saponin, flavonoid, tanin dan triterpenoid/steroid. Hasil skrining dapat dilihat pada Tabel 4.1 berikut.
Tabel 4.1. Hasil skrining fitokimia ekstrak etanol, fraksi n-heksan, fraksi kloroform dan fraksi etil asetat
No Senyawa Hasil skrining daun jambu mete
Serbuk
Pada serbuk simplisia daun jambu mete yang ditambah dengan serbuk Mg dan serbuk Zn dengan asam klorida pekat memberikan warna merah, menunjukkan adanya senyawa flavonoid. Skrining glikosida ditunjukkan dengan penambahan pereaksi Molish dan asam sulfat pekat dimana terbentuk cincin ungu. Penambahan FeCl31% memberikan warna biru kehitaman yang menunjukkan
adanya senyawa tanin. Penambahan Liebermann-Burchard memberikan warna biru hijau menunjukkan adanya steroid. Adanya kandungan senyawa flavonoid, tanin, steroid menunjukkan bahwa daun jambu mete mempunyai aktivitas sebagai antibakteri (Jayalakshmi, 2011).
Hasil maserasi 500 g serbuk simplisia daun jambu mete diperoleh 58,8 g ekstrak etanol. Terhadap 20 g ekstrak etanol daun jambu mete dilakukan fraksinasi menggunakan pelarut n-heksan, setelah diuapkan diperoleh sebanyak 3,5 g. Hasil difraksinasi dengan pelarut kloroform setelah diuapkan diperoleh sebanyak 4,3 g. Hasil difraksinasi dengan pelarut etilasetat setelah diuapkan diperoleh sebanyak 4,5 g.
Tabel 4.2 Hasil pengukuran diameter daerah hambatan ekstrak etanol daun jambu mete terhadap pertumbuhan bakteri Staphylococcus epidermidis, Streptococcus mutans, Staphylococcus aureus dan Escherichia coli. Konsentrasi
Ekstrak etanol (mg/ml)
Diameter daerah hambatan (mm)* SE
Keterangan: (*) hasil rata-rata tiga kali pengukuran, (-) tidak ada hambatan SE = Staphylococcus epidermidis, SM = Streptococcus mutans, SA =Staphylococcus aureus, EC = Escherichia coli
Efektifitas flavonoid melawan patogen dengan cara merusak permeabilitas dinding sel dan porin pada membran sel terluar pada mikroorganisme, hal ini dapat menghalangi masuknya asam amino pada porin. Aktifitas flavonoid juga dapat melalui kemampuannya membentuk komplek dengan ekstraseluler dan protein yang larut dan dilanjutkan dengan dinding sel. Mekanisme kerja tanin adalah dengan menciutkan dan mengendapkan protein sel yang dapat mengganggu permeabilitas sel, sehingga pertumbuhannya akan terhambat atau bahkan mati (Saleem, 2009).
Tanin memiliki kemampuan sebagai antibakteri dengan cara mengganggu fungsi membran sitoplasma yang menyebabkan bocornya metabolit penting yang menginaktifkan system enzim bakteri. Sifat tanin yang sebagai pengelat memiliki efek spasmolitik yang menciutkan dinding sel sehingga mengganggu permeabilitas sel sehingga menghambat pertumbuhan (Wonghirundecha dan Punnanee, 2012).
Diameter daerah hambatan terbesar pada konsentrasi 500 mg/ml ekstrak etanol terhadap SE (23,73 mm), SM (22,13 mm), SA (22,00 mm) dan EC (21,90 mm). Pada data di atas telah memenuhi syarat Farmakope Indonesia yaitu ekstrak etanol konsentrasi 50 mg/ml diameter hambat efektif 14 mm terhadap SE dan konsentrasi 100 mg/ml diameter hambat efektif terhadap SM (15,01 mm), SA (14,73 mm) dan EC (15,80 mm).
mm), SM (14,20 mm), SA (14,48 mm)dan konsentrasi 5 mg/ml terhadap bakteri EC ( 14,10 mm).
Tabel 4.3 Hasil pengukuran diameter daerah hambatan fraksi etilasetat daun jambu mete terhadap pertumbuhan bakteri Staphylococcus epidermidis, Streptococcus mutans, Staphylococcus aureus dan Escherichia coli.
Konsentrasi fraksi etilasetat
(mg/ml)
Diameter daerah hambatan (mm)* SE
Keterangan: (*) hasil rata-rata tiga kali pengukuran, (-) tidak ada hambatan SE = Staphylococcus epidermidis, SM = Streptococcus mutans,
SA =Staphylococcus aureus, EC = Escherichia coli
dan dapat menghambat pertumbuhan beberapa jenis bakteri sepertiStaphylococcus aureus,Escherichia coli (Jayalakshmi, et al., 2011) dan Streptococcus mutans ( Masaki dan Isao, 1991).
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
a. hasil skrining daun jambu mete menunjukkan adanya golongan senyawa kimia yang terdapat dalam simplisia dan ekstrak etanol yaitu tanin, flavonoida, triterpenoida/steroida, glikosida, dan saponin. Golongan senyawa kimia yang terdapat dalam fraksi n-heksan yaitu triterpenoida/steroida. Pada fraksi kloroform tidak mengandung metabolit sekunder. Golongan senyawa kimia yang terdapat pada fraksi etilasetat yaitu tanin, flavonoida, glikosida dan saponin.
b. hasil uji aktivitas antibakteri ekstrak etanol pada konsentrasi 50 mg/ml diameter hambat efektif 14 mm terhadap SE dan konsentrasi 100 mg/ml diameter hambat efektif terhadap SM (15,01 mm), SA (14,73 mm) dan EC (15,80 mm).dan untuk fraksi etilasetat pada konsentrasi 10 mg/ml terhadap bakteri SE (16,15 mm), SM (14,20 mm), SA (14,48 mm)dan konsentrasi 5 mg/ml terhadap bakteri EC ( 14,10 mm). Fraksi n-heksan dan fraksi kloroform tidak memberikan daya hambat.
5.2 Saran
BAB II
TINJAUAN PUSTAKA
2.1Uraian Tumbuhan
Uraian tumbuhan meliputi, morfologi tumbuhan,habitat dan daerah tumbuh, sistematika tumbuhan, nama asing, penggunaan tumbuhan serta kandungan senyawa kimia.
2.1.1 Morfologi tumbuhan
Pohon tinggi 8-12 m, memiliki cabang dan ranting yang banyak. Batang melengkung, berkayu, bergetah, percabangan mulai dari bagian pangkalnya (Dalimartha, 2008) batang berwarna putih kotor (Sherley, 2008). Daun tunggal, bertangkai, panjang 4-22,5 cm, lebar 2,5-15 cm. Helaian daun berbentuk bulat telur sungsang, tepi rata, pangkal runcing, ujung membulat dengan lekukan kecil di bagian tengah, pertulangan menyirip, berwarna hijau (Dalimartha, 2000).
Bunga majemuk, bentuk malai, terletak di ketiak daun dan di ujung cabang, mempunyai daun pelindung berbentuk bulat telur dengan panjang 4-55 mm dan berwarna hijau muda. Mahkota bunga berbentuk runcing, saat masih muda berwarna putih setelah tua berwarna merah (Sherley, 2008). Bunga berumah satu memiliki bunga betina dan bunga jantan (Dalimartha, 2000).
cokelat tua (Dalimartha, 2000). Akarnya berupa akar tunggang dan berwarna cokelat (Sherley, 2008).
2.1.2Habitat dan daerah tumbuh
Jambu mete atau jambu monyet berasal dari Brazil, tersebar di daerah tropik dan ditemukan pada ketinggian antara 1-1.200 m diatas permukaan laut. Jambu mete akan berbuah lebih baik di daerah beriklim kering dengan curah hujan kurang dari 500 mm per tahun. Tanaman ini dapat tumbuh di segala macam tanah, asalkan jangan di tanah lempung yang pekat dan tergenang air. Tanaman tumbuhan jambu mete banyak tumbuh di Jawa Tengah, Jawa Timur dan Yogyakarta (Dalimartha, 2000).
2.1.3 Sistematika Tumbuhan
Sistematika tumbuhan jambu mete: Divisi : Spermatophyta Sub Divisi : Angiospermae Kelas : Dicotyledoneae Bangsa : Sapindales Suku : Anacardiaceae Marga : Anacarrdium
Jenis : Anacardium occidentale L.
Di luar negeri orang menyebutnya Cashew (Inggris), cajou, anacardier (Perancis), kasoy (Tagalog), mamuang, himmaphan, yaruang (Thailand), dao lon hot, cay dieu (Vietnam), hijli-badam, kaju (India&Pakistan)(Dalimartha, 2000).
(Sumatera), jambu mede, jambu mete, jambu siki (Jawa), buwah monyet, jambu jipang, jambu dwipa, nyambu monyet, jambu parang, jambu sempal (Kalimantan),jambu dare, jambu sereng (Sulawesi), kanoke, ( Maluku) (Dalimartha, 2000).
2.1.4 Penggunaan tumbuhan
Tanaman asal Brazil ini, memiliki buah yang tergolong unik. Buah Jambu Monyet merupakan tangkai buah yang mengalami penggelembungan dan menjadi buah semu yang lunak.Biji bulat panjang, melengkung pipih dan berwarna coklat tua. Biji inilah yang sering disebut kacang mete (Dalimartha, 2000).
Kulit kayu berbau lemah, rasanya kelatdan lama-kelamaan menimbulkan rasa tebal di lidah. Khasiatnya sebagai pencahar, astringen dan memacu aktivitas enzim percernaan. Penggunaan dalam masyarakat untuk mengobati sembelit , 10 g kulit kayu jambu mete dicuci sampai bersih, lalu rebus dalam 2 gelas air (selama 20 menit). Disaring setelah dingin dan air saringannya diminum sehari 2 kali (sama banyak) (Dalimartha, 2008).
Akar daun jambu mete digunakan sebagai pencuci perut. Daun jambu mete yang masih muda dimanfaatkan sebagai lalap di daerah Jawa bagian timur sebagai salah satu pengganti sayuran dalam konsumsi mereka sehari-hari(Dalimartha, 2000).
2.1.5 Kandungan kimia tumbuhan
Kulit kayu mengandung tanin yang cukup banyak zat samak, asam galat, dan gingkol katekin. Daun mengandung tanin-galat, flavonol, asam anakardiol, asam elegat, senyawa fenol, kardol, dan metil kardol. Buah mengandung protein, lemak, vitamin (A,B dan C), kalsium, fosfor, besi dan belerang. Asam anakardat berkhasiat bakterisidal, fungisidal, mematikan cacing dan protozoa (Dalimartha, 2008).Daun jambu mete mengandung senyawa flavonoid, terpenoid/steroid, tanin dan glikosida (Jayalakshmi, 2011).
2.2 Kandungan Kimia 2.2.1Flavonoida
Flavonoid merupakan salah satu golongan terbesar senyawa metabolit sekunder dan terdistribusi pada spesies tanaman yang beragam (Saleem, et al., 2009). Flavonoid terdapat dalam semua tumbuhan hijau, mengandung 15 atom karbon dalam inti dasarnya, yang tersusun dalam konfigurasi C6-C3-C6 yaitu dua
Semua jenis flavonoid saling berkaitan karena alur biosintesis yang sama yang memasukkan prazat dari alur sikimat dan alur asetat-malonat. Flavonoid pertama dihasilkan segera setelah kedua alur itu bertemu. Sekarang flavonoidyang dianggap pertama kali terbentuk pada biosintesis adalah kalkon dan semua bentuk lain diturunkan darinya melalui berbagai alur (Markham, 1982).Flavonoid mencakup banyak pigmen yang paling umum dan terdapat dalam seluruh dunia tumbuhan mulai dari fungus sampai angiospermae. Pada tumbuhan tinggi, flavonoid terdapat baik dalam bagian vegetatif maupun dalam bunga. Flavonoid berperan sebagai pengatur fotosintesis, antimikroba dan antivirus (Robinson, 1995).
Flavonoid melindungi tumbuhan dari radiasi sinar UV dan pengaruh lingkungan, flavonoid juga memiliki kandungan antioksidan (Saleem, 2009). Flavonoid memiliki manfaat ekologi yang besar di alam berkat warnanya sebagai penarik serangga dan burung untuk membantu penyerbukan tanaman. Flavonoid tertentu juga mempengaruhi rasa misalnya rasa pahit pada tanaman (Heinrich, 2009).
2.2.2 Triterpenoida dan steroida
Senyawa triterpenoida adalah terpenoid turunan C30 yang terdistribusi
sangat luas, tanaman, fungi, bakteri, karang lunak dan amfibi. Kelompok triterpen meliputi beberapa molekul yang sangat penting yaitu steroid (Heinrich, 2009).
Triterpenoida kebanyakan berupa alkohol, aldehida atau asam karboksilat, berbentuk kristal, mempunyai titik leleh yang tinggi dan optik aktif. Triterpenoida dapat dibagi menjadi sekurang-kurangnya empat golongan yaitu triterpenoida sebenarnya, steroid, saponin, dan glikosida jantung. Uji yang banyak digunakan untuk mendeteksi senyawa ini adalah reaksi Lieberman-Burchard (Harborne, 1987).Steroida merupakan senyawa golongan triterpenoida yang mengandung inti siklopentanoperhidrofenantren yaitu terdiri dari tiga cincin sikloheksana dan sebuah cincin siklopentana (Harborne, 1987).Senyawa triterpenoida ini memiliki aktifitas fisiologi yaitu untuk penyakit diabetes, gangguan menstruasi, gangguan kulit, kerusakan hati dan malaria (Robinson, 1995).
2.2.3 Tanin
peranan sebagai pertahanan bagi tumbuhan untuk mengusir hewan pemakan tumbuhan (Robinson, 1995).
Tanin memiliki kemampuan sebagai antibakteri dengan cara mengganggu fungsi membran sitoplasma yang menyebabkan bocornya metabolit penting yang menginaktifkan sistem enzim bakteri. Sifat tanin yang sebagai pengelat memiliki efek spasmolitik yang menciutkan dinding sel sehingga mengganggupermeabilitas sel sehingga menghambat pertumbuhan (Wonghirundecha dan Punnanee, 2012). 2.2.4 Glikosida
Glikosida adalah istilah generik untuk bahan alam yang secara kimia berikatan dengan gula. Glikosida terdiri atas dua bagian: gula dan aglikon. Aglikon dapat berupa terpen, flavonoid, kumarin atau bahan alam lainnya. Ada dua golongan dasar glikosida: C-glikosida, yaitu gula melekat pada aglikon melalui ikatan karbon-karbon dan O-glikosida yakni yang terhubung pada aglikon melalui ikatan oksigen-karbon. Glikosida biasanya lebih polar daripada aglikonnya dan pembentukan glikosida umumnya meningkatkan kelarutannya dalam air. Hal ini memungkinkan organisme penghasil untuk mentranspor dan menyimpan glikosida secara efektif (Heinrich, 2009).
2.3 Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak larut menggunakan pelarut cair. Senyawa aktif yang terdapat dalam berbagai simplisia dapat digolongkan kedalam golongan minyak atsiri, alkaloida, flavonoida dan lain-lain (Ditjen POM, 2000).
A.Cara Dingin 1. Maserasi
Maserasi adalah proses pengekstrakan simplisia dengan menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur ruangan (kamar). Maserasi kinetik berarti dilakukan pengadukan yang kontinu (terus-menerus). Remaserasi berarti dilakukan pengulangan penambahan pelarut setelah dilakukan penyaringan maserat pertama, dan seterusnya.
2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai penyarian sempurna, umumnya dilakukan di temperatur ruangan. Proses ini terdiri dari tahapan pelembaban bahan, tahap pendiaman antara, dan tahap perkolasi sebenarnya (penetesan/penampungan ekstrak), yang terus menerus sampai ekstrak yang diinginkan habis tersari. Tahap pelembaban bahan dilakukan menggunakan cairan penyari sekurang-kurangnya 3 jam, hal ini penting terutama untuk serbuk yang keras dan bahan yang mudah mengembang.
B.Cara Panas 1. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut yang relatif konstan dengan adanya pendingin balik.
2. Sokletasi
ini adalah sampel erekstraksi dengan sempurna, proses ekstraksi lebih cepat dan pelarut yang digunakan sedikit. Kelemahan dari metode ini adalah sampel yang digunakan harus tahan panas.
3. Digesti
Digesti adalah maserasi kinetik dengan pengadukan kontinu pada temperatur yang lebih tinggi dari temperatur ruangan yaitu secara umum dilakukan pada temperatur 40-50ºC.
4. Infundasi
Infundasi adalah ekstraksi dengan pelarut air pada temperatur penangas air mendidih, temperatur terukur 90ºC selama waktu tertentu (15menit). Kekurangan metode ini sari pada tumbuhan tidak tersari sempurna, untuk kandungan yang tidak tahan panas tidak dapat tersari seluruhnya.
5. Dekoktasi
Dekoktasi adalah ekstraksi dengan pelarut air pada temperatur penangas air mendidih, temperatur terukur 90ºC selama waktu tertentu (30 menit).
2.4 Bakteri
2.4.1 Klasifikasi bakteri
Berdasarkan bentuk morfologinya, maka bakteri dapat dibagi atas tiga golongan yaitu:
a. Golongan basil
Golongan basil berbentuk serupa tongkat pendek, silindris. Basil dapat berbentuk satu batang tunggal disebut basil tunggal, bergandengan dua disebut diplobasil, bergandengan memanjang membentuk rantai disebut streptobasil (Irianto, 2007).
b. Golongan kokus
Golongan kokus merupakan bakteri berbentuk bulat atau bola. Kokus ada yang berbentuk bola tunggal disebut monokokus, berbentuk bola yang bergandeng dua-dua disebut diplokokus, berbentuk bola yang berkelompok empat-empat disebut sarkina dan berbentuk bola yang berkelompok memanjang membentuk rantai disebut streptokokus (Irianto, 2007).
c. Golongan spiral
Golongan spiral merupakan bakteri memiliki satu atau lebih lekukan dan dalam bentuk lurus. Bakteri berbentuk spiral ini dibedakan menjadi beberapa jenis. Bakteri yang berbentuk batang melengkung menyerupai koma disebut vibrio. Bakteri yang berpilin kaku disebut spirilla, sedangkan bakteri yang berpilin fleksibel disebut spirochaeta (Pratiwi, 2008).
a. Bakteri Staphylococcus aureus
Sistematika bakteri Staphylococcus aureus menurut Bergey edisi ke-7 (Dwidjoseputro, 1987) adalah sebagai berikut :
Divisi : Schizophyta Kelas : Schizomycetes Ordo : Eubacteriales Familia : Micrococcaceae Genus : Staphylococcus
Species : Staphylococcus aureus
permukaan kulit tampak sebagai jerawatdan ruam pada kulit berupa yang membuat kulit menjadi kemerahan dan terasa gatal (Hawley, 2003). b. Bakteri Staphylococcus epidermidis
Sistematika bakteri Staphylococcus epidermidis menurut Bergeys edisi ke-7 (Dwidjoseputro, 198ke-7) adalah sebagai berikut:
Divisi : Schizophyta Kelas : Schizomycetes Ordo : Eubacteriales Familia : Micrococcaceae Genus : Staphylococcus
Species : Staphylococcus epidermidis
Staphylococcus epidermidis merupakan sebagian dari flora normal pada kulit manusia, saluran pernafasan dan saluran pencernaan makanan. Bakteri ini juga terdapat di udara dan lingkungan sekitar. Berbentuk bola atau kokus, diameter 0,5 – 0,6 µm. Bakteri ini termasuk gram positif(Dwidjoseputro, 1987). c. Bakteri Streptococcus mutans
Sistematika bakteri Streptococcus mutans (Brook, et al., 2001):
Streptococcus mutans merupakan bakteri gram positif, bersifat nonmotil (tidak bergerak), berdiameter 1 - 2 µm berbentuk bulat atau bulat telur, tersusun dalam bentuk rantaidan tidak membentuk spora.
Genus : Streptococcus
Species :Streptococcus mutans
Streptococcus mutans merupakan bakteri gram positif, bersifat nonmotil (tidak bergerak), berdiameter 1 - 2 µm berbentuk bulat atau bulat telur, tersusun dalam bentuk rantaidan tidak membentuk spora. Bakteri ini tumbuh secara optimal pada suhu sekitar 18 - 40˚C. Streptococcus mutans biasanya ditemukan pada rongga mulut manusia dan menjadi yang paling kondusif menyebabkan bau mulut dan karies untuk email gigi (Pratiwi, 2008).
d. Bakteri Escherichia coli
Sistematika bakteri Escherichia coli menurut Bergey edisi ke-7 (Dwidjoseputro, 1987) adalah sebagai berikut:
Divisi : Schizophyta Kelas : Schizomycetes Ordo : Eubacteriales Familia : Enterobacteriaceae Genus : Escherichia
Species : Escherichia coli
Escherichia coli merupakan bakteri opurtunis yang banyak ditemukan di dalam usus besar manusia sebagai flora normal. Berbentuk batang pendek, merupakan bakteri gram negatif, ukuran 0,4 – 0,7 µm. Bakteri ini tumbuh baik pada suhu 37ºC tetapi dapat tumbuh pada suhu 8-40ºC, membentuk koloni yang bundar, cembung, halus, dan dengan tepi rata (Jawetz, 2001).
pembelahan biner, di mana dari satu sel bakteri dapat dihasilkan dua sel anakan yang sama besar. Interval waktu yang dibutuhkan bagi sel untuk membelah diri dikenal dengan waktu generasi. Waktu yang dibutuhkan untuk meningkatkan jumlah populasi menjadi dua kali lipat dikenal dengan waktu ganda. Berdasarkan perbedaannya dalam menyerap zat warna ram bakteri dibagi dua golongan yaitu bakteri gram positif dan gram negatif. Bakteri gram positif menyerap zat warna pertama yaitu kristal violet yang menyebabkan berwarna ungu (Hardv, 2002).
Ada empat macam fase pertumbuhan mikroorganisme (Pratiwi, 2008): 1. Fase lag
Fase lag merupakan fase adaptasi, yaitu fase penyesuaian mikroorganisme pada suatu lingkungan baru. Ciri fase lag adalah tidak adanya peningkatan jumlah sel, yang ada hanyalah peningkatan ukuran sel. Lama fase lag pada bakteri sangat bervariasi, tergantung pada komposisi media, pH, suhu, aerasi, jumlah sel pada inokulum awal dan sifat fisiologis mikroorganisme pada media sebelumnya
2. Fase log
Fase log merupakan fase di mana mikroorganisme tumbuh dan membelah pada kecepatan maksimum, tergantung pada genetika mikroorganisme. Sel baru yang terbentuk dengan laju konstan dan masa yang bertambah secara eksponensial. Fase ini ditandai dengan terjadinya periode pertumbuhan yang cepat. Variasi pertumbuhan dipengaruhi oleh kadar nutrien dalam media, suhu inkubasi dan pH. 3. Fase stasioner
4. Fase kematian
Jumlah sel yang mati meningkat dikarenakan ketidaktersediaan nutrisi dan akumulasi produk buangan yang toksik. Faktor-faktor yang mempengaruhipertumbuhan mikroorganisme dapat meliputi temperatur, pH, tekanan osmotik, oksigen dan nutrisi dalam media pertumbuhan (Pratiwi, 2008) : 1. Temperatur
Pertumbuhan bakteri sangat dipengaruhi oleh temperatur. Setiap mikroorganisme mempunyai temperatur optimum yaitu temperatur dimana terjadi kecepatan pertumbuhan optimal dan dihasilkan jumlah sel yang maksimal. Temperatur yang terlalu tinggi dapat menyebabkan denaturasi protein sedangkan temperatur yang sangat rendah aktivitas enzim akan terhenti. Berdasarkan batas temperatur dibagi atas tiga golongan:
a. psikofril yaitu mikroorganisme yang suka hidup pada suhu dingin pada temperatur -5 sampai 30ºC dengan optimum 10 sampai 20ºC.
b. mesofil yaitu mikroorganisme yang dapat hidup maksimal pada temperatur 10 sampai 45ºC dengan optimum 20 sampai 40ºC.
c. termofil yaitu mikroorganisme yang tumbuh optimal pada suhu tinggi pada temperatur 25 sampai 80ºC dengan optimum 50 sampai 60ºC (Pratiwi, 2008). 2. Derajat Keasaman
disesuaikanpHnya maka pH ini berubah karena adanya senyawa asam atau basa yang dihasilkan elama pertumbuhan (Pelczar dan Chan, 2006).
3. Oksigen
Berdasarkan kebutuhan oksigen dikenal mikroorganisme dibagi menjadi 5 golongan yaitu:
a. Anaerob obligat, hidup tanpa oksigen, oksigen toksik terhadap golongan ini. b. Anaerob aerotoleran, tidak mati dengan adanya oksigen.
c. Anaerob fakultatif, mampu tumbuh baik dalam suasana dengan atau tanpa oksigen.
d. Aerob obligat, tumbuh subur bila ada oksigen dalam jumlah besar.
e. Mikroaerofilik, hanya tumbuh baik dalam tekanan oksigen yang rendah (Pratiwi, 2008).
4. Tekanan osmosis
Osmosis merupakan perpindahan air melewati membran semipermeabel karena ketidakseimbangan material terlarut dalam media. Medium yang baik untuk pertumbuhan sel adalah medium isotonis terhadap sel tersebut. Dalam larutan hipotonik air akan masuk ke dalam sel sehingga menyebabkan sel membengkak, sedangkan dalam larutan hipertonik air akan keluar dari sel sehingga membran plasma mengerut dan lepas dari dinding sel (plasmolisis). Tekanan osmosis sangat berpengaruh pada pertumbuhan mikroorganisme, jika tekanan osmosis tidak sesuai akan menyebabkan kematian (Pratiwi, 2008).
5. Nutrisi
yaitu makroelemen (elemen yang diperlukan dalam jumlah banyak) dan mikroelemen (elemen nutrisi yang diperlukan dalam jumlah sedikit) (Pratiwi, 2008).
Bahan nutrisi untuk pertumbuhan mikroorganisme terdapat pada media. Media juga dapat digunakan untuk membedakan mikroorganisme dengan mengetahui habitatnya (Pratiwi, 2008). Menurut kegunaannya media terdiri dari: a. Media selektif merupakan media yang digunakan untuk memacu pertumbuhan
suatu mikroba yang spesifik dengan menekan pertumbuhan mikroba lainnya. Dengan menggunakan media ini kita dapat menyeleksi mikroorganisme tertentu.Contoh :
- Saboraut Agardigunakan untuk menumbuhkan jamurkarena mempunyai
pH 5,5 dan mengandung konsentrasi gula yang tinggi.
- Brilian Green Agar digunakan untuk menyeleksi bakteri gram negatif
bentuk batang dari genus Salmonella.
b. Media diferensial digunakan untuk menyeleksi suatu mikroorganisme dari berbagai jenis dalam suatu lempengan (plate) agar.Contoh :
- Media agar darah yang digunakan untuk membedakan mikroorganisme yang mampu menghemolisis darah merah dengan yang tidak mampu, misalnya dapat dilihat pada bakteri patogen spesimen tenggorokan seperti streptococcus pyogenes.
2.4.2 Uji aktifitas antibakteri
Uji kepekaan terhadap obat antimikroba pada dasarnya dapat dilakukan melalui tiga cara yaitu:
Cara ini digunakan untuk menentukan KHM (kadar hambat minimum) dan KBM (kadar bunuh minimum) dari obat antimikroba. Prinsip dari metode dilusi adalah menggunakan satu seri tabung reaksi yang diisi media cair dan sejumlah tertentu sel mikroba yang diuji. Masing-masing tabung diuji dengan obat yang telah diencerkan secara serial. Seri tabung diinkubasi pada suhu 37ºC selama 18-24 jam dan diamati terjadinya kekeruhan pada tabung. Konsentrasi terendah obat pada tabung yang ditunjukkan dengan hasil biakan yang mulai tampak jernih (tidak ada pertumbuhan mikroba) adalah KHM dari obat. Konsentrasi terendah obat pada biakan padat yang ditunjukkan dengan tidak adanya pertumbuhan koloni mikroba adalah KBM dari obat terhadap bakteri uji. Kelemahan metode ini memerlukan waktu yang lama serta biaya yang mahal (Pratiwi, 2008).
b. Metode difusi
Prinsip dari metode difusi adalah sebagai berikut:
obat dijenuhkan ke dalam kertas saring (cakram kertas), cakram kertas yang mengandung obat tertentu ditanam pada media pembenihan agar padat yang telah dicampur dengan mikroba yang diuji, kemudian diinkubasi pada suhu 37ºC selama 18-24 jam. Selanjutnya diamati adanya pertumbuhan mikroba. Kelebihan metode ini bisa melakukan pengujian dalam jumlah banyak. Kekurangan metode ini tidak diketahui secara pasti bakterisid atau bakteriostatik (Brooks, 2001). c. Metode turbidimetri
antibiotik ditentukan berdasarkan perbandingan serapannya terhadap serapan standar (Wattimena, 1991).
BAB I PENDAHULUAN
1.1Latar Belakang
Sejarah penggunaan obat tradisional biasanya berdasarkan pengalaman masyarakat terdahulu yang telah menggunakan obat tradisional secara aman dan berkhasiat (WHO, 2000). Selama ratusan tahun, tradisi diseluruh dunia telah menggunakan herbal untuk mengobati berbagai penyakit dan menjaga kesehatan. Banyak obat yang berasal dari tumbuhan memiliki nilai yang tidak hanya pada kandungan aktif yang dimilikinya tapi juga mineral, vitamin, minyak atsiri, glikosida, alkaloid, asam, alkohol, ester dan lainnya (Majumbar, et al., 2008).
Masyarakat Indonesia telah lama mengenal dan menggunakan tanaman berkhasiat obat, salah satu diantaranya sebagai upaya dalam menanggulangi masalah kesehatan. Pengetahuan tentang tanaman berkhasiat obat berdasarkan pada pengalaman dan keterampilan yang secara turun temurun telah diwariskan dari satu generasi ke generasi berikutnya (Kumala dan Oktora, 2006).
merupakansenyawa metabolit sekunder pada tumbuhan yang bersifat sebagai antibakterimemiliki kemampuan menyamak kulit dan juga dikenal sebagai astringensia (Robinson, 1995).
Kulit kayu dari tanaman ini dapat digunakan sebagai antidiare, biji dapat digunakan sebagai penawar racun gigitan ular, daun dari tumbuhan ini memiliki khasiat sebagai antimikroba, anti-inflamasi, dan astringen (Dahake, et al., 2009). Terutama daun jambu mete juga berkhasiat sebagai antidiare yang disebabkan oleh bakteri Escherichia coli (Jayalakshmi, et al., 2011) disentri dan nyeri usus besar (Vijayakumar dan Kalaichelvan, 2011), ruam kulit yang disebabkan bakteri Staphylococcus aureus (Dalimartha, 2000).Ketika daun dan kulit biji tidak digunakan secara luas untuk tujuan ekonomi maka banyak peneliti yang melakukan penelitian dengan memanfaatkan bagian daun dan kulit biji dari tanaman tersebut untuk meningkatkan nilai ekonomi dari tanaman tersebut (Vijayakumar dan Kalaichelvan, 2011).
1.2Perumusan Masalah
a. golongan senyawa kimia apa saja yang terdapat dalam simplisia, ekstrak etanol, fraksi n-heksan, kloroform dan etilasetat daun jambu mete.
b. apakah ekstrak etanol, fraksi n-heksan, kloroform dan etilasetat mempunyai aktivitas antibakteri terhadap Staphylococcusepidermidis, Streptococcus mutans, Staphylococcus aureus dan Escherichia coli.
1.3Hipotesis
a. golongan senyawa kimia yang terdapat dalam simplisia dan ekstrak etanol bersifat antibakteri yaitu tanin, flavonoida, triterpenoida/steroida dan saponin. Golongan senyawa kimia yang terdapat dalam fraksi n-heksan yaitu metabolit sekunder yang bersifat nonpolar. Golongan senyawa kimia yang terdapat dalam fraksi kloroform yaitu senyawa metabolit sekunder bersifat semipolar. Golongan senyawa kimia yang terdapat pada fraksi etilasetat yaitu metabolit sekunder yang bersifat polar.
b. ekstrak etanol, fraksi n-heksan, kloroform dan etilasetat dari daun jambu mete mempunyai aktivitas antibakteri terhadap bakteri Staphylococcusepidermidis, Streptococcus mutans, Staphylococcus aureus dan Escherichia coli
1.4Tujuan
b. mengetahui aktivitas antibakteri ekstrak etanol, fraksi n-heksan, kloroform dan etilasetat terhadap bakteri Staphylococcusepidermidis, Streptococcus mutans, Staphylococcus aureus dan Escherichia coli.
1.5Manfaat Penelitian
Uji Aktivitas Antibakteri ekstrak Etanol, Fraksi n-heksan, Fraksi Kloroform dan Fraksi Etilasetat daun Jambu Mete (Anacardium occidentale L.)
Abstrak
Masyarakat Indonesia telah lama mengenal dan menggunakan tanaman berkhasiat obat, sebagai upaya dalam menanggulangi masalah kesehatan. Salah satunya daun jambu mete yang biasa dikonsumsi sebagai sayur oleh masyarakat Indonesia. Daun jambu mete mengandung flavonoid dan tanin yang berkhasiat sebagai antibakteri.
Skrining fitokimia serbuk simplisia, ekstrak etanol, fraksi n-heksan, fraksi kloroform dan fraksi etilasetat. Ekstraksi dilakukan dengan cara maserasi menggunakan pelarut alkohol 80% dan dilanjutkan dengan fraksinasi secara berturut-turut menggunakan pelarut n-heksan, kloroform dan etilasetat. Masing-masing ekstrak dan fraksi dilakukan uji aktivitas antibakteri terhadap bakteri Staphylococcus epidermidis, Streptococcus mutans, Staphylococcus aureus dan Escherichia coli dengan metode difusi agar menggunakan silinder logam.
Hasil skrining fitokimia serbuk simplisia dan ekstrak etanol daun jambu mete menunjukkan adanya glikosida, saponin, flavonoida, tanin dan triterpenoida/steroid. Fraksi n-heksan menunjukkan adanya triterpenoida/steroida, fraksi kloroform mengandung senyawa alkaloid, fraksi etilasetat menunjukkan adanya glikosida, saponin, flavonoida dan tanin. Hasil uji aktivitas antibakteri menunjukkan bahwa ekstrak etanol dan fraksi etil asetat memberikan efek terhadap bakteri Staphylococcus epidermidis, Streptococcus mutans, Staphylococcus aureus dan Escherichia coli dengan konsentrasi hambat minimum (KHM) sebesar 10 mg/ml dengan diameter berturut-turut sebesar 11,66 mm; 11,10 mm; 11,13 mm; dan 10,98 mm. Fraksi etilasetat pada konsentrasi 5 mg/ml dengan diameter sebesar 13,33 mm; 13,33 mm; 14,11 mm dan 14,10 mm. Fraksi n-heksan dan kloroform tidak memberikan aktivitas antibakteri.
Antibacterial Activity Of Ethanol Extract, n-Hexane Fraction, Chloroform Fraction and Aethylacetate Fraction Of Cashew Nut Leaves
(Anacardium occidentale L) Abstract
Indonesian society has rocignized and consumed medicinal plants as taking health care. One of them is cashew nut leaves which consumed as vegetable by Indonesian people. It contains flavonoid and tanin which use as antibacterial activity.
The phytochemical screening of simplex powder, extract ethanol, n-hexane fraction, chloroform fraction and aethylacetate fraction. The extration process by maceration method using ethanol as solvent and fractionated with n-hexane, chloroform then aethylacetate. The antibacterial activity for each extract and fractination was measured by means of agar diffusion method using punch hole.
The phytochemical screening result of cashew nut leaves shows the presence of glycoside, saponine, flavonoid, tanin and triterpenopida/steroid. n-hexane fraction presence of triterpenoid/steroid. aethylacetate fraction presence of glycoside, saponine, flavonoid and tanin. Chloroform fraction presence of alkaloid. The result of antibacterial activity examination showed ethanol extract and aethylacetate fraction gave antibacterial activity effect against Staphylococcus epidermidis, Streptococcus mutans, Staphylococcus aureus and Escherichia coli with minimum inhibitory concentration (MIC) were 10 mg/ml and inhibition diameter were consecutively as follows 11.66 mm, 11.10 mm, 11.13 mm and 10.98 mm. For aethylacetate fraction were 5 mg/ml and inhibition diameter were consecutively as follows 13.33 mm, 13.33 mm, 14.11 mm and 14.10 mm. The n-hexane fraction and chloroform fraction has no antibacterial effect.
UJI AKTIVITAS ANTIBAKTERI EKSTRAK ETANOL, FRAKSI
n-HEKSAN, FRAKSI KLOROFORM DAN FRAKSI ETILASETAT
DAUN JAMBU METE
(Anacardium occidentale L.)
SKRIPSI
OLEH:
MELYA LESTARI
NIM 111524009
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
UJI AKTIVITAS ANTIBAKTERI EKSTRAK ETANOL, FRAKSI
n-HEKSAN, FRAKSI KLOROFORM DAN FRAKSI ETILASETAT
DAUN JAMBU METE
(Anacardium occidentale L.)
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara OLEH:
MELYA LESTARI NIM 111524009
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
UJI AKTIVITAS ANTIBAKTERI EKSTRAK ETANOL,
FRAKSI n-HEKSAN, FRAKSI KLOROFORM DAN FRAKSI
ETILASETAT DAUN JAMBU METE
(Anacardium occidentale L.)
OLEH: MELYA LESTARI
NIM 111524009
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sumatera Utara Pada Tanggal: 4 September 2015
Pembimbing I, Panitia Penguji,
Dra. Erly Sitompul, M.Si., Apt. Dra. Aswita Hafni Lubis, M.Si., Apt.
NIP 195006121980032001 NIP 195304031983032001
Pembimbing II, Dr. Erly Sitompul., M.Si., Apt. NIP 195006121980032001
Dr. Marline Nainggolan, M.S.,Apt. Dra. Suwarti Aris, M.Si., Apt. NIP 195709091985112001 NIP 195107231982032001
KATA PENGANTAR
Puji dan syukur kehadirat Allah SWT yang telah melimpahkan rahmat dan karunia-Nya kepada penulis dalam menjalani masa perkuliahan hingga penulis dapat menyelesaikan penelitian dan penulisan skripsi ini dengan baik. Judul skripsi ini adalah “Uji Aktivitas Antibakteri Ekstrak Etanol, Fraksi n-heksan, Fraksi Kloroform dan Fraksi Etilasetat daun Jambu Mete (Anacardium occidentale L)”. Skripsi ini merupakan salah satu persyaratan yang harus dipenuhi dan dilaksanakan untuk memperoleh gelar Sarjana Farmasi di fakultas Farmasi Universitas Sumatera Utara.
kritikan kepada penulis hingga selesainya penulisan skripsi ini. Bapak dan Ibu staf pengajar Fakultas Farmasi USU yang telah membina dan mendidik penulis selama menuntut ilmu di Fakultas Farmasi.
Penulis juga mengucapkan terima kasih yang tiada terhingga kepada Ayahanda dan Ibunda tercinta, Selamet dan Sri Ana, serta adik Septian Aditya atas doa, dorongan dan pengorbanan baik moril maupun materil selama menempuh pendidikan Strata 1 Farmasi.
Penulis menyadari bahwa tulisan ini masih memiliki banyak kekurangan, oleh karena itu dengan segala kerendahan hati penulis bersedia menerima kritikan dan saran yang membangun pada skripsi ini. Semoga skripsi ini bermanfaat bagi kita semua.
Medan, September 2015 Penulis
Uji Aktivitas Antibakteri ekstrak Etanol, Fraksi n-heksan, Fraksi Kloroform dan Fraksi Etilasetat daun Jambu Mete (Anacardium occidentale L.)
Abstrak
Masyarakat Indonesia telah lama mengenal dan menggunakan tanaman berkhasiat obat, sebagai upaya dalam menanggulangi masalah kesehatan. Salah satunya daun jambu mete yang biasa dikonsumsi sebagai sayur oleh masyarakat Indonesia. Daun jambu mete mengandung flavonoid dan tanin yang berkhasiat sebagai antibakteri.
Skrining fitokimia serbuk simplisia, ekstrak etanol, fraksi n-heksan, fraksi kloroform dan fraksi etilasetat. Ekstraksi dilakukan dengan cara maserasi menggunakan pelarut alkohol 80% dan dilanjutkan dengan fraksinasi secara berturut-turut menggunakan pelarut n-heksan, kloroform dan etilasetat. Masing-masing ekstrak dan fraksi dilakukan uji aktivitas antibakteri terhadap bakteri Staphylococcus epidermidis, Streptococcus mutans, Staphylococcus aureus dan Escherichia coli dengan metode difusi agar menggunakan silinder logam.
Hasil skrining fitokimia serbuk simplisia dan ekstrak etanol daun jambu mete menunjukkan adanya glikosida, saponin, flavonoida, tanin dan triterpenoida/steroid. Fraksi n-heksan menunjukkan adanya triterpenoida/steroida, fraksi kloroform mengandung senyawa alkaloid, fraksi etilasetat menunjukkan adanya glikosida, saponin, flavonoida dan tanin. Hasil uji aktivitas antibakteri menunjukkan bahwa ekstrak etanol dan fraksi etil asetat memberikan efek terhadap bakteri Staphylococcus epidermidis, Streptococcus mutans, Staphylococcus aureus dan Escherichia coli dengan konsentrasi hambat minimum (KHM) sebesar 10 mg/ml dengan diameter berturut-turut sebesar 11,66 mm; 11,10 mm; 11,13 mm; dan 10,98 mm. Fraksi etilasetat pada konsentrasi 5 mg/ml dengan diameter sebesar 13,33 mm; 13,33 mm; 14,11 mm dan 14,10 mm. Fraksi n-heksan dan kloroform tidak memberikan aktivitas antibakteri.
Antibacterial Activity Of Ethanol Extract, n-Hexane Fraction, Chloroform Fraction and Aethylacetate Fraction Of Cashew Nut Leaves
(Anacardium occidentale L) Abstract
Indonesian society has rocignized and consumed medicinal plants as taking health care. One of them is cashew nut leaves which consumed as vegetable by Indonesian people. It contains flavonoid and tanin which use as antibacterial activity.
The phytochemical screening of simplex powder, extract ethanol, n-hexane fraction, chloroform fraction and aethylacetate fraction. The extration process by maceration method using ethanol as solvent and fractionated with n-hexane, chloroform then aethylacetate. The antibacterial activity for each extract and fractination was measured by means of agar diffusion method using punch hole.
The phytochemical screening result of cashew nut leaves shows the presence of glycoside, saponine, flavonoid, tanin and triterpenopida/steroid. n-hexane fraction presence of triterpenoid/steroid. aethylacetate fraction presence of glycoside, saponine, flavonoid and tanin. Chloroform fraction presence of alkaloid. The result of antibacterial activity examination showed ethanol extract and aethylacetate fraction gave antibacterial activity effect against Staphylococcus epidermidis, Streptococcus mutans, Staphylococcus aureus and Escherichia coli with minimum inhibitory concentration (MIC) were 10 mg/ml and inhibition diameter were consecutively as follows 11.66 mm, 11.10 mm, 11.13 mm and 10.98 mm. For aethylacetate fraction were 5 mg/ml and inhibition diameter were consecutively as follows 13.33 mm, 13.33 mm, 14.11 mm and 14.10 mm. The n-hexane fraction and chloroform fraction has no antibacterial effect.
DAFTAR ISI
2.2.2 Triterpenoida/steroida ... 9
3.3 Pengumpulan Bahan Tumbuhan ... 24
3.4.6 Pereaksi Liebermann-burchard ... 25
3.4.7 Pereaksi Mayer ... 25
3.5.6 Pemeriksaan steroida/triterpenoida ... 28
3.5.7 Pemeriksaan saponin ... 28
3.6 Pembuatan Ekstrak Etanol Daun Jambu Mete (Anacardium occidentale) ... 28
3.7 Pembuatan Fraksi n-Heksan, Kloroform Dan Etilasetat Daun Jambu Mete (Anacardium occidentale) ... 29
3.8 Sterilisasi Alat ... 29
3.14 Uji Aktivitas Antibakteri Ekstrak Etanol, Fraksin-Heksan, Kloroform DanEtilasetat Daun Jambu Mete (Anacardium
occidentale) ... 32
BAB IV HASIL DAN PEMBAHASAN ... 33
4.1 Identifikasi Tumbuhan ... 33
4.2 Hasil skrining Fitokimia ... 33
4.3 Hasil Uji Aktivitas Antibakteri Ekstrak Etanol, Fraksin-Heksan, Kloroform Dan Etilasetat Terhadap Streptococcus epidermidis, Streptococcus mutans, Staphylococcus aureus dan Escherichia coli ... 34
BAB V KESIMPULAN DAN SARAN ... 39
5.1 Kesimpulan ... 39
5.2 Saran ... 39
DAFTAR PUSTAKA ... 40
DAFTAR TABEL
Tabel Halaman
4.1 Hasil skrining fitokimia ekstrak etanol, fraksi n-heksan, fraksikloroform dan fraksi etilasetat ... 33 4.2 Hasil pengukuran diameter daerah hambatan pertumbuhan
Streptococcus epidermidis, Streptococcus mutans, Staphylococcus aureus dan Escherichia coli dari ekstrak etanol
daun jambu mete ... 35 4.3 Hasil pengukuran diameter daerah hambatan pertumbuhan
DAFTAR LAMPIRAN
Lampiran Halaman
1. Identifikasi Tumbuhan ... 43 2. Gambar tumbuhan jambu mete (Anacardium occidentale) . 44 3. Gambar daun segar dan simplisia dari daun jambu
mete(Anacardium occidentale) ... 45 4. Bagan pembuatan ekstrak dan fraksinasi ... 46 5. Bagan pengujian aktivitas antibakteri ... 47 6. Hasil pengukuran diameter daerah hambat ekstrak etanol
daun jambu mete terhadap pertumbuhan bakteri
Staphylococcus epidermidis ... 48 7. Hasil pengukuran diameter daerah hambat ekstrak etanol
daun jambu mete terhadap pertumbuhan bakteri
Streptococcus mutans ... 59 8. Hasil pengukuran diameter daerah hambat ekstrak etanol
daun jambu mete terhadap pertumbuhan bakteri
Staphylococcus aureus ... 50
9. Hasil pengukuran diameter daerah hambat ekstrak etanol daun jambu mete terhadap pertumbuhan bakteri
Escherichia coli ... 51
10. Hasil pengukuran diameter daerah hambat fraksi etilasetat daun jambu mete daun jambu mete terhadap pertumbuhan
bakteri Staphylococcus epidermidis ... 52
11. Hasil pengukuran diameter daerah hambat fraksi etilasetat daun jambu mete daun jambu mete terhadap pertumbuhan
bakteri Streptococcus mutans ... 53
12. Hasil pengukuran diameter daerah hambat fraksi etilasetat daun jambu mete daun jambu mete terhadap pertumbuhan
bakteri Staphylococcus aureus ... 54
13. Hasil pengukuran diameter daerah hambat fraksi etilasetat daun jambu mete daun jambu mete terhadap pertumbuhan
14. Hasil uji aktivitas antibakteri ekstrak etanol daun jambu
mete terhadap bakteri Staphylococcus epidermidis ... 56
15 Hasil uji aktivitas antibakteri ekstrak etanol daun jambu
mete terhadap bakteri Streptococcus mutans ... 57 16. Hasil uji aktivitas antibakteri ekstrak etanol daun jambu
mete terhadap bakteri Staphylococcus aureus ... 58 17. Hasil uji aktivitas antibakteri ekstrak etanol daun jambu
mete terhadap bakteri Escherichia coli ... 59
18. Hasil uji aktivitas antibakteri fraksi n-heksan daun jambu
mete terhadap bakteri Staphylococcus epidermidis ... 60
19. Hasil uji aktivitas antibakteri fraksi n-heksan daun jambu
mete terhadap bakteri Streptococcus mutans ... 61
20. Hasil uji aktivitas antibakteri fraksi n-heksan daun jambu
mete terhadap bakteri Staphylococcus aureus ... 62
21. Hasil uji aktivitas antibakteri fraksi n-heksan daun jambu
mete terhadap bakteri Escherichia coli ... 63
22. Hasil uji aktivitas antibakteri fraksi kloroform daun jambu
mete terhadap bakteri Staphylococcus epidermidis ... 64
23. Hasil uji aktivitas antibakteri fraksi kloroform daun jambu
mete terhadap bakteri Streptococcus mutans ... 65
24. Hasil uji aktivitas antibakteri fraksi kloroform daun jambu
mete terhadap bakteri Staphylococcus aureus ... 66
25. Hasil uji aktivitas antibakteri fraksi kloroform daun jambu
mete terhadap bakteri Escherichia coli ... 67
26. Hasil uji aktivitas antibakteri fraksi etilasetat daun jambu
mete terhadap bakteri Staphylococcus epidermidis ... 68
27. Hasil uji aktivitas antibakteri fraksi etilasetat daun jambu
28. Hasil uji aktivitas antibakteri fraksi etilasetat daun jambu
mete terhadap bakteri Staphylococcus aureus ... 70
29. Hasil uji aktivitas antibakteri fraksi etilasetat daun jambu