Dihaluskan dengan menggunakan Blender
Diperas menggunakan kain blacu berwarna putih
Direndam selama lebih kurang 24 jam Filtrat dibuang
Dilakukan pencucian berulang-ulang
Dikeringkan dibawah matahari Masa lembab dikeringkan di lemari
pengering pada suhu 40oC - 42oC selama lebih kurang 24 jam
5 Kg biji jagung
Residu Filtrat
Pati putih
Lampiran 2. Flowsheet pembuatan pati jagung pragelatinasi
Dibuat suspensi pati jagung dalam air 16,6% b/v Dipanaskan pada suhu 60oC sampai mengental Dituang di atas porselin lalu dikeringkan pada
suhu 60oC selama 3 jam
Pati kering dipecah-pecah dan diblender menggunakan blender tepung
Hasilnya ditimbang
Dibasahkan dengan mucilago amili 10% sampai memperoleh massa yang kompak
Dikeringkan dilemari pengering pada suhu 40oC - 60oC selama lebih kurang 3 jam
Diayak dengan ayakan mesh 20, 60 dan 100
Digunakan sebagai Bahan pengisi
Laktosa
Laktosa kering
Mesh 20 Mesh 60 Mesh 100
Granul
Lampiran 4. Contoh perhitungan pembuatan tablet Vitamin C
Sebagai contoh diambil tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 50% (formula F6)
Berat 100 tablet = 100 x 0,3 g = 30 g Berat Vitamin C dalam tablet = 100 x 0,12 g = 12 g
Amilim manihot 5% = 5% x 30 g = 1,5 g
Mg Stearat = 1% x 30 g = 0,3 g
Talkum = 1% x 30 g = 0,3 g
Pengisi = 30 g – ( 12 g + 1,5 g + 0,3 g + 0,3 g ) - Pati jagung pragelatinasi 50 % = 50 % x 15,9 g = 7,95 g
a) Tabel data hasil uji waktu alir
b) Tabel data hasil uji sudut diam
Lampiran 5. (lanjutan)
c) Tabel data hasil uji indeks tap
FORMULA
Indeks Tap ( % )
V1 ( ml ) V2 ( ml ) I ( % )
F1 33 27 18,18
F2 35 29 17,14
F3 36 30 16,67
F4 37 32 13,51
F5 41 35 14,63
F6 44 36 18,18
F7 45 38 15,55
Contoh perhitungan Indeks Tap Rumus : I = x 100% Keterangan :
I = Indeks Tap (%)
V1 = Volume sebelum hentakan ( ml ) V2 = Volume setelah hentakan ( ml )
Syarat : Granul akan mempunyai sifat alir yang baik jika mempunyai I ≤ 20% Sebagai contoh diambil tablet Vitamin C formula F6 (50%)
Volume sebelum hentakan ( V1 ) = 44 ml Volume setelah hentakan ( V2 ) = 36 ml Indeks Tap = x 100% =
44 36 44−
a) Tabel data hasil uji kekerasan tablet Vitamin C
Tablet
Kekerasan ( Kg )
F1 F2 F3 F4 F5 F6 F7
1 4,0 4,2 5,5 4,9 5,2 4,2 4,4
2 4,2 4,3 5,7 4,5 5,5 4,6 4,6
3 4,1 4,3 5,5 4,8 5,3 4,5 4,5
4 4,2 4,4 5,8 4,9 5,5 4,6 4,6
5 4,0 4,1 5,8 4,7 5,3 4,4 4,4
6 4,1 4,3 5,7 4,8 5,4 4,5 4,5
Rata – rata 4,1 4,2 5,6 4,7 5,3 4,4 4,5
b) Tabel data hasil uji waktu hancur
Formula Tablet Waktu Hancur (menit)
FI
1 06,17
2 06,20
3 06,55
4 07,45
5 08,15
6 08,30
Rata-rata 07,14
F2
1 06,20
2 06,56
3 07,25
4 08,33
5 08,42
6 08,56
Lampiran 6. (lanjutan)
F3
1 08,10
2 08,35
3 08,45
4 09,11
5 09,25
6 09,43
Rata-rata 09,19
F4
1 06,45
2 07,37
3 07,48
4 08,23
5 09,15
6 09,50
Rata-rata 08,03
F5
1 07,21
2 07,32
3 08,20
4 08,53
5 09,20
6 09,43
F6
1 07,15
2 07,36
3 07,50
4 08,13
5 08,58
6 09,14
Rata-rata 08,38
F7
1 07,10
2 07,32
3 07,51
4 08,30
5 08,36
6 08,47
Rata-rata 08,25
c) Tabel data hasil uji friabilitas
Formula Berat 20 tablet Friabilitas (%)
Awal (gr) Akhir (gr)
F1 8,6236 8,5836 0,46
F2 8,3928 8,3498 0,51
F3 8,8245 8,7645 0,67
F4 8,5471 8,4941 0,62
F5 8,7821 8,7241 0,66
F6 8,5829 8,5369 0,53
Lampiran 6. (lanjutan)
Contoh Perhitungan Friabilitas Tablet Vitamin C Rumus : F = (a-b)/a x 100%
Keterangan : F = Friabilitas
a = Bobot tablet sebelum diputar dalam alat Friabilitas Tester selama 4 menit (100 putaran)
b = Bobot tablet setelah diputar dalam alat Friabilitas Tester selama 4 menit (100 putaran)
Syarat friabilitas tablet : Kehilangan bobot tidak boleh lebih dari 0,8 % (x ≤ 0,8%), sebagai contoh diambil tablet formula F6
Lampiran 8. Kurva kalibrasi Vitamin C pada panjang gelombang
C (μg/ml) Dengan nilai r sebagai berikut :
Lampiran 9. Perhitungan kadar tablet Vitamin C
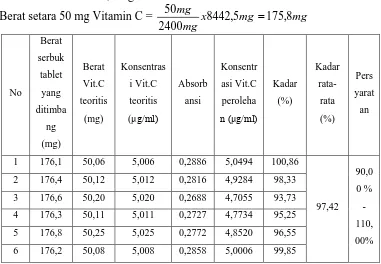
Misalnya untuk formula F7 ( 40 % ) Berat 20 tablet = 8442,5 mg
Berat Vitamin C dalam 20 tablet = 20 x 50 mg = 2400 mg
Berat setara 50 mg Vitamin C = 50 mg / 2400 mg x 8442,5 mg = 175,8 mg Berat serbuk yang ditimbang = 176,1 mg
Berat Vitamin C di dalam serbuk tablet secara teoritis = (176,1 mg) / 8442,5 mg x 2400 = 50,06 mg
Dilarutkan sampai 100 ml, dipipet 10 ml diencerkan dalam labu tentukur sampai 100 ml, kemudian di pipet 5 ml diencerkan di dalam labu tentukur sampai 50 ml maka konsentrasi Vitamin C teoritis didalam larutan sampel = (50,06 x 1000 μg) / (100 ml) x (10 ml) / (100 ml) x (5 ml) / (50 ml = 5,006μg/ml
Diukur absorbansi nya diperoleh : a = 0,2886
Persamaan regresi yang diperoleh dari kurva kalibrasi
Lampiran 10. (lanjutan)
t hitung data 5 =
[ ]
6 744 , 287 , 0
= 0,1294
t hitung data 6 =
[ ]
6 744 , 243 , 2
= 0,3616
Semua data diterima
Jadi kadar sebenarnya terletak antara : μ = ± t(1-1/2α)dk x
: 97,42 ± 4,032 6 744 , 2
: 97,42 ± 4,5167
Lampiran 12. Perhitungan keseragaman kandungan tablet Vitamin C
Misalnya untuk formula F6 (50%)
Timbang 10 tablet satu per satu masing-masing berat tablet :
1.399,1 6.383,0
2.377,2 7.365,3
3.364,8 8.363,8
4.374,5 9.369,7
5.384,5 10.357,4
Berat Vitamin C dalam 1 tablet 120 mg. Misal pada tablet 1 dengan berat 399,1 mg -Pengujian I
Satu tablet digerus dan dilakukan pengujian seperti pada penetapan kadar, Maka diperoleh serapan ( Y ) = 0,2863
Konsentrasi natrium diklofenak dapat dihitung dengan memasukkan nilai absorbansi ke persamaan regresi berikut :
Y = 0,05755x + (-0,002)
Diketahui konsentrasi teoritisnya = 5,000 μg/ml Maka kadar natrium diklofenak =
- Pengujian III
Kadar Vitamin C = 100,65% - Pengujian IV
Kadar Vitamin C = 99,79% - Pengujian V
Kadar Vitamin C = 99,54% - Pengujian VI
Kadar Vitamin C = 100,98 % -Pengujian VII
Kadar Vitamin C = 99,97% -Pengujian VIII
Kadar Vitamin C = 100,73% -Pengujian I X
Kadar Vitamin C = 99,69% -Pengujian X
Kadar Vitamin C = 99,36%
Rata–rata hasil penetapan kadar = 100,13% x 120 mg
SD =
=
1 10
7468 , 2
−
= 0,55
RSD = x 100%
= 13 , 100
552 , 0
Data hasil uji keseragaman kandungan
Formula
Kadar rata – rata ( % )
Simpangan Baku (SD)
RSD
Persyaratan (%)
F 1 89,52 1,260 1,40 85,0 – 115,0
F 2 93,79 0,853 0,90 85,0 – 115,0
F 3 113,64 0,583 0,51 85,0 – 115,0
F 4 109,11 2,158 1,97 85,0 – 115,0
F 5 103,64 1,477 1,43 85,0 – 115,0
F 6 100,13 0,552 0,55 85,0 – 115,0
Lampiran 14. Perhitungan disolusi tablet Vitamin C
Misalnya pada formula F5 (60%) -Pengujian I
1. Konsentrasi (C)
Dengan persamaan regresi Y = 0,05755 X + (-0,002) X = Konsentrasi
Y = Absorbansi
Pada t = 1 menit, Y = 0,1041 0,4559 = 0,05755 X + (-0,002) X = 8,0674 μg/ml
2. Faktor Pengenceran
Fp = (pengenceran dalam labu 25 ml) / jumlah pemipetan aliquot = 25 / 5
Fp = 5
3. Konsentrasi dalam 1 ml (Cp x Fp) Contoh pada t = 5 menit
C = 8,0674 mcg/ml x 5 = 40,337 mcg/ml 4. konsentrasi dalam 900ml
C dalam 900ml = Cdalam 1ml x 900 Contoh pada t = 5 menit
C (1’) = 40,337 mcg/ml x 900 ml = 36303,3 mcg/900 ml 5. Faktor Penambahan
6. Vitamin C yang terlepas
Vitamin C yang terlepas = C dalam 900ml + faktor penambahan Contoh pada t = 5 menit
Vitamin C yang terlepas = 36303,3 mcg + 0 = 36303,3 mcg = 36,3033 mg 7. Persen Kumulatif
% kumulatif = 100%
120
terlepas yang
C Vitamin
x mg
Dosis Vitamin C = 120 mg Contoh pada t = 5 menit % kumulatif =
mg mg 120
3033 , 36
x 100%
Lampiran 16. Gambar alat yang digunakan
Alat Uji Kekerasan (Copley) Alat Uji Waktu Hancur (Copley)
Mesin Pencetak Tablet (Erweke) Alat Flowmeter (Copley)
Mikroskopik Pati Jagung Pragelatinasi Mikroskopik Pati Jagung Alami
Lampiran 19. Gambar tablet Vitamin C menggunakan pati jagung
Lampiran 19. (lanjutan)
Abu-izza., Khawla, A.L., Vincent, H.L., Jee, L.P., Graham D.S., dan Matthew, K. (2009). Fast Dissolving Tablet. Dalam: Bhupendra G Prajapati and Nayan Ratnakar. A Review On Recent Patents On Fast Dissolving Drug Delivery System. International Journal of PharmTech Research. 1(3): 790-798.
Ansel, H.C. (1989). Pengantar Bentuk Sediaan Farmasi. Edisi IV. Jakarta: UI Press. Halaman 154-155,244.
Andarwulan, N., dan Koswara, S. (1989). Kimia Vitamin. Jakarta: Rajawali Press. Halaman 23-44.
Ayu, K.M., Arisanti, S., dan Indra, E.S. (2012). Pengaruh Konsentrasi Amilum Jagung Pregelatinasi Sebagai Bahan Penghancur Terhadap Sifat Fisik Tablet Vitamin E pada Anjing. Jurnal Farmasi Udayana. Diunduh dari
Diakses 18 juli 2014.
Cartensen, J.T. (1977). Pharmaceutical of Solid Dosage Forms. New York: A Wiley Interscience Publication John Wiley and Son. Halaman. 133-135, 209, 216-218, 342.
Charles, J.P. (2010). Teknologi Farmasi Sediaan Tablet Dasar-dasar Praktis. Jakarta: Penerbit Buku Kedokteran EGC. Halaman 236.
Dachriyanus. (2004). Analisis Struktur Senyawa Organik Secara Spektroskopi. Cetakan Pertama. Padang: Andalas University Press. Halaman 3.
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Direktorat Jendral Pengawasan Obat dan Makanan Departemen Kesehatan RI. Halaman 4, 108, 649-650, 925, 1000, 1043, 1085, 1124.
Fahn, J. (1992). Teknologi Pengolahan Jagung Untuk Menunjang Agroindustri Pedesaan. Makalah Simposium Penelitian Tanaman Pangan III. Jakarta/Bogor. 23-25 Agustus 1993. Puslitbangtan. Bogor.
Glicksman, M. 1969. Gum Technology in The Food Industry. Academic Press, New York. Halaman 145.
Hartono, S. (2007). Modifiksi Pati Jagung (Zea mays L). Cetakan Pertama. Bogor: Institut Pertanian Bogor Press. Halaman 79,80.
Lachman, L., Lieberman, H.A., dan Kaning J.L. (1994). Teori dan Praktek Farmasi Industri. Edisi Ketiga. Jakarta: UI Press. Halaman 654, 697. Mandasari, L., Dalimunthe, A., dan Tanuwijaya, T. (2012). Studi Pembuatan
Tablet Isoniazida Menggunakan Kombinasi Granul Pati Jagung (Amylum Myadis) dan Granul Laktosa Sebagai Bahan Pengisi Secara Cetak Langsung. Skripsi. Medan: Fakultas Farmasi Universitas Sumatera utara. Halaman 41.
Moffat, C.A., Osselton, M.D., dan Widdop, B. (2005). Clarke’s Analysis of Drugs and Poisons. London: Pharmaceutical Press. Halaman. 1208. Parrot, E.L. (1971). Pharmaceutical Technology Fundamental Pharmaceutical.
United States of America: Burgess Publishing Company. Halaman 82-83.
Sharma, R., Rajput, M., Prakash, P., dan Sharma, S. (2011). Fast Disolving5Delivery Sytem On review. International Journal of Pharmacy. 2(10): 21-29.
Sheth, B.B., Bandelin, F.J., dan Shangraw, R.F. (1980). Compressed Tablets in Pharmaceutical Dosage Farm: Tablet. Volume I. New York: Marcel Decker Inc. Halaman 89-93.
Suarni., dan Sarsutha, I.G.P. (2002). Teknologi Pengolahan Jagung untuk Meningkatkan Nilai Tambah dalam Pengembangan Agro Industri. Prosiding Seminar Nasional, BPTP Sulawesi Tengah. Halaman 1-5. Sudarmadji. (1989). Prosedur Analisa untuk Bahan Makanan dan Pertanian.
Yogyakarta: Liberty Press. Halaman 24.
United States Pharmacopeia Convention. 2007. United StatesPharmacopoeia
National Formulary, USP 30/NF 25. Twinbrook Parkway: United
States Pharmacopeial Convention. Halaman. 1922.
United States Pharmacopeia. Edisi XXI. The National Formulary.Edisi XVI. (1985). United States Pharmacopeia Convention Inc. Twinbrook Parkway Rockville.
BAB III
METODE PENELITIAN
3.1 Alat
Alat yang digunakan dalam penelitian ini adalah neraca listrik (Dj- Series), timbangan dan anak timbangan, thermometer, stopwatch, mortar dan stamfer, lemari pengering, viscometer, alat sudut diam, alat uji waktu alir, pencetak tablet Single Punch, Strong Cobb Hardness Tester, Disintegration Tester, Disolution Tester, ayakan dan alat-alat gelas laboratorium.
3.2 Bahan
Bahan- bahan yang digunakan dalam penelitian ini adalah Vitamin C pati jagung pragelatinasi, Mg stearat, air suling, talkum, laktosa, dan amilum manihot.
3.3 Pati Jagung
3.3.1 Pengambilan sampel
Pengambilan sampel dilakukan dengan cara purposif, yaitu tanpa membandingkan dengan daerah lain. Umur sampel yang diambil yang sudah tua tetapi sebelum kulitnya mengering dan biji pada tongkolnya sudah penuh. Sampel yang digunakan adalah jagung yang diambil dari Pasar Tradisional, Sei Kambing, Sumatera Utara.
3.3.2 Prosedur isolasi pati jagung
cairan atas dibuang dan dilakukan pencucian dengan cara menambahkan air suling secara berulang-ulang sampai diperoleh pati yang putih. Pati yang diperoleh selanjutnya dikeringkan dibawah sinar matahari. Massa lembab dikeringkan di lemari pengering pada suhu 40oC - 60oC selama lebih kurang 24 jam.
3.3.3 Pembuatan pati jagung pragelatinasi
Dibuat suspensi pati jagung dalam air dengan konsentrasi 16,6 % b/v lalu dipanaskan di atas penangas air aduk perlahan-lahan agar amilum terdispersi merata. Suhu dibiarkan naik perlahan-lahan hingga 60°C kemudian didinginkan dengan cara direndam dengan air dingin. Suspensi setelah mencapai suhu kamar disaring dengan penyaring kemudian dikeringkan dalam lemari pengering dengan suhu 60°C selama satu malam maka akan terbentuk slug (lembaran padatan) dari amilum pragelatinasi kemudian dipecah-pecah diayak dengan ayakan mesh 20 (Ayu, dkk., 2012).
3.3.4 Pati jagung pragelatinasi mesh 20
Pati jagung pragelatinasi yang telah dikeringkan diayak dengan ayakan mesh 20, 60, dan 100 dan dicatat berapa berat dari masing-masing ukuran partikel yang dihasilkan. Pati jagung pragelatinasi dengan ayakan mesh 20 digunakan sebagai bahan pengisi pada pembuatan tablet secara cetak langsung.
3.3.5 Prosedur pembuatan granul laktosa
selama lebih kurang 3 jam. Laktosa yang telah dikeringkan lalu di ayak dengan ayakan mesh 20, 60, dan 100. Granul laktosa dengan ayakan mesh 20 digunakan sebagai bahan pengisi pada pembuatan tablet secara cetak langsung.
3.3.6 Pemeriksaan karakteristik pati jagung pragelatinasi
a. Mikroskopik
Pati diletakkan di atas objek glass ditambah aquades, lalu ditutup dengan dec glass. Lihat di bawah mikroskop dengan perbesaran 10 x 40.
b. Uji komprimabilitas
Uji komprimabilitas dilakukan pada mesin tablet single punch (Ateliers) dengan cara mencetak tablet hanya dengan granul pati jagung secara manual pada skala tinggi die yang berbeda dan dengan meningkatkan skala kompressi sehingga menghasilkan tablet dengan kekerasan tertinggi.
3.4 Pembuatan Tablet
Tablet dibuat dengan metode secara cetak langsung, dimana zat aktif (Vitamin C) ditambahkan amilum manihot, talkum, dan mg stearat. Lalu pati jagung pragelatinasi dan granul laktosa mesh 20 ditambahkan sebagai pengisi dicampur sampai homogen. Kemudian dilakukan uji preformulasi dan dicetak. Uji preformulasi yang dilakukan meliputi sudut diam, waktu alir, dan indeks tap.
Formula: R/ Vitamin C 120 mg Amilum manihot 5%
Pati jagung pragelatinasi (% bervariasi) Granul Laktosa ad q.s (% bervariasi) m.f. tab. dtd. No
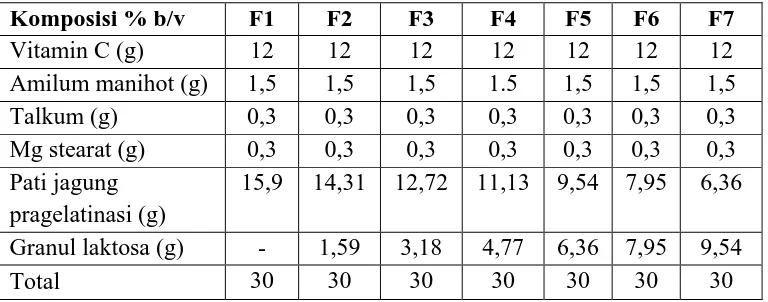
Tabel 3.1 Formula Tablet Vitamin C
Komposisi % b/v F1 F2 F3 F4 F5 F6 F7
F1 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinsi 100%
F2 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 90% dan granul laktosa 10%
F3 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 80% dan granul laktosa 20%
F4 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 70% dan granul laktosa 30%
F5 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 60% dan granul laktosa 40%
F6 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 50% dan granul laktosa 50%
F7 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 40% dan granul laktosa 60%
3.5 Uji Preformulasi 3.5.1 Sudut diam
biarkan granul mengalir sampai habis. Tinggi kerucut yang terbentuk diukur. Sudut diam diukur dengan rumus:
tg€= 2h/ D
Keterangan : θ = sudut diam D = diameter
H = tinggi kerucut (cm)
Persyaratan: Uji dikatakan memenuhi syarat apabila berada pada 200 < θ < 400 (Cartensen, 1977).
3.5.2 Waktu alir
Uji waktu alir dilakukan menurut metode yang dibuat oleh Cartensen (1977). Granul sebanyak 100 gram dimasukkan kedalam corong yang telah dirangkai, kemudian permukaannya diratakan. Penutup bawah corong dibuka dan secara serentak stopwatch dihidupkan. Stopwatch dihentikan saat granul telah habis melewati corong dan dicatat waktu alirnya. Menurut Guyot (1978), waktu alir yang diperlukan oleh sejumlah serbuk untuk mengalir harus lebih singkat dari 10 detik.
3.5.3 Indeks tap
Kedalam gelas ukur 100 ml, dimasukkan sejumlah granul hingga 100 ml. Ditap dengan alat yang dimodifikasi sampai konstan. Setelah hentakan, volumenya dihitung dengan rumus:
I= V1-V2 / V1 x 100%
Granul akan mempunyai sifat alir yang baik jika mempunyai indeks tap ≤ 20%.
3.6 Evaluasi Tablet 3.6.1 Uji kekerasan tablet
Alat: Hardness Tester (Copley)
Cara: Diambil 6 tablet, masing-masing diletakkan pada tempat yang tersedia pada alat dengan posisi tidur, alat diatur, kemudian ditekan tombol start. Pada saat tablet pecah angka yang tertera pada layar digital dicatat. (Abu-Izza, et al., 2004).
3.6.2 Uji Waktu Hancur
Alat: Desintegration Tester (Copley)
Cara: Dimasukkan 6 tablet pada masing-masing tabung di keranjang, lalu letakkan 6 tablet dengan cakram penuntun di atasnya dan dijalankan alat. Dicelupkan pada air dengan suhu 370C (±10C) dengan tinggi air tidak boleh kurang dari 15 cm, sehingga tabung dapat dinaik turunkan secara teratur 30 kali permenit. Pada kedudukan tertinggi, kawat kasa tepat pada permukaan air, Angkat keranjang dan amati seluruh tablet. Tablet dinyatakan hancur jika tidak ada lagi tablet yang tertinggal pada kawat kasa dan dicatat waktu setiap tablet hancur. Bila 1 tablet atau 2 tablet tidak hancur sempurna, ulangi pengujian dengan 12 tablet lainnya, tidak kurang 16 dari 18 tablet yang diuji harus hancur sempurna (Ditjen POM 1945).
3.6.3 Uji friabilitas
Alat: Friabilator (Copley)
4 menit (100 kali putaran). Setelah batas waktu yang ditentukan tablet dikeluarkan dan dibersihkan dari debu, lalu ditimbang beratnya (b gram). Friabilitas (F) = (a – b)/a x 100%.
Ketentuan umum : Kehilangan berat ≤ 0,8% (Sharma, et al., 2011).
3.6.4 Uji keseragaman kandungan
Tablet yang dibuat yaitu tablet Vitamin C dengan berat satu tablet 300 mg dan mengandung Vitamin C 120 mg, berarti bobot zat berkhasiat lebih kecil dari 50% bobot sediaan karena itu penetapan keseragaman sediaan dilakukan dengan menetapkan keseragaman kandungan (Ditjen POM, 1995) yang dilakukan sebagai berikut :
Diambil setiap formula yang dibuat, diuji homogenitas dengan mengambil secara acak 10 tablet, dan masing-masing tablet Vitamin C tersebut digerus dan ditimbang, lalu dimasukkan ke dalam labu tentukur 100 ml dan dilarutkan dan diencerkan dengan air suling hingga garis tanda. Kemudian disaring, 10 ml filtrat pertama dibuang. Dipipet 10 ml filtrat, dimasukkan ke dalam labu tentukur 100 ml, dan diencerkan lagi dengan air suling, lalu dipipet 5 ml dan dimasukkan kedalam labu tentukur 50 ml dan dicukupkan hingga garis tanda, lalu dikocok sampai homogen. Larutan ini lalu diukur serapannya dengan menggunakan spektrofotometri Uv.
1995).
3.7 Penetapan Kadar Tablet Vitamin C 3.7.1 Pembuatan larutan induk baku
Ditimbang 50 mg bahan baku Vitamin C, dimasukkan ke dalam labu tentukur 100 ml. Ditambahkan air suling dikocok sampai larut, lalu dicukupkan dengan air suling sampai garis tanda, konsentrasi teoritis adalah 500 mcg/ ml (LIB I). Selanjutnya dipipet sebanyak 10 ml dari LIB I lalu dimasukkan ke dalam labu tentukur 100 ml lalu dicukupkan dengan air suling sampai garis tanda, kemudian dikocok hingga homogen, sehingga diperoleh larutan dengan konsentrasi teoritis 50 mcg/ ml (LIB II).
3.7.2 Pembuatan kurva serapan
Dipipet LIB II sebanyak 4 ml, lalu dimasukkan kedalam labu tentukur 25 ml dan ditambahkan air suling hingga garis tanda, kemudian dikocok homogen sehingga diperoleh larutan dengan konsentrasi teoritis 8 mcg/ ml. Diukur pada panjang gelombang 200 - 400 nm.
3.7.3 Pembuatan kurva kalibrasi
Dipipet LIB II sebanyak 1,8 ml, 2,7 ml, 3,6 ml, 4,5 ml, dan 5,4 ml, masing-masing dimasukkan ke dalam labu tentukur 25 ml, dicukupkan dengan air suling sampai garis tanda. Dikocok homogen sehingga diperoleh larutan dengan konsentrasi 3,6 mcg/ ml, 5,4 mcg/ ml, 7,2 mcg/ ml, 9,0 mcg/ ml, 10,8 mcg/ ml. Diukur serapannya pada panjang gelombang 243,5 nm.
Ditimbang 20 tablet, dicatat beratnya, kemudian digerus sampai homogen. Ditimbang sejumlah serbuk setara dengan 50 mg Vitamin C sebanyak 6 kali, masing-masing dimasukkan ke dalam labu tentukur 100 ml,tambahkan air suling sampai garis tanda. Saring dengan kertas saring, filtrat pertama dibuang 10 ml.
Dari larutan ini pipet 10 ml, masukkan ke dalam labu tentukur 100 ml, encerkan dengan air suling sampai garis tanda. selanjutnya dipipet 5 ml filtrat, dimasukkan kedalam labu tentukur 50 ml dan dicukupkan sampai garis tanda kocok hingga homogen. Kemudian ukur serapannya pada panjang gelombang maksimum yang diperoleh.
3.8 Uji Disolusi Tablet
Medium : 900 ml larutan air suling Alat : tipe 2 (tipe dayung) Kecepatan putaran : 50 rpm
Waktu : 45 menit
Prosedur:
diambil (Ditjen POM, 1995).
Persyaratan: Dalam waktu 45 menit harus larut tidak kurang dari 75% (Q) C6H8O6 dari jumlah yang tertera pada etiket (USP 2007).
Interpretasi: Persyaratan dipenuhi bila jumlah zat aktif yang terlarut dari sediaan yang diuji sesuai dengan tabel penerimaan. Apabila tidak memenuhi persyaratan maka pengujian dilanjutkan sampai tiga tahap, kecuali bila hasil pengujian memenuhi tahap S1 atau S2. Kriteria penerimaan zat aktif yang larut dengan disolusi dapat dilihat pada Tabel 2.2.
Tabel 3.2 Kriteria Penerimaan Zat Aktif Yang Larut Dengan Disolusi
Tahap Jumlah Yang Diuji Kriteria Penerimaan
S1 6 Tiap Unit sediaan tidak kurang dari Q + 5%
S2 6
Rata-rata dari 12 unit (S1 + S2 ) adalah sama dengan atau lebih besar dari Q dan tidak satu unit sediaan yang lebih kecil dari Q - 15%
S3 12
Rata-rata dari 24 unit adalah sama dengan atau lebih besar dari Q tidak lebih dari 2 unit sediaan yang lebih kecil dari Q - 15% dan tidak 1 unit pun kurang dari Q - 25%
BAB IV
HASIL DAN PEMBAHASAN
4.1 Pati Jagung
Rendemen = 100% 6,19%
Pati jagung pragelatinasi diperoleh dari pengayakan dengan ayakan mesh 20, 60, dan 100 dari total pengeringan pati jagung yang didapat dari proses isolasi biji jagung (Zea mays L). sehingga didapatkan masing-masing berat dari ukuran partikel mesh 20,60, dan 100. Hasil uji distribusi partikel dapat dilihat pada tabel.
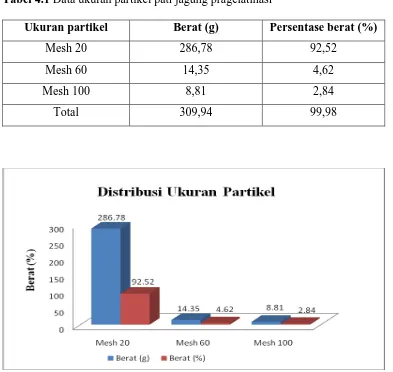
Tabel 4.1 Data ukuran partikel pati jagung pragelatinasi
Ukuran partikel Berat (g) Persentase berat (%)
Mesh 20 286,78 92,52
Mesh 60 14,35 4,62
Mesh 100 8,81 2,84
Total 309,94 99,98
Gambar 4.1 Histogram Distribusi Partikel
Uji komprimabilitas dilakukan untuk dapat menghasilkan tablet dengan kekerasan tertinggi. Hal ini dilakukan dengan cara mencetak tablet dengan meningkatkan skala kompresi.
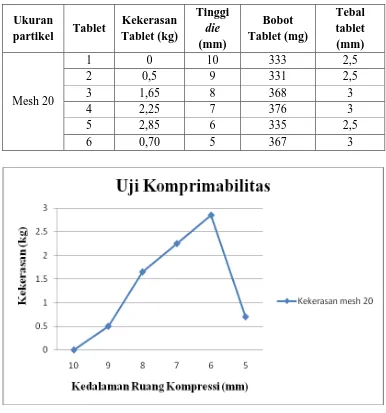
Tabel 4.2 Data uji komprimabilitas terhadap pati jagung pragelatinasi
Ukuran
partikel Tablet
Kekerasan Tablet (kg)
Tinggi
die
(mm)
Bobot Tablet (mg)
Tebal tablet (mm)
Mesh 20
1 0 10 333 2,5
2 0,5 9 331 2,5
3 1,65 8 368 3
4 2,25 7 376 3
5 2,85 6 335 2,5
6 0,70 5 367 3
Gambar 4.2 Grafik Uji Komprimabilitas
kekerasan tablet mencapai 2,25 kg, dan pada ketinggian die 6 mm, kekerasan tablet mencapai 2,85 kg. Rasio kekerasan tablet berkisar antara 2 - 3 kg.
Berdasarkan grafik dari Gambar 4.2 dapat dilihat bahwa hasil uji komprimabilitas untuk pati jagung pragelatinasi dengan mesh 20 dapat digunakan sebagai bahan pengisi tablet secara cetak langsung.
4.2 Hasil Uji Preformulasi
Hasil uji preformulasi yang dilakukan terhadap semua formula Vitamin C yang dibuat dengan menggunakan pati jagung pragelatinasi ukuran partikel mesh 20 sebagai bahan pengisi yang meliputi uji sudut diam, uji waktu alir, dan uji indeks tap. Berikut tabel hasil uji preformulasi berbagai formula yang dibuat.
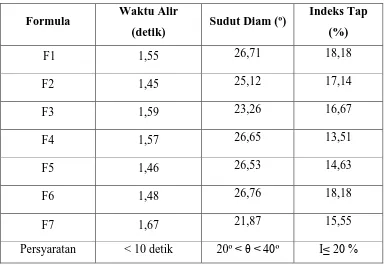
Tabel 4.3 Data Hasil Uji Preformulasi
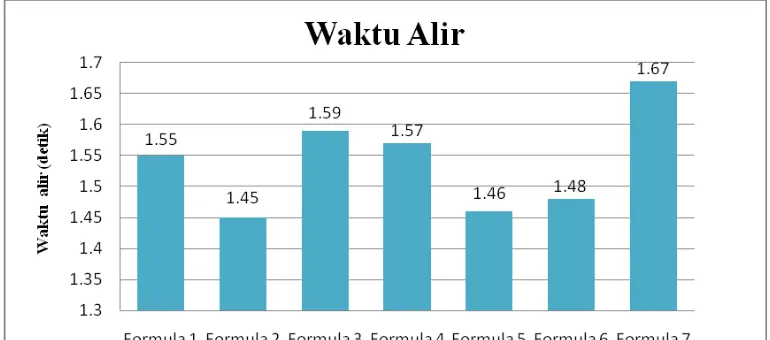
Formula Waktu Alir
(detik) Sudut Diam (º)
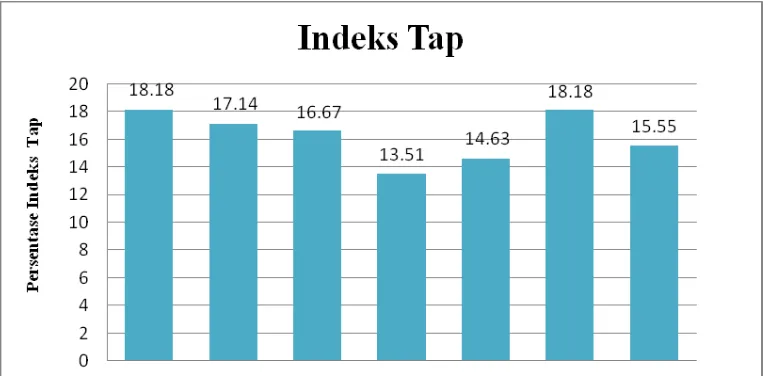
Indeks Tap (%)
F1 1,55 26,71 18,18
F2 1,45 25,12 17,14
F3 1,59 23,26 16,67
F4 1,57 26,65 13,51
F5 1,46 26,53 14,63
F6 1,48 26,76 18,18
F7 1,67 21,87 15,55
100%
F2 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 90% dan granul laktosa 10%
F3 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 80% dan granul laktosa 20%
F4 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 70% dan granul laktosa 30%
F5 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 60% dan granul laktosa 40%
F6 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 50% dan granul laktosa 50%
F7 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 40% dan granul laktosa 60
Gambar 4.3 Histogram Waktu Alir
Gambar 4.4 Histogram Sudut Diam
Berdasarkan Grafik dari Gambar 4.4 menunjukkan bahwa sudut diam granul memenuhi syarat yang ditetapkan yaitu 20o < θ < 40o. Semakin besar sudut diam yang dibentuk oleh granul, maka semakin banyak pula serbuk yang terdapat pada granul yang di uji dan waktu alirnya kurang baik.
indeks tap juga memenuhi syarat karena menunjukkan selisih volume lebih kecil dari 20% sebelum dan sesudah di tap. Hasil uji preformulasi menunjukkan bahwa formula memenuhi persyaratan.
4.3 Hasil Evaluasi Tablet
Evaluasi tablet Vitamin C yang dilakukan adalah uji kekerasan tablet, uji waktu hancur, penetapan kadar, uji friabilitas, keseragaman kandungan dan uji disolusi tablet.
4.3.1 Hasil uji kekerasan tablet
Uji kekerasan tablet dapat dilihat pada tabel di bawah ini.
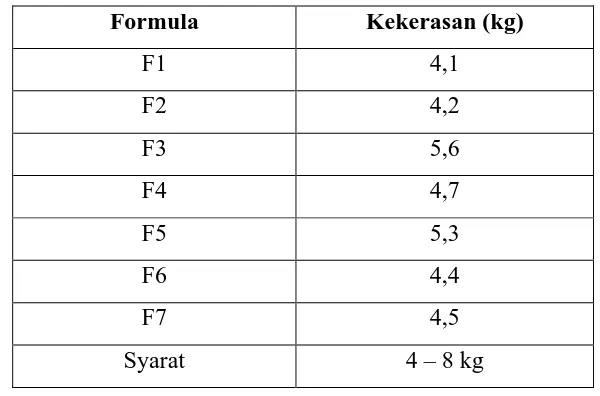
Tabel 4.4 Data Hasil Uji Kekerasan Tablet Vitamin C
Formula Kekerasan (kg)
F1 4,1
F2 4,2
F3 5,6
F4 4,7
F5 5,3
F6 4,4
F7 4,5
Syarat 4 – 8 kg
Keterangan:
F1 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinsi 100%
F3 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 80% dan granul laktosa 20%
F4 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 70% dan granul laktosa 30%
F5 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 60% dan granul laktosa 40%
F6 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 50% dan granul laktosa 50%
F7 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 40% dan granul laktosa 60%
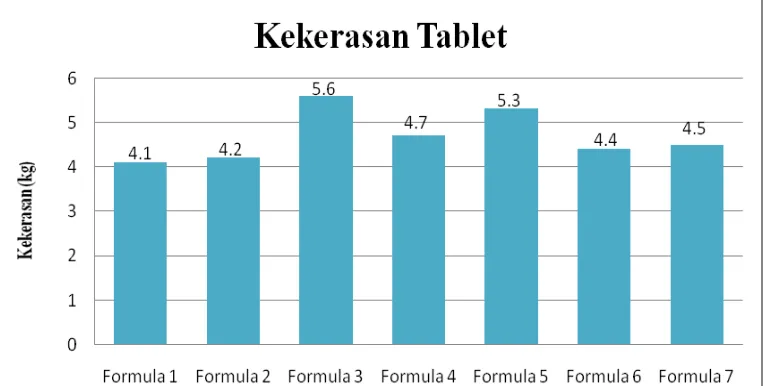
Gambar 4.6 Histogram Uji Kekerasan Tablet
Berdasarkan Grafik dari Gambar 4.6 dapat dilihat bahwa kekerasan tablet semua formula memenuhi syarat yaitu 4 - 8 kg, dengan hasil yang bervariasi.
4.3.2 Hasil uji waktu hancur
Uji waktu hancur dapat dilihat pada tabel di bawah ini.
Tabel 4.5 Data Hasil Uji Waktu Hancur Tablet Vitamin C
Formula Waktu Hancur (menit)
F1 07,14
F4 08,03
F5 08,32
F6 08,38
F7 08,25
Syarat <15 menit
Keterangan:
F1 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinsi 100%
F2 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 90% dan granul laktosa 10%
F3 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 80% dan granul laktosa 20%
F4 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 70% dan granul laktosa 30%
F5 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 60% dan granul laktosa 40%
F6 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 50% dan granul laktosa 50%
F7 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 40% dan granul laktosa 60%
Berdasarkan Grafik dari Gambar 4.7 menunjukkan bahwa data waktu hancur tablet Vitamin C yang diformulasi dengan menggunakan bahan tambahan pati jagung pragelatinasi sebagai bahan pengisi menghasilkan waktu hancur tablet yang berbeda-beda. Tetapi masing-masing formula memenuhi syarat yaitu <15 menit.
4.3.3 Hasil uji penetapan kadar
Uji penetapan kadar dapat dilihat pada tabel di bawah ini.
Tabel 4.6 Data Hasil Uji Penetapan Kadar Tablet Vitamin C
Formula Kadar Vitamin C yang
diperoleh (%)
F1 94,13 ± 3,97
F2 94,37 ± 3,39
F3 107,93 ± 2,43
F4 101,19 ± 3,52
F5 99,02 ± 5,37
F6 97,98 ± 2,64
F7 97,42 ± 2,74
Syarat 90,00% - 110,00%
Keterangan:
F1 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinsi 100%
F2 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 90% dan granul laktosa 10%
F3 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 80% dan granul laktosa 20%
F4 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 70% dan granul laktosa 30%
F5 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 60% dan granul laktosa 40%
40% dan granul laktosa 60%
Gambar 4.8 Histogram Kadar Tablet Vitamin C
digunakan dalam formula mempengaruhi kadar Vitamin C yang terkandung di dalam tablet.
4.3.4 Hasil uji friabilitas
Uji friabilitas dapat dilihat pada tabel di bawah ini.
Tabel 4.7 Data Hasil Uji Friabilitas Tablet Vitamin C
Formula Friabilitas (%)
F1 0,46
F2 0,51
F3 0,67
F4 0,62
F5 0,66
F6 0,53
F7 0,58
Syarat < 0,8%
Keterangan:
F1 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinsi 100%
F2 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 90% dan granul laktosa 10%
F3 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 80% dan granul laktosa 20%
F4 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 70% dan granul laktosa 30%
F5 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 60% dan granul laktosa 40%
F6 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 50% dan granul laktosa 50%
Gambar 4.9 Histogram Uji Friabilitas
Berdasarkan Grafik dari Gambar 4.9 menunjukkan bahwa semua formula memenuhi syarat yaitu < 0,8 %.
4.3.5 Hasil uji keseragaman kandungan
Uji keseragaman Kandungan dapat dilihat pada tabel di bawah ini.
Tabel 4.8 Data Hasil Uji Keseragaman Kandungan Tablet Vitamin C
Formula Kadar Vitamin C (%) RSD (%)
F1 89,52 1,40
F2 93,79 0,90
F3 113,64 0,51
F4 109,11 1,97
F5 103,10 1,43
F6 100,13 0,55
F7 97,46 0,95
Keterangan:
F1 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinsi 100%
F2 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 90% dan granul laktosa 10%
F3 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 80% dan granul laktosa 20%
F4 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 70% dan granul laktosa 30%
F5 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 60% dan granul laktosa 40%
F6 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 50% dan granul laktosa 50%
F7 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 40% dan granul laktosa 60%
Gambar 4.10 Histogram Uji Keseragaman Kandungan
Uji disolusi dapat dilihat pada tabel di bawah ini.
Tabel 4.9 Data Hasil Uji Disolusi Tablet Vitamin C Waktu
(menit)
Persentase Kumulatif Vitamin C yang terlepas (%)
F1 F2 F3 F4 F5 F6 F7
5 17,11 19,15 33,28 28,20 30,25 25,16 22,16 10 27,25 30,25 46,40 40,25 42,39 37,26 34,46 15 47,27 49,38 58,44 54,31 56,46 52,80 51,58 20 57,40 59,40 69,52 64,45 67,54 61,76 60,44 35 65,43 67,48 78,58 75,49 75,51 70,56 69,52 45 78,43 80,59 86,83 84,40 85,62 82,72 82,50
Keterangan:
F1 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinsi 100%
F2 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 90% dan granul laktosa 10%
F3 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 80% dan granul laktosa 20%
F4 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 70% dan granul laktosa 30%
F5 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 60% dan granul laktosa 40%
F6 : Formula tablet Vitamin C dengan konsentrasi pati jagung pragelatinasi 50% dan granul laktosa 50%
Gambar 4.11 Grafik % Kumulatif Disolusi Tablet Vitamin C
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan penelitian yang telah dilakukan, maka kesimpulan dari penelitian ini adalah :
a. Pati jagung pragelatinasi mesh 20 dapat digunakan sebagai bahan pengisi pada pembuatan tablet Vitamin C secara cetak langsung, baik dikombinasikan maupun tidak dikombinasikan.
b. Konsentrasi kombinasi pati jagung pragelatinasi mesh 20 dan granul laktosa mesh 20 yang paling baik digunakan sebagai bahan pengisi pada pembuatan tablet Vitamin C secara cetak langsung adalah konsentrasi pati jagung pragelatinasi 80% dan granul laktosa 20%.
5.2 Saran
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan 2.1.1 Pati jagung
Jagung banyak digunakan pada industri makanan, minuman, dan farmasi. Berdasarkan komposisi dan kandungan nutrisi, jagung mempunyai prospek sebagai pangan dan bahan baku industri (Suarni dan Sarasutha, 2002).
Pati adalah karbohidrat yang terjadi dari rangkaian molekul panjang yang berbentuk butiran. Pati dapat diperoleh dari berbagai bagian tanaman seperti biji, umbi, batang, dan buah. Pati dalam jaringan mempunyai bentuk butir yang berbeda-beda. Umumnya butir padi terdiri dari lapisan-lapisan yang mengelilingi satu titik yang disebut hillum. Hillum dapat terletak di tengah atau dapat pula di pinggir. Biji jagung mengandung pati 54,1% - 71,7%, karbohidarat pada jagung sebagian besar merupakan komponen pati, sedangkan komponen lainnya adalah pentose, dekstrin, sukrosa, dan gula pereduksi (Fahn, 1992).
modifikasi genetika. Perlakuan ini dapat mencakup penggunaan panas, asam, alkali, zat pengoksidasi atau bahan kimia lainnya yang akan menghasilkan gugus kimia yang baru dan atau perubahan bentuk, ukuran serta struktur molekul pati. Pati yang termodifikasi mempunyai kekentalan yang stabil baik pada suhu tinggi maupun suhu rendah, mempunyai ketahanan yang baik terhadap perlakuan mekanis, dan daya pengentalannya tahan pada kondisi asam (Glicksman, 1969).
Granul pati utuh tidak larut dalam air dingin. Granul pati dapat menyerap air dan mengembang, tetapi tidak dapat kembali seperti semula. Air yang terserap dalam molekul menyebabkan granul mengembang. Apabila granul pati ditambahkan air panas atau dingin yang kemudian dipanaskan, maka pati dapat mengalami gelatinasi (Winarno, 1995).
2.1.2 Klasifikasi tanaman jagung
Division : Spermatophyta Sub-divisio : Angiospermae Klass : Monocotyledoneae Ordo : Graminae
Famili : Graminaceae Genus : Zea
2.1.3 Nama lain tanaman jagung
Nama Jagung di Indonesia beranekaragam yaitu jagong (Sunda, aceh, Batak, Ambon), jhaghung (Madura), rigi (Nias), wataru (Sumba), latung (Flores), pena (Timor), gandung (Toraja) (Hartono, 2007).
2.2 Vitamin
Vitamin adalah senyawa organik yang diperlukan oleh tubuh dalam jumlah sedikit, tetapi penting untuk melakukan fungsi metabolik di dalam tubuh. Vitamin tidak dapat disintesa oleh tubuh kecuali vitamin K, maka vitamin harus ada dalam makanan yang dikonsumsi (Andarwulan dan Koswara, 1989).
Vitamin dapat dibedakan menjadi dua golongan yaitu vitamin yang dapat larut dalam air dan vitamin yang dapat larut dalam lemak. Jenis vitamin yang dapat larut dalam air adalah vitamin B kompleks dan vitamin C. Vitamin
yang dapat larut dalam lemak adalah A, D, E, dan K, serta provitamin A yaitu β-karoten. Bahan makanan yang kaya akan vitamin adalah sayur-sayuran dan
buah-buahan (Sudarmadji, 1989).
2.2.1 Vitamin C
sejenisnya. Vitamin C tidak stabil dalam bentuk larutan, terutama jika terdapat udara, logam-logam seperti Cu, Fe, dan cahaya (Andarwulan dan Koswara, 1989). Struktur kimia vitamin C dapat dilihat pada Gambar 2.1 di bawah ini (Ditjen POM, 1995) :
Gambar 2.1 Struktur Kimia Vitamin C
2.3 Amilum
Amilum merupakan campuran dua macam struktur polisakarida yang berbeda amilosa dan amilopektin. Amilosa mempunyai struktur lurus dan terdiri dari 250 sampai 300 unit D-glukopiranosa yang tersusun dalam ikatan α -1,4 glukosa. Amilosa merupakan polisakarida, polimer yang tersusun dari glukosa sebagai monomernya. Amilosa merupakan polimer tidak bercabang yang bersama-sama dengan amilopektin menjadi komponen penyusun pati.
Amilopektin merupakan polisakarida yang tersusun dari monomer α -glukosa. Amilopektin merupakan molekul raksasa dan mudah ditemukan karena menjadi satu dari dua senyawa penyusun pati, bersama-sama dengan amilosa. Walaupun tersusun dari monomer yang sama, amilopektin berbeda dengan amilosa, yang terlihat dari karakteristik fisiknya. Secara struktural, amilopektin terbentuk dari rantai glukosa yang terikat dengan ikatan α -1,6-glukosa, sama dengan amilosa. Namun, pada amilopektin terbentuk cabang-cabang (sekitar tiap 20 mata rantai glukosa) dengan ikatan α-1,4-glukosa.
Gambar 2.3 Struktur Kimia Amilopektin
Kedua fraksi tersebut dapat dibedakan berdasarkan reaksinya terhadap larutan yodium, dimana amilosa memberikan warna biru ungu sedangkan amilopektin warna merah ungu. Pada umumnya amilum mempunyai kandungan amilosa 25% dan amilopektin 75% (Charles, 2010).
2.4 Laktosa
sedangkan hewan menyusui lainnya mengandung 3% - 5% laktosa. Laktosa berupa kristalin keras atau serbuk putih, stabil di udara, larut dalam 5 ml air dan larut dalam 2,6 ml air mendidih (USP edisi XXI).
2.5 Uraian Tablet 2.5.1 Pengertian tablet
Tablet adalah sediaan padat yang mengandung bahan obat dengan atau tanpa bahan pengisi. Sebagian besar tablet dibuat dengn cara pengempaan dan merupakan bentuk sediaan yang paling banyak digunakan. Tablet kempa dibuat dengan memberikan tekanan tinggi pada serbuk atau granul menggunakan cetakan baja. Tablet dibuat dengan berbagai ukuran, bentuk dan penandaan permukaan tergantung pada desain cetakan (Ditjen POM, 1995).
Untuk mendapatkan tablet yang baik, maka bahan pengisi yang akan dikempa menjadi tablet harus memenuhi sifat-sifat berikut:
a. Mudah mengalir, artinya jumlah bahan yang mengalir dalam corong alir ke dalam ruang cetakan selalu sama setiap saat, dengan demikian bobot tablet tidak akan memiliki variasi yang besar.
b. Kompatibel, artinya bahan mudah kompak jika dikempa, sehingga dihasilkan tablet yang keras.
2.5.2 Bahan pengisi
Bahan pengisi adalah suatu zat yang inert secara farmakologis yang ditambahkan kedalam suatu formulasi sediaaan tablet yang bertujuan untuk penyesuaian bobot, ukuran tablet sesuai yang dipersyaratkan, untuk membantu kemudahan dalam pembuatan tablet, dan meningkatkan mutu sediaan tablet (Charles, 2010).
Macam-macam bahan pengisi (Charles, 2010) : 1. Golongan Gula
Laktosa : disebut juga gula susu atau Saccharum Lactis.
Sukrosa : disebut juga gula pasir atau Saccaharum album.
Manitol : berupa Kristal dengan rasa manis, larut dalam air.
Sorbitol : serbuk mikro kristalin berwarna putih, tak berbau, rasa manis, larut dalam air.
2. Golongan Amylum
Disebut juga pati, yaitu serbuk berwarna putih, tidak berbau, tidak berasa, tidak larut dalam air, bila dididihkan dengan air setelah dingin akan membentuk larutan kental yang jernih.
Pati dapat dipoeroleh dari :
pragelatinasi. Pati pragelatinasi terbuat dari pati alami. Setelah di pragelatinasi bentuknya berupa granul yang free flowing dan mempunyai daya ikat sehingga bisa dibuat cetak langsung.
3. Golongan organik dan anorgnik
Bolus alba.
Natrium klorida.
Natrium sulfat.
Magnesium karbonat. 4. Zat pengisi lainnya
Avicel
Aerosil
2.5.3 Metode pembuatan tablet
Tablet dibuat dengan 3 cara umum, yaitu granulasi basah, granulasi kering (mesin rol atau mesin slug) dan kempa langsung. Tujuan granulasi basah dan kering adalah untuk meningkatkan aliran campuran dan atau kemampuan kempa. Granulat kering dibuat dengan cara menekan massa serbuk pada tekanan tinggi sehingga menjadi tablet yang besar kemudian digiling dan diayak hingga diperoleh granul dengan ukuran partikel yang diinginkan. Cetak langsung merupakan pengempaan langsung dengan kecepatan tinggi tanpa tahap granulasi terlebih dahulu (Ditjen POM, 1995).
Zat berkhasiat, pengisi dan penghancur dicampur homogen, lalu dibasahi dengan larutan pengikat, bila perlu ditambahkan pewarna. Diayak menjadi granul dan dikeringkan dalam lemari pengering pada suhu 40oC - 50oC. setelah kering diayak lagi untuk memperoleh granul dengan ukuran yang diperlukan dan ditambahkan bahan pelicin dan dicetak dengan mesin tablet (Anief, 1994). Granulasi basah adalah proses menambahkan cairan pada suatu serbuk atau campuran serbuk dalam suatu wadah yang dilengkapi dengan pengadukan yang akan menghasilkan granul (Lachman, dkk., 1994).
b. Granulasi kering
Granulasi kering dilakukan apabila zat aktif tidak mungkin di granulasi basah karena tidak stabil atau peka terhadap panas dan lembab, tidak dapat dikempa langsung menjadi tablet karena zat aktif tidak dapat mengalir bebas dan dosis efektif zat aktif terlalu besar untuk cetak langsung (Lachman, dkk.,1994).
Setelah penimbangan dan pencampuran bahan, serbuk di slugged atau dicetak langsung menjadi tablet yang tebal dan datar dengan garis tengah sekitar 1 inci. Tablet harus cukup keras agar ketika dipecahkan tidak menimbulkan serbuk yang berceceran. Tablet ini dipecahkan dengan tangan atau alat dan diayak dengan lubang yang di inginkan, pelicin ditambahkan dan tablet dikempa (Ansel, 1989).
c. Cetak Langsung
1989). Proses tablet cetak langsung dari campuran serbuk zat aktif dan eksipien yang sesuai (termasuk pengisi, desintegran, dan pelicin), yang akan mengalir dengan seragam ke dalam lubang kempa dan membentuk suatu padatan yang kokoh (Charles, 2010).
2.5.4 Metode cetak langsung
Metode ini digunakan untuk bahan yang mempunyai sifat mudah mengalir sebagaimana sifat-sifat kohesinya yang memungkinkan untuk langsung dicetak dalam tablet tanpa memerlukan granulasi basah atau kering (Sheth,dkk., 1980)
Cetak langsung dapat diartikan sebagai pembuatan tablet dari bahan-bahan yang berbentuk kristal atau serbuk tanpa merubah karakter fisiknya. Metode ini digunakan pada bahan-bahan (baik obat mupun bahan tambahan) yang mudah mengalir dan memiliki kompresibilitas yang baik yang memungkinkan untuk langsung di cetak dalam mesin tablet tanpa memerlukan proses granulasi. Pada umumnya obat yang dapat dibuat dengan metode kempa langsung hanya sedikit, karena bahan-bahan yang memiliki sifat-sifat tersebut di atas tidak banyak.
kemungkinan terjadi perubahan zat aktif akibat pengkristalan kembali yang tidak terkendali selama proses pengeringan.
Kecepatan pelarutan obatnya akan lebih baik karena zat aktif tidak terdapat dalam granul, sehingga dapat segera dilepaskan dan siap dengan pelarutan setelah tablet hancur.
Untuk obat dengan dosis tinggi, jika volume bulk tinggi, kompresibilitas yang jelek dan sifat alir yang jelek, tidak akan memungkinkan campuran untuk cetak langsung. Perbedaan ukuran partikel atau densitas antara obat dan partikel bahan tambahan akan mempengaruhi homogenitas campuran. Pemilihan bahan pembawa, serbuk yang bersifat kompresibilitas setelah dicetak akan mengalami deformasi plastik, yaitu terjadinya perubahan bentuk dari partikel aslinya, setelah tekanan tidak akan kembali ke bentuk semula. (Sheth, dkk.,1980).
2.5.5 Teori pencampuran
pada waktu pencampuran, partikel-partikel yang ideal berbentuk bola karena lebih mudah bergerak, sedangkan partikel yang berbentuk jarum dan partikel yang tidak teratur lebih sukar bergerak dan membentuk agregat.
Kerapatan massa, dalam proses pencampuran di dalam alat pencampuran dapat terjadi segresi karena gesekan dari partikel yang mempunyai perbedaan kerapatan massa, untuk komponen yang kerapatan massanya besar akan turun ke bawah, sedangkan komponen yang kerapatan massanya kecil akan tetap diatas sehingga dibutuhkan waktu pencampuran yang lebih lama untuk mendapatkan campuran yang homogen.
Kelengketan dan kelicinan, untuk bahan yang bersifat lengket, maka pada proses pencampuran partikelnya akan bergerombol satu sama lain dan melekat pada dinding sehingga proses pencampuran akan lebih sukar, lain halnya bila didapatkan bahan yang licin, bahan tersebut akan membantu dalam proses pencampuran.
Kelembaban, pengaruh kelembaban tinggi yang dominan adalah gaya kapiler, gaya ini mengkibatkan bahan cenderung menggumpal dan melekat pada dinding, sedangkan pada kelembaban yang rendah gaya yang dominan adalah gaya elektrostatik, gaya ini menyebabkan partikel-partikel bermuatan, cenderung membentuk agregat dan mengalami segresi.
sudah homogen bila proses pencampurannya dilanjutkan maka pada waktu yang lama tidak homogen lagi (Parrot, 1997).
2.5.6 Komposisi tablet
Komposisi umum dalam tablet adalah (Chrles, 2010) : 1. Zat berkhasiat
2. Bahan pengisi : ditambahkan untuk mendapatkan berat yang diinginkan. Bahan pengisi harus bersifat inert.
3. Bahan pengikat : ditambahkan untuk mengikat komponen-komponen tablet untuk dijadikan granul dengan ukuran yang sama dan bentuk speris setelah dipaksakan melewati ayakan. Dengan adanya bahan pengikat, komponen tablet akan mudah dibentuk menjadi granul, sehingga akan memudahkan dalam pencetakan.
4. Bahan pengembang : ditambahkan untuk memecahkan tablet menjadi partikel kecil sehingga luas permukaan diperbesar dan absorpsi dipermudah.
5. Bahan pelicin : ditambahkan dengan maksud untuk meningkatkan daya alir granul-granul pada corong pengisi, mencegah melekatnya massa pada punch dan die, mengurangi gesekan antara butir-butir granul dan mempermudah pengeluaran tablet dari die.
7. Zat pewangi dan pemanis : ditambahkan untuk menutupi bau dan rasa yang tidak enak, memberikan bau tertentu.
8. Adjuvants : ditambahkan sebagai antioksidan dan mengurangi efek samping.
9. Absorban : ditambahkan untuk melindungi bahan berkhasiat dari pengaruh lembab, menghomogenkan distribusi zat berkhasiat, menghindari kebasahan akibat sifat dan kombinasi zat berkhasiat.
10. Bahan pembasah : ditambahkan untuk mempercepat hancurnya tablet. Misalnya: Natrium lauril sulfat, polisorbat, dan aerosil dimana bahan ini akan mempercepat penetrasi air ke dalam tablet.
2.5.7 Evaluasi tablet
1. Kadar zat berkhasiat
Kadar zat berkhasiat tertera dalam monografi masing-masing tablet baik batasan nilainya maupun cara penetapannya.
2. Kekerasan Tablet
Ketahanan dari tablet terhadap goncangan pada waktu pengangkutan, pengemasan dan peredaran bergantung pada kekerasan tablet. Kekerasan dinyatakan dalam satuan kg dari tenaga yang dibutuhkan untuk memecah tablet (Lachman, dkk., 1994).
3. Friabilitas
4. Waktu Hancur
Uji waktu hancur tidak menyatakan bahwa sediaan atau bahan aktifnya terlarut sempurna, tetapi hanya menyatakan waktu yang diperlukan tablet untuk hancur di bawah kondisi yang ditetapkan (Lachman, dkk.,1994).
Waktu hancur yang semakin cepat akan semakin cepat pula pelarutan dari bahan berkhasiat sehingga akan lebih cepat berkhasiat dalam tubuh (Murni, 2008).
5. Keseragaman Sediaan (Ditjen POM, 1995)
Keseragaman sediaan dapat ditetapkan dengan dua cara, yaitu:
a) Keragaman bobot, dilakukan terhadap tablet yang 50% bahan aktifnya lebih besar atau sama dengan 50 mg.
b) Keseragaman kandungan, dilakukan terhadap tablet yang 50% bahan aktifnya kurang dari 50 mg.
6. Disolusi
Adalah proses melarutnya suatu obat (Ansel, 1989). Saat sekarang ini disolusi dipandang sebagai salah satu uji pengawasan mutu yang paling penting dilakukan pada sediaan farmasi. Pada uji disolusi dapat diketahui Cepatnya obat atau tablet melarut menentukan kadar bahan berkhasiat yang terlepas di dalam tubuh. Karena itu laju larut berhubungan langsung dengan kemajuan dari tablet dan perbedaan bioavibilitas dari berbagai formula (Lachman, dkk., 1994).
biarkan mencapai temperatur 37 C ± 0,5 C. kemudian 1 tablet yang diuji di masukkan ke dalam bejana atau ditempatkan dalam keranjang dan pengaduk diputar dengan kecepatan seperti yang ditetapkan dalam monografi. Tablet harus memenuhi persyaratan seperti yang terdapat dalam monografi untuk kecepatan disolusi (Ansel,1989).
2.5.8 Masalah dalam pembuatan tablet
Pada pembuatan tablet dan pengembangan formula atau proses
pencetakan tablet selalu timbul masalah-masalah yang disebabkan karena kesalahan formula, mesin pencetak ataupun keduanya.
Masalah-masalah yang timbul dalam pembuatan tablet dan pengembangan formula tersebut antara lain (Lachman, dkk., 1994) :
1. Capping (splitting)
Yaitu retak pada permukaan atas atau bawah tablet. Penyebabnya :
a. Kurangnya bahan pengikat atau bahan tidak sesuai
Ini dapat diatasi dengan menambahkan lagi bahan pengikat, dan digranulasi kembali atau mengganti jenis pengikat. Untuk bahan-bahan yang hidrofob dipakai bahan pengikat yang kuat misalnya : gom arab dan turunan selulosa. b. Kerusakan Punch atau die
ini akan bertambah besar, sehingga tablet akan dikeluarkan melalui lubang yang lebih sempit diatasnya yang menyebabkan capping.
c. Granul-granul terlalu kering
Dapat diatasi dengan menyemprotkan air atau menambahkan zat yang higroskopis untuk mempertahankan tingkat kelembaban yang dikehendaki, misalnya : Polietilen glikol 4000, Sorbitol atau Metil selulosa.
d. Tekanan yang berlebihan
Mengatasinya dengan cara mengatur besarnya tekanan pada mesin cetak. e. Pengaturan Punch yang tidak sesuai
Punch bawah pada saat naik harus rata dengan permukaan die ketika tablet akan dikeluarkan, bila permukaan berada di bawah dari permukaan die maka pada proses pengeluaran tablet, sebagian dari tablet akan berada dalam die sehingga pada saat penyapu tablet mengeluarkan tablet keluar dan sebagian tablet tersebut akan tertinggal dalam die.
2. Picking dan sticking
Picking adalah melekatnya massa pada permukaan punch sedangkan Sticking adalah melekatnya massa pada dinding die.
Penyebabnya :
• Kurang keringnya granul-granul
• Kurangnya bahan pelicin
• Punch dan die yang kotor ataupun kasar
Humidity (kelembaban) relatif ruang cetak akan berbeda pada saat pagi, siang dan sore dimana jumlah lembab sangat berpengaruh terhadap pencetakan zat berkhasiat yang higroskopis.
4. Motling
Yaitu ketidaksamaan distribusi warna, sehingga warna dari tablet tidak merata. Penyebabnya :
• Pencampuran yang kurang homogen.
• Suhu pengeringan yang terlalu tinggi.
2.6 Spektrofotometri Ultraviolet (Uv)
Spektrofotometri Uv adalah pengukuran panjang gelombang dari intensitas sinar ultraviolet yang diabsorbsi oleh sampel. Sinar ultraviolet berada pada panjang gelombang 200 - 400 nm. Panjang gelombang adalah jarak antara satu lembah dan satu puncak, sebagai sumber cahaya biasanya digunakan lampu hidrogen atau deutrum untuk pengukuran Uv (Dachriyanus, 2004).
BAB I
PENDAHULUAN
1.1 Latar Belakang
Tablet adalah sediaan padat mengandung bahan obat dengan atau tanpa bahan pengisi. Berdasarkan metode pembuatan, dapat digolongkan sebagai tablet cetak dan tablet kempa. Selain bahan pengisi digunakan juga zat tambahan lain yang berfungsi sebagai bahan pengembang, pengikat, pelicin, pembasah atau zat lain yang cocok (Ditjen POM, 1995).
Sediaan tablet semakin popular pemakaiannya dan merupakan sediaan yang paling banyak diproduksi. Tablet merupakan salah satu sediaan yang banyak mengalami perkembangan dari segi formulasi. Beberapa keuntungan sediaan tablet diantaranya adalah sediaan kompak, biaya pembuatannya lebih murah, dosisnya tepat, mudah pengemasannya, sehingga penggunaannya lebih praktis jika dibandingkan dengan sediaan lain (Lachman, dkk., 1994).
Beberapa keunggulan tablet adalah dosis pemakaiannya tepat, mudah pemakaiannya, sifat kimia dari bahan obat relatif stabil sehingga memungkinkan tablet disimpan lebih lama. Oleh karena itu bidang pengembangan dan produksinya terus meningkat (Voigt, 1994).
Tablet dibuat dengan cara dimapatkan bahan obat atau campuran bahan obat dengan atau tanpa bahan tambahan dengan cara cetak langsung, granulasi basah atau granulasi kering (Lachman, dkk., 1994).
Kristal putih, tidak berwarna, tidak berbau dan mencair pada suhu 190 C -192oC. Senyawa ini bersifat reduktor kuat dan mempunyai rasa asam. Vitamin C sangat mudah larut dalam air (1 g dapat larut sempurna dalam 3 ml air), sedikit larut dalam benzene, eter, kloroform, minyak, dan sejenisnya (Andarwulan dan Koswara, 1989).
Jagung banyak digunakan pada industri makanan, minuman, dan farmasi. Berdasarkan komposisi dan kandungan nutrisi, jagung mempunyai prospek sebagai pangan dan bahan baku industri (Suarni dan Sarasutha, 2002).
Pati memegang peranan penting dalam industri pengolahan pangan antara lain tablet, glukosa, dekstrosa, sirup fruktosa, permen, dan lain-lain. Dalam perdagangan dikenal dua macam pati yaitu pati yang belum dimodifikasi dan pati yang telah dimodifikasi. Pati yang belum dimodifikasi atau pati alami adalah semua jenis pati yang dihasilkan dari pabrik pengolahan dasar misalnya pati jagung. Sedangkan pati termodifikasi adalah pati yang gugus hidroksinya telah diubah atau diberi perlakuan tertentu misalnya dengan pemanasan (Suarni dan Sarasutha, 2002).
Amilum pragelatinasi merupakan amilum yang telah dibuat menjadi pati pragelatinasi dengan cara memanaskan campuran pati dan air hingga suhu di atas 600C kemudian dikeringkan. Tujuan pragelatinasi amilum ini memperbaiki sifat alir dan kompresibilitasnya (Suarni dan Sarasutha, 2002).
Laktosa mempunyai alur komprimabilitas yang baik, artinya dengan sedikit menaikkan tekanan kompresi akan diperoleh kekerasan tablet yang naik drastis, dengan demikian diperoleh tablet yang sifat fisiknya baik (Charles, 2010).
Metode cetak langsung merupakan suatu metode pembuatan tablet yang memiliki prosedur sangat sederhana, dimana bahan obat dengan atau tanpa bahan tambahan setelah dicampur homogen dapat langsung di cetak menjadi tablet. Oleh karena itu, metode ini paling efisien energi, paling cepat pembuatannya dan paling ekonomis untuk memproduksi tablet (Charles, 2010).
Bahan pengisi dalam formulasi tablet adalah untuk mendapatkan berat yang diinginkan dengan syarat: kompresibilitas baik, mudah mengalir (free flowing), dan bersifat inert. Bahan-bahan pengisi yaitu laktosa, sukrosa, sorbitol, manitol, natrium sulfat, dan magnesium karbonat (Charles, 2010).
konsentrasi granul pati jagung 60% dan granul laktosa 40% (Mandasari, 2012). Oleh karena itu peneliti tertarik mencoba, apakah kombinasi pati jagung pragelatinasi mesh 20 dengan granul laktosa mesh 20 dapat digunakan sebagai bahan pengisi pada pembuatan tablet secara cetak langsung, dalam hal ini zat berkhasiat yang digunakan adalah Vitamin C, karena Vitamin C bersifat kristal sehingga tablet bisa di cetak secara cetak langsung.
1.2 Perumusan Masalah
Berdasarkan uraian di atas, maka permasalahan dalam penelitian ini dapat dirumuskan sebagai berikut :
a. apakah pati jagung pragelatinasi mesh 20 dapat digunakan sebagai bahan pengisi pada pembuatan tablet Vitamin C secara cetak langsung, baik dikombinasikan dengan granul laktosa mesh 20 ataupun tidak dikombinasikan?
b. berapakah konsentrasi kombinasi pati jagung pragelatinasi mesh 20 dan granul laktosa mesh 20 yang paling baik digunakan sebagai bahan pengisi pada formulasi tablet?
1.3Hipotesis
Berdasarkan perumusan masalah di atas, maka yang menjadi hipotesis dalam penelitian ini adalah :
dikombinasikan dengan granul laktosa mesh 20 ataupun tidak dikombinasikan.
b. konsentrasi kombinasi pati jagung pragelatinasi mesh 20 dan granul laktosa mesh 20 yang paling baik digunakan sebagai bahan pengisi pada formulasi tablet adalah konsentrasi 50% pati jagung pragelatinasi mesh 20 dan 50% granul laktosa mesh 20.
1.4 Tujuan Penelitian
Berdasarkan hipotesis di atas, maka yang menjadi tujuan dalam penelitian ini adalah :
a. untuk dapat menggunakan kombinasi pati jagung pragelatinasi mesh 20 dan granul laktosa mesh 20 sebagai bahan pengisi pada pembuatan tablet Vitamin C secara cetak langsung.
b. untuk mengetahui konsentrasi kombinasi pati jagung pragelatinasi mesh 20 dan granul laktosa mesh 20 yang paling baik digunakan sebagai bahan pengisi pada formulasi tablet.
1.5Manfaat Penelitian
MESH 20 DENGAN GRANUL LAKTOSA MESH 20 SEBAGAI BAHAN PENGISI PADA PEMBUATAN TABLET VITAMIN C SECARA
CETAK LANGSUNG
Abstrak
Bahan pengisi dalam formulasi tablet adalah suatu zat inert secara farmakologis yang ditambahkan ke dalam suatu formula sediaan tablet yang bertujuan untuk penyesuaian bobot, ukuran tablet yang diharapkan, untuk membantu kemudahan dalam membuat tablet, dan meningkatkan mutu sediaan tablet. Tujuan penelitian ini adalah untuk membuat tablet Vitamin C menggunakan kombinasi pati jagung pragelatinasi dan granul laktosa ukuran mesh 20 sebagai bahan pengisi secara cetak langsung.
Pati jagung pragelatinasi yang digunakan adalah pati jagung pragelatinasi yang diisolasi dari biji jagung (Zea mays L) dan dibuat granul ukuran mesh 20. Bahan pengisi yang digunakan ialah kombinasi pati jagung pragelatinasi ukuran mesh 20 dan granul laktosa ukuran mesh 20 dengan variasi konsentrasi: F1 (pati jagung pragelatinasi 100%), F2 (pati jagung pragelatinasi 90%, granul laktosa 10%), F3 (pati jagung pragelatinasi 80%, granul laktosa 20%), F4 (pati jagung pragelatinasi 70%, granul laktosa 30%), F5 (pati jagung pragelatinasi 60%, granul laktosa 40%), F6 (pati jagung pragelatinasi 50%, granul laktosa 50 %), dan F7 (pati jagung pragelatinasi 40%, granul laktosa 60%). Pengujian yang dilakukan adalah uji preformulasi yaitu uji waktu alir, sudut diam, indeks tap yang dilakukan terhadap massa tablet sebelum dicetak menjadi tablet; dan uji evaluasi tablet yaitu kekerasan, waktu hancur, uji friabilitas, keseragaman kandungan, penetapan kadar, dan uji disolusi. Pada uji penetapan kadar dan uji disolusi digunakan air suling sebagai media dan serapannya diukur secara spektrofotometri Uv dengan panjang gelombang 243.5 nm.
Hasil penelitian menunjukkan kombinasi pati jagung pragelatinasi dan granul laktosa ukuran mesh 20 dapat digunakan sebagai bahan pengisi dalam membuat tablet Vitamin C. Hasil uji preformulasi dan evaluasi tablet memenuhi persyaratan. Kombinasi paling baik terlihat pada formula 3 dengan perbandingan pati jagung pragelatinasi 80%, laktosa 20% yang memberikan hasil waktu alir 1,59 detik, sudut diam 23,26 θ, indeks tap 16,67%, kekerasan tablet 5,6 kg, waktu hancur 09,19 menit, friabilitas 0,62%, keseragaman kandungan 113,64%, kadar tablet 107,93%, dan persen kumulatif Vitamin C yang terlepas dari uji disolusi lebih besar dibandingkan dengan formula lainnya.
COMBINED USE OF CORN STARCH PRGELATINIZED MESH 20 WITH LACTOSE GRANULES MESH 20 AS FILLER TABLETS
VITAMIN C BY COMPRESSED DIRECTLY
Abstract
Excipients in the tablet formulation is a pharmacologically inert substance that is added to a tablet dosage form that aims to adjust the weight, the size of the tablet is expected to help ease in making tablets, and improve the quality of tablet dosage. The purpose of this research is to make Vitamin C tablets using a combination of corn starch granules pragelatinized and 20 mesh size lactose as filler material is compressed directly.
Pragelatinized used corn starch is corn starch pragelatinized isolated from the seeds of corn (Zea mays L) and made 20 mesh size granules. The filler used is a combination of corn starch pragelatinized 20 mesh size and mesh size 20 lactose granules with various concentration: F1 (corn starch pragelatinized 100%), F2 (corn starch pragelatinized 90%, lactose granules 10%), F3 (corn starch pragelatinized 80 %, lactose granules 20%), F4 (corn starch pragelatinized 70%, lactose granules 30%), F5 (corn starch pragelatinized 60%, lactose granules 40%), F6 (corn starch pragelatinized 50%, lactose granules 50%), and F7 (corn starch pragelatinized 40%, lactose granules 60%). Testing is done is test is test flow time preformulation, angle of repose, tapp index committed against the masses molded into a tablet before the tablet; test and evaluation of tablets, namely hardness, disintegration time test, friability test, content uniformity, assay and dissolution test. In the test assay and dissolution test is used as a medium of distilled water and Uv spectrophotometric absorbance measured with 243.5 nm wavelength.
The results showed a combination of corn starch and granulated lactose pragelatinized mesh size 20 can be used as filler in making a tablet of Vitamin C. Preformulation and evaluation of test results meet the requirements of a tablet. The combination is best seen in formula 3 with a ratio of 80% pragelatinized corn starch, granules lactose 20% which gives the results of the flow time of 1.59 seconds, angle of repose 23.26 θ, tapp index 16.67%, 5.6 kg of a tablet hardness, disintegration time test 09.19 minutes, friability 0.62%, content uniformity of 113.64%, tablet content of 107.93%, and cumulative percent of Vitamin C that regardless of the dissolution test is greater than the other formulas.
PENGGUNAAN KOMBINASI PATI JAGUNG
PRAGELATINASI MESH 20 DENGAN GRANUL LAKTOSA
MESH 20 SEBAGAI BAHAN PENGISI PADA PEMBUATAN
TABLET VITAMIN C SECARA CETAK LANGSUNG
SKRIPSI
OLEH:
SAMIRA KHOIRIAH
NIM 081501011
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
PENGGUNAAN KOMBINASI PATI JAGUNG
PRAGELATINASI MESH 20 DENGAN GRANUL LAKTOSA
MESH 20 SEBAGAI BAHAN PENGISI PADA PEMBUATAN
TABLET VITAMIN C SECARA CETAK LANGSUNG
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara