Penentuan Kadar Klorida Pada Air Sumur Dan Air Limbah Dengan Spektrofotometer Portable DR/2010
Teks penuh
Gambar

Dokumen terkait
Angka penyabunan minyak biji bunga matahari tergolong rendah disebabkan oleh karena tersusun dari asam oleat yang merupakan asam lemak tidak jenuh dengan berat
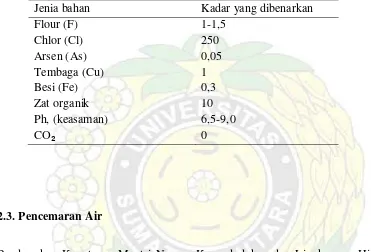
Zat klorida dapat digunakan sebagai indikator adanya pencemaran, yaitu dengan mengukur terlebih dahulu kadar klorida pada sumber air yang diperkirakan tidak
Metode ini digunakan sebagai penentuan kadar klorida karena pelaksanaannya yang mudah dan cepat serta memiliki ketepatan dan kecepatan yang tinggi, juga dapat digunakan
Percobaan yang berjudul “Penentuan Kadar Besi (Fe) dalam Sampel dengan Teknik Spektrofotometer UV-VIS” yang dilakukan pada Hari Rabu, 4 November 2015 di Laboratorium Kimia
Pada praktikum ini adalah uji penentuan kadar klorofil dimana kita dapat menghitung dari kadar klorofil total, klorofil a dan klorofil b pada daun yang memiliki umur yang berbeda
Bahan-bahan yang digunakan pada percobaan penentuan kadar tembaga (Cu) dalam sampel air sumur dengan metode Spektrofotometri Serapan Atom (SSA) adalah sampel air sumur, HNO
Ion-ion yang dapat mengganggu dalam penetapan kadar klorida metode argentometri atau pengendapan adalah: Bahan-bahan yang terdapat dalam air minum dalam jumlah yang normal
3 Istilah dan definisi 3.1 larutan baku klorida, Cl- larutan yang mempunyai kadar klorida, Cl- yang diencerkan dengan air suling sampai kadar tertentu 3.2 larutan blanko bebas