SEMI SINTESIS N,N-BIS(2-HIDROKSIETIL)-3-(4-METOKSIFENIL)
AKRILAMIDA DARI ETIL P-METOKSISINAMAT HASIL ISOLASI RIMPANG KENCUR (Kaempferia galanga, L) MELALUI AMIDASI DENGAN
DIETANOLAMIN
SKRIPSI
ROBIJANTO BANGUN 060802038
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul :SEMI SINTESIS
N,N-BIS(2-HIDROKSIETIL)-3-(4-METOKSIFENIL) AKRILAMIDA DARI ETIL P-METOKSISINAMAT HASIL ISOLASI RIMPANG KENCUR (Kaempferia galanga, L) MELALUI AMIDASI DENGAN DIETANOLAMIN
Kategori : SKRIPSI
Nama : ROBIJANTO BANGUN
Nomor Induk Mahasiswa : 060802038
Program Studi : SARJANA (S1)
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM UNIVERSITAS SUMATERA UTARA Disetujui di,
Medan, Januari 2011 Komisi Pembimbing
Pembimbing 2 Pembimbing 1
Dr. Mimpin Ginting, MS Drs. Darwis Surbakti, MS NIP. 195510131986011001 NIP. 195307071983031001
Diketahui/Disetujui oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
SEMI SINTESIS N,N-BIS(2-HIDROKSIETIL)-3-(4-METOKSIFENIL) AKRILAMIDA DARI ETIL P-METOKSISINAMAT HASIL ISOLASI RIMPANG
KENCUR (Kaempferia galanga, L) MELALUI AMIDASI DENGAN DIETANOLAMIN
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan-ringkasan masing-masing disebutkan sumbernya.
Medan, Januari 2011
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Tuhan Yesus Maha Esa atas kasih dan karuniaNya penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini pada waktunya.
Dalam pelaksanaan penelitian hingga penyelesaian skripsi ini, penulis menyadari banyak mendapat bantuan, motivasi dan dukungan dariberbagai pihak. Untuk itu pada kesempatan ini penulis menyampaikan terimakasih kepada:
1. Bapak Drs.Darwis Surbakti,MS., selaku pembimbing I dan Bapak Dr.Mimpin Ginting,MS., selaku pembimbing II yang telah meluangkan waktu untuk memberikan bimbingan, pengarahan dan saran kepada penulis selama melakukan penelitian dan penyusunan skripsi ini.
2. Dr.Rumondang Bulan Nst,MS dan Drs.Firman Sebayang,MS sebagai ketua dan sekretaris Departemen Kimia FMIPA USU
3. Drs.Adil Ginting, M.Sc, sebagai Kepala Laboratorium Kimia Organik FMIPA USU dan kepada Bapak/ibu dosen Organik Bapak Prof.Dr.Jamaran Kaban,M.Sc, Ibu Juliati Tarigan S.Si,M.Si, Ibu Dra.Herlince Sihotang ,MSi, Ibu Cut Fatimah Zuhra,S.Si,M.Si dan Ibu Helmina br Sembiring,SSi,M.Si atas segala dorongan dan waktu diskusinya
4. Seluruh dosen Departemen Kimia FMIPA USU yang telah memberikan waktunya untuk memberi bimbingan selama penulis mengikuti kuliah di Departemen Kimia F-MIPA USU
5. Sahabat-sahabat terbaik (Marcel, Aspriadi, Feli, Merry, Yemima, AgusManto, Sevia Lity, dan Judika) yang telah membantu, memberi semangat dan motivasi kepada penulis untuk melakukan penelitian ini
6. Teman-teman asisten Laboratorium Kimia Organik ( Cristi, Silo, Bayu, Deni, Sion, Mutiara, dan Samuel)
7. Pihak-pihak yang tidak desebutkan namun tulus membantu penulis dalam penyelesaian skripsi ini.
Sardiana Bangun, Yuli karsina tarigan, dan Doglas Tarigan) dan kepada bibik Uda dan Bapak Uda (I. Br Surbakti, S. Tarigan) terima kasih atas doa dan dukungannya,
Semoga Tuhan selalu memberkati rahmat dan kasih karuniaNya kepada kita semua.
Medan, Januari 2011
ABSTRAK
Etil p-Metoksisinamat dapat diisolasi dari rimpang kencur (Kaempferia galanga, L) secara perkolasi menggunakan pelarut etanol. Pemurnian etil p-metoksisinamat dari hasil ekstraksi dapat dilakukan melalui rekristalisasi mengunakan pelarut etanol. Selanjutnya etil p-metoksisinamat yang memiliki gugus fungsi ester dapat ditransformasikan melalui amidasi menghasilakan senyawa amida turunan sinamat
ABSTRACT
Ethyl p-metoxycinnamate can be isolated from Kaempferia Galanga L (rimpang kencur) by percolation using ethanol as the solvent. Then, the ethyl p-metoxycinnamate, as extraction product, is purified through recrystallization process by using ethanol as the solvent. Ethyl p-metoxycinnamate which has ester functional group can be transformed into amide substance as cinnamate’s derivative by amidation process.
DAFTAR ISI
Daftar Lampiran xiii
Bab 1 Pendahuluan
1.1 Latar Belakang 1
1.2 Permasalahan 2
1.3 Tujuan Penelitian 3
1.4 Manfaat Penelitian 3
1.5 Lokasi Penelitian 3
1.6 Metodologi Penelitian 3
Bab 2 Tinjauan Pustaka
2.1 Tanaman Kencur (Kaemferia galanga, L) 5 2.1.1. Kandungan Kimia dari Kencur 7
2.2 Senyawa Etil p-Metoksisinamat 8
2.2.1. Biosintesa p-metoksisinamat 10
2.3. Amida 12
2.3.1. Reaksi Pembuatan Amida 13
2.3.2. Kegunaan Amida 14
2.4 Dietanolamin 16
2.5 Surfaktan 16
Bab 3 Metodologi Penelitian 22
3.1 Alat-alat 22
3.2 Bahan-bahan 23
3.3 Prosedur Percobaan 24
3.3.1 Preparasi Sampel 24
3.3.3 Amidasi Etil p-metoksisinamat dengan dietanolamin 24 3.3.4 Penentuan Nilai Hidrofil Lopofil Balance (HLB) 25
3.4 Bagan penelitian 27
3.4.1 Preparasi sampel 27
3.4.2 Isolasi Etil p-metoksisinamat dari kencur 27 3.4.3 Amidasi Etil p-metoksisinamat dengan dietanolamin 28 3.4.4 Penentuan Nilai Hidrofil Lipofil Balance (HLB) 29
Bab 4 Hasil dan Pembahasan 30
4.1 Hasil 30
4.1.1 Isolasi Etil p-metoksisinamat dari Rimpang Kencur 30 4.1.2 Amidasi Etil p-metoksisinamat Dengan Dietanolamin
N,N-bis(2-hidroksiasetil)-3-(4-metoksifenil)akrilamida 30
4.2 Pembahasan 32
4.2.1 Isolasi Etil p-metoksisinamat dari Rimpang Kencur 32 4.2.2 Amidasi Etil p-metoksisinamat Dengan Dietanolamin 33
Bab 5 Kesimpulan dan Saran 37
5.1 Kesimpulan 37
5.2 Saran 37
Daftar Pustaka 38
DAFTAR GAMBAR
Halaman Gambar 2.1. Jalur asan sikhimat dalam biosintesa fenilpropanoid
DAFTAR TABEL
Halaman Tabel 2.1. Harga HLB beberapa gugus hidrofilik dan lopofilik 20 Tabel 2.2. Nilai HLB dalam kaitannya dengan kegunaan industri 21 Tabel 4.1. Hasil analisa Kromatografi Lapis Tipis Senyawa
Etil p-metoksisinamat hasil isolasi dan senyawa amida hasil
Sintesis 31
DAFTAR LAMPIRAN
Halaman Lampiran A. Spektrum FT-IR Etil p-metoksisinamat 41 Lampiran B. Spektrum FT-IR N,N-bis(2-hidroksietil)-3-
(4-metoksifenil)akrilamida 42
Lampiran C. Perhitungan harga HLB 43
ABSTRAK
Etil p-Metoksisinamat dapat diisolasi dari rimpang kencur (Kaempferia galanga, L) secara perkolasi menggunakan pelarut etanol. Pemurnian etil p-metoksisinamat dari hasil ekstraksi dapat dilakukan melalui rekristalisasi mengunakan pelarut etanol. Selanjutnya etil p-metoksisinamat yang memiliki gugus fungsi ester dapat ditransformasikan melalui amidasi menghasilakan senyawa amida turunan sinamat
BAB I
PENDAHULUAN
1.1. Latar Belakang
Pemanfaatan hasil isolasi bahan alam menjadi bahan dasar untuk mensintesa senyawa lain yang lebih bermanfaat adalah salah satu peningkatan bahan alam menjadi produk yang lebih potensial. Selanjutnya produk alam yang dapat digunakan menjadi bahan dasar sintesa adalah produk alam yang banyak tersedia dan mengandung gugus fungsi yang dapat ditransformasi menjadi gugus fungsi yang lain.
Etil p-metoksisinamat adalah salah satu produk alam yang terdapat pada rimpang kencur (Kaempferia galanga L) dalam jumlah yang relatif besar. Isolasi dan pemurnian etil p-metoksisinamat dapat dilakukan dengan mudah, selain itu etil p-metoksisinamat mempunyai gugus fungsi yang reaktif sehingga sangat mudah ditransformasikan menjadi gugus fungsi yang lain. Etil p-metoksisinamat adalah ester alam dimana gugus esternya dapat diamidasi menjadi senyawa amida yang lebih bermanfaat sehingga etil p-metoksisinamat memungkinkan sebagai bahan dasar sintesa amida turunan sinamat (Taufikurohmah,2008).
Kencur merupakan tanaman tropis yang banyak tumbuh di berbagai daerah di Indonesia sebagai tanaman yang dibudidayakan. Biasanya tanaman ini dari umbinya digunakan sebagai ramuan obat tradisional sebagai pengaktif. Dalam kehidupan sehari-hari kencur digunakan sebagai bumbu yang disertakan dalam berbagai masakan sehingga sekarang ini kencur sudah banyak dibudidayakan sebagai hasil pertanian yang diperdagangkan dalam jumlah yang besar (Hamida,2007).
kandungan kimia ini etil p-metoksisinamat merupakan komponen utama yang dengan mudah dapat diisolasi dan dimurnikan. Perkolasi serbuk kencur kering dalam etanol teknis sebagai pelarut bedasarkan hasil peneliti sebelumnya dapat menghasilkan 1,1 % Etil p-metoksisinamat dari berat kencur segar (Barus,2009)
Adanya gugus fungsi ester yang sangat reaktif pada etil p-metoksisinamat menyebabkan senyawa ini sangat mudah diamidasi menjadi senyawa amida turunan sinamat. Pada dasarnya transformasi gugus fungsi ester menjadi gugus fungsi amida dapat dilakukan dengan mereaksikan langsung dengan pereaksi senyawa amina seperti dietanolamin pada kondisi tertentu. Seperti yang telah dilakukan sebelumnya mengamidasi Etil p-metoksisinamat dengan glisin menggunkana katalis NaOCH3 (Barus,2009).
Dalam hal ini peneliti ingin mengamidasi N,N-bis(2-hidroksietil)-3-(4-metoksifenil) akrilamida melalui amidasi etil p-metoksisinamat hasil isolasi dari kencur dengan dietanolamin sehingga diharapkan dapat digunakan sebagai surfaktan dan antimikroba.
1.2. Permasalahan
- Apakah senyawa etil p-metoksisinamat yang mengandung gugus ester dapat di isolasi dari kencur dengan metode perkolasi menggunakan pelarut etanol
1.3. Tujuan Penelitian
- Untuk mengisolasi etil p-metoksisinamat dari kencur dengan menggunakan metode perkolasi dengan menggunakan pelarut etanol.
- Untuk mengamidasi etil p-metoksisinamat dengan dietanolamin menggunakan katalis NaOCH3, menghasilkan senyawa N,N-Bis(2-hidroksietil)-3-(4-metoksifenil)akrilamida.
1.4.Manfaat Penelitian
- Penelitian ini diharapkan dapat memberikan informasi ilmiah terutama transformasi terhadap etil p-metoksisinamat yang terdapat pada kencur dan perkembangan ilmu kimia khususnya dalam bidang sintesis kimia organik, selanjutnya hasil amidasi senyawa N,N-Bis(2-hidroksietil)-3-(4-metoksifenil)akrilamida yang diperoleh diharapkan dapat digunakan sebagai surfaktan dan antimikroba
1.5. Lokasi Penelitian
Penelitian ini akan dilakukan di laboratorium kimia organik F-MIPA USU. Analisa secara spektroskopi FT-IR di laboratorium perusahaan swasta di Medan.
1.6.Metodologi Penelitian
BAB 2
TINJAUAN PUSTAKA
2.1. Tanaman Kencur ( Kaemferia galanga L)
Kencur (Kaempferia galanga L) merupakan tanaman tropis yang banyak tumbuh diberbagai daerah di Indonesia sebagai tanaman yang dipelihara. Tanaman ini banyak digunakan sebagai ramuan obat tradisional dan sebagai bumbu dalam masakan sehingga para petani banyak yang membudidayakan tanaman kencur sebagai hasil pertanian yang diperdagangkan dalam jumlah yang besar. Bagian dari tanaman kencur yang diperdagangkan adalah buah akar yang tinggal didalam tanah yang disebut dengan rimpang kencur atau rizoma (Soeprapto,1986).
Daun kencur berbentuk bulat lebar, tumbuh mendatar diatas permukaan tanah dengan jumlah daun tiga sampai empat helai. Permukaan daun sebelah atas berwarna hijau sedangkan sebelah bawah berwarna hijau pucat. Panjang daun berukuran 10 – 12 cm dengan lebar 8 – 10 cm mempunyai sirip daun yang tipis dari pangkal daun tanpa tulang tulang induk daun yang nyata (Backer,1986).
Rimpang kencur terdapat didalam tanah bergerombol dan bercabang cabang dengan induk rimpang ditengah. Kulit ari berwarna coklat dan bagian dalam putih berair dengan aroma yang tajam. Rimpang yang masih muda berwarna putih kekuningan dengan kandungan air yang lebih banyak dan rimpang yang lebih tua ditumbuhi akar pada ruas ruas rimpang berwarna putih kekuningan.
Klasifikasi Kaempferia galanga L di dalam dunia botani adalah sebagai berikut: Kerajaan : Plantae
Divisi : Spermaiophyta Sob Divisi : Angiospermae Kelas : Monocotyledonae Ordo : Zingiberales Famili : Zingiberaceae Subfamili : Zingiberoideae Genus : Kaempferia
Spesies : Kaempferia .galanga
Nama Kaempferia galanga L di berbagai daerah di Indonesia adalah sebagai berikut: Sumatera : ceuku (Aceh), tekur (Gayo), kaciwer (Karo), cakue (Minangkabau) Cokur (lampung)
Jawa : kencur (jawa), cikur (Sunda), kencor (Madura)
Sulawesi : batako (Manado), watan (Minahsa), (Gorontalo), cakuru (Makasar), ceku (Bugis)
Nusa Tenggara: cekuh (Bali), cekur (Sasak), cekur, (Sumba), sokus (Roti) Sukung (Timor)
2.1.1. Kandungan Kimia dari Kencur
Kandungan kimia rimpang kencur telah dilaporkan oleh Afriastini,1990 yaitu (1) etil sinamat, (2) etil p-metoksisinamat, (3) p-metoksistiren, (4) karen (5) borneol, dan (6) parafin
Diantara kandungan kimia ini, etil p-metoksisinamat merupakan komponen utama dari kencur (Afriastini,1990). Tanaman kencur mempunyai kandungan kimia antara lain minyak atsiri 2,4-2,9% yang terjadi atas etil parametoksi sinamat (30%). Kamfer, borneol, sineol, penta dekana. Adanya kandungan etil para metoksi sinamat dalam kencur yang merupakan senyawa turunan sinamat (Inayatullah,1997 dan Jani, 1993).
pabrik-pabrik jamu maupun dibuat sendiri, rimpang mempunyai khasiat obat antara lain untuk menyembuhkan batuk dan keluarnya dahak, mengeluarkan angin dari dalam perut, bisa juga untuk melindungi pakaian dari serangga perusak, caranya rimpang kering kencur disimpan diantara lipatan-lipatan kain (Afrianstini,1990).
Kencur (Kamferia galanga L) adalah salah satu jenis temu-temuan yang banyak dimanfaatkan oleh rumah tangga dan industri obat maupun makanan serta minuman dan industri rokok kretek yang memiliki prospek pasar cukup baik. Kandungan etil p-metoksisinamat (EPMS) didalam rimpang kencur menjadi bagian yang penting didalam industri kosmetik karena bermanfaat sebagai bahan pemutih dan juga anti eging atau penuaan jaringan kulit (Rosita,2007).
2.2. Senyawa Etil P-Metoksisinamat
Penelitian telah membuktikan kebenaran pengalaman nenek moyang kita bahwa dalam tanaman kencur memang mengandung senyawa tabir surya yaitu etil p-metoksisinamat. Etil p-metoksisinamat (EPMS) adalah salah satu senyawa hasil isolasi rimpang kencur yang merupakan bahan dasar senyawa tabir surya yaitu pelindung kulit dari sengatan sinar matahari. Senyawa tabir surya terutama yang berasal dari alam dirasa sangat penting saat ini dimana tidak hanya wanita saja yang memerlukan perlindungan kulit akan tetapi pria pun memerlukan tabir surya untuk melindungi kulit agar tidak coklat atau hitam tersengat sinar matahari. Kulit dengan perlindungan akan tampak lebih baik dalam hal warna yaitu terlihat lebih bersih dan putih (Barus,2009).
senyawa sebagai tabir surya, selain dari itu juga untuk mengurangi tingkat bahaya terhadap kulit.
EPMS termasuk turunan asam sinamat, dimana asam sinamat adalah turunan senyawa phenil propanoad. Senyawa-senyawa yang termasuk turunan sinamat adalah para hidroksi sinamat (7), 3,4-dihidroksisinamat (8), dan 3,4,5 trimetoksisinamat (9):
EPMS termasuk kedalam senyawa ester yang mengandung cincin benzene dan gugus metoksi yang bersifat nonpolar dan juga gugus karbonil yang mengikat etil yang bersifat sedikit polar sehingga dalam ekstraksinya dapat menggunakan pelarut-pelarut yang mempunyai variasi kepolaran yaitu etanol, etil asetat, metanol, air dan heksana.
Dalam ekstraksi suatu senyawa yang harus diperhatikan adalah kepolaran antara lain pelarut dengan senyawa yang diekstrak, keduanya harus memiliki kepolaran yang sama atau mendekati sama. EPMS adalah suatu ester yang mengandung cincin benzene dan gugus metoksi yang bersifat nonpolar dan mengandung gugus karbonil yang mengikat etil yang bersifat agak polar menyebabakan senyawa ini mampu larut dalam beberapa pelarut dengan kepolaran bervariasi (Taufikhurohmah,2008).
2.2.1. Biosintesa p-metoksisinamat
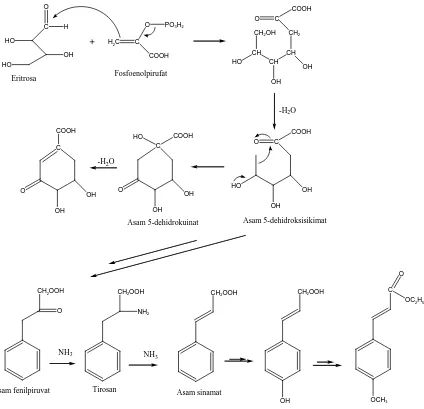
Pembentukan asam shikimat dimulai dengan kondensasi aldol antara suatu tetrosa, yakni eritrosa, dan asam fosfoenolpiruvat. Pada kondensasi ini, gugus metilen C=CH2 dari asam fosfoenolpiruvat berlaku sebagai nukleofil dan beradisi dengan gugus karbonil C=O dari eritrosa, menghasilkan suatu gula yang terdiri dari 7 atom karbon. Selanjutnya, reaksi yang analog (intramolekuler) menghasilkan asam 5-dehidrokuinat yang mempunyai lingkar sikloheksana, yang kemudian diubah menjadi asam shikimat. Reaksi pararel yang sejenis terhadap tirosin yang mempunyai tingkat oksidasi yang lebih tinggi menghasilakn asam p-kumarat.
Senyawa turunan sinamat termasuk senyawa fenolik alam dari golongan fenilpropanoid, yakni senyawa-senyawa dengan kerangka dasar karbon C6-C3,terdiri dari cincin benzen (C6) yang terikat pada ujung dari rantai karbon propan (C3). Dari segi biogenetik senyawa turunan sinamat berasal dari jalur biosintesa asam sikhimat, seperti tercantum dalam gambar 2.1. Karena itu, pola oksidasi cincin benzen pada turunan sinamat adalah sama dengan pola oksidasi pada asam shikimat. Lazimnya cincin benzena ditemukan tersubstitusi oleh satu atau lebih gugus hidroksi atau gugus lain yang ekivalen seperti pada asam p-kumarat dan asam kafeat. Sedangkan kemungkinan lain dari cincin aromatik adalah tidak tersubstitusi sama sekali seperti pada asam sikimat.
O
Gambar 2.1. Jalur asan sikhimat dalam biosintesa fenilpropanoid unruk menghasilkan etil p-metoksisinamat. (Sumber dan Norman,1978)
p-metoksisinamat hasil isolasi menunjukkan konfigurasi trans.dan beberapa ester (Madhatil,1927).
2.3. Amida
Suatu amida ialah senyawa yang mempunyai nitrogen trivalen terikat pada suatu gugus karbonil. Suatu amida diberi nama asam karboksilat induknya, dengan mengubah imbuhan asam…-oat (atau –at) menjadi amida.
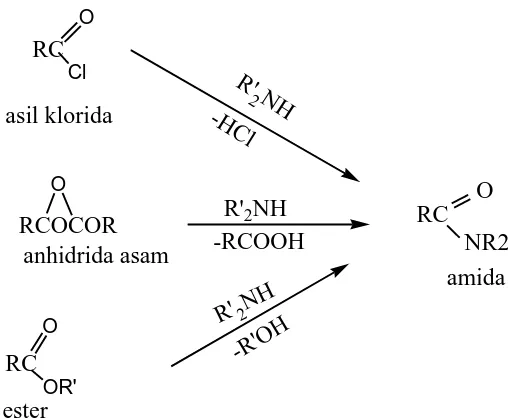
Amida disintesis dari derivat asam karboksilat dan ammonia atau amina yang sesuai gambar 2.2.
Gambar 2.2. Reaksi Umum Sintesis Pembentukan Amida
membentuk suatu ikatan pi dengan karbon karbonil. Pelepasan elektron ini menstabilkan hibrida resonansi (Bresnick,1996).
2.3.1. Reaksi Pembuatan Amida
Amida asam lemak pada industri oleokimia dapat dibuat dengan mereaksikan asam lemak atau metil ester asam lemak dengan suatu amina (Maag,1984). Amida asam lemak dibuat secara sintesis pada industri oleokimia dalam proses batch, dimana ammonia dan asam lemak bebas bereaksi pada suhu 200o C dan tekanan 345-690 kpa selama 10-12 jam. Dengan proses tersebutlah dibuat amida primer seperti lauramida, stearamida serta lainnya.
Amida primer juga dibuat dengan mereaksikan ammonia dengan metil ester asam lemak. Reaksi ini mengikuti konsep HSAB dimana H+ dari ammonia merupakan hard acid yang mudah bereaksi dengan hard base CH3O- untuk membentuk metanol. Sebaliknya NH2- lebih soft-base dibandingkan dengan CH3O- akan terikat dengan R-CO+ yamng lebih soft acid dibandingkan H+ membentuk amida.
R C
Pembuatan amida sekunder dilakukan dengan mereaksikan asam lemak dengan amina.
RCO2H + RNH2 150-200oC RCONHR + H
2O
NaOMe baru dapat terjadi pada suhu 100o-120o C, sedangkan apabila tidak digunakan katalis maka reaksi baru dapat berjalan pada suhu 150o-250o C (Gabriel,1984).
Senyawa N-palmitoyl glisinida yang dihasilkan melalui reaksi amidasi Metil Palmitat dengan Glisin dan di murnikan dengan metode rekristalisasi dari campuran pelarut petroleum benzen:etanol = 1:1 (v/v). Reaksinya sebagai berikut :
H3C (CH)14 C
Sintesis senyawa-senyawa amida turunan etil p-metoksisinamat dilakukan dengan memanfaatkan unit fungsional ester dari molekul etil p-metoksisinamat yang diperoleh dari ekstrak etanol tanaman kencur, sebagai unit kimia yang potensial untuk melangsungkan sintesis. Transformasi melibatkan pemutusan ikatan C-O asil melalui adisi-eliminasi nukleofilik terhadap bentuk antara p-metoksisinamoil klorida oleh suatu seri pereaksi anilin tersubstitusi para, yakni: anilin, p-nitroanilin, p-metoksianilin (p-anisidin) dan p-nitroanilin. Melalui amonolisis p-metoksisinamoil klorida ini, dapat disintesis senyawa amida p-metoksisinamanilida (Nakanishi,1974).
2.3.2. Kegunaan Amida
Amida asam lemak digunakan sebagai bahan pelumas pada proses pembuatan resin, maka amida tersebut digunakan baik sebagai pelumas internal maupun eksternal, amida tersbut berperam mengurangi gaya kohesi dari polimer sehingga meningkatkan aliran polimer pada proses pengolahan (Brahmana,1994).
Amida berperan untuk mempengaruhi polimer yang melebur agar terlepas dari permukaan wadah logam pengolahan resin. Sebagai pelumas internal, amida berperan untuk mengurangi gaya kohesi dari polimer dan meningkatkan aliran polimer pada proses pengolahannya (Reck,1984).
Surfaktan adalah suatu senyawa aktif penurun tegangan permukaan (surfaceactive agent) yang sekaligus memiliki gugus hidrofilik dan gugus hidrofobik dalam satu struktur molekul yang sama. Senyawa ini dapat menurunkan tegangan antarmuka antara dua fasa cairan yang berbeda kepolarannya seperti minyak/air atau air/minyak. Sifat yang unik tersebut, menyebabkan surfaktan sangat potensial digunakan sebagai komponen bahan adhesif, bahan penggumpal, pembasah, pembusa, pengemulsi, dan bahan penetrasi serta telah diaplikasikan secara luas pada berbagai bidang industri proses yang menggunakan sistem multifasa seperti pada industri makanan, farmasi, kosmetika, tekstil, polimer, cat, detergen dan agrokimia.
Alkanolamida yang digunakan untuk formula pangan, kosmetika dan obat obatan haruslah bebas dari bahan beracun, pelarut, asam lemak bebas, amina yang berlebih serta harus tidak berbau dan bentuknya menarik. Namun penelitian untuk memproduksi alkanolamida pada skala industri masih kurang karena penghilangan pelarut dan warna yang tidak diinginkan memerlukan tahapan yang rumit dan biaya yang tinggi (Daniel, 2007).
2.4. Dietanolamina
Dietanolamina adalah senyawa yang terdiri dari gugus amina dan dialkohol. Dialkohol menunjukkan adanya dua gugus hidroksil pada molekulnya. Dietanolamina juga dikenal dengan nama bis (hydroxyethyl)amine, diethylolamine, hydroxtdiethylamine, diolamine dan 2,2-iminodiethanol. Sidat-sifat dietanolamina adalah sebagai berikut :
a. Rumus molekul : C4H11NO2 b. Berat molekul : 105,1364 g/mol c. Densitas : 1,090 g/cm3 d. Titik leleh : 28ºC (1atm) e. Titik didih : 268,8ºC (1atm) f. Kelarutan : H2O, alcohol, eter
Dietanolamina banyak digunakan dalam produk kosmetik dan detergen karena mampu menciptakan tekstur yang lembut dan foaming agent
2.5. Surfaktan
Molekul-molekul atau ion-ion yang teradsorpsi pada pembatasan (interfasa) disebut sebagai bahan aktif permukaan (surface active agents) atau surfaktan (surfactants). Surfaktan mempunyai peran penting untuk menurunkan tegangan permukaan bahanyang dikenai. Penggunaan surfaktan terbagi atas tiga golongan, yaitu sebagai bahan pembasah (wetting agent), bahan pengemusi (emulsifying), dan sebagai bahan penglarut (solubilizing agent). Aktifitas kerja suatu surfaktan karena sifat ganda dari molekul tersebut (Pavia,1976). Molekull surfaktan memiliki bagian polaryang suka akan air dan bagian yang nonpolar yang suka akan minyak/lemak. Bagian polar molekul surfaktan dapat bermuatan positif, negatif ataunetral (Lehninger,1988). Siat rangkap ini yang menyebabkan surfaktan dapat diadsorpsi pada antar muka udara-air, minyak-air dan zat padat-air, membentuk lapisan tunggal dimana gugus hidrofilik berada pada fase air dan rantai hidrokarbon ke udara, dalam kontak dengan zat padat ataupun terendam dalam fase minyak.
Surfaktan turunan asam lemak dengan alkohol merupakan surfaktan nonionik yang banyak digunakan sebagai pengemulsi dalam makanan, sediana farmasi dan kosmetik karena tidak toksis. Emulsi yang dihasilkan umumnya tidak sensitif terdapat pengaruh elektrolit, sehingga yang diperoleh relatif stabil (Meffert,1984).
Penelitian sifat-sifat biologis dari surfaktan termasuk skrining dari efikasi antimikroba dan biodegradabilitas. Asam lemak dari berbagai jenis asam lemak berantai panjang dikenal karena sifat antimikrobanya. Biodegradabilitas dari surfaktan telah menjadi subjek dari berbagai penelitian beberapa tahun belakangan ini sehingga menjadi ketertarikan yang luas dalam pengembangan molekul surfaktan yang memiliki sifat antimikroba dan juga kompatibilitas terhadap lingkungan. Bermacam-macam surfaktan yang telah disintesis dan beberapa diantaranya telah diaplikasikan terutamauntuk kosmetik dan makanan (Sivasamy,2001).
memperpanjang masa simpangnya, yang termasuk dalam golongan surfaktan adalah pengemulsi, penstabil, dan pembasah (Winarno,1997).
Klasifikasi surfaktanbedasarkan muatannya dibagi menjadi empat golongan (Swern,1979) yaitu :
1. Surfaktan anionik yaitu surfaktan yang bagian alkilnya terikat pada suatu anion 2. Surfaktan kationik yaitu surfaktan yang bagian alkilnya terikat pada suatu kation 3. Surfaktan non-ionik yaitu surfaktan yang bagian alkilnya tidak bermuatan
Ester sukrosa asam lemak merupakan salah satu contoh surfaktan non-ionik dengan residu sukrosa sebagai polarnya (Brahmana,1993).
4. Surfaktan amfoter yaitu surfaktan yang bagian alkilnya mempunyai muatan positif dan negatif
Sebagai gambaran untuk perimbangan hidrofil-lipofil bahan-bahan aktif permukaan, dapat digunakan skala keseimbangan hidrofil-lipofil yang sering disebut HLB (Hidrophilic-lipophilic balance) yang ditemukan oleh Grifin (1949). Dengan bantuan harga keseimbangan ini, maka kita dapat membentuk rentang HLB setiap surfaktan secara optimal (gambar 2.3). Makin besar nilai HLB suatu bahan maka bahan tersebut semakin bersifat hidrofilik.
Hubungan antara silai HLB dengan penggunaanya sebagai surfaktan dapat dilihat pada gambar berikut:
Gambar 2.3. Skala Keseimbangan Hidrofil Lipofil (HLB)
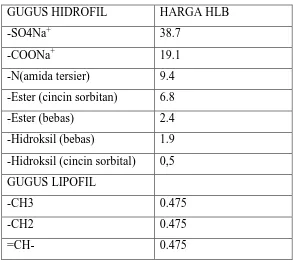
Tabel 2.1. Harga HLB beberapa gugus hidrofilik dan lipofilik
GUGUS HIDROFIL HARGA HLB
-SO4Na+ 38.7
-COONa+ 19.1
-N(amida tersier) 9.4 -Ester (cincin sorbitan) 6.8
-Ester (bebas) 2.4
-Hidroksil (bebas) 1.9 -Hidroksil (cincin sorbital) 0,5 GUGUS LIPOFIL
-CH3 0.475
-CH2 0.475
=CH- 0.475
Bedasarkan harga yang terdapat pada tabel 2.1. diatas dapat ditentukan harga HLB secara teori dengan menggunakan rumus sebagai berikut:
HLB = (gugus hidrofil) – (gugus lipofil) + 7
Harga HLB dapat ditentukan dengan harga CMC (Critical micelle Concentrstion). Harga CMC diperoleh dengan mengunakan alat tensiometer. Kemudian dengan menggunakan rumus berikut maka akan diperoleh harga HLB (Brahmana,dkk,1993).
HLB = 7-0,36 ln (Co/Cn)
Dimana :Cw = Harga CMC Co = 100-Cw
HLB =20 (1-S/A)
Dimana : S = bilangan penyabunan A = bilangan asam
Nilai HLB untuk beberapa bahan dan nilai yang sehubungan dengan tujuan penerapannya tercantum pada tabel 2.2.
Tabel 2.2. Nilai HLB dalam kaitannya dengan kegunaan industri
Kisaran HLB Penggunaan
3-6 7-9 8-18 15-18
BAB 3
METODE PENELITIAN
3.1. Alat-alat
- Neraca Analitik Mettler PM 200
- Perkolator -
- Labu Leher Dua Pyrex
- Labu Takar Pyrex
- Gelas Erlemeyer Pyrex
- Gelas Beaker Pyrex
- Gelas Ukur Pyrex
- Corong Pisah Pyrex
- Corong Saring Pyrex
- Termometer Fisher Scientific
- Buret Pyrex
- Pendingin Bola Jena
- Hotplate Stirer Pisons
- Rotarievaporator Heildolph VV2000
- Tabung CaCl2 -
- Botol Aquades -
- Magnetik Stirer -
- Desikator -
- Spektrofotometer FT-IR Shimadzu
3.2. Bahan-bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah:
- Dietanolamin p.a.E’Merck
- Natrium Metoksida p.a.E’Merck
- Etanol p.a.E’Merck
- Akuades
- Calsium Klorida anhidrous p.a.E’Merck - Natriun Sulfat anhidrous p.a.E’Merck - Kencur
- Metanol p.a.E’Merck
- Kalium Hidroksida p.a.E’Merck
- Indikator Fenolphtalein p.a.E’Merck
3.3. Prosedur Percobaan 3.3.1 Preparasi Sampel
Sebanyak 10 kg kencur dibersihakan dan di kupas sampai kulit dasar terpisah. Kemudian kencur di blender sampai halus, setelah itu kencur yang di blender tersebut diangin-anginkan selama 3-4 harri. Setelah kencur yang dijemur bewana coklat muda dikumpulkan menjadi satu.
3.3.2. Isolasi Etil p-metoksisinamat dari kencur
Sebanyak 400 gram bubuk kencur dimasukkan dalam alat perkolator lalu ditambahkan 500 ml etanol kemudian direndam selama 5 hari. Dikeluarkan ekstrak kencur lalu diuapkan etanolnya dengan mengunakan rotarievaporator. Residu yang diperoleh di diamkan sehingga terbentuk kristal kemudian disaring. Kristal yang di peroleh di rekristalisasi dengan pelarut etanol sehingga dihasilkan kristal putih. Kristal putih yang diperoleh diuji kemurnianya dengan penentuan titik lebur demikian juga pemeriksaan melalaui analisa Kromatografi Lapisan Tipis dengan menggunakan fasa diam silika gel 60F254. Fase gerak yang digunakan adalah campuran n-heksan : etil asetat, terhadap kristal yang di peroleh tersebut dilakukan juga analisa melalui pemeriksaan secara analisa spektroskofi FT-IR.
3.3.3. Amidasi Etil p-metoksisinamat dengan dietanolamin menjadi N,N-bis(2- hidroksietil)-3-(4-metoksifenil) akrilamida
eter dan lapisan eternya di cuci dengan NaCl jenuh, kemudian dikeringkan dengan NaSO4 anhidrous selama 1 jam di dalam desikator. Disaring NaSO4 anhidraus dan diuapkan melalui rotarievaporator. Residu yang diperoleh dilakukaan pemerikasaan melalui analisis Kromatografi Lapisan Tipis (KLT) dengan menggunakan fasa diam silika gel 60F254. Fase gerak yang digunakan adalah campuran n-heksan : etil asetat dan selanjutnya dianalisa dengan spektrosfotometer FT-IR.
3.3.4. Penentuan Nilai Hidrofil Lipofil Balance (HLB) dari Senyawa N,N-bis(2-hidroksietil)-3-(4-metoksifenil) akrilamida
a. Penentuan Bilangan Penyabunan (S)
Sebanyak 1,0 g N,N-bis(2-hidroksietil)-3-(4-metoksifenil) akrilamida ditimbang dan dimasukkan kedalam gelas Erlemeyer 250 ml, kemudian ditambahkan sebanyak 50 ml KOH Alkohol 0,5 N. Labu ditutup dengan gabus karet selanjutnya dipanaskan sampai N,N-bis(2-hidroksietil)-3-(4-metoksifenil) akrilamida larut. Setelah dingin kemudian dititrasi dengan HCl 0,5N menggunakan indikator fenolftalein hingga warna merah muda hilang.Dicatat volume HCl 0,5 N yang terpakai dan dihitung bilangan penyabunan dengan rumus:
Bil.penyabunan = V(blanko - Vtitrasi) x NHCl x 56,1 Massa Sampel (gram)
b. Penentuan Bilangan Asam (A)
dengan KOH 0,02 N menggunakan indikator fenolftalein sampai tepat warna merah muda, Dihitung volume KOH yang dipakai dan dihitung bilangan asam dengan menggunakan rumus:
Bilangan asam= VKOH x NKOHs x 56,1 Massa Sampel (gram)
Harga HLB dapat diperoleh dari bilangan asam dan bilangan penyabunan dengan menggunakan rumus:
− =
A S HLB 20 1
3.4. Bagan Penelitian 3.4.1. Preparasi Sampel
3.4.2. Isolasi Etil p-Metoksisinamat dari Rimpang Kencur
Kristal Putih
Analisa FT-IR
Titik Lebur Analisis KLT
dimasukkan kedalam perkolator
ditambahkan etanol teknis 500 ml direndam selama 4 hari
dirotarievaporasi
dibiarkan hingga terbentuk kristal
disaring
direkristalisasi
400 g bubuk kencur kering
3.4.3. Amidasi Etil p-Metoksisinamat Dengan Dietanolamin
dimasukkan kedalam labu leher dua
ditambahkan 2 gram (0,019 mol) dietanolamin ditambahkan 0,093 mol NaOCH3
dirangkai alat refluks
dipanaskan pada suhu 80-90 oC sambil diaduk selama 5 jam
dirotarievaporasi
dilarutkan di dalam 100 ml dietil eter
dicuci dengan larutan NaCl sebanyak tiga kali masing-masing 25 ml
ditambahkan Na2SO4 anhidrous
didiamkan selama 45 menit disaring
dirotarievaporasi
Residu Destilat
Lapisan atas Lapisan bawah
Filtrat Residu
Campuran
3 gram (0,014 m0l) kristal EPMS
Destilat Rrsidu
3.4.4. Penentuan Nilaai Hidrofil Lifofil Balance (HLB) a. Penentuan Bilangan Penyabunan
b. Penentuan Bilangan Asam
1,0 g N,N-bis(2-hidroksietil)-3-(4-metoksifenil) akrilamida
Ditimbang
Dimasukkan ke dalam gelas Erlemeyer 250 ml
Ditambahkan 50 ml KOH Alkohol 0,5 N
Campuran
Ditutup
Dipanaskan hingga larut
Didinginkan
Ditambahkan 3 tetes indikator penolphtalein
Larutan Merah Muda
Dititrasi dengan HCL 0,5 N hingga warna hilamg
Hasil
1,0 g N,N-bis(2-hidroksietil)-3-(4-metoksifenil) akrilamida
Ditimbang
Dimasukkan ke dalam gelas Erlemeyer 250 ml
Ditambahkan 10 ml Alkohol netral 95%
Campuran
Ditutup
Dipanaskan sambil diaduk hingga larut
Didinginkan
Ditambahkan 3 tetes indikator penolphtalein
Dititrasi dengan KOH 0,02N hingga warna merah muda
BAB IV
HASIL DAN PEMBAHASAN
4.1. Hasil
4.1.1. Isolasi Etil p-Metoksisinamat dari Rimpang Kencur
Etil p-metoksisinamat diisolasi dengan metode perkolasi menggunakan pelarut etanol dan dilanjutkan dengan metode rekristalisasi menghasilkan kristal 1,1% dari berat kencur segar. Hasil titik lebur dari etil p-metoksisinamat sebesar 55-560C. Hasil pemerikasaan melalui analisis Kromatografi Lapis Tipis (KLT) dengan menggunakan fasa diam silika gel 60F254, serta developer campuran n-heksan : etil asetat (Tabel 4.1).
Spektrum FT-IR dari Etil p-metoksisinamat memberikan puncak-puncak serapan kimia pada daerah bilangan gelombang 3008,15,3040 cm-1, 1706,4 cm-1, 1631-1603 cm-1, 2937-2843 cm-1, 1253-1208 cm-1, 1025-1005 cm-1, dan 1420-1290 cm-1 (Lampiran A)
4.1.2. Amidasi Etil p-Metoksisinamat Dengan Dietanolamin N,N-bis(2-hidroksietil)-3-(4-metoksifenil) akrilamida
Hasil analisis spektroskopi FT-IR dari Senyawa N,N-bis(2-hidroksietil)-3-(4-metoksifenil) akrilamida memberikan spektrum dengan puncak-puncak serapan kimia pada daerah bilangan gelombang 3650-3200 cm-1, ester 1253-1208 cm-1, 1630-1510 cm-1, untuk karbonil amida 1642 cm-1, 1604 cm-1, dan 1075-1000 cm-1 (Lampiran B).
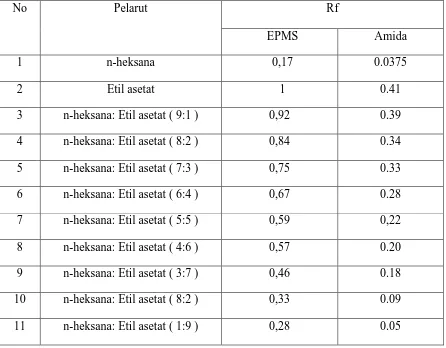
Tabel 4.1.Hasil analisa Kromatografi Lapis Tipis Senyawa Etil p-metoksisinamat hasil isolasai dan senyawa amida hasil sintesis
No Pelarut Rf
EPMS Amida
1 n-heksana 0,17 0.0375
2 Etil asetat 1 0.41
3 n-heksana: Etil asetat ( 9:1 ) 0,92 0.39
4 n-heksana: Etil asetat ( 8:2 ) 0,84 0.34
5 n-heksana: Etil asetat ( 7:3 ) 0,75 0.33
6 n-heksana: Etil asetat ( 6:4 ) 0,67 0.28
7 n-heksana: Etil asetat ( 5:5 ) 0,59 0,22
8 n-heksana: Etil asetat ( 4:6 ) 0,57 0.20
9 n-heksana: Etil asetat ( 3:7 ) 0,46 0.18
10 n-heksana: Etil asetat ( 8:2 ) 0,33 0.09
11 n-heksana: Etil asetat ( 1:9 ) 0,28 0.05
Etil p-metoksisinamat mempunyai banyak gugus seperti benzen, eter, ena, dan ester sehingga dapat larut dalam banyak pelarut seperti ditunjukkan pada tabel 4.2
Pelarut EPMS N,N-bis(2-hidroksietil)-3-(4-metoksifenil) akrilamida
Aquades Tidak larut Tidak larut
Etanol Larut Tidak larut
N-heksan Larut Larut
Kloroform Larut Tidak larut
Benzen Larut Tidak larut
Petrolium Benzen Larut Larut
Etil Asetat Larut Sedikit larut
Aseton Larut Larut
4.2. Pembahasan
4.2.1. Isolasi Etil p-Metoksisinamat dari Rimpang Kencur
Etil p-metoksisinamat diperoleh dari hasil isolasi rimpang kencur melalui metode perkolasi menggunakan pelarut etanol diikuti penguapan dan rekristalisasi sehingga menghasilkan kristal. Kandungan kimia rimpang kencur telah dilaporkan oleh Madhathil dkk (1927) yaitu etil sinamat, etil p-metoksisinamat, p-metoksistiren, karen, borneol, dan paraffin. Etil p-metoksisinamat yang hanya berupa padatan dari semua kandungan kimia dari kencur sehingga etil p-metoksisinamat mudah di isolasi menggunakan pelarut etanol dan juga dapat dimurnikan melalui rekristalisasi oleh pelarut etanol.
Hasil isolasi diananalisis dengan menggunakan spektrofotometer FT-IR. Spektrum hasil analisa FT-IR (Lampiran A) memberikan spektrum dengan puncak serapan pada daerah bilangan gelombang 3008 cm-1 menunjukkan adanya vibrasi strechin C-H sp2 pada aromatik, dan –C=C- (alkena). Puncak serapan pada daerah bilanagan gelombang 2042 dan 1911 cm-1 menunjukan pita kombinasi untuk senyawa aromatik tersubstitusi, yang didukung oleh puncak serapan pada bilangan gelombang 831 cm-1 dan 778 cm-1 yang menunjukkan adanya dua substituen pada aromatik yang tersubstitusi pada posisi para, puncak sama dengan yang terdapat pada literatur yakni pada bilangan gelombang 860-780.(Bieman, 1983).Adanya ikatan rangkap C=C aromatik ditunjukkan oleh bilangan gelombang 1571 cm-1 - 1475 cm-1 . Pita serapan pada bilangan gelombang 1631-1603 menunjukkan vibrasi streching –C=C- rantai terbuka. Puncak serapan pada daerah bilangan gelombang 2937-2981 cm-1 menunjukkan vibrasi streching C-H sp3 yang didukung oleh vibrasi bending C-H sp3 pada 1479-1421 cm-1 dan 1391-1304 cm-1. Puncak serapan pada bilangan gelombang 1706 cm-1menunjukkan vibrasi streching C=O karbonil dari ester, dimana bilangangelombang lebih rendah dari vibrasi streching untuk ester (1735 cm-1), hal ini disebabkan karna adanya konjugasi ikatan rangkap C=C dan C=) sehingga memperpanjang ikatan karbonil, dengan demikian ikatan karbonil menjadi lemah akibat bilangan gelombang semakin kecil. (Silverstein,1962). Hal ini dapat ditunjukkan seperti struktur di bawah ini:
H3CO
ikatan karbonil menjadi lebih panjang sehingga vibrasi semakin keci.
Adanya gugus karbonil didukung oleh vibrasi streching C=O karbonil didukung oleh overton C=O streching pada bilangan gelombang 3380 (Silverstein,1962). Vibrasi streching c-o ester terdiri dari dua puncak yang pertama vibrasi C-(C=O)-O pada bilangan gelombang 1208 cm-1 puncak melebar dan lebih kuat dari pita absorbsi C=O streching. Puncak yang kedua yaitu vibrasi O-C-C pada bilangan gelombang 1025-1005 cm-1 dimana bedasarkan literatur 1064-1000 cm-1 yang tumpang tinding dengan vibrasi streching C-O-C eter.
4.2.2. Amidasi Etil p-Metoksisinamat Dengan Dietanolamin
Amidasi Etil p-metoksisinamat dengan dietanolamin menggunakan katalis NaOCH3 menghasilkan N,N-bis(2-hidroksietil)-3-(4-metoksifenil) akrilamida bedasarkan prinsip HSAB (Hard Soft Acid Base), dimana H+ dari NH merupakan asam yang lebih keras (hard acid) dibandingkan dengan Hα dietanolamin sehingga bereaksi dengan CH3-CH3O -dari etil p-metoksisinamat yang merupakan basa keras (hard base) dan N- dari dietanolamin merupakan basa lunak (soft base) yang mudah bereaksi dengan gugus asil RCO+ dari EPMS yang merupakan asam lunak (soft acid).
Reaksi yang terjadi secara hipotesis adalah :
didukung oleh vibrasi bending O-H pada daerah bilangan gelombang 1642-1604 cm-1 dimana puncak pada bilangan gelombang tersebut tumpang tindih dengan vibrasi streching C-N terbentuknya amida ini ditandai dengan hilangnya vibrasi C-O-C ester pada bilangan gelombang 1253-1208 cm-1, serapan pada daerah bilanga gelombang 2940-2580 cm-1 menunjukkan vibrasi steching C-H sp3 yang didukung oleh vibrasi bending pada bilangan gelombang 1464 cm-1 dan 1366 cm-1, serapan pada daerah bilangan gelombang 1075-1000 cm-1 menunjukkan adanya gugus C-O, serapan pada daerah bilangan gelombang 1235-1210 cm-1 menunjukan adanya gugus C-O-C, serapan pada daerah bilangan gelombang 1630-1510 cm-1 menunjukkan adanya gugus N-C-O, berubahnya serapan pada daerah bilangan gelombang 1706,4 cm-1 adanya gugus C=O ester menjadi serapan pada daerah bilangan gelombang 1642 cm-1 menunjukkan vibrasi steching dari gugus C=O untuk karbonil amida.
Pembuatan senyawa N,N-bis(2-hidroksietil)-3-(4-metoksifenil) akrilamida melalaui reaksi amidasi diatas dengan bahan dasar Etil p-metoksisinamat dengan dietanolamin menggunakan dietanolamin yang berlebih karena dietanolamin mudah dipisahkan, pemurniannya dilarutkan dengan dietil eter dan dicuci dengan NaCl jenuh dikeringkan dengan NaSO4 anhidrous.
Senyawa N,N-bis(2-hidroksietil)-3-(4-metoksifenil) akrilamida juga ditentukan harga HLB dengan menggunakan metode titrasi dengan menentukan bilangan penyabunan (S) dan bilangan asam (A)
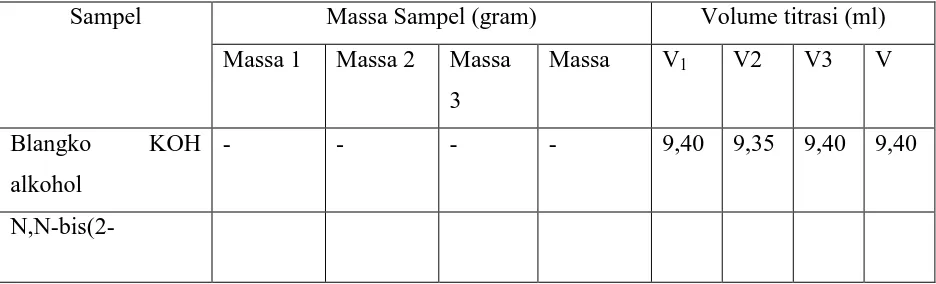
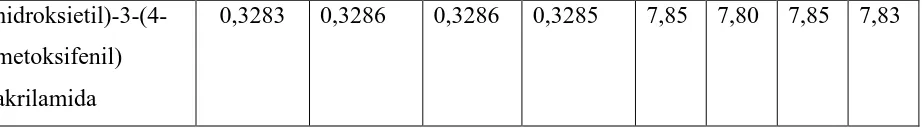
Tabel 4.3.Hasil Penentuan Bilangan Penyabunan Dengan Metode Titrasi
Sampel Massa Sampel (gram) Volume titrasi (ml)
hidroksietil)-3-(4-metoksifenil) akrilamida
0,3283 0,3286 0,3286 0,3285 7,85 7,80 7,85 7,83
Tabel 4.4.Hasil Penentuan Bilangan Asam Dengan Metode Titrasi
Sampel Massa Sampel (gram) Volume titrasi (ml) Massa 1 Massa 2 Massa 3 Massa V1 V2 V3 V
N,N-bis(2- hidroksietil)-3-(4-metoksifenil) akrilamida
0,3078 0,3079 0,3078 0,3078 5,90 5,90 6,00 5,93
Kemudian untuk mencari nilai HLB dapat dihitung dengan menggunakan rumus:
HLB = 20 S
A
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
1. Etil p-metoksisinamat dapat diisolasi dari kencur dengan menggunakan metode perkolasi dengan pelarut etanol menghasilkan 1,1% dari berat kencur segar.
2. Senyawa N,N-bis(2-hidroksietil)-3-(4-metoksifenil) akrilamida dapat dihasikan melalui amidasi etil p-metoksisinamat dengan dietanolamin dengan rendemen sebesar 27,93% selanjutnya dari pennetuan nilai HLB (Hydrophylic Lipophylic Balance) diperoleh sebesar 15,03
5.2. Saran
Daftar Pustaka
Afriastini.J.J. 1990. Bertanam Kencur. Wakarta Penebar Swadaya. Jakarta
Backer. C. A. R. C. B. Van den Briak.1968. Flora of Java. Vol 2. Walters Noordhoff.N.V. Groningen. P. 33
Barus,R.2009. Amidasi Etil p-metoksisinamat yang Diisolasi Dari Kencur. Thesis Pasca Sarjana USU. Medan
Belitz,H.D and Grosch,w. 1986. Food Chemistry.Berlin: Heidelberg Springer Verlag.
Brahmana,H.R. 1991. Sintesis Ester Sukrosa Asam Lemak Dari Beberapa Minyak Yang Dapat Digunakan Sebagai Pengemulsi Dalam Bahan Makanan Dan Kosmetik.
Lembaga Penelitian USU. Medan
Fessenden. R. J. Dan J. Fessenden.1999. Kimia Organik. Edisi Ketiga. Jilid 2.Jakarta: Erlangga
Hamida. L HJ.2007. Seni Tanaman Rempah Kencur. CV. Habsa Jaya. Bandung Hart. H.2003. Kimia Organik. Edisi Kesebelas. Erlangga. Jakarta
Inayatullah. M. S.1997. Standarisasi Rimpang Kencur dengan Parameter Etil Para Metoksi sinamat. Skripsi Fakultas Farmasi Universitas Erlangga.Surabaya
Jani.1993.Uji Aktifitas Tabir Matahari Senyawa Para Metoksi Transinamat dari Rimpang Kencur (Kaempferia Galanga Linn). Skripsi Fakultas Farmasi Universitas. Surabaya
Lehninger,A.L. 1988. Dasar-Dasar Biokimia. Jilid 1. Jakarta : Erlangga
Madhatil,P. 1927. Essential Oil from the Rhizoma of Kaempferia Galanga Linn.Chemical Abstracts.
Meffert,A. 1984. Technical Unes Of Fatty Acid Ester.J.Am.Oil.Chem.Soc.61.255. Nakanishi, K.1474. Natural product Chenistry. Vol I. Tokyo:Kodansha Ltd.
Naibaho,M. 2008. Sintesis N-Palmitoil Glisinida Melalui Amidasi Meril Palimita Dengan Glisin.Skripsi Fakultas MIPA USU.Medan
Rosita. S. M. D. O. Rostiana dan W. Haryudin.2006. Respon Kencur (Kaempferia Galanga Linn) Terhadap Pemupukan. Prosiding Seminar Nasional dan Pemeran Tumbuhan obat Indonesia XXVIII
Soeparto. S.1986. Jamu Jawa Asli. Pustaka Sinar Harapan. Jakarta.
Swern,D.B. 1982. Bailey’s Industrial Oil and Fat Product. Vol 2.4. New York : John Wiley and Sons.
Taufikurohmah. T. Rusmini. Nurhayati.2008. Pemilihan Pelarut Optimasi Suhu Pada Isolasi Senyawa Etil Para Metoksi Sinamat (EPMS) Dari Rimpang Kencur Sebagai Bahan Tabir Surya Pada Industri Kosmetik, (online), (http:www.google.com, diakses 7 november 2009).
LAMPIRAN
1.Penentuan bilangan Penyabunan dari Hasil Titrasi N HCl = 0,1
BM KOH = 56.1
Bilangan Penyabunan =
(Vol.Blangko - Vol.Titrasi) x N HCl x BMKOH
Massa Sampel
=
(9,40-7,85) x 0,1 x 56,1
0,3285
= 26,81
2.Penentuan Bilangan Asam dari Hasil Titrasi N KOH = 0,1
1. Pembuatan Larutan HCl 0,1 N
Diukur sebanyak 2,07 ml larutan HCl 37%, lalu diencerkan dengan akuades dalam labu takar 250 ml sampai garis batas dan distandarisasi dengan menggunakan larutan Na2CO3 0,1 N..
2. Pembuatan Larutan Na2CO3 0,5 N
Sebanyak 6,625 gram Na2CO3 dilarutkan dengan aquades dalam labu takar 250 ml sampai garis batas.
3. Pembuatan Larutan KOH-Alkohol 0,5 N
Ditimbang KOH sebanyak 7,0125 gram dan dilarutkan dengan alkohol dalam labu takar 250 ml sampai garis batas dan distandarisasi dengan menggunakan larutan H2C2O4 0,1 N dan indikator fenolptalein
4. Pembuatan Larutan KOH 0,1 N
Ditimbang KOH sebanyak 1,4 gram dan dilarutkan dengan akuades dalam labu takar 250 ml sampai garis batas dan distandarisasi dengan menggunakan larutan H2C2O4 0,1 N indikator fhenolptalen
5. Pembuatan Larutan KOH 0,02 N
Diukur sebanyak 50 ml larutan KOH 0,1 N dan diencerkan dalam labu takar 250 ml dengan menggunakan akuades batas.
6. Pembuatan Larutan H2C2O4 0,1 N
Ditimbang 1,575 gram H2C2O4.2H2O dimasukkan kedalam labu takar 250 ml dan diencerkan dengan akuades sampai garis batas.
Ditimbang 1 gram Fenolptalein dan dilarutkan dengan alkohol dalam labu takar 100 ml.
8. Pembuatan Alkohol Netral