i
KEMAMPUAN BAKTERI ENDOFIT PENGHASIL ASAM INDOL
ASETAT DAN PENGARUHNYA TERHADAP SERANGAN VIRUS
GEMINI PADA TANAMAN CABAI
(Capsicum annum
L.
)
RINA NOVIANTI
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
iii
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi berjudul Kemampuan Bakteri Endofit Penghasil Asam Indol Asetat dan Pengaruhnya terhadap Serangan Virus Gemini pada Tanaman Cabai (Capsicum annum L.) adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
ABSTRAK
RINA NOVIANTI. Kemampuan bakteri endofit penghasil asam indol asetat dan pengaruhnya terhadap serangan virus gemini pada tanaman cabai (Capsicum annum L.). Dibimbing oleh SYAMSUL FALAH dan IFA MANZILA.
Produksi cabai di Indonesia menurun karena adanya virus gemini yang menyerang tanaman cabai. Penyakit ini ditularkan oleh serangga vektor yaitu kutu kebul (Bemisia tabaci). Salah satu metode yang dapat digunakan untuk meningkatkan ketahanan tubuh terhadap infeksi virus adalah dengan pemberian bakteri endofit atau biasa disebut dengan Plant Rrowth Promoting Rhizobacteria (PGPR) yang menghasilkan hormon AIA (Asam Indol Asetat). Hormon AIA berfungsi sebagai pemacu pertumbuhan dan ketahanan tanaman. Tujuan dari penelitian ini adalah untuk menguji kemampuan 50 isolat bakteri endofit dalam menghasilkan hormon AIA dan menganalisis pengaruhnya terhadap pertumbuhan tanaman cabai yang terserang virus gemini. Rancangan percobaan yang digunakan dalam penelitian ini adalah faktorial RAL dengan tiga perlakuan konsentrasi AIA yang berbeda dan perlakuan dua varietas dari tanaman cabai. Percobaan ini diulang sebanyak lima kali. Hasil penelitian menunjukkan pemberian konsentrasi AIA dapat mengurangi tingkat serangan virus gemini pada tanaman cabai dan meningkatkan pertumbuhan.
Kata kunci: cabai, bakteri endofit, hormon AIA, Plant Growth Promoting Rhizobacteria, virus gemini.
ABSTRACT
RINA NOVIANTI. The ability of endophytic bacteria producing indole acetic acid and its effect on virus attacks gemini in chili (Capsicum annuum L.). Supervised by SYAMSUL FALAH and IFA MANZILA.
Production of red chilli in Indonesia decreased because of gemini virus disease. The disease is transmitted by Bemisia tabacias insect vector. One of possibility methods is to improve plant resistancecan be supported byendhopytic bacteria or Plant Growth Promoting Rhizobacteria (PGPR) which can produce IAA (Indole Asetic Acid) hormone. IAA hormone can serves as a growth promoter and plant resistance. The aims of this research are to test the effect of 50 isolates endhopytic bacteria producing hormones in the IAA and analyze the effect on growth of chilli plants that Gemini virus. The experimental design was factorial randomize complete block design which three AIA treatment and two variety of chilli treatments as factors. These treatments were replicated in five blocks. The results showed that infection by Gemini virus could reduce and increase plant growth.
iii
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Biokimia
KEMAMPUAN BAKTERI ENDOFIT PENGHASIL ASAM INDOL
ASETAT DAN PENGARUHNYA TERHADAP SERANGAN VIRUS
GEMINI PADA TANAMAN CABAI
(
Capsicum annum
L
.
)
RINA NOVIANTI
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
v
Judul Skripsi : Kemampuan Bakteri Endofit Penghasil Asam Indol Asetat dan Pengaruhnya dalam Mengendalikan Virus Gemini pada Tanaman Cabai (Capsicum annum L.)
Nama : Rina Novianti NIM : G84090040
Disetujui oleh
Dr Syamsul Falah, SHut MSi Pembimbing I
Dr Ifa Manzila, MSi Pembimbing II
Diketahui oleh
Dr Ir I Made Artika, MAppSc Ketua Departemen Biokimia
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Judul yang dipilih dalam penelitian ialah “Kemampuan Bakteri Endofit Penghasil Asam Indol Asetat dan Peengaruhnya dalam Mengendalikan Virus Gemini pada Tanaman Cabai (Capsicum annumL.)”.Penelitian ini dilaksanakan dari bulan Februari hingga Agustus 2013 bertempat di Balai Besar Penelitian dan Pengembangan Bioteknologi dan Sumberdaya Genetik Pertanian (BB-Biogen).
Terima kasih penulis ucapkan kepada Dr Syamsul Falah, SHut MSi dan Dr Ifa Manzila, MSi selaku pembimbing, serta Ibu Pipit, Ibu Susi yang telah banyak memberi saran. Di samping itu, ungkapan terima kasih juga disampaikan kepada Ibu Bintang, Ibu Suryani, Pak Zainal dan seluruh dosen Departemen Biokimimia serta ayah, ibu, seluruh keluarga, Azka Rabbani, teman-teman Biokimia 46 dan Biokimia 47atas segala do’a dan kasih sayangnya.
Semoga karya ilmiah ini bermanfaat.
DAFTAR ISI
DAFTAR TABEL vi
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vi
PENDAHULUAN 1
METODE 2
Waktu dan Tempat Penelitian 2
Bahan 2
Alat 2
Prosedur Penelitian 2
HASIL DAN PEMBAHASAN 5
Hasil 5
Pembahasan 11
SIMPULAN DAN SARAN 16
Simpulan 16
Saran 16
DAFTAR PUSTAKA 16
LAMPIRAN 19
DAFTAR GAMBAR
1 Variasi gejala infeksi virus yang menyerang tanaman cabai 7 2 Variasi gejala infeksi virus yang menyerang tanaman cabai Jatilaba 7 3 Variasi gejala infeksi virus yang menyerang tanaman cabai Landung 8 4 Pengaruh konsentrasi AIA terhadap berbagai parameter pertumbuhan
tanaman cabai Jatilaba 9
5 Pengaruh konsentrasi AIA terhadap berbagai parameter pertumbuhan
tanaman cabai Landung 9
6 Hasil panen buah berbagai tanaman cabai varietas Jatilaba dan Landung 10 7 Pengaruh konsentrasi AIA terhadap kandungan klorofil tanaman 11 8 Pengaruh konsentrasi AIA terhadap ekspresi gen ketahanan dan
pertumbuhan 15
DAFTAR LAMPIRAN
1 Diagram Alir Penelitian 19
2 Pembuatan pereaksi 19
3 Pengukuran absorbansi standar dan contoh perhitungan konsentrasi AIA 22
4 Perhitungan intensitas serangan 27
5 Hasil uji duncan terhadap perlakuan konsentrasi AIA tanaman cabai 28
DAFTAR TABEL
PENDAHULUAN
Tanaman cabai memiliki nilai ekonomis yang baik sehingga mendapat prioritas untuk dikembangkan (DJPTPH 2002). Produktivitas cabai di Indonesia masih sangat rendah, berdasarkan data Badan Pusat Statistik dan Direktorat Jenderal Holtikultura 2012 produktivitas cabai saat ini hanya mencapai 7,94 ton/ha. Jumlah ini tidak sebanding dengan produktivitas yang bisa kita raih.Potensi produktivitas cabai bisa kita raih seharusnya dapat mencapai 10 ton/ha (Setiadi 2007).
Salah satu faktor penyebab rendahnya produksi cabai ialah tidak optimalnya pertumbuhan tanaman karena lahan yang digunakan berupa lahan kering dan tingkat kesuburannya relatif rendah yang mendominasi di Indonesia (Timmusk 2003). Adapun faktor penting lain yang menyebabkan rendahnya produksi cabai adalah gangguan hama dan infeksi penyakit berupa patogen maupun virus (Duriat 2009).
Beberapa penyakit yang menyerang tanaman cabai diantaranya adalah antraknosa, bercak daun cercospora, bercak phytophthora, layu fusarium, layu bakteri, dan penyakit yang disebabkan oleh infeksi virus.Infeksi virus yang banyak menyerang tanaman cabai adalah virus gemini. Tanda serangan virus gemini ini adalah berupa daun yang menguning dan ukuran daun menjadi kecil. Virus gemini ini dapat ditularkan melalui tiga cara penularan yaitu inokulasi mekanis, penyambungan dan serangga vektor yaitu Bemisia tabaci.
Salah satu alternatif untuk mengendalikan serangan virus dan memperbaiki pertumbuhan tanaman yang terserang virus gemini adalah dengan menggunakan bakteri endofit penghasil AIA. Menurut Hallman (2001), Bakteri endofit dapat berpengaruh pada kesehatan tanaman terutama dalam hal antagonisme langsung, menginduksi ketahanan sistematik, dan meningkatkan toleransi tanaman terhadap tekanan biotik dan abiotik lingkungan. Bakteri tersebut mulai dipelajari untuk untuk keperluan industri dan pertanian.
Bakteri endofit merupakan bakteri yang hidup di tanah dan berkolonisasi dengan akar. Bakteri endofit juga berperan sebagai pemacu pertumbuhan tanaman yang disebut PGPR. Bakteri endofit ini dapat meningkatkan ketahanan tanaman inang terhadap serangan hama dan patogen. Hal ini dimungkinkan karena beberapa bakteri dapat masuk ke bagian dalam dari akar tanaman, berasosiasi dengan tanaman dan memicu pengaktifan gen pertumbuhan, gen ketahanan dan berperan dalam proses apoptosis dan autofagi. Selain itu bakteri ini juga dapat memfiksasi nitrogen dari dalam tanah sehingga nutrisi tanaman tetap terjaga. Mekanisme bakteri endofit dalam menginduksi ketahanan adalah dengan menstimulasi tanaman untuk meningkatkan produksi senyawa metabolit yang berperan dalam ketahanan tanaman tersebut yaitu dengan hormon AIA (Ryu dan Kloepper 2004).
2
METODE
Waktu dan Tempat Penelitian
Penelitian dilaksanakan mulai bulan Februari hingga Agustus 2013. Bertempat di laboratorium Mikrobiologi dan Biokimia, Balai Besar Penelitian dan Pengembangan Bioteknologi dan Sumberdaya Genetik Pertanian, Jalan Tentara Pelajar No.3A, Bogor.
Bahan
Bahan-bahan yang digunakan dalam penelitian ini antara lain bibit cabai varietas Landung dan Jatilaba, isolat bakteri endofit asal Bali dan Jember koleksi dari BB Biogen (Lampiran 3), serangga vektor Bemicia tabaci, larutan standar AIA 1000 mgL-1, pereaksi Salkowski, medium LB (Luria Bertani)/NB (Nutrient Broth), KH2PO4, Na2HPO4, MgSO4.7H2O, CaCl2.2H2O, FeSO4.7H2O, MnSO4.H2O, Na2MoO4.H2O, H2SO4, Na2HPO4.2H2O, NaCl2, glukosa, L-triptofan dan yeast ekstrak.
Alat
Alat-alat yang digunakan dalam penelitian ini antara lain berbagai macam peralatan gelas. Peralatan pendukung yaitu shaker, autoklaf, mikropipet, tip mikro, alumunium foil, kapas, magnetik stirer, inkubator, Vortex, Waterbath, sentrifus, Spectrophotometer UV-Visible Hitachi U-2800, refrigerator, polybag, membran milipor, autoklaf, neraca analitik Pricisa XR-3054, microsyringe, jarum ose, dan Refrigerator.
ProsedurPenelitian
Peremajaan Isolat Bakteri Endofit dan Penumbuhan Isolat Bakteri Endofitik (Iacobellis et al. 2009)
Sebanyak 50 isolat bakteri endofit diinokulasikan dari stok kultur yang tersedia ke dalam media NA (Nutrient Agar) miring berupa 5 g NaCl, 10 g pepton dan 10 g ektrak daging sapi dalam 1 L akuades. Kemudian digoreskan secara zigzag. Proses peremajaan dilakukan secara steril di ruang laminar. Selanjutnya bakteri diinkubasi selama kurang lebih 2 hari pada suhu ruang. Setelah terlihat pertumbuhan bakteri, isolat yang sudah diremajakan disimpan dan diawetkan pada ruang dingin (refrigerator) 40C.
Penumbuhan isolat bakteri endofit dilakukan dengan cara serbuk triptofan sebanyak 2 g yang dilarutkan ke dalam 100 mL akuades steril, disterilisasi dengan saringan milipore 0.2 µm. Larutan tersebut dimasukkan kedalam tabung ulir yang berisi 9 mL media NB steril sebanyak 1 mL secara aseptik.
Analisis Kuantitatif Asam Indol Asetat (Patten dan Glick 2002)
Isolat yang diuji didapatkan dari beberapa daerah asal Bali dan Jember koleksi jangka panjang BB-Biogen. Jumlah isolat yang diuji ada 50 isolat. Pengukuran kandungan AIA yang dihasilkan oleh isolat-isolat tersebut dilakukan menggunakan pereaksi Salkowski yang mengacu pada prosedur Patten dan Glick (2002).
Bakteri ditumbuhkan dalam medium NB selama 24 jam dengan shaker incubator (1500 rpm pada suhu ruang). Setelah inkubasi, 100 l kultur diinkubasi ke dalam 10 ml medium minimum salt yang sudah ditambahkan dengan 5 mM L-triptofan. Bakteri ditumbuhkan kembali selama 48 jam dengan shaker incubator. Kultur disentrifus pada kecepatan 8000 rpm pada suhu 4°C selama 10 menit, supernatan yang merupakan sumber AIA dipisahkan. Sebanyak 1 mL supernatan dipipet ke dalam tabung reaksi bersih lalu ditambahkan dengan 2 mL pereaksi Salkowski. Campuran supernatan dan pereaksi dikocok dan diinkubasi selama 25
menit, kemudian ukur absorbansinya pada =530 nm.
Pembuatan larutan standar AIA dilakukan dengan konsentrasi 0.2, 1.0, 5.0, 15.0, 20.0, 25.0, 30.0, 35.0, 40.0, 45.0 mgL-1 dari larutan stok AIA 100 mgL-1. Setelah ditambahkan masing-masing 1 mL larutan standar dengan 2 mL pereaksi Salkowski, larutan dikocok dan diinkubasi selama 25 menit. Ukur absorbansi larutan standar dikurangi absorbansi blanko kurva standar menyatakan hubungan konsentrasi AIA (x) dan absorbansi sampel (y) dengan persamaan regresi y = a+bx.
Konversikan nilai absorbansi sampel (y) menjadi konsentrasi AIA (x) menggunakan persamaan kurva standar AIA:
� � ����=( − )
Keterangan : y = Absorbansi Contoh a = Intersep
b = Slope
Uji Pengaruh Bakteri Penghasil AIA terhadap Pertumbuhan Tanaman Cabai
Aplikasi Bakteri Endofit Penghasil AIA ke dalam Tanaman Cabai (Harni et al.2007). Bibit cabai varietas Jatilaba (A) dan Landung (B) direndam dengan air panas 40°-50°C selama 10 menit yang kemudian dipindahkan ke atas kertas saring, setelah itu bibit ditanam ke dalam polybag. Cabai ditumbuhkan selama tiga minggu kemudian diaplikasikan dengan pemberian PGPR. Isolat bakteri endofit yang telah terpilih dibiakkan dalam media LB cair selama 24 jam pada suhu28°C kecepatan 130 rpm sebagai starter, kemudian isolat bakteri tersebut diambil kembali 5 mL untuk ditumbuhkan pada media LB satu liter kemudian pada kecepatan 130 rpm suhu 28°C selama 24 jam. Sebanyak 5 mL bakteri dengan konsentrasi yang telah dipilih tersebut ditambahkan pada tanaman dengan cara menyiramkannya pada tanah dekat dengan perakarannya kemudian dilakukan penularan virus gemini dengan serangga vektor Bemisia tabaci.
4
dari Cikabayan. Serangga dibiakkan pada tanaman sehat dalam kurungan ( terbuat dari plastik dan kain kasa). Serangga imago diberi periode makan akuisisi pada tanaman sakit selama 24 jam. Umur tanaman uji pada saat penularan dilakukan adalah 3 minggu setelah tanam. Setelah itu serangga tersebut dipindahkan ke tanaman uji sebanyak sepuluh ekor serangga per tanaman untuk diberikan periode inokulasi selama 24 jam dengan cara menyungkup tanaman dengan gelas plastik yang sudah dibolongi. Setelah melalui periode makan inokulasi serangga dimusnahkan satu per satu agar tidak menyebar dan menyerang tanaman lain.
Pengamatan dilakukan dengan mengukur masa inkubasi virus, kejadian penyakit dan gejala virus yang menyerang tanaman cabai dan intensitas serangannya.
Intensitas Serangan (Suganda et al.2002). Pengamatan intensitas serangan virus dilakukan setelah aplikasi. Intensitas infeksi virus pada tanaman cabai ditentukan dengan menggunakan rumus (Suganda 2002)
I =
�� x 100 %
Keterangan: I = Intensitas serangan (%); n = Tanaman yang menunjukkan gejala pada perlakuan tertentu; v = Nilai skala pada tiap tanaman; N = Jumlah tanaman yang diamati; dan Z = Nilai skala tertinggi. Nilai skala yang digunakan adalah 0: tidak ada serangan; 1:satu daun terserang; 2:dua-tiga daun terserang; 3: semua daun terserang kecuali dua dan tiga daun pucuk; 4: semua daun terserang atau menguning; dan 5: tanaman mati.
Analisis Klorofil (Sumendaet al. 2011)
Helaian daun tiap sampel diambil sebanyak 1 gram, dihaluskan dan diekstraksi dengan alkohol 95% sampai semua klorofil terlarut. Ekstrak disaring dan supernatan ditampung dalam labu ukur 100 mL, lalu ditambahkan alkohol 95% sampai 100 mL. Ekstrak dipindahkan ke dalam tabung reaksi, dan dimasukkan ke dalam termos yang berisi es. Kandungan klorofil diukur dengan spektrofotometer pada 64λ dan 665 nm. Kadar klorofil total dihitung dengan rumus Wintermans dan de Mots dalam Dahlia (2001) :
Klorofil Total (mgL-1) = 20 (OD649) + 6,1 (OD665) Keterangan: OD (optical density) = nilai absorbansi klorofil
Analisis Statistik Hasil Pengamatan (Matjik dan Sumertajaya 2002)
Yij= µ + τi+ εij
dimana : i = 1, 2, 3, dan 4 (jumlah perlakuan) j = 1, 2, dan 3 (jumlah ulangan)
µ = rataan umum
τi = pengaruh perlakuan ke-i
εij= pengaruh perlakuan ke-i ulangan ke-j
Uji lanjut dilakukan dengan menggunakan uji ANOVA dan uji Duncan. Uji Anova digunakan untuk melihat dalam perlakuan yang diberikan terdapat perbedaan atau tidak. Uji Duncan biasa dilakukan untuk membandingkan perbedaan setiap perlakuan tanpa memperhatikan jumlah perlakuan.
HASIL DAN PEMBAHASAN
Hasil
Peremajaan dan Penumbuhan Isolat Bakteri Endofit
Sebanyak 50 isolat bakteri endofit berhasil diremajakan dan ditumbuhkan. Koloni bakteri tersebut berwarna kuning dan putih. Bakteri yang telah diremajakan diuji kandungan AIA-nya secara kuantitatif. Sebanyak tiga bakteri dipilih berdasarkan konsentrasi yaitu tinggi (92.7 mgL-1), sedang (26.7 mgL-1) dan rendah (8.3 mgL-1) yang selanjutnya digunakan untuk dilihat keefektifannya dalam mengendalikan virus gemini pada tanaman cabai. Peremajaan dan penumbuhan isolat bakteri endofit ini dilakukan sebagai upaya untuk mempertahankan sifat alami bakteri yang diisolasi agar hasil analisis kandungan AIA dalam isolat ini lebih optimal.
Analisis Kuantitatif Uji Penghasil IAA
Hasil pengukuran konsentrasi menunjukan adanya variasi kemampuan bakteri dalam menghasilkan AIA. Pada Tabel 1 menunjukkan hasil analisis yang dilakukan pada 50 isolat diketahui bahwa sebanyak 31 isolat menghasilkan AIA dengan konsentrasi yang berbeda.
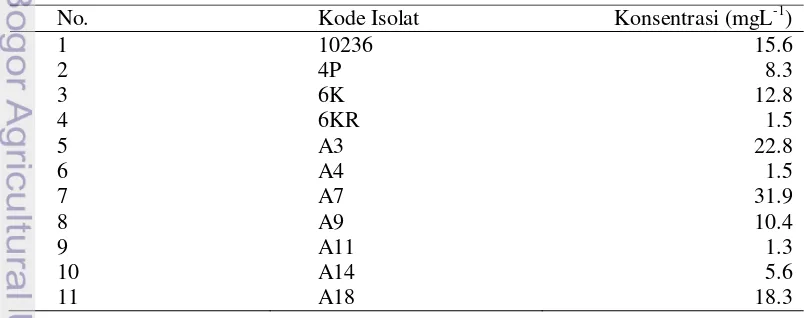
Tabel 1 Nilai konsentrasi 31 isolat bakteri endofit penghasil AIA
6
Tabel 1 Nilai konsentrasi 31 isolat bakteri endofit penghasil AIA (lanjutan)
No. Kode isolat Konsentrasi (mgL-1) menghasilkan AIA dengan konsentrasi terendah diperoleh dari isolat 6KR yaitu 1.5 mgL-1 sedangkan yang tertinggi adalah isolat PTB C14 yaitu 92.7 mgL-1. Berdasarkan data diatas dipilih 3 isolat dengan konsentrasi AIA tertinggi, sedang dan rendah yang akan diaplikasikan pada tanaman. Isolat dengan konsentrasi AIA tertinggi adalah isolat PTB C14 dengan konsentrasi 92,7 mgL-1. Isolat dengan konsentrasi sedang adalah PTB C13 dengan konsentrasi 26,7 mgL-1 dan isolat dengan konsentrasi rendah adalah 4P dengan konsentrasi 8.3 mgL-1. Isolat yang dipilih selanjutnya diujikan terhadap tanaman cabai yang diinfeksikan dengan virus gemini.
Penularan virus dengan Bemisia tabaci
Pada Tabel 2 berikut merupakan hasil penularan virus dengan berbagai konsentrasi AIA yaitu konsentrasi tinggi 92.7 mgL-1, konsentrasi sedang 26.7 mgL-1dan konsentrasi rendah 8.3 mgL-1. Varietas yang digunakan adalah varietas Jatilaba (A) dan varietas Landung (B). Parameter yang diamati berupa masa inkubasi virus, kejadian penyakit dan gejala virus menyerang tanaman cabai.
Tabel 2 Data Penularan Virus dengan Berbagai Konsentrasi AIA
No Perlakuan Aplikasi Bakteri Masa Inkubasi
Ket :A1 = Jatilaba konsentrasi AIA tinggi; A2: Jatilaba konsentrasi AIA sedang; A3 = Jatilana konsentrasi AIA rendah; A4 = Jatilaba konsentrasi AIA nol; B1 = Landung konsentrasi AIA tinggi; B2 = Landung konsentrasi AIA sedang; B3 = Landung konsentrasi AIA rendah; B4 = Landung konsentrasi AIA nol; Ji = Jumlah tanaman bergejala; Jn = Jumlah tanaman yang diinokulasi; Kn = kuning; Knr = Kuning ringan; Dk = Daun berkerut; Mlf = Malforasi; Kd = Kerdil
Gejala infeksi yang terjadi pada tanaman dalam berbagai perlakuan tidak memberikan respon yang berbeda jauh. Gejala infeksi virus gemini ini menyebabkan daun tanaman mengkerut, berwarna kuning, perubahan bentuk daun (malforasi), daun berkerut dan ukuran lebih kecil seperti yang terlihat pada Gambar 1. Gejala tersebut cukup jelas terlihat pada kontrol. Gejala yang terlihat pada tanaman yang diberi perlakuan konsentrasi AIA tinggi dan sedang yaitu berupa gejala ringan yang terlihat pada beberapa daun yang mengkerut saja dan satu atau dua daun yang menguning ringan.
Berdasarkan masa inkubasi, kejadian penyakit, dan gejala yang muncul dapat disimpulkan bahwa masing-masing perlakuan memiliki tingkat virulensi yang berbeda. Hal tersebut dapat dilihat pada Gambar 2 dan 3. Pada tanaman perlakuan konsentrasi AIA rendah terdapat beberapa daun yang berwarna kuning.Pemberian AIA pada tanaman cabai dapat menghambat masa inkubasi virus, kejadian penyakit dan mengurangi gejala tanaman yang terinfeksi.
Gambar 1 Variasi gejala infeksi virus yang menyerang tanaman cabai A) Daun menguning, B) Daun berkerut, C) Daun menguning pada bagian pucuk, D) Perubahan bentuk daun (malforasi)
C D
8
Gambar 2 Variasi serangan virus yang menyerang tanaman cabai A) A1, B) A2,C) A3, D) A4
Gambar 3 Variasi serangan virus yang menyerang tanaman cabai A) B1, B) B2,C) B3, D) B4
Intensitas Serangan
Intensitas serangan merupakan tingkat keparahan atau kerusakan tanaman yang disebabkan oleh suatu patogen.Virus gemini dapat menginfeksi tanaman varietas Jatilaba dengan perlakuan AIA dengan intensitas serangan paling rendah berkisar antara 24% sampai dengan 40% sedangkan intensitas serangan tertinggi terdapat pada tanaman kontrol sebesar 80%. Pada tanaman varietas Landung dengan perlakuan AIA intensitas serangan mencapai 32% sampai 40%. Bila dibandingkan dengan kontrol, intensitas serangan pada tanaman yang diberi perlakuan AIA lebih rendah daripada yang tidak diberi perlakuan AIA.
A B
A B
C D
Tabel 3 Hasil inokulasi gemini virus berbagai perlakuan pada tanaman cabai
No Perlakuan Intensitas Serangan Rata-rata (%)
Ket : A = Tanaman cabai varietas Jatilaba; B = Tanaman cabai varietas Landung Hal ini berarti tingkat kerusakan tanaman cabai yang terserang virus gemini pada perlakuan AIA tidak separah tingkat kerusakan tanaman yang tidak diberi perlakuan AIA yaitu tanaman kontrol. Tanaman perlakuan AIA lebih tahan daripada tanaman kontrol. Hal tersebut terlihat pada tabel 3.
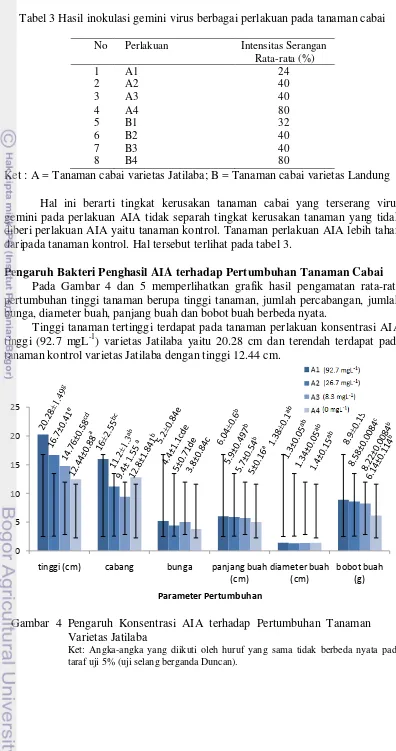
Pengaruh Bakteri Penghasil AIA terhadap Pertumbuhan Tanaman Cabai Pada Gambar 4 dan 5 memperlihatkan grafik hasil pengamatan rata-rata pertumbuhan tinggi tanaman berupa tinggi tanaman, jumlah percabangan, jumlah bunga, diameter buah, panjang buah dan bobot buah berbeda nyata.
Tinggi tanaman tertinggi terdapat pada tanaman perlakuan konsentrasi AIA tinggi (92.7 mgL-1) varietas Jatilaba yaitu 20.28 cm dan terendah terdapat pada tanaman kontrol varietas Jatilaba dengan tinggi 12.44 cm.
Gambar 4 Pengaruh Konsentrasi AIA terhadap Pertumbuhan Tanaman Varietas Jatilaba
Ket: Angka-angka yang diikuti oleh huruf yang sama tidak berbeda nyata pada taraf uji 5% (uji selang berganda Duncan).
0
tinggi (cm) cabang bunga panjang buah
10
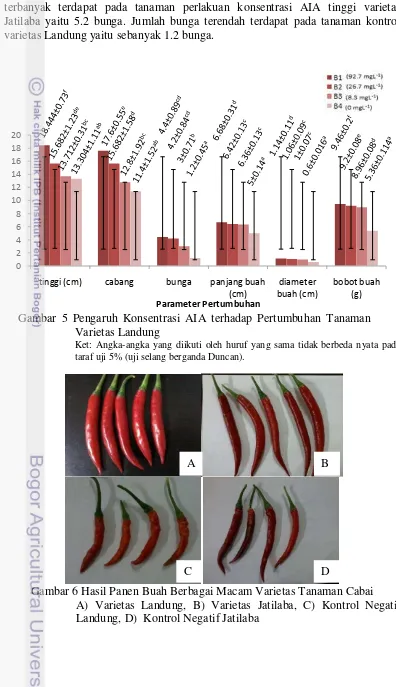
Cabang terbanyak terdapat pada tanaman varietas Landung perlakuan konsentrasi AIA tinggi yaitu sebanyak 17.6 cabang. Cabang paling sedikit terdapat pada tanaman varietas Jatilaba yaitu 10 cabang. Kemudian jumlah bunga terbanyak terdapat pada tanaman perlakuan konsentrasi AIA tinggi varietas Jatilaba yaitu 5.2 bunga. Jumlah bunga terendah terdapat pada tanaman kontrol varietas Landung yaitu sebanyak 1.2 bunga.
Gambar 5 Pengaruh Konsentrasi AIA terhadap Pertumbuhan Tanaman Varietas Landung
Ket: Angka-angka yang diikuti oleh huruf yang sama tidak berbeda nyata pada taraf uji 5% (uji selang berganda Duncan).
Gambar 6 Hasil Panen Buah Berbagai Macam Varietas Tanaman Cabai A) Varietas Landung, B) Varietas Jatilaba, C) Kontrol Negatif Landung, D) Kontrol Negatif Jatilaba
0 2 4 6 8 10 12 14 16 18 20
tinggi (cm) cabang bunga panjang buah
(cm)
diameter buah (cm)
bobot buah (g) Parameter Pertumbuhan
A B
Pada Gambar 6 terlihat buah pada tanaman cabai varietas Landung lebih besar dan lebih pendek daripada varietas Jatilaba.Diameter buah dan bobot buah terbesar terdapat pada tanaman perlakuan konsentrasi AIA tinggi varietas Landung yaitu 1.14 cm dan 9.46 g. Diameter buah dan bobot buah terendah terdapat pada tanaman kontrol varietas Jatilaba yaitu 0.59 cm dan 5.26 g. Panjang buah tertinggi terdapat pada tanaman cabai varietas Jatilaba konsentrasi tinggi yaitu 7.08 cm dan terendah pada tanaman cabai kontrol varietas Landung yaitu 5 cm. Maka dapat dikatakan bahwa tanaman cabai yang telah diaplikasikan AIA memiliki respon pertumbuhan yang lebih baik terhadap serangan virus gemini daripada tanaman kontrol yang tidak diberi perlakuan AIA.
Analisis Klorofil
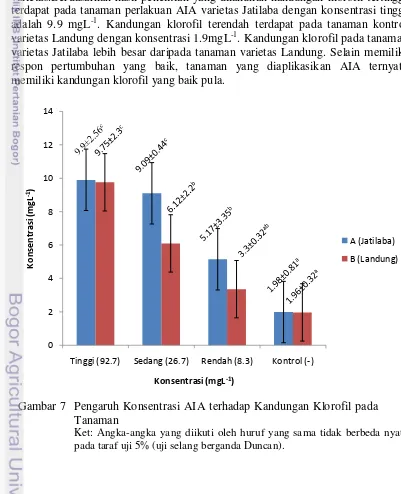
Pada Gambar 7 menunjukkan kandungan klorofil pada daun cabai kontrol berbeda nyata dengan tanaman perlakuan konsentrasi AIA dan antar varietas.Berdasarkan hasil penelitian yang dilakukan kandungan klorofil tertinggi terdapat pada tanaman perlakuan AIA varietas Jatilaba dengan konsentrasi tinggi adalah 9.9 mgL-1. Kandungan klorofil terendah terdapat pada tanaman kontrol varietas Landung dengan konsentrasi 1.9mgL-1. Kandungan klorofil pada tanaman varietas Jatilaba lebih besar daripada tanaman varietas Landung. Selain memiliki respon pertumbuhan yang baik, tanaman yang diaplikasikan AIA ternyata memiliki kandungan klorofil yang baik pula.
Gambar 7 Pengaruh Konsentrasi AIA terhadap Kandungan Klorofil pada Tanaman
Ket: Angka-angka yang diikuti oleh huruf yang sama tidak berbeda nyata pada taraf uji 5% (uji selang berganda Duncan).
0
Tinggi (92.7) Sedang (26.7) Rendah (8.3) Kontrol (-)
12
Pembahasan
Peremajaan dan Penumbuhan Isolat Bakteri Endofit
Bakteri yang diremajakan adalah jenis bakteri biakan murni yaitu bakteri yang terdiri dari satu jenis bakteri yang dibutuhkan tanpa adanya kontaminasi. Perlakuan aseptik dibutuhkan untuk mendapatkan biakan murni. Selain itu peremajaan biakan diperlukan untuk tindakan pemeliharaan kultur yang penting dalam mikrobiologi untuk mencegah terjadinya kerusakan bakteri. Kerusakan yang dapat terjadi meliputi penurunan viabilitas dan stabilitas sel bahkan suatu bakteri akan kehilangan potensinya sebagai suatu bakteri (Unus 2005).
Media tumbuh merupakan bahan yang digunakan untuk menumbuhkan mikroba. Komposisi media tumbuh disesuaikan dengan mikroba yang akan ditumbuhkan. Penggunaan agar miring dilakukan untuk mendapatkan permukaan yang luas sebagai tempat tumbuhnya bakteri dan mencegah terjadinya kontaminasi dari mikroba lain karena jarak antara bibir tabung dan agar cukup jauh. Media NA juga merupakan media sederhana yang dibuat dari ekstrak beef, pepton, dan agar. NA merupakan salah satu media yang umum digunakan dalam prosedur bakteriologi seperti uji biasa dari air, sewage, produk pangan, untuk membawa stok kultur, untuk pertumbuhan sampel pada uji bakteri, dan untuk mengisolasi organisme dalam kultur murni.
Mikroorganisme memanfaatkan nutrisi di dalam media berupa molekul-molekul kecil yang dirakit untuk menyusun komponen sel. Dengan media, pertumbuhan dapat dilakukan dengan isolasi mikroorganisme menjadi kultur murni dan juga memanipulasi komposisi media pertumbuhannya. Bahan dasar adalah air (H2O) sebagai pelarut dari agar-agar (rumput laut) dimana agar-agar tersebut berfungsi sebagai pemadat media.
Analisis Kuantitatif Uji Penghasil AIA
Pengujian produksi zat pengatur tumbuh AIA secara kuantitatif dari beberapa isolat dilakukan untuk pemilihan isolat terbaik dalam menghasilkan AIA yang akan digunakan dalam pengujian pengaruh pemberian zat pengatur tumbuh AIA terhadap pertumbuhan tanaman cabai pada mediaNB. Isolat yang diuji didapatkan dari beberapa daerah asal Bali dan Jember koleksi jangka panjang BB-Biogen.
Pengujian AIA dilakukan terhadap 50 isolat bakteri dengan penambahan triptofan yang berperan sebagai asam amino prekursor dalam pembentukan senyawa asam indol asetat. AIA adalah produk umum dari metabolisme L-triptofan oleh beberapa mikroba termasuk PGPR. Menurut Kaga et al. (2009) tidak semua bakteri endofit menghasilkan hormon AIA. Hal tersebut terlihat dari 50 isolat yang diisolasi hanya 31 bakteri yang menghasilkan AIA.
Penularan Virus dengan Bemisia tabaci dan Intensitas Serangan Virus Gemini
Pada hasil pengamatan terlihat masa inkubasi tercepat, kejadian penyakit terbesar, gejala paling parah dan intensitas serangan terdapat pada tanaman kontrol atau yang tidak diberi perlakuan konsentrasi AIA varietas Jatilaba dan Landung.Tanaman cabai memerlukan unsur makro dan mikro untuk pertumbuhannya terutama dalam ketahanannya terhadap serangan penyakit dalam hal ini penyakit yang disebabkan virus gemini.
Secara fisiologi tumbuhan yang ditanam pada kondisi optimum tidak mudah terserang penyakit karena mempunyai kekebalan tubuh yang baik dibandingkan dengan tanaman yang mengalami defisiensi nutrisi terutama unsur makro. Nutrisi diperoleh dengan adanya hormon AIA sebagai pemacu pertumbuhan dan ketahanan.Hal ini terlihat pada tanaman cabai yang diberi perlakuan konsentrasi AIA memiliki masa inkubasi, kejadian penyakit dan gejala terendah.Tanaman cabai diberi AIA ini bertujuan untuk mengoptimalkan pertumbuhan dan kekebalan tubuhnya.Apabila pertumbuhan tanaman cepat, pembelahan sel cepat daripada replikasi virus, maka gejala infeksi tidak akan muncul pada tanaman tersebut.
Menurut Funayama dan Terashima (2006) virus gemini ditularkan oleh Bemisia tabaci ini menyerang tanaman dengan cara penghambatan translokasi nutrisi. Dengan terhambatnya aliran nutrisi dari akar ke daun maupun buah maka akan terjadi defisiensi nutrisi (klorosis). Virus ini menginfeksi tanaman dengan melakukan replikasi sehingga menyebabkan peningkatan kebutuhan unsur makro khususnya nitrogen dalam tanaman untuk sintesis virus tersebut kemudian peningkatan aktivitas enzim anaplerotik,laju fotosintesis dan kandungan pati. Ketika sintesis virus menurun, laju fotosintesis dan kandungan pati dalam daun akan menurun, pembentukan klorofil pun menjadi terhambat.sedangkan glikolisis dan respirasi dalam mitokondria akan meningkat. Oleh karena itu pada daun tanaman cabai yang diinfeksikan virus gemini berubah menjadi berwarna kuning. Hal ini terlihat pada tanaman cabai yang diinfeksikan virus yaitu kontrol negatif.Hampir 80% tanaman cabai tersebut mengalami klorosis.Berbeda dengan tanaman cabai yang diberi perlakuan AIA hanya beberapa daun saja berwarna kuning.
14
Pengaruh Bakteri Penghasil AIA terhadap Pertumbuhan Tanaman Cabai Hormon auksin atau AIA terbukti mampu meningkatkan pertumbuhan tanaman.Selain itu hormon ini juga diketahui mampu meningkatkan ketahanan tanaman terhadap serangan patogen terutama virus.Hasil pengamatan menunjukkan bakteri endofit penghasil AIA ini mampu meningkatkan ketahanan terhadap serangan virus gemini dan memperbaiki pertumbuhannya. Tanaman cabai perlakuan konsentrasi AIA tinggi memiliki respon pertumbuhan tanaman berupa tinggi tanaman, jumlah percabangan, jumlah bunga, diameter buah, bobot buah dan panjang buah yang paling baik dibandingkan kontrol. Tanaman kontrol memiliki pertumbuhan yang kurang baik dikarenakan virus gemini ini menyebabkan pertumbuhan terhambat, daun klorosis atau berwarna kuning, dan tidak dapat menghasilkan bunga dan buah. (Suseno et al. 2003).
Selain itu tanaman yang terinfeksi virus akan mengalami keterlambatan waktu munculnya bunga pertama yang diakibatkan menurunnya produksi hormon pertumbuhan terutama berkaitan dengan proses pembungaan. Tanaman membutuhakan karbohidrat yang cukup dalam bentuk pati untuk membentuk buah, bunga dan biji. Laju fotosintesis yang rendah menyebabkan karbohidrat yang terbentuk sangat sedikit sehingga akan menghambat produksi bunga dan buah. Seperti pada tanaman kontrol negatif yaitu tanaman yang terinfeksi virus terlihat hasil produksi bunga dan buah yang rendah dibandingkan dengan tanaman perlakuan konsentrasi.
Asam indol asetat adalah auksin yang paling aktif untuk berbagai tanaman dan berperan penting dalam pemacuan pertumbuhan, seperti inisiasi akar, pembesaran sel, diferensiasi pembuluh dan pemacu pembungaan.Tanaman kurang mampu menghasilkan AIA yang cukup untuk pertumbuhan yang optimal. Sejumlah bakteri telah diidentifikasi mensintesis AIA pada biakan murni dan di tanah. Oleh karena itu, tanaman sering kali diberi bakteri penghasil AIA agar pertumbuhannya optimal (Husen dan Saraswati 2003).
Menurut Dewi (2008), AIA mendorong pemanjangan sel batang hanya pada konsentrasi tertentu yaitu 0,9 gL-1 atau 900 mgL-1. Di atas konsentrasi tersebut AIA akan menghambat pemanjangan sel batang karena akan memacu pembentukan hormon etilen yang akan menghambat pertumbuhan. Hasil yang diperoleh konsentrasi AIA tertinggi yaitu 92.7 mgL-1 dan dua konsentrasi lainnya yaitu 26.7 mgL-1 dan 8.3 mgL-1 memiliki pertumbuhan kurang optimal untuk ketahanan terhadap gemini virus diduga dikarenakan oleh konsentrasi AIA yang digunakan kurang dari 900 mgL-1.
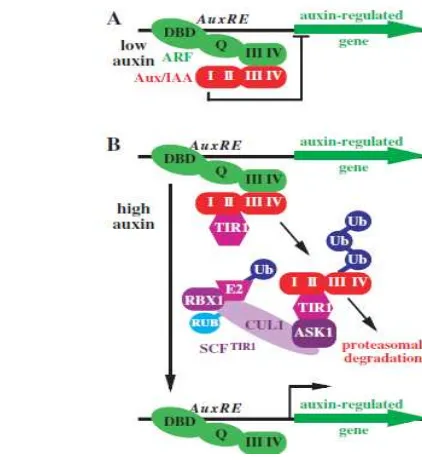
serangkaian mekanisme biosinyal yaitu dengan menggunakan VOC (Volatile Organic Compound) dan AHLs (N-acyl-L-homoserine Lactones) untuk mendapatkan bantuan dari bakteri endofit (PGPR) sehingga konsentrasi auksin dapat ditingkatkan.VOC merupakan suatu sinyal bahaya (mediator) bagi tanaman yang terinfeksi patogen. Sedangkan AHLs digunakan sebagai proses komunikasi antar sel tanaman maupun bakteri sehingga membantu proses QS (Qourum Sensing) yaitu mekanisme regulasi biosintesis dan metabolisme yang dipengaruhi oleh kepadatan populasi bakteri juga memodulasi ekspresi gen pertumbuhan. Auksin yang telah meningkat ini akan mengekspresi gen ketahanan dan pertumbuhan pada tahaman (Castro ROet al. 2009)
Menurut Woodward dan Bartel (2005) auksin dalam konsentrasi yang tinggi membantu ekspresi gen-gen yang berperan dalam mekanisme biosinyal yang berkaitan dengan proses apoptosis dan autofagi serta meningkatkan ekspresi gen pertumbuhan. Auksin dalam konsentrasi rendah tidak mampu mengekspresikan gen-gen tersebut karena terikat oleh protein regulator sisi aktif yaitu ARF (Auxin Respone Factor). ARF berada dalam keadaan aktif setelah protein regulator, protein (Aux/IAA) mengalami degradasi proteosomal oleh ubiquitin (Gambar 15) Analisis Klorofil
Tanaman cabai perlakuan konsentrasi AIA tinggi memiliki kandungan klorofil yang tinggi dibandingkan dengan tanaman kontrol. Seperti yang telah disebutkan sebelumnya tanaman yang terserang virus, aliran nutrisi dari akar ke daun menjadi terhambat.Oleh karena itu tanaman tanpa perlakuan AIA memiliki kandungan klorofil paling rendah. Kurangnya nutrisi pada daun akan menghambat pembentukan kloroplas sehingga mengakibatkan menurunnya kandungan klorofil dan laju fotosintesisnya menurun pula (Funayama dan Terashima 2006).
SIMPULAN DAN SARAN
Simpulan
Hasil pengamatan menunjukkan bahwa terdapat 31 isolat bakteri endofit yang menghasilkan AIA dengan konsentrasi yang bervariasi. Tanaman cabai yang diberi konsentrasi AIA tinggi (92.7 mgL-1) terbukti memiliki ketahanan yang lebih besar daripada kontrol (0 mgL-1). Tanaman dengan konsentrasi terbesar AIA menghasilkan pertumbuhan yang lebih baik terlihat dari intensitas serangan dan respon pertumbuhannya.Tanaman cabai yang diberi AIA memiliki intensitas serangan 24%. Selain itu tanaman ini juga memiliki kandungan klorofil terbesar yaitu 9.9 mgL-1.
Saran
Penelitian ini perlu dilakukan optimasi terhadap perlakuan tanaman cabai dengan berbagai konsentrasi AIA agar hasil lebih akurat dan optimal. Uji analisis virus seperti uji ELISA juga perlu dilakukan untuk mengetahui keberadaan virus gemini tersebut. Selain itu perlu dilakukan uji in vitro untuk mengetahui kemampuan bakteri endofit dalam menghasilkan senyawa lain serta uji lanjut untuk mengetahui kemampuan bakteri endofit dalam memfiksasi nitrogen.
DAFTAR PUSTAKA
Agrios GN. 2005. Plant Pathology. Ed ke-5. San Diego: Academic Pr.hlm 952 Bacon CW dan Hinton DM. 2006.Growth-inhibiting effects of concentrations of
fusaric acid on the growth of Bacillus mojavensis and other biocontrol Bacillus species.J Applied Microbiol. 100: 185-194.
Dewi IR. 2008 Peranan dan Fungsi Fitohormon bagi Pertumbuhan Tanaman. Bandung: Universitas Padjadjaran Press. 43.
Duriat AS. 2009. Pengendalian Penyakit Kuning Keriting pada Tanaman Cabai.Bandung: Balai Penelitian Tanaman Sayur.hlm 1-4.
DJPTPH. 2002. Luas Panen, Produktivitas dan Produk Tanaman Sayuran, Buah-Buahan dan Aneka Tanaman di Indonesia Tahun 2001 Angka Tetap. Jakarta : Direktorat Bina Program Tanaman Pangan dan Holtikultira Departemen Pertanian..
Funayama S dan Terashima I. 2006.Effect of Eupatorium Yellow Vein Virus Infection on Photosynthetic Rate, Chlorophyll Content and Chloroplast Structure in Leaves of Euphatorum makinoi During Leaf Development.Functional Plant Biol. P. 165-175.
Harni R, Munif A, Mustika I. 2007. Potensi Bakteri Endofit Pengendali Nematoda Peluka Akar (Pratylenchus brachyurus) pada Nilam.HAYATI.Vol. 14.No.1. Husen E dan Saraswati R. 2003.Effect of IAA-producing bacteria on the growth of
hot pepper.J Mikrob Indonesia8:22-26
Iacobellis NC, Shanmugaiah V, Lo Cantore P. 2009. Selection of antagonistic bean rhizosphere bacteria for the biologycal control of bean diseases caused bybacteria and fungi. Petri 19(S): 28-30.
Kaga H, Mano H, Tanaka F, Watanabe A, Kaneko S dan Morisaki H. 2009. Rice seeds as source of endophtic bacteria. Microbes Environ2:154-162.
MahmoodT, Hein GL, French RC. 2010. Inhibition of Tomato Yellow Leaf Curl Virus (TYLCV) using whey proteins. Plant Dis. 81:250-253.
Matjik AA. Sumertajaya MI. 2002. Perancangan Percobaan. IPB Press. Bogor
Patten CL and Glick BR. 2002.Role of Pseudomonas putida Indole Acetic Acid in Development of The Host Plant Root System.App and Environmental Microb. 68 (8): 3795-3801.
Ortiz CR. Hexon ACC. Macias R. Jose LB. 2005.The role of microbial signals in plant growth and development. Plant Signalling & Behavior 4:8, 701-712.
Setiadi. 2007. Bertanam Cabe.Jakarta: Penebar Swadaya
Ryu CM, Murphy JF, Mysore KS, Kloepper JW. 2004. Plant growth promoting rhizobacteria systemically protect Arabidopsis thaliana against cucumber mosaic virus by aslliyclic acid and NPR1 independent and jasmonis acid dependent signaling pathway. Plant J 31:1-12
Setiadi. 2007. Bertanam Cabe. Jakarta: Penebar Swadaya
Spaepen S, Vanderleyden J, Remans R. 2007. Indole-3-acetic acid in microbial and microorganism plant signaling. FEMS Microbial Rev 31: 425-448
Sumenda L, Rampe HL dan Mantin FR. 2011. Analisis Kandungan Klorofil Daun Mangga (Mangifera indica L.) pada Tingkat Kandungan Daun yang Berbeda.Fakulatas MIPA, Universitas Sam Ratulangi Manado
Suseno RS, Hidayat S, Harjosudarmono J dan Sosromarsono S. 2003. Respon Beberapa Kultivar Cabai terhadap Penyebab Penyakit Daun Keriting Kuning Cabai.Prosid.Konggress Nasional XVII.PFI. Bandung. 6-8 Agustus.
Suganda TE, Rismawati E, Yulia, Nasahi C. 2002. Pengujian beberapa bahan kimia dan air perasan daun tumbuhan dalam menginduksi resistensi tanaman padi terhadap penyakit bercak daun Cercospora.Jurnal Bionatura4:17-28
Sumarni N, Agus M. 2008. Sukses Bertanam Cabai di Musim Hujan dan Kemarau.Jakarta: Papas Sinar Sinanti.
Suryadi Y, Manzila I, Priyatno TP, Samudra IM, Susilowati DN, Solomo C, Irawati W. 2010. Bioprospeksi isolate-isolat bakteri asal Bali: uji daya antipatogen, produksi IAA dan enzim ekstraseluler kitinase. BB-Biogen.
18
Timmusk S. 2003. Mechanism of action of the plant-growth-promoting rhizobacterium Paenibacillus poyimyxa [disertasi]. Uppsala, Sweden: Departemen of Cell and Molekular Biology, Uppsala University.
Unus S. 2005. Mikrobiologi Dasar.Papas Sinar Sinanti. Jakarta. 76.
Woodward AW dan Bartel B. 2004. Auxin: Regulation, Action and Interaction. Annals Bot. 95: 707-735, 2005.
20
Lampiran 1 Diagram alir penelitian
Peremajaan dan Penumbuhan Isolat Bakteri
Aplikasi Bakteri Endofit penghasil AIA Penanaman cabai
Penularan Virus
Analisis Kandungan Klorofil Analisis Uji Kandungan AIA
Lampiran 2 Pembuatan Pereaksi Pembuatan Pereaksi Salkowski
Dipipet sebanyak 20 mL FeCl 0,1 M ; 400 mL H2SO4 pekat ; 580 mL akuades kemudian dimasukkkan ke botol coklat 1000 mL dan disimpan dalam ruang gelap. Pembuatan Larutan Standar Induk AIA 1000 mgL-1
Standar Asam Indol Asetat ditimbang 0,1 g dimasukkan ke gelas piala 100 mL. Kemudian dilarutkan dengan 30 mL etanol dan larutan dihomogenkan dengan magnetic stirer, setelah larut dimasukkan ke labu takar 100 mL dan ditambahkan akuades sampai tanda tera.
Pembuatan deret standar AIA dari standar induk 1000 mgL-1
Larutan deret standar dibuat dengan konsentrasi 0.2; 1.0; 5.0; 15.0; 20.0; 25.0; 30.0; 40.0;45.0 mgL-1 dari larutan induk 1000 mgL-1. Larutan induk dipipet menggunakan pipet mikro kemudin dimasukkan ke tabung reaksi makro dan ditambahkan akuades sampai dengan volume 5 mL.
No Konsentrasi (mgL-1)
Volume (mL) Standar AIA Akuades
1 0.2 0.01 4.99
2 1.0 0.05 4.95
3 5.0 0.25 4.75
4 15.0 0.75 4.25
5 20.0 1.00 4.00
6 25.0 1.25 3.75
7 30.0 1.50 3.50
8 35.0 1.75 3.25
9 40.0 2.00 3.00
22
Lampiran 3 Hasil Pengukuran Absorbansi Standar dan Contoh Perhitungan Konsentrasi Asam Indol Asetat
1. Pengukuran ke-1
A. Hasil pengukuran Absorbansi dan Kurva Standar Asam Indol Asetat (1)
Konsentrasi (mgL-1) Absorbansi (A)
B. Hasil Pengujian Asam Indol Asetat (AIA) pada Isolat Bakteri (1)
Contoh Perhitungan Analisis Kuantitatif AIA pada Isolat 4 Putih Bali berdasarkan persmaan Kurva standar
= +
= 0.0112x + 0.0528
=0.146 ( Nilai absorbansi sampel isolat 4P )
� � �=( − )= (0.146−0.0528)
0.0112
= 8.321
No Kode Isolat Absorbansi Konsentrasi (mgL-1)
1 4P 0.146 8.321
2 6K 0.196 12.786
3 6KR 0.070 1.536
4 A11 0.145 8.232
5 A14 0.116 5.642
6 A18 0.258 18.321
7 A3 0.308 22.786
8 A4 0.021 -2.776
9 A7 0.410 31.893
10 A9 0.169 10.375
11 C11 0.168 10.286
12 C2 0.190 12.250
13 C21 0.266 19.035
14 C4 0.141 7.875
15 C6 0.420 32.786
16 C8 0.138 7.607
17 PTB C11 0.213 14.368
18 PTB C13 0.352 26.700
24
2. Pengukuran ke-2
A. Hasil pengukuran Absorbansi dan Kurva Standar Asam Indol Asetat (2)
Konsentrasi (mgL-1) Absorbansi
0.2 0.071
1.0 0.216
5.0 0.315
15.0 0.688
20.0 0.782
25.0 0.784
30.0 0.827
35.0 0.842
40.0 0.863
45.0 0.878
y = 0.018x + 0.197 R² = 0.835
0 0.2 0.4 0.6 0.8 1 1.2
0 10 20 30 40 50
A
b
so
rb
a
n
si
(A
)
Konsentrasi (mgL-1)
A. Hasil Pengujian Asam Indol Asetat (AIA) pada Isolat Bakteri (2)
No Kode Isolat Absorbansi (A)
A. Hasil pengukuran Absorbansi dan Kurva Standar Asam Indol Asetat (3)
Konsentrasi (mgL-1) Absorbansi (A)
26
B. Hasil Pengujian Asam Indol Asetat (AIA) pada Isolat Bakteri (3)
No. Kode Isolat Absorbansi (A) Konsentrasi
Lampiran 4 Perhitungan Intensitas Serangan atau menguning; dan 5: tanaman mati.
Contoh perhitungan:
1 A konsentrasi tinggi 3 0.24 Daun menggulung, satu/dua daun menguning
5 B konsentrasi tinggi 4 0.32 Daun menggulung, satu/dua daun menguning
Intensitas serangan tanaman cabai Jatilaba (A) konsentrasi tinggi:
I =Ʃ � ��
�
I =
3 228
Lampiran 5 Hasil Uji Duncan Terhadap Perlakuan Konsentrasi AIA pada Tanaman Cabai
1. Tinggi Tanaman Cabai
Anova Sum of
Squares df Mean Square F Sig.
Between Groups
253.658 7 36.237 42.246 .000
Within Groups
27.448 32 .858
Total 281.106 39
Duncan
perlakuan N
Subset for alpha = 0.05
1 2 3 4 5 6 7
A nol
5 12.4380
B nol
5 13.3040 13.3040
B rendah
5 13.7120 13.7120
A rendah
5 14.7580 14.7580
B sedang
5 15.6810 15.6810
A sedang
5 16.6980
B tinggi
5 18.4440
A tinggi
5 20.2820
Sig.
2. Jumlah Cabang
ANOVA
JumlahCabang
Sum of Squares df Mean Square F Sig.
Between Groups 224.400 7 32.057 12.330 .000
Within Groups 83.200 32 2.600
Total 307.600 39
JumlahCabang
Duncan
Perlakuan N
Subset for alpha = 0.05
1 2 3 4 5
A Kontrol (-) 5 10.0000
B Kontrol (-) 5 11.4000 11.4000
A Rendah 5 12.0000 12.0000 12.0000
B Rendah 5 12.8000 12.8000
A Sedang 5 14.0000 14.0000
B Sedang 5 15.0000
A Tinggi 5 16.0000 16.0000
B Tinggi 5 17.6000
30
3. Jumlah Bunga
JumlahBunga
Duncan
Perlakuan N
Subset for alpha = 0.05
1 2 3 4
B Kontrol (-) 5 1.2000
B Rendah 5 3.0000
A Kontrol (-) 5 3.8000 3.8000
B Sedang 5 4.2000 4.2000
A Sedang 5 4.4000 4.4000
B Tinggi 5 4.4000 4.4000
A Rendah 5 5.0000
A Tinggi 5 5.2000
Sig. 1.000 .133 .301 .094
ANOVA
JumlahBunga
Sum of Squares df Mean Square F Sig.
Between Groups 58.000 7 8.286 12.275 .000
Within Groups 21.600 32 .675
4. Panjang Buah ANOVA
PanjangBuah
Sum of Squares df Mean Square F Sig.
Between Groups 24.778 7 3.540 138.811 .000
Within Groups .816 32 .026
Total 25.594 39
PanjangBuah
Duncan
Perlakuan N
Subset for alpha = 0.05
1 2 3 4
B Kontrol (-) 5 5.0000
A Kontrol (-) 5 5.1000
B Rendah 5 6.3600
B Sedang 5 6.4200
B Tinggi 5 6.6800
A Rendah 5 7.0200
A Sedang 5 7.0400
A Tinggi 5 7.0800
Sig. .330 .557 1.000 .581
32
5. Diameter Buah
ANOVA
DiameterBuah
Sum of Squares df Mean Square F Sig.
Between Groups 1.385 7 .198 52.625 .000
Within Groups .120 32 .004
Total 1.505 39
DiameterBuah
Duncan
Perlakuan N
Subset for alpha = 0.05
1 2 3 4
A Kontrol (-) 5 .5920
B Kontrol (-) 5 .6080
A Rendah 5 .8180
A Sedang 5 .8200
A Tinggi 5 .8420
B Rendah 5 1.0000
B Sedang 5 1.0600
B Tinggi 5 1.1400
Sig. .683 .565 .132 1.000
6. Berat Buah
ANOVA
Beratbuah
Sum of Squares df Mean Square F Sig.
Between Groups 100.878 7 14.411 466.156 .000
Within Groups .989 32 .031
Total 101.868 39
Duncan
Perlakuan N
Subset for alpha = 0.05
1 2 3 4 5 6
A Kontrol (-) 5 5.2580
B Kontrol (-) 5 5.3600
A Rendah 5 8.2200
A Sedang 5 8.5800
A Tinggi 5 8.9000
B Rendah 5 8.9600
B Sedang 5 9.2000
B Tinggi 5 9.4600
34
7. Kandungan Klorofil
ANOVA
Konsentrasi Klorofil
Sum of Squares df Mean Square F Sig.
Between Groups 238.151 7 34.022 12.856 .000
Within Groups 42.343 16 2.646
Total 280.494 23
Duncan
Perlakuan N
Subset for alpha = 0.05
1 2 3
B Kontrol (-) 3 1.9569
A Kontrol (-) 3 1.9804
B Rendah 3 3.3503 3.3503
A rendah 3 5.1757
B Sedang 3 6.1181
A sedang 3 9.0873
B Tinggi 3 9.7883
A tinggi 3 9.9156
Sig. .335 .065 .563
RIWAYAT HIDUP
Penulis dilahirkan di Pandeglang, pada tanggal 12 September 1991 dari ayah Sunardi dan Nurhayati. Penulis merupakan anak ketiga dari tiga bersaudara.Pendidikan penulis dimulai dari SD Mexico 06 Petang Jakarta, melanjutkan pendidikan ke SLTPN 19 Jakarta dan melanjutkan pendidikan ke SMAN 87 Jakarta. Penulis lulus tahun 2009 dari SMAN 87 Jakarta dan pada tahun yang sama lulus masuk seleksi IPB melalui USMI. Penulis memilih mayor Biokimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan, penulis pernah melakukan Praktik Lapang (PL) di BPBPI, Taman Kencana, Bogor selama periode Juli 2012 hingga Agustus 2012
dengan judul “Transformasi Genetik Melalui Agrobacterium ke dalam Kalus Tebu
(Saccharum officinarumL.)”.
Penulis dalam bidang karya ilmiah pernah mendapat hibah dana bersaing dari Direktorat Jenderal Pendidikan Tinggi (DIKTI) dalam Program Kreativitas Mahasiswa (PKM) untuk kategori Bidang Penelitian pada tahun 2013 ”Pesona
Eksotika Batang Bunga Matahari sebagai Antikanker Kolon”. Penulis pada saat