ABSTRAK
STUDI PENENTUAN JENISOUTLETLIMBAH CAIR KARET REMAH UNTUK PERTUMBUHAN MIKROALGA DENGAN SISTEMOPEN
PONDS Oleh
ANGGUN KOMALASARI
Limbah cair industri karet remah bersumber dari tahap koagulasi, penggilingan dan pencucian mengandung bahan organik yang berasal dari serum dan partikel karet yang belum terkoagulasi berpotensi mencemari lingkungan perairan. Supaya tidak mencemari lingkungan perairan, dilakukan penanganan melalui Instalasi Pengolahan Air Limbah. Namun karakteristik limbah cair diduga cocok untuk media kultivasi Nannochloropsis sp. Nannochloropsis sp. mengandung minyak 31-68% berpotensi sebagai bahan baku biofuel khususnya biodiesel yang dapat dijadikan sebagai sumber energi. Tujuan dari penelitian ini adalah mendapatkan jenis outlet limbah cair karet remah yang optimal untuk pertumbuhan mikroalga dengan sistem Open Ponds. Penelitian ini dilaksanakan dalam dua tahap yaitu tahap pertama adalah karakterisasi limbah cair. Limbah cair yang digunakan adalah limbah cair karet remah yang berasal dari outlet kolam Fakultatif II (F2), outlet kolam Aerobik I (Ae1), dan outlet kolam Aerobik II (Ae2) dengan volume kerja masing-masing 5 L sebagai tiga taraf perlakuan media pertumbuhan Nannochloropsis sp. Tahap yang kedua adalah tahap kultivasi Nannochloropsis sp. sebanyak 25% v/v kerja. Pengamatan yang dilakukan adalah kepadatan mikroalga (OD), analisa N-NH3, N-total, P-PO4, pH, suhu, kandungan Chemical Oxygen Demand (COD), Dissolved Oxygen (DO) dan perolehan yield kering. Hasil optimum pertumbuhan Nannochloropsis sp. terdapat pada media outlet limbah cair kolam Fakultatif II dengan kepadatan sel mencapai 3,3 x 107 sel/mL. Selain itu dapat menurunkan kandungan bahan organik limbah cair karet remah berupa N-NH3 mencapai 98%, P-PO4 89%, N-total 92%, dan perolehan yield kering sebesar 0,87 g/L.
ABSTRACT
STUDY OF DETERMINATION THE TYPE OF CRUMB RUBBER WASTE WATER OUTLET FOR THE GROWTH OF MICROALGAE
USING OPEN PONDS SYSTEM
By
ANGGUN KOMALASARI
Crumb rubber industrial waste water was originated from coagulation, milling, and leaching stage contains organic material derived from serum and rubber particles whichhaven’tbeen coagulated yet. The materials are potential to pollute the water. Therefore the crumb rubber industrial waste water, should be conducted through the waste water plant. However, the characteristics of waste water are estimated suitable for the cultivation of Nannochloropsis sp substrate. Nannochloropsis sp. contains oil of about 31-68% that is potential as raw material of biofuel be used as a source of energy. The purpose of this study was determine the kind of the outlet of the crumb rubber waste water to suitable for microalgae growth using open ponds system. This study was conducted in two phases: the first phase is characterization of wastewater. Waste water used was crumb rubber waste water derived from outlet of Facultative II pond (F2), Aerobic I (Ae1) pond, and Aerobic II (Ae2) pond with a working volume of each 5 L as a three-stage treatment of growth substrate of Nannochloropsis sp. The second phase is cultivation of Nannochloropsis sp. as much as 25% v / v of work. The parameters were measured: microalgae density (OD), analysis of N-NH3, N-total, P-PO4, pH, temperature, content of Chemical Oxygen Demand (COD), Dissolved Oxygen (DO) and dried yield acquisition. The optimum result growth of Nannochloropsis sp. was on outlet Facultative II pond media with density of cell was about 3.3 x 107 cells / mL. Moreover, it reduced the organic material that content of crumb rubber waste water reaches 98% of N-NH3,89% of P-PO4, 92% of N-total, and 0.87 g /L of dry yield acquisition.
STUDI PENENTUAN JENISOUTLETLIMBAH CAIR KARET REMAH UNTUK PERTUMBUHAN MIKROALGA DENGAN SISTEMOPEN
PONDS
Oleh :
ANGGUN KOMALASARI
Skripsi
Sebagai Salah Satu Syarat Untuk Mencapai Gelar
SARJANA TEKNOLOGI PERTANIAN
Pada
Jurusan Teknologi Hasil Pertanian
Fakultas Pertanian Universitas Lampung
FAKULTAS PERTANIAN
UNIVERSITAS LAMPUNG
RIWAYAT HIDUP
Penulis dilahirkan di Wonodadi, Gadingrejo, Pringsewu pada tanggal 7 Agustus
1992, sebagai putri sulung dari dua bersaudara pasangan Bapak Slamet dan Ibu
Surasmiati.
Penulis menyelesaikan pendidikan Sekolah Dasar di SD Negeri 1 Wonodadi pada
tahun 2005, Sekolah Lanjutan Tingkat Pertama di SMP Negeri 1 Gadingrejo pada
tahun 2008, dan Sekolah Menengah Atas di SMA Negeri 1 Gadingrejo pada tahun
2011.
Pada tahun 2011, penulis terdaftar sebagai mahasiswa Jurusan Teknologi Hasil
Pertanian Fakultas Pertanian Universitas Lampung. Selama menjadi mahasiswa
penulis pernah menjadi asisten praktikum mata kuliah Biokimia Umum pada
tahun ajaran 2012/2013 dan 2013/2014. Pada tahun 2014, penulis melaksanakan
Kuliah Kerja Nyata (KKN) Tematik di Desa Srigading, Kecamatan Labuhan
Maringgai, Kabupaten Lampung Timur dan tahun 2014, penulis melaksanakan
Praktik Umum (PU) di PT. Perkebunan Nusantara VII (Persero) Unit Usaha Way
Puji dan syukur kehadirat Allah S.W.T.
Maha Suci Allah Yang Maha Pengasih dan Penyayang
Aku persembahkan sebuah karya ini untuk:
Ibu, bapak, adik dan seluruh keluarga besar atas dukungannya
Semua sahabat yang mengajari saya arti persahabatan
Serta almamaterku tercinta
SANWACANA
Alhamdulillahi rabbil „aalamiin, puji syukur penulis panjatkan kehadirat Allah
SWT atas nikmat, petunjuk serta ridho-Nya sehingga penulis dapat menyelesaikan
penulisan skripsi ini yang berjudul “Studi Penentuan Jenis Outlet Limbah Cair Karet Remah untuk Pertumbuhan Mikroalga dengan Sistem Open Ponds” Dalam kesempatan ini penulis mengucapkan terima kasih kepada:
1. Bapak Prof. Dr. Ir. Wan Abbas Zakaria, M.S. selaku Dekan Fakultas Pertanian
Universitas Lampung. dan Ibu Ir. Susilawati, M.Si. selaku Ketua Jurusan
Teknologi Hasil Pertanian FP Unila atas segala bantuan yang diberikan selama
penulis menimba ilmu di Universitas Lampung.
2. Bapak Dr. Ir. Tanto Pratondo Utomo, M.Si. selaku pembimbing pertama atas
bimbingan, bantuan dan arahannya dalam proses penyelesaian skripsi penulis.
3. Ibu Ir. Otik Nawansih, M.P. selaku pembimbing kedua atas saran dan
bimbingannya dalam proses penyelesaian skripsi penulis.
4. Ibu Dr. Sri Hidayati, S.T.P., M.P., selaku pembahas atas saran, bimbingan dan
evaluasinya terhadap karya skripsi penulis.
5. Besar Balai Besar Pengembanan Budidaya Laut Lampung telah memberikan
izin kepada penulis untuk belajar dan melakukan penelitian.
6. PTPN VII Unit Usaha Way Berulu telah memberikan izin menggunakan
vii
7. Ibu Prof. Ir. Neti Yuliana, M.Si., Ph.D. selaku dosen pembimbing akademik
yang telah memberikan bimbingan dan perhatiannya kepada penulis.
8. Keluarga tercinta: Bapak, Ibu, Bude, Pakde, serta adikku atas do‟a, dukungan
moril, motivasi, serta kasih sayang yang tiada henti demi keberhasilanku.
9. Seluruh Bapak dan Ibu dosen pengajar, staff administrasi dan laboratorium di
Jurusan Teknologi Hasil Pertanian Fakultas Pertanian Universitas Lampung.
10.Keluarga besar Laboratorium Penggelolaan Limbah Agroindustri THP FP
Unila: Pak Udin, Mas Joko, Mbak Amel, Icha, Uul, dan Widya atas
bantuannya selama penulis melakukan penelitian.
11.Sahabat-sahabatku : Ulan Trihastuti (Giving motivation), Velly (My partner), Rayung (My team), Wika (Good advisor), Tias, Yoan, Nabil, Ani, Isnaini, Lia Marley, Rifka, Mae, Armal, Dea, Ara, Devi, Amur, Sihol, Via, St, Inun,
Mboy, Pawe, Artha, Fidah, Neri, Lis, Ratri, Ira, Pute, Yati, Isah, Icacil, Shely,
Oci, Tesa, Algi, Yudha, Wildan, Oos, Ginta, Satria, Rian, Indra, Ganesha,
Ijal, Wahyu, Fitra, Udin, Ori, Wayan, Danang atas persahabatan dan
kebersamaannya selama ini, suka dan duka yang menghiasi kehidupan kampus
penulis, semoga persahabatan kita akan selalu terjalin.
Penulis berharap semoga Allah SWT membalas segala amal dan kebaikan semua
pihak di atas dan skripsi ini dapat bermanfaat bagi penulis dan pihak-pihak terkait.
Aamiin.
Bandar Lampung, 7 Juni 2015
DAFTAR ISI
Halaman
DAFTAR TABEL... x
DAFTAR GAMBAR... xi
I. PENDAHULUAN... 1
A. Latar Belakang dan Masalah ... 1
B. Tujuan Penelitian... 3
C. Kerangka Pemikiran ... 4
II. TINJAUAN PUSTAKA... 7
A. Definisi dan Peranan Mikroalga... 7
B. Faktor-Faktor yang Mempengaruhi Pertumbuhan Mikroalga... 10
1. Suhu ... 10
2. Cahaya ... 11
3. pH ... 11
4. Nutrien ... 12
C. Nannochloropsissp ... 13
D. Karakteristik Limbah Cair Karet Remah ... 17
E. Nutrien Limbah Cair Karet... 18
1. Nitrogen ... 18
2. Fosfor... 19
F. Open Ponds System... 20
III. METODE PENELITIAN... 22
A. Tempat dan Waktu Penelitian ... 22
ix
C. Metode Penelitian... 23
D. Pelaksanaan Penelitian ... 24
IV. HASIL DAN PEMBAHASAN... 30
A. Karakteristik Limbah Cair Karet Remah ... 30
B. KultivasiNannochloropsissp ... 31
1. Kepadatan MikroalgaNannochloropsissp... 32
2. Amonia (N-NH3) ... 34
3. Nitrogen Total... 36
4. Ortofosfat (P-PO4) ... 37
5. Derajat Keasaman (pH) ... 39
6. Chemical Oxygen Demand(COD) ... 41
7. Disolved Oxygen(DO) ... 42
8. YieldKering ... 44
V. SIMPULAN DAN SARAN... 47
A. Kesimpulan ... 47
B. Saran ... 47
DAFTAR PUSTAKA ... 48
DAFTAR TABEL
Tabel Halaman
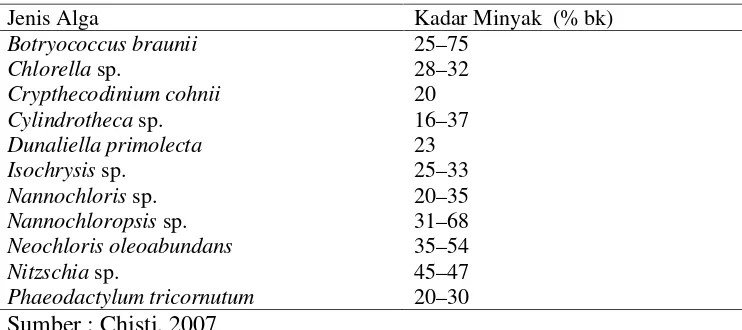
1. Kadar minyak pada mikroalga ... 15
2. Karakteristik limbah cair karet remah berbahan baku lateks kebun influen 17
3. Parameter dan baku mutuoutletair limbah unit pabrik karet Way Berulu . 18 4. Karakteristik limbah cair karet remah dan persyaratan media kultur mikroalga
DAFTAR GAMBAR
Gambar Halaman
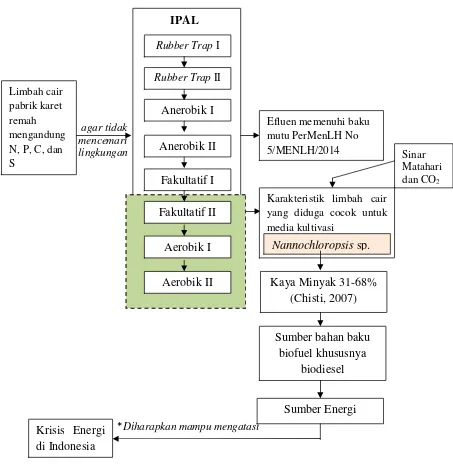
1. Diagram alir pemanfaatan limbah cair karet ... 6
2. BentukNannochloropsissp. ... 14
3. Kurva pertumbuhan... 16
4. Bentuk reaktor... 21
5. Skema reaktor... 23
6. Diagram alir perolehanyield Nannochloropsis sp ... 24
7. Grafik pertumbuhanNannochloropsissp. pada media limbah cair karet darioutletkolam Fakultatif II, Aerobik I dan Aerobik II ... 32
8. Penurunan N-NH3pada media limbah cair karet darioutlet kolam Fakultatif II, Aerobik I dan Aerobik II... 35
9. Penurunan Ntotal pada media limbah cair karet darioutlet kolam Fakultatif II, Aerobik I dan Aerobik II... 36
10. Penurunan P-PO4pada media limbah cair karet darioutlet kolam Fakultatif II, Aerobik I dan Aerobik II... 38
11. Kenaikan pH setelah panen pada media limbah cair karet darioutlet kolam Fakultatif II, Aerobik I dan Aerobik II... 39
12. Penurunan COD pada media limbah cair karet darioutlet kolam Fakultatif II, Aerobik I dan Aerobik II... 41
13. Penurunan DO pada media limbah cair karet darioutletkolam Fakultatif II, Aerobik I dan Aerobik II ... 43
14. Persiapan limbah cair sebagai media kultivasi... 59
15. IsolatNannochloropsissp. ... 59
xii
17. Pengamatan OD dan Pengambilan sampel limbah untuk analisa ... 60
18. Analisa Kimia... 60
19. Spektrophotometer, DO meter dan pH meter ... 60
20. Analisa COD ... 61
21. Media kultivasi... 61
22. Penambahan NaOH untuk panen ... 61
23. Pengendapan dan penyaringan ... 62
I. PENDAHULUAN
A. Latar Belakang dan Masalah
Pencemaran masalah lingkungan terutama perairan sekarang lebih diperhatikan,
terutama setelah berkembangnya kawasan industri baik dari sektor pertanian
maupun sektor teknologi industri. Salah satu industri di Indonesia yang semakin
berkembang adalah industri pengolahan karet. Perkembangan industri karet
memberikan dampak yang positif sebagai salah satu agroindustri potensial sebagai
penghasil devisa negara. Saat ini produksi karet alam di Indonesia melebihi 3 juta
ton per tahun dan akan terus ditingkatkan lagi mengingat potensi lahan yang ada
mencapai 2,5 juta hektar. Pendapatan devisa dari komoditi karet ini pada tahun
2006 mencapai US $ 4,3 milyar dan dalam kurun waktu lima tahun terakhir, karet
menyumbang devisa dari 25% hingga 40% terhadap total ekspor produk
perkebunan (Neraca, 2015)
Namun dalam proses pengolahan karet olahan seperti karet remah menghasilkan
limbah cair yang bersumber dari tahap koagulasi, penggilingan dan pencucian.
Limbah tersebut mengandung bahan organik yang berasal dari serum dan partikel
karet yang belum terkoagulasi (Utomo dkk, 2012). Apabila limbah cair tersebut
tidak dilakukan penanganan akan berpotensi mencemari lingkungan perairan.
2
kewajiban yang harus dipenuhi untuk mengendalikan pencemaran dan buangan
limbah cair yang dihasilkan dari proses produksi.
Karakteristik limbah cair karet menunjukkan limbah cair karet remah
mengandung bahan organik dan nutrien yang tinggi sehingga berpotensi untuk
digunakan sebagai media pertumbuhan mikroalga. Mikroalga merupakan salah
satu tumbuhan air mikroskopik yang diduga memiliki peran dalam mendegradasi
polutan dalam limbah cair karet. Hal ini didukung dengan pendapat yang
dinyatakan oleh Palmer (1985) bahwa mikroalga yang tumbuh pada limbah cair
karet adalah mikroalga yang memiliki peran yang penting dalam proses
dekomposisi limbah cair karet. Menurut Loehr (1974), alga dapat menyimpan
kelebihan nutrien dalam masa selnya, oleh karena itu dapat digunakan sebagai alat
untuk mengambil beberapa nutrien N dan P yang terdapat pada hasil buangan atau
limbah cair. Bahan organik pada kolam limbah cair karet remah dimetabolisme
oleh bakteri dengan produk akhir dari metabolisme tersebut adalah
karbondioksida, ion amonium, ion nitrat dan ion fosfat. Mikroalga mendapatkan
energi dari sinar matahari dan menggunakan bahan anorganik seperti CO2,
amonium atau fosfat untuk pertambahan selnya.
Sistem penanganan limbah cair dengan memanfaatkan mikroalga merupakan
salah satu alternatif pemecahan masalah limbah cair, karena penanganannya
mudah, murah, dan di dalam limbah cair cukup tersedia nutrien yang dibutuhkan
mikroorganisme tersebut serta ramah lingkungan. Sistem ini diharapkan dapat
memberikan kontribusi solusi untuk mengurangi dampak buruk terhadap
3
karet remah. Selain itu, hasil dari sistem penanganan secara biologis tersebut
berupa biomasa yang dapat dimanfaatkan lebih lanjut menjadi sumber energi baru
berupa biodiesel. Nannochloropsissp. merupakan salah satu jenis mikroalga yang memiliki potensi sebagai bahan baku alternatif pembuatan biodiesel karena
memiliki kandungan minyak sekitar 31-68% (Chisti, 2007). Salah satu sistem
yang dapat digunakan dalam optimasi pertumbuhan mikroalga pada limbah cair
karet remah ini adalahOpen Ponds System.
Nannochloropsis sp. ini akan dikultivasi pada limbah cair karet remah yang berasal dari kolam yang berbeda. Limbah cair yang digunakan berasal dari kolam
Fakultatif II, kolam Aerobik I, dan kolam Aerobik II sebagai media pertumbuhan
Nannochloropsis sp. Ketiga jenis kolam yang digunakan memiliki karakteristik yang berbeda berdasarkan kandungan bahan organik. Bahan organik yang
terkandung di dalam limbah cair ini berpotensi untuk digunakan sebagai
pengganti nutrien N dan P yang diperlukanNannochloropsissp. untuk melakukan pertumbuhan dan perkembangan. Oleh karena itu, perlu dilakukan penelitian
mengenai optimasi pertumbuhan mikroalga pada limbah cair karet remah untuk
mendapatkan media limbah cair karet yang paling berpotensi sebagai media
pertumbuhanNannochloropsissp.
B. Tujuan
4
C. Kerangka Pemikiran
Limbah cair agroindustri pada umumnya kaya akan hara N (nitrat), P (fosfat), C
(karbon), dan S (sulfat), karena terdapat bahan organik yang berasal dari serum
dan partikel karet yang belum terkoagulasi (Utomo dkk, 2012). Serum lateks
terdiri atas air, karbohidrat dan inosotol, protein dan senyawa nitrogen, asam
nukleat dan nukleosida, ion anorganik, dan ion logam (Utomo dkk, 2012).
Karakteristik limbah cair karet menunjukkan limbah cair karet remah
mengandung bahan organik dan nutrien sehingga memiliki potensi menimbulkan
dampak negatif terhadap organisme yang ada di perairan lingkungan pabrik.
Limbah cair karet remah yang kaya akan unsur hara (N, P, dan K) dapat dijadikan
salah satu alternatif pengganti air laut bersih sebagai media tumbuh
Nannochloropsis sp. tanpa penambahan pupuk. Selain itu, karakteristik limbah cair karet remah dari beberapa kolam limbah seperti pH, salinitas, dan kebutuhan
nutrien telah memenuhi syarat tumbuhNannochloropsis sp.
Pada kolaminlet Rubber trapdanoutlet IPAL Anaerobik memiliki pH yang asam sehingga Nannochloropsis sp. diasumsikan tidak dapat tumbuh, sedangkan pH untuk outlet IPAL atau kolam Aerobik II memiliki pH 7,82 (Utomo, 2008).
Diduga pH untuk kolam Fakultatif II dan Aerobik I memiliki nilai pH yang
mendekati nilai pH pada kolam Aerobik II serta ketiganya memiliki salinitas 0o/oo,
maka mikroalgaNannochloropsis sp. dapat tumbuh pada ketiga media limbah cair karet remah. Namun pada kolam Fakultatif II mengandung bahan organik yang
lebih tinggi, sehingga kolam tersebut lebih berpotensi sebagai media yang optimal
5
pada limbah cair karet dapat dilakukan dengan sistem Open ponds dimana kegiatan dilakukan di ruang terbuka tanpa dinding, beratap transparan untuk
memanfaatkan cahaya matahari. Sistem ini dilakukan untuk menyesuaikan
kondisis instalasi pengolahan air limbah karet dengan harapan Nannochloropsis
sp. dapat diaplikasikan untuk penanganan limbah cair karet.
Pengendalian limbah cair secara hayati menggunakan mikroalga dianggap lebih
ramah lingkungan. Mikroalga juga memiliki kandungan minyak cukup besar dan
dapat digunakan sebagai salah satu bahan utama penghasil bahan bakar (Lubis,
2014). Mikroalga menghasilkan biomassa yang dapat dimanfaatkan menjadi
sumber energi baru, diharapkan mampu memberikan solusi masalah krisis energi.
Pemanfaatan mikroalga sebagai bahan baku biofuel khususnya biodiesel dapat
dijadikan upaya untuk memenuhi kebutuhan energi yang semakin meningkat,
dimana konsumsi bahan bakar minyak (BBM) sendiri di Indonesia tahun 2014
menurut Kementrian Energi dan Sumber Daya Mineral mencapai 34.696.383 Kilo
Liter. Hal ini mendorong upaya penyediaan bahan bakar alternatif dari sumber
nabati ini, diharapkan mampu mengurangi ketergantungan BBM tersebut.
Biodiesel adalah bahan bakar alternatif pengganti solar yang ke depan akan sangat
penting dalam mengatasi masalah krisis energi di Indonesia. Biodiesel umumnya
diproduksi dari sumber daya hayati yang mengandung lemak tinggi, salah satunya
adalah mikroalga. Mikroalga seperti Nannochloropsissp. mempunyai kandungan lipid sekitar 31-68% (Chisti, 2007). Dengan kandungan lipid yang tinggi, maka
6
agar tidak mencemari lingkungan
*Diharapkan mampu mengatasi
Gambar 1. Diagram alir pemanfaatan limbah cair karet
II. TINJAUAN PUSTAKA
A. Definisi dan Peranan Alga
Alga termasuk mikroorganisme eukariotik yang merupakan tumbuhan tingkat
rendah dan termasuk dalam anggota divisi Thallophyta (tumbuhan thallus), satu
kelompok dengan bakteri dan jamur (Cambra dan Aboal, 1992 dalam Febrianty,
2011). Pada umumnya alga bersifat fotosintetik dengan pigmen fotosintetik hijau
(klorofil), biru kehijauan (fikobilin), coklat (fikosantin), dan merah (fikoeritrin).
Secara morfologi, alga ada yang berbentuk uniseluler dan ada pula yang
multiseluler. Alga dapat hidup di permukaan atau dalam perairan (aquatik)
maupun daratan (terestrial) yang terkena sinar matahari, namun kebanyakan hidup
di perairan. Alga uniseluler (mikroskopik) dapat berupa sel tunggal atau tumbuh
dalam bentuk rantai atau filamen.
Sifat fotosintetik pada alga dapat bersifat mutlak (obligat fototrof). Oleh karena
itu, alga tumbuh di tempat-tempat yang terkena cahaya matahari (Wasetiawan,
2009). Alga tertentu dapat mengasimilasi senyawa organik sederhana dengan
menggunakan sumber energi cahaya (fotoheterotrof) (Wasetiawan, 2009). Pada
alga tertentu dapat tidak terjadi proses fotosintesa sama sekali. Dalam hal ini
pemenuhan kebutuhan nutrisi didapatkan secara heterotrof. Alga akan tumbuh
8
selama 6-8 minggu pada suhu dibawah 100C, sedangkan pada suhu diatas 200C
alga akan tumbuh selama 1-2 minggu (IACR, 1999 dalam Febrianty, 2011).
Pelczar dan Chan (1986) mendefinisikan alga sebagai organisme yang mampu
menghasilkan oksigen melalui fotosintesis dan mempunyai khloroplas. Alga juga
mengandung pigmen lain selain khloropil untuk melangsungkan fotosintesis.
Bentuk dan ukuran alga sangat beragam dari beberapa mikrometer sampai
bermeter-meter panjangnya. Alga tersebar luas di alam dan dijumpai hampir di
setiap lingkungan yang terkena sinar matahari. Kabinawa (2001), mikroalga
adalah mikroorganisme atau jasad renik dengan tingkat organisasi sel termasuk
kedalam tumbuhan tingkat rendah. Mikroalga dikelompokan dalam filum Talofita
karena tidak memiliki akar, batang dan daun sejati, namun memiliki zat pigmen
klorofil yang mampu melakukan fotosintesis. Menurut Kabinawa (2001),
mikroalga merupakan sumber daya hayati perairan yang lebih dikenal dengan
nama fitoplankton.
Menurut Loehr (1974), alga dapat menyimpan kelebihan nutrien dalam masa
selnya, oleh karena itu dapat digunakan sebagai alat untuk mengambil beberapa
nutrien yang terdapat pada hasil buangan atau limbah cair. Pengambilan nutrien
dalam sistem alga akan menghasilkan hasil yang baik apabila tersedia tanah yang
luas, cukup mendapatkan sinar matahari dan jenis alga yang ditumbuhkan cukup
mudah dipanen dan dimanfaatkan. Alga mendapatkan energi dari sinar matahari
dan menggunakan bahan anorganik seperti CO2, amonium atau fosfat dalam
sintesis pertambahan selnya. Richmond (1986) dan Kabinawa (1988) menyatakan
9
produksi, seperti protein sel tunggal (PST) baik untuk pakan maupun pangan,
asam lemak, gliserol, pigmen alami, enzim, asam amino, antibiotika, vitamin,
karoten, yodium, gas hidrogen, bahan-bahan hayati seperti metana dan
polisakarida, pupuk hayati pemurnian air limbah dan rekayasa genetika.
Diperkirakan alga mampu menghasilkan minyak 200 kali lebih banyak
dibandingkan dengan tumbuhan penghasil minyak (kelapa sawit, jarak pagar, dan
lain-lain) pada kondisi terbaiknya. Hasil riset National Renewable Energy
Laboratory Colorado menunjukkan bahwa untuk luasan areal yang sama
mikroalga dapat menghasilkan minyak 30 kali lebih banyak dibandingkan
tanaman darat. Hasil penelitian Shifrin pada tahun 1984 diperoleh bahwa rata-rata
produktivitas mikroalga secara umum dapat mencapai 15 – 25 gram/ m2/ hari.
Nilai produktivitas ini masih 10% dibawah teori hitungan maksimumnya.
Berdasarkan hal tersebut, jika diasumsikan, rendemen minyak dalam mikroalga
misalnya 30-50% dan waktu efektif 300 hari, maka untuk satu hektar lahan
budidaya dalam satu tahun akan dihasilkan minyak sebanyak 15,8-37,5 ton.
Hasil ini jauh lebih tinggi jika dibandingkan tanaman darat misalnya jarak 1,5
ton/hektar tahun atau sawit 3,3 - 6,0 ton/hektar/tahun (Rahardjo, 2008).
Mikroalga dapat menjadi solusi yang nyata untuk mengganti solar. Hal ini karena
tidak ada cadangan bahan baku lain yang cukup memiliki banyak minyak
sehingga mampu digunakan untuk memproduksi minyak dalam jumlah yang
besar. Sebagai perbandingan dengan tumbuhan di daratan, tumbuhan seperti
kelapa sawit dan kacang kacangan membutuhkan lahan yang sangat luas untuk
10
negara. Hal ini tidak nyata dan akan mengalami kendala apabila
diimplementasikan pada negara dengan luas wilayah yang kecil. Berdasarkan
perhitungan, pengolahan alga pada lahan seluas 10 juta acre (1 acre =0.4646 ha)
mampu menghasilkan biodiesel yang akan dapat mengganti seluruh kebutuhan
solar di Amerika Serikat. Luas lahan ini hanya 1% dari total lahan yang sekarang
digunakan untuk lahan pertanian dan padang rumput (sekitar 1 milliar acre)
(Rahardjo, 2008).
B. Faktor-Faktor yang Mempengaruhi Pertumbuhan Alga
Pertumbuhan alga dapat dipengaruhi oleh faktor eksternal seperti faktor
lingkungan. Faktor lingkungan yang mempengaruhi laju pertumbuhan alga
diantaranya adalah suhu, cahaya, pH, dan konsentrasi elemen-elemen esensial
atau nutrien yang dipakai untuk fotosintesis.
1. Suhu
Suhu juga sangat berperan mengendalikan kondisi ekosistem perairan. Organisme
akuatik memilki kisaran suhu tertentu (batas atas dan batas bawah) yang disukai
bagi pertumbuhannya. misalnya alga dari filum Chlorophyta akan tumbuh dengan
baik pada kisaran suhu 200C-300C (Goldman dan Horne, 1983). Skala suhu untuk
pertumbuhan alga Cladophora antara 150C-250C (Harris 2005 dalam Summers,
2008). Tidak terlalu signifikan pertumbuhan filamentus alga lainnya yang
ditemukan pada beberapa sungai dengan air yang dingin (suhu maksimum 200C)
11
2. Cahaya
Cahaya sangat mempengaruhi tingkah laku organisme akuatik. Alga planktonik
menunjukkan respon yang berbeda terhadap perubahan intensitas cahaya. Pigmen
klorofil menyerap cahaya biru dan merah, karoten menyerap cahaya biru dan
hijau, fikoeritrin menyerap warna hijau, dan fikosianin menyerap cahaya kuning.
Menurut Wells et al. (1999), di perairan cahaya memiliki dua fungsi utama yaitu memanasi air sehingga terjadi perubahan suhu dan berat jenis (densitas) dan
selanjutnya menyebabkan terjadinya pencampuran massa dan kimia air, dan
merupakan sumber energi bagi proses fotosintesis alga dan tumbuhan air.
Menurut BBPBL (2007), kedalaman kolam kulitvasi sebaiknya tidak lebih dari 1
meter karena apabila kedalaman lebih dari 1 meter dikhawatirkan daya tembus
cahaya tidak sampai ke dasar kolam. Apabila sinar matahari tidak sampai ke
dasar, maka fitoplankton yang dikultur akan mempunyai laju pertambahan sel
yang lambat atau bahkan bisa mati.
3. pH
pH juga mempengaruhi toksisitas suatu senyawa kimia. Senyawa amonium yang
dapat terionisasi banyak ditemukan pada perairan yang memiliki pH rendah.
Amonium bersifat tidak toksik. Namun, pada suasana alkalis (pH tinggi) lebih
banyak ditemukan amonia yang tak terionisasi dan berifat toksik (Tebbut, 1992).
Pada pH kurang dari 4, sebagian besar tumbuhan air mati karena tidak dapat
bertoleransi terhadap pH rendah (Haslam, 1995). Fitoplankton dapat berkembang
12
4. Nutrien
Suplai nutrien berasal dari hasil dekomposisi bahan organik dan regenerasi dari
nutrien, dan oleh pengadukan vertikal air yang memungkinkan sediaan nutrien
yang tersimpan di lapisan air di bawah dapat dimanfaatkan di lapisan air
permukaan. Asimilasi nutrien untuk pertumbuhan tumbuhan akan mengurangi
konsentrasinya di perairan, yang kelak pada saat nutrien sangat rendah maka laju
produksi menjadi terbatas. Riley et al. (1949) dalam Goldman & Horne (1983) menyatakan bahwa laju populasi fitoplankton di perairan dibatasi oleh konsentrasi
fosfat. Nitogen dan Fosfor akan menyatu di dalam struktur sel alga dengan rasio
N:P yaitu 16:1 (Redfield 1958 dalam Summers, 2008). Menurut Frandy (2009),
komposisi nutrien dalam pupuk yang mendukung pertumbuhan alga adalah
komposisi pupuk dengan rasio N:P yang rendah.
a. Nitrogen
Beberapa alga dapat menggunakan NO3-, NO2- atau NH4+ sebagai sumber
nitrogen. Nitrat (NO3) merupakan bentuk nitrogen utama di perairan alami dan
juga merupakan nutrien utama bagi pertumbuhan tanaman dan alga. Nitrat dan
amonium adalah sumber utama nitrogen di perairan. Namun, amonium lebih
disukai oleh tumbuhan. Amonium biasanya diikuti dengan nitrat yang besar pula
karena konsentrasi NH4+ diatas 0,5–1,0 μ mol/l akan menghambat pengambilan
NO3- (Darley, 1982). Keseimbangan antara amonium dan amonia di dalam air
sangat dipengaruhi oleh nilai pH air. Pada pH 6, yang terdapat dalam air adalah
100% amonium, pada pH 7 perbandingan antara keduanya adalah 1% amonia dan
99% amonium, pada pH 8 terdapat 4% amonia dan 96% amonium, pada pH 9
13
semakin tinggi nilai pH akan menyebabkan keseimbangan antara amonium
dengan amonia semakin bergeser ke arah amonia, artinya kenaikan pH akan
meningkatkan konsentrasi amonia (Barus, 2002). Kandungan nitrat-nitrogen yang
lebih dari 0,2 mg/l dapat mengakibatkan terjadinya pengayaan nutrien, sehingga
dapat menstimulir pertumbuhan alga dan tumbuhan air di perairan tersebut secara
cepat (Darley, 1982). Menurut Boyd (1988), fitoplankton lebih banyak
memanfaatkan unsur N dibanding unsur P
b. Fosfor
Fosfat merupakan bentuk fosfor yang dapat dimanfaatkan oleh tumbuh-tumbuhan
(Dugan, 1972). Fosfor juga merupakan unsur yang esensial bagi tumbuhan
tingkat tinggi dan alga, sehingga unsur ini menjadi faktor pembatas bagi
tumbuhan dan alga serta sangat mempengaruhi tingkat produktivitas perairan
(Goldman & Horne, 1983). Ortofosfat, PO4-3, merupakan fosfor anorganik
sumber P yang sangat penting untuk pertumbuhan alga. Walaupun sumber P
lebih dapat diperoleh dari berbagai macam fosfat organik. Beberapa alga
menyediakan PO4-3sebagai polyfosfat dalam butiran sitoplasmik dengan diameter
sebesar 30–500 nm. Alga akan tumbuh di permukaan air dibatasi oleh keberadaan
fosfor di perairan tersebut (Summers, 2008). Idealnya, kondisi pertumbuhan alga
pada musim panas dapat terjadi dengan adanya konsentrasi fosfat anorganik
kurang dari 0,005–0,01 mg/l (Kawaga 1989 dalam Summers, 2008).
C. Nannochloropsissp.
14
Kingdom : Chromista
Super Divisi : Eukaryotes
Divisi : Chroniophyta
Kelas : Eustigmatophyceae
Ordo : Eustigmatales
Famili : Monodopsidaceae
Genus :Nannochloropsis
Spesies :Nannochloropsissp.
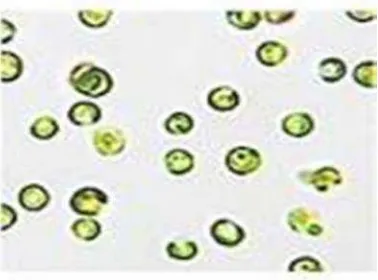
Nannochloropsis sp. merupakan mikroalga berwarna kehijauan, selnya berbentuk bola, berukuran kecil dengan diamater 2-4 μ m, memiliki 2 flagel dengan salah
satu flagelnya berambut tipis. Ciri khas dariNannochloropsissp. adalah memiliki dinding sel yang terbuat dari komponen selulosa (Fachrullah, 2011). Bentuk
Nannochloropsissp.dapat dilihat pada Gambar 2
Gambar 2. BentukNannochloropsissp. (Waggoner dan Speer, 1999 dalam Nindri, 2013).
Nannchloropsis sp. memiliki kandungan lemak yang cukup tinggi (31-68%), sedangkan Isochrysis (17,07%) dan Dunaliella hanya (6%) (Erlania, 2010). Kandungan lemak mikroalga tergantung dari jenis mikroalga, rata-rata
15
membutuhkan cahaya untuk berfotosintesis. Kurangnya cahaya yang dibutuhkan
untuk aktifitas fotosintesis akan menyebabkan proses fotosintesis tidak
berlangsung normal sehingga mengganggu metabolisme selanjutnya (Andriyono,
2001). Periode penyinaran dapat berpengaruh dalam proses sintesa bahan organik
pada fotosintesis karena hanya dengan energi yang cukup proses tersebut dapat
berjalan dengan lancar.
Tabel 1. Kadar minyak pada mikroalga
Jenis Alga Kadar Minyak (% bk)
Botryococcus braunii 25–75
Pertumbuhan Nannochloropsissp. dipengaruhi oleh lingkungan seperti suhu, pH, salinitas, juga kandungan nitrogen yang ada di media kultur (Gunawan, 2012).
Perubahan salinitas dan CO2pada tahap kedua dapat meningkatkan kepadatan dan
mengubah kandungan lipid. Nannochloropsis sp. membutuhkan nitrogen sebagai makronutrien untuk pertumbuhannya. Yanuaris dkk. (2012) menyatakan bahwa
ketersediaan unsur nitrogen mempengaruhi pertumbuhan Nannochloropsis sp. Pemenuhan sumber hara (N, P, dan K) yang mencukupi kebutuhan dapat
16
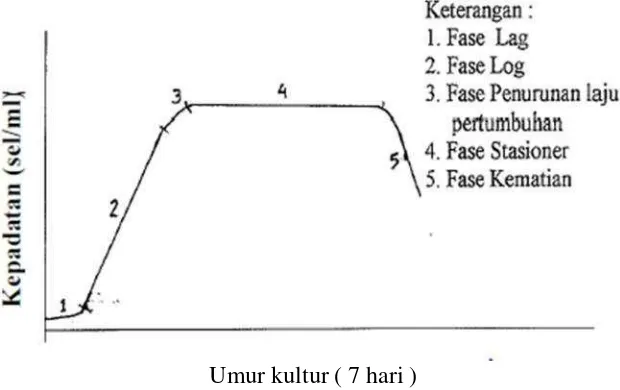
Kurva pertumbuhanNannochloropsissp. dapat dilihat dalam Gambar 3.
Umur kultur ( 7 hari )
Gambar 3. Kurva pertumbuhanNannochloropsissp. (Pujiastuti, 2010). Pujiastuti (2010) membagi pola pertumbuhan atau kurva pertumbuhan tersebut
menjadi 5 fase pertumbuhan sebagai berikut:
1. Pada fase lag penambahan jumlah densitas fitoplankton sangat rendah atau
bahkan dapat dikatakan belum ada penambahan densitas. Hal tersebut
disebabkan karena sel-sel fitoplankton masih dalam proses adaptasi secara
fisiologis terhadap medium tumbuh sehingga metabolisme untuk tumbuh
manjadi lamban.
2. Pada fase log/eksponensial, terjadi pertambahan kepadatan sel fitoplankton (N)
dalam waktu (t) dengan kecepatan tumbuh (μ ) sesuai dengan rumus
eksponensial.
3. Pada fase penurunan kecepatan tumbuh pembelahan sel mulai melambat
karena kondisi fisik dan kimia kultur mulai membatasi pertumbuhan.
4. Pada fase stasioner, faktor pembatas dan kecepatan tumbuh sama karena
17
5. Pada fase kematian, kualitas fisika dan kimia media kultur berada pada titik
dimana sel tidak mampu lagi mengalami pembelahan.
D. Karakteristik Limbah Cair Karet Remah
Limbah cair didefinisikan sebagai buangan cair yang berasal dari suatu
lingkungan masyarakat dan lingkungan industri dimana komponen utamanya
adalah air yang telah digunakan dan mengandung benda padat yang terdiri dari
zat-zat organik dan anorganik (Mahida, 1984). Menurut Tchobanoglous dan
Burton (1991), berdasarkan asalnya limbah cair dapat dibedakan empat macam
yaitu air limbah rumah tangga (domestic waste), air limbah industri (indutrial waste), rembesan air tanah lewat saluran dan luapan air hujan. Limbah cair pengolahan karet alam, tergantung pada jenis karet yang dihasilkan, merupakan
buangan pabrik yang bersumber dari koagulasi, penggilingan dan pencucian.
Limbah cair yang dihasilkan mengandung bahan organik yang berasal dari serum
dan partikel karet yang belum terkoagulasi. Serum karet mengandung protein,
gula, lemak, garam anorganik, dan mikroorganisme (Nasrudin dan Faimin, 1992).
Di antara beberapa jenis polutan, kandungan bahan organik dalam suatu limbah
yang masuk ke dalam badan air bebas perlu mendapat perhatian sebab dapat
mengancam kehidupan biologis pada badan air tersebut.
Tabel 2. Karakteristik limbah cair karet remah berbahan baku lateks kebun
Parameter Satuan BakuMutu* Hasil Analisis Inlet Rubber tap
18
Kandungan bahan organik yang sangat tinggi memungkinkan terjadinya proses
oksidasi bahan organik oleh mikroorganisme dalam badan air. Proses tersebut
akan menggunakan oksigen bagi kehidupan di lingkungan tersebut berkurang. Hal
ini dapat membawa kematian makhluk hidup di dalamnya (Tchobanoglous dan
Burton, 1991). Adapun parameter dan baku mutu air limbah outlet Unit Pabrik
karet Way Berulu terdapat pada Tabel 3.
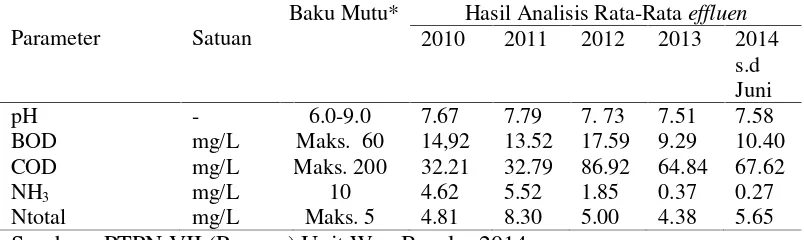
Tabel 3. Parameter dan baku mutuoutletair limbah unit pabrik karet Way Berulu
Parameter Satuan
Baku Mutu* Hasil Analisis Rata-Rataeffluen
2010 2011 2012 2013 2014 s.d Juni
pH - 6.0-9.0 7.67 7.79 7. 73 7.51 7.58
BOD mg/L Maks. 60 14,92 13.52 17.59 9.29 10.40 COD mg/L Maks. 200 32.21 32.79 86.92 64.84 67.62
NH3 mg/L 10 4.62 5.52 1.85 0.37 0.27
Ntotal mg/L Maks. 5 4.81 8.30 5.00 4.38 5.65
Sumber : PTPN VII (Persero) Unit Way Berulu, 2014
E. Nutrien Limbah Karet
Nutrien yang dibutuhkan dalam jumlah yang besar untuk pertumbuhan alga
adalah karbon, fosfor, nitrogen dan besi yang diabsorbsi oleh tanaman. Beberapa
nutrien yang terkandung dalam limbah karet antara lain:
1. Nitrogen
Nitrogen terlarut dalam sistem cairan dan limbah cair yang kemudian dikonversi
menjadi beberapa bentuk yaitu amonia (NH3), ion nitrit (NO2-), ion nitrat (NO3-),
dan molekul organik seperti asam amino melalui proses bebas (NH3) yang bersifat
toksik terhadap ikan terutama pada konsentrasi 1 mg/L (Verstraeta dan
19
paling dominan dan selanjutnya berturut-turut adalah amonia dan nitrit. Sifat
yang mudah dioksidasi dan atau direduksi oleh berbagai proses lingkungan dari
semua bentuk nitrogen, sehingga dapat ditemui pada berbagai jenis lingkungan.
Adanya senyawa nitrogen dalam air yang khususnya berupa nitrogen-amonia
(N-NH4+) dapat dijadikan petunjuk adanya pencemaran. Nitrogen amonia merupakan
indikasi tentang kemungkinan pencemaran yang masih baru, sedangkan absennya
senyawa ini yang diikuti oleh senyawa nitrat dapat digunakan sebagai indikasi
pencemaran yang telah lama (Wisjnuprapto, 1988).
Konsentrasi kritis dari amonia pada sistem perairan tidak dibatasi yang artinya
pada semua konsentrasi dapat menimbulkan gangguan, kecuali sifat racun
terhadap ikan yang tergantung pada pH dan suhu dari sistem perairan tersebut
(Metcalf dan Eddy, 1991). Amonia bersifat sangat beracun terhadap mamalia dan
pada konsentrasi 0,2 mg/L berbahaya terhadap sejumlah organisme akuatik
(Sawyeret. al., 1994). Menurut Metcalf dan Eddy (1991), senyawa nitrat (NO3-) yang terdapat dalam sistem perairan menimbulkan gangguan dengan menstimulasi
pertumbuhan alga dan organisme akuatik lain dengan konsentrasi 0,9 mg/L, dan
dapat menimbulkan gangguan pada bayi (blue babbies) dengan konsentrasi kritis 45 mg/L.
2. Fosfor
Fosfor bersifat larut dalam sistem perairan akibat proses pelapukan batuan dan
pada saat melarut ortofosfat dapat menjadi tiga bentuk yaitu H3PO4-, H2PO4-,
HPO42- yang tergantung pada pH sistem dan pH netral bentuk yang dominan
adalah H2PO4-, dan HPO42-(Waite,1984). Senyawa fosfor yang terdapat dalam
20
pertumbuhan ganggang dan organisme akuatik dengan konsentrasi kritis 0,015
mg/L, mengganggu proses koagulasi dengan konsentrasi kritis 0,2-0,4 mg/L, dan
menganggu proses pelunakan air menggunakan soda kapur dengan konsentrasi
kritis 0,3 mg/L (Metcalf dan Eddy, 1991). Konsentrasi 0,5 mg/L PO4 dapat
mencegah pertumbuhan alga, sedangkan pertumbuhan alga dapat dihentikan pada
konsentrasi PO4di bawah 0,005 mg/L (Chen dan Fuhs, 1975).
F. Open Ponds System
Open ponds merupakan sistem budidaya mikroalga tertua dan paling sederhana. Sistem tersebut sering dioperasikan secara kontinyu. Umpan segar (mengandung
nutrisi termasuk nitrogen, phosphor, dan garam inorganik) ditambahkan di depan
paddlewheel dan setelah beredar melalui loop-loop mikroalga tersebut dapat dipanen di bagian belakang dari paddlewheel. Paddlewheel digunakan untuk
proses sirkulasi dan proses pencampuran mikroalga dengan nutrisi. Beberapa
sumber limbah cair dapat digunakan sebagai kultur dalam budidaya mikroalga.
Pemilihan sumber limbah cair tersebut berdasarkan pemenuhan kebutuhan nutrisi
dari mikroalga. Mikroalga laut dapat menggunakan air laut atau air dengan
tingkat salinitas tinggi sebagai media kultur. Biaya operasional sistemopen ponds
lebih rendah dibandingkan dengan sistemphotobioreactor, namun sistem tersebut memiliki beberapa kelemahan. Open ponds merupakan sistem kolam terbuka sehingga mengalami evaporasi akut, dan penggunaan karbon dioksida (CO2)
menjadi tidak efisien. Produktivitas mikroalga juga dibatasi oleh kontaminasi dari
21
Gambar 4. Bentuk reaktor (Iswara, 2011).
Sistem kultivasi terbuka (Open Ponds) dapat diartikan sebagai berikut: a. Dapat dikategorikan menjadi:
b. Sistem kolam terbuka alami yang memanfaatkan sungai, danau, kolam sebagai
tempat kultivasi
c. Dapat pula menggunakan sistem buatan dengan membuat kolam buatan atau
wadah kultivasi
- Keuntungan: kemudahan dalam konstruksi dan pengoperasiannya
- Kendala
• Sering terjadi efekself-shadingdalam sel • CO2yang terdifusi ke atmosfer
• Area yang dibutuhkan luas
• Sering terjadi kontaminasi dari luar
• Mekanisme pengadukan yang kurang efisien, laju transfer masaa kurang
III. METODE PENELITIAN
A. Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan pada bulan Januari - Februari 2015 di Balai Besar
Pengembangan Budidaya Laut Lampung dan Laboratorium Pengelolaan Limbah
Agroindustri Jurusan Teknologi Hasil Pertanian Fakultas Pertanian Universitas
Lampung.
B. Alat dan Bahan
Bahan-bahan yang digunakan sebagai media kultivasi dalam penelitian ini adalah
limbah cair karet remah yang berasal dari Instalansi Pengolahan Air Limbah
(IPAL) Unit Usaha Way Berulu berupa air limbah dari outletkolam Fakultatif II, kolam Aerobik I, dan kolam Aerobik II. Mikroalga yang digunakan adalah
Nannochloropsissp.yang berasal dari Balai Besar Pengembangan Budidaya Laut Lampung serta bahan kimia sebagai penunjang analisis N-NH3, Ntotal, P-PO4,
dan COD.
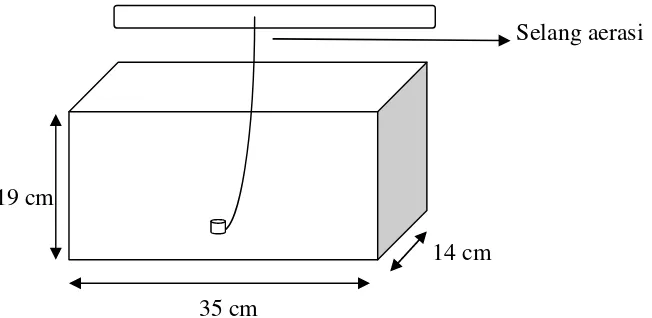
Alat-alat yang digunakan dalam penelitian ini berupa reaktor terbuka (Gambar 5)
sebagai pertumbuhan mikroalga yang terbuat dari kaca ukuran (35x14x19) cm
23
spektrofotometri DR 4000, DRB 200, pH meter, DO meter, oven, desikator dan
alat penunjang lainnya.
C. Metode Penelitian
Penelitian ini dilaksanakan dalam dua tahap yaitu tahap pertama adalah
karakterisasi limbah cair. Limbah cair yang digunakan adalah outlet limbah cair karet remah (LCKR) Fakultatif II (F2), outlet LCKR kolam Aerobik I (Ae1), dan
outlet LCKR kolam Aerobik II (Ae2) dengan volume kerja masing-masing 5 L sebagai tiga taraf perlakuan media pertumbuhan Nannochloropsissp. Tahap yang kedua adalah tahap kultivasi. Pada tahap ini yang dilakukan adalah
mempersiapkan isolat Nannochloropsissp. sebanyak 25% v/v kerja pada masing-masing media yang dikultivasi dilakukan selama 8 hari. Setiap perlakuan diulang
sebanyak tiga kali sehingga menghasilkan 3x3=9 satuan percobaan. Data hasil
analisis yang diperoleh disajikan dalam bentuk tabel dan grafik serta dianalisis
secara deskriptif.
Selang aerasi
19 cm
14 cm
35 cm
24
D. Pelaksanaan Penelitian
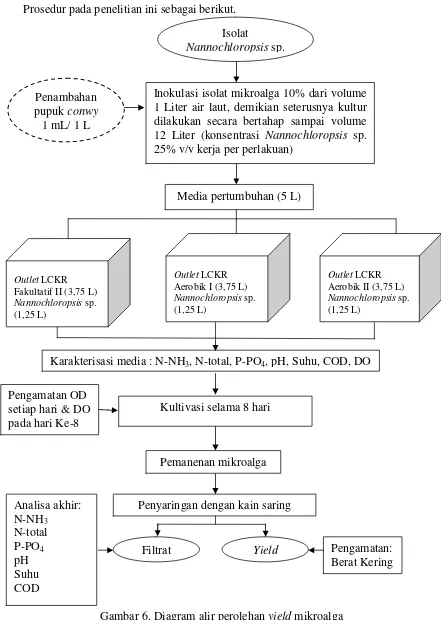
Prosedur pada penelitian ini sebagai berikut.
Gambar 6. Diagram alir perolehanyieldmikroalga Isolat
Nannochloropsissp.
Inokulasi isolat mikroalga 10% dari volume 1 Liter air laut, demikian seterusnya kultur dilakukan secara bertahap sampai volume 12 Liter (konsentrasi Nannochloropsis sp. 25% v/v kerja per perlakuan)
Penambahan pupukconwy
1 mL/ 1 L
Media pertumbuhan (5 L)
Karakterisasi media : N-NH3, N-total, P-PO4, pH, Suhu, COD, DO
25
1. Karakterisasi Media
Media yang digunakan untuk kultivasi mikroalga adalah limbah cair karet remah
yang berasal dari Instalansi Pengolahan Air Limbah (IPAL) Unit Usaha Way
Berulu berupa limbah cair dari outlet kolam Fakultatif II, kolam Aerobik I dan kolam Aerobik II. Sebelum digunakan sebagai media kultivasi Nannochloropsis
sp., limbah cair karet dianalisis untuk mengetahui nilai awal dari N-NH3,N-total,
P-PO4, pH, suhu, kandungan Chemical Oxygen Demand (COD), dan Dissolved
Oxygen (DO). Media limbah cair yang digunakan dikultivasi pada reaktor seperti diperlihatkan pada Gambar 5.
2. Persiapan Inokulum
Isolat Nannochloropsissp. sebanyak 1 Liter dikultur ke dalam 3 Liter media air laut yang telah disterilisasi dalam waktu 4–7 hari. Setelah itu, kultur stock yang
didapatkan dikultur kembali dengan membagi menjadi 3 wadah kultur, dimana 1
Liter kultur stock dikultur ke dalam 3 Liter media air laut selama 4-7 hari untuk
mencapai volume kultur Nannochloropsis sp. 12 Liter dengan kepadatan mencapai 106 sel/ml media. Konsentrasi Nannochloropsis sp. yang digunakan sebesar 25% v/v kerja per perlakuan atau sebanyak 11,25 Liter untuk seluruh
perlakuan.
3. Kultivasi Alga
Pelaksanaan kultivasi mikroalga dilakukan dengan sistem kolam terbuka.
Kultivasi dilakukan dengan memasukkan inokulum mikroalga hasil dari
perbanyakan dengan konsentrasi mikroalga 25% dari volume media limbah cair
26
dilakukan sirkulasi menggunakan selang aerasi sebagai sumber O2/CO2 dan
sekaligus berfungsi sebagai pengaduk (sirkulasi) air media pertumbuhan.
4. Pengamatan
Pengamatan yang dilakukan terbagi menjadi beberapa waktu. Pengamatan yang
dilakukan sebelum media dikultivasi adalah analisa N-NH3, N-total, P-PO4, pH,
suhu, kandungan Chemical Oxygen Demand (COD), dan Dissolved Oxygen
(DO). Pengamatan yang dilakukan setiap harinya adalah kepadatan biomassa
(OD), sedangkan pengamatan yang dilakukan setelah kultivasi adalah analisa
N-NH3, N-total, P-PO4, pH, suhu, kandungan Chemical Oxygen Demand (COD),
Dissolved Oxygen(DO) dan perolehanYieldkering.
a. Kepadatan mikroalgaNannochloropsissp.
Perhitungan kepadatan mikroalga Nannocholorpsis sp. dilakukan dengan menggunakan Haemacytometer pada Microscop Olympus CX31 dengan bantuan
Handcounter(Pratama, 2011).
b. Analisis Nitrogen Total - N-NH3(SNI, 2005)
Analisis N-NH3dilakukan dengan tahapan sebagai berikut :
Sampel limbah cair sebanyak 25 mL disaring dengan kertas saring berdiameter
0,45 um dimasukkan ke dalam erlenmeyer 100 mL. Kemudian, ditambahkan 1
mL larutan fenol, 1 mL larutan nitroprusid dan 2,5 mL larutan oksidator, dikocok
dan didiamkan 10 menit. Pengukuran dilakukan dengan Spektrofotometri pada
27
- Nitrit (NO2) (SNI, 2004)
Sampel limbah cair sebanyak 25 mL disaring dengan kertas saring berdiameter
0,45 um dimasukkan ke dalam erlenmeyer 100 mL. Kemudian, ditambahkan 1
mL larutan pewarna, dikocok dan didiamkan 10 menit. Pengukuran dilakukan
dengan Spektrofotometri pada panjang gelombang 543 nm.
- Nitrat (NO3) (SNI, 2002)
Sampel limbah cair sebanyak 5 mL yang sudah disaring dengan kertas Whatman paperno. 42 dimasukkan ke dalambeaker glass50 mL. Kemudian, ditambahkan 1 tetes sodium arsenit, 0,25 mL brucine dan 5 mL larutan asam sulfat, dikocok
dan didiamkan 10 menit. Pengukuran dilakukan dengan Spektrofotometri pada
panjang gelombang 410 nm.
c. Analisis P-PO4(SNI, 2005)
Metode yang digunakan dalam analisis P-PO4 adalah dengan menggunakan
Pereaksi P pekat (larutan amonium molibdat). Sampel 25 mL dimasukkan ke
dalam tabung reaksi. Ditambahkan 1 mL Pereaksi P pekat dan 5 tetes larutan
SnCl2 ke dalam sampel, dikocok dan didiamkan selama 10 menit. Kemudian
diukur dengan alat spektrophotometer pada panjang gelombang 690 nm.
d. Analisis pH
Pengamatan pH mengacu pada SNI (2004), yaitu dengan menggunakan pH meter.
Sebelum pengukuran dilakukan, pH meter dikalibrasi dengan larutan penyangga.
Keringkan dengan tisu selanjutnya bilas elektroda dengan air suling. Dicelupkan
elektroda kedalam media uji sampai pH meter menunjukkan pembacaan yang
28
e. Analisis COD (HACH Company, 2004)
Analisis COD limbah cair karet remah dilakukan dengan cara 0,2 mL larutan
sampel (standar tanda pengenceran) diambil kemudian ditambahkan 5 mL larutan
reagen COD (larutan pencerna 1,5 mL + larutan pereaksi asam sulfat 3,5 mL).
Selanjutnya dipanaskan pada DRB 200 dengan suhu 150oC selama 2 jam
kemudian didinginkan selama 30 menit. Kemudian diukur kadar COD dengan alat
HACH spektrophotometri DR 4000 pada panjang gelombang 420 nm.
f. Analisis DO (SNI, 2005)
Cara penentuan oksigen terlarut dengan metoda elektrokimia adalah cara langsung
untuk menentukan oksigen terlarut dengan alat DO meter. Cara penggunaannya
alat ini adalah dengan mencelupkan alat DO meter tersebut ke dalam sampel air
yang diukur dan melihat skala yang terlihat.
g. YieldKering
Analisis Yield dilakukan setelah mikroalga dipanen dengan menghitung berat basah dan berat kering dari mikroalga. Untuk memperoleh yield kering, maka dilakukan pengukuran kadar air yield basah terlebih dahulu yang sebelumnya dilakukan penimbangan berat basah. Adapun pengukuran kadar air dapat
dilakukan dengan cara : Cawan Porselin dikeringkan terlebih dahulu selama 1 jam
dalam oven pada suhu 105°C, lalu didinginkan dalam desikator dan kemudian
beratnya ditimbang (x). Sampel basah ditimbang (y), dimasukkan ke dalam
cawan yang telah ditimbang, kemudian dimasukkan ke dalam oven selama 4 – 6
jam pada suhu 105°C, lalu didinginkan dalam desikator dan ditimbang kembali.
29
berturut-turut kurang dari 0,2 mg) (Sulaeman et al, 2005). Adapun rumus penentuan kadar air sebagai berikut:
Kadar Air =( )x 100%
Perhitungan perolehanyieldkering sampel dapat dilakukan dengan rumus :
V. KESIMPULAN DAN SARAN
A. Kesimpulan
1. Berdasarkan penelitian yang telah dilakuan dapat disimpulkan bahwa outlet
limbah cair karet yang berasal dari kolam Fakultatif II, Aerobik I dan Aeorbik
II dapat digunakan sebagai media pertumbuhan mikroalga.
2. Perlakuan dengan menggunakan media limbah cair dari outlet kolam Fakultatif II merupakan perlakuan terbaik karena memiliki tingkat kepadatan
sel Nannochloropsis sp. paling tinggi yaitu mencapai 3,3 x 107 sel/mL dan dapat menurunkan kandungan bahan organik limbah cair karet remah berupa
N-NH3mencapai 98%, P-PO489%, N-total 92%, serta perolehan yield kering
sebesar 0,87 g/L.
B. Saran
Perlu dilakukan penelitian lanjutan mengenai jenis mikroalga yang berpotensi
DAFTAR PUSTAKA
Andriyono, S. 2001. Pengaruh periode penyinaran terhadap pertumbuhan
isochrysis galbanaklon tahiti.(Skripsi). Institut Pertanian Bogor. Bogor. Badan Standarisasi Nasional. 2002. Metode Pengujian Kadar Nitrat dalam Air
Secara Kolorimetri SNI 03-6856-2002. Badan Standardisasi Nasional. Jakarta.
Badan Standarisasi Nasional. 2004. Cara Uji Derajat Nitrit (NO2-N) dengan Spektrofototmetri SNI 06-6989.9-2004. Badan Standardisasi Nasional. Jakarta.
Badan Standarisasi Nasional. 2004. Cara Uji Derajat Keasaman (pH) dengan Menggunakan Alat pH Meter SNI 06-6989.11-2004. Badan Standardisasi Nasional. Jakarta.
Badan Standarisasi Nasional. 2004. Cara Uji Oksigen Terlarut secara Yodometri SNI 06-6989.14-2004. Badan Standardisasi Nasional. Jakarta.
Badan Standarisasi Nasional. 2005. Cara Uji Kadar Amonia dengan Spektrofototmeter secara fenat SNI 06-6989.30-2005. Badan Standardisasi Nasional. Jakarta.
Badan Standarisasi Nasional. 2005. Cara Uji Kadar Fosfat dengan Spektrofototmeter secara asam askorbat SNI 06-6989.31-2005. Badan Standardisasi Nasional. Jakarta.
Barus, T.A. 2002.Pengantar Limnologi. Jurusan Biologi FMIPA USU. Medan. Balai Besar Pengembangan Budidaya Laut. 2007. Budidaya Fitoplankton &
Zooplankton. Balai Besar Pengembangan Budidaya Laut. Lampung. 4-42 hlm.
49
Chen and Fuhs, G.W. 1975. Microbiological Basis of Phospore Removal in the Activated Sludge Process for the Treatment of Waste water.EcologyVol.2. 1975. Springer Verlag. New York. Inc.
Chisti, Y. 2007. Biodiesel from microalgae. Biotechnology Advances 25(3):294-306.
Darley, W.M. 1982. Algal Biology: A Physiological Approach. Department of Botany. The University of Georgia.
Dessy, A. dan Noer, A.H. 2010. Mikroalga Sebagai Sumber Biomasa Terbarukan:Teknik Kultivasi Dan Pemanenan. Jurnal Teknik Kimia. Universitas Diponegoro. Semarang.
Dugan, P.R. 1972. Biochemical Ecology of Water Pollution Control. 2nd edition. McGraw-Hill, Inc., New York. Pp 400.
Erlania. 2010. Penyimpanan RotiferaInstan (Branchionus rotundiformis) pada Suhu yangBerbeda dengan Pemberian PakanMikroalga Konsentrat. J. Ris. Akuakultur5: 287-297
Fachrullah, M.R. 2011. Laju pertumbuhan mikroalga penghasil biofuel jenis
Chlorellasp. danNannochloropsissp. yang dikultivasi menggunakan air limbah hasil penambangan timah di Pulau Bangka.(Skripsi). Fakultas Perikanan dan Ilmu Kelautan. IPB. Bogor. 3-11 pp.
Febrianty, E. 2011. Produktivitas alga hydrodictyon pada sistem perairan tertutp (closed system).(Skripsi). Institut Pertanian Bogor. Bogor.
Fitri, Kurniati. 2011. Peran Chlorella vulgarisdalam Pengelolaan Lingkungan (Kajian Penggunaan untuk Menurunkan Nitrogen Amonia Air Limbah Domestik dan Potensinya sebagai Bahan Minyak Biodiesel).(Tesis). Departemen Teknik Kimia Universitas Indonesia. Depok.
Frandy, Y.H.E. 2009. Dinamika komunitas plankton dan potensinya sebagai pakan alami di kolam pemeliharaan larva ikan nilem (Osteochilus hasselti
C.V.). (Skripsi). Institut Pertanian Bogor. Bogor.
Goldman, C.R & Horne, A.J. 1983.Limnology. McGraw-Hill Book Company. Gunawan. 2012. Pengaruh Perbedaan pH pada Pertumbuhan Mikroalga Kelas
Chlorophyta.Jurnal Bioscientiae 9: 62–65.
50
Haslam, S.M. 1995. River Pollution and Ecological Perspective. John Wiley and Sons, Chichester, UK. Pp 253.
Isnansetyo, A dan Kurniastuty. 1995.Teknik Kultur Phytoplankton dan Zooplankton Pakan alami untuk Pembenihan Organisme Laut. Kanisius.Yogyakarta.
Iswara, A.P. 2011. Pengaruh Aerasi dan Pencahayaan Alami padaKemampuan High Rate Algae Reactor (HRAR) dalamPenurunan Bahan Organik Limbah DomestikPerkotaan. Makalah Presentasi. Institut Teknologi Sepuluh Nopember. Surabaya.
Kabinawa, I.N.K. 1988. Mikroalga: Sumber Berbagai Produksi. Suara Pembaharuan, 4 Maret 1988. Jakarta.
Kabinawa, I.N.K. 1999. Konsep Penanggulangan Limbah Cair dengan Mikroalga,
Prosiding Seminar Nasional, Teknologi Proses Kimia I, Jurusan Teknik Gas & Petrokimia, Ui, Depok. 104-111 hlm.
Kabinawa, I.N.K.2001. Mikroalga Sebagai Sumber Daya Hayati Perairan dalam Persepektif Bioteknologi. Puslitbang- Biotek. LIPI. Bogor.
Kementrian Energi dan Sumber Daya Mineral. 2014. Realisasi Penjualan Bbm di Seluruh Indonesia. Jakarta.
Komala, P.S., Helard, D., Delimas, D. 2012. Identifikasi Mikroba Anaerob Dominan padaPengolahan Limbah Cair Pabrik Karet dengan SistemMulti Soil Layering (MSL).Jurnal Teknik LingkunganUNAND 9 (1) : 74-88 Loehr,R.C.1974. Agriculture Waste Management; Proplem, Process and
Approach. Academic Press. New York.
Lubis, D.F. 2014. The Identification of Potential Microalga as Degradable Agent in the Rubber Waste PT. Ricry, Pekanbaru. Jurnal. Universita Riau. Pekanbaru.
Mahida, U.N. 1984. Pencemaran Air dan Pemanfaatan Limbah Industri. C.V. Rajawali, Jakarta.
Mara, D., Mills, S.W., Pearson, H.W,.&Alabaster, G.P. 2007. WasteStabilization Ponds : a ViableAlternative for Small CommunityTreatment Systems. Water andEnvironmentJournal,74.
Metcalf dan Eddy.1991. WastewaterEngineering: Treatment Disposal Reuse. McGraw-Hill Book Co. Singapore.
51
Neraca, 2015. Kemenperin Siapkan Langkah Dorong Konsumsi Karet Alam. Harian Ekonomi Neraca, Jakarta. Diakses 14 Mei 2015 http://www.neraca.co.id/article/53663/kemenperin-siapkan-langkah-dorong-konsumsi-karet-alam.
Nindri, Y. 2013. Pengaruh salinitas dan nitrogenterhadap kandungan protein total
Nannochloropsis sp.(Skripsi). Program Studi Budidaya PerairanFakultas Pertanian Universitas Lampung. Lampung. 6 pp.
Palmer, C.M. 1985.Key For Identification Of Freswater Algae Common In Water Supplies And Polluted Water. Di dalam aninim. 1985. Standart Method For The examination of Water And Wastewater, 14thed., American Public Health Association Inc., New York. Pp 1194
Pelczar Jr., M.J. dan Chan E. C. S. 1986. Dasar-Dasar Mikrobiologi. Terjemahan UI-Press. Jakarta.
Peraturan Menteri Lingkungan Hidup. 2014. Peraturan Menteri Lingkungan Hidup Nomor 5 Tahun 2014 Tentang Baku Mutu Air Limbah. Jakarta.
Pratama, Irfan. 2011. Pengaruh metode pemanenan mikroalga terhadap biomassa dan kandungan esensialChlorella vulgaris.(Skripsi). Program Studi Teknik Kimia Fakultas Teknik Universitas Indonesia. Depok.
PTPerkebunan Nusantara VII. 2014.Parameter dan Baku Mutu Air Limbh Outlet Unit Pabrik Karet Way Berulu. Bandar Lampung.
Pujiastuti, A. 2010. pengaruh penggunaan media yang berbeda terhadap kemampuan penyerapan logam berat pb (timbal) oleh Tetraselmis
sp.(Skripsi). Universitas Lampung. Lampung.
Rahardjo, Djoko, 2008, Mikroalga Sumber Energi Alternatif Masa Depan, http://egamesbox.com/viewthread.php?tid=3761&page=1&authorid=281.
Richmond, A.E. 1986. Microagriculture. CRC. Critical Rev. Biotechnol, 4 (4): 369-438.
Rusyani, E. 2001. Pengaruh dosis zeolityang berbeda terhadappertumbuhan
Isochrysis galbanaklon Tahiti skala laboratoriumdalam media komersial. (Skripsi).IPB. Bogor. 53 pp.
Rusyani, E., A.I.M. Sapta, M. Firdaus. 2007. Budidaya Phytoplankton dan Zooplankton Skala Laboratorium. Seri Budidaya Laut No. 9. Balai Besar Pengembangan Budidaya Laut Lampung. Direktorat Jenderal Perikanan Budidaya Laut. Departemen Kelautan Dan Perikanan.
52
Kelautan Vol. 4 No. 2, November 2012. Fakultas Perikanan dan Kelautan. Universitas Airlangga.
Sarief, S. 1985.Konservasi Tanah dan Air. Cetakan ketiga. Pustaka Buana.
Sawyer, C.N., P.L. Mc Carry, and G.F Parkin. 1994. Chestry For Enviromental Engeneering.4thed. Mc Graw-Hill International Edition. New York.
Sriharti, 2004. Pengaruh Species Clorella dalam MenetralisirLimbah Cair Karet.
ProsidingSeminar Nasional Rekayasa Kimia dan Proses.Subang.
Subroto dan Akrimi. 2002. Teknik Pengamatan dan Kualitas Air dan Plankton Danau Arang-Arang. Jambi.
Sulaeman, Suparto, dan Eviati. 2005. Petunjuk Teknis Analisis Kimia Tanah, Tanaman, Air, dan Pupuk. Baliptan Deptan. Bogor.
Sulastri. 2005. Komposisi, kelimpahan, dan distribusi fitoplankton sebagai dasar analisis pencemaran Danau Maninjau, Sumatera Barat. Puslit Limnologi LIPI. Cibinong-Bogor.
Summers, J. 2008. Assesment of Filamentous Algae in the Greenbrier River and other West Virginia Streams. Diakses 1 November 2014. http://www.dep.wv.gov/WWE/watershed/wqmonitoring/Documents/Greenb rier/Assesment_Filamentous_Algae_Greenbrie_%20River.pdf.
Tchobagnoulous, G. And F.L. Burton. 1991.Wastewater Engeneering, Treatment, Disposal, Reuse, Series Water Resource and Enviromental Engeneering
6thed. McGraw Hill Book Co., Singapore.
Tebbut, T.H.Y. 1992. Principles of Water Quality Control. 4thedition. Pergamon Press. Oxford. 251p.
Ugwu, C.U, Aoyagi,H & Uchiyama,H. 2007. Photobioreactor for Mass
Cultivation of alga, Bioresource Technology.
Utomo, T.P. 2008.Rancang bangun proses produksi karet remah berbasis produksi bersih.(Disertasi). Sekolah Pascasarjana Institut Pertanian Bogor. Bogor.
Utomo, T.P., Hasanudin, U., Suroso, E. 2012. Agroindustri Karet Indonesia. PT Sarana Tutorial Nurani Sejahtera. Bandung. 92 hlm
Verstraeta, W and E. Van Vaernberg. 1986. Aerobic Activated Sludge. In Biotechnologi 8: Microbial Degradation. W. Schonborn (ed) VCH. Weihnhem.
53
Wasetiawan. 2009. Alga. Diakses 1 November 2014. http://www.science.org.
Wells, R.D.S., Hall, J.A., Clayton, J.S., Champion, P.D., Payne, G.W., and Hofstra, D.E. 1999. The Rise and Fall of Water Net (Hydrodictyon reticulatum) in New Zealand. J. Aquat. Plant Manage. 37:49-55. Diakses 1 November 2014. http://www.bryoecol.mtu.edu/chapters/Hydrodictyon.pdf.
Wakatsuki, T., H. Esumi dan S. Omura, 1993. High performance and N &Premovableon-site domesticwastewater treatment system by MultiSoil Layering Method,Wat. Sci. Tech., 27, (1), 31-40
Wisjnuprapto. 1988. Pengolahan Air Limbah secara Biologi. Diktat Kuliah. PAU Bioteknologi ITB. Bandung.
Yanuaris, L, M., Rahayu K. dan Kismiyati. 2012. Pengaruh Fermentasi
Actinobacillus sp. pada Kotoran Sapi Sebagai Pupuk Terhadap PertumbuhanNannochloropsissp.Jurnal Ilmiah Perikanan dan Kelautan 4: 21-26.