ABSTRACT
HEALTH MANAGEMENT IMPLEMENTATION OF VANNAMEI SHRIMP (Litopenaeus vannamei) CULTURE AT CENTER OF SIDODADI
AND GEBANG VILLAGE PADANG CERMIN SUBDISTRICT PESAWARAN REGENCY
By
GESTY AYU AKBAIDAR
The purpose of this research was to know application of especially biosecurity in farming area and its effect to harvest, to identify parasites of vannamei shrimp, to know healthy status of vannamei shrimp. This research was conducted on February through May 2013 in shrimp farming area of Sidodadi and Gebang village. Samples examination carried out in Main Center of Mariculture Development of Lampung. The research method includes, samples examination by Polymerase Chain Reaction (PCR) technique, parasites species observation, secondary data collection through interview and documentation, and followed by descriptive data analysis. The results of laboratory examination vannamei shrimp samples from Sidodadi and Gedang village’ s farming area were negative WSSV and IMNV. Parasites species were found were Zoothamnium sp. and Nematoda.
ABSTRAK
PENERAPAN MANAJEMEN KESEHATAN BUDIDAYA UDANG VANNAMEI (Litopenaeus vannamei) DI SENTRA BUDIDAYA UDANG DESA SIDODADI DAN DESA GEBANG
KABUPATEN PESAWARAN
Oleh
GESTY AYU AKBAIDAR
Penelitian ini bertujuan untuk mengetahui penerapan sistem biosekuritas di lingkungan budidaya udang vannamei dan pengaruhnya terhadap produksi, mengidentifikasi jenis parasit pada udang vannamei, mengetahui status kesehatan udang vannamei yang dibudidayakan di daerah pertambakan Desa Sidodadi dan Desa Gebang dari kemungkinan infeksi virus dalam lingkungan tambak. Penelitian ini dilaksanakan bulan Februari hingga Mei 2013 di sentra budidaya tambak udang Desa Sidodadi dan Desa Gebang, Pesawaran. Pengujian sampel dilakukan di Balai Besar Pengembangan Budidaya Laut Lampung. Metode penelitian meliputi pemeriksaan sampel dengan teknik Polymerase Chain Reaction (PCR), pengamatan jenis parasit, pengumpulan data sekunder melalui wawancara dan dokumentasi, dan dilanjutkan dengan analisis data secara deskriptif. Hasil uji laboratorium udang vannamei yang diperiksa dengan teknik PCR dari tambak Desa Sidodadi dan Desa Gebang menunjukkan bahwa negatif WSSV dan negatif IMNV. Jenis parasit yang ditemukan adalah Zoothamnium sp. dan Nematoda.
I. PENDAHULUAN
1.1 Latar Belakang
Kegiatan budidaya udang di Indonesia dengan komoditas utama yaitu udang
windu (Penaeus monodon), berkembang sangat pesat dengan menerapkan sistem
budidaya secara intensif dan telah menghasilkan devisa negara yang cukup besar
(KKP, 2009).Budidaya udang windu mengalami berbagai kasus kematian sejak
tahun 1990-an, baik akibat dari lingkungan yang kurang mendukung maupun
adanya serangan penyakit seperti bakteri dan virus (Tenriulo et al., 2010).Kondisi
tersebut membuat banyak petambak mulai beralih ke budidaya udang vannamei
(Litopenaeus vannamei). Udang vannamei memiliki banyak keunggulan seperti
relatif tahan penyakit, produktivitasnya tinggi, waktu pemeliharaan relatif singkat,
tingkat kelangsungan hidup (survival rate) selama masa pemeliharaan tinggi dan
permintaan pasar terus meningkat (Hendrajat et al., 2007).
Udang vannamei mulai dibudidayakan secara intensif di Indonesia sejak tahun
2001, berdasarkan SK Menteri Kelautan dan Perikanan No. 41/2001 tanggal 12
Juli 2001 (Adiwidjaya, 2008).Produktivitas udang vannamei saat ini cenderung
menurun, bahkan sering terjadi kegagalan hasil produksi.Penyebaran penyakit
dalam lingkungan budidaya udang vannmei menjadi penyebab utama terjadinya
kegagalan budidaya.Jenis penyakit yang dapat menyerang udang antara lain
utama pada budidaya udang vannamei (Munajah, 2011). White Spot Syndrome
Virus (WSSV) dan Infectious Myonecrosis Virus( IMNV) adalah penyebab
beberapa kasus kematian udang vannamei yang belum dapat diatasi secara tuntas
(Zhang etal., 2004).
Penyebab lain terjadinya kegagalan dalam budidaya adalah menurunnya mutu
lingkungan budidaya. Padat tebar yang tinggi, diikuti dengan pemberian pakan
yang lebih banyak per satuan luas tambak akan menambah berat beban lingkungan
(Nurjanah, 2009). Kondisi lingkungan diperburuk dengan sistem pembuangan air
sisa pemeliharaan yang kurang baik, akibatnya terjadi akumulasi bahan organik
sisa pakan dan kotoran udang dalam lingkungan budidaya (Dirjerkesling
,2005).Upaya untuk mengantisipasi penyebaran penyakit dan mengurangi resiko
kegagalan produksi sangat diperlukan dalam sistem budidaya.
Tindakan yang dapat dilakukan untuk mengantisipasi penyebaran penyakit dan
mengurangi resiko kegagalan produksi dalam lingkungan budidaya adalah
melakukan peringatan dini (early warning), pemantauan terhadap keberadaan
patogendi lingkungan tambak selama masa budidaya, penerapan manajemen
kesehatan udang (biosekuritas), manajemen pemberian pakan, manajemen
lingkungan), dan penerapan teknologi budidaya yang tepat (Adiwidjaya et al.,
1.2Tujuan Penelitian
Tujuandari penelitian ini adalah:
1. Mengetahui penerapan sistem biosekuritas di lingkungan budidaya udang
vannamei dan pengaruhnya terhadap produksi;
2. Mengidentifikasi jenis parasit pada udang vannamei ;
3. Mengetahui status kesehatan udang vannamei yang dibudidayakan di daerah
pertambakan Desa Sidodadi dan Desa Gebang dari kemungkinan infeksi virus
dalam lingkungan tambak.
1.3 Manfaat Penelitian
Hasil penelitian diharapkan dapat memberikan informasi kepada petambak
udangtentang manfaat penerapan manajemen kesehatan budidaya udang vannamei
terutama penerapan biosekuritas sebagai upaya pencegahan penyakit di sentra
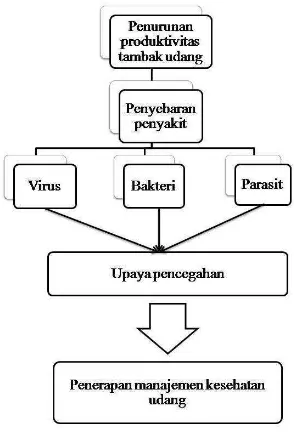
1.4Kerangka Pemikiran
II.TINJAUAN PUSTAKA
2.1 Klasifikasi dan Morfologi Udang vannamei
Menurut Wybanet al(2000), klasifikasi udang vannamei sebagai berikut: Kingdom : Animalia
Filum : Anthropoda
Kelas :Crustacea
Ordo :Decapoda
Famili :Penaidae
Genus :Litopenaeus
Spesies :Litopenaeus vannamei
Bagian tubuh udang vannamei terdiri dari kepala yang bergabung dengan dada
(cephalothorax) dan perut (abdomen). Kepala udang vannamei terdiri dari
antenula, antena, mandibula, dan sepasang maxillae. Kepala udang vannamei juga
dilengkapi dengan 5 pasang kaki jalan (periopod) yang terdiri dari
2pasang maxillae dan 3 pasang maxiliped. Bagian abdomen terdiri dari 6 ruas dan
terdapat 6 pasang kaki renang (pleopod) serta sepasang uropod (mirip ekor) yang
Gambar2 . Morfologi udang vannamei (Litopenaeus vannamei) Sumber : Dokumentasi pribadi ( 3Maret 2013)
2.2 Sifat Biologis
Sifat biologis udang vannamei, yaitu aktif pada kondisi gelap (nocturnal) dan
dapat hidup pada kisaran salinitas yang luas (euryhaline) yaitu 2-40 ppt. Udang
vannamei akan mati jika terpapar suhu dibawah 15oC atau diatas 33oC selama 24
jam(Wyban et al., 1991).
Udang vannamei bersifat kanibal, mencari makan lewat organ sensor dan tipe yang
pemakan lambat, memiliki 5 stadia naupli, 3 stadia zoea, 3 stadia mysis sebelum
menjadi post larva yang merupakan siklus hidupnya. Stadia post larva berkembang
menjadi juvenil dan akhirnya menjadi dewasa. Post larva udang vannamei di
perairan bebas akan bermigrasi memasuki perairan estuaria untuk tumbuh dan
2.3 Manajeman Kesehatan Udang
2.3.1Biosekuritas
Biosekuritas merupakan upaya pengamanan sistem budidaya dari kontaminasi
patogen yang berasal dari karir patogen luar dengan cara-cara yang tidak merusak
lingkungan (KKP, 2007 ).
Penerapan biosekuritas dalam lingkungan budidaya menurut Timmons and
Ebeling (2010), terdiri dari kegiatan dan prosedur berikut:
a. Mengurangi resiko masuknya patogen pada fasilitas budidaya;
b. Mengurangi resiko menyebarnya patogen ke seluruh fasilitas budidaya;
c. Mengurangi kondisi bertambahnya penyakit, yang berasal dari agen
penyebab penyakit seperti seperti ikan liar dan hewan invertebrata.
2.3.2 Manajemen Pakan
Usaha budidaya berkembang dengan pesat mulai dari sistem ekstensif hingga
sistem intensif. Perkembangantersebut telah menimbulkan masalah terutama
dalam hal usaha budidaya yang berkelanjutan. Nutrien yang tersedia dalam pakan,
sebagian besar dapat menjadi polutan pada lingkungan budidaya, seperti nitrogen,
fosfor, bahan organik, dan hidrogen sulfida (Alifuddin et al., 2003).
Semakin tinggi padat tebar membawa konsekuensi pada peningkatan limbah
metabolik yang dihasilkan. Limbah metabolik tersebut akan terakumulasi dalam
media budidaya, sehingga menjadi zat racun yang menghambat pertumbuhan
Akumulasi bahan organik yang berlebih menjadi pemicu kondisi lingkungan yang
anaerob, tingginya kebutuhan oksigen di sedimen, terjadinya penurunan mutu
lingkungan yang pada akhirnya berdampak pada respon pertumbuhan kultivan
yang rendah (Avnimelech et al., 2003).
2.3.3 Manajemen Lingkungan Budidaya
Pengawasan (monitoring) lingkungan merupakan faktor penting dalam penentu
keberhasilan suatu budidaya (Lio-Po et al., 2001). Kegiatan budidaya udang
vannamei dengan metode intensif mengakibatkan udang yang dibudidayakan
menjadi mudahstres karena padat tebar yang tinggi, penanganan, dan turunnya
mutu kualitas air (Hendrajat et al., 2007).
Parameter kualitas air media harus berada pada kondisi yang optimal. Parameter
yang berpengaruh dalam budidaya tersebut adalah pH, oksigen terlarut,nitrat,
amonia, bahan organik, suhu, salinitas, dan nitrit. Tingkat optimum serta kisaran
kualitas air yang mampu diterima oleh udang vannamei (Tabel 1).
Tabel 1. Kisaran nilai optimum parameter kualitaspada pemeliharaan udang vannamei (Litopenaeus vannamei)
No Parameter air Nilai optimum
1. Suhu 28,5 - 31,5oC
2. Salinitas 15 – 25ppt
3. Kecerahan 30 - 45cm
4. Oksigen terlarut >3,5mg/l
5. pH 7,5 - 8,5
6. Alkalinitas 100 – 150mg/l
7. CO2 < 25 mg/l
8. Amonia <0,01mg/l
9. Nitrit (NO2) 0,01mg/l
[image:10.595.117.505.540.708.2]2.4 Penyakit Virus
2.4.1 White Spot Syndrome Virus (WSSV)
2.4.2 Klasifikasidan Morfologi
WSSV termasuk dalam family Nimaviridae genus Whispovirus (Vlak et al., 2002).
WSSV mempunyai bentuk lonjong dan berdiameter antara 120–150 nm, panjang
270–190 nm, mempunyai tiga lapis selaput (envelope) yang melindungi inti
(nucleocapsid ) (Sunarto, 2003).
2.4.3Patogenitas dan Gejala Penyakit
Udang windu yang terserang WSSV ditandai dengan munculnya bintik putih
berdiameter 0,5–3 mm disekitar lapisan epidermis. WSSV pertama kali
menginfeksi beberapa bagian segmen karapaks bagian sel dalam tubuh.Gejala
udang yang terinfeksi WSSV ditunjukkan dengan terlepasnya kutikula ditubuh
udang, indikasi lainnya adalah udang berenang dipermukaan dan mengumpul di
sekitar pematang kolam dengan luka pada antenna (Lio-Po et al., 2001).
Udang mulai kehilangan nafsu makan dan akan berenang kepermukaan kolam
secara tidak normal sejak hari pertama udang terinfeksi. WSSV mulai tampak di
bagian karapaks dan insang udang pada infeksi hari kedua dan ketiga. Gejala
kronis ditandai dengan perubahan warna tubuh udang menjadi kemerah- merahan,
selanjutnya diikuti dengan penempelan protozoa Zoothamnium dan Vorticella.
Mortalitas yang tinggi pada udangakan terjadi apabila dalam waktu beberapa
minggu tidak ditangani. Kasus di Amerika Serikat, diperkirakan bahwa impor
udang beku menghasilkan limbah berupa air yang menyebarkan penyakit dari
Penelitian dilaboratorium menunjukkan bahwa WSSV menginfeksi udang pada
stadia post larva dan juvenil. WSSV banyak menyerang jenis udang seperti
L.vannamei, P. stylirostris, P. setiferus, P. aztecus, and P.
Duorarum(Lightneretal., 1998dalam McClennen, 2004).
2.4.4 Penyebaran Penyakit
WSSV pertama kali menyerang sentra budidaya tambak udang di Taiwan yang
menyebabkan kematian massal pada udang Penaeus japonicus tahun 1992,
kemudian menyebar melalui udang impor ke selatan Jepang, Thailand, Indonesia
dan pantai Indiatahun 1993 (Chou, 1995).WSSV mulai menyerang Amerika
Selatan yaitu di Ekuador dan Peru pada akhir tahun 1998dan menyebabkan
kegagalan panen dengan morbiditas dan mortalitas tinggi mencapai
100%(McClennen, 2004).
Mayoritas arthropoda seperti kepiting liar Portunus pelagicus dan udang renik
kemungkinan menjadi karier dan dapat mentransmisikan virus ke sistem budidaya
udang melalui saluran inlet (Supamattya et al., 1996) dan proses kanibalisme
udang yang baru mati lewat air yang terkontaminasi (Chang et al., 1996).
2.4.5 IMNV (Infectious Myonecrosis Virus)
2.4.6 Klasifikasi dan Morfologi
IMNV merupakan jenis virus yang tidak beramplop(non enveloped)dengan
karakteristik ikosahedral, berdiameter 40 nm, dengan kepadatan apung 1,336 g/ml
dalam cesium klorida (CsCl), termasukke dalam famili Totiviridae berdasarkan
stranded(ds) RNA, dan salah satu untai RNA-nya ekuivalen dengan mRNA
(Pouloset al., 2006).
Pengurutan genom virus menunjukkan pembacaan dua rangka secara
terbuka(ORFs) yang tidak saling tumpang tindih,yaitu ORF1 dan ORF2. ORF 1
berfungsi sebagai pengkode protein pengikat RNA dan protein kapsid, ORF2
berfungsi sebagai pengkode RNA–dependent RNA polymerase (RdRp)(Munajah,
2011).
2.4.7 Patogenisitas dan Gejala Penyakit
IMNV disebabkan oleh virus IMNV jenis RNA (Ribo Nucleic Acid). Udang
vannamei yang terinfeksi IMNVmengalami kematian akut 40-70% (Rivers,1937).
Kematian udang vannamei ditandai dengan munculnya gejala klinis yaitu otot
putih (opaque), ekor kemerahan, pembesaran lymphoid organ (Pouloset al, 2006).
Serangan IMNV sama dengan otot putih, tetapi tidak semua otot putih merupakan
akibat serangan IMNV. Otot putih bisa juga disebabkan oleh kondisi hipoksia
(kekurangan oksigen) (Sutanto, 2010).
Merebaknya penyakit IMNV dikaitkan dengan penurunan kualitas lingkungan,
yaitu penurunan salinitas dan suhu secara ekstrim serta penangkapan dengan jala
dan buruknya kualitas pakan (McClennen, 2004).
2.4.8 Penyebaran Penyakit
Penyebaran IMNV yang ditandai dengan otot putih dan kematian masal pada
udang vannamei yang dibudidayakan.Penyakit tersebut disebabkan oleh virus
teridentifikasi di Indonesia yaitu di Kabupaten Situbondo, Jawa Timur tahun 2006.
Sampel udang yang terinfeksi dianalisis dan diperoleh hasil bahwa 99,6% urutan
identitas asam nukleatnya serupa dengan IMNV yang di Brazil (Senapin et al.,
2006).
2.5 Penyakit Parasit
Parasit adalah adalah organisme yang hidup pada tubuh organisme lain yang dapat
menimbulkan kerugian atau efek negatif pada organisme yang ditempatinya
(Yanto, 2006).Parasit dapat merugikandan membahayakan inang jika jumlahnya
cukup banyak. Infeksi parasit dapat mendatangkan kerugian kepada inang.
Kerugian yang ditimbulkan adalah menghambat pertumbuhan inang,
menyebabkan terjadinya alergi, dan menurunkan ketahanan inang terhadap
penyakit lain (Levine, 1990).
2.5.1 Zoothamnium sp.
Zoothamniumsp. termasuk dalam Phylum: Protozoa, Kelas: Ciliata, Ordo:
Peritricha, Famili: Zoothamnidae, Genus: Zoothamnium, Spesies: Zoothamnium
sp. (Patterson, 2010). Zoothamniumsp. berbentuk kerucut yang hampir
membulat.Parasit ini bersifat koloni yang tersusun pada tangkai yang bercabang–
cabang (Alifuddin, 1993).
2.5.2 Nematoda
Nematoda merupakan anggota dari filum Nemathelmintes yangmempunyaisaluran
pencernaan yang lengkap dan rongga tubuh. Rongga tubuh dilapisi dengan selaput
dengan kutikula yang hanya terlihat secara mikroskopis dan memiliki struktur
yang bervariasi pada tiap spesies (Levine, 1990).
Kutikula pada nematoda berfungsi untuk mengambil oksigen sebagai selubung
pelindung yang lentur dan kenyal serta resisten terhadap enzim pencernaan inang
terutama untuk cacing dewasa. Kutikula terdiri dari sejumlah lapisan dan
sedikitnya lima protein yang berbeda. Terdapat tiga lapisan dibawah kutikula yaitu
lapisan korteks dipermukaan, lapisan matriks di tengah, dan lapisan basal (Cheng,
1974).
2.6 Metode Polymerase Chain Reaction (PCR)
Polymerase Chain Reaction (PCR) adalah suatu teknik uji terhadap virus melalui
hasil reaksi berantai suatu primer dari rangkaian yang menggunakan enzim
polymerase, sehingga menjadi amplifikasi DNA secara in vitro (Sunarto, 2003) .
Teknik PCR menurut Wuryastuti (2002), terdiri dari tiga reaksi yaitu:
1. Denaturasi DNA, yaitu pemecahan DNA target dari untai ganda DNA
(dsDNA) menjadi dua untai tunggal yang identik. Proses denaturasi dapat
secara mudah dicapai dengan pemanasan secara cepat yang diikuti
pendinginan. Untai ganda DNA secara umum akan mengalami denaturasi pada
suhu sekitar 94oC. Waktu denaturasi yang baik untuk setiap putaran berkisar
antara 30 detik sampai 2 menit. Waktu denaturasi yang optimal untuk
beberapa macam cetakan adalah 1 menit.
2. Annealing, yaitu perlekatan primer pada DNA untai tunggal. Temperatur harus
diturunkan secepat mungkin untuk mencegah terjadinya perlekatan kembali
menentukan spesifisitas dan sensitivitas dari reaksi. Primerakan menempel
pada pangkal dan ujung dari masing-masing DNA untai tunggal yang
berkomplementer pada suhu 60oC, sehingga mengapit daerah tertentu dari
rangkaian DNA target. Waktu yang umumnya digunakan dalam proses
annealing berkisar 0,5–2 menit.
3. Extention, yaitu pemanjangan primer dengan bantuan enzim Taq polymerase
menggunakan rantai komplementer sebagai template dan deoksiribonukleotida
sebagai bahan utama untuk membentuk untai DNA yang lengkap. Kisaran
temperatur untuk proses perpanjangan primer adalah 75-80oC, sedangkan
temperatur optimalnya adalah 72oC, sehingga pada akhir proses akan terbentuk
2 buah DNA untai tunggal baru yang komplemen terhadap urutan DNA target.
2.7 IQ 2000 WIT MultiVirTM Sistem
IQ2000 WIT MultiVirTM Sistem merupakan program bio - chip diagnose yang
pertama untuk penyakit udang didunia yang disebabkan oleh virus. IQ2000 WIT
MultiVirTM Sistem didesain untuk mendeteksi virus yang menyerang dalam
budidaya udang vanamei. IQ2000 WIT MultiVirTM sistem merupakan reaksi
tunggal dan multi fungsional yang mengkobinasikan keunggulan dari PCR dan
bio-chipyang terbukti lebih sensitif, spesifik, akurat dan mudah untuk
diinterprestasikan dibanding dengan PCR yang konversional, dot blot,
III. METODE PENELITIAN
3.1 Waktu dan Tempat Pelaksanaan
Penelitian ini dilaksanakan pada bulan Februari sampai dengan Mei 2013.Lokasi
pengambilan sampel meliputi wilayah pertambakan di Kabupaten Pesawaran.
Pengujian dan pemeriksaan sampel dilakukan di Laboratorium Divisi Kesehatan
Ikan dan Lingkungan Balai Besar Pengembangan Budidaya Laut (BBPBL)
Lampung, Desa Hanura, Kecamatan Padang Cermin, Kabupaten Pesawaran.
3.2 AlatdanBahan
Alat dan bahan yang digunakan dalam penelitian sebagai berikut:
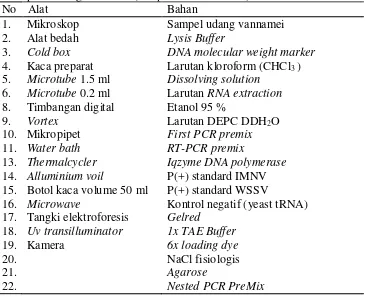
Tabel 2. Alat dan bahan yang dibutuhkan dalam uji PCR dan identifikasi parasit pada udang vannamei (Litopenaeus vannamei)
No Alat Bahan
1. Mikroskop Sampel udang vannamei
2. Alat bedah Lysis Buffer
3. Cold box DNA molecular weight marker
4. Kaca preparat Larutan kloroform (CHCl3 )
5. Microtube 1.5 ml Dissolving solution
6. Microtube 0.2 ml Larutan RNA extraction
8. Timbangan digital Etanol 95 %
9. Vortex Larutan DEPC DDH2O
10. Mikropipet First PCR premix
11. Water bath RT-PCR premix
13. Thermalcycler Iqzyme DNA polymerase
14. Alluminium voil P(+) standard IMNV
15. Botol kaca volume 50 ml P(+) standard WSSV
16. Microwave Kontrol negatif (yeast tRNA)
17. Tangki elektroforesis Gelred
18. Uv transilluminator 1x TAE Buffer
19. Kamera 6x loading dye
20. NaCl fisiologis
21. Agarose
[image:17.595.132.500.456.753.2]3.3 Prosedur Penelitian
3.3.1 Wawancara
Wawancara dilakukan dengan teknisi atau pemilik tambak yang memahami
kondisi di lokasi pertambakan, meliputi:
a. Informasi umum mengenai tambak (luas lokasi tambak, jumlah petak tambak,
tahun beroperasi, substrat dasar tambak, sistem budidaya, luas petak tambak,
dan jumlah kincir);
b. Data mengenai udang budidaya (spesies, asal benur, umur, biomassa, populasi
udang), manajemen pemberian pakan (jenis pakan, Feeding Rate, Feeding
Periode, Feeding Method) ;
c. Data kualitas air (sumber air, perlakuan air, kecerahan, suhu, pH, DO, salinitas,
dan amonia) ;
d. Informasi mengenai aplikasi biosekuritas di lokasi pertambakan.
3.3.2 Penentuan Lokasi Pengambilan Sampel
Lokasi pengambilan sampel dilakukan di dua sentra budidaya tambak udang
intensif di Kabupaten Pesawaran. Lokasi pertama dilakukan di tambak udang Desa
Sidodadi , sedangkan lokasi kedua dilakukan di tambak udang Desa Gebang.
3.3.3 PengambilanSampel
Sampel yang digunakan dalam pengamatan parasit dan virus adalah udang
vannamei dengan umur yang tidak ditentukan. Sampel dibawa ke laboratorium
dalam keadaan hidup yang dimasukkan ke dalam termos berisi es batu. Sampel
struktur DNA sampel tidak rusak, kemudian sampel diperiksa dengan metode
analisis PCR.
3.3.4 Pemeriksaan Sampel
Pemeriksaan sampel dilakukan melalui metode analisis PCR dilaksanakan
berdasarkan Instruction Manual IQ2000TM Detection and Prevention System yang
merupakan kesatuan instrumen (berupa kit/ paket) yang digunakan untuk
menggandakan DNA dengan bantuan enzim.
a. PemeriksaanInfectious Mynecrosis Virus(IMNV)
Pemeriksaan Infectious Mynecrosis Virusdilakukan dengan metode pemeriksaan
IQ2000TM IMNV (nested) Instruction Manual (2007).
b.PemeriksaanWhite Spot syndrome Virus
Pemeriksaan White Spot syndrome Virus dilakukan dengan metode pemeriksaan
IQ2000TM WSSV (nested) Instruction Manual (2008).
c. Pengamatan Parasit
Pengamatan parasit pada sempel udang vannamei dilakukan melalui dua
pengamatan antara lain:
Pengamatan Ektoparasit :
1. Disiapkan sampel udang yang akan diamati;
2. Diamati permukaan tubuh udang secara visual ;
3. Lendir pada permukaan tubuh dikerik, dan dibuat preparat ulas pada gelas
objek ;
4. Preparat diamatidi bawah mikroskop.
Pengamatan Endoparasit :
2. Diamati permukaan organ secara visual dengan bantuan kaca pembesar ;
3. Organ dalam insang dan usus diangkat dan dimasukkan ke dalam cawan petri
yang berisi larutan garam fisiologis ;
4. Dibuat preparat ulas pada gelas objek ;
5. Preparat diamatidi bawah mikroskop.
3.4Parameter yang Diamati
Parameter penelitian yang diamati adalah:
1. Pengamatan kondisi lingkungan budidaya (prinsip manajemen kesehatan udang
biosekuritas yang diterapkan ditambak) menggunakan kuisioner.
2. Diagnosis penyakit virus antara lain IMNV dan WSSV.
3. Pengamatan parasit pada udang vannamei yang sakit atau berada di pematang
atau tertangkap anco.
4. Pertumbuhan udang; ADG (Average Daily Gain) dan ABW (Average Body
Weight).
5. FCR (Food Convertion Rate).
6. Hasil produksi (panen).
7. Kualitas air.
3.5 Analisis Data
Penelitian ini dianalisis secara deskriptif. Data yang dihasilkan dalam bentuk
gambar dan tabel. Data hasil wawancara akan dianalisis untuk mengetahui
pengaruh kondisi umum penerapan biosekuritas tambak terhadap penyebaran
V. SIMPULAN DAN SARAN
5.1Simpulan
Simpulan yang dapat diambil dari penelitian ini antara lain :
1. Penerapan manajemen kesehatan udang di tambak Desa Sidodadi lebih baikdibandingkan tambak Desa Gebang.
2. Status kesehatan sampel udang vannamei yang telah dianalisis melalui metode PCR pada tambak Desa Sidodadi dan Desa Gebang adalah negatif IMNV dan WSSV.
3. Jenis parasit yang ditemukan pada sampel udang vannamei di Desa Sidodadi dan Desa Gebang adalah Zoothamnium sp.dan Nematoda.
5.2Saran
DAFTAR PUSTAKA
Adiwidjaya, D., C. Kokarkin., Supito. 2001. Teknik Operasional Budidaya Udang Ramah Lingkungan. Departemen Kelautan dan Perikanan. Direktorat Jenderal Perikanan Budidaya. Balai Besar Pengembangan Budidaya Air Payau Jepara. 29 hlm.
Adiwidjaya, D., Supito., I. Sumantri. 2008. Penerapan Teknik Budidaya udang Vannamei (Litopenaeus vannamei) Semi - Intensif pada Lokasi Tambak Salinitas Tinggi. Departemen Kelautan dan Perikanan. Direktorat Jendral Perikanan Budidaya.Balai Besar Pengembangan Budidaya Air Payau Jepara. 19 hlm.
Alifuddin, M.1993. Penyakit Protozoa Pada Ikan. Lab Kesehatan Ikan. Jurusan Budidaya Perairan, Fakultas Perikanan – Institut Pertanian Bogor. Bogor.
Alifuddin, M., D. Dana., M. Eidman., M.B. Malole., F.S Pasaribu. 2003. Patogenesis Infeksi Virus White Spot (WSV) Pada Udang Windu (Penaeus monodon Fab. ). Jurnal Akuakultur Indonesia. 2(2): 85-92.
Avault, J.W,.1996. Fundamental of Aquaculture a Step by Step Guide to Comercial Aquaculture. AVA Publishing. Baton Rouge. USA.
Avnimelech, Y ., and G. Ritvo.2003. Shrimp and fish pond soiln: processes and management. Aquaculture. 220:549-567.
Boyd, C.E. 1990. Water Quality in Pond for Aquaculture. Department of Fisheries and Allied Aquacultures. Auburn University, Alabama, USA.482 pp.
Cheng, T.C. 1974. General Parasitology. Academic Press. London. 821- 886 pp.
Chang, P.S., Y.C. Wang ., C.F. Lo., G.H. Kou. 1996. Infection of White Syndrome Associated with non – occluded Baculovirus in Cultured and Wild Shrimp in Taiwan. 2nd . Int Conference on the Culture of Panaeid Prawns And Shrimp. Book of abstracts, SEAFDEC/ AQD. Iloilo City, Philiphines.
Chou, H.Y., C.Y. Huang., C.H. Wang., H.C. Chiang., C.F. Lo. 1995. Pathogenicity Of A Baculovirus Infection Causing White Spot Syndrome in Cultured Penaeid Shrimp In Taiwan. Diseases of Aquatic Organisms. 23:165-173.
Clifford, H.C. 1994. Semi-Intensive Sensation : A Case Study in Marine Shrimp Pond Management. World Aquaculture.25 (3):10.
Direktorat Kesehatan Ikan dan Lingkungan. 2005. Pengelolaan Air Buangan Tambak dengan Tandon Resirkulasi. Direktorat Jenderal Perikanan Budidaya.Departemen Kelautan dan Perikanan Republik Indonesia.
FAO, NACA. 2003. Quarterly Aquatic Animal Disease Report (Asia and Pacific Region) January-March 2003) Accessed from: http://www.enaca.org/NACA-Publications/QAAD/QAAD-2003-1.pdf,
Hendrajat, A.E., M. Mangampa., H. Suryanto. 2007. Budidaya Udang Vannamei Pola Tradisional Plus di Kabupaten Maros Sulawesi Selatan. Media Akuakultur .2 (2):4.
[KKP] Kementerian Kelautan dan Perikanan. 2009. Rencana Strategi Budidaya Udang. Jakarta.
Lightner, D.V. 1999. The Penaeid Shrimp Viruses TSV, IHHNV, WSSV, and YHV: Current Status in the Americas, Available Diagnostic Methods, and Management Strategies. Journal of Applied Aquaculture. 9:27-52.
Lio- Po, G.D., C.R. Lavilla., E.R. Cruz- Lacierda. 2001. Health Management in Aquaculture. Aquaculture Department Southeast Asian Fisheries Development Center. Tigbauan. Iloilo. Philippines.
McClennen, Caleb. 2004. White Spot Syndrome Virus The Economic, Environmental, and Technical Implication on The Development of Latin America Shrimp Farming. Thesis. Tuft University. 106 pp.
Molnar. 2006. Phylum Nematoda In Fish Disease and Disorders, Volume 1: Protozoan and Metazoan Infections Second Edition. Edit by PTK Woo. Canada: CABI Publishing.
Munajah, M. 2011. Insidensi White Spot Syndrome Virus (WSSV) dan Taura Syndrome Virus (TSV) Pada Udang Putih (Litopenaeus vannamei) di Pertambakan Sekitar Teluk Lampung Tahun 2010 dengan Metode Analisis Polymerase Chain Reaction (PCR). Skripsi. Program Studi Budidaya Perairan. Universitas Lampung. Bandar Lampung.
Murdjani, M. 2007. PenerapanBest Management Practise Pada Budidaya Udang Windu (Penaeus monodon Fabricius) Intensif. Departemen Kelautan Dan Perikanan Direktorat Jenderal Perikanan Budidaya. Balai Besar Pengembangan Budidaya Air Payau. Jepara. 77 hlm.
Novita, H., T. Mufidah, T. Koesharyani. 2010. Perbandingan Penggunaan Berbagai Preservasi RNA Jaringan dengan RNA Later, Alkohol, dan Alkohol-Gliserol untuk Deteksi IMNV dengan PCR. Jakarta: Pusat Riset Perikanan Budidaya.
Poulos, B.T., K.F.J. Tang., C.R. Pantoja., J.R. Bonami., D.V. Lightner. 2006. Purification and characterization of infectious myonecrosis virus of penaeid shrimp. Journal of General Virology. 87:987-996.
Office International des Epizooties. 2007. Instruction Manual Infection Myonecrosis Virus (IMNV).
Office International des Epizooties. 2008. Instruction Manual White Spot Syndrome Virus (WSSV).
Office International des Epizooties. 2009. Manual of Diagnosis Tests for Aquatic Animal. Diakses dari http://www.oie.int/ pada 29 Oktober 2012 pukul 17:32 WIB.
Rivers, T.M. 1937. Viruses and Koch's Postulates. The Journal of Bacteriology. 33:1-12.
Routledge, L. M. 1978. Calcium-binding Protein in the Voricellidae spasmone. Rockfeller university press. Journal Cell biology. 7 pp.
Senapin, S., K. Phewsaiya., M. Briggs., T.W. Flegel. 2006. Outbreaks Of InfectiousMyonecrosis Virus (IMNV) in Indonesia Confirmed By Genome Sequencing and use Of An Alternative RT-PCR Detection Method. Aquaculture. 266:32-38.
SNI 01-7246-2006. Produksi Udang Vaname (Litopenaeus vannamei) Di Tambak Dengan Teknologi Intensif. Badan Standarisasi Nasional.
Supamattya, K., R. Hoffman., S. Boonyaratpalin. 1996. Transmision Red And White Spot Disease (Basiliform Virus ) from Black Tiger Shrimp Panaeus monodon to Portunid Crab Portunus pelagicus And Krill Acetes sp. 2nd . Int Coference on the Culture of Panaed Prawns And Shrimp . Book of abstracts, SEAFDEC/ AQD. Iloilo City, Philiphines.
Suprapto .2005. Petunjuk Teknis Budidaya Udang vannamei (Litopenaeus vannamei ). CV Biotirta. Bandar Lampung. 25 hlm.
Sutanto, Y. 2010. Penyakit IMNV (Mio) di Indonesia dan Antisipasinya. Dipresentasikan di Workshop MAI pada 20 Januari 2010. Lampung. Aquatic Health Centre, PT. CP Prima. 42 hlm.
Suwoyo, S.H., M. Mangampa. 2010. Aplikasi Probiotik dengan Konsentrasi Berbeda pada Pemeliharaan Udang vannamei (Litopenaeus vannamei ). Prosiding Forum Inovasi Teknologi Akuakultur. 239. 9 hlm.
Tenriulo, A., S. Tonnek ., B.R. Tampangallo., A.F Widodo., A. Parenrengi.2010. Analisis Ekspresi Gen Antivirus PmAV pada Udang windu (Penaeus monodon ) yang ditantang dengan WSSV. Prosiding Forum Inovasi Teknologi Akuakultur. 541. 6 hlm.
Timmons, B.M., M. J. Ebeling. 2010. Recirculating Aquaculture 2nd Edition. Veterinary Medical Officer, USDA. Agricultural Research Service Aquatic Animal Health Research Unit, USDA. ARS AAHRU, 990 Wire Road, Auburn, AL 36832.
Vlak, J. M., J.R. Bonami., T.W. Flegel., G.H. Kou., D.V. Lighner., C.F. Lo., P.C. Loh and P.J. Walker. 2002. A New Virus Family Infecting Aquatik Invertebrates. 12th International Congress of Virology. Paris.
Wyban, J.A., J.N. Sweeney. 1991. Intensive Shrimp Production Technology. The Oceanic Institute. Hawaii.
Wyban, J.A.,J.N. Sweeney. 2000. Intensive Shrimp Production Technology. The Oceanic Institute. Honolulu, Hawai, USA.13-14 pp.
Yanto, H. 2006. Diagnosa dan Identifikasi Penyakit Udang Asal Tambak Intensif Dan Panti Benih di Kalimantan Barat. Jurnal Penelitian Sains & Teknologi. 1: 17-32.