Chilli Veinal Mottle Potyvirus (ChiVMV )
PENYEBAB PENYAKIT BELANG PADA CABAI (Capsicum
annuum L.): KERAGAMAN ISOLAT DAN STRATEGI
PENGENDALIANNYA MELALUI INDUKSI
VARIASI SOMAKLONAL
IFA MANZILA
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa disertasi berjudul “Chilli Veinal Mottle Potyvirus (ChiVMV) Penyebab Penyakit Belang pada Cabai (Capsicum annuum L.): Keragaman Isolat dan Strategi Pengendaliannya Melalui Induksi Variasi Somaklonal” adalah karya saya sendiri, dengan arahan Komisi Pembimbing dan belum pernah diajukan dalam bentuk apapun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka dibagian akhir setiap topik disertasi ini.
Bogor,12 April 2011
ABSTRACT
IFA MANZILA Chilli Veinal Mottle Potyvirus (ChiVMV) the causal agent of mottle diseases on Chilli Pepper (Capsicum annuum L.): Isolates diversity and its control strategy through induction of somaclonal variation. Supervised by SRI HENDRASTUTI HIDAYAT, IKA MARISKA, SRIANI SUJIPRIHATI
Chilli veinal mottle potyvirus (ChiVMV) is one of important viruses infecting chilli pepper plant. It was reported that ChiVMV infection may cause 50% to 100% yield losses. The virus has a very wide host range and strain diversity. The aim of this research are to characterize biological variation of ChiVMV and to obtain plant resistance source via somaclonal variation through induced mutation. Six isolates of ChiVMV was collected from different geographical region of chilli pepper production area. Based on their infection on 10 genotypes of chilli pepper, it was indicated that they have differences in virulence level and symptom type. Isolate collected from Cikabayan, Bogor, Jawa Barat (ChiVMV CKB) was able to infect all 10 genotypes with severe symptoms showing mottle, vein banding, leaf cramping and malformation. Analysis of coat protein gene indicated that ChiVMV isolates collected in this study can be differentiated into 3 groups although they have close relationship with other strains of ChiVMV published earlier in GeneBank. However, further analysis of amino acid revealed that ChiVMV CKB has different motif of octapeptide compared to other strains. The most virulent strain, ChiVMV CKB, was used for evaluation of somaclonal plants produced by in vitro propagation combined with induced mutation using EMS. Twenty somaclonal plants showed resistant response to ChiVMV infection and potential to be used as genetic resources to develop resistant plant.
IFA MANZILA. Chilli Veinal Mottle Potyvirus (ChiVMV) Penyebab Penyakit Belang Pada Cabai (Capsicum annum L.): Keragaman Isolat dan Strategi Pengendaliannya Melalui Induksi Variasi Somaklonal. Dibimbing oleh SRI HENDRASTUTI HIDAYAT, IKA MARISKA, SRIANI SUJIPRIHATI.
Chilli veinal mottle potyvirus adalah salah satu virus utama yang menyerang tanaman cabai. Walaupun keberadaannya di Indonesia tergolong baru, namun penyebarannya dapat ditemukan hampir disetiap pertanaman cabai. Infeksi ChiVMV dapat mengakibatkan penurunan hasil 50% hingga 100%. Untuk mengatasi terjadinya ledakan penyakit, menggunakan varietas yang tahan terhadap virus merupakan salah satu alternatif. Namun sampai saat ini belum diperoleh varietas cabai tahan ChiVMV. Bila sumber gen ketahanan terhadap virus masih terbatas, maka salah satu upaya peningkatan sumber gen ketahanan tersebut dapat dilakukan melalui induksi keragaman somaklonal yang dikombinasi dengan induksi mutasi.
Penelitian dilakukan pada Juli 2007 sampai Desember 2009 dengan tujuan : 1) mendapatkan informasi mengenai keragaman isolat ChiVMV yang menginfeksi tanaman cabai (Capsicum annuum) pada sentra produksi cabai di Indonesia berdasarkan variasi biologi dan molekuler, 2) mendapatkan informasi tingkat virulensi ChiVMV dan respon beberapa galur cabai terhadap infeksi ChiVMV, 3) mendapatkan varian somaklonal tanaman cabai melalui induksi dengan ethyl methane sulfonate (EMS), 4) mendapatkan tanaman varian somaklonal tanaman cabai yang tahan terhadap ChiVMV. Penelitian di lakukan di laboratorium Biologi Sel dan Jaringan Balai Besar Penelitian dan Pengembangan Bioteknologi dan Sumberdaya Genetik Pertanian, Cimanggu Bogor dan Laboratorium Virologi Tumbuhan serta rumah kaca Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor.
DQ854961). Kelompok kedua adalah ChiVMV Cikabayan (CKB), dan Cikabayan2 (GeneBank DQ854960), sedangkan kelompok ketiga adalah ChiVMV Tanah Datar (TD), ChiVMV Nusa Indah (NI), ChiVMV Gayo Barat (GB), dan ChiVMV Taiwan (GeneBank DQ854948). Ketiga kelompok tersebut memiliki jarak genetik terdekat berturut-turut yaitu (0,05 sampai 0,06), (0,05) dan (0,02 sampai 0,48). Hasil penelitian ini menunjukkan bahwa perbedaan gejala yang tidak terlalu nyata diantara isolat-isolat ChiVMV berhubungan dengan tingkat variabilitas gen selubung protein yang rendah. Berdasarkan analisis asam amino isolat ChiVMV CKB memiliki susunan asam amino yang sangat berbeda dengan isolat ChiVMV lainnya. Asam amino pada isolat ChiVMV CKB, motif octapeptide-nya telah termutasi secara total menjadi motif EMETEVPQ; sedangkan pada CP ChiVMV BL dan KR hanya termutasi menjadi TQEEDTER. Apakah mutasi motif octapeptide pada CP ChiVMV CKB menyebabkan isolat ChiVMV CKB menjadi virulen, masih perlu dikaji secara mendalam.
Pemanfaatan teknik kultur in vitro yang dikombinasikan dengan induksi mutagen EMS adalah upaya untuk meningkatkan keragaman genetik tanaman dan memperoleh tanaman yang tahan terhadap ChiVMV. Upaya tersebut dilakukan karena relatif lebih aman dan murah. Hasil perlakuan EMS menunjukkan bahwa persentase kematian eksplan akan meningkat dengan semakin tingginya konsentrasi EMS dan semakin panjangnya waktu perendaman eksplan. Perlakuan EMS terhadap lima genotipe uji yaitu Jatilaba, ICPN12 no.4, PBC495, Helem dan Gelora, memperlihatkan respon yang berbeda terhadap persentase kematian jaringan. Pada perendaman 15, 30, dan 60 menit dengan konsentrasi EMS 0,25% jaringan yang mati berturut-turut berkisar antara 10% sampai 36%, 10% sampai 46%, dan 30% sampai 80%; pada konsentrasi EMS 0.5% berturut turut adalah 30% sampai 80%, 30% sampai 97% dan 49% sampai 96%; sedangkan pada konsentrasi EMS 1% dengan masa perendaman yang sama seperti di atas kematian jaringan berkisar antara 58% sampai 100%. Berdasarkan persentase jaringan tanaman yang hidup, nilai LC50 diperoleh pada konsentrasi EMS 0,5%
pada saat perlakuan induksi akar.
Tanaman yang berhasil diaklimatisasi dan dapat bertahan hidup adalah tanaman mutan somaklon dari genotipe Gelora. Tanaman mutan somaklon tersebut mampu menghasilkan buah dan benih cabai. Penampilan tanaman mutan somaklon tidak jauh berbeda dengan tanaman normal. Walaupun demikian kedua tanaman mutan somaklon cenderung memiliki tinggi tanaman dan tinggi cabang yang lebih rendah dibandingkan tanaman normal.
Evaluasi ketahanan untuk tanaman mutan somaklon dilakukan berturut-turut terhadap 245 dan 243 benih mutan somaklonl 1 (M1.1) dan mutan somaklon 2 (M1.2) yang dipilih secara acak. Setelah inokulasi ChiVMV, jumlah tanaman bergejala pada populasi M1.1 adalah 229 tanaman, sedangkan pada populasi M1.2 adalah 223 tanaman. Persentase tanaman terinfeksi dari kedua populasi mutan somaklon tersebut berturut turut adalah 95,5% dan 91,7%, sedangkan tanaman yang tidak memperlihatkan gejala atau toleran berturut-turut adalah 6,5% dan 8,23%. Konfirmasi melalui deteksi DAS-ELISA menunjukkan bahwa jumlah tanaman terinfeksi pada masing-masing tanaman mutan somaklon lebih tinggi dibandingkan hasil pengamatan berdasarkan gejala. Hasil deteksi dengan ELISA memastikan bahwa 20 dari total 488 tanaman cabai uji berasal dari 2 mutan somaklon tidak terinfeksi ChiVMV. Hasil tersebut menunjukkan adanya fenomena gejala lemah atau gejala laten. Dengan demikian ke 20 tanaman tersebut digolongkan tahan ChiVMV dan dapat digunakan sebagai sumber gen ketahanan didalam meningkatkan perluasan varietas melalui perakitan tanaman yang memiliki sifat unggul lainnya.
Kata kunci: Capsicum annuum, Chilli veinal mottle potyvirus, induksi mutasi, keragaman biologi, keragaman molekuler.
© Hak cipta milik Institut Pertanian Bogor, tahun 2011
Hak cipta dilindungi Undang Undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah
b. Pengutipan tidak merugikan kepentingan yang wajar IPB
PENYEBAB PENYAKIT BELANG PADA CABAI (Capsicum
annuum L.): KERAGAMAN ISOLAT DAN STRATEGI
PENGENDALIANNYA MELALUI INDUKSI
VARIASI SOMAKLONAL
IFA MANZILA
Disertasi
Sebagai salah satu syarat untuk memperoleh gelar Doktor
pada
Program Studi Entomologi-Fitopatologi
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Penguji Luar Komisi pada Ujian Tertutup: Dr Ir Endang Nurhayati, MS Dr Ir Dewi Sukma, MSi
Judul Disertasi : Chilli Veinal Mottle Potyvirus (ChiVMV) Penyebab Penyakit Belang pada Cabai (Capsicum annuum L.): Keragaman Isolat dan Strategi Pengendaliannya Melalui Induksi Variasi Somaklonal
Nama Mahasiswa : IFA MANZILA
NIM : A461060091
Disetujui Komisi Pembimbing
Dr Ir Sri Hendrastuti Hidayat, MSc Prof Dr Ir Sriani Sujiprihati, MS Ketua Anggota
Dr Ir Ika Mariska, MSc, APU Anggota
Diketahui
Ketua Program Studi Dekan Sekolah Pascasarjana Entomologi-Fitopatologi
Dr Ir Sri Hendrastuti Hidayat, MSc Dr Ir Dahrul Syah, MSc Agr
PRAKATA
Puji dan syukur penulis panjatkan kehadirat Allah SWT. Karena berkat
dan rahmat-Nya sehingga disertasi yang berjudul ”Chilli Veinal Mottle Potyvirus (ChiVMV) Penyebab Penyakit Belang pada Cabai (Capsicum annum L.): Keragaman Isolat dan Strategi Pengendaliannya melalui Induksi Variasi Somaklonal” dapat terselesaikan.
Penulis menyampaikan rasa terima kasih yang tak terhingga kepada Dr Ir
Sri Hendrastuti Hidayat MSc selaku Ketua komisi pembimbing, Prof Dr Ir Sriani
Sujiprihati MS, dan Dr Ir Ika Mariska MSc, APU selaku anggota komisi
pembimbing, atas segala kesabaran dan bimbingan, kritik, saran , serta dukungan
moril yang sangat besar peranannya dalam terselesaikannya disertasi ini.
Penulis juga mengucapkan terima kasih kepada Kepala Badan Litbang
Pertanian, Ketua Komisi Pembinaan Tenaga Badan Litbang Pertanian, Kepala
Balai Besar Penelitian dan Pengembangan Bioteknologi dan Sumberdaya Genetik
Pertanian(BB-BIOGEN), yang telah menugaskan dan memberi kesempatan
kepada penulis untuk melanjutkan pendidikan, serta pimpinan dan staf bendahara
Badan Litbang Pertanian yang telah membantu mempermudah penyaluran dana
pendidikan penulis.
Kepada Ketua Kelompok Peneliti Biokimia BB-BIOGEN, yang telah
memberi ijin dan kesempatan kepada penulis untuk melanjutkan pendidikan.
Kepada Kepala Program Penelitian Badan Litbang Pertanian dalam proyek
Kerjasama Kemitraan Penelitian Pertanian dengan Perguruan Tinggi (KKP3T)
penulis mengucapkan terima kasih atas bantuan dana penelitian yang berjudul
INDUKSI VARIASI SOMAKLONAL UNTUK MENDAPATKAN GALUR CABAI (Capsicum annuum L.) TAHAN CHILLI VEINAL MOTTLE POTYVIRUS.
Kepada Ketua Kelompok Peneliti Biologi Seluler dan Jaringan
BB-BIOGEN beserta Staf dan Kepala Laboratorium Virologi Departemen Proteksi
Tanaman Faperta IPB yang telah memberi izin dan kesempatan penulis untuk
melakukan penelitian dan mengerjakan sebagian dari proyek penelitian yang
penguji pada ujian prakualifikasi penulis mengucapkan terima kasih.
Kepada Dr Ir Endang Nurhayati MSc dan Dr Ir Dewi Sukma MSi yang
telah berkenan untuk menjadi penguji pada ujian sidang tertutup penulis
mengucapkan terima kasih.
Kepada Ketua Program Studi Entomologi-Fitopatologi dan semua staf
dosen IPB penulis mengucapkan terima kasih atas ilmu yang telah diberikan,
Penulis juga menyampaikan rasa terima kasih dan penghargaan kepada
teman-teman Laboratorium Virologi, Tuti Susanti Legiastuti, Dr I Gede Rai Maya
Temaja, Dr Jumsu Trisno, Irwan Lakani MSi, Rika MSi, Rita Noveriza MSc, Sri
Budi Utami Sp, Devi Agustina MSi, Fitrianingrum Sp, Wawan MSi, Endang
Opriana MSi, Latifah MSi, Mila MSi, Putri Sp, Damayanti Sp, Ani Rahmini MSi,
Adik-adik mahasiswa S1, Pak Emput. Ucapan terima kasih juga penulis
sampaikan kepada teman-teman PS Entomologi-Fitopatologi terutama kepada Dr
Yusmani; Dr N Usyati, Dr Rita Harni, Dr. Iwa Munara, Samsudin MSi, Efi Taufik
MSi.
Ucapan terima kasih penulis sampaikan kepada Dr Tri Puji Prayitno MSc,
Dr I Made Samudera, Dr Chairani, Yadi Suryadi MSc, Alina Ahdiyah MSi.
Secara khusus penulis menyampaikan penghargaan dan terima kasih
kepada yang tercinta, Ayahanda Abdul Aziz (Alm), Ibunda H. Siti Zubaidah, dan
semua kakak, adik-adik, keponakan atas segala pengertian, dorongan, dan doa
yang tiada henti sehingga penulis dapat menyelesaikan pendidikan. Ungkapan
terima kasih juga disampaikan kepada ananda tersayang Muhamad Alif
Nadhirahman dan Daniella Ridha Artanti atas segala dorongan semangat,
pengertian, kasih sayang, motivasi dan inspirasi selama penulis menempuh studi.
Akhirnya penulis berharap mudah-mudahan tulisan ini dapat bermanfaat
bagi kita semua.
Bogor, 12 April 2011
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 02 Januari 1965 dari pasangan
Bapak Abdul Aziz (Alm) dan ibu Hj. Siti Zubaidah. Penulis merupakan putri ke
empat dari delapan bersaudara.
Tahun 1983 penulis lulus dari SMA Negeri 38 Jakarta dan pada tahun
yang sama masuk Universitas Nasional Jakarta Jurusan Biologi. Tahun 1987
penulis mendapat gelar Sarjana Biologi. Di tahun yang sama penulis diterima
bekerja di Pusat Pengembangan Agribisnis (Konsultan). Sejak tahun 1993, penulis
bekerja sebagai staf peneliti pada Kelti Fitopatologi yang sekarang berganti nama
menjadi Kelti Biokimia, Balai Besar Penelitian dan Pengembangan Bioteknologi
dan Sumberdaya Genetik Pertanian, Jl. Tentara Pelajar 3A Bogor, Jawa Barat.
Tahun 1996 penulis mendapat kesempatan untuk melanjutkan studi Program
Magister Sains di Program Pascasarjana IPB dengan beasiswa dari BB-BIOGEN.
Tahun 1999 penulis lulus dan mendapat gelar Magister Sains (M.Si). Di tahun
yang sama penulis menikah dan dikaruniai dua orang anak putra dan putri,
Muhamad Alif Nadhirahman Nugroho (10 tahun) dan Daniella Ridha Artanti
Nugroho (8 tahun). Tahun 2006 penulis diterima sebagai mahasiswa Program
Doktor (S3) pada program studi Entomologi dan Fitopatologi Sekolah
Pascasarjana IPB dengan beasiswa dari Badan Penelitian dan Pengembangan
Pertanian, Departemen Pertanian.
Penulis saat ini bekerja sebagai staf peneliti di Kelompok Peneliti
Biokimia, Balai Besar Penelitian dan Pengembangan Bioteknologi dan
Sumberdaya Genetik Pertanian (BB-BIOGEN) Bogor, sejak tahun 1993 sampai
Halaman
DAFTAR TABEL ……… xvi
DAFTAR GAMBAR ... xix
DAFTAR LAMPIRAN ... xx
I. PENDAHULUAN ………... 1
Latar Belakang ...………... 1
Tujuan Penelitian ………... 4
Hipotesis ………... 5
Diagram alur ruang lingkup penelitian ………... 6
Daftar Pustaka ... 7
II. TINJAUAN PUSTAKA ………. 9
Karakter Molekuler Chilli Veinal Mottle Potyvirus ... Hama dan Penyakit Tanaman Cabai ... Gejala infeksi ChiVMV pada tanaman cabai ... 9 12 13 Kisaran Inang dan Mekanisme Penularan ChiVMV ... 14
Deteksi dan Karakterisasi Virus ... 14
Ketahanan Tanaman terhadap ChiVMV ... 16
Pembentukan Variasi Somaklonal ... 18
Penyebab Variasi Somaklonal ... 21
Mutasi Secara Fisik dan Kimia ... 21
Variasi Somaklonal untuk mendapatkan Resistensi terhadap Penyakit... Pemanfaatan dan Penerapan Variasi Somaklonal... 24 25 Daftar Pustaka ... 26
III. VIRULENSI BEBERAPA ISOLAT Chilli Veinal Mottle Potyvirus PADA TANAMAN CABAI (Capsicum annuum L.): ... 32 Abstrak ... 32
Abstract ... 33
Pendahuluan ... 34
xiv
Hasil ... 38
Pembahasan ... 44
Simpulan dan Saran... 46
Daftar Pustaka ... 47
IV.
ANALISIS GEN SELUBUNG PROTEIN
Chilli Veinal
Mottle Potyvirus
DARI BEBERAPA DAERAH DI
INDONESIA
49 Abstrak ... 49Abstract ... 50
Pendahuluan ... 51
Bahan dan Metode ... 52
Hasil ... 56
Pembahasan ... 65
Simpulan dan Saran... 69
Daftar Pustaka …... 70
V. INDUKSI KALUS DAN REGENERASI TUNAS DAN AKAR CABAI (Capsicum annuum L.) MELALUI KULTUR IN VITRO... 74 Abstrak ... 74
Abstract ... 75
Pendahuluan ... 76
Bahan dan Metode ... 77
Hasil ... 80
Pembahasan ... 80
Simpulan dan Saran... 88
VI. PENGARUH PERLAKUAN Ethyl Methane Sulfonate PADA TANAMAN CABAI (Capsicum annuum L.) DAN KETAHANANNYA TERHADAP Chilli veinal mottle potyvirus (ChiVMV)
91
Abstrak ... 91
Abstract ... 92
Pendahuluan ... 93
Bahan dan Metode ... 94
Hasil ... 97
Pembahasan ... 97
Simpulan dan Saran... 106
Daftar Pustaka ... 106
VII. PEMBAHASAN UMUM ... Daftar Pustaka ……….
109 113
VIII. SIMPULAN DAN SARAN UMUM...
115
xvi
DAFTAR TABEL
Halaman
2.1 Fungsi beberapa protein yang terdapat dalam struktur genom Potyvirus ...
10
3.1
3.2
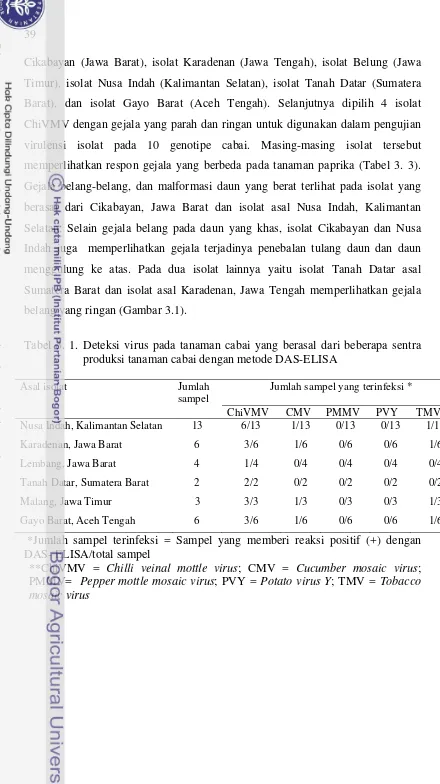
Deteksi beberapa virus pada tanaman cabai yang berasal dari beberapa sentra produksi tanaman cabai dengan metode DAS-ELISA ...
Deskripsi gejala tanaman yang terinfeksi ChiVMV secara tunggal dari beberapa lokasi penanaman cabai ...
39
40
3.3 Deskripsi isolat ChiVMV yang digunakan dalam pengujian virulensi ...
40
3.4 Hasil inokulasi ChiVMV isolat Cikabayan pada 10 genotipe cabai ……….
42
3.5 Hasil inokulasi ChiVMV isolat Nusa Indah pada 10 genotipe cabai ………
42
3.6 Hasil inokulasi ChiVMV isolat Tanah Datar pada 10 genotipe cabai ………..……….
43
3.7 Hasil inokulasi ChiVMV isolat Karadenan pada 10 genotipe cabai ……….
43
4.1 Isolat-isolat Chilli veinal mottle potyvirus asal Indonesia dan beberapa virus asal Asia (GeneBank) yang digunakan dalam analisis CP- ChiVMV………..………...
55
4.2
4.3
Deskripsi gejala isolat-isolat ChiVMV yang berasal dari Karadenan (KR), Cikabayan (CKB), Tanah Datar (TD), Nusa Indah (NI), Belung (BL) dan Gayo Barat (GB) ...
Ukuran panjang gen CP beberapa isolat ChiVMV ...
56
58
4.4 Tingkat kesamaan isolat ChiVMV yang berasal dari beberapa daerah di Indonesia berdasarkan runutan nukleotida gen Coat protein ...
58
4.5 Tingkat kesamaan 9 isolat ChiVMV berdasarkan runutan asam amino seelubung protein ...
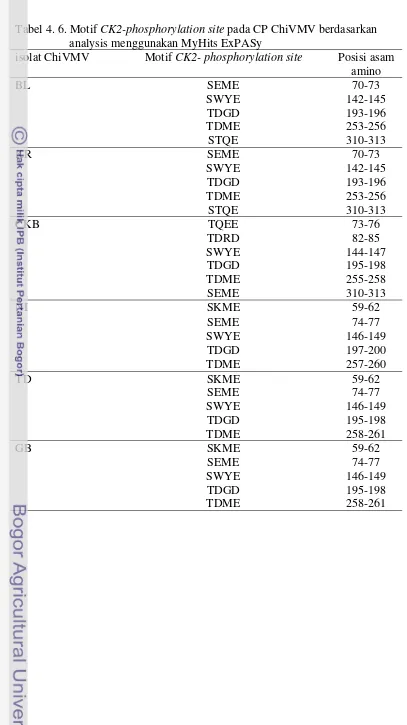
4.6 Motif CK2I-phospholylation site pada CP ChiVMV berdasarkan analysis menggunakan MyHits ExPASy...
64
5.1 Pembentukan kalus dari eksplan daun muda cabai genotype Gelora, Sudra, dan Chili 109 pada media MSdengan tiga taraf konsentrasi BAP ………..….……….……….
81
5.2 Pembentukan kalus dari eksplan hipokotil cabai genotipe Gelora,Sudra, dan Chili 109 pada media MS dengan tiga taraf
konsentrasi BAP ………..…….………
82
5.3 Pembentukan kalus dari eksplan ujung akar cabai genotipe Gelora, Sudra, dan Chili 109 pada media MS dengan tiga taraf konsentrasi BAP…..…….. ……….………..……….
83
5.4 Pembentukan kalus embriogenik dari kalus cabai cv Gelora, Sudra dan Chili 109 yang ditanam pada media induksi kalus embriogenik dengan tiga taraf konsentrasi 2,4D ………
84
5.5 Waktu inisiasi tunas, jumlah tunas, tinggi tunas, serta jumlah daun yang terbentuk pada kalus yang berasal dari eksplan daun muda cabai genotipe Gelora, Sudra, dan Chili 109 yang ditanam pada tiga media regenerasi yang mengandung tiga taraf konsentrasi BAP ………..………
86
5.6
6.1
Respon pembentukan akar pada tunas yang berasal dari eksplan daun muda cabai genotipe Gelora dan Chili 109 terhadap dua taraf konsentrasi NAA yang berbeda …..………..
Pengelompokan tipe ketahanan tanaman berdasarkan reaksi terhadap infeksi ChiVMV...
87
97
6.2 Pengaruh konsentrasi EMS dan waktu perendaman terhadap kematian jaringan eksplan cabai ………
99
6.3 Waktu inisiasi tunas, jumlah tunas, tinggi tunas, dan jumlah daun yang terbentuk pada eksplan tunas terminal Jatilaba, PBC495 dan Gelora yang ditanam pada media MS +.BAP 5 mg l-1 + TDZ 0,5
mg l-1*) ………..
101
6.4 Karakter varian morfologi pada tanaman mutan somaklon (M1.1 dan M1.2) hasil induksi mutasi dengan EMS 0,5% dan waktu perendaman 60 menit ...
101
6.5 Karakter buah yang dihasilkan oleh tanaman mutan somaklonal hasil induksi mutasi dengan EMS 0,5% dan waktu perendaman 60 menit ...
xviii
6.7 Penapisan dan evaluasi respon mutan somaklon cabai hasil kombinasi induksi mutasi dengan EMS dan ketahananya terhadap ChiVMV ………...
DAFTAR GAMBAR
Halaman
1. 1
2. 1
Diagram alur penelitian ”Chilli Veinal Mottle Potyvirus (ChiVMV) Penyebab Penyakit Belang Pada Cabai (Capsicum annum): Keragaman Isolat dan Strategi Pengendaliannya Melalui Induksi Variasi Somaklonal” ………..
Organisasi genom potyvirus...
6
10
3. 1 Variasi gejala infeksi beberapa isolat ChiVMV pada Tanaman cabai paprika genotipe Beauty Bell ...
41
4. 1 Berbagai tipe belang pada permukaan daun tanaman cabai paprika genotipe Beauty Bell yang terinfeksi ChiVMV ...
56
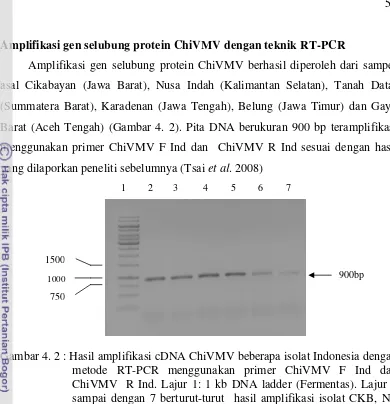
4. 2 Hasil amplifikasi cDNA ChiVMV isolat Indonesia dengan metode RT-PCR menggunakan primer ChiVMV F Ind dan ChiVMV R Ind ...
57
4. 3 Analisis filogenetika 12 isolat ChiVMV yang berasal dari beberapa daerah yang berbeda di Indonesia dan Asia (GeneBank) ...
59
4. 4 Analisis homologi asam amino CP-ChiVMV yang berasal dari Cikabayan, Jawa Barat (ChiVMV CKB), Karadenan, Jawa Tengah (ChiVMV KR), Belung, Jawa Timur (ChiVMV BL), Nusa Indah, Kalimantan Selatan(ChiVMV NI), Tanah Datar, Sumatra Barat (ChiVMV TD) dan Gayo Barat, Aceh Tengah (ChiVMV GB). ………..
62
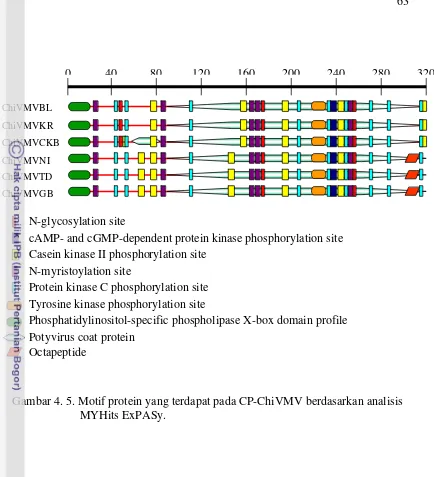
4. 5 Motif protein yang terdapat pada CP-ChiVMV berdasarkan analisis MYHits ExPASy………...
63
4. 6 Analisis filogenetika asam amino CP-ChiVMV yang berasal dari Jawa Barat (Cikabayan), Jawa Tengah (Karadenan), Jawa Timur (Belung), Kalimantan Selatan (Nusa Indah), Sumatra Barat (Tanah Datar), Aceh Tengah (Gayo Barat) terhadap isolat Indonesia dan Asia yang ada pada GeneBank (Cikabayan2, Pataruman dan Taiwan)...
65
5. 1 Pertumbuhan kalus dari eksplan daun muda cabai genotipe Gelora pada media MS+2,4- D +Thidiazuron 0,1mg/l …..……...
xx
5. 2 Perkembangan kultur cabai varietas Gelora mulai dari eksplan hingga pembentukan tunas………..
87
a
6. 1 A: Kecambah cabai merah berumur 21 hari yang dipakai sebagai sumber eksplan dari genotipe gelora, B: Ujung tunas terminal ………..
95
6. 2 Respon eksplan genotipe cabai‘Gelora‘terhadap perlakuan berbagai konsentrasi EMS dengan waktu perendaman 60 menit A) 0.25%, B) 0.5%, C) 1% ...
98
6. 3 Aklimatisasi planlet cabai setelah perlakuan EMS 0,5% dengan perendaman selama 60 menit...
102
6. 4 Tanaman mutan somaklon genotipe Gelora…………...……… 103
6. 5 Buah cabai yang dipanen dari tanaman mutan somaklon …….... 104
6. 6 Penapisan dan evaluasi tanaman mutan somaklonal cabai terhadap infeksi ChiVMV ………..…..………..
105
DAFTAR LAMPIRAN
Halaman
1 Perunutan DNA yang berasal dari 12 isolat ChiVMV Indonesia dan Asia (Gene Bank) menunjukkan nukleotida yang identik ………..
Latar Belakang
Tanaman cabai (Capsicum annun L.) merupakan salah satu komoditas
andalan hortikultura di Indonesia. Menurut data Direktorat Jenderal Bina Produksi
Hortikultura (2009) luas panen cabai merupakan luas panen terbesar diantara
tanaman sayuran lainnya yaitu 103.837 ha. Tanaman tersebut ditanam di seluruh
provinsi di Indonesia dan memiliki nilai ekonomis yang cukup baik sehingga
mendapat prioritas untuk dikembangkan.
Produksi cabai di Indonesia masih sangat rendah yaitu 6,72 ton/ha apabila
dibandingkan dengan potensi produksi yang dapat mencapai 12,99 ton/ha.
Produksi nasional cabai dari tahun 2003 sampai tahun 2009 mengalami penurunan
yaitu berturut-turut 774.408 dan 668.970 ton (Direktorat Jendral Hortikultura
2009). Padahal permintaan cabai nasional terus meningkat dari waktu ke waktu
sejalan dengan meningkatnya rata-rata konsumsi cabai dan meningkatnya jumlah
penduduk.
Beberapa faktor penyebab turunnya produksi cabai secara nasional adalah
berkurangnya luas panen, belum tepatnya cara bercocok tanam, belum
berimbangnya pemupukan dan sukarnya mendapatkan benih yang bermutu dan
murah. Selain faktor-faktor di atas, rendahnya produksi cabai nasional juga
diakibatkan oleh adanya gangguan hama dan penyakit (Duriat et al. 1996).
Direktorat Perlindungan Tanaman Hortikultura (2009) mencatat beberapa
penyakit penting pada tanaman cabai diantaranya adalah antraknosa, bercak daun
Cercospora, bercak Phytophthora, layu Fusarium, layu bakteri dan penyakit yang
disebabkan oleh infeksi virus. Hasil beberapa laporan penelitian menunjukkan
bahwa virus utama yang menyerang tanaman cabai dan hampir ditemukan di
setiap pertanaman cabai adalah Geminivirus, Cucumber mosaic virus (CMV) dan
Chilli veinal mottle virus (ChiVMV) (Sulandari et al. 2006, Taufik et al. 2005,
Trisno et al. 2009)
Infeksi ChiVMV menjadi penting karena prevalensi penyakit yang
disebabkan oleh virus ini dari waktu ke waktu mengalami peningkatan dan
kerugian yang ditimbulkannya cukup besar. Di Malaysia, ChiVMV dapat
2
Dilaporkan oleh AVRDC (2003) bahwa kehilangan hasil akibat infeksi ChiVMV
bisa mencapai 100%. Hasil survei yang dilakukan Taufik et al. (2005)
memperkuat bukti penyebaran ChiVMV yang sangat luas di Indonesia. Infeksi
virus tersebut dapat ditemukan pada setiap pertanaman cabai yang diamati di Jawa
Barat, Jawa Tengah, dan Sulawesi Selatan walaupun kejadian penyakit
berbeda-beda untuk setiap tempat.
Tanaman cabai yang terinfeksi, pada daunnya akan memperlihatkan gejala
belang-belang hijau gelap, dan kadang-kadang pola-pola tersebut menyatu ke
tulang daun di dekatnya, leaf cupping, epinasti dan nekrosis. Gejala yang
disebabkan oleh ChiVMV bervariasi tergantung pada inang, strain virus, waktu
infeksi dan kondisi lingkungan. (CABI 2005). Infeksi yang terjadi pada fase
pertumbuhan awal mengurangi ukuran daun yang diikuti dengan distorsi, serta
produksi buah yang lebih sedikit dan lebih kecil (Shah dan Khalid 2001).
ChiVMV termasuk jenis virus yang sulit dikendalikan antara lain karena
virus ini ditularkan oleh serangga vektor yaitu Aphid spp. secara non persisten.
Penyebaran virus ini terjadi dalam waktu yang cepat dikarenakan oleh aktifitas
serangga vektor. Disamping itu ChiVMV juga memiliki kisaran inang yang cukup
luas. Selain menginfeksi Capsicum annuum, ChiVMV dilaporkan menginfeksi C.
frutescens, Lycopersicon esculentum, Solanum melongena, Datura stramonium,
Nicotiana spp, dan Chenopodium spp. (Green et al. 1999).
Usaha pengendalian penyakit belang pada cabai yang disebabkan oleh
ChiVMV sampai saat ini masih sulit untuk dilakukan karena tidak ada bahan
kimia yang dapat diaplikasikan secara langsung untuk mengendalikan virus
tersebut. Pengendalian umumnya dilakukan secara tidak langsung antara lain
dengan mengurangi sumber inokulum dengan cara mencabut tanaman-tanaman
yang telah menunjukkan gejala serangan virus, melakukan pergiliran tanaman,
dan pemberantasan gulma yang dapat menjadi inang alternatif virus, dan
mengendalikan perkembangan serangga vektor dengan menggunakan pestisida.
Cara-cara pengendalian tersebut terkadang tidak efektif karena proses penularan
virus dapat terjadi dengan cepat mengingat kutu daun dapat menularkan virus ke
tanaman sehat hanya dalam hitungan menit sampai jam. Hal lain yang perlu
buah dan membahayakan, mencemari lingkungan serta membutuhkan biaya yang
besar. Dengan demikian penggunaan varietas tahan merupakan pilihan yang tepat
untuk mengendalikan virus karena metode ini relatif lebih aman dan murah bila
dibandingkan dengan metode pengendalian yang lain (Dolores 1998) .
Beberapa pendekatan dalam melakukan perakitan varietas tahan virus
dapat dilakukan diantaranya adalah pendekatan konvensional, rekayasa genetik
dan melalui pemanfaatan kultur in vitro yang dikombinasi dengan induksi mutasi
menggunakan mutagen kimia. Pendekatan konvensional untuk pengembangan
varietas tahan virus memiliki beberapa keterbatasan, diantaranya adalah sumber
gen ketahanan terhadap virus masih belum ditemukan pada koleksi plasma nutfah
cabai di Indonesia. Selain itu, kultivar tahan yang dihasilkan melalui pemuliaan
konvensional seringkali mudah terpatahkan karena perubahan genetik dari virus
yang cepat akibat adanya rekombinasi dan adanya variasi genetik yang tinggi dari
virus. Kultivar tahan yang dihasilkan mungkin hanya spesifik untuk strain atau
isolat tertentu. Bila sumber gen ketahanan terhadap virus sangat terbatas, maka
diperlukan pendekatan lain seperti pemanfaatan teknik kultur in vitro untuk
mendapatkan varian somaklonal. Teknik ini banyak dilakukan karena selain dapat
menghasilkan tanaman dalam jumlah yang banyak, juga dapat menghasilkan
keragaman somaklonal. Keragaman somaklonal dapat dilakukan melalui
beberapa perlakuan, diantaranya melalui perlakuan zat pengatur tumbuh (ZPT),
subkultur berulang dengan periode kultur in vitro yang panjang (Ahloowalia
2004). Keragaman genetik melalui kultur in vitro dapat ditingkatkan apabila
dikombinasikan dengan perlakuan mutagen fisik dan kimiawi (Girija dan
Dhanavel 2009). Pemanfaatan teknik tersebut adalah upaya untuk meningkatkan
keragaman genetik tanaman dan memperoleh gen baru yang lebih luas (Mattjik
2005). Sifat ketahanan tanaman terhadap beberapa cekaman biotik seperti
misalnya cendawan, virus dan bakteri telah dapat diperbaiki dengan pendekatan
ini.
Di dalam pengembangan tanaman cabai tahan virus, adanya informasi
tentang keragaman genetik virus akan dapat bermanfaat dalam hal pemilihan
lokasi yang spesifik untuk genotipe terhadap isolat-isolat tertentu, sehingga
4
suatu strain virus yang menginfeksi tanaman cabai perlu diketahui sehingga dapat
diambil langkah-langkah pengendaliannya. Isolat-isolat ChiVMV di India,
Vietnam, Taiwan, dan China telah berhasil diidentifikasi secara molekuler. Di
Indonesia, keragaman genetik ChiVMV berdasarkan perunutan basa DNA belum
banyak dilaporkan. Usaha identifikasi melalui teknik hibridisasi asam nukleat dan
PCR telah dirintis oleh beberapa peneliti (Taufik 2006; Opriana 2009). Namun
demikian, informasi yang lebih mendalam mengenai urutan DNA dari ChiVMV
yang ada di Indonesia untuk menunjukkan adanya keragaman genetik diantara
ChiVMV belum pernah dilakukan.
Dalam rangka pengembangan genotipe cabai yang tahan terhadap
ChiVMV telah dilakukan penelitian berjudul “ Chilli Veinal Mottle Potyvirus
(ChiVMV) Penyebab Penyakit Belang Pada Cabai (Capsicum annum): Keragaman
Isolat dan Strategi Pengendaliannya Melalui Induksi Variasi Somaklonal” melalui
tahapan survey ChiVMV, isolasi dan karakterisasi strain ChiVMV, induksi mutasi,
dan evaluasi ketahan tanaman mutan somaklon (Gambar 1.1)
Tujuan Penelitian
1. Memperoleh informasi tentang sebaran ChiVMV pada pertanaman cabai di
beberapa sentra produksi di Indonesia melalui survey dan deteksi
menggunakan metode Double antibody sandwich – Enzyme linked
immunosorbend assay (DAS-ELISA) dan Polymerase chain reaction (PCR).
2. Mendapatkan informasi tentang tingkat virulensi isolat-isolat ChiVMV
terhadap 10 genotipe cabai.
3. Mengetahui keragaman gen selubung protein beberapa isolat-isolat ChiVMV
Indonesia.
4. Mendapatkan varian somaklon tanaman cabai melalui teknik kombinasi
antara kultur in vitro dan induksi dengan ethyl methane sulfonate (EMS)
Hipotesis
1. ChiVMV telah menyebar di beberapa sentra produksi cabai di Indonesia
diantaranya di Jawa Barat, Jawa Tengah, Jawa Timur, Kalimantan Selatan,
Sumatera Barat, Aceh Tengah.
2. Isolat-isolat ChiVMV memiliki tingkat virulensi yang berbeda terhadap 10
genotipe cabai tanaman uji.
3. Strain-strain ChiVMV di Indonesia memiliki keragaman pada gen
selubung proteinnya
4. Teknik kultur in vitro dapat meningkatkan keragaman somaklonal
tanaman
5. Variasi somaklonal yang dikombinasikan dengan mutagen kimia ethyl
methane sulphonate pada tunas terminal dapat menghasilkan genotipe
baru dengan karakter agronomis dan sifat ketahanan terhadap ChiVMV
yang berbeda.
6. Terdapat perbedaan sifat ketahanan terhadap ChiVMV pada tanaman hasil
6
Gambar 1. 1. Diagram alur penelitian“ Chilli Veinal Mottle Potyvirus (ChiVMV) Penyebab Penyakit Belang Pada Cabai (Capsicum annum):
Keragaman Isolat dan Strategi Pengendaliannya Melalui Induksi Variasi Somaklonal”
Mutan somaklon yang tahan ChiVMV
Evaluasi tanaman mutan somaklon untuk karakter Agronomis (M0) Optimasi dan evaluasi berbagai konsentrasi dan lama perendaman mutagen EMS pada beberapa eksplan genotipe cabai
Uji Virulensi isolat ChiVMV terhadap 10 genotipe cabai
Regenerasi planlet dari tunas ganda yang telah diperlakukan mutagen EMS
Evaluasi Tanaman M1 terhadap infeksi strain ChiVMV yang paling virulen
Survei sebaran ChiVMV di beberapa sentra produksi cabai di Jawa, Sumbar, Kalsel, Aceh Tengah
Studi regenerasi kalus dan tunas terminal membentuk tunas adventif dan tunas ganda dalam media kultur in vitro
DAFTAR PUSTAKA
Ahloowalia BS, Prakash J, Savangikar VA, Savangikar C. 2004. Plant tissue culture. International Atomic Energy Agency. Austria. P. 3-10
AVRDC. 2003. AVRDC Progress Report 2002. Shanhua, Tainan, Taiwan. Hlm 182
[CABI] Centre in Agricultural and Biological Institute. 2005. Chilli veinal mottle virus. Crop Protection Compendium [CD-ROM]. London: CABI Publish.
[DBPH] Direktorat Bina Program Tanaman Pangan dan Hortikultura RI. 2009. Luas panen, rata-rata hasil dan produksi tanaman hortikultura di Indonesia. Departemen Pertanian. Jakarta
[Ditlinhorti] Direktorat Perlindungan Tanaman Hortikultura 2009. Luas Pertanaman Cabai Merah. (http:www.deptan.go.id/ditlinhorti/da-its-2009 (5 Maret 2010)
[Ditjen Hort] Direktorat Jendral Hortikultura. 2009. Perkembangan luas panen sayuran tahun 2003-2009. http://www.deptan.go.id [25 Desember 2010].
Dolores LM. 1996. Management of pepper viruses. Proceeding of the AVNET II Final Workshop Philippines 21-25 Februari 1995. AVRDC.
Duriat AS. 1996. Cabai merah: Komoditas Prospektif dan Andalan. Di dalam: Duriat AS, Widjaja W. Hadisoeganda A, Soetiarso TA dan Prabaningrum L, editor. TeknologiProduksi Cabai Merah. Pusat Penelitian dan Pengembangan Hortikultura, Badan Penelitian dan Pengembangan Pertanian. Hlm 1-3
Girija M, Dhanavel D. 2009. Mutagenic effectiveness and efficiency of gamma rays Ethyl Methane Sulfonate and their combined treatments in Cowpea (Vigna ungiculata L. Walp). Glob J of Mol Scien 4(2):68-75.
Green SK, Hiskias Y, Lesemann DE, Vetten HJ, 1999. Characterization of chilli veinal mottle virus as a potyvirus distinct from pepper veinal mottle virus. Petria 9(3):332.
Mattjik NA. 2005. Peran Kultur Jaringan dalam Perbaikan Tanaman, Fakultas Pertanian, IPB. Bogor. Hlm 102.
Ong CA. 1995. Symptomatic variants of CVMV in Malaysia. Proceeding of the AVNET II Midterm Workshop Philippines 21-25 Februari 1995. AVRDC.
8
Sulandari S, Suseno R, Hidayat SH, Harjosudarmo J, Sosromarsono S. 2006. Deteksi dan kajian kisaran inang virus penyebab penyakit daun keriting kuning cabai. Hayati 13:1-6
Taufik M, Astuti AP, Hidayat SH. 2005. Survey infeksi Cucumber mosaic virus dan Chilli veinal mottle virus pada tanaman cabai dan seleksi ketahanan beberapa kultivar cabai. J. Agrikultura 16:146-152.
Karakter Molekuler Chilli Veinal Mottle Potyvirus
Chilli veinal mottle potyvirus (ChiVMV) adalah salah satu virus penyebab
penyakit pada tanaman cabai. Virus tersebut pertamakali diisolasi oleh Burnett
pada tahun 1947 dari Capsicum annuum di Malaysia. Partikel virus berbentuk
batang lentur dengan panjang sekitar 750 nm dan diameter kira-kira 12 nm
(International Taxonomy on Committee of Viruses, 2002). ChiVMV termasuk
dalam kelompok atau genus Potyvirus (famili Potyviridae) dengan genom berupa
RNA utas tunggal berorientasi positif (+ ssRNA) berukuran 9711 nukleotida (nt)
(Fauquet et al. 2005). Genus Potyvirus sendiri termasuk kelompok virus yang
paling banyak menyerang tanaman, yaitu mencapai lebih dari 100 jenis virus
( Ong 1995).
Potyvirus memiliki selubung protein yang berfungsi untuk penularan
melalui kutu daun, pergerakan virus dari sel ke sel dan pergerakan virus secara
sistemik, pembentukan selubung virus, dan replikasi virus (Tabel 2. 1)
(Urcuqui-Inchima et al. 2001). Menurut Moury et al. (2005), ChiVMV dapat dibedakan dari
Pepper veinal mottle virus berdasarkan runutan asam amino selubung protein.
Tingkat kesamaan runutan asam amino kedua jenis virus tersebut hanya mencapai
80%, sedangkan antara strain yang berbeda dalam spesies yang sama mempunyai
tingkat kesamaan mencapai 83%-99% (Fauquet et al. 2005).
Genom Potyvirus mempunyai satu open reading frame (ORF) yang
mengkode 340-350 KDa prekursor poliprotein. Translasi RNA Potyvirus dimulai
dari kodon awal AUG pada posisi nukleotida 145-147 dari ujung 5’ genom
Potyvirus, kodon stop terletak pada nukleotida ke 9525- 9589 dari ujung 3’ genom
10
Tabel 2. 1. Fungsi beberapa protein yang terdapat dalam struktur genom
Potyvirus*)
Protein Fungsi protein
P1 Proteinase; yang diduga berperan dalam perpindahan virus dari sel ke sel
Hc-Pro Sarana /media penularan virus dengan bantuan serangga kutu daun P3 Fungsi sebenarnya belum diketahui dengan pasti, tetapi
kemungkinannya berperan dalam replikasi virus
CI Replikasi genom
CP Selubung protein, yang berhubungan dengan penularan melalui serangga vektor, dan perpindahan virus dari sel ke sel.
NIa-VPg VPg (protein yang menempel pada ujung 5’RNA untuk permulaan sintesis RNA)
Nia-Pro Proteinase major
Nib Replikasi genom (RNA dependent RNA polymerase/RdRp)
6K1&6K2 Belum diketahui dengan pasti, kemungkinannya berhubungan dengan replikasi RNA; mengatur fungsi translokasi Nia nuclear
*
Sumber : Uncuqui-Inchima et al. (2001)
Gambar 2. 1. Organisasi genom potyvirus (Shukla et al. 1994)
Ekspresi genom Potyvirus terjadi melalui translasi poliprotein dari genom
virus. Poliprotein kemudian mengalami pemotongan dalam sitoplasma menjdi
protein fungsional dan struktural sesuai dengan gen yang disandikannya.
Pemotongan poliprotein dilakukan dengan protease yang terjadi selama dan
sesudah translasi. Protease yang memotong poliprotein juga disandikan oleh gen
yang terdapat dalam genom Potyvirus.
Poliprotein yang diekspresikan oleh genom virus diproses menjadi 10
protein fungsional oleh tiga jenis enzim proteinase yang dihasilkan oleh virus itu
sendiri (Tabel 2.1) (Hull 2002). Protein inklusi yang berbentuk silindris (CI) dan
protein selubung (CP) digunakan oleh virus untuk pergerakan dari satu sel inang
virion protein dalam jaringan vaskuler melalui interaksi dengan Hc-Pro pada
domain C- dan N- terminalnya. Selain berperan di dalam perpindahan virus pada
jaringan vaskuler, HC-Pro juga berfungsi menekan mekanisme pertahanan
tanaman menggunakan antiviral yang disebut RNA silencing (pembungkaman
RNA). Viral genome-linked protein (VPg) yang berada pada ujung 5’ genom virus
adalah protein multifungsi yang berperan pada saat amplifikasi dan pergerakan
virus. Protein ini merupakan bagian N-proximal dari protein inklusi inti (NIa) dan
terpisah secara autokalatik dari domain C-proximal proteinase (NIa-Pro). VPg
berikatan secara kovalen dengan ujung 5’ RNA virus melalui ikatan fosfodiester
pada residu asam amino tirosin yang terletak di bagian N-proximal. Keberadaan
VPg sangat diperlukan untuk proses infeksi virus. VPg juga berinteraksi dengan
faktor inisiasi translasi (eIF(iso)4E) (Schaad et al. 2000), dan diperlukan untuk
infeksi secara sistemik (Leornard et al. 2000) Dalam genom Potyvirus terdapat
daerah yang tidak berubah (conserved) dan daerah yang bervariasi. Daerah yang
conserved adalah daerah Hc-Pro dan Nib. Daerah yang bervariasi adalah P1, P3,
dan CP. Protein P3 merupakan daerah yang conserved di antara strain (Eleman et
al. 1997) .
Replikasi virus yang mempunyai genom +ssRNA terjadi melalui beberapa
tahap, yaitu 1) virus masuk ke dalam sitoplasma tanaman inang, 2) komponen
virus akan terpisah antara selubung protein dan asam nukleat, 3) RNA virus
bergabung dengan ribosom tanaman inang dan sintesis polimerase untuk replikasi
RNA, sehingga dihasil untai negatif RNA, 4) sintesis untai RNA positif dan
mRNA protein selubung menggunakan untai RNA negatif sebagai cetakannya, 5)
pembentukan subunit protein selubung dalam jumlah besar, dan 6) virion
12
selubung. Selanjutnya virus menyebar ke sel sekelilingnya melalui
plasmodesmata.
Keragaman genetik pada genus Potyvirus telah banyak dilakukan
berdasarkan gen-gen yang terlibat didalam pembentukan selubung protein dan
daerah 3’UTR. Daerah tersebut diketahui merupakan daerah yang bervariasi
diantara kelompok Potyvirus. Shukla dan Ward (1988) menggunakan runutan
asam amino selubung protein (CP) untuk menilai hubungan kekerabatan berbagai
virus dalam kelompok Potyvirus. Hasil kajian tersebut menunjukkan virus-virus
yang berbeda mempunyai kesamaan runutan asam amino CP 38% hingga 71%,
sedangkan untuk strain dari virus yang sama tingkat kesamaannya mencapai 90%
sampai 99%.Demikian pula hasil analisis runutan nukleotida 3’UTR strain-strain
Peanut stripe virus (PStV) menunjukkan bahwa strain virus tersebut mempunyai
kesamaan antara 97,9% sampai 100% (Akin 2002). Penelitian mengenai
keragaman pada tingkat molekuler berdasarkan runutan nukleotida sistron
penyandi selubung protein dan 3’ UTR dilakukan pula oleh Tsai et al. (2008) pada
ChiVMV, dimana tingkat kesamaan asam amino dan runutan nukleotida isolat
ChiVMV di Asia termasuk Indonesia masing-masing berkisar 94,8% dan 89,5%.
Hama dan Penyakit Tanaman Cabai
Selain faktor agronomis yang dapat menghambat produksi cabai,
gangguan hama dan penyakit juga menjadi masalah yang utama di dalam
budidaya tanaman cabai. Prabaningrum dan Moekasan (1996) melaporkan
berbagai hama yang dapat menyerang tanaman cabai seperti kutu daun (Myzus
persicae Sulz), Thrips (Thrips parvisipinus Karny), ulat daun (Helicoverpa
armigera Hubner), kepik (Empoasca lybica (de Bergevin dan Zanon)), lalat buah
tungau (Polyphagotarsonemus latus Banks). Direktorat Jendral Perlindungan
Tanaman Hortikultura (2009) mencatat beberapa penyakit penting pada tanaman
cabai diantaranya adalah antraknosa, bercak daun Cercospora, busuk
Phytophthora, layu Fusarium, layu bakteri dan penyakit yang disebabkan oleh
infeksi virus seperti Pepper veinal mottle virus(PMMV) , Genimivirus, Cucumber
mosaic virus (CMV). Potato virus Y (PVY), Tobacco mosaic virus (TMV).
Gejala Infeksi ChiVMV pada Tanaman Cabai
Menurut Ong (1995) virus ini pertama kali dilaporkan oleh Burnett pada
tahun 1947 pada Capsium annum di Malaysia. Selanjutnya virus ini telah
menyebabkan penyakit dibanyak negara Asia dimana cabai ditanam secara
komersial. Di Indonesia, keberadaan ChiVMV telah dilaporkan oleh Duriat et al.
(1989). Gejala yang timbul karena infeksi ChiVMV pada tanaman cabai sangat
bervariasi, tergantung pada strain virus, umur tanaman pada waktu terinfeksi, dan
lingkungan. Umumnya gejala yang ditimbulkan pada tanaman cabai sangat nyata
terlihat pada daun. Daun yang terinfeksi oleh ChiVMV menampakkan gejala
belang-belang hijau gelap, bercak-bercak hijau gelap, kadang-kadang pola-pola
tersebut menyatu ke tulang daun di dekatnya, leaf cupping, epinasti dan nekrosis
(Ong 1995; Sulyo et al. 1995; Chiemsombat dan Kittipakorn 1996).
Daun-daun yang terinfeksi secara umum menjadi kerdil dan mengalami
malformasi. Kadang-kadang buah juga dipengaruhi sehingga menjadi
belang-belang atau distorsi sehingga produksi dan kualitasnya menjadi rendah (Shah dan
14
Kisaran Inang dan Mekanisme Penularan ChiVMV
Beberapa penulis melaporkan tanaman yang dapat menjadi inang bagi
ChiVMV diantaranya adalah Nicotiana tabacum, N. benthamiana, Physalis
minima, P. floridana, C. annum, C. frutescens, N. glutinosa. Nicandra physalodes,
Solanum melongena dan S. aethiopicum (Womdim et al. 2001).
ChiVMV dapat ditularkan melalui inokulasi mekanis, penyambungan dan
serangga vektor seperti A.craccivora, A. gossypii, A. spiraecola, M. persicae,
Toxoptera citricidus, Hystreroneura setariae dan R. maydis secara non persisten,
tetapi tidak dapat ditularkan melalui biji (Ong et al. 1979). Infeksi ChiVMV pada
tanaman cabai terjadi secara sistemik pada seluruh fase pertumbuhan tanaman.
Deteksi dan Karakterisasi ChiVMV
Deteksi dan karakterisasi ChiVMV pada tanaman cabai, dapat dilakukan
dengan beberapa cara misalnya dengan pengamatan gejala, menggunakan teknik
serologi molekuler seperti Enzyme linked immunosorbent assays (ELISA) dan
Reverse Transcriptase-Polymerase chain reaction (RT-PCR) serta perunutan
nukleotida dan asam amino (Tsai et al. 2008). Deteksi melalui pengamatan gejala
terkendala adanya kemungkinan tanaman terinfeksi lebih dari satu virus atau
terinfeksi virus secara campuran. Serodiagnosis merupakan cara deteksi virus
dengan memanfaatkan reaksi antara antigen dan antibodi (Agrios 2005). Metode
ini mempunyai banyak keuntungan antara lain cepat, tepat dan dapat digunakan
untuk karakterisasi virus serta untuk mengetahui hubungan kekerabatan suatu
virus. Metode tersebut dilakukan karena gejala penyakit dari lapang
kadang-kadang meragukan sehingga sulit dilakukan identifikasi yang jelas tentang virus
Teknik serologi dengan metode ELISA untuk mendeteksi keberadaan
ChiVMV telah banyak digunakan. Hasil deteksi dengan metode tersebut
menunjukkan bahwa teknik DAS-ELISA cukup sensitif yaitu mampu mendeteksi
ChiVMV sampai pengenceran 1:1000 (Opriana, 2009).
Teknik RT-PCR digunakan untuk virus yang memiliki tipe genom RNA.
Enzim transkriptase balik (reverse trancriptase) yang digunakan dalam RT-PCR
adalah enzim DNA polimerase dan molekul RNA yang berperan sebagai cetakan
didalam mensintesis molekul DNA (cDNA) yang komplementer. RT-PCR adalah
metode yang sangat sensitif, cepat dan banyak digunakan untuk mendeteksi virus
tanaman seperti ChiVMV, Chysanthemum B carlavirus (CVB) (Tsai et al. 2008;
Ram et al. 2005 ).
Analisis perunutan nukleotida dan asam amino saat ini memiliki peranan
yang tidak kalah penting didalam melakukan deteksi dan karakterisasi virus. Dari
hasil analisis perunutan nukleotidan dan asam amino dapat diketahui tingkat
kesamaan nukleotida dan dapat menentukan kelompok suatu virus maupun
strain-strain dari virus yang sama (Shukla et al 1994). Analisis tersebut digunakan
sebagai pelengkap proses deteksi dan karakterisasi virus. Teknik yang selama ini
dilakukan adalah menggunakan inang diferensial, serologi, dan RT-PCR dimana
masing-masing metode tersebut mempunyai kelebihan dan kekurangan.
Inang diferensial atau tanaman indikator merupakan salah satu cara untuk
mengarakterisasi masing-masing isolat berdasarkan kesesuaian pada suatu inang.
Selain itu dapat juga digunakan untuk mengetahui virulensi masing-masing isolat
tersebut. Pada awal perkembangan ilmu virologi penggunaan inang diferensial
menjadi salah satu metode yang rutin digunakan untuk mendeteksi dan
16
Keunggulan masing-masing metode deteksi sangat ditentukan oleh
berbagai faktor. Identifikasi virus dengan kajian biologi memerlukan waktu yang
cukup lama karena harus mempersiapkan tanaman inang indikator, tetapi biaya
yang dikeluarkannya tidak banyak. Metode serologi dan RT-PCR adalah metode
yang lebih dapat dipercaya dan lebih sensitif sebagai metode pendeteksian virus
atau indexing, dibandingkan dengan kajian biologi, sering terjadi bahwa virus
tidak terdeteksi pada kajian biologi, tetapi menunjukkan hasil positif dengan
metode serologi dan RT-PCR yang dapat mendeteksi virus pada konsentrasi
rendah (Moury et al. 2005). Hanya saja metode ini pun masing-masing
menemukan kendala, dimana metode RT-PCR tidak dapat membedakan virus
pada kelompokan virus yang sama atau tidak dapat mengetahui variabilitas yang
terjadi diantara strain-strain virus itu sendiri.
Ketahanan Tanaman terhadap ChiVMV
Sistem pertahanan tanaman terhadap infeksi patogen secara umum terjadi
melalui satu atau beberapa cara, yaitu struktural maupun reaksi biokimia.
Ketahanan secara struktural adalah bentuk penghambatan fisik oleh tanaman yang
mengakibatkan patogen tidak dapat melakukan penetrasi dan berkembang,
sedangkan ketahanan secara biokimia, yaitu tanaman menghasilkan senyawa yang
bersifat toksik, atau menghambat pertumbuhan patogen (Agrios 2005).
Tanaman yang tahan terhadap virus adalah tanaman yang mampu
menghambat replikasi virus dan penyebaran virus di dalam tanaman (Fraser 2000).
Ketahanan ini dapat diwujudkan sebagai kemampuan tanaman untuk membatasi
perkembangan virus pada sel tertentu sehingga tidak menyebar ke sel lainnya
(Hull 2002). Respon tanaman inang terhadap infeksi suatu virus dapat
yang rentan dicirikan oleh adanya gejala yang jelas dan replikasi virus yang tinggi,
sementara respon inang yang tahan terdiri atas imun, agak tahan, toleran dan
hipersensitif. Imun dicirikan oleh tidak adanya gejala dan ketidakmampuan virus
untuk bereplikasi. Toleran dicirikan oleh adanya gejala dan replikasi virus namun
tidak mempengaruhi kehilangan hasil. Hipersensitif ditunjukkan oleh adanya
gejala khas (lesio lokal) (Fraser 2000).
Untuk mendapatkan kultivar yang tahan terhadap patogen seorang pemulia
tanaman biasanya melakukan seleksi atau skrining terhadap beberapa kultivar
yang berasal dari koleksi plasma nutfah, kultivar komersial, spesies liar sekerabat,
spesies lain dalam satu genus, atau genus lain. Hasil seleksi diperoleh genotipe
yang tahan terhadap patogen yang akan dihibridisasi dengan tetua yang
mempunyai sifat unggul lainnya seperti produksi yang tinggi. Untuk
memindahkan sifat tahan ke tetua yang mempunyai sifat produksi tinggi dapat
dilakukan metode back cross atau silang balik selama beberapa kali sehingga
diperoleh individu yang mempunyai sifat atau karakter yang tahan terhadap
patogen namun memiliki sifat tetua ulang (recurent parents) (Mangoendidjojo
2003)
Beberapa peneliti telah melaporkan bahwa sampai saat ini belum
diperoleh genotipe cabai yang tahan terhadap ChiVMV (Taufik 2005). Walaupun
demikian di Indonesia juga telah dilakukan pengujian ketahanan beberapa
genotipe cabai terhadap ChiVMV namun, terdapat genotipe cabai yang potensial
untuk digunakan di dalam program pemuliaan untuk dikembangkan menjadi
kultivar baru yang tahan. Salah satu diantaranya adalah genotipe LV 3633-R asal
Indonesia menunjukkan ketahanan terhadap semua isolat ChiVMV (Chiemsombat
18
beberapa genotipe cabai terhadap ChiVMV namun, hasil yang diperoleh masih
sedikit (Millah 2007; Latifah 2007). Oleh karena itu diperlukan teknik lain yang
memungkinkan untuk mendapatkan tanaman yang tahan terhadap penyakit, yaitu
melalui variasi somaklonal.
Pembentukan Variasi Somaklonal
Kultur in vitro atau kultur jaringan adalah suatu metode untuk mengisolasi
bagian dari tanaman seperti protoplasma, sel, sekelompok sel, jaringan, dan organ,
serta menumbuhkannya dalam kondisi aseptik (Gunawan 1988). Teknik ini
seringkali dapat menginduksi terjadinya keragaman genetik pada populasi
tanaman yang dihasilkan. Oleh karena itu, keragaman genetik yang terjadi akibat
kultur in vitro disebut keragaman somaklonal (variation somaclonal) (Larkin dan
Scowcroft 1981). Saat ini banyak penelitian yang menekankan pentingnya variasi
somaklonal untuk perbaikan tanaman hortikultura. Variasi yang muncul selama
proses kultur in vitro disebut variasi somaklonal dan merupakan variasi yang
umum terjadi antar tanaman yang berasal dari kultur jaringan atau kultur sel.
Menurut Ahloowalia (2001), variasi somaklonal yang terjadi dapat mengakibatkan
perubahan. Perubahan tersebut diantaranya adalah defisiensi klorofil, aneuploidi,
resistensi terhadap penyakit atau kadang-kadang muncul variasi yang sebelumnya
tidak pernah ada di alam. Variasi dapat juga terjadi pada sifat seperti tinggi
tanaman, luas daun, panjang daun, ketebalan batang, vigor, pembungaan, fertilitas
dan hasil.
Variasi somaklonal akan berguna jika: (1) menambah komponen varian
dengan variasi yang tidak terdapat di alam, (2) mengubah satu atau beberapa sifat
dari kultivar yang sudah ada sehingga menjadi lebih baik terutama pada tanaman
somaklonal akan dibatasi penggunaannya jika perubahan yang terjadi terlalu jauh
dari harapan atau terlalu drastis dan mengubah banyak gen.
Untuk menghasilkan tanaman somaklonal dengan suatu karakter baru
maka perlu diketahui faktor-faktor kritis yang mempengaruhi variasi somaklonal.
Faktor-faktor tersebut adalah (1) genotipe, (2) lingkungan kultur (zat pengatur
tumbuh), (3) sumber eksplan, dan (4) lama fase kalus dan lama durasi kultur
(Arous et al. 2001). Genotipe merupakan faktor penting di dalam menimbulkan
variasi somaklonal, karena genotipe dapat mempengaruhi frekuensi regenerasi dan
frekuensi variasi somaklonal yang terjadi. Christopher dan Rajam (1999) mencatat
frekuensi keragaman genotipe yang tinggi terjadi pada beberapa kultivar cabai
Capsicum praetermissum, C. baccatum dan C. annuum cvs. G4.
Menurut Fratini dan Ruiz (2002) banyak bukti menunjukkan variasi
somaklonal dipengaruhi oleh pemilihan zat pengatur tumbuh terutama
berhubungan dengan jumlah konsentrasi yang ditambahkan dalam media. Zat
pengatur tumbuh sitokinin sering digunakan dalam perbanyakan in vitro untuk
mendapatkan multiplikasi yang tinggi. Sitokinin terbagi dua kelompok yaitu
sitokinin alami dan sintetis. Sitokinin alami (endogen) adalah zeatin dan sitokinin
sintetis adalah N6-Benzyl amino purine (BAP) dan Furfuryl acetic acid (kinetin).
Berdasarkan struktur kimia, sitokinin adalah turunan adenine (BAP, kinetin,
zeatin) dan turunan fenilurea (TDZ). TDZ dan BAP mempunyai respon fisiologi
yang sama, yaitu berperan dalam regulasi pembelahan sel, diferensiasi dan
pertumbuhan jaringan, organ serta biosintesis klorofil (Gaba 2005). Keefektifan
BAP dan TDZ dalam menginduksi multiplikasi tunas berbeda-beda bergantung
pada jenis tanamannya. Pada tanaman cabai konsentrasi optimal BAP dan TDZ
20
pada tanaman Coffea arabica L. dan C. canephora perlakuan 7 mg/l BAP
menghasilkan jumlah tunas per eksplan hampir sama dengan perlakuan 2 mg/l
TDZ tetapi persentase eksplan membentuk tunas pada perlakuan TDZ lebih tinggi
dibandingkan perlakuan BAP (Giridhar et al. 2004). Selain keduanya, zat
pengatur tumbuh 2,4 D adalah termasuk zat pengatur tumbuh yang sering kali
mengakibatkan variabilitas kromosom. Konsentrasi 2,4 D yang berpengaruh
terhadap peningkatan variabilitas pada tanaman horseradish (Amoracia rusticana
L.) adalah 0,1 µM yang dikombinasikan dengan 0, 0,1, dan 1,0 µM BA. Bila
konsentrasi 2,4D lebih dari 0,1 µM kalus tidak beregenerasi (Yuliadi 2008).
Dalam perbanyakan in vitro, sesungguhnya hampir selalu diperoleh planlet
yang di luar tipe yang biasanya dibuang. Setelah penelitian mengenai variasi
somaklonal dimulai dan dirasakan manfaatnya dalam pemuliaan tanaman maka
justru yang di luar tipe ini yang menjadi perhatian. Setiap spesies berbeda jenis
dan frekuensi variasinya dan setiap kultivar atau genotipe pada spesies yang
samapun berbeda variasi somaklonnya. Mekanisme terjadinya keragaman
somaklonal diantaranya disebabkan oleh perubahan genetik spesifik, misalnya
mutasi titik (single nucleotide changes), perubahan jumlah kopi gen tertentu,
aktivasi transposable elemen, perubahan jumlah kromosom, chromosomal
rearrangements, dan metilasi DNA. Metilasi diketahui meningkatkan frekuensi
mutasi CG ke AT (Keappler dan Philip 1993).
Penggunaan keragaman somaklonal memiliki kelemahan. Keragaman
yang ditimbulkan tidak dapat diprediksi di alam. Dengan menggunakan kultur
jaringan mungkin keragaman variasi genetik atau epigenetik dapat diinduksi,
namun terjadinya keragaman epigenetik lebih banyak terjadi dari pada keragaman
Penyebab Variasi Somaklonal
Penyebab munculnya variasi somaklonal ada dua yaitu variasi genetik
yang memang sudah ada dalam eksplan dan variasi induksi atau variasi epigenetik
yang muncul selama fase kultur in vitro. Variasi genetik bersifat stabil baik
melalui perbanyakan seksual dan aseksual, sedangkan variasi epigenetik tidak
stabil dan berpotensi dapat balik (reversible) (Keappler et al. 2000). Timbulnya
keragaman genetik selama proses in vitro dipengaruhi oleh faktor internal maupun
ekstenal. Faktor internal yang dapat mempengaruhi frekuensi munculnya variasi
somaklonal dalam kultur in vitro adalah genotipe tanaman induk, sumber eksplan
yang digunakan, umur jaringan dan tingkat ploidi, sedangkan faktor eksternal
adalah konsentrasi berbagai komponen media pertumbuhan, jumlah subkultur, dan
konsentrasi zat pengatur tumbuh serta proses regenerasinya (Nwauzoma et al.
2002; Jayasankar 2005). Mutasi gen merupakan mutasi yang paling diharapkan
terjadi dalam pemuliaan yang menggunakan variasi somaklonal, karena mutasi
gen hanya akan merubah sifat tertentu yang dikendalikan gen tersebut. Menurut
Arnim (2005) mutasi gen bisa terjadi di tingkat DNA (perubahan satu basa), di
tingkat protein (perubahan kode triplet untuk asam amino), atau dapat terjadi
mutasi ke arah liarnya dan bahkan dapat terjadi mutasi balik.
Mutasi Secara Fisik dan Kimia
Pada saat ini teknik in vitro dan mutagenesis merupakan metode yang
paling banyak digunakan untuk meningkatkan keragaman pada tanaman. Teknik
mutasi yang dikombinasikan dengan kultur in vitro dan metode molekuler akan
menyediakan metode yang kuat untuk meningkatkan keragaman somaklonal
(Ahloowalia et al. 2004). Mutagenesis adalah keseluruhan proses yang
22
diinduksi dengan agen penginduksi mutasi (mutagen). Mutasi buatan
dimaksudkan untuk mendapatkan keragaman genetik yang tercermin dari
mutan-mutan yang dihasilkan. Selanjutnya mutan-mutan-mutan-mutan yang memiliki karakter yang
dikehendaki diseleksi secara langsung dan diperbanyak secara vegetatif atau
mutan tersebut diserbuk sendiri untuk menstabilkan karakter mutan tersebut
(Poehlman 1996).
Mutasi buatan merupakan mutasi yang sengaja dilakukan sebagai salah
satu cara untuk menimbulkan keragaman genetik. Mutasi buatan ini biasanya
diinduksi secara fisik, kimia dan biologi. Berbagai unsur fisik seperti suhu, cahaya
dengan gelombang tertentu (sinar x, y) dapat mengakibatkan mutasi. Bahan
kimiawi yang mengandung senyawa yang bersifat mutagen diantaranya etil metan
sulfonat (EMS), dietil sulfat (dES), nitroso etil urea (ENH), nitroso metil urea
(MNH), dan etilenamin (EI) (Van Harten 1998).
Kelebihan penggunaan agen mutagenik kimia adalah (1) sebagian besar
mutasi yang terjadi merupakan mutasi titik; (2) kerusakan kromosom lebih kecil,
dan (3) mutasi terjadi dengan frekuensi tinggi. Kelemahannya adalah (1) penetrasi
jaringan multisel seringkali sulit, (2) reproduksibilitas rendah, dan (3) agen
mutagenik kimia sangat berbahaya karena bersifat karsinogenik (Van Harten
1998).
Perlakuan dengan mutagen fisik dapat menimbulkan pengaruh pada
generasi pertama yaitu (1) kerusakan dan menyebabkan kematian jaringan (letal),
(2) steril, (3) khimera. Kerusakan yang diakibatkan radiasi ini diantaranya
kerusakan fisiologis, kerusakan kromosom (mutasi kromosom), kerusakan
sitoplasma (mutasi sitoplasma). Menurut Ahloowalia et al. (2004) dan Hussien et
sehingga dapat merubah struktur kromosom (delesi, inversi, duplikasi dan
translokasi). Radiasi juga dapat merusak benang-benang spindel yang berfungsi
menarik kromosom ke kutub-kutubnya pada fase metafase dalam proses mitosis
sehingga akan merubah jumlah kromosom dan dapat menyebabkan euploidi dan
aneuploidi.
Ethyl methane sulfonate (EMS) termasuk senyawa alkil yang mempunyai
potensi tinggi sebagai mutagen yang efisien untuk tanaman. Penggunaan EMS ini
lebih sering dilakukan karena mudah didapat, harganya murah dan tidak toksik
bagi jaringan tanaman yang di beri perlakuan EMS(Van Harten 1998; Nasir 2002).
EMS (CH3SO2OC2H5) adalah suatu alcylating agent. Gugus alkil bereaksi dengan
DNA dengan cara mengalkilasi gugus fosfat dan basa purin serta basa pirimidin
yang seringkali terjadi jika reaksi melibatkan basa nitrogen pada DNA. Alcylating
agent seperti EMS sangat reaktif dan dapat bereaksi dengan air. Oleh karena itu
larutan EMS harus selalu dibuat segar, artinya begitu dibuat langsung digunakan,
tidak boleh disimpan. Reaksi dengan air merupakan suatu reaksi hidrolisis yang
mengakibatkan EMS tidak lagi bersifat mutagenik. Konsentrasi EMS yang
dibutuhkan untuk setiap tanaman berbeda-beda tergantung dari tanaman dan jenis
eksplan yang digunakan. Pada tanaman cabai, krisan, ubijalar, anggur, dan
kacang-kacangan konsentrasi EMS yang dapat digunakan berturut turut adalah
0,5%, 0,77% , 0,04% dan 0,25-0,5% (Jabeen dan Mirza 2004; Luan et al. 2007;
Singh et al 2007; Svetleva dan Crino 2005). Tanaman yang diperlakukan EMS
akan mempelihatkan defisiensi klorofil dan variasi genetik umumnya lebih tinggi
24
Variasi Somaklonal untuk mendapatkan Resistensi terhadap Penyakit
Pada saat ini teknik in vitro dan mutagenesis merupakan metode yang
paling banyak digunakan untuk meningkatkan keragaman pada tanaman. Induksi
mutasi merupakan suatu cara untuk memperoleh mutan-mutan yang diharapkan
membawa sifat yang menguntungkan tanaman, dan telah banyak dilakukan oleh
beberapa peneliti. Pada banyak tanaman yang diperbanyak secara vegetatif
induksi mutasi yang dikombinasikan dengan teknik kultur in vitro merupakan
salah satu metode yang efektif untuk meningkatkan hasil tanaman, namun
hambatan yang sering dijumpai pada tanaman berbiak vegetatif adalah timbulnya
kimera setelah perlakuan mutagen fisik maupun kimia (Linberger 2007).
Pemanfaatan fenomena variasi somaklonal dalam pemuliaan mula-mula
dilakukan dengan mendorong terjadinya varian atau keragaman somaklonal.
Selanjutnya dilakukan seleksi terhadap somaklonal yang memiliki sifat-sifat
tertentu. Keragaman somaklonal dapat diinduksi secara terarah dengan
menggunakan suatu media/agen seleksi dalam media kultur atau dengan
memberikan kondisi tertentu agar dihasilkan somaklonal-somaklonal yang
mempunyai sifat-sifat yang diinginkan. Untuk mendapatkan tanaman yang tahan
terhadap penyakit yang disebabkan oleh cendawan misalnya, dapat dilakukan
seleksi pada tahapan kultur in vitro dengan menambahkan fusaric acid yang
merupakan toksin utama yang dihasilkan oleh Fusarium ke dalam media kultur in
vitro. Teknik seleksi pada tanaman kultur in vitro dapat pula dilakukan terhadap
patogen lainnya, seperti bakteri dan virus (Hwang and Ko 2004; Snikder et al.
2004; Imelda et al. 2000 ). Akan tetapi, untuk mendapatkan tanaman yang tahan
terhadap penyakit yang disebabkan oleh virus, seleksi dilakukan pada saat
Agar efektif, seleksi untuk mendapatkan tanaman yang tahan terhadap
penyakit harus memenuhi tiga syarat. Pertama, kultur in vitro menghasilkan
keragaman yang tinggi. Kedua, metode seleksi terhadap somaklon dengan
sifat-sifat yang diinginkan harus dapat dilakukan dengan mudah. Ketiga, perubahan
yang terjadi adalah perubahan genetik yang dapat diturunkan pada zuriatnya dan
tetap stabil pada waktu tanaman diperbanyak baik secara seksual maupun aseksual
(Ahlowalia dan Maluszynski 2001).
Pemanfaatan dan Penerapan Variasi Somaklonal
Variasi somaklonal dapat memberikan kontribusi yang nyata pada
pemuliaan tanaman. Walaupun variasi tidak mempengaruhi semua sifat dan tidak
selalu menguntungkan di dalam pertanian, tetapi dengan seleksi kemungkinan
dapat diperoleh genotipe-genotipe yang berguna dari sumber variasi tersebut.
Beberapa contoh pemanfaatan variasi somaklonal adalah peningkatan ketahanan
terhadap herbisida klorosulfuran pada tanaman jagung, ketahanan terhadap
Erwinia carotovora pv. carotovora pada Zantesdechia spp. (Araceae), toleransi
terhadap garam pada ubijalar serta tanaman kedelai toleran aluminium (Hughes
1983; Snijder et al. 2004; Luan et al. 2007; Mariska et al. 2004).
Contoh lain pemanfaatan variasi somaklonal adalah untuk membentuk
tanaman genotipe unggul baru pada pisang di Indonesia yang sulit dilakukan
karena tingkat ploidi yang tinggi dan steril. Tanaman pisang yang diberi perlakuan
radiasi dengan sinar gamma 1000 rad dapat menginduksi sifat ketahanan terhadap
penyakit layu Fusarium (Panama disease) yang disebabkan oleh Fusarium
oxysporum Schlect f.sp. cubesense (Smith et al. 2006, Mariska et al. 2006)
Pada C. annuum (cabai), mutan pertama diperoleh tahun 1972 melalui
26
selama 3 jam. Perlakuan tersebut dapat meningkatkan kandungan vitamin C, umur
genjah dan menginduksi perubahan morfologi (Daskalov 1991; Daskalov 2001;
Jabeen dan Mirza 2004).
Perlakuan irradiasi pada Glycine max L (kedelai) menggunakan sinar
gamma dan UV, yang dikombinasikan dengan mutagen kimia (EMS, DES, NMH,
DMS) menghasilkan mutan yang berproduksi tinggi, tahan virus, toleran
aluminium dan kekeringan, protein tinggi, genjah, kadar minyak meningkat dan
toleran lahan masam (Bhatnagar dan Tiwari 1991, Mariska et al 2004).
DAFTAR PUSTAKA
Agrios GN. 2005. Plant Pathology. Ed ke-5. New York: Elsevier Academic
Press.
Ahlowalia BS, M. Maluszynski 2001. Induced mutation A new paradigma in plant
breeding. Euphytica 118:167-173.
Ahlowalia BS, Maluszynski M, Nichterlein K. 2004. Global impact og
mutation-derived. Review. Euphytica 135:187-204.
Akin MH. 2002. Variabilitas strain-strain PStV pada tingkat moleku berdasarkan
gen protein selubung dan 3’UTR (Untranslated region) genom RNS PStV.
J.Perlin. Tan. Ind. 8:86-93
Arnim AG (2005). Molecular Approches to the Study og Plant Development. Di
dalam Trigiano RN, Gray JD, editor. Plant Developmen and Biotechnology.
CRC. Press. New York. P. 119-129
Arous S, Boussaid M, Marrakchi M. 2001. Plant regeneration from zygotic
embryo hypocotyls of Tunisian chili (Capsicum annuum L.) J. Appl. Hort.
3(1): 17-22.
Bhatnagar PS, Tiwari SP. 1991. Soybean improvement through mutation breeding
in India Vol. 1 IAEA : 381-391
Chiemsombat P, Kittipakorn K. 1996a. Determination of isolates of CMV dan
CVMV and screening of pepper cultivars for virus resistance. Proceeding of
Christopher T, Rajam MV. 1999. Effect of genotype, explants and medium on in
vitro regeneration of red pepper. Plant Cell, Tissue and Organ Culture
46:245-250
Clark MF, Adams AN. 1977. Characteristics of the microplate methode of
enzyme-linked immunosorbent assay for the detection of plant viruses. J.
Gen. Virol. 34:475-483
Daskalov S. 1991. Experimental mutagenesis an