MENGGUNAKAN PAPAIN UNTUK MENGHASILKAN PEPTON
WARDANA
F351020311
PROGRAM STUDI TEKNOLOGI INDUSTRI PERTANIAN
SEKOLAH PASCASARJANA
▸ Baca selengkapnya: struktur cerita keong mas
(2)Dengan ini saya menyatakan bahwa tesis Hidrolisis Protein Keong Mas (Pomacea canaliculata Lamarck) Menggunakan Papain untuk Menghasilkan Pepton adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Februari 2008
Wardana
Wardana. Hydrolysis of Apple Snail (Pomacea canaliculata Lamarck) Protein Using Papain to produce Peptone. Under direction of MUHAMMAD ROMLI, ANI SURYANI, and LIEBESTINI HARTOTO.
Apple snail (Pomacea canaliculata Lamarck) is one of agricultural plant pest that can be used as a protein source in food and feed. The protein content of apple snail flesh is about 12.2%, so it can be considered as a raw material to make peptone using papain for nitrogen source in media for microbial growth.
The purpose of this research is to obtain the best papain concentration, pH and temperature, and also to know the effect of Apple snail peptone on microbial growth.
This research was divided into three steps, firstly was collection apple snail from rice field area, secondly was making of snail powder by taking apple snail flesh from shell after boiling for 20 minutes. Before powdering, it was dried in oven at 80 C for 24 hours. The last was making apple snail peptone powder from apple snail powder by papain to hydrolyzed. To remove its fat content, it was put in refrigerator at ± 4 C for 24 hours.
Chemical analyses of apple snail powder was done to determine its protein content, includes pH and protein hydrolysis degree, and for peptone include nitrogen total and composition by HPLC. Apple snail peptone was analyzed to know its ability become nitrogen source in microbial growth, includes specific growth rate and biomass production. Micro organisms used in this case were
Escherichia coli, Staphylococcus aureus, Saccharomyces cerevisiae and
Aspergillus niger. To evaluate apple snail peptone quality on microbial growth, Difco and Oxoid peptone were used as comparators. Beside that, yield calculation and production cost were done.
The result showed that nitrogen total of apple snail peptone was 46.20 %, by using papain proteolysis activities of 59.45 Unit/mg, papain concentration of 0.2%, pH of 5.5 and temperature of 65 C for 8 hours. Apple snail peptone gave a best growth rate compare to Difco and Oxoid peptone for growing A. niger and S. cerevisiae. That was caused by the existence of higher carbohydrate in apple snail peptone compared to others and also because of enzyme of fungus group more able decompose apple snail peptone compound to be more used compare to other peptone. The bacterial microbes group, i.e. Escherichia coli and Staphylococcus aurues, apple snail peptone gave lower growth rate compare Difco and Oxoid peptone. Yield of making apple snail peptone was 10.2%, while production cost was 81,500.- /kg, cheaper than Difco and Oxoid peptone price (Rp 1,900,000.- /kg and Rp 2,600,000.-).
Wardana. Hidrolisis Protein Keong Mas (Pomacea canaliculata Lamarck) Menggunakan Papain Untuk Menghasilkan Pepton. Dibimbing oleh MUHAMMAD ROMLI, ANI SURYANI dan LIESBETINI HARTOTO.
Keong mas (Pomacea canaliculata Lamarck) adalah salah satu hama tanaman padi yang dapat digunakan sebagai sumber protein bagi bahan pangan dan pakan ternak. Kandungan protein daging keong mas kurang lebih 12,2%, sehingga dapat dipertimbangkan sebagai bahan baku pembuatan pepton yang merupakan sumber nitrogen utama dalam media mikrobiologi untuk pertumbuhan bakteri. Tujuan penelitian ini adalah mendapatkan konsentrasi papain, suhu dan pH terbaik serta mengetahui pengaruh pepton keong mas pada pertumbuhan mikroba.
Penelitian ini dibagi atas tiga tahap, tahap pertama yaitu pengumpulan keong mas dari daerah persawahan, tahap kedua yaitu pembuatan tepung keong dengan cara pengambilan daging keong mas dari dalam cangkangnya setelah direbus selama 20 menit. Sebelum dijadikan tepung, daging keong mas dikeringkan di dalam oven pada suhu 80 0C selama 24 jam. Tahap terakhir yaitu pembuatan pepton keong mas dari tepung keong mas dengan menggunakan papain untuk menghidrolisisnya. Untuk menghilangkan lemaknya, disimpan di tempat dingin pada suhu ±4 C selama 24 jam.
Analisis kimia pada tepung keong mas dilakukan untuk menentukan kandungan protein sebelum hidrolisis terhadap tepung keong mas dilakukan, analisis tepung keong mas meliputi pH dan derajat hidrolisis protein, sedangkan untuk pepton meliputi total nitrogen dan kandungannya dengan menggunakan HPLC. Pepton keong mas dianalisis untuk mengetahui kemampuannya menjadi sumber nitrogen bagi pertumbuhan mikroba, termasuk tingkat pertumbuhan spesifik dan produksi biomassa. Mikroorganisme yang digunakan adalah
Escherichia coli, Staphylococcus aureus, Saccharomyces cerevisiae dan
Aspergillus niger. Untuk mengevaluasi kualitas pepton keong mas pada pertumbuhan mikroba, pepton Difco dan Oxoid digunakan sebagai pembanding. Selain itu, perhitungan rendemen dan biaya produksi pepmbuatan pepton keong mas juga dilakukan.
Penelitian ini menunjukkan hasil bahwa total nitrogen pepton keong mas 46,20% dengan menggunakan papain beraktivitas proteolitik sebesar 59,45 Unit/mg, konsentrasi papain 0,2%, pH 5,5 dan suhu 65 C selama 8 jam. Pepton keong mas memberikan laju pertumbuhan yang terbaik dibandingkan pepton Oxoid dan Difco untuk pertumbuhan mikroba golongan A. niger dan S. cerevisiae, sedangkan untuk mikroba golongan bakteri, yaitu Escherichia coli dan
Stephalococcus aurues, pepton keong mas memberikan hasil laju pertumbuhan di bawah pepton Oxoid dan Difco. Rendemen pembuatan pepton keong mas adalah sebesar 10,2% memiliki biaya produksi sebesar 81.500,- /kg, lebih murah dibandingkan harga pepton Difco dan Oxoid (Rp 1.900.000,- /kg dan Rp 2.600.000,- /kg).
@Hak cipta milik Insitut Pertanian Bogor, Tahun 2008
Hak cipta dilindungi Undang-undang
1.
Dilarang mengutip sebagian atau seluruh karya ini tanpa
mencantumkan atau menyebutkan sumber
a.
Pengutipan hanya untuk kepentingan pendidikan, penelitian,
penulisan karya ilmiah, penyusunan laporan, kritik atau
tinjauan suatu masalah
b.
Pengutipan tidak merugikan kepentingan yang wajar Institut
Pertanian Bogor
PEPTON
WARDANA
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Departemen Teknologi Industri Pertanian
PROGRAM STUDI TEKNOLOGI INDUSTRI PERTANIAN
SEKOLAH PASCASARJANA
NIM : F351020311
Disetujui Komisi Pembimbing
Dr. Ir. Muhammad Romli, MSc.St Ketua
Dr. Ir. Ani Suryani, DEA Anggota
Dr. Ir. Liesbetini Hartoto, MS Anggota
Diketahui
Ketua Program Studi Teknologi Industri Pertanian
Dekan Sekolah Pascasarjana
Dr. Ir. Irawadi Jumaran Dr. Ir. Naresworo Nugroho, MSi
Puji syukur penulis panjatkan kehadirat Allah Subhanahu Wata’ala karena hanya dengan berkat dan rahmat-Nya jualah penulis dapat menyelesaikan penelitian ini, sebagai salah satu syarat untuk memperoleh gelar Magister Sains di Program Pascasarjana Institut Pertanian Bogor. Topik yang dipilih dalam penelitian ini adalah pemanfaatan daging keong mas sebagai bahan baku pembuatan pepton yang merupakan sumber nitrogen bagi mikroorganisme, dengan judul : Hidrolisis Protein Keong Mas (Pomacea canaliculata Lamarck) Menggunakan Papain Untuk Menghasilkan Pepton.
Penulis mengucapkan banyak terima kasih kepada Bapak Dr. Ir. Muhammad Romli, MScSt selaku Ketua Komisi Pembimbing, Ibu Dr. Ir. Ani Suryani, DEA, dan Ibu Dr. Ir. Liesbetini Hartoto, MS selaku anggota komisi pembimbing yang telah banyak memberikan bimbingan, dorongan, masukan, dan saran hingga selesainya tesis ini. Kepada semua pihak yang telah banyak membantu penulis ucapkan terima kasih, semoga Tuhan Yang Maha Esa membalasnya.
Ucapan terima kasih penulis sampaikan kepada Rektor IPB, Dekan Sekolah Pascasarjana IPB, Dekan Fakultas Teknologi Pertanian IPB. Ketua Departemen Teknologi Industri Pertanian IPB dan Ketua Program Studi Teknologi Industri Pertanian Sekolah Pascasarjana IPB atas segala bantuan dan pelayanannya. Ucapan terima kasih penulis sampaikan kepada seluruh staf Pengajar Program Studi Teknologi Industri Pertanian IPB yang telah memberikan curahan waktu, ilmu dan pengalamannya selama penulis menempuh pendidikan di IPB.
Rasa hormat dan terima kasih yang sangat dalam penulis haturkan kepada Ayahanda Rifani Joenani dan Ibunda Mastiah, Tante Rusnilayati dan Om Saiful Bahrie, Ayah mertua La AA dan Ibu mertua La Ira serta adik semuanya yang telah memberikan doa restu, dorongan, semangat, dan motivasi. Penghargaan dan kebanggaan dengan segala ketulusan disampaikan kepada istri tercinta Muzuna, Sp.MSi yang sabar dan penuh pengertian, anak-anakku tercinta Raihan Anugrah Wardana dan Nazela Dwi Ramadhani atas segala pengorbanan, pengertian, ketulusan, ketabahan dan dorongan semangat yang telah diberikan selama penulis menempuh pendidikan.
Ucapan terima kasih juga penulis sampaikan kepada teman-teman perwira 6 (Pak Yazid, Banun, Asniah, IIk, Pak Toto, Pak Cahyo, Yuli, Nirwan, Bubun, Sumarno, Ilham, Pak Wagiman, Ida, Wiwin, dan teman-teman) atas dukungan dan rasa kebersamaannya. Dan juga kepada pihak-pihak lain yang telah membantu penulis selama mengikuti pendidikan sampai selesainya tesis ini, yang tidak dapat disebutkan satu per satu, disampaikan terima kasih.
Penulis menyadari banyak kekurangan yang terdapat dalam tulisan ini, karena itu kritik dan saran penulis sangat harapkan. Akhir kata semoga tulisan ini bermanfaat bagi pengembangan teknologi industri pertanian.
Bogor, Februari 2008
1976 sebagai anak pertama dari Ibu Mastiah (Alm) dan Ayah Rifani Joenani. Penulis menyelesaikan pendidikan SD pada tahun 1990 di SDN Kota I Banjarbaru, SMP pada tahun 1993 di SLTPN I Banjarbaru dan SMA pada tahun 1996 di SMUN Banjarbaru.
Tahun 2001 penulis memperoleh gelar sarjana Kehutanan Jurusan Teknologi Hasil Hutan, Fakultas Kehutanan, Universitas Lambung Mangkurat, Kalimantan Selatan. Tahun 2002 penulis mengikuti pendidikan Magister Sains Program Studi Teknologi Industri Pertanian, Sekolah Pascasarjana, Institut Pertanian Bogor.
DAFTAR TABEL ... iii
Saccharomyces cerevisiae ... 14
Fase-fase Pertumbuhan Mikroorganisme... 14
III. BAHAN DAN METODE ... 17
Pengaruh Konsentrasi Papain ... 29
Pengaruh pH ... 30
Pengaruh Suhu ... 31
Derajat Hidrolisis ... 32
Uji Penggunaan Pepton Keong ... 34
Perhitungan Neraca Massa ... 44
V. KESIMPULAN DAN SARAN ... 46
Kesimpulan... 46
Saran ... 46 DAFTAR PUSTAKA
1 Kandungan Gizi dari 100 gram Daging Keong Mas... 5 2 Komposisi Media Tumbuh Mikroorganisme Berdasarkan
1 Keong Mas (Pomacea canaliculata Lamarck) ... 4
2 Diagram Alir Pembuatan Pepton Kepala Ikan Tuna (siswanto, 2000) 8
3 Diagram Alir Pembuatan Tepung Keong (Bagus, 1999) ... 20
4 Diagram Alir Pembuatan Pepton Keong dari Tepung Keong (Modifikasi Penelitian Siswanto, 2000) ... 23
5 Pengaruh Konsentrasi Papain terhadap Kadar Protein Hidrolisat ... 29
6 Pengaruh pH terhadap Konsentrasi Protein Hidrolisat ... 30
7 Pengaruh Suhu terhadap Konsentrasi Protein Hidrolisat ... 31
8 Derajat Hidrolisis dari Perlakuan Konsentrasi Papain 0,2% ... 32
9 Grafik Hasil Analisa HPLC Asam Amino terhadap Pepton Keong, Oxoid dan Difco ... 33
10 Hasil Pengamatan Pemakaian Nitrogen oleh Eschercia coli pada Pepton Keong, Oxoid dan Difco ... 34
11 Hasil Pengamatan Pertumbuhan Eschercia coli pada Pepton Keong, Oxoid dan Difco ... 35
12 Hasil Perhitungan Laju Pertumbuhan Eschercia coli ... 35
13 Hasil Pengamatan Pemakaian Nitrogen oleh S. aureus pada Pepton Keong, Oxoid dan Difco ... 36
14 Hasil Pengamatan Pertumbuhan S. aureus pada Pepton Keong, Oxoid dan Difco ... 37
15 Hasil Perhitungan Laju Pertumbuhan Stephalococcus aureus ... 38
16 Hasil Pengamatan Pemakaian Nitrogen oleh Aspergillus niger pada Pepton Keong, Oxoid dan Difco ... 39
17 Hasil Pengamatan Pertumbuhan Aspergillus niger pada Pepton Keong, Oxoid dan Difco ... 39
18 Hasil Perhitungan Laju Pertumbuhan Aspergillus niger ... 40
1 Penentuan Aktivitas Enzim Papain (Bergmeyer, 1983) ... 50
2 Jumlah Nitrogen Total Metode Kjeldahl (AOAC, 1999) ... 52
3 Analisa Hasil Pengambilan Sampel pada Tahap Hidrolisis Tepung Keong Mas ... 53
4 Prosedur Analisa Asam Amino Menggunakan HPLC ... 54
5 Pengaruh Konsentrasi Papain terhadap Kadar Protein Hidrolisat ... 56
6 Pengaruh pH terhadap Kadar Protein Hidrolisat ... 57
7 Pengaruh Suhu terhadap Kadar Protein Hidrolisat ... 58
8 Nilai Derajat Hidrolisis ... 59
9 Hasil Analisa HPLC Asam Amino terhadap Pepton Keong, Difco dan Oxoid ... 60
10 Hasil Perhitungan Laju Pertumbuhan Eschercia coli ... 61
11 Hasil Perhitungan Laju Pertumbuhan Staphalococcus aureus ... 62
12 Hasil Perhitungan Laju Pertumbuhan Aspergillus niger ... 63
Latar Belakang
Keong mas atau keong murbai (Pomacea canaliculata Lamarck) termasuk keong air tawar, dengan cangkang berbentuk bulat mengerucut berwarna kuning keemasan. Keong ini berasal dari daerah Amazon, Amerika Selatan dan diperkirakan masuk ke Indonesia melalui perdagangan ikan hias sekitar tahun 1984. Keong mas saat ini banyak dijumpai dan sebagian besar belum dapat dimanfaatkan disebabkan perkembangan pupulasinya yang cepat (Sihombing. 1999).
Beberapa negara di dunia seperti Amerika, Cina, Taiwan, Jepang dan Korea, termasuk Indonesia telah memanfaatkan keong sebagai makanan yang banyak digemari karena memiliki kandungan protein yang tinggi dan rasanya yang lezat, selain itu keong mas dapat juga digunakan sebagai pakan ternak seperti ikan, bebek, ayam dan ternak lainnya. (Sihombing, 1999). Menurut Siswanto (1999), keong mas merupakan sumber protein yang sangat potensial karena dagingnya mengandung 12,2% protein. Kandungan protein keong mas lebih tinggi bila dijadikan tepung dibandingkan tepung ikan, yaitu sekitar 50,74% (Siswanto, 1999), sedangkan tepung ikan hanya sekitar 30% (Soegeng, 2003).
Kandungan protein keong dapat dipertimbangkan sebagai sumberdaya yang berharga. Salah satu pemanfaatannya adalah dapat dijadikan sebagai bahan baku pepton. Pepton merupakan sumber nitrogen utama dalam media mikrobiologi untuk pertumbuhan mikroorganisme.
rekayasa genetika mikroorganisme. Harga pepton komersial di Indonesia sangat mahal karena masih harus diimpor dari luar negeri. Menurut Biro Pusat Statistik (1999) dari Januari hingga Desember impor pepton dan turunannya sebesar 59.868.979 kg dengan nilai sebesar US $ 38.800.155 atau rata-rata seharga US $ 0,65 / kg, sedangkan pada tahun 2001 dari bulan Januari hingga Juni harga pepton meningkat, yaitu seharga US $ 3,08 /kg. (BPS, 2001). Dan pada tahun 2006, impor pepton dan turunannya sebesar 45.22.814 kg dengan nilai harga sebesar US $ 10.464.637 atau rata-rata seharga US $ 2,31 /kg. Setelah masuk ke distributur dan diolah serta dikemas maka pepton Oxoid dijual sebesar Rp 2.600.000,- per kilogram dan pepton Difco dijual sebesar dan Rp 1.900.000,- per kilogram (tahun 2008). Pepton adalah produk campuran polipeptida, dipeptida, dan asam amino yang dapat dihasilkan dari bahan-bahan yang mengandung protein melalui reaksi hidrolisis asam atau enzimatis. Enzim protease yang sering digunakan untuk menghidrolisis protein adalah papain. Papain merupakan enzim proteolitik yang dihasilkan dari getah pepaya, yang berasal dari hampir seluruh bagian dari pohon pepaya kecuali akar dan biji. Menurut Suhartono (1992) papain merupakan salah satu enzim yang dapat mengkatalisis reaksi hidrolisis substrat protein.
Keong mas banyak memberikan manfaat karena dagingnya mempunyai kandungan protein yang tinggi, namun keong mas ini juga menimbulkan kekhawatiran terutama kepada petani padi karena dapat merusak tanaman padi yang berakibat menurunkan produksi panen. Pada awal tahun 90-an, keong mas telah menjadi hama yang menyebabkan kerusakan ribuan hektar tanaman padi.
mempunyai kandungan protein yang cukup tinggi guna menghasilkan bahan baku pembuatan pepton. Penggunaan daging keong mas sebagai bahan baku pepton saat ini belum diteliti, mengingat keperluan pepton di Indonesia terus meningkat seiring dengan peningkatan penggunaan mikroorganisme di bidang bioteknologi.
Penelitian ini mengkaji proses pembuatan pepton keong mas hasil proses hidrolisis dengan menggunakan papain untuk mendapatkan pepton yang bermutu, yaitu sanggup memenuhi kebutuhan mikroorganisme (bakteri, khamir dan kapang) terhadap sumber nitrogen dalam media tumbuh mikroorganisme dan bersifat ekonomis, yaitu mempunyai harga produksi yang lebih murah daripada pepon komersial yang telah ada sebelumnya, sehingga pepton keong mas dapat dijadikan sebagai pepton alternatif dari pepton komersial seperti pepton kedelai dan pepton pankreas hasil produksi Oxoid dan Difco.
Tujuan
Tujuan penelitian ini adalah untuk mendapatkan konsentrasi papain, pH dan suhu terbaik pada hidrolisis keong mas menjadi pepton dan mengetahui pengaruhnya terhadap pertumbuhan mikroba.
Ruang Lingkup
II. TINJAUAN PUSTAKA
Keong Mas (Pomacea canaliculata Lamarck)
Keong mas atau siput murbai (Pomacea canaliculata Lamarck) merupakan salah satu hama utama yang dapat menimbulkan masalah dalam produksi padi (Gambar 1). Badan Pangan Dunia (FAO) dari Perserikatan Bangsa-Bangsa (UNO) menduga kehilangan hasil yang disebabkan hama ini mencapai 40% dari areal padi sawah di Filipina pada tahun 1989 yang menyebabkan kehilangan hasil cukup besar (Hendarsih, 2004).
Keong mas banyak ditemukan di lingkungan basah seperti persawahan dan rawa-rawa. Siklus hidupnya cukup lama yaitu 2 hingga 6 tahun dengan kemampuan bertelur mencapai 1000 hingga 1200 butir dalam sebulan mengakibatkan pertumbuhan populasi yang tinggi (Hendarsih, 2004).
Keong mas memakan beragam tumbuhan seperti ganggang, azola, rumput bebek. eceng gondok, bibit padi dan tumbuhan berdaun sukulen lainnya. Habitatnya berupa kolam, rawa, sawah irigasi. saluran air dan areal yang selalu tergenang (Hendarsih, 2004).
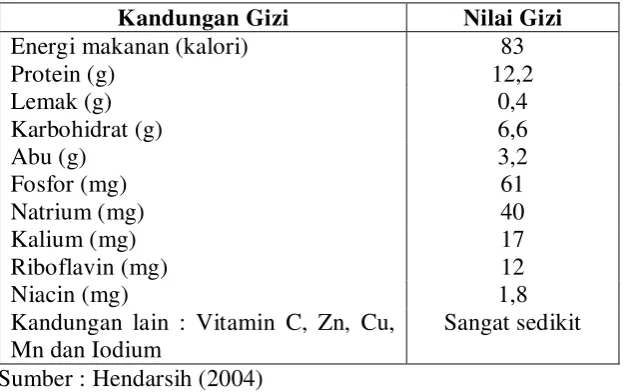
Kandungan nilai gizi dari 100 gram keong mas adalah sebagai berikut: Tabel 1. Kandungan gizi dari 100 gram daging keong mas
Kandungan Gizi Nilai Gizi ikan. Kandungan protein tepung keong lebih tinggi dibandingkan dengan tepung ikan yang selama ini menjadi sumber protein dalam pakan ternak. Menurut Siswanto (1999) kadar protein tepung keong mas (Pomacea canaliculata)adalah sebesar 50,74%, sedangkan kadar protein tepung ikan sekitar 30 % (Soegeng, 2003).
Pepton
mengandung vitamin dan karbohidrat. Penguraian bahan-bahan protein tesebut dapat dilakukan dengan suatu senyawa asam atau berupa enzim. Pepton mempunyai kemampuan berbeda dalam hal menunjang pertumbuhan bakteri tergantung jenis protein yang digunakan dan proses ekstraksinya.
Menurut Clausen (1985), pepton dapat diperoleh dari hasil hidrolisis protein hewani, baik limbah (jeroan) atau daging yang tidak bernilai ekonomis tinggi, gelatin, susu, kasein, tanaman maupun khamir. Sedangkan menurut Bridsson dan Brecker (1970) pepton adalah hidrolisat protein terbuat dari bahan-bahan berprotein tinggi seperti pada: daging, ikan, kasein, gelatin, tepung kedelai, khamir, biji kapas, dan bunga matahari. Hidrolisis secara umum dapat menggunakan enzim proteolitik seperti papain, pepsin dan tripsin. (Heritage et al., 2000).
Bridsson dan Brecker (1970) menerangkan bahwa kandungan protein pada bahan baku pembuatan pepton sebagai media pertumbuhan bakteri dapat bervariasi dari protein hewani dengan kadar 50-90% berat kering hingga dari protein biji-bijian dengan kandungan protein kurang dari 1%. Protease mengkatalisis proses hidrolisis protein menjadi pepton yang terdiri dari campuran polipeptida, dipeptida, dan asam amino.
Kandungan pepton merupakan campuran kompleks bahan larut air yang berasal dari turunan protein daging tanpa lemak dan sumber lainnya, termasuk jantung, otot, kasein dan tepung kedelai. Kandungan senyawa utama pepton adalah proteosa, asam amino, garam anorganik dan vitamin. (Heritage et al., 2000).
Pembuatan pepton kepala tuna
hingga seragam ukurannya, kemudian dimaserasi dalam air suling pada perbandingan antara bahan dengan air 4 : 1. Sebanyak 0,2% (volume/bobot) enzim alkalise ditambahkan ke dalam bubur limbah. Campuran tersebut kemudian dimasukkan ke inkubator bersuhu 50 C.
Campuran direndam dalam penangas air bersuhu 85°C selama 15 menit untuk menonaktifkan enzim dan selanjutnya disaring.. Sentrifugasi selanjutnya dilakukan pada suhu 4°C dengan kecepatan 13000 rpm selama 10 menit. Fase cair dianalisa kandungan nitrogennya dan selanjutnya disimpan pada suhu 4°C selama semalam, fraksi lemak yang mengambang dipermukaannya dibuang. Larutan pepton tersebut selanjutnya dikeringkan dengan menggunakan pengering tipe semprot pada tekanan nozzle 2000 mBar, suhu masuk 180°C, dan suhu keluar 100°C (Gambar 2). Hasil penelitian menunjukkan perlakuan tekanan nozzle memberikan pengaruh nyata terhadap rendemen dan tingkat kekeruhan, dan dihasilkan bubuk pepton berkadar air sebesar 5,56 - 6,80% (basis basah), rendemen berkisar antara 5,72 - 6,53 (b/b), kadar protein berkisar antara 83,55 - 85,09%, tingkat kekeruhannya berkisar antara 39,78 - 43,78
Gambar 2. Diagram alir pembuatan pepton kepala ikan tuna (Siswanto, 2000)
Variabel perlakuan pembuatan pepton kepala ikan tuna yang digunakan dalam penelitian Siswanto (2000), adalah persentase enzim alkalase (0,2, 0,4, dan 0,6 % (v/b)), suhu hidrolisis (50, 60, dan 70°C), dan pada perlakuan spray dryer, yaitu tekanan nozzle (1500, 1750, dan 2000 mBar), suhu pemasukan (180, 190, dan 200°C) dan suhu keluaran (90, 95, dan 100°C). Perlakuan yang menghasilkan kandungan nitrogen tertinggi adalah pada suhu 50oC, konsentrasi enzim 0,2% (v/b) dan pada perlakuan spray dryer adalah tekanan nozzle 2000 mBar, suhu inlet 180oC dan outlet 100oC.
Limbah perikanan (kepala ikan tuna)
Maserasi dalam air suling dengan perbandingan 1:4 (bahan:air)
Penambahan enzim alkalase 0,2% (v/b)
Inaktivasi enzim dengan air 85 C, 10 menit
Sentrifugasi (13.000 rpm, 10 menit)
Penyimpanan pada suhu 4 C, 12 jam
Pembuangan lemak pada permukaan
Larutan (ekstrak) pepton kasar
Pengeringan dengan Spray Drier
Papain
Papain adalah enzim protease yang berasal dari tanaman pepaya (Carica papaya Linn). Harganya lebih murah dibandingkan enzim yang berasal dari mikroba. Enzim ini dapat digunakan sebagai pengempuk daging (Suhartono, 1992) dan bahan campuran detergen (Khaparde dan Singhal, 2000),
Papain adalah rantai polipeptida yang terdiri atas 212 asam amino. Bagian penting dalam rantai polipeptida papain adalah asam amino sistein-25 dan histidin-159 yang merupakan bagian utama dalam proses katalisis. Aktivitasnya ditentukan oleh 2 gugus sulfihidril bebas dari semua 6 gugus sulfihidril yang dimiliki. Papain termasuk golongan enzim protease sulfihidril karena mempunyai gugus aktif- SH. Nama papain digunakan baik untuk getah kering maupun enzim proteolitik yang dikristalkan (Suhartono, 1992).
Menurut Winarno (1986), bahwa papain merupakan salah satu enzim katalisator protein. Aktivitas enzim yang dilakukan dalam proses katalisis adalah dengan menurunkan energi aktivitas reaksi secara spesifik. Pengubahan energi aktivasi dilakukan dengan cara menurunkan hambatan energi sehingga reaksi dapat berjalan lebih cepat (Rehm dan Reed, 1995). Energi aktivasi adalah jumlah energi (dalam kalori) yang diperlukan untuk membawa semua molekul pada satu mol senyawa pada suhu tertentu menuju tingkat transisi pada puncak batas energi (Muchtadi, 1992). Kestabilan papain terhadap suhu dengan senyawa sorbitol,sucrose,xylose dan glycerol cukup baik (Sathish et all, 2005).
Selain itu, nilai kecepatan hidrolisis juga dipengaruhi oleh keberadaan aktivator dan inhibitor (Wilson dan Walker, 2000).
Aktivitas papain meningkat dengan penambahan senyawa pereduksi seperti glutation, sistein atau sulfit, atau pengkelat seperti etilen diamin tetra asetat (EDTA), namun akan menurun apabila enzim ini direaksikan dengan senyawa pengganggu gugus tiol, yaitu oksidator, senyawa disufida, dan ion logam berat (Suhartono, 1992).
Pemilihan enzim proteolitik untuk proses hidrolisis didasarkan pada spesifikasi enzim, pH optimum, kestabilan panas, pengaruh aktivator dan inhibitor, harga dan ketersediaan enzim tersebut (Johnson dan Peterson, 1978). Aktivitas enzim papain berada pada daerah pH yang luas. Nilai pH optimummya berkisar dari 6,0 sampai 8,0, pada pH dibawah 3 atau diatas 12 dapat menyebabkan denaturasi papain secara tak dapat balik (irreversible). Papain relatif stabil terhadap suhu, bahkan masih aktif hingga suhu mendekati 75°C (Suhartono, 1992).
kecil, sehingga lebih mudah larut dibandingkan molekul sebelumnya.
Terdapat tiga perubahan hidrolisis ikatan peptida, yaitu : (1) peningkatan jumlah gugus terionisasi (NH4+, COO-) sehingga produk lebih bersifat hidrofilik, (2) penurunan ukuran molekul rantai polipeptida yang mengakibatkan sifat antigenisitas menurun tajam, dan (3) perubahan struktur molekul membentuk struktur hidrofobik yang terbuka terhadap lingkungan berair (Mahmoud, 1994). Zayas (1997) menyatakan hal yang sama, yaitu hidrolisis ikatan peptida dapat meningkatkan jumlah gugus bermuatan dan jumlah sisi hidrofilik karena molekul protein menjadi terbuka strukturnya, sehingga meningkatkan kelarutan dan menurunkan viskositas. Hal ini ditunjukkan dengan peningkatan derajat hidrolisis. Dasar proses hidrolisi enzimatis adalah pemutusan ikatan peptida oleh enzim dengan bantuan air, secara kimiawi digambarkan sebagai berikut (Peterson, 1981).
-CHR’-CO-NH-CHR’’ + H2O CHR’-COOH + NH2-CHR’’
Escherichia coli
Escherichia coli merupakan bakteri gram negatif yang bersifat anaerob fakultatif dan motil. Ciri biokimia bakteri tersebut adalah memiliki kemampuan memfermentasi laktosa, reaksi indol positif, uji Voger-Proskauer (VP) negatif, dan tidak menggunakan sitrat sebagai satu-satunya sumber karbon. Bakteri ini menimbulkan warna hijau metalik pada media selektif EMB. Beberapa galur bakteri ini bersifat patogen (Buchanan dan Gibbons, 1974; Doyle dan Padhye,1994).
E. coli mempunyai struktur utama berupa flagella di sekitar sel (flagella peritrikus). Flagella adalah rambut-rambut yang teramat tipis mencuat menembus dinding sel dan bermula dari tubuh dasar, suatu struktur granular tepat di bawah membran sel di dalam sitoplasma (Pelczar, 1986).
E. coli adalah indikator dalam penentuan tercemarnya air oleh limbah domestik, seperti limbah rumah tangga, hotel, dan lain-lain. Bakteri ini biasanya ke luar menuju alam bebas bersama tinja. Keberadaan E. coli dalam air menunjukkan air tersebut tercemar tinja manusia dan mungkin mengandung bibit penyakit berbahaya, sehingga air yang tercemar E. coli perlu diwaspadai atau tidak layak diminum. Bakteri ini dapat menimbulkan gangguan kesehatan jika masuk ke saluran pencernaan, baik melalui minuman maupun makanan. Gangguan kesehatan tersebut, bisa berupa tifus, kolera, hepatitis, diare, dan lain-lain (Anonimous, 2007).
Staphylococcus aureus
(Shewan, 1970). Bakteri ini sering hidup pada kulit atau di dalam hidung manusia, yang dapat menyebabkan bermacam-macam penyakit kulit, seperti jerawat, cellulitis dan bisul, selain itu penyakit dalam seperti radang paru-paru, radang selaput otak, sumsum belakang, endocarditis, dan keracunan darah (Anonimus, 2007).
Menurut Effendi (1992), Staphylococcus aureus juga mempunyai sifat dapat menghidrolisis urea, memfermentasi glukosa dan fruktosa, menghidrolisis lemak, mereduksi nitrat menjadi nitrit dan bersifat proteolitik, yaitu dapat memecah protein menjadi peptida dan asam amino yang digunakan untuk sintesa protein dan sumber energi.
Aspergillus niger
Aspergillus niger adalah kapang yang paling banyak dari genus Aspergillus. Mikroba ini mudah diisolasi dari udara, lahan, pantai pasir, rawa bakau, air yang tercampur bahan organik, kotoran limbah, pupuk kompos, bahan makanan terutama buah-buahan dan sayur-mayur, pupuk binatang, bulu burung, bubur kayu, benih, dan bahan tekstil. Spesies ini menyebabkan penyakit noda hitam pada sayur-mayur dan buah-buahan tertentu seperti buah anggur, bawang, dan kacang tanah. Umumnya jenis ini adalah suatu zat pencemar makanan. Beberapa galur A. niger telah dilaporkan menghasilkan mikotoxin kuat yang disebut ochratoxin (Anonimous, 2006 dan Sahay, 2004). A. niger juga menimbulkan penyakit pada manusia. Menurut Anonimous (2006) A. niger
bakar, yang mungkin kaya bahan spora Aspergillus. A. niger juga adalah salah satu penyebab umum otomycosis (peradangan telinga), yang dapat menyebabkan hilang pendengaran sementara hingga kerusakan pada saluran telinga dan selaput
tympanic.
Manfaat dari A. niger di industri kimia adalah dalam pembuatan asam sitrat (E330) dan asam glukonat (E574) dan telah diizinkan penggunaannya oleh Organisasi Kesehatan Dunia. Selain itu, enzim dari A. niger, yaitu glukoamilase digunakan untuk produksi sirup jagung fruktosa kadar tinggi, dan enzim pektinase digunakan dalam pembuatan minuman dari buah apel dan anggur.
Saccharomyces cerevisiae
Saccharomyces cerevisiae adalah sejenis khamir. Khamir sendiri adalah mikroba eukariotik bersel tunggal golongan fungi, non motil dan tidak berklorofil. Menurut Pelzcar (1978), habitat khamir cukup luas, dapat ditemukan di tanah, air dan tanaman, serta dapat tumbuh pada berbagai tempat dan kondisi. Khamir telah dikenal sejak beberapa ratus tahun yang lalu, digunakan untuk pembuatan alkohol secara anaerobik. Pada kondisi aerobik, khamir dapat mengkonsumsi bahan organik sebagai substrat mulai dari molekul sederhana seperti metanol sampai molekul besar seperti alkana (Doelle, 1994).
Fase-fase Pertumbuhan Mikroorganisme
Menurut Volk dan Wheeler (1988), hampir semua mikroorganisme mampu berkembang biak dengan cepat jika kebutuhan nitrisi dan kondisi lainnya memenuhi kebutuhannya, seperti pH dan suhu. Waktu generasi adalah waktu yang diperlukan mikroorganisme untuk membentuk generasi baru. Pada beberapa bakteri, seperti E. coli, waktu generasi rata-rata sekitar 20 menit untuk membelah diri, sedangkan pada jenis lainnya sekitar 15 sampai 20 jam. Waktu generasi selama pertumbuhan aktif bervariasi sesuai dengan jenis bakteri, walaupun kebanyakan kurang dari 1 jam.
Laju pertumbuhan bakteri dapat diproyeksikan sebagai logaritma jumlah sel terhadap waktu pertumbuhan, sehingga diperoleh kurva pertumbuhan bakteri yang dapat dibagi menjadi empat fase, yaitu :
1. Fase Tenggang (Lag), yaitu periode penyesuaaian pada lingkungan. Mikroorganisme mulai mensintesa enzim-enzim dan menggunakan cadangan makanan.
2. Fase logaritma (Log), yaitu periode pembiakan yang cepat dan merupakan periode berciri khas sel-sel yang aktif. Selama fase ini waktu generasi tetap tidak berubah bagi setiap jenis, jika dibuat proyeksi logaritma jumlah organisme terhadap waktu, fase log ini berupa garis lurus. Waktu generasi suatu organisme dapat ditentukan selama fase ini. Setiap generasi mikroba menghasilkan jumlah sel yang berlipat dua. Dan akan diperoleh rumus :
Bt = B0 X 2n Dimana :
Bt = Jumlah bakteri pada akhir interval waktu (t) g = waktu generasi, biasanya dinyataan dalam menit t = waktu, biasanya dinyatakan dalam menit
n = jumlah generasi
Nilai n dapat diperoleh dengan :
Karena :
Dan
Maka diperoleh
Sehingga waktu generasi (g) dapat diperoleh dengan rumus :
Waktu generasi beraneka menurut jenis mikroorganisme, kadar nutrien dalam medium dan suhu inkubasi. Kondisi lain seperti pH, persediaan oksigen bagi yang bersifat aerob, akan mempengaruhi pula.
cenderung menumpuk dan mungkin menjadi racun bagimikroorganisme tersebut.
Pemilihan bahan dan metode penelitian pembuatan pepton keong mas ditentukan dengan beberapa pertimbangan untuk mendapatkan hasil yang maksimal dan ekonomis. Hal-hal yang dipertimbangan tersebut adalah sebagai berikut :
Keong mas yang banyak ditemukan di lahan pertanian kurang dimanfaatkan oleh industriawan, kecuali sebagai bahan pakan unggas dan sebagai bahan makanan di masyarakat karena kandungan proteinnya yang cukup tinggi. Hal ini menjadi pertimbangan keong mas sebagai bahan baku penelitian ini.
Enzim papain merupakan enzim protease yang mempunyai harga lebih murah dibandingkan enzim yang berasal dari mikroba, selain itu aktivitas enzim papain berada pada selang suhu yang lebar (60 - 70 C). Hal ini menjadi pertimbangan pemilihan enzim papain sebagai enzim penghidrolisis pada penelitian ini.
Pembuatan pepton keong mas diusahakan dapat bersaing dengan pepton impor, oleh sebab itu dihindari penggunaan peralatan berbiaya tinggi (contohnya spray drier) dengan tujuan menekan biaya produksi.
Penggunaan mikroba Escherichia coli, Staphylococcus aureus, Saccharomyces cerevisiae dan Aspergillus niger dilakukan untuk mengevaluasi qualitas pepton keong mas, karena Escherichia coli mewakili kelombok bakteri gram negatif,
Tempat dan Waktu
Penelitian dilakukan di Laboratorium Departeman Teknologi Industri Pertanian, Institut Pertanian Bogor (IPB), dan di Laboratorium Rekayasa Bioproses Pusat Antar Universitas (PAU) IPB. Penelitian ini dilaksanakan selama 5 bulan, mulai bulan Juli hingga bulan Desember 2006.
Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah sebagai berikut :
keong mas sebagai bahan utama, papain sebagai enzim penghidrolisis protein, pepton dari Difco dan Oxoid, bahan-bahan kimia untuk analisa nitrogen, isolat mikroorganisme, yaitu Escherichia coli, Staphylococcus aureus, Saccharomyces cerevisiae dan Aspergillus niger serta Nutrient Broth (Difco) dan glukosa.
Alat yang digunakan dalam penelitian ini antara lain adalah sebagai berikut: wadah untuk memanaskan daging keong, oven, penggiling daging, seperangkat alat Kjeldahl, pH meter, sentrifus, kertas saring, labu erlenmeyer, dan High Performance Liquid Chromatography (HPLC) dengan kolom type khusus untuk analisis asam amino.
Metode Penelitian 1. Pengumpulan Keong Mas
Keong mas yang telah terkumpul dipungut secara langsung dari tempat tersebut dan tempat lainnya, seperti pematang sawah.
2. Pembuatan Tepung Keong
Keong mas yang telah terkumpul dari alam tidak langsung diproses menjadi pepton tetapi dirubah dahulu menjadi tepung keong. Pembuatan tepung keong mas bertujuan untuk menyeragamkan bahan baku dan memudahkan bahan baku tersebut untuk disimpan sehingga ketersediaan bahan baku yang seragam tetap terjamin.
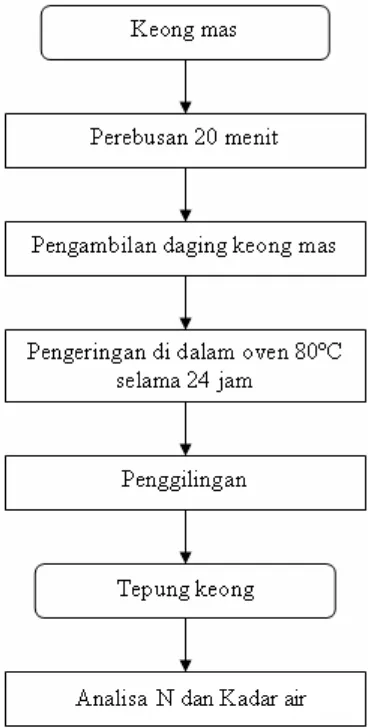
Pembuatan tepung keong dilakukan dalam beberapa tahap, yaitu perebusan, pengeringan dan penggilingan. Perebusan keong mas dilakukan selama 20 menit untuk mengurangi kadar lemak dan memudahkan mengeluarkan daging keong dari dalam cangkangnya. Daging keong tersebut selanjutnya dikeringkan dalam oven 65 ºC selama 24 jam. Daging keong kering yang diperoleh selanjutnya dihaluskan dengan menggunakan mesin penggiling untuk menghasilkan tepung keong mas (Bagus, 1999). Tepung keong tersebut selanjutnya dianalisa proksimat, yaitu kadar nitrogen dan kadar air.
Gambar 3. Diagram alir pembuatan tepung keong (Bagus, 1999)
Penelitian ini menggunakan metode hasil penelitian Bagus (1999) untuk menghasilkan tepung keong, tetapi pada tahapan pengeringan daging keong di oven pada suhu 60°C selama 48 jam. Jika digunakan suhu 80°C selama 24°, daging keong akan hangus.
total berat nitrogen tepung keong. Faktor yang diberikan adalah dengan taraf 0,2 %, 0,4 %, dan 0,6%, penentuan kondisi ini berdasarkan hasil penelitian Fachraniah (2002) yang menggunakan papain untuk membuat pepton dari bungkil kedelai dan pepton dari limbah bir dengan kondisi terbaik konsentrasi papain adalah 0,2 % dan 0,4%. Jenis faktor kedua yang diberikan adalah faktor pH, yaitu pH 4,5 ; 5 ; 5,5 ; 6 ; 6,6 dan 7. Jenis faktor berikutnya yang diberikan adalah faktor suhu, yang tujuannya untuk mendapatkan suhu terbaik, taraf faktor suhu yang diberikan yaitu suhu 60 oC, 65 oC, 70 oC dan 75 oC, dan dasar dari penggunaan faktor suhu ini adalah dari kondisi optimum suhu papain bekerja, yaitu antara 60 oC hingga 75 oC. Yang diamati dari jenis ketiga faktor tersebut adalah kadar nitrogen.
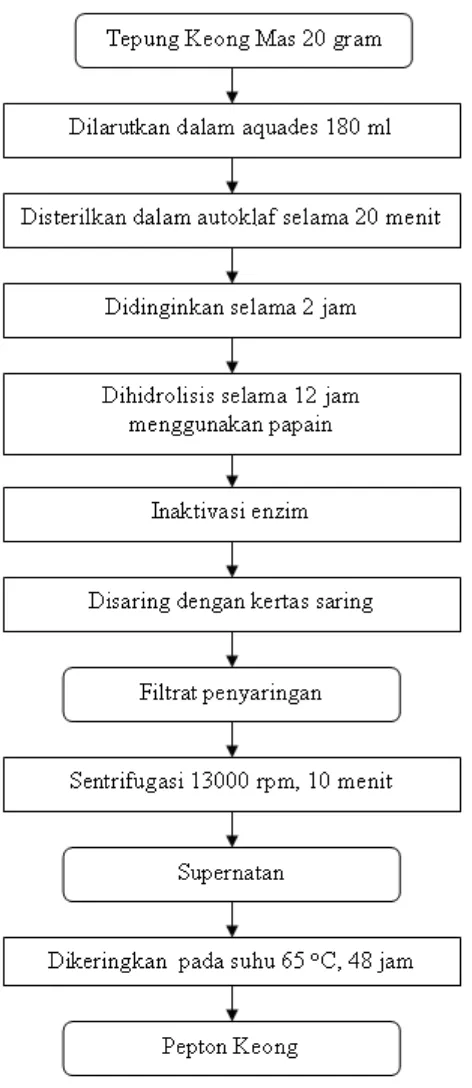
4. Pembuatan Pepton Keong
Prosedur pembuatan pepton keong dalam penelitian ini adalah hasil modifikasi pembuatan pepton dari limbah ikan tuna hasil penelitian Siswanto (2000). Perbedaan dalam penelitian ini yaitu tidak digunakan pengering tipe semprot yang bertujuan menekan biaya penggunaan alat, sebagai gantinya digunakan oven.
sampel setiap 2 jam. Analisa yang dilakukan terhadap sampel hidrolisat tepung keong adalah derajat hidrolisis protein (Rehm dan Reed, 1995).
Tahap selanjutnya setelah hidrolisis meliputi tahap inaktivasi enzim papain dengan cara memanaskan hidrolisat pada suhu 100ºC selama 10 menit di dalam air mendidih. Selanjutnya disaring dengan kertas saring. Tahap berikutnya adalah mensentrifugasi filtrat hasil penyaringan selama 10 menit pada kecepatan 13000 rpm untuk diambil supernatannya. Selanjutnya dikeringkan menggunakan oven pada suhu 65 oC selama 48 jam. Hasil pengeringan ini selanjutnya dianalisa kandungan nitrogennya dengan menggunakan uji Kjeldahl (Lampiran 2) dan analisa HPLC untuk asam amino (Lampiran 4).
Tepung pepton keong selanjutnya diuji secara mikrobiologis sebagai media tumbuh mikroba Escherichia coli, Staphylococcus aureus, Saccharomyces cerevisiae
dan Aspergillus niger masing-masing 2 ulangan duplo, dan sebagai pembanding media digunakan pepton dari Oxoid dan Difco. Kriteria yang diamati pada perbandingan tersebut adalah pertambahan biomassa dan pemakaian nitrogen oleh mikroorganisme.
Prosedur Analisis 1. Analisis Proksimat
Prosedur analisis proksimat yang dilakukan terhadap keong mas dapat dilihat pada Lampiran 2. Analisis tersebut dilakukan memperoleh data pembuatan neraca massa yang berguna untuk mengetahui mengetahui adanya sejumlah kehilangan bahan dalam meningkatkan effisiensi penggunaan bahan baku.
2. Analisa Hasil Pengambilan Sampel pada Tahap Hidrolisis Tepung Keong Analisa sampel hidrolisis tepung keong mas dilakukan setiap 2 jam sekali dan prosedur analisisnya dapat dilihat pada Lampiran 3. Tujuan analisis tersebut adalah mengetahui kondisi hidrolisis yang sedang berlangsung, yaitu banyaknya nitrogen yang terasimilasi oleh papain dan kemungkinan adanya perubahan pH yang mungkin dapat mengganggu tahapan hidrolisis.
3. Analisa Mikrobiologi
Analisa mikrobiologi yang digunakan adalah dengan membandingkan kemampuan tumbuh mikroba di media dengan menggunakan sumber nitrogen pepton keong dengan kemampuan tumbuh mikroba di media pepton dari Difco dan Merck dalam hal laju pertumbuhan, total pertumbuhan dan produksi massa sel mikroorganisme.
a. Sumber Mikroorganisme
yang digunakan berasal dari isolat murni, yaitu Escherichia coli, Staphylococcus aureus, Saccharomyces cerevisiae dan Aspergillus niger. b. Persiapan Media Tumbuh
Media tumbuh dibuat sesederhana mungkin dengan asumsi apabila pepton berhasil mendukung pertumbuhan mikroorganisme dengan komposisi medium yang sederhana, maka pepton akan lebih baik digunakan dalam medium yang diperkaya. Medium pertumbuhan dibuat dengan melarutkan bubuk pepton uji maupun pepton komersial sebanyak 0,5%(v/b) ke dalam wadah 1000 ml yang berisi akuades dengan asumsi kandungan protein pada masing-masing pepton adalah sama. Masing-masing media pepton ditambah dengan glukosa sebesar 0,1 % untuk media bakteri dan 1% untuk media kapang dan khamir (Tabel 2). Sebelum sterilisasi, pH media diatur dengan menggunakan HCl 0,1 N atau NaOH 0,1 N, pH bakteri yang digunakana adalah 7,00 ± 0,01 dan untuk pH kapang dan khamir adalah 5,50 ± 0,01. Tabel 2. Komposisi media tumbuh mikroorganisme berdasarkan jenis pepton yang
c. Persiapan Kultur Mikroorganisme c.1. Kultur Bakteri
Kultur murni bakteri (E. coli dan S. aureus) disuspensikan ke dalam 100 ml nutrient broth kemudian diinkubasikan selama 24 jam pada suhu 37ºC. Selanjutnya kultur diinokulasikan pada tingkat pengenceran 10-2 ke dalam media pertumbuhan yang berisi pepton yang diuji.
c.2. Kultur Khamir (Saccharomyces cerevisiae)
Kultur murni Saccharomyces cerevisiae disuspensikan di Potato Dextrose Agar (PDA) selama 48 jam lalu dipropagasi di Potato Dextrose Broth (PDB) selama 24 jam. Selanjutnya diambil 2,5 ml dan dimasukkan ke dalam 50 ml media pertumbuhan berpepton, dan kemudian diamati selama 48 jam dengan waktu pengambilan sampel setiap 6 jam sekali. c.3. Kultur kapang (Aspergillus niger)
Kultur murni Aspergillus niger disuspensikan di Potato Dextrose Agar (PDA) selama 5 hari. Selanjutnya permukaan kultur dibilas menggunakan 10 ml larutan aqudes steril. Sebanyak 1 ml larutan pembilas tersebut diinokulasikan ke dalam 50 ml media pertumbuhan steril yang mengandung pepton untuk diuji selama 48 jam dengan waktu pengambilan sampel setiap 6 jam sekali.
d. Kurva pertumbuhan, Laju Pertumbuhan dan Total Pertumbuhan
jam sekali selama 24 jam, sedangkan sampel biomassa kapang dan khamir diambil menggunakan kertas saring setiap 6 jam sekali selama 48 jam.
Sampel bakteri disentrifugasi pada kecepatan 4000 rpm, suhu 4ºC, selama 10 menit. Setelah didekantasikan, endapan yang terpisah dari cairan kemudian dikeringkan di dalam oven pada suhu 100ºC selama 24 jam, sedangkan kertas saring yang berisi kultur kapang dan khamir langsung dikeringkan dengan oven pada suhu 100ºC selama 24 jam.
Bahan Baku
Keong mas adalah salah satu hama di lahan pertanian yang banyak mengandung protein, sehingga sering dijadikan sebagai bahan makananan unggas seperti bebek, berdasarkan hal inilah keong mas dijadikan bahan baku pembuatan pepton dalam penelitian ini. Penelitian ini menggunakan bahan baku berupa keong mas segar dengan ukuran berkisar 40 mm dengan pertimbangan ukuran tersebut paling banyak ditemukan. Kemudian keong mas tersebut diolah menjadi tepung untuk selanjutnya dihidrolisis menjadi pepton menggunakan enzim papain.
Tepung keong mas yang dihasilkan dari hasil pengeringan daging keong mas untuk kemudian dicacah dan dihaluskan dengan grinder menghasilkan tepung berwarna hitam kecoklatan berupa butiran kecil dan selanjutnya disaring dengan saringan berukuran 50 mesh. Sifat kimia tepung keong yaitu : kadar air 8,41% (wb), kadar protein 68,15%, karbohidrat 12,37% dan lemak 6,65%. Hasil penelitian ini berbeda dengan hasil penelitian Siswanto (1999) yang menyatakan kadar protein tepung keong adalah 50,74%. Hal ini kemungkinan disebabkan perbedaan umur keong dan lokasi pengambilan keong tersebut.
Papain
Enzim papain sangat mudah dijumpai di pasaran sebagai pengempuk daging, akan tetapi karena zat pengempuk daging tersebut banyak mengandung garam yang dikhawatirkan dapat menjadi faktor penghambat pertumbuhan mikroorganisme, oleh sebab itu digunakan enzim papain kasar (crude papain)
yang digunakan berbentuk bubuk berwarna kuning keputihan dengan kadar air 11,6957% (wb), kadar nitrogennya 68,15%, kadar karbohidrat 6,26% dan kadar lemak 2,20%.
Pengaruh Konsentrasi Papain
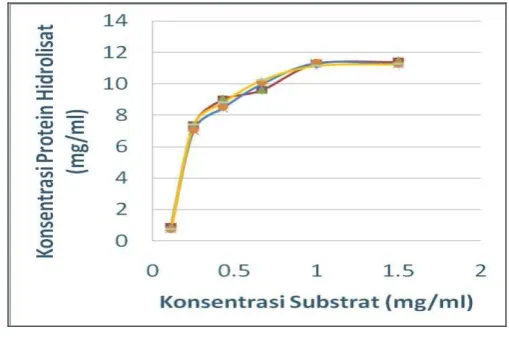
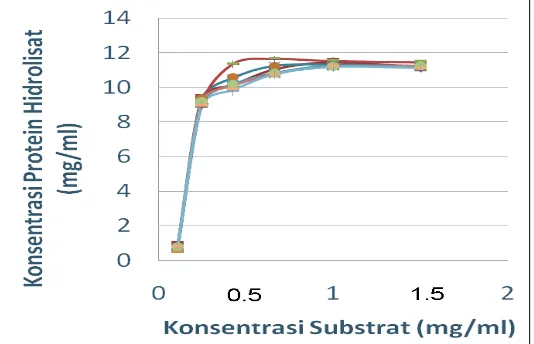
Penelitian ini terdiri atas tiga tahap. Tujuan tahapan pertama adalah memperoleh konsentrasi enzim papain terbaik yang akan digunakan dalam penelitian selanjutnya. Penelitian tahap pertama ini dilakukan dengan menggunakan konsentrasi enzim papain 0,2%, 0,4% dan 0,6% yang ditambahkan berdasarkan bobot tepung keong mas yang dihidrolisis. Hidrolisis sendiri dilakukan selama 12 jam dan selanjutnya diukur absorbansinya untuk mendapatkan konsentrasi protein hidrolisat. Gambar 5 menunjukkan bahwa setiap perlakuan memberikan nilai konsentrasi protein hidrolisat yang hampir sama.
Keterangan :
Papain 0,2% Papain 0,4% Papain 0,6%
Hasil analisa keragamanan menunjukkan konsentrasi papain tidak memberikan pengaruh yang nyata , hal ini disebabkan konsentrasi papain 0,2 % hingga 0,6 % memberikan jumlah partikel hidrolisat yang sama sehingga ditetapkan perlakuan konsentrasi yang terbaik adalah menggunakan papain konsentrasi terkecil, yaitu 0,2% dengan pertimbangan penghematan bahan pendukung, yaitu papain.
Pengaruh pH
Berdasarkan hasil perlakuan konsentrasi papain sebelumnya, maka dilakukan penelitian tahap selanjutnya, yaitu menentukan pH terbaik untuk kondisi hidrolisis. Gambar 6 memperlihatkan taraf faktor yang terbaik dari faktor pH yaitu taraf faktor pH 5,5 karena kondisi hidrolisis pada pH 5,5 memberikan hasil hidrolisat terbanyak.
Keterangan : pH 4,5 pH 5,0 pH 5,5 pH 6,0 pH 6,5 pH 7,0
Pengaruh Suhu
Penelitian pengaruh suhu adalah lanjutan dari penelitian pengaruh konsentrasi papain dan pengaruh pH. Hasil yang diperoleh dari penelitian tersebut menunjukkan suhu 65°C hingga suhu 70°C memberikan hasil perlakuan tertinggi, tetapi berdasarkan hasil uji keragaman pengaruh perlakuan tersebut sama, sehingga data yang digunakan adalah suhu yang terkecil, yaitu 65°C.
Gambar 7 memperlihatkan bahwa konsentrasi substrat sekitar 0,5 mg/ml dan suhu 65°C hingga 70°C, proses hidrolisis lebih banyak menghasilkan jumlah hidrolisat dibandingkan suhu 60°C dan 75°C. Energi yang menyebabkan partikel-partikel enzim menyatu membentuk kompleks substrat lebih rendah pada suhu 60°C, sehingga proses hidrolisis berjalan lebih pelan dibandingkan pada lingkungan yang bersuhu lebih tinggi, sedangkan pada suhu 75°C enzim papain banyak mengalami kerusakan sehingga kemampuan enzim papain untuk menghidrolisis lebih besar pada suhu 65°C dan 70°C.
Keterangan :
Suhu 60°C Suhu 65°C Suhu 70°C Suhu 75°C
Derajat Hidrolisis
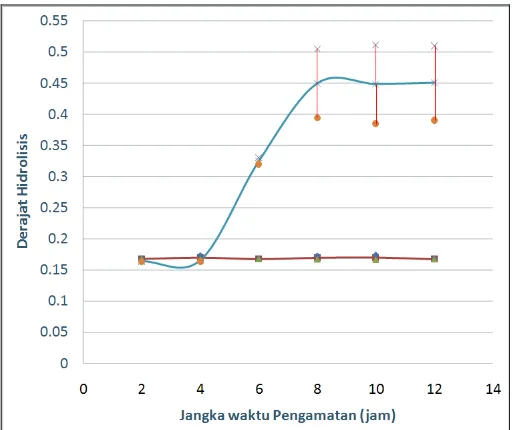
Proses hidrolisis menghasilkan produk berupa peptida dan asam-asam amino. Jumlah produk berupa asam amino dinyatakan dalam bentuk nilai nitrogen yang terasimilasi. Perbandingan nitrogen terasimilasi dengan jumlah nitrogen total dinamakan derajat hidrolisis. Derajat hidrolisis dalam penelitian ini digunakan untuk mengetahui lama hidrolisis yang terbaik. Hasil analisa derajat hidrolisis dapat dilihat pada Gambar 8.
Keterangan :
Substrat Tepung Keong Mas tanpa perlakuan (Kontrol)
Substrat Tepung Keong Mas dengan Konsentrasi Papain 0.2 %, pH 5.5, dan suhu 65 oC
Gambar 8. Derajat Hidrolisis Substrat Tepung Keong Mas
Penelitian dengan menggunakan data pendahuluan, yaitu konsentrasi papain 0,2%, pH 5.5 dan suhu 65 oC, menghasilkan pepton keong dengan kandungan nitrogen sebesar 46,20 % dengan nilai derajat hidrolisis sebesar 49,08 %, sedangkan nilai total nitrogen dari Difco adalah 62.93 % dan nilai total Oxoid adalah 73,75 %. Hasil analisa terhadap pepton keong dan pepton pembandingnya menggunakan HPLC asam amino menghasilkan grafik data pada Gambar 9.
Gambar 9. Grafik Hasil Analisa HPLC Asam Amino terhadap pepton Keong, Oxoid dan Difco
Uji Penggunaan Pepton Keong
Kualitas pepton keong diuji kemampuannya sebagai sumber nitrogen bagi mikroorganisme, untuk mengujinya digunakan 4 macam mikroba, yaitu
Escherichia coli, Staphylococcus aureus, Saccharomyces cerevisiae dan
Aspergillus niger.
1. Escherichia coli
Gambar 10 menunjukkan penggunaan nitrogen pada pepton keong mas berada diantara pepton Difco dan Oxoid. Gambar tersebut menunjukkan jumlah penggunaan nitrogen pada media. Kesimpulan yang dapat diambil dari gambar tersebut adalah penggunaan nitrogen oleh E.coli lebih baik pada pepton Oxoid, artinya nitrogen pada pepton Oxoid lebih mudah dikonsumsi oleh E.coli daripada nitrogen pepton keong dan Difco, karena semakin miring kecenderungan suatu garis penggunaan konsumsi nitrogen berarti semakin mudah mikroba dalam media tersebut mengkonsumsinya.
Keterangan :
Pepton Oxoid Pepton Keong Pepton Difco
Keterangan :
Pepton Oxoid Pepton Keong Pepton Difco
Gambar 11. Hasil pengamatan pertumbuhan Escherichia coli pada pepton Keong, Oxoid dan Difco
Gambar 12 menunjukkan grafik nilai pertumbuhan E.coli pada media pepton keong dibawah nilai pertumbuhan pada media lainnya. Hal ini dikarenakan kebutuhan E.coli terhadap nitrogen bebas kurang terpenuhi, sehingga jumlah sel mikroba ini lebih cepat mengalami kematian dibandingkan di media yang lain.
Keterangan :
Pepton Keong (y = 0,38x - 9,66 ; R² = 0,92) Pepton Oxoid (y = 0,42x - 9,35 ; R² = 0,89) Pepton Difco (y = 0,40x - 9,31 ; R² = 0,80)
Hasil pengukuran terhadap laju pertumbuhan pada menunjukkan laju pertumbuhan E.coli yang paling cepat adalah pada Oxoid, yaitu sebesar 0,42 mg/ml per jam (Gambar 12). Hal ini sesuai dengan hasil yang ditunjukkan pada konsumsi nitrogen E.coli.
2. Staphylococcus aurues
Pemakaian nitrogen oleh S. aurues lebih banyak jumlahnya pada pepton oxoid (seperti ditunjukkan Gambar 13), kemungkinan hal ini disebabkan kemudahan digunakannya pepton Oxoid oleh bakteri dibandingkan pepton lainnya, yaitu lebih mudah menguraikan rantai peptida pepton Oxoid untuk menggunakan nitrogennya.
Keterangan :
Pepton Oxoid Pepton Keong Pepton Difco
Gambar 13. Hasil Pengamatan Pemakaian Nitrogen oleh S. aurues pada Pepton Keong, Oxoid dan Difco
Keterangan :
Pepton Oxoid Pepton Keong Pepton Difco
Gambar 14. Hasil Pengamatan Pertumbuhan Staphylococcus aurues pada Pepton Keong, Oxoid dan Difco
Gambar 13 dan Gambar 14 menunjukkan grafik pertumbuhan S. aurues
pada pepton keong lebih baik daripada pertumbuhannya pada pepton Difco. Hal ini menunjukkan bahwa bakteri ini lebih mampu mengkonsumsi pepton keong daripada mengkonsumsi pepton Difco.
Perhitungan laju pertumbuhan menunjukkan besarnya laju pertumbuhan
S. aurues pada media pepton Oxoid adalah sebesar 0,66 mg/ml per jam. Hal tersebut dapat dilihat pada Gambar 15.
Keterangan :
Pepton Keong (y = 0,51x - 9,09 ; R² = 0,91) Pepton Oxoid (y = 0,66x - 10,14 ; R² = 0,94) Pepton Difco (y = 0,60x - 10,10 ; R² = 0,89)
Gambar 15. Hasil Perhitungan Laju Pertumbuhan Staphylococcus aurues
3. Aspergillus niger
Keterangan :
Pepton Oxoid Pepton Keong Pepton Difco
Gambar 16. Hasil Pengamatan Pemakaian Nitrogen oleh Aspergillus niger
pada Pepton Keong, Oxoid dan Difco
Keterangan :
Pepton Oxoid Pepton Keong Pepton Difco
Gambar 17 menunjukkan pertumbuhan A. niger pada pepton Keong jauh lebih baik daripada pepton Oxoid dan Difco, hal ini karena salah satu syarat tumbuh A. niger adalah adanya kandungan karbohidrat pada media tumbuhnya. Hasil pengukuran kandungan karbohidrat pada pepton keong adalah sebesar 6,31 %, sedangkan pepton Oxoid 0,20 % dan Difco 3,55 %. Selain itu juga karena kemungkinan adanya enzim dari A. niger lebih mudah menguraikan pepton Keong dibandingkan pepton lainnya sehingga hasil penguraian tersebut lebih mudah digunakan oleh A. niger.
Berdasarkan perhitungan laju pertumbuhan A. niger, urutan rangking laju pertumbuhan untuk media pepton berturut-turut adalah pepton keong sebesar 0,21 mg/ml per jam, pepton Difco 0,07 mg/ml per jam dan yang terakhir adalah pepton Oxoid 0,06 mg/ml per jam (seperti yang ditunjukkan pada Gambar 18)
Keterangan :
Pepton Keong (y = 0,60x - 10,10 ; R² = 0,89) Pepton Oxoid (y = 0,06x - 8,34 ; R² = 0,82) Pepton Difco (y = 0,07x - 8,33 ; R² = 0,90)
4. Saccharomyces cerevisiae
Gambar 19 menunjukkan persentase pemakaian nitrogen oleh Khamir pada berbagai media berpepton. Gambar menujukkan persentase nitrogen dari titik waktu pengamatan 0 jam hingga 48 jam mengalami penurunan, hal ini disebabkan jumlah nitrogen terlarut dalam media berkurang karena digunakan sebagai nutrien oleh S. cerevisiae.
Keterangan :
Pepton Oxoid Pepton Keong Pepton Difco
Gambar 19. Hasil pengamatan pemakaian nitrogen oleh Saccharomyces cerevisiae pada pepton Keong, Oxoid dan Difco
Keterangan :
Pepton Oxoid Pepton Keong Pepton Difco
Gambar 20. Hasil Pengamatan Pertumbuhan Saccharomyces cerevisiae pada Pepton Keong, Oxoid dan Difco
Keterangan :
Pepton Keong (y = 0,21x - 8,29 ; R² = 0,95) Pepton Oxoid (y = 0,06x – 8,34 ; R2 = 0,82) Pepton Difco (y = 0,07x – 8,33 ; R2 = 0,89)
Gambar 21. Hasil Perhitungan Laju Pertumbuhan Saccharomyces cerevisiae
Perhitungan Neraca Massa
Perhitungan jumlah bahan baku untuk mendapatkan sejumlah produk diperlukan dalam industri. Hasil perhitungan tersebut ditampilkan dalam perhitungan neraca massa. Tujuan pembuatan neraca massa adalah untuk menentukan jumlah bahan baku yang diperlukan untuk mendapatkan produk yang diinginkan, selain itu mengetahui adanya sejumlah kehilangan bahan dalam meningkatkan effisiensi penggunaan bahan baku dan kemungkinan dapat dikembangkan proses tersebut berdasarkan neraca massa untuk mencapai proses
Perhitungan neraca massa menghasilkan data rendemen pembuatan pepton keong dengan bahan baku keong hidup adalah sebesar 10,2 %, dan rincian biaya untuk memperoleh Pepton Keong Mas sebanyak 1 kg dapat dilihat pada Tabel 3. Tabel 3. Rincian Biaya Produksi pepton Keong Mas Skala Laboratorium
Uraian Biaya Total
V. SIMPULAN DAN SARAN Simpulan
1. Daging keong mas dapat dijadikan sebagai bahan baku pembuatan pepton dengan kandungan total nitrogen 46,20 %
2. Perlakuan terbaik hidrolisis tepung keong menggunakan papain dengan aktivitas proteolitik sebesar 59,44 Unit/mg adalah pada konsentrasi papain 0,2%, pH 5.5 dan suhu 65°C dalam jangka waktu 8 jam
3. Penggunaan suhu yang terlalu tinggi diatas suhu 65°C dalam hidrolisi tepung daging keong mengakibatkan rusaknya molekul papain sehingga efektivitas papain sebagai enzim peptidase terganggu.
4. Pepton keong memberikan laju pertumbuhan yang terbaik dibandingkan pepton Oxoid dan Difco untuk mikroba golongan kapang dan khamir, yaitu Aspergillus niger dan Saccharomyces cerevisiae, hal ini kemungkinan disebabkan karena adanya ketersediaan karbohidrat yang lebih besar di pepton keong dibandingkan yang lain juga karena adanya enzim pengurai dari golongan kapang dan khamir ini yang lebih mampu menguraikan senyawa pepton keong untuk dapat lebih mudah digunakan dibandingkan senyawa dari pepton lainnya,, sedangkan untuk mikroba golongan bakteri, yaitu Escherichia coli dan
Staphylococcus aurues, pepton keong memberikan hasil laju pertumbuhan dibawah pepton Oxoid dan Difco.
5. Rendemen pembuatan pepton keong mas adalah 10,2%
6. Harga pembuatan pepton keong lebih murah, yaitu Rp 81.500,- per kilogram
Saran
Sihombing DTH. 1999. Satwa Harapan I. Pengantar Ilmu dan Teknologi Budidaya. Cetakan Pertama. Penerbit Pustaka Wirausaha Muda. Bogor. Siswanto B. 2000. Optimasi Produksi Bubuk Pepton dari Limbah Perikanan
dengan Menggunakan Pengering Tipe Pengering Semprot (Spray Dryer).. Skripsi Fakultas Teknologi Pertanian. Institut Pertanian Bogor.
Soegeng S. 2004. Gondang untuk Pakan dan Pelet.
www.indomedia.com/sripo/2003/02/28/2802kot4.htm
Suhartono M. 1992. Protease. Departement Pendidikan dan Kebudayaan. Direktorat Jendral Pendidikan Tinggi. Pusat Antar Universitas Bioteknologi. IPB. Bogor.
Sukainah A. 2003. Kondisi Proses Hidrolisis Protein Cacing Tanah dan Operasi Pemisahan Asama Amino Berbasis Teknologi Membran. Tesis, Program Pascasarjana IPB, Bogor (tidak diterbitkan).
Sutandi A. 2002. Karakteristik Isolat Protein Saga Pohon (Adenanthera pavonina
L.) Tanpa Kulit. Skripsi Fakultas Teknologi Pertanian. Institut Pertanian Bogor.
Thenawidjaja, 1984. Pengantar Kinetika Enzim. Fakultas Teknologi Pertanian. Institut Pertanian Bogor
Volk, Wesley dan Wheeler, Margaret. 1988. Mikrobiologi Dasar. Edisi 5. Penerjemah : Soenarto Adi Soemarto, Ph.D. Penerbit Erlangga.
Lampiran 1. Penentuan Aktivitas Enzim Papain (Bergmeyer, 1983)
Bahan : 1. NaOH 1 M
Dibuat melarutkan 4 gram NaOH dengan akuades menjadi 100 ml 2. Buffer phosphat pH 7
Campuran larutan NaH2PO4, 0,2 M (0,24 gram NaH2PO4, dalam 100 ml akuades), NaOH 0,2 M (0,8 gram NaOH dalam 100 ml akuades) dan akuades (perbandingan 5 : 3 : 2). Disimpan dalam lemari es.
3. Larutan kasein dengan konsentrasi 0,2 % dalam larutan buffer phosphat 7,0 4. Penimbangan 30 gram TCA kemudian dilarutkan ke dalam 100 ml akuades 5. Na2CO3 0,4 M
Dibuat melarutkan 4.24 gram Na2CO3 dalam akuades menjadi 100 ml 6. Tirosin 5 mM yang berisi 250 µ l kasein dan 250 µ l buffer phosphat dengan pH 7.
Perlakuan pada blanko dan standar, enzim digant ikan dengan akuades dan tirosin 5 mM. kemudian larutan diinkubasi pada suhu dan waktu tertentu. Reaksi hidrolisis dihentikan dengan cara penambahan 500 µI TCA 5%.
Sebanyak 375 µl supernatan ditambahkan ke dalam tabung berisi 1,25 ml Na2CO3 0,4 M dan 250 µ l Folin Ciocalteau (1:2), lalu diinkubasi kembali pada suhu 37°C selama 20 menit. Absorbansi larutan diukur pada panjang gelombang 578 nm. Satu unit aktivitas protease didefinisikan sebagai jumlah enzim yang dapat menghasailkan satu µ mol produk tirosin per menit pada kondisi pengukuran. Aktivitas enzim dihitung berdasarkan persamaan berikut :
Aktivitas protease (µ /ml) = x faktor pengenceran A
Enzim dalam CaCl2 (2 mmol/l 0.05
Tirosin standar (5 mml/l) 0.05
Akuades 0.05
Inkubasi pada suhu 37ºC selama 10 menit
TCA 0.1 M 0.5 0.5 0.5
Enzim dalam CaCl2 (2 mmol/l) 0.05 0.05
Inkubasi pada suhu 37ºC selama 10 menit, sentrifusi 4000 rpm selama 10 menit
Filtrat 0.375 0.375 0.375
Na2CO3 0.4 M 1.25 1.25 1.25
Pereaksi fenol 0.25 0.25 0.25
Inkubasi pada suhu 37ºC selama 20 menit, absorbansi pada 578 nm
U = x P x
U = unit aktivitas dalam IU per menit Asp = Nilai absorbansi sampel
Abl = Nilai absorbansi blanko
Ast = Nilai absorbansi standar (tirosin) P = Faktor pengenceran
Lampiran 2. Prosedur Analisis Proksimat
1. Jumlah Nitrogen Total Metode Kjeldahl (AOAC, 1999)
Sampel sebanyak 0,2 gram ditimbang dan dipindahkan ke labu kjeldahl. Ditambahkan 1,9 gram K2SO4, 40 mg HgO dan 2,0 ml H2SO4 pekat. Campuran didihkan selama 1,5 jam sampai cairan menjadi jernih. Setelah dingin, ditambahkan akuades sebanyak 5 ml ke dalam labu.
Isi labu dipindahkan ke dalam alat destilasi dan labu dicuci beberapa kali dengan 1-2 ml akuades. Erlenmeyer 125 ml yang berisi 5 ml larutan H2BO3 dan 2 tetes indikator metil merah dan metil blue (perbandingan 0,2 gram : 0,1 gam dalam 100 ml akuades) dipasang dibawah kondensor. Ujung tabung kondensor harus direndam dalann H2BO3 lalu ditambahkan larutan NaOH sebanyak 8 ml. Destilasi dilakukan sampai tertampung kira-kira 15 ml destilat dalam erlenmeyer.
Destilat yang tertampung kemudian dititrasi dengan HCl 0,02 N sampai terjadi perubahan warna menjadi ungu. Hal yang sama dilakukan terhadap blanko. Setelah itu dilakukan perhitungan menggunan rumus sebagai berikut :
( ) 14, 007 100
%N mlHCl mlBlanko xNormalitasx x
mgsampel
2. Kadar air Metode Oven (Fardiaz, et al, 1989)
Cawan dikeringkan dalam oven selama 15 menit 100ºC dan didinginkan selama 5 menit dalam desikator. Cawan ditimbang (a) kemudian dimasukkan x gram sampel dan ditimbang kembali (X). Sampel dikeringkan dalam oven sampai beratnya tetap (6 jam). Setelah diangkat dari oven sampel didinginkan dalam desikator selama 5 menit dan ditimbang (Y).
Lampiran 3. Analisa Hasil Pengambilan Sampel pada Tahap Hidrolisis Tepung Keong Mas
1. Nilai pH (Apriyantono, 1989)
Perubahan nilai pH selama hidrolisis berlangsung diamati dengan mengambil sampel yang telah diinaktivasi. Nilai pH kemudian diukur dengan menggunakan pH meter
2. Derajat Hidrolisis Protein (Rehm dan Reed, 1995)
Derajat hidrolisis protein dapat diketahui melalui pembandingan nilai N-terasimilasi terhadap nilai total nitrogen sampel. Derajat hidrolisis protein diperoleh melalui perhitungan sebagai berikut :
DH(%) = (N-terasimilasi / Ntotal) x 100%
Nilai N-terasimilasi diperoleh dengan menggunakan metode titrasi formol (Gump et al., 1995). Sebanyak 0,5 ml hidrolisat tepung keong diencerkan dengan menggunakan akuades hingga mencapai volume 10 ml. Hasil pengenceran dinetralkan menggunakan larutan NaOH 0,2 N hingga mencapai nilai pH 8,0. Selanjutnya, ke dalam sampel dimasukkan 2 ml formaldehid yang sebelumnya telah dinetralkan menggunakan larutan NaOH 0,2 N hingga pH 8,0. Hasil pencampuran sampel dengan formaldehid dititrasi menggunakan NaOH 0,02 N hingga mencapai pH 8,0. Jumlah produk berupa asam amino dinyatakan dalam bentuk nilai nitrogen terasmilasi yang diperoleh melalui perhitungan menggunakan persamaan sebagai berikut.
N-as = VNaOH (mL) x (0,10 meq OH-/mL) x P x 10 x 14 (mg N/mmol) Keterangan :
Lampiran 4. Prosedur Analisa Asam Amino Menggunakan HPLC phenylisothiocanate (PITC) dan 50 µl (p.a)
c. Buffer Natrium Asetat 1 M pH 5,75 (pelarut A)
19 gram natrium asetat trihidrat ditambah 1000 ml HPLC grade water, kemudian disaring. Selanjutnya ditambah 0,5 ml TEA, kemudian pH diatur mencapai pH 5,75 dengan asam asetat glasial.
d. Larutan Asetonitril 60% (pelarut B)
650 HPLC grade asetonitril disaring dengan penyaring organik, kemudian ditambah 450 ml HPLC HPLC grade water. Selanjutnya 600 ml asetonitril dicampur dengan 400 ml akuades, dan gas dihilangkan dengan penangas sonik selama 15 detik.
2. Persiapan sampel
diencerkan dengan 200 µ l larutan pengencer (natrium asetat 1 M) sehingga diperoleh larutan contoh yang siap dianalisa. Asam mino yang terdeteksi oleh HPLC dihitung menggunakan rumus sebagai berikut :
% Asam amino =
Sampel Berat
FP x BM Standar x i
Konsentras X
Sampel Area
Luas
Standar Area
Luas
Lampiran 5. Pengaruh Konsentrasi Papain terhadap Kadar Protein Hidrolisat [Substrat]
(mg/ml)
[Protein] (mg/ml)
0.2 % papain 0.4 % papain 0.6 % papain
0.11 0.87 ± 0.007 0.75 ± 0.003 0.76 ± 0.003
0.25 7.34 ± 0.035 7.03 ± 0.045 7.38 ± 0.040
0.43 8.99 ± 0.095 8.46 ± 0.060 8.79 ± 0.050
0.67 9.60 ± 0.020 9.98 ± 0.115 10.22 ± 0.015
1.00 11.28 ± 0.065 11.33 ± 0.015 11.14 ± 0.010
Lampiran 6. Pengaruh pH terhadap Kadar Protein Hidrolisat [Substrat]
(mg/ml)
[Protein] (mg/ml)
pH 4.5 pH 5 pH 5.5 pH 6 pH 6.5 pH 7
0.11 0.84 ± 0.002 0.70 ± 0 0.80 ± 0.005 0.70 ± 0.001 0.78 ± 0.001 0.81 ± 0.002
0.25 9.35 ± 0.045 9.28 ± 0.075 9.02 ± 0.005 9.06 ± 0.045 9.16 ± 0.010 8.98 ± 0.035
0.43 10.12 ± 0.035 10.53 ± 0.07 11.05 ± 0.005 10.16 ± 0.015 10.08 ± 0.10 9.85 ± 0.090
0.67 11.04 ± 0.04 11.23 ± 0.01 11.42 ± 0.060 10.83 ± 0.015 10.78 ± 0.025 10.77 ± 0.020
1.00 11.45 ± 0.075 11.30 ± 0.025 11.51 ± 0.040 11.25 ± 0.050 11.19 ± 0.015 11.19 ± 0.035
Lampiran 7. Pengaruh Suhu terhadap Kadar Protein Hidrolisat
[Substrat] (mg/ml) [Protein] (mg/ml)
Suhu 60ºC Suhu 65 ºC Suhu 70 ºC Suhu 75 ºC
0.11 0.66 ± 0 0.70 ± 0.005 0.72 ± 0.006 0.73 ± 0.001
0.25 7.11 ± 0 7.51 ± 0.015 7.86 ± 0.010 8.01 ± 0.105
0.43 7.90 ± 0.080 8.17 ± 0.070 8.54 ± 0.020 9.13 ± 0.045
0.67 8.68 ± 0.040 9.13 ± 0.035 9.54 ± 0.040 10.31 ± 0.015
1.00 9.71 ± 0 9.93 ± 0.015 10.36 ± 0.045 10.37 ± 0.030
Lampiran 8. Nilai Derajat Hidrolisis Waktu
(Jam)
Ulangan Kontrol Perlakuan (pH 5,5 ; Suhu 65 ; papain