SKRIPSI
PENGARUH PERLAKUAN PASSING, KONSENTRASI Na2CO3, DAN
KADAR AIR TERHADAP MUTU FISIK MI BASAH JAGUNG YANG DIBUAT MENGGUNAKAN EKSTRUDER ULIR PEMASAK
Oleh
Eneng Cucun Etikawati F24103003
2007
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
PENGARUH PERLAKUAN PASSING, KONSENTRASI Na2CO3, DAN
KADAR AIR TERHADAP MUTU FISIK MI BASAH JAGUNG YANG DIBUAT MENGGUNAKAN EKSTRUDER ULIR PEMASAK
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN Pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh :
Eneng Cucun Etikawati F24103003
Dilahirkan pada tanggal 11 September 1984 Di Sumedang
Tanggal lulus: September 2007
Menyetujui, Bogor, September 2007
Ir. Subarna, MSi. Ir. Tjahja Muhandri, MT. Dosen Pembimbing I Dosen Pembimbing II
Mengetahui,
Eneng Cucun Etikawati. F 24103003. Pengaruh Perlakuan Passing, Konsentrasi Na2CO3, dan Kadar Air Terhadap Mutu Fisik Mi basah Jagung yang Dibuat
Menggunakan Ekstruder Ulir Pemasak. Di bawah bimbingan Ir. Subarna, MSi. dan Ir. Tjahja Muhandri, MT.
RINGKASAN
Pada penelitian ini dilakukan pembuatan mi basah jagung menggunakan ekstruder ulir tipe pemasak. Dalam ekstruder ulir tipe pemasak ini, adonan mengalami pemasakan dan pembentukan menjadi untaian mi yang panjang. Pembuatan mi jagung dengan teknik ekstrusi memiliki kelebihan yaitu proses lebih sederhana karena tidak memerlukan tahapan proses pengukusan pertama, pengulian, dan pembentukan lembaran serta dapat dilakukan dalam waktu yang relatif singkat.
Tujuan dari penelitian ini adalah untuk mempelajari pengaruh passing, kadar air, dan kadar Na2CO3 terhadap karakteristik fisik mi basah jagung. Manfaat
yang diharapkan dari penelitian ini adalah hasil penelitian ini dapat dijadikan acuan dalam aplikasi pembuatan mi basah jagung menggunakan ekstruder pemasak dan pembentuk.
Penelitian ini dilakukan dengan tahapan karakterisasi tepung jagung dan tahapan kajian pembuatan mi basah jagung. Penepungan jagung dilakukan dengan metode penggilingan semi basah menggunakan alat penggiling disc mill. Variabel perlakuan yang diterapkan pada penelitian ini yaitu perlakuan kadar air (70%, 75%, dan 80%), kadar Na2CO3 (0%, 0.3%, dan 0.6%), serta passing (1, 2, dan 3)
dalam pembuatan mi basah jagung.
Pembuatan mi basah jagung diawali dengan pencampuran tepung jagung kering, Na2CO3 yang jumlahnya 0%, 0.3%, 0.6%, dan air yang jumlahnya 70 %,
75%, dan 80 % berdasarkan berat kering. Campuran ini kemudian dimasukan ke dalam ekstruder dengan mengatur suhu dan kecepatan ekstruder. Suhu yang digunakan adalah 900C dan kecepatan ulir yang digunakan adalah 130 rpm. Hal ini didasarkan pada penelitian Fahmi (2007).
Adonan yang mengalami pemasakan dan gelatinisasi dalam ekstruder, kemudian dicetak menjadi untaian mi saat keluar melalui die ekstruder dengan ukuran diameter die 2.5 mm. Untaian mi yang telah diperoleh harus dimatangkan lebih lanjut dengan cara perebusan selama 3 menit. Analisis sifat fisik yang dilakukan pada penelitian ini meliputi analisis derajat gelatinisasi, warna, persen elongasi, tensile strength, kekerasan, kelengketan, kekenyalan, dan kehilangan padatan akibat pemasakan.
Hasil analisis proksimat tepung jagung P-21 menunjukkan bahwa tepung jagung yang dihasilkan mengandung air 5.46%, protein 6.32%, lemak 1.73%, abu 0.31%, karbohidrat 86.18%, amilosa 23.04%, amilopektin 43.52%, dan total pati 66.56%. nilai derajat L tepung jagung yang dihasilkan adalah sebesar 86.20. Ini berarti bahwa tepung jagung P-21 memiliki warna yang cerah. Sedangkan nilai
0
Hue adalah sebesar 82.65 yang berarti warna tepung jagung yang dihasilkan adalah kuning kemerahan.
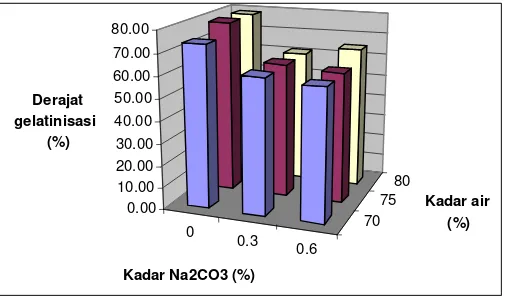
Derajat gelatinisasi cenderung meningkat dengan meningkatnya passing dan kadar air. Sedangkan peningkatan kadar Na2CO3 cenderung menurunkan
Kecerahan mi basah jagung cenderung meningkat dengan peningkatan passing, sedangkan peningkatan kadar Na2CO3 cenderung menurunkan kecerahan mi
basah jagung. Kekerasan cenderung menurun dengan meningkatnya passing dan kadar Na2CO3. Kelengketan cenderung menurun dengan meningkatnya passing
dan meningkat dengan meningkatnya kadar Na2CO3. Elongasi mi basah jagung
cenderung meningkat dengan meningkatnya passing. Tensile strength cenderung menurun dengan meningkatnya kadar air. Peningkatan kadar Na2CO3 cenderung
RIWAYAT HIDUP
Penulis bernama Eneng Cucun Etikawati dilahirkan pada tanggal 11 September 1984 di Sumedang dan merupakan anak kedua dari dua bersaudara pasangan Talim Halim dan Atik Atikah. Penulis menempuh pendidikan kanak-kanak di TK Bakti Pertiwi (1989-1991), pendidikan dasar di SDN Panyingkiran II (1991-1997), pendidikan menengah pertama di SLTPN 1 Sumedang (1997-2000), dan pendidikan lanjutan di SMUN 1 Sumedang (2000-2003).
Penulis diterima di Departemen Ilmu dan Teknologi Pangan Insitut Pertanian Bogor pada tahun 2003 melalui jalur USMI. Selama menempuh pendidikan di IPB penulis pernah menjadi panitia Konferensi I HMPPI (Himpunan Mahasiswa Peduli Pangan Indonesia) dan panitia LCTIP (Lomba Cepat Tepat Ilmu Pangan) XIII. Sebagai tugas akhir, penulis melakukan penelitian yang berjudul “Pengaruh Perlakuan Passing, Konsentrasi Na2CO3, dan Kadar Air
KATA PENGANTAR
Penulis mengucapkan syukur dan terima kasih kepada Allah SWT atas rahmat, karunia, serta berkah-Nya yang telah diberikan kepada penulis sehingga penulis dapat menyelesaikan penelitian yang berjudul “Pengaruh Perlakuan Passing, Konsentrasi Na2CO3, dan Kadar Air Terhadap Mutu Fisik dan Sensori
Mi basah Jagung yang Dibuat Menggunakan Ekstruder Ulir Pemasak”. Shalawat dan Salam semoga selalu tercurahkan kepada Nabi Besar Muhammad, SAW.
Pada kesempatan ini, perkenankanlah penulis mengucapkan terima kasih kepada pihak-pihak yang telah membantu, mendukung, serta membimbing penulis baik secara langsung maupun tidak langsung hingga skripsi ini selesai ditulis, terutama kepada :
1. Mamah dan Apa atas doa, kasih sayang, nasihat, dorongan dan motivasi yang dicurahkan tiada henti.
2. Ir. Subarna, M.Si. selaku Dosen Pembimbing I yang selalu sabar dan bijaksana dalam membimbing dan mendukung penulis.
3. Ir. Tjahja Muhandri, MT. selaku Dosen Pembimbing II yang telah mendanai penelitian ini serta membimbing penulis dengan penuh kesabaran.
4. Dr. Ir. Sukarno MSc. atas kesediaan untuk menjadi dosen penguji.
5. Seluruh dosen dan staf Departemen Ilmu dan Teknologi Pangan yang telah memberikan ilmu dan mendukung kemajuan penulis.
6. Aa, Teh Eneng dan seluruh keluarga atas doa, kasih sayang, nasihat, dorongan dan motivasi.
7. Harri Sapto Wijaya atas kasih sayang dan dorongan yang diberikan. 8. Partner penelitian : Susi dan Erik atas bantuan ilmu, tenaga, dan waktu. 9. Idham atas bantuannya mengurus alat-alat lab.
10.Reza atas pinjaman lokernya.
12.Teman-teman terbaikku : Vina, Tilo, Nooy, Primuz, Lichan, Ekuz, Jengjeng, Mba’ Lina dan Lasty. Kalian membuat hari–hariku penuh dengan canda tawa.
13.Teman-teman ITP 40 lainnya Mba’ Asih, Maya, Yoga, Nchuz, Gilang, Angel, Tathan, Mae, Gading, Herher, Hayhay, Dhani dan semuanya yang tak dapat disebutkan satu per satu. Banyak kenangan indah yang terukir bersama kalian.
14.Teman-teman kost WINDY lainnya : Ikong, Dewong, Lestong, Endang, Ruby, Mba’ Nur, Maya, Sarong, Femi, Dhia, dan Angga. Terima kasih atas dorongan semangat dan keceriaan yang diberikan.
15.Bu Rubiyah, Pak Sobirin, Pak Wahid, Teh Ida, Pak Gatot, Pak Yahya, Mas Edi, Pak Rojak, Pak Iyas, Pak Nur, Pak Koko dan semua laboran di laboratorium ITP lainnya atas bantuan dan kerjasamanya.
16.Seluruh pustakawan dan pustakawati di PAU, PITP, dan LSI yang telah membantu penulis dalam mencari literatur.
Penulis menyadari masih banyak kekurangan dalam skripsi ini, oleh sebab itu masukan dan kritik yang membangun selalu penulis tunggu. Semoga skripsi ini bermanfaat bagi pihak-pihak yang membutuhkan.
Bogor, September 2007
DAFTAR ISI
Halaman
DAFTAR ISI ... i
DAFTAR TABEL ... iv
DAFTAR GAMBAR ... vi
DAFTAR LAMPIRAN ... viii
I PENDAHULUAN ... 1
A. Latar Belakang ... 1
B. Tujuan ... 3
C. Manfaat ... 3
II. TINJAUAN PUSTAKA ... 4
A. Jagung ... 4
1. Jenis Jagung ... 4
2. Morfologi Jagung ... 5
3. Anatomi Biji Jagung ... 6
4. Komposisi Kimia Biji Jagung ... 8
B. Proses Penepungan Jagung ... 10
C. Pati Jagung ... 11
1. Amilosa ... 12
2. Amilopektin ... 13
3. Granula Pati ... 13
D. Gelatinisasi ... 14
1. Konsep dan Mekanisme Gelatinisasi ... 14
2. Suhu Gelatinisasi ... 15
3. Sifat Birefringence ... 16
E. Ekstrusi ... 17
1. Ekstruder ... 17
2. Proses Ekstrusi ... 19
3. Ekstrusi Pasta ... 20
1. Definisi Mi Basah ... 20
2. Penggunaan Alkali Pada Mi ... 21
G. Mi Jagung ... 23
III. METODOLOGI PENELITIAN ... 25
A. Bahan dan Alat ... 25
B. Metodologi ... 25
1. Tahapan Penelitian ... 26
a. Karakterisasi Tepung Jagung ... 26
b. Kajian Pembuatan Mi Basah Jagung ... 27
2. Rancangan Percobaan ... 30
3. Pengamatan ... 31
a. Analisis Kimia ... 31
a.1. Analisis Kadar Air ... 31
a.2. Analisis Kadar Abu ... 31
a.3. Analisis Kadar Lemak ... 32
a.4. Analisis Kadar Protein ... 32
a.5. Analisis Kadar Karbohidrat ... 33
a.6. Analisis Total Pati ... 33
a.7. Analisis Kadar Amilosa ... 34
a.8. Analisis Kadar Amilopektin ... 35
b. Analisis Fisik ... 35
b.1. Analisis Warna ... 35
b.2. Analisis Tekstur ... 35
b.3. Analisis Persen Elongasi ... 36
b.4. Pengukuran Kehilangan Padatan Akibat Pemasakan... 37
b.5. Pengukuran Derajat Gelatinisasi ... 37
IV. HASIL DAN PEMBAHASAN ... 39
A. Karakterisasi Tepung Jagung ... 39.
1. Komposisi Kimia Tepung Jagung P-21 ... 40
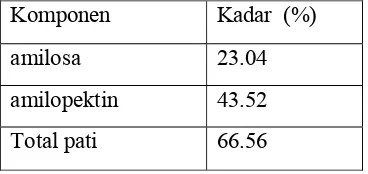
2. Total Pati, Amilosa, dan Amilopektin ... 41
3. Warna Tepung Jagung P-21 ... 42
C. Analisis Sifat Fisik Mi Basah Jagung ... 44
1. Derajat Gelatinisasi ... 44
2. Warna Mi Basah Jagung ... 46
3. Kekerasan Mi Basah Jagung ... 49
4. Kelengketan Mi Basah Jagung ... 52
5. Kekenyalan Mi Basah Jagung ... 55
6. Persen Elongasi ... 57
7. Tensile Strength ... 60
8. Kehilangan Padatan Akibat Pemasakan ... 62
V. KESIMPULAN DAN SARAN ... 66
A. Kesimpulan ... 66
B. Saran ... 67
DAFTAR PUSTAKA ... 68
SKRIPSI
PENGARUH PERLAKUAN PASSING, KONSENTRASI Na2CO3, DAN
KADAR AIR TERHADAP MUTU FISIK MI BASAH JAGUNG YANG DIBUAT MENGGUNAKAN EKSTRUDER ULIR PEMASAK
Oleh
Eneng Cucun Etikawati F24103003
2007
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
PENGARUH PERLAKUAN PASSING, KONSENTRASI Na2CO3, DAN
KADAR AIR TERHADAP MUTU FISIK MI BASAH JAGUNG YANG DIBUAT MENGGUNAKAN EKSTRUDER ULIR PEMASAK
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN Pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh :
Eneng Cucun Etikawati F24103003
Dilahirkan pada tanggal 11 September 1984 Di Sumedang
Tanggal lulus: September 2007
Menyetujui, Bogor, September 2007
Ir. Subarna, MSi. Ir. Tjahja Muhandri, MT. Dosen Pembimbing I Dosen Pembimbing II
Mengetahui,
Eneng Cucun Etikawati. F 24103003. Pengaruh Perlakuan Passing, Konsentrasi Na2CO3, dan Kadar Air Terhadap Mutu Fisik Mi basah Jagung yang Dibuat
Menggunakan Ekstruder Ulir Pemasak. Di bawah bimbingan Ir. Subarna, MSi. dan Ir. Tjahja Muhandri, MT.
RINGKASAN
Pada penelitian ini dilakukan pembuatan mi basah jagung menggunakan ekstruder ulir tipe pemasak. Dalam ekstruder ulir tipe pemasak ini, adonan mengalami pemasakan dan pembentukan menjadi untaian mi yang panjang. Pembuatan mi jagung dengan teknik ekstrusi memiliki kelebihan yaitu proses lebih sederhana karena tidak memerlukan tahapan proses pengukusan pertama, pengulian, dan pembentukan lembaran serta dapat dilakukan dalam waktu yang relatif singkat.
Tujuan dari penelitian ini adalah untuk mempelajari pengaruh passing, kadar air, dan kadar Na2CO3 terhadap karakteristik fisik mi basah jagung. Manfaat
yang diharapkan dari penelitian ini adalah hasil penelitian ini dapat dijadikan acuan dalam aplikasi pembuatan mi basah jagung menggunakan ekstruder pemasak dan pembentuk.
Penelitian ini dilakukan dengan tahapan karakterisasi tepung jagung dan tahapan kajian pembuatan mi basah jagung. Penepungan jagung dilakukan dengan metode penggilingan semi basah menggunakan alat penggiling disc mill. Variabel perlakuan yang diterapkan pada penelitian ini yaitu perlakuan kadar air (70%, 75%, dan 80%), kadar Na2CO3 (0%, 0.3%, dan 0.6%), serta passing (1, 2, dan 3)
dalam pembuatan mi basah jagung.
Pembuatan mi basah jagung diawali dengan pencampuran tepung jagung kering, Na2CO3 yang jumlahnya 0%, 0.3%, 0.6%, dan air yang jumlahnya 70 %,
75%, dan 80 % berdasarkan berat kering. Campuran ini kemudian dimasukan ke dalam ekstruder dengan mengatur suhu dan kecepatan ekstruder. Suhu yang digunakan adalah 900C dan kecepatan ulir yang digunakan adalah 130 rpm. Hal ini didasarkan pada penelitian Fahmi (2007).
Adonan yang mengalami pemasakan dan gelatinisasi dalam ekstruder, kemudian dicetak menjadi untaian mi saat keluar melalui die ekstruder dengan ukuran diameter die 2.5 mm. Untaian mi yang telah diperoleh harus dimatangkan lebih lanjut dengan cara perebusan selama 3 menit. Analisis sifat fisik yang dilakukan pada penelitian ini meliputi analisis derajat gelatinisasi, warna, persen elongasi, tensile strength, kekerasan, kelengketan, kekenyalan, dan kehilangan padatan akibat pemasakan.
Hasil analisis proksimat tepung jagung P-21 menunjukkan bahwa tepung jagung yang dihasilkan mengandung air 5.46%, protein 6.32%, lemak 1.73%, abu 0.31%, karbohidrat 86.18%, amilosa 23.04%, amilopektin 43.52%, dan total pati 66.56%. nilai derajat L tepung jagung yang dihasilkan adalah sebesar 86.20. Ini berarti bahwa tepung jagung P-21 memiliki warna yang cerah. Sedangkan nilai
0
Hue adalah sebesar 82.65 yang berarti warna tepung jagung yang dihasilkan adalah kuning kemerahan.
Derajat gelatinisasi cenderung meningkat dengan meningkatnya passing dan kadar air. Sedangkan peningkatan kadar Na2CO3 cenderung menurunkan
Kecerahan mi basah jagung cenderung meningkat dengan peningkatan passing, sedangkan peningkatan kadar Na2CO3 cenderung menurunkan kecerahan mi
basah jagung. Kekerasan cenderung menurun dengan meningkatnya passing dan kadar Na2CO3. Kelengketan cenderung menurun dengan meningkatnya passing
dan meningkat dengan meningkatnya kadar Na2CO3. Elongasi mi basah jagung
cenderung meningkat dengan meningkatnya passing. Tensile strength cenderung menurun dengan meningkatnya kadar air. Peningkatan kadar Na2CO3 cenderung
RIWAYAT HIDUP
Penulis bernama Eneng Cucun Etikawati dilahirkan pada tanggal 11 September 1984 di Sumedang dan merupakan anak kedua dari dua bersaudara pasangan Talim Halim dan Atik Atikah. Penulis menempuh pendidikan kanak-kanak di TK Bakti Pertiwi (1989-1991), pendidikan dasar di SDN Panyingkiran II (1991-1997), pendidikan menengah pertama di SLTPN 1 Sumedang (1997-2000), dan pendidikan lanjutan di SMUN 1 Sumedang (2000-2003).
Penulis diterima di Departemen Ilmu dan Teknologi Pangan Insitut Pertanian Bogor pada tahun 2003 melalui jalur USMI. Selama menempuh pendidikan di IPB penulis pernah menjadi panitia Konferensi I HMPPI (Himpunan Mahasiswa Peduli Pangan Indonesia) dan panitia LCTIP (Lomba Cepat Tepat Ilmu Pangan) XIII. Sebagai tugas akhir, penulis melakukan penelitian yang berjudul “Pengaruh Perlakuan Passing, Konsentrasi Na2CO3, dan Kadar Air
KATA PENGANTAR
Penulis mengucapkan syukur dan terima kasih kepada Allah SWT atas rahmat, karunia, serta berkah-Nya yang telah diberikan kepada penulis sehingga penulis dapat menyelesaikan penelitian yang berjudul “Pengaruh Perlakuan Passing, Konsentrasi Na2CO3, dan Kadar Air Terhadap Mutu Fisik dan Sensori
Mi basah Jagung yang Dibuat Menggunakan Ekstruder Ulir Pemasak”. Shalawat dan Salam semoga selalu tercurahkan kepada Nabi Besar Muhammad, SAW.
Pada kesempatan ini, perkenankanlah penulis mengucapkan terima kasih kepada pihak-pihak yang telah membantu, mendukung, serta membimbing penulis baik secara langsung maupun tidak langsung hingga skripsi ini selesai ditulis, terutama kepada :
1. Mamah dan Apa atas doa, kasih sayang, nasihat, dorongan dan motivasi yang dicurahkan tiada henti.
2. Ir. Subarna, M.Si. selaku Dosen Pembimbing I yang selalu sabar dan bijaksana dalam membimbing dan mendukung penulis.
3. Ir. Tjahja Muhandri, MT. selaku Dosen Pembimbing II yang telah mendanai penelitian ini serta membimbing penulis dengan penuh kesabaran.
4. Dr. Ir. Sukarno MSc. atas kesediaan untuk menjadi dosen penguji.
5. Seluruh dosen dan staf Departemen Ilmu dan Teknologi Pangan yang telah memberikan ilmu dan mendukung kemajuan penulis.
6. Aa, Teh Eneng dan seluruh keluarga atas doa, kasih sayang, nasihat, dorongan dan motivasi.
7. Harri Sapto Wijaya atas kasih sayang dan dorongan yang diberikan. 8. Partner penelitian : Susi dan Erik atas bantuan ilmu, tenaga, dan waktu. 9. Idham atas bantuannya mengurus alat-alat lab.
10.Reza atas pinjaman lokernya.
12.Teman-teman terbaikku : Vina, Tilo, Nooy, Primuz, Lichan, Ekuz, Jengjeng, Mba’ Lina dan Lasty. Kalian membuat hari–hariku penuh dengan canda tawa.
13.Teman-teman ITP 40 lainnya Mba’ Asih, Maya, Yoga, Nchuz, Gilang, Angel, Tathan, Mae, Gading, Herher, Hayhay, Dhani dan semuanya yang tak dapat disebutkan satu per satu. Banyak kenangan indah yang terukir bersama kalian.
14.Teman-teman kost WINDY lainnya : Ikong, Dewong, Lestong, Endang, Ruby, Mba’ Nur, Maya, Sarong, Femi, Dhia, dan Angga. Terima kasih atas dorongan semangat dan keceriaan yang diberikan.
15.Bu Rubiyah, Pak Sobirin, Pak Wahid, Teh Ida, Pak Gatot, Pak Yahya, Mas Edi, Pak Rojak, Pak Iyas, Pak Nur, Pak Koko dan semua laboran di laboratorium ITP lainnya atas bantuan dan kerjasamanya.
16.Seluruh pustakawan dan pustakawati di PAU, PITP, dan LSI yang telah membantu penulis dalam mencari literatur.
Penulis menyadari masih banyak kekurangan dalam skripsi ini, oleh sebab itu masukan dan kritik yang membangun selalu penulis tunggu. Semoga skripsi ini bermanfaat bagi pihak-pihak yang membutuhkan.
Bogor, September 2007
DAFTAR ISI
Halaman
DAFTAR ISI ... i
DAFTAR TABEL ... iv
DAFTAR GAMBAR ... vi
DAFTAR LAMPIRAN ... viii
I PENDAHULUAN ... 1
A. Latar Belakang ... 1
B. Tujuan ... 3
C. Manfaat ... 3
II. TINJAUAN PUSTAKA ... 4
A. Jagung ... 4
1. Jenis Jagung ... 4
2. Morfologi Jagung ... 5
3. Anatomi Biji Jagung ... 6
4. Komposisi Kimia Biji Jagung ... 8
B. Proses Penepungan Jagung ... 10
C. Pati Jagung ... 11
1. Amilosa ... 12
2. Amilopektin ... 13
3. Granula Pati ... 13
D. Gelatinisasi ... 14
1. Konsep dan Mekanisme Gelatinisasi ... 14
2. Suhu Gelatinisasi ... 15
3. Sifat Birefringence ... 16
E. Ekstrusi ... 17
1. Ekstruder ... 17
2. Proses Ekstrusi ... 19
3. Ekstrusi Pasta ... 20
1. Definisi Mi Basah ... 20
2. Penggunaan Alkali Pada Mi ... 21
G. Mi Jagung ... 23
III. METODOLOGI PENELITIAN ... 25
A. Bahan dan Alat ... 25
B. Metodologi ... 25
1. Tahapan Penelitian ... 26
a. Karakterisasi Tepung Jagung ... 26
b. Kajian Pembuatan Mi Basah Jagung ... 27
2. Rancangan Percobaan ... 30
3. Pengamatan ... 31
a. Analisis Kimia ... 31
a.1. Analisis Kadar Air ... 31
a.2. Analisis Kadar Abu ... 31
a.3. Analisis Kadar Lemak ... 32
a.4. Analisis Kadar Protein ... 32
a.5. Analisis Kadar Karbohidrat ... 33
a.6. Analisis Total Pati ... 33
a.7. Analisis Kadar Amilosa ... 34
a.8. Analisis Kadar Amilopektin ... 35
b. Analisis Fisik ... 35
b.1. Analisis Warna ... 35
b.2. Analisis Tekstur ... 35
b.3. Analisis Persen Elongasi ... 36
b.4. Pengukuran Kehilangan Padatan Akibat Pemasakan... 37
b.5. Pengukuran Derajat Gelatinisasi ... 37
IV. HASIL DAN PEMBAHASAN ... 39
A. Karakterisasi Tepung Jagung ... 39.
1. Komposisi Kimia Tepung Jagung P-21 ... 40
2. Total Pati, Amilosa, dan Amilopektin ... 41
3. Warna Tepung Jagung P-21 ... 42
C. Analisis Sifat Fisik Mi Basah Jagung ... 44
1. Derajat Gelatinisasi ... 44
2. Warna Mi Basah Jagung ... 46
3. Kekerasan Mi Basah Jagung ... 49
4. Kelengketan Mi Basah Jagung ... 52
5. Kekenyalan Mi Basah Jagung ... 55
6. Persen Elongasi ... 57
7. Tensile Strength ... 60
8. Kehilangan Padatan Akibat Pemasakan ... 62
V. KESIMPULAN DAN SARAN ... 66
A. Kesimpulan ... 66
B. Saran ... 67
DAFTAR PUSTAKA ... 68
DAFTAR TABEL
Halaman
1. Bagian-bagian anatomi biji jagung ... 6
2. Komposisi kimia biji jagung ... 8
3. Jumlah protein di dalam endosperma pada jagung normal dan varietas opaque-2 ... 9
4. Jumlah mineral pada biji jagung ... 10
5. Suhu gelatinisasi beberapa jenis pati ... 15
6. Klasifikasi ekstruder ulir tunggal ... 18
7. Syarat mutu mi basah ... 21
8. Hasil analisis proksimat tepung jagung Pioneer 21 ... 41
9. Kadar pati, amilosa, dan amilopektin tepung jagung Pioneer 21 ... 41
10.Pengaruh interaksi kadar Na2CO3 (%) dan kadar air (%) terhadap Derajat gelatinisasi mi basah jagung ... 45
11.Pengaruh interaksi kadar Na2CO3 (%) dan kadar air (%) terhadap kecerahan mi basah jagung ... 47
12.Pengaruh interaksi kadar Na2CO3 (%) dan passing terhadap kecerahan mi basah jagung ... 48
13.Pengaruh interaksi kadar Na2CO3 (%) dan kadar air (%) terhadap kekerasan mi basah jagung ... 50
14.Pengaruh interaksi kadar air (%) dan passing terhadap kekerasan mi basah jagung ... 51
15.Pengaruh interaksi kadar Na2CO3 (%), kadar air (%), dan passing terhadap kelengketan mi basah jagung ... 52
16.Pengaruh interaksi kadar Na2CO3 (%), kadar air (%), dan passing terhadap kekenyalan mi basah jagung ... 55
terhadap elongasi mi basah jagung ... 58 19.Pengaruh interaksi kadar air (%) dan passing
terhadap elongasi mi basah jagung ... 59 20.Pengaruh interaksi kadar Na2CO3 (%), kadar air (%), dan passing
terhadap tensile strength mi basah jagung ... 61 21.Pengaruh interaksi kadar Na2CO3 (%), kadar air (%), dan passing
DAFTAR GAMBAR
Halaman
1. Bentuk jagung dari beberapa jenis jagung ... 4 2. Struktur biji jagung ... 7 3. Mekanisme gelatinisasi pati ... 15 4. Bagian-bagian penting alat ekstruder ulir tunggal ... 19 5. Ekstruder tipe LE25-30/C ... 25 6. Diagram alir proses penyiapan tepung ... 26 7. Diagram proses pembuatan mi basah jagung ... 28 8. Diagram prosedur perhitungan waktu ... 29 9. Kurva profil tekstur mi ... 36 10.Tepung jagung P-21 ... 40 11.Mi basah jagung ... 44 12. Histogram pengaruh interaksi kadar Na2CO3 (%) dan kadar
air (%) terhadap derajat gelatinisasi mi basah jagung ... 45 13. Histogram pengaruh passing terhadap derajat gelatinisasi mi basah jagung ... 46 14. Histogram pengaruh interaksi kadar Na2CO3 (%) dan
kadar air (%) terhadap kecerahan mi basah jagung ... 47 15. Histogram pengaruh interaksi kadar Na2CO3 (%) dan passing terhadap
kecerahan mi basah jagung ... 49 16 Histogram pengaruh interaksi kadar Na2CO3 (%) dan
kadar air (%) terhadap kekerasan mi basah jagung... 50 17. Histogram pengaruh interaksi kadar air (%) dan passing terhadap
kekerasan mi basah jagung ... 51 18. Histogram pengaruh interaksi kadar Na2CO3 (%) dan kadar air (%)
terhadap elongasi mi basah jagung ... 57 19. Histogram pengaruh interaksi kadar Na2CO3 (%) dan passing
20. Histogram pengaruh interaksi kadar air (%) dan passing
DAFTAR LAMPIRAN
Halaman
1. Hasil pengukuran karakteristik fisik mi basah jagung ... 72 2. Hasil pengukuran warna mi basah jagung ... 76 3. Hasil analisis ragam dan uji lanjut Duncan terhadap derajat
gelatinisasi mi basah jagung ... 77 4. Hasil analisis ragam dan uji lanjut Duncan terhadap derajat
gelatinisasi mi basah jagung ... 80 5. Hasil analisis ragam dan uji lanjut Duncan terhadap kekerasan
mi basah jagung... ... 83 6. Hasil analisis ragam dan uji lanjut Duncan terhadap kelengketan mi basah jagung ... 86 7. Hasil analisis ragam dan uji lanjut Duncan terhadap elongasi
mi basah jagung ... 92 8. Hasil analisis ragam dan uji lanjut Duncan terhadap kekenyalan
mi basah jagung ... 95 9. Hasil analisis ragam dan uji lanjut Duncan terhadap tensile strength mi basah jagung ... 99 10.Hasil analisis ragam dan uji lanjut Duncan terhadap KPAP
I. PENDAHULUAN
A. Latar Belakang
Upaya penganekaragaman pangan dilakukan melalui pengembangan pangan lokal, baik mutu maupun keragamannya. Upaya diversifikasi pangan pokok sangat perlu karena konsumsi beras per kapita Indonesia yang sangat besar. Data BPS menyebutkan produksi beras tahun 2005 sebesar 32,22 juta ton dan konsumsi per kapita sebesar 136,3 kg/tahun. Untuk mencukupi 219 juta jiwa penduduk diperlukan beras sejumlah 29,97 juta ton. Ditambah kebutuhan lain seperti industri makanan, hotel, dan restoran yang diperkirakan 2,9 juta ton, maka total kebutuhan mencapai 32,87 juta ton, sehingga terjadi kekurangan beras sebesar 650 ribu ton. Masyarakat Indonesia terlalu tergantung pada beras, padahal pertumbuhan produksi beras hanya 1,5 persen per tahun, tidak mencukupi untuk mengimbangi pertumbuhan penduduk Indonesia. Karena itu tahun 2005 lalu impor beras nasional mencapai 1,2 juta ton (Anonimb, 2006).
Perlu adanya komitmen nasional untuk mengurangi ketergantungan karbohidrat yang bersumber dari beras. Sektor swasta pun memiliki peran yang cukup besar dalam mengajari masyarakat mendiversifikasi kebutuhan karbohidrat yang tidak semata–mata bersumber pada beras. Dengan kemajuan teknologi yang ada sekarang, sebenarnya bisa dibuat aneka produk berbasis sumber karbohidrat dalam skala industri. Italia punya pengalaman dengan menu yang bahan utamanya dari jagung, singkong, ubi jalar, dan pisang jenis plantain (bukan pisang buah) yang sangat digemari masyarakat (Hariyadi et al., 2003). Ini yang harus dikembangkan melalui pengolahan yang memenuhi standar industri sehingga bisa dibuat secara masal, bergengsi, dan murah.
disajikan dengan praktis, dan dapat memenuhi selera sebagian besar masyarakat baik orang dewasa maupun anak–anak. Selain itu jenis makanan dari mi sangat bervariasi dan mudah dijumpai di tempat–tempat penjual makanan.
Berbagai teknik pembuatan mi jagung telah dikembangkan dan secara umum dapat dikelompokkan menjadi tiga, yaitu : (1) teknik pembuatan mi jagung dengan calendering dan slitting atau modifikasi teknik mi terigu (Budiyah, 2004), (2) teknik pembuatan mi jagung dengan ekstrusi piston atau ram (Subarna dkk, 1999), dan (3) teknik pembuatan mi dengan sistem ekstrusi ulir (Waniska et al., 2000). Ketiga teknik pembuatan mi tersebut melalui tahap pemasakan terlebih dahulu. Teknik yang dikembangkan oleh Budiyah memiliki kelebihan utama dalam produksi massal yaitu peralatan dan mesin yang telah siap. Namun, kelemahan dari teknik ini adalah waktu pengolahan yang lama karena terdiri dari tahapan proses pencampuran bahan, pengukusan pertama, pengulian, pembentukan lembaran, pemotongan, perebusan, perendaman dalam air dingin, dan pelumuran mi dengan minyak.
Teknik ekstrusi pada bahan pangan merupakan perkembangan dari ekstrusi tipe ram atau piston yang digunakan pertama kali pada industri sosis dan pengolahan daging (Harper, 1981). Ekstruder yang digunakan dalam pembuatan mi jagung pada penelitian ini adalah ekstruder ulir tipe pemasak. Pada ekstruder tipe pemasak ini, adonan mengalami pemasakan dan pembentukan menjadi untaian mi yang panjang. Pembuatan mi jagung dengan teknik ekstrusi memiliki kelebihan yaitu proses lebih sederhana karena tidak memerlukan tahapan proses pengukusan pertama, pengulian, dan pembentukan lembaran serta dapat dilakukan dalam waktu yang relatif singkat.
Namun, permasalahan pembuatan mi basah jagung menggunakan teknik ekstrusi adalah belum diketahui formula mi dan kondisi operasi yang tepat untuk menghasilkan mi dengan mutu yang baik. Oleh karena itu, untuk menghasilkan mi dengan mutu yang baik, diperlukan penelitian lebih lanjut mengenai formula mi jagung dan kondisi operasi yang tepat.
B. Tujuan
Mempelajari pengaruh passing, kadar air, dan kadar Na2CO3 terhadap
karakteristik fisik mi basah jagung.
C. Manfaat
II. TINJAUAN PUSTAKA
A. Jagung
1. Jenis jagung
Tanaman jagung (Zea mays L.) merupakan salah satu tanaman biji–bijian dari keluarga rumput–rumputan (Graminae). Tanaman ini awalnya berasal dari Amerika dan merupakan tanaman yang penting di benua tersebut. Menurut sejarahnya, tanaman jagung ini kemudian menyebar ke daerah subtropis dan tropis. Berdasarkan karakter bijinya, jagung dapat dibagi menjadi beberapa jenis yaitu tipe dent, flint, sweet, flour, popcorn, waxy, dan podcorn (Jugenheimer, 1976).
Gambar 1. Bentuk jagung dari beberapa jenis jagung: kiri ke kanan: flint, dent, dan yellow flour. (sumber: Anonima, 2005)
endosperma bening, kulit biji tipis, mengandung sedikit pati, dan pada waktu masak biji mengkerut. Tipe flour mengandung banyak pati yang lunak dan mudah dibuat tepung, merupakan jenis jagung yang paling tua dan telah ditemukan pada zaman Aztec dan Inca. Popcorn memiliki kandungan pati yang lebih sedikit daripada flint. Tipe ini banyak dikonsumsi sebagai jagung pop. Tipe waxy memiliki penampakkan biji seperti berlilin, mengandung 78 % amilopektin dan 22 % amilosa. Yang terakhir adalah tipe podcorn. Tipe ini berbeda dengan jagung pada umumnya. Bijinya diselubungi oleh kelobot dan tipe ini tidak digunakan secara komersil (Jugenheimer, 1976).
Menurut Suprapto dan Marzuki (2005), jagung yang banyak ditanam di Indonesia adalah tipe mutiara (flint) dan setengah mutiara (semiflint), seperti jagung Arjuna, (mutiara), jagung Harapan (setengah mutiara), Pioneer-2 (setengah mutiara), Hibrida C-1 (setengah mutiara), dan lain–lain. Selain jagung tipe mutiara dan setengah mutiara, di Indonesia juga terdapat jagung tipe berondong (pop corn), jagung gigi kuda (dent corn), dan jagung manis (sweet corn).
2. Morfologi Jagung
Biji jagung merupakan biji sereal yang paling besar, dengan berat masing–masing 250–300 mg. Biji jagung berbentuk bulat dan menempel pada tongkol jagung. Warna biji jagung bervariasi dari putih, kuning, merah, ungu, sampai hitam. Jagung lengkap terdiri dari kelobot, tongkol jagung, biji jagung, dan rambut (Efendi dan Sulistiati, 1991).
Kelobot merupakan daun buah atau kelopak yang berguna sebagai pembungkus dan pelindung biji jagung. Jumlah kelobot dalam tongkol jagumg umumnya berjumlah 12–15 lembar. Semakin tua umur jagung, semakin kering kelobotnya (Efendi dan Sulistiati, 1991).
Rambut merupakan tangkai putik yang sangat panjang yang keluar ke ujung kelobot melalui sela–sela deret biji. Rambut merupakan cabang– cabang yang sangat halus sehingga mampu menangkap tepung sari pada saat pembuahan (Efendi dan Sulistiati, 1991).
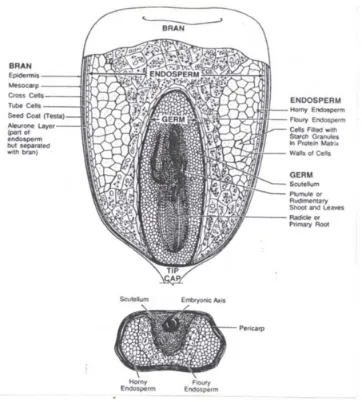
3. Anatomi Biji Jagung
[image:31.612.167.355.267.371.2]Menurut (Inglett, 1970), biji jagung dibagi menjadi empat bagian yaitu kulit (perikarp), endosperma, lembaga, dan tudung pangkal (tip cap). Bagian–bagian anatomi jagung terdapat pada Tabel 1.
Tabel 1. Bagian–bagian anatomi biji jagung Bagian anatomi Jumlah (%) Endosperma
Lembaga Kulit (perikarp) Tip cap
82,3 11,5 5,3 0,8 Sumber : Inglett, 1970
Bagian terkecil pada biji jagung adalah tip cap atau tudung pangkal. Tip cap merupakan bekas tempat melekatnya biji jagung pada tongkol jagung (Inglett,1970).
Perikarp merupakan membran terluar yang tersusun dari jaringan yang tebal. Di bawah lapisan ini terdapat lapisan berongga. Secara morfologi, lapisan ini merupakan bagian dari endosperma (Inglett,1970).
Gambar 2. Struktur biji jagung (Johnson, 1991).
dibandingkan lapisan lunak. Pada lapisan terluar endosperma, tepatnya di bawah aleuron mengandung protein dalam jumlah besar sekitar 28% (Inglett,1970).
4. Komposisi Kimia Biji Jagung
Pati jagung terdiri dari amilosa dan amilopektin sedangkan gulanya berupa glukosa. Lemak jagung sebagian besar terdapat pada lembaganya. Asam lemak penyusunnya terdiri dari asam lemak jenuh seperti palmitat dan stearat serta asam lemak tidak jenuh seperti oleat dan linoleat. Vitamin yang terkandung dalam jagung terdiri atas tiamin, niasin, riboflavin, dan piridoksin. Komposisi kimia biji jagung dapat dilihat pada Tabel 2.
Tabel 2. Komposisi kimia biji jagung Komponen Pati (%) Protein (%) Lipid (%) Gula (%) Abu (%) Biji utuh Endosperma Lembaga Perikarp Tip cap 71,5 86,4 8,2 7,3 5,3 10,3 9,4 18,8 3,7 9,1 4,8 0,8 31,5 1,0 3,8 2,0 0,6 10,8 0,3 1,6 1,4 0,3 10,1 0,8 1,6 Sumber : Inglett, 1970.
Granula pati yang terdapat pada jagung mengandung amilosa dan amilopektin. Secara umum, jagung normal mengandung amilosa sekitar 27 % dan amilopektin sekitar 73 %. Keduanya merupakan polimer dengan bobot molekul yang tinggi. Polimer tersebut tersusun dari unit–unit D-glukosa. Amilopektin yang berbentuk rantai cabang mengandung 40.000 atau lebih unit glukosa. Sedangkan amilosa yang berupa rantai lurus mengandung 1000 unit glukosa (Inglett, 1970).
Tabel 3. Jumlah protein di dalam endosperma pada Jagung normal dan varietas opaque-2
Protein Kandungan pada jagung Normal (%) Opaque-2 (%) Albumin
Globulin Prolamin (zein) Glutelin
3,2 1,5 47,2 35,1
13,2 3,9 22,8 50,0 Sumber : Inglett, 1970
Hampir 85 % minyak jagung terdapat pada bagian lembaga yang merupakan sumber komersil dari minyak jagung. Asam lemak yang terkandung pada minyak jagung terdiri dari 59 % linoleat, 27 % oleat, 12 % palmitat, 2 % stearat, 0,8 % linolenat, dan 0,2 % arakhidat. Komponen lain yang terdapat dalam minyak jagung selain asam lemak adalah vitamin A, vitamin D, vitamin E (0,3–0,7 mg/g), sterol, sterol ferulat (25 mg/g), squalen (0,16–0,42 mg/g), dan ubiquinon (0,12–0,21 mg/g) (Inglett, 1970).
Total gula yang terdapat dalam biji jagung bervariasi antara 1% dan 3%. Sukrosa merupakan gula terbanyak dalam biji jagung. Glukosa, fruktosa, dan rafinosa terdapat dalam jumlah kecil. Biji jagung juga mengandung 2,1–2,3% serat kasar. Perikarp menghasilkan 41–46% hemiselulosa melalui ekstraksi alkali (Inglett, 1970).
Tabel 4. Jumlah mineral pada biji jagung
Mineral Kisaran (%) Rata – rata (%) Kalsium
Fosfor Kalium Magnesium Besi Natrium Sulfur
0,000–0,450 0,030–1,300 0,030–0,920 0,020–0,920 0,001–0,010 0,000–0,130 0,010–0,190
0,030 0,320 0,350 0,170 0,003 0,010 0,120 Sumber : Inglett, 1970
B. Proses Penepungan Jagung
Proses penepungan jagung dapat dilakukan melalui dua cara yaitu proses penggilingan basah dan proses penggilingan kering. Pada penggilingan kering tidak dilakukan tahap perendaman biji jagung seperti pada proses penggilingan basah. Produk yang dihasilkan pada penggilingan basah biji jagung adalah pati. Sedangkan produk yang dihasilkan dari penggilingan kering biji jagung adalah grits, meal dan flour (tepung) (Inglett, 1970).
Secara garis besar, proses penepungan jagung melalui teknik penggilingan basah terdiri atas tahap pencucian, perendaman, penggilingan, penyaringan, sentrifugasi, dan pengeringan. Proses penepungan jagung diawali dengan pencucian biji jagung. Proses ini perlu dilakukan untuk memisahkan biji jagung dari kotoran yang dapat menjadi sumber kontaminasi (Inglett, 1970).
menghancurkannya. Hasil penggilingan kasar ini selanjutnya dialirkan ke hydroclone sehingga lembaga dapat dipisahkan (Inglett, 1970).
Selanjutnya dilakukan penyaringan untuk memisahkan partikel kasar. Hasil penyaringan kemudian digiling menggunakan atrition mill sehingga pati benar–benar keluar. Lalu slurry hasil penggilingan dialirkan ke gyratory shaker untuk memisahkan serat halus. Hasilnya yang tersisa sekarang adalah pati dan gluten. Untuk memisahkan pati dan gluten, digunakan sentrifuse dengan kecepatan tinggi sebanyak dua kali sehingga gluten yang tersisa dapat terpisahkan. Tahap terakhir, pati dikeringkan menggunakan oven kemudian digiling (Inglett, 1970).
Tahapan proses pada penggilingan kering berbeda dengan tahapan pada proses penggilingan basah biji jagung. Tahapan pertama yang dilakukan pada penggilingan kering adalah pembersihan biji jagung, jika diperlukan dapat dilakukan pencucian. Kemudian dilakukan tempering dengan penambahan air yang terkontrol. Hal ini dilakukan untuk melunakkan biji jagung sehingga mempermudah pelepasan lembaga dari endosperma jagung. Setelah tempering, dilakukan degerming untuk melepaskan kulit, tip cap, dan lembaga. Lalu dilakukan pengeringan dan pendinginan untuk persiapan fraksinasi. Fraksinasi dilakukan menggunakan serangkaian alat yaitu roller mill, sifter, gravity table separator, dan purifier untuk memisahkan komponen grits, meal, dan flour. Tahap terakhir dilakukan pengeringan jika diperlukan (Inglett, 1970).
C. Pati Jagung
air dingin. Oleh karena itulah pati sangat sulit dijadikan massa adonan yang nantinya mengalami pencetakan. Sifat pati jagung berbeda dengan tepung jagung yang komposisinya masih lengkap. Pati jagung atau yang dikenal dengan nama dagang maizena merupakan produk utama dari industri penggilingan jagung dengan teknik basah (Greenwood, 1975).
Pati tersusun dari unit–unit glukosa. Pati tersusun paling sedikit oleh tiga komponen utama yaitu amilosa, amilopektin, dan material antara seperti protein dan lemak (Banks dan Greenwood, 1975). Umumnya pati mengandung 12–30% amilosa, 75–80% amilopektin dan 5–10% material antara. Pati biji-bijian memiliki kandungan lemak yang rendah. Lemak yang berikatan dengan pati umumnya adalah lemak polar. Jumlah lemak yang dikandung oleh pati biji–bijian adalah sekitar 0.5–1.0%. Selain itu, pati mengandung mineral seperti fosfat dan nitrogen. Pada biji–bijian, umumnya fosfat berbentuk fosfolipid (Hoseney, 1998). Struktur dan jenis material antara tiap sumber pati berbeda tergantung sifat-sifat botani sumber pati tersebut. Secara umum dapat dikatakan bahwa pati biji-bijian mengandung bahan antara yang lebih besar dibandingkan pati batang dan pati umbi (Greenwood, 1979).
1. Amilosa
Amilosa merupakan homoglikan D-glukosa dengan ikatan α-(1,4) dari struktur cincin piranosa, yang membentuk rantai lurus umumnya dikatakan sebagai linier dari pati. Meskipun sebenarnnya jika amilosa dihidrolisa dengan -amilase pada beberapa jenis pati tidak diperoleh hasil hidrolisis yang sempurna. -amilase menghidrolisa amilosa menjadi unit-unit residu glukosa dengan memutuskan ikatan α-(1,4) dari ujung non pereduksi rantai amilosa menghasilkan maltosa (Hoseney, 1998).
amilosa berinteraksi dengan iodin membentuk kompleks berwarna biru merupakan cara untuk mendeteksi adanya pati (Hoseney, 1998).
2. Amilopektin
Amilopektin seperti amilosa juga mempunyai ikatan α-(1,4) pada rantai lurusnya, serta ikatan α-(1,6) pada titik percabangannya. Ikatan percabangan tersebut berjumlah sekitar 4–5% dari seluruh ikatan yang ada pada amilopektin. Bobot molekul amilopektin berkisar antara 107 – 5 x 108 (Fennema, 1996).
Amilopektin terkandung pada semua pati. Biasanya pati mengandung hampir 75% amilopektin. Beberapa pati mengandung amilopektin seluruhnya dan dinamakan waxy starch (pati berlilin) contohnya jagung berlilin (Fennema, 1996).
3. Granula Pati
Dalam keadaan murni granula pati berwarna putih, mengkilat, tidak berbau dan tidak berasa. Secara mikroskopik terlihat bahwa granula pati dibentuk oleh molekul-molekul yang membentuk lapisan tipis yang tersusun terpusat. Granula pati bervariasi dalam bentuk tidak beraturan. Pati jagung biasa memiliki diameter berkisar antara 2–30 μm, Pati jagung berlilin juga memiliki diameter berkisar antara 2–30 μm, jagung yang tinggi amilosa 2-24 μm, kentang 5-100 μm, tapioka 4-35 μm, dan gandum 2-55 μm (Fennnema, 1996).
D. Gelatinisasi
1. Konsep dan Mekanisme Gelatinisasi
Granula pati tidak larut dalam air dingin tetapi akan mengembang dalam air panas atau hangat. Pengembangan granula pati tersebut bersifat bolak–balik (reversible) jika tidak melewati suhu gelatinisasi dan akan menjadi tidak bolak–balik (irreversible) jika telah mencapai suhu gelatinisasi (Greenwood dan Munro, 1979).
Beberapa perubahan selama terjadinya gelatinisasi dapat diamati. Mula–mula suspensi yang keruh mulai menjadi jernih pada suhu tertentu, tergantung jenis pati yang digunakan. Terjadinya translusi larutan pati tersebut biasanya diikuti dengan pembengkakan granula. Bila energi kinetik molekul–molekul air menjadi lebih kuat daripada gaya tarik– menarik antar molekul pati di dalam granula, air dapat masuk ke dalam butir–butir granula. Hal inilah yang menyebabkan bengkaknya granula pati. Indeks refraksi butir–butir pati yang membengkak itu mendekati indeks refraksi air, hal inilah yang menyebabkan sifat translusen. Karena jumlah gugus hidroksil dalam molekul pati sangat besar, maka kemampuan menyerap air sangat besar. Peningkatan viskositas disebabkan air yang awalnya berada di luar granula dan bebas bergerak sebelum suspensi dipanaskan, kini sudah berada di dalam butir–butir pati dan tidak dapat bergerak bebas lagi (Winarno, 1997).
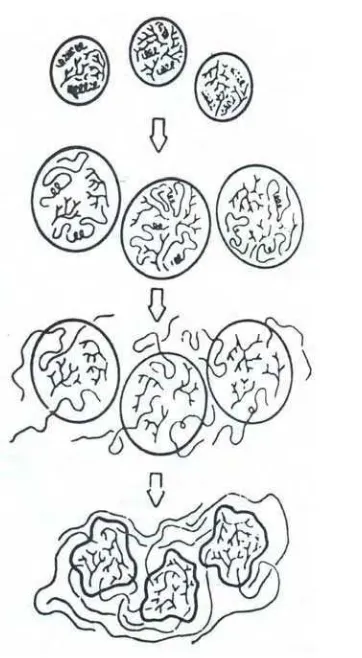
Pada dasarnya mekanisme gelatinisasi terjadi dalam tiga tahap, yaitu : (1) penyerapan air oleh granula pati sampai batas yang akan mengembang secara lambat dimana air secara perlahan-lahan dan bolak-balik berimbibisi ke dalam granula, sehingga terjadi pemutusan ikatan hidrogen antara molekul-molekul granula, (2) pengembangan granula secara cepat karena menyerap air secara cepat sampai kehilangan sifat birefriengence-nya dan (3) granula pecah jika cukup air dan suhu terus naik sehingga molekul amilosa keluar dari granula (Swinkels, 1985).
2. Suhu Gelatinisasi
Fennema (1996) menyatakan bahwa suhu atau titik gelatinisasi adalah titik saat sifat birefrigence pati mulai menghilang. Suhu gelatinisasi tidak sama pada berbagai jenis pati. Suhu gelatinisasi pada berbagai jenis pati ditunjukkan oleh Tabel 5.
Tabel 5. Suhu gelatinisasi beberapa jenis pati Sumber pati Suhu gelatinisasi (oC)
Beras 65-73
Ubi jalar 82-83
[image:40.612.162.343.74.403.2]Tapioka 59-70 Jagung 61-72 Gandum 53-64 Sumber: Fennema (1996)
Gambar 3. Mekanisme gelatinisasi pati (Harper, 1981)
Granula pati tersusun dari amilosa (berpilin) dan amilopektin (bercabang)
Masuknya air merusak kristalinitas amilosa dan merusak helix. Granula membengkak
Adanya panas dan air menyebabkan
pembengkakan tinggi. Amilosa berdifusi keluar dari granula
Suhu gelatinisasi diawali dengan pembengkakan yang irreversible granula pati dalam air panas dan diakhiri tepat ketika granula pati telah kehilangan sifat kristalnya Dalam suatu larutan pati, suhu gelatinisasi berupa kisaran. Hal ini disebabkan populasi pati yang bervariasi dalam ukuran, bentuk, dan energi yang diperlukan untuk mengembang. Selain itu, suhu gelatinisasi dipengaruhi oleh ukuran amilosa amilopektin serta keadaan media pemanasan.
3. Sifat Birefringence
Dengan pengamatan di bawah mikroskop (polarizing microscope) dapat diketahui keberadaan sifat birefringence pati, yaitu sifat merefleksikan cahaya terpolarisasi, sehingga terlihat kristal gelap terang. Intensitas birefringence pati sangat tergantung dari derajat dan orientasi kristal. Pati yang mempunyai kadar amilosa tinggi, intensitas sifat birefringencenya lemah jika dibandingkan dengan pati dengan kadar amilopektin tinggi (Hoseney, 1998).
E. Ekstrusi 1. Ekstruder
Ekstruder adalah alat untuk mencetak bahan melalui proses ekstrusi (Harper, 1981). Ekstruder terdiri atas berbagai bentuk, yang paling sederhana adalah ekstruder tipe ram atau piston.
Ekstrusi pemasakan dapat digambarkan sebagai proses dimana bahan pangan yang mengandung pati dan protein dimasak dan diadon menjadi adonan yang viskos dan plastis. Panas yang digunakan dalam proses pemasakan dapat berasal dari injeksi uap (secara langsung), dari jaket pemanas (secara tidak langsung), dan berasal dari energi mekanik yang timbul dari gesekan adonan selama proses ekstrusi (Harper, 1981).
Ekstruder dapat diklasifikasikan berdasarkan sifat termodinamika, kadar air, sifat fungsional, dan jumlah ulir. Menurut Harper (1981), berdasarkan sifat fungsional, ekstruder terdiri atas pasta extruder, high-pressure forming extruder, low–shear cooking extruder, coolet extruder, dan high–shear cooking extruder. Secara termodinamika, ekstruder terbagi atas tiga jenis yaitu : autogenous yaitu ekstruder yang menghasilkan panas dengan mengkonversi energi mekanik pada aliran proses; isotermal ekstruder; dan polythropic yaitu ekstruder yang prinsip kerjanya menggabungkan antara autogenous ekstruder dan isotermal ekstruder dimana panas diperoleh dari konversi energi mekanik dan dari transfer panas. Berdasarkan kadar air, ekstruder terbagi atas low moisture extruder dengan kadar air bahan sampai 20%, intermediate moisture extruder dengan kadar air bahan 20-28%, dan high moisture extruder dengan kadar air bahan lebih dari 28%. Berdasarkan jumlah ulirnya, ekstruder terbagi atas ekstruder berulir tunggal dan ekstruder berulir ganda.
ekstruder berulir ganda, selain itu tidak dibutuhkan tenaga ahli untuk pengoperasian dan perawatan ekstruder berulir tungggal (Fellows, 2000).
Menurut Smith (1981) ekstruder berulir tunggal dibagi atas tiga kelompok yaitu Low Shear, Medium Shear, dan High Shear. Jenis-jenis ekstruder tersebut dapat dilihat pada Tabel 6.
Tabel 6. Klasifikasi Ekstruder Ulir Tunggal (Smith, 1980)
Kategori Low
Shear
Medium Shear
High Shear
Kadar Air Produk (%) 25 – 75 15 – 30 5 – 8 Densitas produk (g/ 100ml) 32 – 80 16 – 51 3.2 – 20 Suhu barrel maksimum (°C) 20 – 65 55 – 145 110 – 180 Tekanan barrel maksimum
(kg / cm2) 6 – 63 21 – 42 42 – 84
Kecepatan ulir (rpm) 100 200 200
Produk khas
Produk pasta daging
Roti, makanan
ternak
Snack, breakfast
cereal
Gambar 4. Bagian-Bagian Penting Alat Ekstruder Tunggal
2. Proses Ekstrusi
Ekstrusi adalah proses pengolahan pangan yang mengkombinasikan beberapa proses secara berkesinambungan antara lain pencampuran, pemasakan, pengadonan, shearing, dan pembentukan (Fellows, 2000). Dalam proses ekstrusi, adanya aliran adonan adalah karena pengaruh tekanan ’shear’ (σ), dimana tekanan ’shear’ tergantung pada kecepatan ’shear’ dan viskositas bahan. Pada aliran newtonian terjadi hubungan linear antara tekanan ’shear’ dan kecepatan ’shear’. Aliran seperti ini biasanya terdapat pada aliran gas. Pada bahan pangan, karena mengandung senyawa-senyawa biopolimer seperti pati dan protein, sifat alirannya mengikuti kaedah non-newtonian (Harper, 1981).
3. Ekstrusi Pasta
Pada umumnya, pasta terbuat dari semolina. Pembuatan pasta cukup sederhana. Air dicampur dengan semolina untuk mendapatkan kadar air 31%. Semolina yang telah dicampur air kemudian dimasukan ke dalam ekstruder. Ulir yang terdapat di dalam ekstruder mengadon campuran dan mendorongnya keluar melalui die. Selanjutanya pasta yang keluar melalui die dikeringkan dan dikemas (Hoseney, 1998).
Pasta diekstrusi pada berbagai bentuk dan ukuran. Kecepatan aliran adonan melalui die sangatlah penting karena adanya fluktuasi kecepatan aliran adonan melalui die dapat menyebabkan variasi pada ukuran produk.
F. Mi Basah
1. Definisi Mi Basah
Menurut Astawan (1999), mi basah adalah jenis mi yang mengalami pemasakan setelah tahap pemotongan. Sedangkan menurut Dewan Standarisasi Nasional (1992), definisi mi basah adalah produk pangan yang terbuat dari tepung terigu dengan atau tanpa penambahan bahan lain dan bahan tambahan pangan yang diizinkan, berbentuk khas mi yang tidak dikeringkan. Mi basah memiliki kadar air maksimal 35% (b/b).
Berdasarkan bahan baku yang digunakan, ada dua macam mi yaitu mi yang berbasis protein dan mi yang berbasis pati. Bahan baku mi berbasis protein berasal dari gandum. Sedangkan bahan baku mi yang berbasis pati dapat berasal dari kacang hijau, ubi jalar, maupun sorgum (Fuglie dan Hermann, 2001).
Berdasarkan bentuk produk mi yang ada di pasaran, mi dapat diklasifikasikan menjadi mi basah mentah yaitu mi yang diproses tanpa pemasakan dan pengeringan, mi basah matang yaitu mi basah yang mengalami pemasakan dan tanpa pengeringan, serta mi kering yaitu mi yang mengalami pengeringan (Anonimc , 2006).
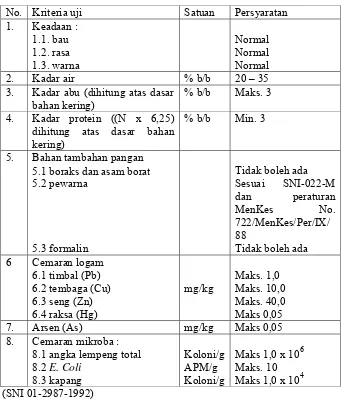
Tabel 7. Syarat Mutu Mi Basah
No. Kriteria uji Satuan Persyaratan 1. Keadaan :
1.1. bau 1.2. rasa 1.3. warna Normal Normal Normal
2. Kadar air % b/b 20 – 35
3. Kadar abu (dihitung atas dasar bahan kering)
% b/b Maks. 3 4. Kadar protein ((N x 6,25)
dihitung atas dasar bahan kering)
% b/b Min. 3
5. Bahan tambahan pangan 5.1 boraks dan asam borat 5.2 pewarna
5.3 formalin
Tidak boleh ada
Sesuai SNI-022-M dan peraturan MenKes No. 722/MenKes/Per/IX/
88
Tidak boleh ada 6 Cemaran logam
6.1 timbal (Pb) 6.2 tembaga (Cu) 6.3 seng (Zn) 6.4 raksa (Hg)
mg/kg
Maks. 1,0 Maks. 10,0 Maks. 40,0 Maks 0,05
7. Arsen (As) mg/kg Maks 0,05
8. Cemaran mikroba : 8.1 angka lempeng total 8.2 E. Coli
8.3 kapang
Koloni/g APM/g Koloni/g
Maks 1,0 x 106 Maks. 10 Maks 1,0 x 104 (SNI 01-2987-1992)
2. Penggunaan alkali pada mi
Berdasarkan warnanya, mi di Asia dapat dibedakan menjadi dua yaitu mi putih yang mengandung garam dan mi kuning yang mengandung alkali. Proses pembuatan kedua mi tersebut sama, yang membedakannya adalah penambahan alkali. Mi alkali ini dapat ditemukan di Jepang, Malaysia, Singapura, Indonesia, Thailand, Taiwan, Hongkong, dan Cina bagian selatan.
fleksibilitas mi, meningkatkan kehalusan tekstur, dan meningkatkan sifat kenyal.
Garam alkali yang umum digunakan di Asia Tenggara adalah Na2CO3 (natrium karbonat). Alkali yang digunakan dapat berupa bubuk
maupun larutan atau air kansui. Bubuk alkali harus dilarutkan dalam air terlebih dahulu sebelum dicampurkan dengan tepung.
Penambahan alkali dapat memberikan aroma yang khas terhadap mi, menyebabkan warna yang lebih gelap, dan meningkatkan kekenyalan mi. Penambahan alkali juga dapat memodifikasi adonan, mempengaruhi derajat gelatinisasi pati, dan mempengaruhi karakteristik pemasakan mi. Pada umumnya pH mi alkali antara 9-11, berbeda dengan mi yang hanya mengandung garam yaitu sekitar 7 (Miskelly, 1996).
G. Mi Jagung
Mi jagung merupakan mi dengan bahan baku utama pati atau tepung jagung. Di Filipina mi yang terbuat dari pati jagung maupun tepung jagung dinamakan bijon. Tekstur permukaannya opaque, agak kasar dan berwarna putih karena terbuat dari jagung putih (Inglett, 1970).
Proses pembuatan mi jagung dengan pembentukan lembaran terdiri dari beberapa tahap yaitu pencampuran bahan, pengukusan pertama, pengulian, pressing, slitting, perebusan, perendaman dalam air dingin, dan pelumuran dengan minyak. Proses pengolahan mi basah jagung berbeda dengan proses pengolahan mi basah terigu karena setelah pencampuran bahan baku dilakukan pengukusan. Pengukusan dilakukan agar adonan dapat dibentuk dan dicetak menjadi mi. Hal ini terjadi karena 60% protein endosperma jagung terdiri dari zein, sedangkan pada terigu, endospermanya terdiri dari gliadin dan glutenin. Gliadin dan glutenin merupakan jenis protein yang mempunyai sifat dapat membentuk massa yang elastic-cohesive bila ditambahkan air dan diuleni (Soraya, 2006).
menyebabkan pati dalam tepung basah mengalami gelatinisasi. Setelah pengukusan, ditambahkan tepung jagung kering ke dalam campuran, kemudian diuleni. Pengukusan menyebabkan terbentuknya massa yang elastis dan kohesif setelah pengulenan (Soraya, 2006).
Tahap selanjutnya adalah pressing untuk pembentukan lembaran. Pengepresan lembaran dilakukan bertahap dengan melewatkan adonan di antara roll pengepres sehingga didapatkan ketebalan 2 mm. Lembaran ini kemudian dipotong menjadi untaian mi. Agar untaian mi tidak mudah patah, maka jumlah pati yang dipregelatinisasi harus cukup karena pati inilah yang berfungsi sebagai pengikat (Soraya, 2006).
Selanjutnya, untaian mi dimatangkan dengan cara perebusan. Mi yang telah matang direndam dalam air dingin selama 10 detik untuk mengurangi kelengketan antara untaian mi. Lalu mi ditiriskan dan dilumuri dengan minyak (Soraya, 2006).
Pembuatan mi jagung dapat dilakukan dengan cara lain yaitu menggunakan sistem ekstrusi Waniska et al. (2000) menggunakan ekstruder pasta untuk membuat mi berbahan dasar tepung jagung dan air yang dipanaskan.
Proses pembuatan mi jagung menurut Waniska et al. (2000) diawali dengan pencampuran tepung jagung, garam, Natrium metabisulfit, dan air. Penambahan Natrium metabisulfit dapat meningkatkan viskositas pasta pati. Hal ini disebabkan banyak granula pati yang terdispersi dan lebih banyak pati yang tergelatinisasi selama proses. Viskositas pasta pati juga dipengaruhi oleh kadar air dan suhu. Semakin tinggi kadar air, maka viskositasnya semakin rendah dan semakin tinggi suhu, viskositasnya semakin tinggi. Kadar air dalam campuran bahan pembuat mi yang tinggi dapat menurunkan cooking loss namun meningkatkan waktu pemasakan (Waniska et al., 2000).
III. METODOLOGI PENELITIAN
A. Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah jagung kuning varietas Pioneer-21, Na2CO3, dan air, serta bahan–bahan kimia untuk
keperluan analisis.
Sedangkan alat yang digunakan adalah penggiling tepung (disc mill), pencetak mie (forming-cooking extruder model Scientific Laboratory Single Screw Extruder type LE25-30/C dari Labtech Engineering Co. Ltd., Thailand) dengan spesifikasi alat sebagai berikut :
• Ulir : ulir tunggal
• Barrel : barrel berupa pipa berbentuk silinder dengan diameter dalam 2.5 cm, permukaan halus tanpa alur
• Die : die terdiri dari dua lubang berbentuk bundar dengan diameter
2.5 mm
• Breaker plate : berbentuk lingkaran, diameter 2.8 cm dengan 49 lubang masing–masing berdiameter 2.5 mm
Gambar 5. Ekstruder tipe LE25-30/C
B. Metodologi
Penelitian ini dilakukan dengan tahapan karakterisasi tepung jagung dan tahapan kajian pembuatan mi basah jagung.
1. Tahapan Penelitian
a. Karakterisasi Tepung Jagung
Jagung yang digunakan adalah varietas P-21 (Pioneer-21). Varietas ini diperoleh dari Dinas Pertanian Kabupaten Ponorogo. Penyiapan tepung dilakukan dengan cara sebagai berikut :
Penggilingan dengan disc mill, saringan yang dipakai 12 mesh
Pengambangan dalam air untuk dibuang kulit ari dan lembaganya
Pengendapan selama 30 menit lalu cairan dibuang
Penjemuran
Penggilingan dengan disc mill, saringan yang dipasang 48 mesh
Pengeringan pada oven bersuhu 450C selama 30 menit
Pengayakan manual dengan saringan 100 mesh
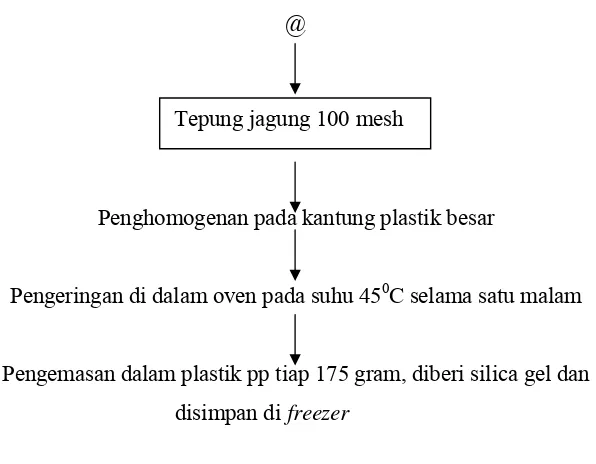
@ Jagung
@
Penghomogenan pada kantung plastik besar
Pengeringan di dalam oven pada suhu 450C selama satu malam
[image:52.612.197.495.75.307.2]Pengemasan dalam plastik pp tiap 175 gram, diberi silica gel dan disimpan di freezer
Gambar 6. Proses penyiapan tepung
Tepung jagung yang digunakan dalam penelitian ini berukuran 100 mesh. Sedangkan bila lebih dari 100 mesh, maka rendemen tepung yang dihasilkan akan lebih kecil. Penetapan ukuran partikel tepung didasarkan pada pernyataan Waniska et al (1999), bahwa partikel tepung jagung dengan ukuran kecil lebih bagus dibandingkan dengan ukuran yang lebih besar.
Karakterisasi tepung jagung dilakukan melalui pengukuran sifat kimia dengan analisis proksimat yang meliputi kadar air, kadar abu, kadar protein kasar, dan kadar lemak kasar, penentuan kadar karbohidrat yang dilakukan secara by difference, kadar amilosa, kadar amilopektin, serta total pati. Selain itu, dilakukan pula pengukuran terhadap sifat fisik tepung jagung yaitu warna.
b. Kajian Pembuatan Mi basah Jagung
Pembuatan mi basah jagung dilakukan menggunakan ekstruder tipe LE25-30/C. Pada tahap ini dilakukan pembuatan mi basah jagung pada berbagai variabel yaitu passing (1,2,3), kadar air (70%, 75%, 80%), dan kadar Na2CO3 (0%, 0.3%, 0.6%). Suhu yang digunakan
adalah 900 dan kecepatan ulir yang digunakan adalah 130 rpm. Hal ini didasarkan pada penelitian Fahmi (2007).
Cara pembuatan mi basah jagung menggunakan ekstruder adalah sebagai berikut:
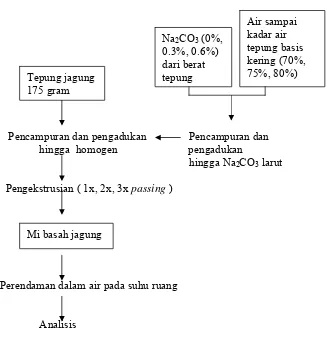
Pencampuran dan pengadukan Pencampuran dan hingga homogen pengadukan
hingga Na2CO3 larut
Pengekstrusian ( 1x, 2x, 3x passing )
Perendaman dalam air pada suhu ruang
[image:53.612.181.508.171.514.2]Analisis
Gambar 7. Proses Pembuatan Mi Basah Jagung
Pencampuran tepung jagung dan air dilakukan dengan terlebih dahulu melarutkan Na2CO3 dengan air. Kemudian larutan tersebut
dicampur dengan tepung jagung dalam wadah dan diaduk secara manual hingga benar-benar homogen.
Mi yang digunakan untuk analisis pada tiap passing sepanjang 132 cm. Setelah mi keluar dari ekstruder, mi direndam dalam wadah untuk kemudian dianalisis. Waktu sejak mi keluar dari ekstruder sampai analisis + 15 menit.
Tepung jagung 175 gram
Mi basah jagung
Air sampai kadar air tepung basis kering (70%, 75%, 80%) Na2CO3 (0%,
Parameter yang diukur pada tahap ini adalah sifat fisik mi. Parameter fisik yang diukur meliputi warna, persen elongasi, tensile strength, analisis profil tekstur, pengukuran kehilangan padatan akibat pemasakan (KPAP), dan derajat gelatinisasi.
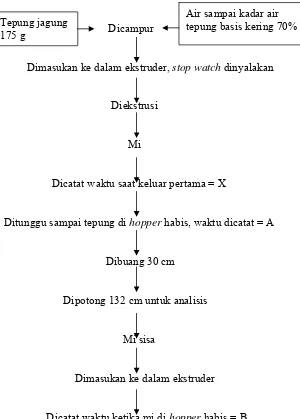
Perhitungan waktu untuk tiap passing dilakukan menggunakan tepung sebanyak 175 gram yang telah ditambah akuades hingga kadar air tepung basis kering mencapai 70%.
Dicampur
Dimasukan ke dalam ekstruder, stop watch dinyalakan
Diekstrusi
Mi
Dicatat waktu saat keluar pertama = X
Ditunggu sampai tepung di hopper habis, waktu dicatat = A
Dibuang 30 cm
Dipotong 132 cm untuk analisis
Mi sisa
Dimasukan ke dalam ekstruder
[image:54.612.191.491.234.653.2]Dicatat waktu ketika mi di hopper habis = B
Gambar 8. Prosedur Perhitungan Waktu Tepung jagung
175 g
Berdasarkan waktu yang dicatat, didapat X = 45.10 detik; A = 2 menit 12 detik; dan B = 1 menit 37 detik. Waktu yang diperlukan untuk passing 1 : X < waktu < X + A = 45.10 detik < waktu < 2 menit 12 detik; passing 2 : X + A < waktu < X + A + B = 2 menit 57.10 detik < waktu < 4 menit 34.10 detik; passing 3 : waktu > X + A + B = waktu > 4 menit 34.10 detik.
2. Rancangan Percobaan
Rancangan percobaan yang digunakan adalah rancangan acak lengkap (RAL) faktorial dengan tiga kali ulangan. Model persamaan matematika yang digunakan adalah sebagai berikut :
Yijkl = μ + αi + j + k + (α )ij + ( )jk + (α )ik + (α )ijk + εijkl
Dengan :
Yijkl = respon terukur
μ = rataan umum
αi = pengaruh passing pada taraf ke-i
j = pengaruh kadar Na2CO3 pada taraf ke-j k = pengaruh kadar air pada taraf ke-k
(α )ij = pengaruh interaksi antara passing pada taraf ke-i dan kadar
Na2CO3 pada taraf ke-j
( )jk = pengaruh intteraksi antara kadar Na2CO3 pada taraf ke-j dan
kadar air pada taraf ke-k
(α )ik = pengaruh interaksi antara passing pada taraf ke-i dan kadar air
pada taraf ke-k
(α )ijk = pengaruh interaksi antara passing pada taraf ke-i, kadar
Na2CO3 pada taraf ke-j, dan kadar air pada taraf ke-k
εijkl = galat percobaan untuk passing pada taraf ke-i, kadar Na2CO3
Perlakuan yang diterapkan :
A : passing dengan taraf 1, 2, dan 3
B : kadar Na2CO3 dengan taraf 0%, 0.3%, dan 0.6%
C : kadar air dengan taraf 70%, 75%, dan 80% 3. Pengamatan
a. Analisis Kimia
Analisis kimia yang dimaksud meliputi analisis proksimat, total pati, kadar amilosa, dan amilopektin. Analisis proksimat yang dilakukan meliputi analisis kadar air, kadar protein kasar, lemak kasar, dan abu. Penentuan kadar karbohidrat dilakukan secara by difference.
a. 1 Analisis Kadar Air Metode Oven (Apriyantono et al., 1989)
Cawan aluminium dikeringkan dalam oven selama 15 menit, didinginkan dalam desikator selama 10 menit kemudian ditimbang. Sejumlah sampel (sekitar lima gram) dimasukkan ke dalam cawan yang telah diketahui beratnya. Cawan beserta isinya dimasukkan ke dalam oven bersuhu 1000C selama kurang lebih enam jam atau sampai beratnya konstan. Selanjutnya cawan beserta isinya didinginkan dalam desikator selama 10 menit dan ditimbang. Perhitungan kadar air dilakukan dengan rumus :
kadar air (% b.b) = c – ( a- b ) x 100% c
keterangan : a = berat cawan dan sampel akhir (g) b = berat cawan (g)
c = berat sampel awal (g)
a. 2 Kadar Abu (AOAC, 1995)
tidak berasap lagi, kemudian dilakukan pengabuan di dalam tanur listrik pada suhu 400–6000C selama 4–6 jam atau sampai terbentuk abu berwarna putih. Sampel kemudian didinginkan dalam desikator dan ditimbang.
Kadar abu (% b.b) = c – ( a- b ) x 100% c
keterangan : a = berat cawan dan sampel akhir (g) b = berat cawan (g)
c = berat sampel awal (g)
a. 3 Kadar Lemak Metode Soxhlet (AOAC, 1995)
Labu lemak yang akan digunakan dikeringkan dalam oven bersuhu 100–1100C, didinginkan dalam desikator dan ditimbang. Sampel tepung ditimbang sebanyak lima gram, dibungkus dengan kertas saring dan dimasukkan ke dalam alat ekstraksi (soxhlet) yang telah berisi pelarut (heksana atau dietil eter).
Refluks dilakukan selama lima jam (minimum) dan pelarut yang ada di dalam labu lemak didistilasi. Selanjutnya, labu lemak yang berisi lemak hasil ekstraksi dipanaskan dalam oven yang bersuhu 1000C sampai beratnya konstan, didinginkan dalam desikator, dan ditimbang.
Kadar lemak (%b.b) = a – b x 100% c
keterangan : a = berat labu dan sampel akhir (g) b = berat labu kosong (g)
c = berat sampel awal (g)
a. 4. Kadar Protein Metode Mikro – Kjeldahl (AOAC, 1995)
dari 15 mg, ditambahkan 0,1 ml H2SO4 untuk setiap 10 mg bahan
organik di atas 15 mg. Sampel dididihkan selama 1–1,5 jam sampai cairan menjadi jernih.
Larutan kemudian dimasukkan ke dalam alat destilasi, dibilas dengan akuades, dan ditambahkan 10 ml larutan NaOH– Na2S2O3. Gas NH3 yang dihasilkan dari reaksi dalam alat destilasi
ditangkap oleh H3BO3 dalam erlenmeyer yang telah ditambahkan 3
tetes indikator (campuran 2 bagian merah metil 0,2% dalam alkohol dan 1 bagian methylene blue 0,2% dalam alkohol). Kondensat tersebut kemudian dititrasi dengan HCl 0,02 N yang sudah distandardisasi hingga terjadi perubahan warna kondensat menjadi abu–abu. Penetapan blanko dilakukan dengan metode yang sama seperti penetapan sampel. Kadar protein dihitung dengan rumus :
Kadar N (%) = (ml HCl spl – ml HCl blk) x N HCl x 14,007 x 100 mg sampel
Kadar protein (% b.b) = % N x 6,25 (faktor konversi)
a. 5 Kadar Karbohidrat (by difference)
Kadar karbohidrat (% b.b) = 100% - ( P + KA + A + L ) Keterangan : P = kadar protein (%)
KA = kadar air (%) A = kadar abu (%) L = kadar lemak (%)
a. 6 Total Pati (AOAC, 1970)
selama 2.5 jam. Setelah dingin dinetralkan dengan larutan NaOH 45% dan diencerkan sampai volume 500 ml, kemudian disaring. Kadar gula dinyatakan sebagai glukosa dari filtrat yang diperoleh. Berat glukosa dikalikan 0.9 merupakan berat pati.
a. 7 Kadar Amilosa (Apriyantono et al., 1989)
Penentuan kadar amilosa diawali dengan pembuatan kurva standar. Sampel 40 mg amilosa murni dimasukkan ke dalam tabung reaksi dan ditambahkan 1 ml etanol 95% dan 9 ml NaOH 1 N. Lalu dipanaskan dalam air mendidih selama 10 menit dan didinginkan. Larutan dipipet masing-masing sebanyak 1, 2, 3, 4, dan 5 ml ke dalam labu takar 100 ml. Ke dalam masing-masing labu takar ditambahkan asam asetat 1 N masing-masing 0.2, 0.4, 0.6, 0.8, dan 1 ml lalu ditambahkan masing-masing 2 ml larutan iod. Campuran ditepatkan hingga tanda tera dan didiamkan selama 20 menit. Intensitas warna biru yang terbentuk diukur dengan spektrofotometer pada panjang gelombang 625 nm. Kurva standar dibuat dengan memplotkan kadar amilosa pada sumbu X dan absorbansi pada sumbu Y. Kemudian dihitung persamaan linear yang menggambarkan hubungan antar keduanya. Persamaan linear yang diperoleh berupa :
Y = a + bX
panjang gelombang 625 nm. Kadar amilosa dihitung menggunakan persamaan linear yang diperoleh dari kurva standar.
a. 8. Kadar Amilopektin
Kadar Amilopektin = Total pati - Kadar Amilosa
b . Analisis Fisik
Analisis fisik dilakukan pada mi basah jagung. Analisis fisik yang dilakukan terhadap mi basah jagung meliputi analisis warna, elongasi, tensile strength, Texture Profile Analysis (TPA), Kehilangan Padatan Akibat Pemasakan (KPAP), dan derajat gelatinisasi. Sedangkan analisis fisik yang dilakukan terhadap tepung jagung berupa analisis warna.
b. 1 Analisis Warna Menggunakan Metode Hunter
Pengukuran warna dilakukan menggunakan Chromameter CR 300 Minolta. Sampel mi ditempatkan pada alas putih. Untuk sampel tepung ditempatkan pada wadah sampel tepung. Pengukuran menghasilkan nilai L dan derajat Hue. L menyatakan parameter kecerahan (warna kromatis, 0: hitam sampai 100: putih). Derajat Hue menunjukkan warna yang terllihat. Nilai hue dikelompokkan sebagai berikut : oHue 342-18 : Red purple; oHue 162-198 : Green; oHue 18-54 : Red; oHue 306-342 : Purple; oHue 54-90 : Yellow red; oHue 270-306 : Blue purple; oHue 90-126 : Yellow; oHue 198-234 : Blue green; oHue 234-270 : Blue; oHue 126-162 : Yellow green.
b.2 Texture Profile Analysis (TPA) menggunakan alat Texture Analyzer TAXT – 2
Seuntai sampel dengan panjang yang melebihi diameter probe diletakkan di atas landasan lalu ditekan oleh probe. Hasilnya berupa kurva yang menunjukkan hubungan antara gaya untuk mendeformasi dan waktu. Nilai kekerasan ditunjukkan dengan absolute (+) peak yaitu gaya maksimal, dan nilai kelengketan ditunjukkan dengan absolute (-) peak. Satuan kedua parameter ini adalah gram Force (gF). Sedangkan kekenyalan ditunjukkan dengan perbandingan luas area peak kedua dengan peak pertama.
Gambar 9. Kurva Profil Tekstur Mi
b.3 Analisis Persen Elongasi Menggunakan Texture Analyzer
Elongasi menunjukkan persen pertambahan panjang maksimum mi yang mengalami tarikan sebelum putus.
Sampel dililitkan pada probe dengan jarak antar probe sebesar 2 cm dan kecepatan probe 0.3 cm/s. Persen elongasi dihitung dengan rumus :
b. 4 Pengukuran Kehilangan Padatan Akibat Pemasakan
Penentuan KPAP dilakukan dengan cara merebus 5 gram mi dalam 150 ml air selama 3 menit lalu mi ditiriskan. Mi kemudian dikeringkan pada suhu 1000C sampai beratnya konstan, lalu ditimbang kembali. KPAP dihitung dengan rumus berikut :
KPAP = 1 – berat sampel setelah dikeringkan x 100% berat awal x (1–fraksi air contoh)
b. 5 Pengukuran Derajat Gelatinisasi
Penentuan derajat gelatinisasi diawali dengan pe