ISOLASI DAN UJI KEMAMPUAN ANTIFUNGAL FUNGI ENDOFIT DARI TANAMAN ANDALIMAN (Zanthoxylum acanthopodium DC.) TERHADAP
FUNGI PERUSAK MAKANAN
SKRIPSI
MAYSARAH 050805001
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
ii
LEMBAR PENGESAHAN
JUDUL : ISOLASI DAN UJI KEMAMPUAN ANTIFUNGAL FUNGI
ENDOFIT DARI TANAMAN ANDALIMAN (Zanthoxylum acanthopodium DC.) TERHADAP FUNGI PERUSAK MAKANAN
NAMA : MAYSARAH
NIM : 050805001
No Nama Keterangan Tanggal Tanda Tangan
1. Drs. Kiki Nurtjahja, M. Sc Dosen Pembimbing I
2. Yurnaliza, S. S i, M. Si Dosen Pembimbing II
3. Dra. Isnaini Nurwahyuni, M. Sc Dosen Penguji I
iii
ISOLASI DAN UJI KEMAMPUAN ANTIFUNGAL FUNGI ENDOFIT DARI TANAMAN ANDALIMAN (Zanthoxylum acanthopodium DC.) TERHADAP
FUNGI PERUSAK MAKANAN
SKRIPSI
Oleh
050805001 MAYSARAH
Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana pada
Fakultas Matematika dan Ilmu Pengetahuan Alam
Universitas Sumatera Utara
Disetujui oleh:
Pembimbing II Pembimbing I
Yurnaliza, S. S i, M. Si____
NIP. 197107181999032001 NIP. 196212111998031001
Drs. Kiki Nurtjahja, M. Sc
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
iv
PENGHARGAAN
Puji syukur penulis ucapkan kehadirat Allah SWT yang Maha Pengasih lagi Maha Penyayang atas rahmat, berkat dan hidayahNya penulis dapat menyelesaikan skripsi ini dengan judul “Isolasi dan Uji Kemampuan Antifungal Fungi Endofit
dari Tanaman Andaliman (Zanthoxylum acanthopodium DC.) Terhadap Fungi Perusak Makanan”.
Ucapan terima kasih penulis sampaikan kepada Bapak Drs. Kiki Nurtjahja, M.Sc dan Ibu Yurnaliza, M. Si selaku Dosen Pembimbing I dan Dosen Pembimbing II yang telah banyak memberikan bimbingan dan arahan serta waktu dan perhatiannya kepada penulis selama menyelesaikan skripsi ini. Penulis juga mengucapkan banyak terima kasih kepada Bapak Dra. Isnaini Nurwahyuni, M. Sc dan Ibu Dra. Elimasni, M. Si sebagai Ketua dan Sekretaris Penguji yang telah banyak memberikan arahan dan saran dalam penyempurnaan penulisan hasil penelitian ini.
Ucapan terimakasih juga saya ucapkan kepada Ibu Dra. Elimasni, M. Si selaku Pembimbing Akademik saya yang selalu memberikan nasehat luar biasanya selama saya menempuh pendidikan di jurusan Biologi ini dan juga kepada Bapak Prof. Dr. Dwi Suryanto, M. Sc Ketua Departemen Biologi FMIPA USU dan Ibu Dra. Nunuk Priyani, M. Sc selaku Sekretaris Departemen Biologi FMIPA USU. Dr Eddy Marlianto, M. Sc selaku Dekan FMIPA USU. Prof. Erman Munir, M. Sc selaku Ketua Laboratorium Mikrobiologi. Staf Pengajar di Departemen Biologi FMIPA USU. Bapak Sukirmanto, Ibu Nurhasni Muluk, Ibu Roslina Ginting, dan Bang Erwin selaku staf pegawai Departemen Biologi FMIPA USU. Serta tak lupa pula penulis mengucapkan terimakasih kepada Tropical Rain Forest Coffee Team yang memberikan beasiswa penelitian kepada penulis khususnya kepada Mr. Wu Tzu Yu, Afrianty Sitanggang, dan Syukural Fajar yang memberi semangat luar biasa kepada penulis.
Ungkapan terimakasih yang tak ternilai penulis ucapkan kepada keluarga yang kusayangi, kepada kedua orangtuaku Ibundaku Siti Khadijah Semel yang sudah memberikan banyak doa, harapan, nasehat luar biasa, semangat, senyuman, jalan keajaiban dalam menempuh hidup ini dan Ayahanda Bakri Imran yang sudah banyak memberikan banyak doa, harapan dan dorongan sehingga penulis dapat menyelesaikan perkuliahan ini. Kepada kakakku Suciati Bakri yang aku banggakan dan sayangi dan abang iparku Razman bin Adnan dan kepada Adindaku tersayang Siti Habiyah Bakri dan Rizaldi Abdillah, bungsu yang hebat. Penulis mengucapkan terimakasih atas segala cinta, kasih sayang, pengorbanan moril maupun materil, motivasi, kesabaran serta doa yang tak akan pernah bisa penulis balas sampai kapanpun.
Teman-v
teman seperjuangan yang spesial di Laboratorium Mikrobiologi (Irfan, Fendi, Kabul, Rahmad, Winda, Nia, Santy, Imus, Utin, Dini, Kak Pida dan Ummi). Teman-temanku Selingkaran yang luar biasa semangatnya dan Morobbi yang selalu memberikan penyejuk hati bagi penulis untuk senantiasa semangat dalam mengarungi hidup ini dan menjadi titik awal perubahan bagi penulis. Juga kepada sahabat-sahabat di UKMI AL-FALAK, Ukhuwah yang luar biasa, MSC, FLP Sumut, Incubator Sains terimakasih atas semua doa, persahabatan, dukungan, semangat dan nasehat yang selalu kalian berikan kepada penulis. Adik-adikku Zulfa, Dwi, Nikma, Ika, Yayan, Nana, Ami, Widya, Siti, Jean, dan Adi, Dan seluruh keluarga besar Biologi, senior, junior di Departemen Biologi serta semua pihak yang terlibat langsung maupun tidak langsung yang tidak dapat disebutkan satu persatu atas dukungan, perhatian, dan bantuannya kepada penulis.
Penulis menyadari bahwa hasil penelitian ini masih jauh dari kesempurnaan. Oleh karena itu penulis mengharapkan kritik dan saran yang bersifat membangun dalam melengkapi kekurangan serta penyempurnaan skripsi ini. Akhir kata semoga skripsi ini bermanfaat bagi kita semua
Medan, Desember 2009
vi
ABSTRAK
Penelitian ini bertujuan untuk mengetahui jenis fungi pada tanaman andaliman dan uji kemampuan antagonisnya dalam menghambat pertumbuhan fungi perusak makanan (Aspergillus sp1. dan Aspergillus sp2.). Akar, batang, daun, dan buah masing-masing disterilisasi permukaan dan ditumbuhkan pada media PDA. Fungi yang tumbuh dikarakterisasi morfologi untuk mengetahui jenisnya. Fungi endofit yang diperoleh selanjutnya diuji kemampuan antagonisnya terhadap fungi uji. Isolasi fungi endofit dari tanaman andaliman (akar, batang, daun dan buah) dapat diperoleh sebanyak tiga puluh dua isolat fungi endofit dengan jumlah terbanyak terdapat pada buah yang terdiri dari tujuh genus yaitu Penicillium, Aspergillus, Rhizopus, Colletotrichum, Cochliobolus, Schizophyllum, dan Trichoderma. Aspergillus dan Penicillium ditemukan pada semua bagian tanaman andaliman. Sebanyak tujuh belas isolat fungi endofit dapat menghambat pertumbuhan fungi uji.
vii
THE ISOLATION AND ABILITY OF ANTIFUNGAL OF ENDOPHYTIC FUNGI FROM ANDALIMAN (Zanthoxylum acanthopodium DC.)
TO FOOD SPOILAGE FUNGI
ABSTRACT
This aims of this study is to determine the type of endophytic fungi isolated from andaliman (Zanthoxylum acanthopodium DC.) and to examined antagonistic activity to inhibit the growth of food spoilage fungi (Aspergillus sp1. and Aspergillus sp2.). Part of the plant sterilized and grown on PDA medium and then the endophytic fungi is examined by antagonistic test. Thirty two endophytic fungi were successfully cultured on Potato Dextrose Agar (PDA) medium. They consist of seven genera, such as Penicillium, Aspergillus, Rhizopus, Colletotrichum, Cochliobolus, Schizophyllum, and Trichoderma. From such genera Aspergillus and Penicillium were very often found. The result showed that seventy endophytic fungi were potential against the food spoilage fungi.
viii
2.5 Kerusakan Makanan dan Bahaya Fungi Kontaminan pada Makanan 8
2.6 Fungi Perusak Makanan 11
BAB 3 Bahan dan Metoda 3.1 Waktu dan Tempat 12
3.2 Bahan 12 3.3 Isolasi Fungi Endofit dari Tanaman Andaliman 13
3.4 Karakterisasi dan Identifikasi Fungi Endofit 13 3.5 Isolasi, Karakterisasi dan Identifikasi Fungi Perusak 14
Makanan (Fungi Uji) 3.6 Uji Antagonis Fungi Endofit terhadap Fungi Perusa Makanan 14
3.7 Pengamatan Visual dan Mikroskopis 15
ix
DAFTAR TABEL
Halaman
Tabel 4.1.1 Karakterisasi morfologi koloni isolat fungi endofit tanaman 17 andaliman
Tabel 4.1.2 Jumlah isolat fungi endofit yang diisolasi dari bagian 21 tanaman andaliman
Tabel 4.2.1 Deskripsi gejala antagonis yang terjadi antara fungi endofit 23 dan fungi perusak makanan
x
DAFTAR GAMBAR
Halaman
Gambar 2.4.1 Andaliman dan buah andaliman 7
Gambar 3.2.1 Morfologi tanaman andaliman dan 12 akar, batang, daun, dan buah andaliman
Gambar 4.1.1 Frekuensi kehadiran genus endofit pada setiap bagian 16 tanaman andaliman Gambar 4.1.2 Frekuensi kehadiran genus fungi endofit pada setiap 18 bagian tanaman andaliman baik akar, batang, daun, dan buah
Gambar 4.1.3 Variasi Koloni dari Aspergillus (Umur Isolat 5 hari) pada 19 andaliman ditumbuhkan pada media PDA dimana
a. Aspergillus sp1, b. Aspergillus sp2., c. Aspergillus sp3., d. Aspergillus sp4. e. Aspergillus sp5., f. Aspergillus sp6.
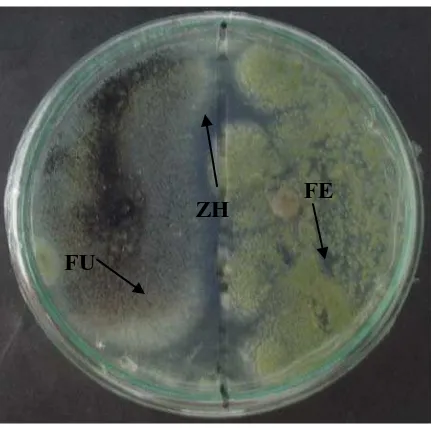
Gambar 4.2.1 Uji antagonis fungi endofit terhadap fungi uji, umur 5 hari. 22 Fungi Endofit (FE), (ZH) Zona Hambat (ZH), Fungi Uji (FU)
Gambar 4.2.2 Beberapa Isolat fungi endofit dari andaliman yang 24 berpotensi antagonis terhadap fungi perusak makanan
(Aspergillus sp1. dan Aspergillus sp2.) yang ditumbuhkan pada media PDA+YE 1% umur 5 hari.
Gambar 4.2.3 Pertumbuhan hifa abnormal pada media PDYA, umur 5 hari 25 a. Hifa normal Aspergillus sp2.
b. Hifa bengkok dari mekanisme antagonis fungi andofit), c. Hifa cebol/kerdil dari mekanisme antagonis fungi endofit,
xi
DAFTAR LAMPIRAN
Halaman
Lampiran A. Deskripsi Lokasi Penelitian dan Data Pengukuran 33 Faktor Fisik Lingkungan dari Lokasi Pengambilan andaliman
Lampiran B. Morfologi makroskopis dan mikroskopis 7 genus 34 fungi endofit yang ditemukan pada tanaman andaliman
umur 15 hari yang ditanam pada media PDA
Lampiran C. Miselium Fungi Perusak Makanan Yang Telah diidentifikasi 35 Uji Antagonis Beberapa Isolat Fungi Endofit Yang Tidak
Berpotensi
vi
ABSTRAK
Penelitian ini bertujuan untuk mengetahui jenis fungi pada tanaman andaliman dan uji kemampuan antagonisnya dalam menghambat pertumbuhan fungi perusak makanan (Aspergillus sp1. dan Aspergillus sp2.). Akar, batang, daun, dan buah masing-masing disterilisasi permukaan dan ditumbuhkan pada media PDA. Fungi yang tumbuh dikarakterisasi morfologi untuk mengetahui jenisnya. Fungi endofit yang diperoleh selanjutnya diuji kemampuan antagonisnya terhadap fungi uji. Isolasi fungi endofit dari tanaman andaliman (akar, batang, daun dan buah) dapat diperoleh sebanyak tiga puluh dua isolat fungi endofit dengan jumlah terbanyak terdapat pada buah yang terdiri dari tujuh genus yaitu Penicillium, Aspergillus, Rhizopus, Colletotrichum, Cochliobolus, Schizophyllum, dan Trichoderma. Aspergillus dan Penicillium ditemukan pada semua bagian tanaman andaliman. Sebanyak tujuh belas isolat fungi endofit dapat menghambat pertumbuhan fungi uji.
vii
THE ISOLATION AND ABILITY OF ANTIFUNGAL OF ENDOPHYTIC FUNGI FROM ANDALIMAN (Zanthoxylum acanthopodium DC.)
TO FOOD SPOILAGE FUNGI
ABSTRACT
This aims of this study is to determine the type of endophytic fungi isolated from andaliman (Zanthoxylum acanthopodium DC.) and to examined antagonistic activity to inhibit the growth of food spoilage fungi (Aspergillus sp1. and Aspergillus sp2.). Part of the plant sterilized and grown on PDA medium and then the endophytic fungi is examined by antagonistic test. Thirty two endophytic fungi were successfully cultured on Potato Dextrose Agar (PDA) medium. They consist of seven genera, such as Penicillium, Aspergillus, Rhizopus, Colletotrichum, Cochliobolus, Schizophyllum, and Trichoderma. From such genera Aspergillus and Penicillium were very often found. The result showed that seventy endophytic fungi were potential against the food spoilage fungi.
xii
BAB 1
PENDAHULUAN
1. 1 Latar Belakang
Andaliman merupakan rempah asli dari Sumatera Utara dan disebut sebagai the
golden spicy from North Sumatera. Tanaman ini ditemukan tumbuh liar di daerah
Tapanuli dan dimanfaatkan sebagai rempah pada masakan adat Batak Angkola dan
Batak Mandailing. Buah andaliman dipakai sebagai bumbu penyedap masakan yang
memberikan rasa pedas dan aroma yang khas (Sibuea, 2002; Katzer, 2004). Menurut
Parhusip (2005), masakan yang menggunakan andaliman umumnya lebih tahan lama.
Andaliman mengandung senyawa terpenoid yang mempunyai aktivitas antimikroba
dan antioksidan (Wijaya, 2000).
Pemanfaatan andaliman masih sebatas penggunaanya sebagai bumbu masakan
tetapi saat ini juga telah berkembang penelitian yang mencoba menggali potensi
andaliman sebagai obat sakit perut, perangsang nafsu makan, dan tonik (Hasairin,
2004). Ekstrak kasar buah andaliman memiliki aktivitas sebagai antioksidan dan
antimikroba yang potensial (Wijaya, 2000; Siregar, 2003). Manfaat lain buah
andaliman berdasarkan hasil penelitian adalah sebagai insektisida untuk menghambat
pertumbuhan Sitophilus zeamais (Andayanie, 2000). Senyawa metabolit yang terdapat
pada tanaman andaliman hanya bisa dimanfaatkan jika dilakukan pengekstraksian
bagian dari tanaman tersebut. Pemanfaatan metabolit secara langsung dari tanamannya
dibutuhkan banyak biomassa atau bagian tanaman sehingga mengganggu
kelangsungan hidup dan keberadaan tanaman ini. Hingga kini usaha budidaya
tanaman ini sulit dilakuka n. Pada umumnya penyebaran tanaman ini dilakukan oleh
burung, hal ini terbukti tidak ada ditemukannya anakan andaliman di sekitar tanaman
xiii
Mikroba endofit adalah organisme hidup yang berukuran mikroskopis (bakteri
dan fungi) yang hidup di dalam jaringan tanaman (xylem dan phloem), daun, akar,
buah, dan batang. Mikroba ini hidup bersimbiosis saling menguntungkan, dalam hal
ini mikroba endofit mendapatkan nutrisi dari hasil metabolisme tanaman dan
memproteksi tanaman melawan herbivora, hama dan penyakit sedangkan tanaman
mendapatkan derivat nutrisi dan senyawa aktif yang diperlukan selama hidupnya
(Tanaka et al., 1999). Hampir setiap tanaman tingkat tinggi memiliki beberapa
mikroorganisme endofit yang mampu menghasilkan metabolit sekunder. Bahan aktif
yang dihasilkan mikroorganisme endofit ini diperkirakan memiliki kemampuan yang
sama dengan bahan aktif yang dihasilkan tanaman inangnya. Telah banyak penelitian
yang dilakukan untuk mengisolasi mikroorganisme endofit pada beberapa tanaman,
misalnya pada tanaman obat (Tan and Zou, 2001), tanaman perkebunan dan tanaman
budidaya seperti kelapa sawit (Wibowo, 2008; Sembiring, 2008), padi (Zinniel et al.,
2002), dan tanaman-tanaman hutan (Strobel, 2002; Suryanarayanan et al., 2002).
Untuk mengetahui potensi mikroorganisme endofit khususnya fungi endofit
pada tanaman andaliman yang dapat berperan sebagai antifungal masih perlu
dilakukan penelitian. Isolasi dan uji kemampuan antifungal fungi endofit dari akar,
batang, daun, dan buah melalui aktivitas antagonis, diharapkan akan diperoleh isolat
fungi endofit yang potensial sebagai antifungal. Selanjutnya isolat tersebut akan
diujikan pada fungi perusak makanan. Fungi perusak makanan yang diperoleh dari
makanan yang sudah rusak yaitu roti dan nasi dijadikan sebagai fungi uji. Setelah
mengetahui adanya aktivitas antifungal dari fungi endofit tanaman andaliman melalui
uji antagonis fungi endofit dengan fungi perusak makanan, diharapkan dapat diperoleh
fungi endofit yang potensial penghasil senyawa antifungal yang baru dan unik dalam
xiv
1. 2 Permasalahan
Pengetahuan tentang fungi endofit khususnya pada tanaman andaliman sangat
sedikit, baik jenis maupun kegunaanya. Isolasi fungi endofit dari tanaman andaliman
menjadi menarik karena pekerjaan ini belum banyak dilakukan. Hal ini disebabkan
andaliman termasuk tumbuhan yang langka untuk daerah tropis khususnya di
Indonesia. Sejauh ini andaliman banyak ditemukan hanya di Sumatera Utara
khususnya di Kabupaten Tapanuli. Fungi endofit yang berasosiasi dengan jaringan
tanaman diperkirakan memiliki kemampuan dalam menghasilkan senyawa metabolit
sekunder yang sama dengan tanaman inangnya. Keanekaragaman fungi endofit dari
tanaman andaliman perlu digali untuk mengetahui kemampuan antifungalnya dalam
menghambat pertumbuhan fungi perusak makanan.
1. 3 Tujuan
Penelitian ini bertujuan untuk mengetahui jenis-jenis fungi endofit yang
terdapat pada akar, batang, daun, dan buah tanaman andaliman dan menguji
kemampuan antifungal fungi endofit terhadap fungi perusak makanan.
1. 4 Hipotesis
Ada beberapa jenis endofit yang dapat diisolasi dari organ tanaman andaliman dan diantaranya memiliki kemampuan dalam menghambat pertumbuhan fungi perusak makanan.
1. 5 Manfaat
Sebagai informasi jenis-jenis fungi endofit pada tanaman andaliman yang
memiliki kemampuan antifungal dan sebagai sumber informasi untuk penelitian lebih
xv
BAB 2
TINJAUAN PUSTAKA
2. 1 Mikroorganisme Endofit
Endofit merupakan asosiasi antara mikroorganisme dengan jaringan tanaman. Tipe
asosiasi biologis antara mikroorganisme endofit dengan tanaman inang bervariasi dari
netral, komensialisme sampai simbiosis. Pada situasi ini tanaman merupakan sumber
makanan bagi mikroorganisme endofit dalam melengkapi siklus hidupnya. Fungi
endofit adalah fungi yang terdapat di dalam sistem jaringan tanaman, seperti daun,
buah, ranting, ataupun akar tanaman (Clay, 1988). Tanaman menyediakan sumber
makanan untuk pertumbuhan dan perkembangbiakan mikroorganisme endofit. Fungi
ini menginfeksi tanaman sehat pada jaringan tertentu dan mampu menghasilkan
mikotoksin, enzim serta antibiotika (Carrol, 1988).
Hampir semua tanaman vaskular memiliki endofit. Endofit masuk ke dalam
jaringan tanaman umumnya melalui akar atau bagian lain dari tanaman. Bakteri
menembus jaringan tanaman di akar atau bagian lain dari tanaman yang luka. Fungi
endofit hidup dalam jaringan tanaman dan membantu tanaman dalam fiksasi nitrogen
(N2). Sementara itu asosiasi fungi endofit dengan tumbuhan inangnya oleh Carrol
(1988) digolongkan menjadi dua kelompok, yaitu mutualisme konstitutif dan induktif.
Mutulisme konstitutif merupakan asosiasi yang relatif erat hubungannya antara fungi
endofit dengan tanaman inang terutama rumput-rumputan. Pada kelompok ini fungi
endofit menginfeksi ovula (benih) inang, dan penyebarannya melalui benih serta
organ penyerbukan inang. Mutualisme induktif merupakan asosiasi antara
mikroorganisme endofit dengan tumbuhan inang yang penyebarannya terjadi secara
xvi
dan sering berada dalam keadaan tidak aktif dalam periode cukup lama dan
membentuk biomassa yang kecil.
Ditinjau dari sisi taksonomi dan ekologi, fungi endofit merupakan organisme
yang sangat heterogen. Petrini et al. (1992), menggolongkan fungi endofit dalam
kelompok Ascomycotina dan Deuteromycotina. Strobel et al. (1996), mengemukakan
bahwa fungi endofit meliputi genus Pestalotia, Pestalotiopsis, Monochaetia, dan
lain-lain. Sedangkan Clay (1988) melaporkan, bahwa fungi endofit dimasukkan dalam
famili Balansiae, Balansiopsis, Epichloe dan Myriogenospora. Genus Balansiae
umumnya dapat menginfeksi tumbuhan tahunan dan hidup secara simbiosis
mutualistik dengan tanaman inangnya. Dalam simbiosis ini, fungi dapat membantu
proses penyerapan unsur hara yang dibutuhkan oleh tanaman untuk proses fotosintesis
serta melindungi tanaman inang dari serangan penyakit, dan hasil dari fotosintesis
dapat digunakan oleh fungi untuk mempertahankan kelangsungan hidupnya (Bacon,
1991; Petrini et al., 1992; Rao, 1994).
2.2 Endofit dan Biodiversitas
Keanekaragaman hayati secara tidak langsung berarti keanekaragaman senyawa
kimia. Kemampuan bertahan hidup dengan tingkat kompetisi yang tinggi
menyebabkan tanaman beradaptasi terhadap perubahan-perubahan yang terjadi. Hal
ini menyebabkan tanaman menghasilkan senyawa-senyawa yang unik secara biologi
dan strukturnya. Keanekaragaman yang tinggi menyebabkan endofit juga
menghasilkan produk alami aktif yang lebih banyak (Wibowo, 2008). Menurut Bills
and Polyshook. (1992) dalam Strobel and Daisy (2003), endofit di daerah tropis
dengan jumlah yang tinggi menghasilkan senyawa metabolit sekunder yang aktif
dalam jumlah yang lebih banyak dibandingkan dengan endofit tanaman-tanaman yang
ada di daerah subtropis. Jadi tanaman inang mempengaruhi proses metabolisme
xvii
2. 3 Manfaat Endofit
Beberapa ahli telah mengisolasi dan meneliti endofit dari berbagai tanaman
diantaranya; tanaman obat (Tan and Zou, 2001), tanaman perkebunan (Zinniel et al.
2002), dan tanaman-tanaman hutan (Strobel, 2002; Suryanarayanan et al., 2003). Dari
sekitar 300.000 jenis tanaman yang tersebar di muka bumi, masing-masing tanaman
mengandung satu atau lebih mikroorganisme endofit yang terdiri dari bakteri dan
fungi (Strobel and Daisy, 2003). Bakteri atau fungi tersebut dapat menghasilkan
senyawa metabolit yang dapat berfungsi sebagai antibiotika (antifungi/antibakteri),
antivirus, antikanker, antidiabetes, antimalaria, antioksidan, antiimunopressif (Strobel
and Daisy, 2003), antiserangga (Azevedo et al., 2000), zat pengatur tumbuh (Tan and
Zou, 2001) dan penghasil enzim-enzim hidrolitik seperti amilase, selulase, xilanase,
ligninase (Choi et al., 2005), kitinase (Zinniel et al., 2002).
Mikroba endofit merupakan bagian dari mikroflora alamiah dari tanaman yang
sehat di lapangan, mikroba ini sebagai kontributor penting bagi kesehatan tanaman
(Aini et al., (2004). Menurut Hallman et al. (1999) dalam Aini et al. (2004), telah
diketahui pula bahwa bakteri endofit dapat berpengaruh pada kesehatan tanaman
dalam hal: (1) antagonisme langsung atau penguasaan niche atas patogen, (2)
menginduksi ketahanan sistemik dan (3) meningkatkan toleransi tanaman terhadap
tekanan lingkungan. Karena sifat-sifat tersebut bakteri endofit telah terbukti dapat
dimanfaatkan sebagai pengendali hayati penyakit tanaman bahkan dapat mengurangi
serangan hama tanaman (Ramamoorthy et al., 2001 dalam Aini et al., (2004).
2.4 Botani Tanaman Andaliman
Andaliman di Indonesia hanya dijumpai pada daerah Tapanuli, Sumatera Utara. Di
Indonesia, tanaman ini tumbuh liar di pegunungan dengan ketinggian 1400 m di atas
xviii
Subtropis. Di dunia, tanaman ini tersebar antara lain di India Utara, Nepal, Pakistan
Timur, Myanmar, Thailand, dan China (Wijaya, 1999; Hasairin, 1994).
Menurut Hasairin (1994), tinggi tanaman andaliman adalah 3-8 m. Batang dan
cabangnya merah, kasar beralur, berbulu halus dan berduri (Gambar 4.2.1). Buahnya
bulat hijau kecil dengan diameter ± 4mm (Gambar 4.2.2) (Tensiska, 2001).
Andaliman mempunyai aroma dan rasa khas yang dapat merangsang produksi air liur.
Hal ini karena tanaman andaliman memiliki sifat karminativum (Hasairin, 1994).
Andaliman mempunyai bunga lengkap dengan panjang ± 3mm (Tensiska, 2001).
Daunnya tersebar, bertangkai, majemuk menyirip beranak daun gasal, panjang
5-20 cm dan lebar 3-15 cm, memiliki kelenjar minyak (Gambar 4.2.1). Tangkai daun
bersayap dengan permukaan berduri, begitu pula dengan anak daun. Permukaan atas
daun berwarna hijau mengkilat dan permukaan bawahnya hijau muda atau pucat,
sedangkan pada daun muda permukaan bawahnya berwarna hijau kemerahan (Siregar,
2003 dan Wijaya 2000). Bunga aksilar, majemuk terbatas, anak payung menggarpu
majemuk, berkelamin dua, berwarna kuning pucat. Buahnya berbentuk kapsul, bulat
hijau kecil seperti lada (merica), jika sudah tua berwarna merah. Tiap buah memiki
satu biji yang berwarna hitam (Wijaya, 2000; Sibuea, 2002 and Siregar, 2003).
Gambar 2.4.1 a. Andaliman dan b. Buah Andaliman
xix
Menurut Hsuan Keng (1978) dalam Wijaya (1999), sistematika tanaman
andaliman adalah sebagai berikut:
Kingdom : Plantae
Divisio : Spermatophyta
Klass : Angiospermae
Sub klass : Dicotyledoneae
Ordo : Rutales
Family : Rutaceae
Genus : Zanthoxylum
Spesies : Zanthoxylum acanthopodium DC.
Andaliman adalah tanaman liar dan langka. Tanaman ini sulit dibudidayakan.
Andaliman tumbuh pada ladang atau lahan bukaan baru di hutan belantara. Andaliman
bukan ditanam, seperti cabai, merica, dan sayur mayur lainnya. Biasanya andaliman
tumbuh begitu saja. Andaliman mengandung senyawa terpenoid yang mempunyai
aktivitas antioksidan yang sangat bermanfaat bagi kesehatan dan berperan penting
untuk mempertahankan mutu produk pangan dari berbagai kerusakan seperti
ketengikan, perubahan nilai gizi serta perubahan warna dan aroma makanan.
Tumbuhan yang mengandung terpenoid juga dapat dimanfaatkan sebagai antimikroba.
Hal ini memberikan peluang bagi andaliman sebagai bahan baku senyawa antioksidan
atau antimikroba bagi industri pangan dan farmasi (Wijaya, 2000).
Saat ini andaliman diperhitungkan menjadi senyawa aromatik dan minyak
esensial. Masyarakat Himalaya, Tibet dan sekitarnya menggunakan tanaman ini
sebagai bahan aromatik, tonik, perangsang nafsu makan dan obat sakit perut (Hasairin,
1994). Manfaat lain buah andaliman berdasarkan penelitian adalah sebagai insektisida
untuk menghambat pertumbuhan serangga Sitophilus zeamais. Efeknya berupa daya
tolak makan serangga dan daya mengurangi makan selera serangga (Andayanie,
xx
Salah satu jenis andaliman dari Cina diimpor oleh Amerika dan digunakan
untuk mencegah penyebaran penyakit kanker pada tanaman jeruk (Katzer, 2004). Di
Jepang, daun andaliman digunakan untuk pemberi aroma dan untuk dekorasi.
Antioksidan ekstrak andaliman kemungkinan dapat dicoba diaplikasikan pada sistem
akeous seperti minuman kaya β-karoten, sup, soto, minuman fungsional kaya rempah,
minuman ringan, pada banyak minyak/lemak, produk pangan berlemak yang
dipanggang serta produk pangan berlemak yang memiliki pH netral (Tensiska, 2001).
Hasil pengujian aktivitas antimikroba menunjukkan bahwa ekstrak buah
andaliman bersifat bakterisidal terhadap bakteri Bacillus stearothermophilus,
Pseudomonas aeruginosa, Vibrio cholera, dan Salmonella thypimurium. Selain itu
andaliman juga mampu menghambat Bacillus cereus, Staphylococcus aureus, dan
Staphylococcus thyposa (Andayanie, 2000).
2.5 Kerusakan Makanan dan Bahaya Fungi Kontaminan pada Makanan
Kerusakan makanan dapat didefinisikan bahwa makanan tersebut telah rusak
sehingga manusia tidak ingin atau tidak dapat mengkonsumsi makanan tersebut.
Kerusakan makanan dapat terjadi karena serangga, kerusakan fisik atau kerusakan
lainnya seperti memar, rusak karena temperatur dingin, aktivitas enzim dan kerusakan
akibat mikroorganisme (Pitt and Hocking, 1993).
Makanan merupakan sumber energi yang dibutuhkan oleh manusia dan hewan
untuk melangsungkan kehidupannya. Namun, makanan dapat menjadi sumber
penyakit jika tidak memenuhi kriteria sebagai makanan baik, sehat dan aman.
Berbagai kontaminan dapat mencemari bahan pangan dan pakan sehingga tidak layak
untuk dikonsumsi. Fungsi makanan yaitu menjaga keberlangsungan hidup dan
menjaga agar makhluk hidup sehat lahir dan batin. Selain itu, kualitas makanan yang
dikonsumsi dapat berpengaruh terhadap kualitas hidup dan perilaku makhluk hidup itu
sendiri. Oleh karena itu, setiap makhluk hidup selayaknya berusaha untuk
xxi
segi fisik dan psikologis, karena kualitas makanan berpengaruh terhadap kualitas
makhluk hidup, terutama manusia (Maryam, 2002).
Kualitas makanan atau bahan makanan di alam ini tidak terlepas dari berbagai
pengaruh seperti kondisi dan lingkungan, yang menjadikan layak atau tidaknya suatu
makanan untuk dikonsumsi. Berbagai bahan pencemar dapat terkandung di dalam
makanan karena penggunaan bahan baku pangan terkontaminasi, proses pengolahan,
dan proses penyimpanan. Kontaminan yang sering ditemukan adalah mikotoksin yang
dihasilkan oleh fungi. Kontaminasi mikotoksin pada makanan sulit dihindari dan
merupakan masalah global, terutama di Indonesia yang mempunyai iklim yang sangat
mendukung pertumbuhan fungi penghasil mikotoksin. Umumnya kontaminasi
mikotoksin terjadi pada komoditi pertanian dan hasil olahannya, atau pada bahan
makanan yang disimpan terlalu lama. Mikotoksikosis dapat terjadi karena adanya
rantai makanan yang saling berkaitan, dimana pemaparan mikotoksin ke dalam tubuh
terjadi karena konsumsi bahan pangan yang sudah tercemar (efek primer) dan
konsumsi produk hewani (efek sekunder) (Maryam, 2002).
Dari begitu banyaknya jenis mikotoksin yang telah ditemukan, aflatoksin
merupakan mikotoksin yang paling banyak dijumpai di alam terutama di negara
beriklim tropis, dan mempunyai toksisitas yang lebih tinggi dari mikotoksin lainnya.
Namun, toksisitas mikotoksin tergantung beberapa faktor seperti dosis, rute
pemaparan, lamanya pemaparan, spesies, umur, jenis kelamin, status fisiologis (
kese-hatan dan gizi), serta adanya efek sinergis dari berbagai mikotoksin dalam makanan.
(Maryam, 2002a).
Selama penyimpanan, makanan atau bahan makanan sangat mudah ditumbuhi
oleh fungi. Iklim tropis yang dimiliki Indonesia dengan curah hujan, suhu dan
kelembaban yang tinggi sangat mendukung pertumbuhan fungi penghasil mikotoksin.
Kontaminasi mikotoksin tidak hanya menurunkan kualitas bahan pangan/pakan dan
mempengaruhi nilai ekonomis, tetapi juga membahayakan kesehatan manusia dan
hewan. Berbagai penyakit dapat ditimbulkan oleh mikotoksin, seperti kanker hati yang
xxii
Hingga saat ini telah dikenal 300 jenis mikotoksin (Cole and Cox, 1981), lima
jenis diantaranya sangat berpotensi menyebabkan penyakit baik pada manusia maupun
hewan, yaitu aflatoksin, okratoksin A, zearalenon, trikotesena (deoksinivalenol, toksin
T2) dan fumonisin. Menurut Bhat dan Miller (1991) sekitar 25-50% komoditas
pertanian tercemar kelima jenis mikotoksin tersebut. Penyakit yang disebabkan karena
adanya pemaparan mikotoksin disebut mikotoksikosis.
Di Indonesia, aflatoksin merupakan mikotoksin yang sering ditemukan pada
produk-produk pertanian dan hasil olahan (Muhilal and Karyadi, 1985). Selain itu,
residu aflatoksin dan metabolitnya juga ditemukan pada produk peternak seperti susu
(Bahri et al., 1995), telur (Maryam et al., 1994), dan daging ayam (Maryam, 1996).
Sudjadi et al (1999) melaporkan bahwa 80 diantara 81 orang pasien (66 orang pria dan
15 orang wanita) menderita kanker hati karena mengkonsumsi oncom, tempe, kacang
goreng, bumbu kacang, kecap dan ikan asin. Aflatoksinterdeteksi pada contoh liver
dari 58% pasien tersebut dengan konsentrasi diatas 400 µg/kg.
2.6 Fungi Perusak Makanan
2.6.1. Aspergillus
Aspergillus adalah suatu genus yang besar, terdiri lebih dari 100 spesies, sebagian
besar tumbuh dengan baik pada kultur laboratorium. Aspergillus merupakan fungi
yang mempunyai arti penting karena menyerang berbagai jenis bahan pangan di
gudang penyimpanan dan banyak spesiesnya yang menghasilkan toksin
(Dharmaputra, 2003b). Toksin yang dihasilkan disebut mikotoksin. Salah satu yang
paling berbahaya adalah aflatoksin yang diproduksi oleh A. flavus dan A. parasiticus.
Kemampuan aflatoksin menyebabkan kerusakan hati telah ditunjukkan pada hewan
menyusui, ikan dan burung. Karsinoma hati oleh aflatoksin diketahui terjadi pada
anak-anak itik, ikan trout, tikus dan sebangsa lingsang. Perannya dalam penyakit
manusia pada umumnya bergantung keadaan, tetapi kenyataannya banyak makanan
xxiii
Aspergillus mempunyai warna yang bervariasi. Struktur tubuh buah semua spesies
mempunyai kepala seperti ragbol dapat sederhana (hanya mempunyai fialid) atau
lebih kompleks (mempunyai metula dan fialid). Beberapa spesies membentuk struktur
xxiv
BAB 3
BAHAN DAN METODA
3. 1 Waktu dan Tempat
Penelitian ini dilakukan dari bulan Mei 2009 sampai Oktober 2009 bertempat
di Laboratorium Mikrobiologi Departemen Biologi FMIPA USU.
3. 2 Bahan
Bahan-bahan yang dipakai adalah akar, batang, daun, dan buah dari tanaman
andaliman (Gambar 3.2.1) yang diperoleh dari desa Paung Dolok Sanggul Sidi Kalang
Simpang Tiga Kecamatan Pollung Kabupaten Humbang Hasundutan (Lampiran A,
hlm. 33).
Gambar 3.2.1 a. Morfologi tanaman andaliman
b. Akar, batang, daun, dan buah andaliman
Dua isolat fungi uji yaitu sp1. (isolat dari nasi yang telah rusak) dan sp2.
(isolat dari roti yang telah rusak) (Lampiran C, hlm. 35), Potato Dextrose Agar
(PDA), Yeast Extract (YE), antibiotik chloramfenikol, aquades steril, alkohol 70%,
sodium hipoklorit 5,3%, etanol 70% dan etanol 75%.
xxv
3. 3 Isolasi Fungi Endofit dari Tanaman Andaliman
Fungi endofit diisolasi dari akar, batang, daun, dan buah tanaman andaliman.
Isolasi fungi endofit dari akar dan batang tanaman dilakukan menurut metode Radu
dan Kqueen (2002). Isolasi fungi endofit dari daun menurut metode Fisher et al.
(1992) dengan modifikasi (Pereira et al., 1999) dan isolasi fungi endofit dari buah
menurut metode Tomita (Lumyong et al., 2001). Tahap awal yang dilakukan adalah
mencuci bagian akar, batang, daun, dan buah andaliman dengan air mengalir selama
20 menit. Selanjutnya disterilisasi permukaan akar, batang, daun, dan buah tanaman.
Sterilisasi permukaan pada akar dan batang tanaman dengan merendam bagian
tanaman berturut-turut dalam etanol 75% selama 2 menit, larutan sodium hipoklorit
5,3% selama 5 menit dan etanol 75% selama 30 detik. Bagian daun disterilisasi
permukaan dengan merendam berturut-turut dalam etanol 70% selama 30 detik,
larutan sodium hipoklorit 3% selama 3 menit dan buah disterilisasi permukaan dalam
larutan etanol 75% selama 1 menit, sodium hipoklorit 5,3% selama 5 menit, dan
terakhir dengan etanol 75% kembali selama 30 detik. Kemudian akar, batang, daun
dan buah tanaman dibilas dengan aquades steril sebanyak 2 kali dan dikeringkan pada
kertas saring steril. Setelah kering, bagian ujung kiri dan kanan dari akar dan batang
tanaman dibuang ± 1 cm. Kemudian masing-masing akar dan batang tersebut dipotong
menjadi 1 cm. Daun dipotong seluas ± 1 cm2 dan buah dipotong menjadi 2 bagian.
Bagian akar, batang, daun dan buah yang telah steril dan telah dipotong,
diletakkan di permukaan media PDA + kloramfenikol (0,03 mg/ml) dengan posisi
bekas potongan ke arah media. Inkubasi dilakukan pada suhu ruang (25º–30ºC)
selama 5 hari. Pengamatan dilakukan setiap hari selama masa inkubasi. Koloni yang
muncul dari bagian akar, batang, daun, dan buah tanaman sebelah dalam
disubkulturkan ke media PDA yang baru untuk mendapatkan isolat murni.
3.4 Karakterisasi dan Identifikasi Fungi Endofit
Isolat fungi endofit yang diperoleh dari akar, batang, daun dan buah dari
xxvi
berdasarkan struktur dan warna koloni kemudian disubkultur. Selanjutnya dilakukan
identifikasi secara mikroskopik dengan mengamati morfologi fungi menurut Pitt and
Hocking (1997), Gilman (1971), Landecker and Moore (1996) dan Ganjar et al.
(1999).
3.5 Isolasi, Karakterisasi dan Identifikasi Fungi Perusak Makanan (Fungi Uji)
Isolasi fungi perusak makanan dilakukan menurut Pitt and Hocking (1997)
yaitu dengan metode penanaman langsung (Direct Plating). Fungi perusak makanan
diperoleh dari nasi dan roti yang telah terkontaminasi oleh fungi. Nasi dan roti
masing-masing diletakkan di permukaan media PDA + kloramfenikol (0,03 mg/ml).
Inkubasi dilakukan pada suhu ruang (25º–30ºC) selama 5 hari. Pengamatan dilakukan
setiap hari selama masa inkubasi. Koloni yang muncul dari bagian nasi dan roti
disubkulturkan ke media PDA yang baru untuk mendapatkan isolat murni, lalu dipilih
masing-masing 1 fungi dari nasi dan roti selanjutnya dikarakterisasi morfologi secara
makroskopis dan mikroskopis dan fungi tersebut dijadikan sebagai fungi uji.
3.6Uji Antagonis Endofit Terhadap Fungi Perusak Makanan
Uji antagonis dilakukan secara kualitatif untuk melihat kemampuan endofit
dalam menghambat pertumbuhan fungi perusak makanan. Masing-masing jenis fungi
endofit yang tumbuh dibuat biakan murninya dengan melakukan penanaman pada
media baru dan diinkubasi pada suhu ruang (± 25–30ºC) selama ± 5 hari sampai
pertumbuhan fungi endofit cukup untuk penyiapan inokulum. Dua lempeng inokulum
(bagian yang digunakan untuk uji antagonis adalah hifa terluar/paling ujung dari
koloni fungi yang tumbuh), yaitu lempeng inokulum dari fungi endofit dan lempeng
inokulum dari fungi perusak makanan yang telah disiapkan diinokulasikan ke dalam
media PDA. Lempeng inokulum yang diinokulasikan dilakukan dengan cara
memotong miselium dari inokulum yang yang tumbuh di permukaan media PDA
dengan menggunakan cork borer diameter 6 mm kemudian dimasukkan ke dalam
xxvii
(± 25ºC – 30ºC) selama ± 5 hari. Hal yang sama dilakukan untuk setiap fungi endofit
yang didapat. Isolat fungi endofit yang berpotensi menunjukkan hambatan
pertumbuhan terhadap fungi perusak makanan yang diujikan, selanjutnya dikoleksi.
3.7Pengamatan Visual dan Mikroskopis
Pengamatan dilakukan dengan 2 cara yaitu secara visual dan mikroskopis.
Pengamatan secara visual dilakukan dengan cara melihat zona/luas pertumbuhan
miselium dari masing-masing lempeng inokulum fungi endofit dan fungi perusak
makanan. Pengamatan secara mikroskopis dilakukan dengan cara mengamati ujung
miselium pada daerah/zona hambat fungi perusak makanan. Ujung miselium fungi
perusak makanan yang tumbuh pada permukaan media PDA dipotong berbentuk block
square kemudian diletakkan pada objek gelas, selanjutnya diamati adanya
abnormalitas pertumbuhan miselium fungi perusak makanan berupa pembengkokan
ujung miselium, miselium pecah, miselium berbelah, miselium bercabang, miselium
xxviii
BAB 4
HASIL DAN PEMBAHASAN
4.1 Isolat Fungi Endofit
Hasil isolasi fungi endofit dari tanaman andaliman diperoleh sebanyak 32 isolat yang
termasuk dalam 7 genus (Gambar 4.1.2), 5 famili, dan 5 ordo dari anggota kelas
Ascomycetes, Zygomycetes, dan Basidiomycetes. Ketujuh genus fungi endofit tersebut
adalah Penicillium, Aspergillus, Rhizopus, Colletotrichum, Cochliobolus,
Schizophyllum, dan Trichoderma. Pada akar tanaman andaliman diperoleh 6 isolat,
pada batang andaliman diperoleh 8 isolat. Pada daun andaliman diperoleh 7 isolat dan
pada buah diperoleh 11 isolat. Seluruh isolat yang berasal dari akar, batang, dan daun
andaliman termasuk pada kelas Ascomycetes sedangkan pada buah andaliman terdiri
dari kelas Ascomycetes dan Basidiomycetes.
Frekuensi kehadiran genus endofit pada setiap bagian tanaman andaliman
dapat dilihat seperti pada Gambar 4.1.1 berikut ini:
xxix
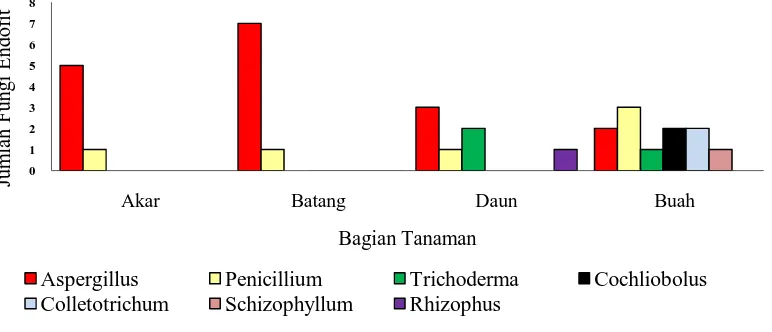
Gambar 4.1.1 menunjukkan bahwa fungi endofit yang paling banyak
ditemukan yaitu pada buah yaitu sebanyak 11 isolat. Fungi endofit pada batang terdiri
dari 8 isolat, daun terdiri dari 7 isolat dan akar terdiri dari 6 isolat. Fungi endofit
paling banyak ditemukan pada buah. diduga asosiasi fungi endofit banyak terjadi pada
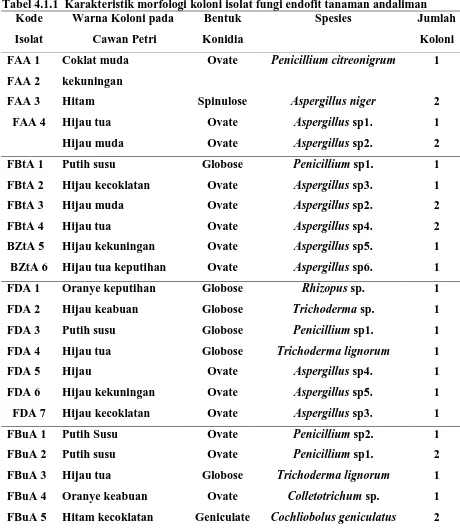
saat pembungaan andaliman. Hasil karakterisasi morfologi koloni isolat fungi endofit
pada tanaman andaliman dapat dilihat pada Table 4.1.1 berikut ini:
Tabel 4.1.1 Karakteristik morfologi koloni isolat fungi endofit tanaman andaliman Kode
Ovate Penicillium citreonigrum 1
Hitam Spinulose Aspergillus niger 2
Hijau tua Ovate Aspergillus sp1. 1
Putih susu Globose Penicillium sp1. 1
Hijau kecoklatan Ovate Aspergillus sp3. 1
Hijau muda Ovate Aspergillus sp2. 2
Hijau tua Ovate Aspergillus sp4. 2
Hijau kekuningan Ovate Aspergillus sp5. 1
Hijau tua keputihan Ovate Aspergillus sp6. 1
FDA 1
Oranye keputihan Globose Rhizopus sp. 1
Hijau keabuan Globose Trichoderma sp. 1
Putih susu Globose Penicillium sp1. 1
Hijau tua Globose Trichoderma lignorum 1
Hijau Ovate Aspergillus sp4. 1
Hijau kekuningan Ovate Aspergillus sp5. 1
Hijau kecoklatan Ovate Aspergillus sp3. 1
FBuA 1
Hijau tua Globose Trichoderma lignorum 1
Oranye keabuan Ovate Colletotrichum sp. 1
xxx
FBuA 6 FBuA 7 FBuA 8
Merah muda keabuan - Schizophyllum communae 1
Merah muda Ovate Colletotrichum
gloesporioides
1
Hijau tua Ovate Aspergillus sp5. 2
Keterangan:
FAA : Fungi Akar Andaliman FBtA : Fungi Batang Andaliman FDA : Fungi Daun Andaliman FBuA : Fungi Buah Andaliman
Pada bagian akar, batang, daun, dan buah andaliman ditemukan 2 genus fungi
endofit yang sama yaitu Aspergillus dan Penicillium. Sedangkan genus Trichoderma
hanya ditemukan pada daun dan buah andaliman, sedangkan Genus Rhizopus hanya
pada daun saja. Pada buah andaliman ditemukan Genus Colletotrichum, Cochliobolus,
Schizophyllum, dan Trichoderma (Gambar 4.1.1). Fungi endofit yang ditemukan pada
setiap bagian tanaman sebenarnya terdiri dari beberapa spesies yang berbeda.
Perbedaan ini dapat dilihat dari warna koloni, bentuk konidia, dan tekstur permukaan
koloni (Tabel 4.1.1 dan Lampiran J, hlm. 42). Hal ini mungkin disebabkan karena
faktor berbedanya asosiasi fungi endofit pada masing-masing bagian tanaman dan
juga ketersedian nutrisi pada setiap bagian tanaman baik dari akar, batang, daun, dan
buahnya. Frekuensi kehadiran genus fungi endofit pada semua bagian tanaman
andaliman baik akar, batang, daun, dan buah dapat dilihat pada Gambar 4.1.2 berikut
ini:
Gambar 4.1.2 Frekuensi kehadiran genus fungi endofit pada akar, batang, daun, dan buah andaliman
Aspergillus Penicillium Trichoderma Cochliobolus Colletotrichum Schizophyllum Rhizophus
xxxi
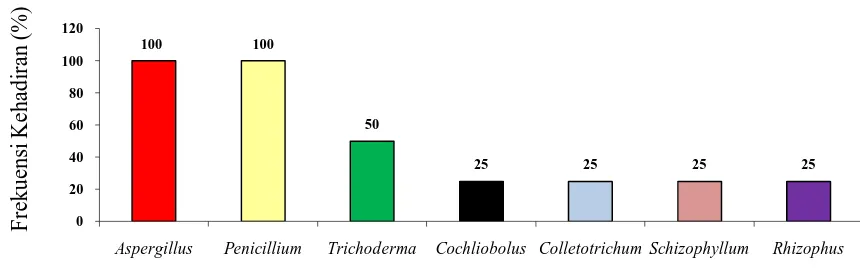
Jika kita lihat berdasarkan kehadiran tiap genus fungi endofit pada semua
bagian tanaman andaliman baik dari akar, batang, daun, dan buah maka Aspergillus
dan Penicillium memiliki frekuensi kehadiran paling tinggi dibandingkan dengan
genus yang lain. Frekuensi kehadiran Aspergillus dan Penicillium mencapai 100%,
diikuti dengan Genus Trichoderma sebesar 50%, dan yang paling sedikit frekuensinya
adalah Colletotrichum, Cochliobolus, Schizophyllum, dan Rhizopus, sebesar 25 %
(Gambar 4.1.2).
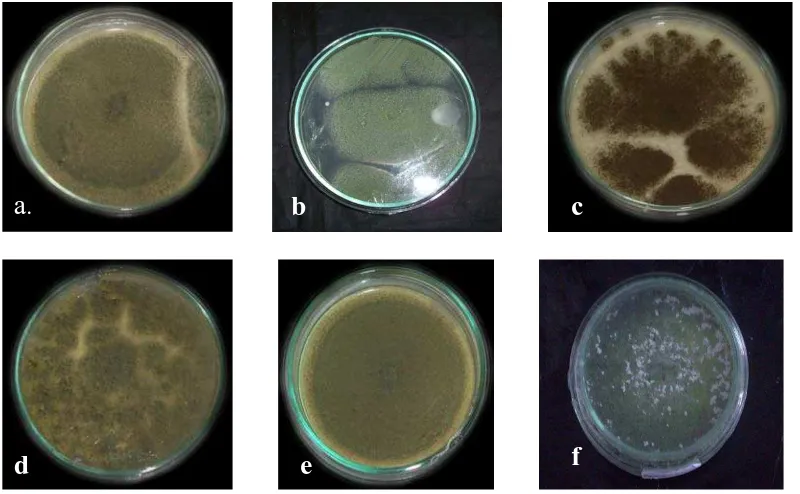
Gambar 4.1.3 Variasi koloni dari Aspergillus (umur isolat 5 hari) pada andaliman ditumbuhkan pada media PDA dimana a. Aspergillus sp1, b. Aspergillus sp2., c. Aspergillus sp3., d. Aspergillus sp4. e. Aspergillus sp5., f. Aspergillus sp6.
Penicillium dan Aspergillus ditemukan hampir pada setiap bagian tanaman
andaliman. Hal ini menunjukkan bahwa Aspergillus dan Penicillium adalah fungi
endofit yang bersifat kosmopolitan, sehingga mikroorganisme ini umum ditemukan.
Menurut Dwidjoseputro (1978), Aspergillus terdapat di mana-mana, baik di daerah
kutub maupun di daerah tropik, dan hampir pada setiap substrat. Aspergillus memiliki
fungsi penting bagi tanaman. Ada 7 spesies Aspergillus yang masing-masing memiliki
a
.b
c
xxxii
Aspergillus sp3., Aspergillus sp4., Aspergillus sp5., dan Aspergillus sp6.. Variasi yang
muncul dapat dilihat dari perbedaan warna koloni, bentuk konidia, dan juga dari
tekstur permukaan koloni (Tabel 4.1.1 dan Gambar 4.1.3).
Penicillium merupakan jenis fungi yang banyak digunakan dalam bidang
medis karena kemampuannya dalam menghasilkan antibiotik untuk menghambat
pertumbuhan mikroorganisme patogen. Menurut Gilman (1971), genus Penicillium
memiliki hifa vegetatif yang menjalar, bersekat, dan bercabang. Konidiofor tegak
lurus, biasanya tidak memiliki percabangan, bersekat, dan pada bagian apeks memiliki
vertisilia yang muncul dari percabangan primer yang tegak lurus, dan masing-masing
memiliki vertisilia sekunder (metula) dan terkadang memiliki percabangan tersier
(phialid). Konidia berbentuk globose, bulat telur (oval) atau ellips, halus ataupun
kasar.
Trichoderma ditemukan hanya pada daun dan buah andaliman. Trichoderma
adalah fungi endofit yang bersifat kosmopolitan, mikroorganisme ini umum
ditemukan pada tanah perkebunan kelapa sawit. Beberapa spesies Trichoderma seperti
T. harzianum, T. viride, T. album telah diteliti peranannya sebagai biokontrol.
Trichoderma spp. dapat ditemui di hampir semua jenis tanah dan pada berbagai
habitat. Fungi ini dapat berkembang biak dengan cepat pada daerah perakaran.
Disamping itu Trichoderma spp. merupakan fungi parasit yang dapat menyerang dan
mengambil nutrisi dari fungi lain. Rhizopus, Colletotrichum, Cochliobolus, dan
Schizophyllum adalah genus yang paling sedikit ditemukan jumlahnya. Keempat
genus ini masing-masing ditemukan pada daun dan buah andaliman saja. Rhizopus
diisolasi dari daun, sedangkan Colletotrichum, Cochliobolus, dan Schizophyllum
diisolasi dari buah andaliman. Rhizopus yang diisolasi memiliki ciri warna koloni atas
oranye keputihan dan koloni bawahnya oranye kemerahan, bentuk konidia globose,
dan tekstur koloni halus. Cochliobolus yang diisolasi memiliki ciri warna koloni atas
berwarna hitam kecoklatan dan hitam pekat pada bagian dasar koloni. Bentuk konidia
dari genus ini genikulat dan tekstur koloninya halus. Colletotrichum yang diisolasi
memiliki ciri warna koloni atas berwarna merah muda dan hitam keabu-abuan pada
xxxiii
Jumlah spesies fungi endofit yang diisolasi dari akar, batang, daun dan buah
andaliman menunjukkan bahwa Aspergillus sebagai jenis yang paling banyak
ditemukan yaitu sebanyak 17 isolat (53%) dari 32 isolat yang ditemukan diikuti
dengan Penicillium 6 isolat (19%), Trichoderma 3 isolat (10%), Cochliobolus dan
Colletotrichum masing-masing 2 isolat (6%) dan Rhizopus dan Schizophyllum 1 isolat
(3%).
Tabel 4.1.2 Jumlah isolat fungi endofit yang diisolasi dari bagian tanaman andaliman
Genus Fungi Endofit Jumlah isolat Persentase (%)
Aspergillus 17 53
Aspergillus dan Penicillium memiliki tingkat presentase yang lebih tinggi
dibandingkan dengan persentase genus lainnya. Hal ini mungkin disebabkan karena
kondisi inang yang sesuai dengan pertumbuhan kedua genus ini seperti ketersediaan
nutrisi. Menurut Dwidjoseputro (1978), Aspergillus terdapat di mana-mana, baik di
daerah kutub maupun di daerah tropik, dan hampir pada setiap substrat. Aspergillus
memiliki fungsi penting bagi tanaman. Menurut Domsch (1993), Penicillium spp.
adalah spesies yang tersebar luas di seluruh dunia, hampir pada semua substrat
walaupun bukan habitat alaminya. Fungi ini banyak ditemukan di daerah yang banyak
bahan organiknya.
4.2 Kemampuan Antagonis Fungi Endofit terhadap Fungi Perusak Makanan (Aspergillus sp1. dan Aspergillus sp2.)
Hasil uji antagonis dari 32 isolat fungi endofit yang diperoleh dari akar, batang, daun,
xxxiv
chloramphenicol menunjukkan sebanyak 17 isolat fungi endofit yang potensial dalam
menghambat pertumbuhan fungi perusak makanan yang diisolasi dari nasi dan roti
(Aspergillus sp1. dan Aspergillus sp2.). Kemampuan antagonis fungi endofit ditandai
dengan adanya pertemuan kedua hifa dari fungi yang diuji membentuk zona
penghambatan pada daerah pertemuan kedua koloni fungi tersebut.
Interaksi antara hifa fungi endofit mendesak miselium fungi uji sehingga
membentuk zona pembatas atau zona hambat antara kedua hifa tersebut (Gambar
4.2.1).
Gambar 4.2.1 Uji antagonis fungi endofit terhadap fungi uji, pada media PDYA, umur fungi 5 hari. Fungi Endofit (FE), (ZH) Zona Hambat (ZH), Fungi Uji (FU)
Mekanisme antagonis yang terjadi antara fungi endofit dan fungi perusak
makanan untuk semua isolat yang potensial yaitu adanya gejala antagonis dimana
pertumbuhan miselium fungi perusak makanan terhambat dan pertumbuhan hifa
mengalami abnormalitas, mengering dan menipis (Tabel 4.2.1 dan Gambar 4.2.2).
Terdapat tiga genus yang mampu melakukan proses penghambatan terhadap
pertumbuhan miselium fungi perusak makanan yaitu Aspergillus, Penicillium, dan
Rhizopus. Kebutuhan faktor lingkungan yang berbeda antara jasad renik memudahkan
untuk memacu antagonisme (Gray & Williams, 1971). Antagonisme dapat terjadi
karena melalui kontak langsung, kemungkinan aktivitas antibiotik, perubahan
FU
xxxv
lingkungan hidup akibat aktivitas metabolisme atau akibat persaingan atas hara
tertentu yang terbatas jumlahnya (Brock, 1966, Gray & Williams, 1971; Clark, 1979).
Tabel 4.2.1 Deskripsi gejala antagonis yang terjadi antara fungi endofit dan fungi perusak makanan
Kode Isolat Spesies Gejala Antagonis
FAA 2 Aspergillus niger
Aspergillus sp1.
Aspergillus sp2.
Pertumbuhan miselium fungi perusak makanan terhambat dan pertumbuhan hifa mengalami abnormalitas
FAA 3 Pertumbuhan miselium fungi perusak
makanan terhambat.
FAA 4 Pertumbuhan miselium fungi perusak
makanan terhambat, kering dan menipis.
FBtA 1 Penicillium sp1.
Aspergillus sp3.
FBtA 2 Pertumbuhan miselium fungi perusak
makanan terhambat.
FBtA 3 Pertumbuhan miselium fungi perusak
makanan terhambat.
FBtA 4 Pertumbuhan miselium fungi perusak
makanan terhambat. Pertumbuhan hifa mengalami abnormalitas
FBtA 5 Pertumbuhan miselium fungi perusak
makanan terhambat, kering dan menipis
FBtA 06 Pertumbuhan miselium fungi perusak
makanan terhambat.
FDA 3 Pertumbuhan miselium fungi perusak
makanan terhambat.
FDA 5 Miselium fungi perusak makanan
terhambat.
xxxvi
Aspergillus sp3.
FDA 7 Pertumbuhan miselium fungi perusak
makanan terhambat.
FBuA 1 Penicillium sp2.
Penicillium sp1.
Aspergillus sp5.
Pertumbuhan miselium fungi perusak makanan terhambat.
FBuA 2 Pertumbuhan miselium fungi perusak
makanan terhambat.
FBuA 8 Pertumbuhan miselium fungi perusak
makanan terhambat.
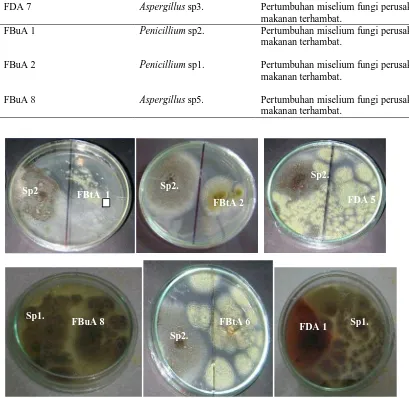
Gambar 4.2.2 Beberapa Isolat fungi endofit dari andaliman yang berpotensi antagonis terhadap fungi perusak makanan (Aspergillus sp1. dan
Aspergillus sp2.) yang ditumbuhkan pada media PDA+YE 1%
umur 5 hari.
Hasil uji antagonis juga menunjukkan bahwa dari akar andaliman diperoleh 3
fungi endofit, pada batang andaliman diperoleh 6 fungi endofit, pada daun andaliman
diperoleh 5 fungi endofit, dan pada buah andaliman terdapat 3 fungi endofit yang
berpotensi untuk menghambat fungi perusak makanan baik terhadap (Aspergillus sp1.
dan Aspergillus sp2.) (Tabel 4.2.1). Fungi endofit yang berasal dari akar, batang,
daun, dan buah memiliki kemampuan antagonistik yang ditandai dengan adanya
penghambatan miselium fungi perusak makanan dan pada akhirnya pertumbuhan hifa
mengalami abnormalitas, menipis, dan mengering.
xxxvii
Fungi endofit yang berasal dari tanaman andaliman mampu menghambat
pertumbuhan miselium fungi perusak makanan dan juga bisa menyebabkan hifa
mengalami kekeringan dan penipisan dinding hifa. Sebelum diuji antagonis fungi
perusak makanan seperti terlihat pada Gambar 4.2.3 a yang merupakan hifa normal
dari fungi perusak makanan. Setelah dilakukan uji antagonis hifa perusak makanan
yang tumbuh mengalami abnormalitas, ditandai dengan pertumbuhan hifa yang
bengkok (Gambar 4.2.3.b) dan berukuran kerdil seperti pada Gambar 4.2.3.c. Fungi
endofit yang bersifat antagonistik terhadap fungi perusak makanan akan berpeluang
sebagai agen bioantifungal hayati. Mekanisme antagonisme pada ketiga genus tersebut
kemungkinan menunjukkan bahwa fungi endofit memiliki senyawa aktif (biosintesis)
yang dapat menghambat fungi perusak makanan tersebut.
a.. Hifa normal Aspergillus sp2.(Perb:10x40)
xxxviii
a. Hifa bengkok dari mekanisme antagonis fungi andofit), b. Hifa cebol/kerdil dari mekanisme antagonis fungi endofit, c. Hifa normal Aspergillus sp2.
Adanya aktivitas antagonistik fungi endofit pada andaliman, tanaman ini dapat
dikembangkan sebagai bahan dasar bioantifungal. Tabel 4.2.1 memperlihatkan isolat
fungi endofit yang mempunyai potensi aktivitas antagonistik, dari 32 isolat terdapat 17
isolat yang berpotensi menghambat fungi perusak makanan dilihat dari gejala
antagonisnya, zona hambat yang terbentuk. Isolat fungi lainnya yang tidak
menunjukkan aktivitas antimikroba diduga mempunyai kandungan senyawa aktif
namun jumlahnya lebih kecil atau mungkin juga mengandung senyawa aktif potensial
yang lain (Son dan Cheah, 2002).
xxxix
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari hasil penelitian tentang isolasi dan uji kemampuan antifungal fungi endofit dari
tanaman andaliman (Zanthoxylum acanthopodium DC.) terhadap fungi perusak
makanan dapat diambil kesimpulan sebagai berikut:
a. Fungi endofit yang diisolasi dari akar, batang, daun, dan buah andaliman
terdiri dari 32 isolat dengan jumlah variasi jenis terbanyak pada buah
andaliman. Aspergillus dan Penicillium ada pada semua organ andaliman
dengan frekuensi kehadiran tertinggi yaitu 100% dan Aspergillus merupakan
genus dengan variasi jenis terbanyak yang ditemukan yaitu 17 isolat (53%).
b. Sebanyak 17 isolat fungi endofit dapat menghambat pertumbuhan Aspergillus
sp1. dan Aspergillus sp2. yang diisolasi dari nasi dan roti yang rusak.
5.2 Saran
Sebaiknya dilakukan penelitian lebih lanjut terhadap 17 isolat potensial dan
kandungan senyawa bioaktif yang dihasilkan fungi endofit untuk menghambat
xl
DAFTAR PUSTAKA
Aini, L. Q. dan A. L. Abadi. 2004. Keragaman bakteri endofitik dalam jaringan akar pisang serta potensi antagonistiknya. Jurnal Ilmu-Ilmu Hayati. 16 (2): hlm. 114-115.
Ali, N., Sardjono, A. Yamashita, and T. Yoshizawa. 1998. Natural occurrence of aflatoxins and fusarium mycotoxins (fumonisins, deoxinivalenol, nivalenol, and zearalenon) in corn from Indonesia. Food. Add. Contaminant. 15: hlm. 377-384.
Andayanie, L. 2000. Kajian Daya Insektisida Alami Nabati Kulit Buah Manggis (Garcinia mangostana. L), Buah Andaliman (Zanthoxylum acanthopodium DC.), Getah Gambir (Uncaria gambir Roxb.) dan Daun Teh (Camellia sinensis L.) terhadap Perkembangan Hama Gudang Sitophilus zeamays Motsch. Skripsi. Bogor: Fakultas Teknologi pertanian IPB. hlm. 36.
Azevedo, J. L., W. Maccheroni Jr, J. O. Pereira, and W. Luiz de Araujo. 2000. Endophytic microorganism: A review on insect control and recent advances on tropical plants. Electronic Journal of Biotechnology. 3 (1): hlm. 40-65.
Bacon, C. 1991. Isolation, culture and maintenance of endophytic fungi and grass. In Hand Book of Mycology (D. K. Aurora, D. Rai, K. G. Mukeri and G. R. Knudsen,1). Athens. Georgia.
Bahri, S., Ohim, Maryam, R. 1995. “Residu aflatoksin M1 pada susu sapi dan hubungannya dengan keberadaan afaltoksin M1 pada pakan sapi”. Kumpulan Makalah Lengkap Kongres Nasional Perhimpunan Mikologi Kedokteran Manusia dan Hewan Indonesia I dan Temu Ilmiah: hlm. 269-275. Bogor: Indonesia: IPB Press.
Bahri, S., Maryam, R dan Widiastuti, R. 2002. Materi Kuliah pada Workshop on “Grain and Feed Quality”, Bogor 30 Januari -1 Pebruari 2002.
Bhat, R. V. and J. D. Miller. 1991. Mycotoxins and food supply. FAO, Food, Nutrition and Agriculture, 1: hlm. 27-31.
Bills, G. F. and Polyshook, J. D. 1992. Recovery of Endophytic fungi from
Chamaechyparisthyoides. Sydowia. 44: hlm. 1-12.
Brock, T. D. 1996. Principles of Microbiology. Prentice Hall Inc. New Jersey. hlm. 288
Carrol, G. C. 1988. Fungal endophytes in stem and leaves. From latent pathogens to mutualistic symbiont. Ecology. 69: hlm. 2-9.
Choi, Y. W. I. J. Hodgkiss and K. D. Hyde. 2005. Enzyme production by endophytes of Brucea javanica. Journal of Agriculture Technology. 1: hlm. 55-65.
xli
Cole, R. J. and Cox, R. H. (Eds.). 1981. Handbook of Toxic Fungal Metabolites. Academic press, New York, pp 1850.
Dharmaputra, 2003b. “Isolasi dan Identifikasi Cendawan Perusak Pasca Panen”. Bogor: Jurusan Biologi FMIPA IPB dan Bagian Proyek Peningkatan Kualitas Sumber Daya Manusia Dirjen Perguruan Tinggi Departemen Pendidikan Nasional.
Dwidjoseputro.1978. Pengantar Mikologi. Edisi Kedua. Bandung. Penerbit Alumni. hlm. 92-127
Fisher, P. J. O., Petrini, and H. M. Lappin-Scot. 1992. The distribution of some fungal and bacteria endophytes in maize (Zea mays), New Phytologist. 122: hlm. 299-303.
Ganjar. I., Robert A. Samson., Karin van den Tweel-Vermeulen., Ariyanti Oetari, Iman Santoso. 1999. Pengenalan Kapang Tropik Umum. Edisi Pertama Depok: Universitas Indonesia (University of Indonesia Culture Collection).
Gilman, J. C. 1971. A manual of Soil fungi. Second edition. Fourth Printing. U.S.A, The Lowa State University Press.
Gray, T. R. G. and S. T. Williams. 1971. Soil Microorganism. Longman. London. hlm. 240.
Hsuan Keng. 1978. “Orders and Families of Malayan Seed Plant”. Dalam Widiastuti, B. Aktivitas Antioksidan dan Immunostimulan Ekstrak Buah Andaliman (Zanthoxylum acanthopodium DC.). Skripsi. Bogor. Fakultas Teknik Pertanian IPB.
Hallman, J., A. Quadt Hallman, W. X. Mahasse, and J. W. Kloepper. 1997. Bacterial and Endophytes in Agricultural Crops. Canadian Journal of Microbiology. 43: hlm. 895-914.
Hasairin, A. 1994. Etnobotani Tanaman Rempah dalam Makanan Adat Masyarakat Batak Angkola dan Mandailing. Thesis. Bogor: Program Pascasarjana IPB. .
Katzer. 2004. Sichuan Pepper (Zanthoxylum piperitum / stimulans / bungeanum / rhetsa / acanthopodium and others). 15 Oktober 2008. http://www.ang.kfunigraz.ac.at/-katzer/engl/Zant-pip.html.
Landecker and E. Moore. 1996. Fundamentals of the Fungi. Fourth edition. New Jersey. Prentice Hall International, Inc. hlm. 82-103.
Lorito, M., G. E. Harman., C. K. Hayes., R. M. Broadway., Tronsmo., S. L. Woo., and A. Di Pietro. 1992. Chitinolytic enzymes produced by Trichoderma
xlii
Lumyong S, Norkaew N, Ponputhachart D, Lumyong P, and Tomita F, 2001. Isolation, Optimitation and Characterization of 2001. Optimitation and Characterization of Xylanase from Endophytic fungi. Biotechnology for Sustainable Utilization of Biological Resources. The Tropic, 15.
Maryam, R., Bahri, S., and Zahari, P. 1994. “Deteksi aflatoksin B1, M1 dan aflatoksikol dalam telur dengan kromatografi cair kinerja tinggi”. Proceeding Teknologi Veteriner untuk Kesehatan Hewan dan Keamanan Pangan: hlm. 22-24. Bogor: IPB Press.
Maryam, R. 1996. ”Residu aflatoksin dan metabolitnya dalam daging dan hati ayam”. Prosiding Temu Ilmiah Nasional Bidang Veteriner: hal. 236-339. Bogor: IPB Press.
Maryam, R. 2000a. Fumonisin: Kelompok mikotoksin Fusarium yang perlu diwaspadai. Jurnal Mikologi Kedokteran Indonesia (Indonesian Journal of Medical Mycology), 1 (1): hlm. 51-57.
Maryam, R. 2002. Mewaspadai bahaya kontaminasi mikotoksin pada makanan. Tugas Mata Kuliah Falsafah Sains. Bogor, Indonesia: Institut Pertanian Bogor.
Miller, J. D., Savard, M. E., Sabilia, A., Rapior, S., Hocking, A. D., Pitt, J. I. 1993. Production of fumonisins and fusarins by Fusarium moniliforme from South East Asia. Mycologia. 85 (3): hlm. 385-391.
Muhilal and D. Karyadi. 1985. Aflatoxin in nuts and grains. Gizi Indonesia. 10 (1): hlm. 75-79.
Parhusip, A. J .N. 2005. Pengaruh Ekstrak Andaliman terhadap Permeabilitas dan Hidrofibisitas Bacilus cereus. http:/www.ipb.ac.id/galery/jurnal/tpg/index.php. Diakses pada tanggal 14 Oktober 2007.
Pereira, J. O. M. L. Carneiro-Vieira, and J. L. Azevedo. 1999. Endophytic fungi from Musa acuminata and their reintroduction an axenic plant. World Journal of Microbiology and Biotechnology. 15: hlm. 47-51.
Petrini, O., T. N. Sieber, L. Toti and O. Viret., 1992. Ecology metabolite production and substrate utilization in endophytics fungi. Natural Toxin. 1: hlm. 185-196.
Pitt, J. L and Hocking. A. D. 1997. Fungi and Food Spoilage. Second Edition. New York: Blackie Academic & Professional.
Radji, M. 2005. Peranan bioteknologi dan mikroba endofit dalam pengembangan obat herbal. Majalah Ilmu Kefarmasian. 2 (3): hlm. 118-121.
xliii
Ramamoorthy. V. R. Viswanathan, T. Raguchander, V. Prakasan, and R. Samiyappan. 2001. Introduction of systematic resistance by plant growth promoting rhizobacteria in crop plants against pests and diseases crop protection. 20: hlm. 1-11.
Rao, N. S. 1994. Mikroorganisme Tanah dan Pertumbuhan Tanaman. Edisi kedua.. Jakarta: Universitas Indonesia Press.
Sembiring, A. M. 2008. Isolasi dan Uji Antagonis Bakteri Endofit Akar dan Daun Kelapa Sawit (Elais guineensis Jacq.) terhadap Ganoderma boninense Pat. Skripsi. Medan: Fakultas Matematika dan Ilmu Pengetahuan Alam USU.
Sibuea, P. 2002. Potensi Andaliman Sebagai Antioksidan Alami. http://www.compas.com. Diakses tanggal 12 Desember, 2008.
Siregar, B. L. 2003. Andaliman (Zanthoxylum acanthopodium DC.) di Sumatera Utara: deskripsi dan perkecambahan. Hayati: 10 (1): hlm. 38.
Son, R. dan Cheah Y. K., 2002. Preliminary Screening of Endophytic Fungi from Medical Plants in Malaysia for Antimicrobial and Antitumor Activity. Malaysian Journal of Medical Sciences, 9(2): 23–33.
Strobel, G. A., W. M. Hess, E. Ford, R. S. Sidhu, and X. Yang., 1996. Taxol from fungal endophytes and the issue of biodiversity. Journal of Industrial Microbiology. 17: hlm. 417-425.
Strobel, G. A. 2002. Microbial gifts from rain forest. Can. J. Plant. Pathol. 24: hlm. 14-20.
Strobel, G. A. and B. Daisy. 2003. Bioprospecting for microbial endophytes and their natural products. Microbiology and Molecular Biology Review. hlm. 419- 502.
Sudjadi, S., Machmud, M., Damardjati, D.S., Hidayat, A., Widowati, S., Widiati, A. 1999. Aflatoxin research in Indonesia. Elimination of Aflatoxin Contamiation in Peanut. Australian Centre for International Agricultural Research. Canberra, pp.23-25.
Suryanarayanan, T. S., G. Venkasten and T. S. Murali. 2003. Endophytic fungal communities in leaves of tropical forest trees: diversity and distribution patterns. Current Science, 85 (4): hal. 489-493.
Tan, R. X., and W. X. Zou. 2001. Endophytes: A rich of functional metabolites. Nat. Prod. Rep. 18: hlm. 448-459.
xliv
Tensiska. 2001. Aktivitas Antioksidan Ekstrak Buah Andaliman(Zanthoxylum acanthopodium DC.) dalam Beberapa Sistem Pangan dan Kestabilan Aktivitasnya terhadap Kondisi Suhu dan pH. Thesis. Bogor: Program Pascasarjana IPB.
Trisiwi. 1996. Identifikasi Kapang Penghasil Mikotoksin pada Pakan Ayam Pedaging dan Petelur di Kotamadya Bandar Lampung. Skripsi. Lampung: Universitas Lampung.
Volk, A.W. & Wheleer. M.F. 1989. Mikrobiologi Dasar. Jilid 2. Edisi kelima. Jakarta: Penerbit Erlangga.
Wibowo, R. H. 2008. Isolasi dan Uji Antagonis Fungi Endofit Akar Kelapa Sawit (Elais guineensis Jacq.) terhadap Ganoderma boninense Pat. Skripsi. Medan: Fakultas Matematika dan Ilmu Pengetahuan Alam USU.
Widiastuti, B. 2002. Aktivitas Antioksidan dan Immunostimulan Ekstrak Buah Andaliman (Zanthoxylum acanthopodium DC.). Skripsi. Bogor. Fakultas Teknik Pertanian IPB.
Wijaya, C. H. 1999. Andaliman, rempah tradisional Sumatera Utara dengan antioksidan dan antimikroba. Teknologi dan Industri Pangan. 2(10): 59-61.
Wijaya, C. H. 2000. Isolasi dan identifikasi senyawa trigeminal aktif buah andaliman (Zanthoxylum acanthopodium DC.). Hayati : 7 (3): 91-92.
xlv
LAMPIRAN
Lampiran A .
A. Deskripsi Lokasi Penelitian No. Lokasi Pengambilan Sampel
Penelitian
Letak Astronomis Ketinggian Lokasi
1 Desa Paung Dolok Sanggul Sidi
B. Data Pengukuran Faktor Fisik Lingkungan dari Lokasi Pengambilan andaliman
No. Lokasi Penelitian Faktor Fisik Lingkungan
Suhu Udara
xlvi
Lampiran B: Morfologi makroskopis dan mikroskopis 7 genus fungi endofit yang ditemukan pada tanaman andaliman umur 15 hari yang ditanam pada media PDA
a. Penicillium b. Rhizopus
c. Aspergillus d.Cochliobolus
e.Trichoderma f. Colletotrichum
xlvii
Lampiran C:
A. Miselium Fungi Perusak Makanan Yang Telah Di identifikasi
a. Aspergillus sp1. b. Aspergillus sp2.
(Nasi) (Roti)
B.Uji Antagonis Beberapa Isolat Fungi Endofit Yang Tidak berpotensi
a. Colletotrichum FBuA 07 b. Cochliobolus FBuA 05
c. Trichoderma lignorum FBuA 03 d. Schizophyllum communae FBuA 06
xlviii
Lampiran D: Gambar-Gambar Penelitian
A. Cara mengisolasi fungi endofit dari akar, batang, daun dan buah andaliman
xlix
Lanjutan lampiran D
D. Pengukuran faktor fisik lingkungan secara in situ
E. Pengambilan andaliman F. Pengambilan Akar andaliman