PRODUKSI PATI ASETAT DENGAN MENGGUNAKAN PATI
SAGU NANOKRISTALIN
YUNITA SAUYANA
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi berjudul Produksi Pati Asetat dengan Menggunakan Pati Sagu Nanokristalin adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
ABSTRAK
YUNITA SAUYANA. Produksi Pati Asetat dengan menggunakan Pati Sagu Nanokristalin. Dibimbing oleh TITI CANDRA SUNARTI
Pati sagu alami memiliki kelemahan jika digunakan matriks untuk pembawa bahan aktif atau obat-obatan karena sifatnya yang tidak tahan asam, daya cerna yang tinggi, serta kelarutan yang rendah. Hal ini menghambat fungsinya sebagai pelindung sehingga bahan aktif tidak mencapai targetnya. Pati nanokristalin terasetilasi merupakan pati termodifikasi yang dapat memperbaiki sifat pati, yang dihasilkan melalui proses lintnerisasi, presipitasi dengan pelarut etanol, dan disubstitusi dengan asetat anhidrida. Penelitian ini bertujuan untuk meningkatkan kinerja pati dan pati termodifikasi sebagai matrik pembawa obat dalam bentuk pati terasetilasi. Tiga jenis pati sagu yang digunakan yaitu pati alami, pati kristalin dan pati nanokristalin yang diasetilasi menggunakan asetat anhidrida dengan konsentrasi 3 dan 6%. Secara umum pati sagu alami lebih mudah diasetilasi dibandingkan pati kristalin dan pati nanokristalin. Hasil memperlihatkan pengaruh asetilasi dalam meningkatkan kelarutan dan swelling power, namun menurunkan daya serap air, daya serap minyak dan daya cerna pati. Konsentrasi asetat anhidrida mempengaruhi kelarutan, % asetil dan derajat subsitusi. Kenaikan konsentrasi asetat anhidrida dari 3% menjadi 6% menyebabkan peningkatan % asetil 0.05-0.53% dan derajat substitusi dari 0.01-0.02 poin, serta mampu meningkatkan kelarutan produk hingga 7%.
Kata kunci: asetilasi, pati sagu, pati kristalin, pati nanokristalin
ABSTRACT
YUNITA SAUYANA. Production of Acetylated Starch Using Nanocrytalline Sago Starch. Supervised by TITI CANDRA SUNARTI.
solubility, % acetyl, and substitution degree. The increasing of acetate hydride concentration from 3% to 6% causes the increasing of % acetyl from 0.05-0.53%, substitution degree from 0.01-0.02 point, and product solubility up to 7%.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian
pada
Departemen Teknologi Industri Pertanian
PRODUKSI PATI ASETAT DENGAN MENGGUNAKAN PATI
SAGU NANOKRISTALIN
YUNITA SAUYANA
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
Judul Skripsi : Produksi Pati Asetat dengan Menggunakan Pati Sagu Nanokristalin
Nama : Yunita Sauyana NIM : F34100067
Disetujui oleh
Dr Ir Titi Candra Sunarti, MSi Pembimbing
Diketahui oleh
Prof Dr Ir Nastiti Siswi Indrasti Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas rahmat dan karunia-Nya yang berlimpah sehingga penulis dapat menyelesaikan karya ilmiah dengan judul Produksi Pati Asetat dengan Menggunakan Pati Sagu Nanokristalin. Penelitian ini merupakan bagian dari penelitian KKP3N 2014 yang didanai oleh Badan Penelitian dan Pengembangan Penelitian. Penulis mengucapkan terima kasih kepada : 1. Dr Ir Titi Candra Sunarti, MSi selaku dosen pembimbing yang telah
bersedia memberikan arahan dan bimbingannya selama pelaksaan penelitian dan penyusunan skripsi.
2. Dr Hj Indah Yuliasih STP, MSi dan Drs. Purwoko, MSi selaku dosen penguji dalam ujian skripsi.
3. Ayah dan ibu serta keluarga besar atas segala doa dan dukungannya. 4. Laboran TIN atas kesediaannya membantu penulis selama penelitian. 5. Keluarga besar TIN 47 atas kebersamaannya serta semua pihak yang
tidak dapat disebutkan oleh penulis, yang senantiasa membantu dalam pelaksanaan penelitian.
Penulis menyadari bahwa karya ilmiah ini masih belum sempurna. Oleh karena itu, penulis mengharapkan segala bentuk kritik dan saran yang membangun agar skripsi ini menjadi lebih baik.
Semoga karya ilmiah ini bermanfaat.
DAFTAR ISI
DAFTAR TABEL DAFTAR GAMBAR DAFTAR LAMPIRAN
PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 1
Tujuan Penelitian 2
Manfaat Penelitian 2
Ruang Lingkup Penelitian 2
METODE 3
Bahan 3
Alat 3
Metode Penelitian 3
HASIL DAN PEMBAHASAN 6
Karakteristik Bahan Baku 6
Produksi Pati Nanokristalin Terasetilasi 7
Karakteristik Pati Asetat 11
SIMPULAN DAN SARAN 20
Simpulan 20
Saran 21
DAFTAR PUSTAKA 21
LAMPIRAN 25
DAFTAR TABEL
Kandungan pati sagu 6
Pengaruh jenis pati dan konsentrasi asam asetat anhidrida terhadap
karakteristik kimia pati terasetilasi 12
Pengaruh jenis pati dan konsentrasi asam asetat anhidrida terhadap
karakteristik fungsional pati terasetilasi 12
Pengaruh jenis pati dan konsentrasi asetat anhidrida terhadap
derajat kristalinitas dan tipe krisalin 14
DAFTAR GAMBAR
Diagram alir proses produksi pati kristalin dengan metode
lintnerisasi 4
Diagram alir proses produksi pati nanokristalin dengan metode
presipitasi 4
Diagram alir proses pati asetat dengan metode asetilasi 5 Struktur amilopektin pada daerah (1) kristalin dan (2) amorf 8 Ilustrasi degradasi daerah amorf selama hidrolisis asam 8 Pengaruh waktu lintnerisasi terhadap total gula dalam filtrat pati 9
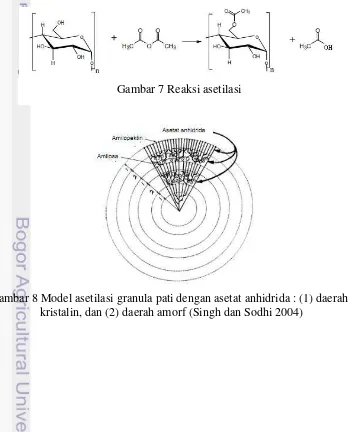
Reaksi asetilasi 10
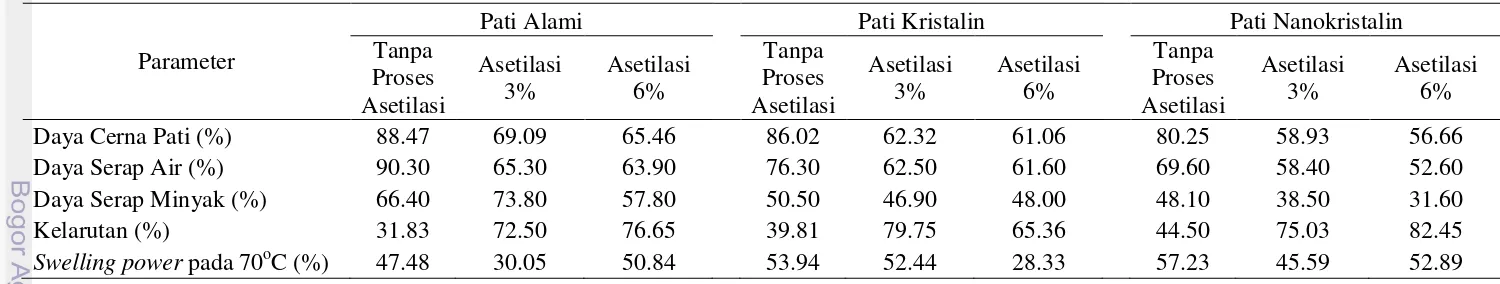
Model asetilasi granula pati dengan asetat anhidrida 10
Pola difraksi sinar X kristalit pati 14
Pola kristalinitas berdasarkan analisa XRD untuk pati alami 15 Pola kristalinitas berdasarkan analisa XRD untuk pati kristalin 15 Pola kristalinitas berdasarkan analisa XRD untuk pati kristalin) 16
Bentuk granula hasil pengujian SEM untuk 17
DAFTAR LAMPIRAN
Karakterisasi bahan baku, pati kristalin dan pati nanokristalin 25
Analisa statistik total gula pada filtrat 31
Analisa statistik kadar air 32
Analisa statistik kadar abu 34
Analisa statistik kadar serat kasar 36
Analisa statistik kadar amilosa 37
Analisa statistik daya cerna 38
Analisa statistik daya serap air 40
Analisa statistik daya serap minyak 42
PENDAHULUAN
Latar Belakang
Sagu merupakan salah satu bahan pangan penghasil karbohidrat yang belum dimanfaatkan secara maksimal. Potensi produksi maupun luas sagu di Indonesia sangat besar, tetapi baru sebagain kecil yang dimanfaatkan. Sekitar 50% tanaman sagu dunia atau 1.128 juta hektar tumbuh di Indonesia, dan 90% dari jumlah tersebut atau sebesar 1.015 juta hektar berkembang di Provinsi Papua dan Maluku (Lakuy dan Limbongan 2003). Satu juta hutan sagu di Indonesia, hanya sekitar 10-30% saja yang baru dimanfaatkan. Diperkirakan pula dari 40 juta ton cadangan pati sagu setiap tahun hanya 0.05-0.20% dimanfaatkan untuk keperluan ekspor dan konsumsi lokal dan sekitar 10% digunakan untuk bahan baku makanan tradisional, sedangkan sisanya sekitar ± 89% belum termanfaatkan.
Pemanfaatan pati di industri sangat luas, baik di bidang pangan maupun non pangan karena kemudahan mendapatkan bahan baku dan harganya yang relatif murah. Namun, beberapa sifat pati alami menjadi kendala apabila digunakan sebagai bahan baku industri, diantaranya sifat pati yang mudah rusak akibat panas dan asam.
Industri pengguna pati menginginkan pati yang mempunyai kekentalan yang stabil baik pada suhu tinggi maupun rendah, mempunyai ketahanan yang baik terhadap perlakuan mekanis, dan daya pengentalannya tahan pada kondisi asam dan suhu tinggi (Koswara 2006). Hal tersebut menjadi alasan dilakukan modifikasi pati agar mendapatkan sifat–sifat penting seperti kecerahannya lebih tinggi (pati lebih putih), retrogradasi yang rendah, kekentalannya lebih rendah, gel yang terbentuk lebih jernih, tekstur gel yang dibentuk lebih lembek, swelling power yang rendah, granula pati yang lebih mudah pecah, serta waktu dan suhu gelatinisasi yang lebih tinggi.
Lee et al. (2008) mengemukakan bahwa seiring dengan berkembangnya teknologi nano saat ini, berdampak pada meningkatnya kebutuhan bahan baku berukuran partikel kecil oleh industri baik industri pangan maupun non pangan yang mendorong dilakukan modifikasi terhadap pati alami. Pada asetilasi terjadi distribusi gugus asetil yang menggantikan gugus OH- yang akan mengurangi kekuatan ikatan hidrogen di antara pati dan menyebabkan granula pati menjadi lebih mengembang (banyak menahan air), mudah larut dalam air, serta meningkatkan freeze-thaw stability pati (Singh dan Sodhi 2004). Penelitian ini bertujuan untuk mengetahui pengaruh proses asetilasi pada karakterisasi pati sagu baik pada pati sagu alami, pati sagu lintnerisasi maupuan pati sagu nanokristalin.
Perumusan Masalah
Pati nanokristalin terasetilasi dapat dihasilkan melalui tiga tahapan, yaitu lintnerisasi, presipitasi dan asetilasi. Lintnerisasi merupakan modifikasi pati melalui hidrolisis asam pada konsentrasi rendah dan suhu kamar untuk memutus bagian amorf dari pati sehingga menghasilkan pati kristalin.
Fraksi yang dipresipitasi adalah larutan pati yang telah tergelatinisasi sempurna, sehingga dihasilkan partikel-partikel pati yang terpisah dengan pelarutnya. Etanol sebagai pelarut organik untuk presipitasi, diharapkan pati yang dihasilkan dapat berukuran nano.
Pada reaksi asetilasi terjadi subsitusi gugus hidroksil di unit anhidroglukosa pada molekul-molekul pati oleh gugus asetil yang berasal dari asetat anhidrida sehingga dihasilkan produk pati asetat. Pati asetat ini diharapkan memiliki suhu gelatinisasi, swelling power, solubility, dan tingkat kejernihan pasta yang tinggi, serta memiliki stabilitas penyimpanan dan pemasakan yang lebih baik jika dibandingkan dengan pati asalnya.
Tujuan Penelitian
Tujuan umum penelitian ini adalah produksi dan karakterisasi pati asetat dari pati sagu nanokristalin.
Tujuan khusus pada tiap tahapan penelitian ini adalah :
1. Mengetahui pengaruh konsentrasi asam asetat anhidrida terhadap karakteristik pati asetat yang dihasilkan.
2. Mengetahui perbedaan karakteristik pati asetat dari bahan baku pati alami, pati kristalin dan pati nanokristalin.
Manfaat Penelitian
Penelitian ini bermanfaat untuk mengetahui karakteristik fungsional dari pati nanokristalin terasetilasi sehingga dapat memperluas pemanfaatan pati. Pati nanokristalin terasetilasi yang dihasilkan dapat diaplikasikan dalam berbagai bidang, salah satunya pada bidang farmasi yang digunakan sebagai bahan pembawa pada obat-obatan. Proses asetilasi dapat meningkatkan hidrofobisitas pada pati. Dengan memanfaatkan pati nanokristalin terasetilasi sebagai matriks dalam pembawa bahan aktif atau obat-obatan ini maka obat yang dikonsumsi lebih tahan terhadap asam lambung dan obat tersebut dapat diadsorbsi lebih baik oleh komponen darah (Grislain et al. 1983).
Ruang Lingkup Penelitian
METODE
Bahan
Bahan baku pati sagu (Metroxylon sp.) diperoleh dari industri pati di daerah Cimahpar, Kota Bogor. Bahan-bahan kimia yang digunakan untuk menghasilkan pati asetat adalah larutan asam asetat anhidrida, NaOH, HCl 0.5 N, serta bahan kimia untuk analisa.
Alat
Peralatan yang digunakan dalam penelitian ini antara lain magnetic stirrer, pH meter, oven pengering, dan peralatan gelas yang digunakan untuk analisa.
Metode Penelitian
Penelitian ini dilaksanakan dalam tiga tahapan, yaitu tahap persiapan dan karakterisasi bahan baku, tahap pembuatan pati nanokristalin dan karakterisasinya serta tahap pembuatan pati asetat dan karakterisasinya
Penyiapan dan Karakterisasi Bahan Baku
Penyiapan bahan baku dilakukan dengan penjemuran bahan dan pengayakan hingga ukuran 100 mesh. Karakterisasi bahan baku meliputi kadar air, kadar abu, kadar lemak, kadar protein, kadar serat kasar, dan kadar amilosa. Prosedur analisa untuk karakterisasi bahan ini disajikan pada Lampiran 1.
Produksi Pati Asetat
a. Lintnerisasi Pati
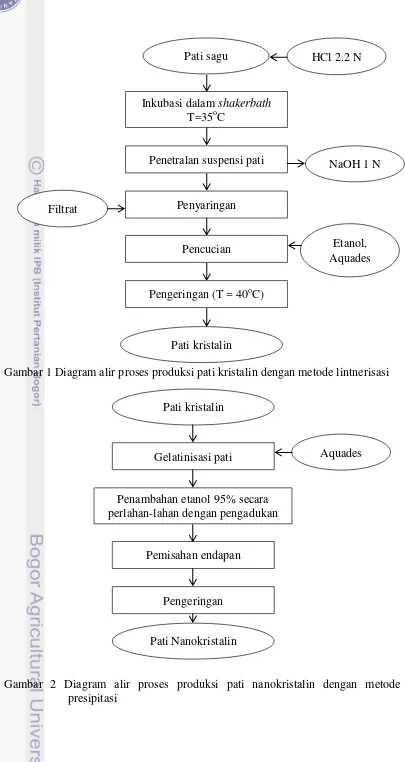
Pati lintnerisasi diproduksi dengan metode Faridah et al. (2010) serta Jayakody dan Hoover (2002). Pati dibuat suspensi dalam larutan HCl 2.2 N dengan perbandingan 1:2. Suspensi pati diinkubasi dalam shaker bath pada suhu 35oC selama 6 jam, di mana pada jam ke 0, 1, 2, 3, 4, 5, dan 6 diambil larutan pati sebanyak 2 ml untuk dilakukan uji total gula pereduksi. Suspensi pati yang telah mengalami perlakuan lintnerisasi kemudian dinetralkan dengan NaOH 1 N, selanjutnya dicuci dengan etanol dan akuades. Pati yang telah dicuci kemudian dikeringkan dalam oven pada suhu 40oC selama 24 jam hingga mencapai kadar air 10-12%. Setelah kering, pati digiling dengan disc mill dan diayak hingga ukuran 40 mesh. Diagram alir proses lintnerisasi disajikan pada Gambar 1.
b. Presipitasi Pati dengan Etanol
Gambar 1 Diagram alir proses produksi pati kristalin dengan metode lintnerisasi
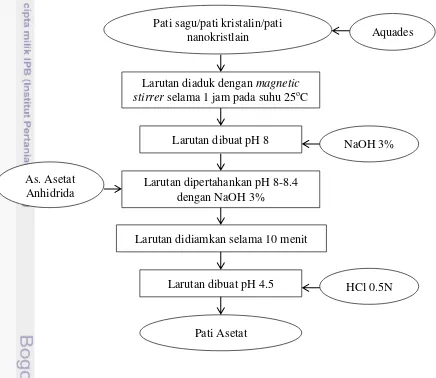
Gambar 2 Diagram alir proses produksi pati nanokristalin dengan metode presipitasi
Pati sagu
Inkubasi dalam shakerbath T=35oC
Penetralan suspensi pati
Penyaringan
Pencucian
Pati kristalin Filtrat
NaOH 1 N HCl 2.2 N
Pengeringan (T = 40oC)
Etanol, Aquades
Pati kristalin
Gelatinisasi pati
Penambahan etanol 95% secara perlahan-lahan dengan pengadukan
Pemisahan endapan
Pati Nanokristalin
Aquades
c. Asetilasi Pati
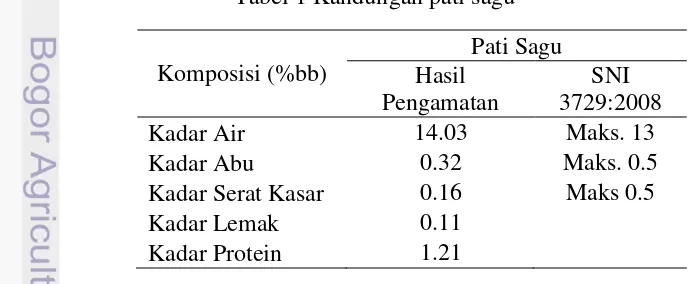
Metode asetilasi yang digunakan dalam penelitian ini adalah asetilasi menggunakan asam asetat anhidrida yang diadaptasi dari Phillips et al. (1999). Pati sagu, kristalin dan nanokristalin dilarutkan dalam air destilata 1 : 2.25 kemudian diaduk dengan magnetic stirrer selama 1 jam pada suhu 25oC. Kemudian ditambahkan NaOH 3%, setelah mencapai pH 8 ditambahkan asam asetat asetat anhidrida kemudian dipertahankan pHnya antara 8-8.4 dengan menggunakan NaOH 3%. Larutan didiamkan selama 10 menit, kemudian larutan dibuat menjadi pH 4.5 dengan penambahan HCl 0.5 N. Setelah pati tersendimentasi, pati dibilas dengan alkohol dan aquades, kemudian dikeringkan. Diagram alir proses asetilasi pati disajikan pada Gambar 3.
Gambar 3 Diagram alir proses pati asetat dengan metode asetilasi
Karakterisasi Pati Asetat
Karakterisasi pati asetat meliputi kadar air, kadar abu, kadar serat kasar, kadar amilosa, total gula, kristalinitas pati, daya cerna pati in vitro, struktur morfologi, daya cerna, daya serap air dan minyak, kelarutan dan swelling power pada pati, % asetilasi serta derajat subsitusi disajikan pada Lampiran 1.
Pati sagu/pati kristalin/pati nanokristlain
Larutan diaduk dengan magnetic stirrer selama 1 jam pada suhu 25oC
Larutan dibuat pH 8
Larutan dipertahankan pH 8-8.4 dengan NaOH 3%
Larutan didiamkan selama 10 menit As. Asetat
Anhidrida
NaOH 3% Aquades
Pati Asetat
Rancangan Percobaan
Rancangan percobaan yang digunakan pada penelitian ini adalah rancangan acak kelompok dengan perlakuan adalah konsentrasi asetat anhidrida (A) terhadap bobot pati dan yang menjadi kelompok adalah jenis pati (P) dengan keterangan : A1 : 3% asetat anhidrida
A2 : 6% asetat anhidrida P1 : Pati alami
P2 : Pati kristalin P3 : Pati nanokristalin
Bentuk hipotesa yang akan diuji adalah H0 : semua τi=0 (i = 1, 2, ..., t)
H1 : paling sedikit ada satu i dimana τi≠ 0 (i = 1, 2, ..., t)
Data yang diperoleh dari hasil penelitian dianalisa menggunakan software SPSS 21.
HASIL DAN PEMBAHASAN
Karakteristik Bahan Baku
air pada pati sagu yang akan digunakan belum memenuhi standar mutu yang ditentukan sehingga diperlukan pengeringan lebih lanjut agar diperoleh kadar air dibawah 13%. Pengeringan mempunyai tujuan untuk mengurangi kadar air sampai batas tertentu sehingga pertumbuhan mikroba dan aktifitas enzim penyebab kerusakan bahan dapat dihambat.
Kadar abu menunjukkan total mineral dalam suatu bahan pangan. Menurut Luallen (2004), sejumlah kecil mineral dan garam anorganik pada pati dianalisis sebagai abu. Abu merupakan residu yang tertinggal setelah suatu bahan pangan dibakar hingga bebas karbon. Semakin besar kadar abu suatu bahan, semakin tinggi pula mineral yang terkandung di dalamnya. Kadar abu digunakan untuk menentukan baik atau tidaknya suatu pengolahan bahan baku, mengetahui jenis bahan yang digunakan dan sebagai penentu parameter nilai gizi suatu bahan makanan. Kadar abu juga dapat berpengaruh terhadap warna dan tekstur pada pati. Berdasarkan hasil karakterisasi bahan baku, kadar abu pati sagu telah memenuhi standar mutu yang ditentukan yaitu 0.32%.
Kadar serat kasar merupakan komponen minor yang terdapat dalam pati. Serat terdiri dari selulosa, hemiselulosa, lignin, dan pektin. Beberapa sifat umum serat yaitu sukar diuraikan, memberi bentuk dan struktur pada tanaman, tidak larut dalam air dingin maupun air panas, tidak dapat dicerna oleh enzim pencernaan manusia sehingga tidak menghasilkan energi tetapi dapat membantu melancarkan pencernaan makanan. Umumnya bahan nabati memiliki kadar serat tinggi karena sel dari tumbuhan memiliki dinding sel. Berdasarkan hasil karakterisasi bahan baku, kadar serat kasar pati sagu telah memenuhi standar mutu yang ditentukan yaitu 0.16%.
Lemak dan minyak adalah bahan-bahan yang tidak larut dalam air, berasal dari tumbuh-tumbuhan dan hewan. Sebagain besar lemak dan minyak merupakan trigliserida dan berbagai jenis asam lemak (Buckle et al. 1985). Analisa kadar lemak yang dilakukan pada pati sagu menunjukan bahwa kadar lemak pada pati sagu adalah 0.11%. sedangkan kadar lemak pada pati sagu menurut Haryanto dan Pangloli (1992) adalah 0.23%.
Menurut Kaletunc dan Breslauer (2003), komponen nitrogen seperti protein, peptida, amida, asam amino, asam nukleat, dan enzim diduga ada dalam granula pati. Hasil analisa terhadap pati sagu diperoleh kadar proteinnya sebesar 1.21%. Kadar protein pati sagu menurut Ruddle et al. (1978) adalah 0.27%, sedangkan menurut Haryanto dan Pangloli (1992) kadar protein pati sagu adalah 0.81% dan menurut Djoefrie (1999) kadar protein pati sagu adalah 0.80%. Perbedaan kadar protein ini dapat disebabkan perbedaan tempat tumbuh dari tanaman sagu yang dianalisis.
Produksi Pati Nanokristalin Terasetilasi
van Bruggen (1993), daerah kristalin pada pati umumnya membentuk struktur superheliks. Struktur amilopektin pada daerah amorf dan kristalin dapat dilihat pada Gambar 4.
Gambar 4 Struktur amilopektin pada daerah (1) kristalin dan (2) amorf (Robin et al. 1974)
Penyiapan pati nanokristalin terasetilasi pada penelitian ini dilakukan dengan 3 tahapan proses, yaitu lintnerisasi (hidrolisis asam secara lambat), presipitasi dan asetilasi. Perlakukan lintnerisasi dilakukan dengan tujuan mendegradasi fraksi amilosa rantai panjang dan titik percabangan pada amilopektin yang terdapat pada daerah amorf sehingga dihasilkan fraksi amilosa rantai pendek dengan bobot molekul yang lebih rendah. Lehmann et al. (2003) mengemukakan bahwa jika fraksi amilosa rantai pendek dalam pati meningkat, maka akan semakin banyak fraksi amilosa yang terkristalisasi karena fraksi amilosa sebagai struktur linear akan memfasilitasi ikatan silang dengan adanya ikatan hidrogen sehingga struktur amilosa membentuk kristalit yang kompak. Dengan dilakukannya proses lintnerisasi, diharapkan pati yang dihasilkan mengalami peningkatan kristalinitas.
Proses lintnerisasi dilakukan dengan menggunakan asam kuat pada suhu dibawah suhu gelatinisasi pati. Asam kuat mampu menghidrolisis ikatan glikosidik sehingga menghasilkan amilosa dengan rantai yang lebih pendek dan bobot molekul menjadi lebih rendah. Pada proses ini terjadi dua tahap penyerangan yang terjadi di dalam granula pati, yaitu tahap penyerangan secara cepat pada daerah amorf dan tahap penyerangan yang lebih lambat pada fraksi amilopektin yang terdapat pada daerah kristalin (Wurzburg 1989). Ilustrasi perusakan daerah amorf dan kristalin pada proses lintnerisasi disajikan dalam Gambar 5. Pati kristalin diperoleh rendemen berkisar 83,75%-93,5%.
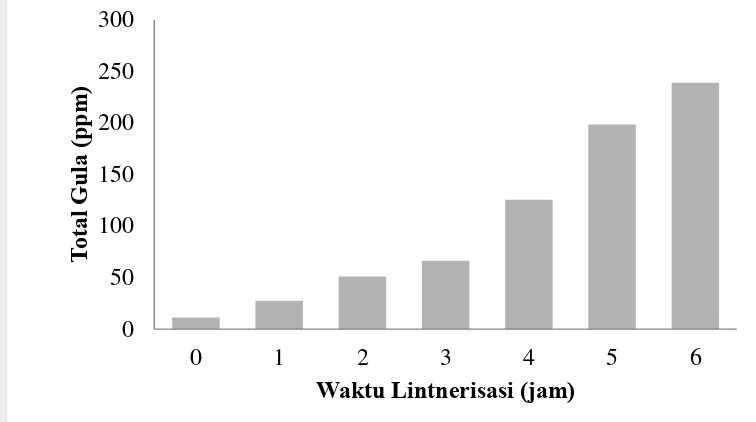
Proses lintnerisasi menyebabkan perusakan daerah amorf dalam granula pati. Daerah amorf merupakan daerah yang lebih mudah mengalami reaksi kimia dibandingkan pada daerah kristalin. Amilosa rantai panjang yang terdapat pada daerah amorf diputus oleh asam sehingga menjadi gula sederhana. Proses hidrolisis asam ini menyebabkan gula-gula sederhana yang terdapat dalam filtrat meningkat. Seiring dengan semakin lamanya waktu hidrolisis, semakin banyak pula ikatan-ikatan hidrogen yang terputus dan semakin meningkat pula gula sederhana dalam filtrat. Berdasarkan grafik yang ditampilkan pada Gambar 6, lintnerisasi total gula pada filtrat pati sagu meningkat seiring dengan bertambahnya waktu lintnerisasi. Hal ini menunjukkan bahwa semakin lama pati berinteraksi dengan asam, maka daerah amorf akan semakin banyak didegradasi. Berdasarkan analisa sidik ragam (Lampiran 2), dapat diambil kesimpulan bahwa kenaikan dari total gula berbeda secara signifikan.
Metode modifikasi pati secara asetilasi dengan derajat substitusi yang rendah telah digunakan secara luas oleh industri makanan selama bertahun-tahun. Hal ini disebabkan oleh keunggulan sifat fisika-kimia yang dimiliki oleh pati asetat seperti suhu gelatinisasi, swelling power, solubility, dan tingkat kejernihan pasta yang tinggi, serta memiliki stabilitas penyimpanan dan pemasakan yang lebih baik jika dibandingkan dengan pati asalnya (Raina et al. 2006). Selain itu, kualitas produk yang dihasilkan dari pati terasetilasi lebih stabil dan tahan terhadap retrogradasi.
Pada proses asetilasi, pengadukan dilakukan agar pati dan asetat anhidrida tercampur merata. Pada reaksi asetilasi terjadi subsitusi gugus hidroksil di unit anhidroglukosa pada molekul-molekul pati oleh gugus asetil yang berasal dari asetat anhidrida sehingga dihasilkan produk pati asetat. Reaksi asetilasi dapat dilihat di Gambar 7. Menurut Chen et al. (2004) reaksi asetilasi pada pati alami terjadi pada seluruh daerah amorf dan hanya berlangsung pada lamela bagian luar dari daerah kristalin dalam granula pati. Reaktifitas amilosa lebih tinggi daripada amilopektin oleh karena amilosa ada di daerah amorf, sedangkan amilopektin adalah penyusun daerah kristalin. Model asetilasi granula pati dengan asetat anhidrida disajikan pada Gambar 8. Proses asetilasi ini menghasilkan rendemen pati 64.9-88.9% untuk konsentrasi asam asetat anhidrida 3% dan 84.98-93.86% untuk konsentrasi asam asetat anhidrida 6%.
Gambar 8 Model asetilasi granula pati dengan asetat anhidrida : (1) daerah kristalin, dan (2) daerah amorf (Singh dan Sodhi 2004)
Karakteristik Pati Asetat
Pati merupakan bahan yang dapat dengan mudah mengalami perubahan karakteristik dari pati alaminya apabila mengalami perlakuan. Modifikasi pati menjadi pati nanokristalin terasetilasi yang dilakukan pada penelitian ini menghasilkan pati yang memiliki karakteristik yang berbeda dari pati alaminya seperti yang disajikan pada Tabel 2 dan Tabel 3.
Kadar Air
Kadar air produk berkisar antara 7.07% sampai dengan 14.025% seperti yang terlihat pada Tabel 2. Berdasarkan analisa sidik ragam pada Lampiran 3a terlihat pati alami tanpa proses asetilasi berbeda nyata kadar airnya dengan pati alami yang diasetilasi dengan konsentrasi asetat anhidrida 3% maupun 6%. Berbeda dengan pati kristalin dimana pati kristain yang tidak mengalami proses asetilasi maupun pati kristalin yang diasetilasi dengan konsentasi 3% maupun 6% saling berbeda nyata kadar airnya (Lampiran 3b), sedangkan pada pati nanokristalin tidak berbeda nyata kadar airnya dengan produk asetatnya (Lampiran 3c)
Kadar Abu
Kadar abu produk berkisar antara 0.12% sampai dengan 1.525% seperti yang terlihat pada Tabel 2. Berdasarkan analisa sidik ragam pada Lampiran 4a terlihat pati alami tanpa proses asetilasi berbeda nyata kadar abunya dengan pati alami yang diasetilasi dengan konsentrasi asetat anhidrida 3% maupun 6%. Hal yang sama juga terjadi pada pati kristalin, dimana pati kristalin tanpa proses asetilasi berbeda nyata kadar abunya dengan pati kristalin yang diasetilasi dengan konsentrasi asetat anhidrida 3% maupun 6% (Lampiran 4b). Berbeda dengan pati nanokristalin, pada pati nanokristalin tidak berbeda nyata kadar abunya dengan produk asetatnya (Lampiran 4c).
Kadar Serat Kasar
Kadar serat kasar produk asetilasi berkisar antara 0.14% sampai dengan 0.63% seperti yang terlihat pada Tabel 2. Berdasarkan analisa sidik ragam pada Lampiran 5a, terlihat pati alami tidak berbeda nyata kadar serat kasarnya dengan produk asetatnya. Hal yang sama juga terlihat pada pati kristalin dimana pati krisalin tidak berbeda nyata kadar serat kasarnya dengan produk aseatnya (Lampiran 5b). Berbeda dengan pati nanokristalin, pati nanokristalin yang diasetilasi dengan konsentrasi asetat 6% berbeda nyata dengan pati nanokristalin dan pati nanokristalin yang diasetilasi dengan konsentrasi asetat 3%.
Tabel 2 Pengaruh jenis pati dan konsentrasi asam asetat anhidrida terhadap karakteristik kimia pati terasetilasi
Tabel 3 Pengaruh jenis pati dan konsentrasi asam asetat anhidrida terhadap karakteristik fungsional pati terasetilasi
Parameter
Pati Alami Pati Kristalin Pati Nanokristalin
Kadar Amilosa
Amilosa dan amilopektin merupakan komponen utama penyusun pati. Secara umum pati sagu memiliki kandungan amilosa sebesar 27% (Swinkels 1985). Kandungan amilosa diukur berdasarkan kemampuan amilosa untuk luruh dalam air panas dan kemampuan dalam mengikat iod. Kandungan amilosa berpengaruh sangat kuat terhadap karakteristik produk. Semakin tinggi kandungan amilosa maka akan semakin mudah produk mengalami retrogradasi.
Kadar amilosa produk berkisar antara 0.14% sampai dengan 0.725% seperti yang terlihat pada Tabel 2. Berdasarkan analisa sidik ragam pada Lampiran 6a terlihat bahwa kadar amilosa pada pati alami berbeda nyata dengan kadar amilosa pati terasetilasi pada konsentrasi asetat anhidrida 3% dan 6%. Pada pati kristalin tidak terdapat perbedaan nyata dengan pati kristalin terasetilasi 3% dan 6%. (Lampiran 6b). Hal serupa juga terjadi pada kadar amilosa pati nanokristalin tidak terdapat perbedaan nyata dengan pati nanokristalin terasetilasi 3% dan 6%.
Pada Tabel 2 terlihat peningkatan kadar amilosa dari pati alaminya. Meningkatnya konsentrasi asam asetat anhidrida juga meningkatkan kadar amilosa. Perlakuan hidrolisis dengan asam selain menghasilkan pemutusan pada rantai amilosa, juga terjadi pada sebagian rantai amilopektin, yang berakibat meningkatnya kandungan amilosa (Saguilan et al., 2005). Selain itu Laga (2006) menyatakan bahwa peningkatan jumlah amilosa terjadi akibat putusnya rantai cabang amilopektin pada ikatan α 1-6 glikosida. Secara otomatis jumlah rantai cabang amilopektin akan berkurang dan meningkatkan jumlah rantai lurus amilosa sebagai hasil pemutusan ikatan cabang amilopektin. Menurut Chen et al., (2004) pada asetilasi, beragamnya derajat substitusi lebih banyak berhubungan dengan bagian amilopektin daripada bagian amilosa, terutama amilosa yang berada pada daerah kristalin, sementara rantai cabang amilopektin meningkatkan daerah amorf pada granula pati. Daerah kristalin yang berada di luar lamela lebih mudah bereaksi dengan asetat anhidrida menghasilkan derajat substitusi yang lebih tinggi dengan keberadaan amilopektin. Meningkatnya kadar amilosa tersebut bukan merupakan amilosa sebenarnya melainkan amilosa rantai pendek yang diperoleh dari pemotongan ikatan α 1-6 glikosida.
Kristalinitas Pati
Kristalinitas granula pati dapat dilihat menggunakan metode pola difraksi sinar X dan dapat ditentukan dengan integrasi kurva di bawah puncak daerah amorf dan kristalinnya. Puncak intensitas dari difraksi sinar X yang dihasilkan pada kurva berhubungan dengan daerah kristalin di dalam granula pati (Pomeranz dan Meloan 2000).
Tabel 4 Pengaruh jenis pati dan konsentrasi asetat anhidrida terhadap derajat kristalinitas dan tipe krisalin
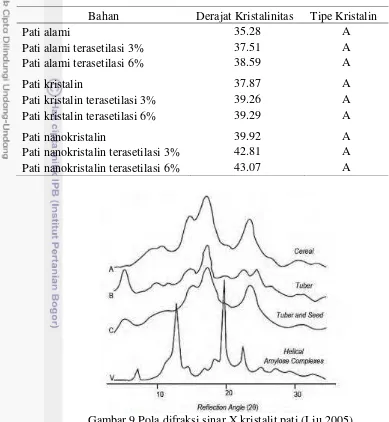
Gambar 9 Pola difraksi sinar X kristalit pati (Liu 2005)
Kristalit granula pati yang diamati dengan difraksi sinar X menunjukkan tiga tipe Kristal yaitu tipe A, B dan C. Rantai heliks ganda dari Kristal A dan B tersusun secara heksagonal, tetapi susunan dari tipe A lebih padat dari tipe B. Struktur tipe C merupakan kombinasi A dan B (Wang et al.1998). Kristalinitas relatif tipe A (31,0-37,1%) lebih besar dari tipe B (27,2-29,8%) dan C (27,8%) (Srichuwong et al. 2005). Pola difraksi sinar X dapat membedakan pola kristalinitas pati menjadi tipe A, B, C dan V seperti yang disediakan pada Gambar 9.
Berdasarkan Tabel 4, derajat kristalinitas mengalami kenaikan. Nilai derajat kristalinitas pada pati alami 35.28% setelah diasetilasi dengan konsentrasi 3% dan 6% mengalami kenaikan menjadi 37.51% dan 38.59%. Nilai derajat kristalinitas pada pati kristalin 37.87% setelah diasetilasi dengan konsentrasi 3% dan 6%
Bahan Derajat Kristalinitas Tipe Kristalin
Pati alami 35.28 A
Pati alami terasetilasi 3% 37.51 A
Pati alami terasetilasi 6% 38.59 A
Pati kristalin 37.87 A
Pati kristalin terasetilasi 3% 39.26 A
Pati kristalin terasetilasi 6% 39.29 A
Pati nanokristalin 39.92 A
mengalami kenaikan menjadi 39.26% dan 39.29%. Nilai derajat kristalinitas pada pati nanokristalin 39.92% setelah diasetilasi dengan konsentrasi 3% dan 6
Tipe kristalin dari pati alami, pati kristalin dan pati nanokristalin beserta produk asetilnya dari hasil pengukuran difraksi sinar X dapat dilihat pada Gambar 10, Gambar 11 dan Gambar 12. Srichuwong et al. (2005) menyatakan bahwa pati sagu memiliki kristalin tipe A. Hal ini bersesuaian dengan yang diperoleh dalam penelitian yang juga menunjukkan kristalin tipe A. Kristalin tipe A ditandai dengan puncak pada 2 tetra yaitu 15o, 17o, 20o dan 23o. Proses asetilasi hanya menyerang daerah amorf sehingga derajat kristalinitas setelah asetilasi tidak banyak berubah dan tidak mengubah tipe kristalin.
Gambar 10 Pola kristalinitas berdasarkan analisa XRD untuk pati alami (a), pati alami asetat 3% (b) dan pati alami asetat 6% (c)
Gambar 11 Pola kristalinitas berdasarkan analisa XRD untuk pati kristalin (a), pati kristalin asetat 3% (b) dan pati alami asetat 6%
a b c
10 12 14 16 18 20 22 24 26 28 30 32 34
In
te
n
si
tas
2θ
Gambar 12 Pola kristalinitas berdasarkan analisa XRD untuk pati nanokristalin (a), pati nanokristalin terasetilasi 3% (b) dan pati nanokristalin terasetilasi 6% (c)
Morfologi Granula Pati
Granula pati dalam jaringan tanaman mempunyai bentuk yang beragam. Dengan mikroskop, granula pati dapat dibedakan berdasarkan perbedaan bentuk dan sifat birefringent-nya (Winarno 1980).
Daya Cerna Pati
Daya Cerna Pati
Karbohidrat dari pati yang akan diserap oleh tubuh harus diubah dahulu menjadi komponen penyusunnya yaitu glukosa. Enzim yang dibutuhkan untuk mengubah menjadi glukosa yaitu α-amilase yang berasal dari saliva dan diinaktivasi oleh pH rendah dalam lambung sehingga tidak terlalu berperan dalam proses pencernaan pati. Enzim α-amilase yang berasal dari pankreas akan berperan memecah pati pada usus halus. Proses tersebut akan diselesaikan pada bagian brush border usus halus dengan bantuan dari enzim glukoamilase dan α -dekstrinase. Selain itu akan terjadi pemecahan disakarida menjadi monosakarida oleh enzim disakaridise (Sardesai 2003).
Proses pencernaan pati dapat dipengaruhi oleh faktor intrinsik dan faktor ekstrinsik. Faktor intrinsik yang menyebabkan pati menjadi lambat dicerna di dalam usus halus yaitu jika bentuk fisik makanan mengganggu pengeluaran amilase pankreatik, khususnya jika granula pati terhalang oleh material lainnya. Sedangkan faktor ekstrinsik yang mempengaruhi daya cerna pati adalah bentuk makanan, konsentrasi amilase dalam usus, jumlah pati, dan adanya komponen pangan lainnya (Mahadevamma et al. 2003).
Berdasarkan Tabel 3, daya cerna pati mengalami penurunan. Nilai daya cerna pati pada pati alami 88.48% setelah diasetilasi dengan konsentrasi 3% dan 6% mengalami penurunan menjadi 69.08% dan 65.46%. Nilai daya cerna pati pada pati kristalin 86.02% setelah diasetilasi dengan konsentrasi 3% dan 6% mengalami penurunan menjadi 62.32% dan 61.06%. Nilai daya cerna pati pada pati nanokristalin 80.25% setelah diasetilasi dengan konsentrasi 3% dan 6% mengalami penurunan menjadi 58.93% dan 56.65%.
Berdasarkan analisa sidik ragam pada Lampiran 7a terlihat bahwa daya cerna pati alami, pati alami yang diasetilasi dengan konsentrasi asetat anhidrida 3% maupun 6% saling berbeda nyata daya cerna patinya. Daya cerna pati kristalin yang tidak mengalami proses asetilasi berbeda nyata daya cerna patinya dengan pati kristalin yang diasetilasi dengan konsentrasi asam asetat 3% maupaun 6% (Lampiran 7b). Hal yang sama juga ditunjukkan pada pati nanokristalin, dimana pati nanokristalin yang tidak mengalami proses astilasi berbeda nyata daya cerna patinya dengan pati nanokristalin yang diasetilasi dengan konsentrasi asam asetat 3% maupun 6% (Lampiran 7c).
Penurunan daya cerna pati disebabkan pada saat lintnerisasi menyebabkan meningkatnya jumlah rantai polimer yang berbobot molekul rendah dan molekul amilosa rantai pendek. Bertambahnya jumlah fraksi amilosa rantai pendek akan memudahkan pati mengalami retrogradasi (Sajilata et al. 2006). Pada proses presipitasi terjadi retrogradasi pati dimana menyebabkan perubahan struktur amilosa dan amilopektin yang dapat menyebabkan perubahan kristanilitas pati yang juga berpengaruh terhadap perubahan sifat daya cerna pada pati yang dihasilkan. Penurunan daya cerna juga terjadi pada proses asetilasi, semakin tinggi konsentrasi asam asetat maka daya cerna menjadi lebih rendah.
Daya Serap Air dan Minyak
Daya serap air merupakan sifat fisik dan kemampuan struktur bahan dalam mencegah terlepasnya air dari struktur tiga dimensi bahan pangan tersebut (Zayas 1997). Daya serap air pada pati dapat ditentukan oleh ukuran granula pati dan struktur kimia dalam pati tersebut. Nilai daya serap air pada pati sagu yang telah diasetilasi mengalami penurunan dari pati alaminya. Pada pati alami mengalami penurunan dari 90.30% menjadi 65.30% pada pati terasetilasi 3%, pada pati terasetilasi 6% juga mengalami penurunan menjadi 63.90%. Nilai daya serap air pada pati kristalin 76.30% setelah diasetilasi dengan konsentrasi 3% dan 6% mengalami penurunan menjadi 62.50% dan 61.60%. Nilai daya serap air pada pati nanokristalin 69.90% setelah diasetilasi dengan konsentrasi 3% dan 6% mengalami penurunan menjadi 58.40% dan 52.60%.
Berdasarkan analisa sidik ragam pada Lampiran 8a terlihat bahwa daya serap air pada pati alami yang tidak mengalami proses asetilasi berbeda nyata daya serap airnya dengan pati alami yang diasetilasi dengan konsentrasi asetat anhidrida 3% maupun 6%. Hal yang sama juga terlihat pada pati kristalin dimana pati kristalin yang tidak mengalami proses asetilasi berbeda nyata daya serap airnya dengan pati kristalin yang diasetilasi dengan konsentrasi asetat anhidrida 3% maupun 6% (Lampiran 8b). Berbeda dengan daya serap air pati nanokristalin, pati nanokristalin yang tidak mengalami proses asetilasi, pati nanokristalin yang diasetilasi dengan konsentrasi asetat anhidrida 3% maupun 6% saling berbeda nyata (Lampiran 8c).
Adanya kemampuan menyerap minyak pada pati menunjukkan bahwa pati memiliki bagian yang bersifat lipofilik. Afdi (1989) mengemukakan bahwa daya serap minyak dipengaruhi oleh adanya protein pada permukaan granula pati, di mana protein ini dapat membentuk kompleks yang dapat memberikan tempat terikatnya minyak pada pati.
kembali amilosa yang terjadi selama proses presipitasi sehingga tidak dapat membentuk komplek amilosa-lipid.
Nilai daya serap minyak pada pati alami 66.40% setelah diasetilasi dengan konsentrasi 3% mengalami peningkatan menjadi 73.8% dan diasetilasi dengan konsentrasi 6% mengalami penurunan menjadi 57.80%. Nilai daya serap minyak pada pati kristalin 50.50% setelah diasetilasi dengan konsentrasi 3% dan 6% mengalami penurunan menjadi 46.90% dan 48%. Nilai daya serap minyak pada pati nanokristalin 48.10% setelah diasetilasi dengan konsentrasi 3% dan 6% mengalami penurunan menjadi 38.5% dan 31.6%. Berdasarkan analisa sidik ragam pada Lampiran 8 terlihat bahwa daya serap minyak pada ketiga jenis bahan tidak berbeda nyata.
Kelarutan dan Swelling Power
Swelling power didefinisikan sebagai pertambahan volume dan berat maksimum yang dialami pati dalam air (Balagopalan et al. 1998). Swelling power terjadi pada daerah amorf granula pati. Ikatan hidrogen yang lemah antar molekul pati pada daerah amorf akan terputus saat pemanasan, sehingga terjadi hidrasi air oleh granula pati. Granula pati akan terus mengembang, sehingga viskositas meningkat hingga volume hidrasi maksimum yang dapat dicapai oleh granula pati (Swinkels 1985). Menurut Pomeranz (1991), kelarutan pati semakin tinggi dengan meningkatnya suhu, serta kecepatan peningkatan kelarutan adalah khas untuk tiap pati.
Proses lintnerisasi berpengaruh terhadap sifat swelling power karena selama proses hidrolisis, asam mendegradasi daerah amorf yang berperan sebagai pengembangan pati. Pada proses presipitasi terjadi peningkatan swelling power yang disebabkan granula pati yang telah dipresipitasi memiliki ukuran yang lebih kecil dan pada saat dilakukan pemanasan ikatan hidrogen pada granula mudah terganggu dan granula mudah membengkak. Proses asetilasi juga mempengaruhi nilai dari swelling power. Semakin besar volume asam asetat maka nilai swelling powernya dan kelarutannya semakin naik. Peningkatan swelling power disebabkan adanya substitusi gugus asetil yang menggantikan gugus hidroksil sehingga ikatan hidrogen menjadi lemah dan akhirnya menyebabkan struktur granula pati menjadi kurang rapat. Hal ini dapat memfasilitasi akses air pada daerah amorf.
Kenaikan konsentrasi asetat anhidrida meningkatkan persen kelarutan, hal ini disebabkan karena melemahnya ikatan hidrogen di dalam pati yang dimodifikasi. Melemahnya ikatan hidrogen di dalam pati memudahkan air untuk masuk ke dalam granula pati sehingga kelarutan meningkat (Singh dan Sodhi 2004). Perbandingan antara amilosa dan amilopektin juga berpengaruh terhadap sifat kelarutan pati. Amilopektin bersifat tidak larut dalam air. Pada proses modifikasi semakin tinggi konsentrasi asetat anhidrida maka semakin banyak senyawa amilopektin yang tereduksi sehingga pati yang dihasilkan semakin mudah larut dalam air, sehingga menyebabkan persen kelarutan.
diasetilasi dengan konsentrasi asetat anhidrida 3% maupun 6% saling berbeda nyata (Lampiran 11a). Swelling power pada pati kristalin tidak berbeda nyata dengan pati kristalin yang diasetilasi dengan konsentrasi asetat anhidrida 3% maupun 6% (Lampiran 10b) tetapi pada kelarutan pati kristalin yang tidak mengalami proses asetilasi berbeda nyata dengan pati kristalin yang diasetilasi dengan konsentrasi asetat anhidrida 6% (Lampiran 11b).Lain halnya dengan pati nanokristalin, pati nanokristalin yang tidak mengalami proses asetilasi berbeda nyata swelling power dan kelarutannya dengan pati nanokristalin yang diasetilasi dengan aseat anhidrida 3% maupun 6%. (Lampiran 10c dan Lampiran 11c)
% Asetil dan Derajat Subsitusi
Derajat subtitusi adalah jumlah rata-rata gugus hidroksil tiap satuan asetat anhidrida yang telah disubtitusi oleh subtituen. Derajat subtitusi berhubungan dengan kadar asetil (%). Kadar asetil yang tinggi memberikan derajat subtitusi yang tinggi. Menurut Wurzbug (1995) gugus asetil dapat dihubungkan dengan derajat subtitusinya. Setiap satu molekul glukosa mengandung tiga gugus hidroksil yang dapat disubtitusi pada atom C nomor 2, 3 dan 6.
Rerata kadar asetil pati sagu termodifikasi asetat berkisar antara 1.075-1.6125%. Berdasarkan analisa sidik ragam (Lampiran 12), dapat diambil kesimpulan bahwa terdapat perbedaan kadar asetil antara konsentrasi 3% dan konsentrasi 6%. Perlakuan konsentrasi 6% memberikan kadar asetil tertinggi. Menurut Seib dan Woo (1999) efektifitas asetilasi dipengaruhi oleh beberapa faktor yaitu lama reaksi, konsentrasi reagen asetilasi, temperature dan pH.
Derajat substitusi gugus hidroksil menjadi gugus asetil pada pati sagu termodifikasi asetat berkisar antara 0,0409 sampai 0,0617. Hasil analisa sidik ragam (Lampiran 13) menunjukan bahwa terdapat perbedaan derajat substitusi pada konsentrasi 3% dan konsentrasi 6%. Derajat substitusi tertinggi terdapat pada konsentrasi 6%.
Menurut Xu et al. (2004), derajat substitusi meningkat karena asam asetat tinggi tidak hanya menimbulkan suatu tingkat benturan molekul yang tinggi tetapi juga ketersediaan molekul-molekul asam asetat yang besar di sekitar pati. Menurut U.S Food Drug Administration (FDA) pati asetat yang bisa digunakan untuk produk pangan adalah pati asetat dengan derajat asetat rendah, yaitu antara 0,01-0,1.
SIMPULAN DAN SARAN
Simpulan
Proses asetilasi pati sagu nanokristalin yang memiliki kemampuan daya cerna pati yang rendah, daya serap air, daya serap minyak dan swelling power yang rendah akan tetapi memiliki kelarutan yang tinggi.
daya cerna pati dimana semakin tinggi konsentrasi asam asetat yang digunakan maka semakin rendah daya cerna dari pati.
Perlakuan asetilasi pada pati alami, pati kristalin dan pati nanokristalin menurunkan daya serap air dan minyak. Daya serap air terendah yaitu pati nanokristalin dengan nilai 2.92 untuk konsentrasi asetat anhidrida 3% dan 2.64 konsentrasi asetat anhidrida 6%. Daya serap minyak terendah yaitu pati nanokristalin dengan nilai 1.93 untuk konsentrasi asetat anhidrida 3% dan 1.58 konsentrasi asetat anhidrida 6%. Konsentrasi asetat anhidrida juga mempengaruhi daya serap air dan minyak dimana semakin tinggi konsentrasi asam asetat yang digunakan maka semakin rendah daya serap air dan minyak dari pati.
Perlakuan asetilasi pada pati alami, pati kristalin dan pati nanokristalin meningkatkan kelarutan dan penurunan swelling power. Kelarutan tertinggi yaitu pati nanokristalin dengan nilai 75.03% untuk konsentrasi asetat anhidrida 3% dan 82.45% konsentrasi asetat anhidrida 6%. Konsentrasi asetat anhidrida juga mempengaruhi kelarutan dan swelling power dimana semakin tinggi konsentrasi asam asetat yang digunakan maka semakin tinggi kelarutan dan swelling power dari pati.
Saran
Perlunya dilakukan pembuatan pati nanokristalin yang menjadi perubahan adalah perbedaan ukuran yang dihasilkan dan perlunya juga dilakukan proses asetilasi dengan menggunakan pelarut asetat lain dan perlakuan lain seperti lama perendaman asetat, suhu, pH serta penambahan katalis untuk mengetahui perbedaan karakteristik pati asetat yang dihasilkan.
DAFTAR PUSTAKA
Afdi E. 1989. Modifikasi pati jagung (Zea mays) [tesis]. Bogor (ID): Institut Pertanian Bogor.
AOAC, 1995. Official Methods of Analysis of The Association of Agriculture Chemist. Washington DC (US): Association of Official Analytical Chemist. AOAC, 1998. Official Methods of Analysis of The Association of Analytical
Chemists. Washington DC (US): Association of Official Analytical Chemist. AOAC, 2000. Official Methods of Analysis of The Association of Analytical
Chemists 17th ed. Washington DC (US): Association of Official Analytical Chemis.
Anderson AK, Guraya HS, James C, Salvaggio L. 2002. Digestibility and pasting properties of rice starch heat-moisture treated at the melting temperature. Starch. 54:401-409.
Badan Standarisasi Nasional. 2008. SNI 3729 : Tepung Sagu. Jakarta (ID): Badan Standarisasi Nasional.
Badan Standarisasi Nasional. 1992. SNI 01-2891-1992: Cara Uji Makanan Minuman. Jakarta (ID): Badan Standarisasi Nasional.
physicochemical and structural characteristics of barley starch. LWT-Food Sci. Technol.43:1434-1440.
BeMiller JN, Whistler RL. 1996. Carbohydrates. OR Fennema, editor. Food Chemistry. Ed k-3. New York (US): Marcel Dekker.
Buckle KA, Edwards RA, Fleet GF, Wooton M. 1985. Ilmu Pangan. Diterjemahkan oleh H. Purnomo dan Adiono. Jakarta (ID): UI Press.
Buleon A, Colonna P, Planchot V, Ball S. 1998. Starch granules: structure and biosynthesis. Int J Biol Macromol. 23:85-112.
Brautlecht CA. 1953. Starch, Its Sources, Production and Uses. New York (US): Reinhold.
Chen Z, Schols HA, Voragen AGJ. 2004. Differently Sized Granules from Acetylated Potato and Sweetpotato Starches Differ in the Acetyl Substitution Pattern of their Amylose Populations. Carbohydr Polym. 56 : 219 – 226.
Dubois M, Gilles KA, Hamilton JK, Rebers PA, Smith F. 1956. Colorimetric Method for Determination of Sugars and Related Substance. Analytical Chem. 28:350-356.
Djoefrie MHB. 1999. Pemberdayaan Tanaman Sagu Sebagai Penghasil Bahan Pangan Alternatif dan Bahan Baku Agroindustri Potensial Dalam Rangka Ketahanan Pangan Nasional. Fakultas Pertanian. Bogor (ID) : IPB.
Faridah DN, Fardiaz D, Andarwulan N, Sunarti TC. 2010. Perubahan struktur pati garut (Maranta arundinaceae) sebagai akibat modifikasi hidrolisis asam, pemotongan titik percabangan dan siklus pemanasan-pendinginan. J Teknol dan Indust Pangan. 21(2):135-142.
Grislain, L Couvreur, P Lenaerts, V Roland, M Deprez Decampeneere, D Speiser. 1983. Pharmacokinetics and Distribution of a Biodegradable Drug-carrier, Int. J Pharm. 15, 335-345.
Haryanto B, Pangloli P. 1992. Potensi dan Pemanfaatan Sagu. Yogyakarta (ID): Kanisius.
Jacobs H, Delcour JA. 1998. Hydrothermal modifications of granular starch with retention of the granular structure: a review. J Agr Food Chem. 46:2895-2905. Jayakody L, Hoover R. 2002. The effect of lintnerization on cereal sarch granules.
Food Res Int. 35:665-680.
Kalentuc G dan KJ Breslauer. 2003. Characterization of Cereals dan Flours. New York (US): Marcel Dekker.
Koswara S. 2009. Teknologi Modifikasi Pati. [Internet]. [diunduh 2014 Januari 20]. Tersedia pada: http://tekpan.unimus.ac.id/wp-content/uploads/2013/07/ TEKNOLOGI-MODIFIKASI-PATI.pdf.
Nasional Sagu Manado; 2003 Oktober 6; Manado, Indonesia. Manado (ID): Balai Penelitian Tanaman Kelapa dan Palma Lain. hlm 41-47.
Lee SB, Lee JY, Song DG, Pan CH, Nho CW, Kim MC. 2008 Cancer chemopreventive effects of Korean seaweeds extracts. Food Sci Biotechnol. 17:613-622.
Lehmann U, Rossler C, Schmiedl D, Jacobash G. 2003. Production and physicochemical characterzation of resistant starch type 3 derived from pea. Starch/Nahrung/Food. 43:60-63.
Liu Q. 2005. Understanding starches and their role in foods. Didalam: Food Carbohydrates: Chemistry, Physical Properties and Applications. Boca Raton(US): Taylor & Francis.
Luallen T. 2004. Utilizing Starch in Product Development. Eliasson AC, editor. Boca Raton (US): CRC Pr.
Ma X, Jian R, Chang PR, Ju Y. 2008. Fabrication and characterization of citric acid-modified starch nanoparticles/ plasticized-starch composites. Biomacromolecular. 9(11):3314-3320.
Mahadevamma MS, Harish KVP, Tarathanan RN. 2003. Resistant starch derived from processed legumes: purification and structura characterization. J Carbohdyr Polym. 54:215-219.
Medcalf DG, Gilles KA. 1965. Wheat starches: comparison of physicochemical properties. Cereal Chem. 42:558-568.
Oostergetel GT, Bruggen EFJV. 1993. The crystalline domains in potato starch granules are arranged in a helical fashion. Carbohydr Polym. 21:7-12.
Phillips DL, Huijum L, Duohai P, Harold C.1999. General application of Raman spectroscopy for the determination of levelof acetylation in modified starches. Cereal Chem. 76:439–443.
Pomeranz Y. 1991. Functional Properties of Food Components. Second Edition. New York (US): Academic Pr.
Robin JP, Mercier C, Charbonniere R, Guilbot A. 1974. Lintnerized starches gel filtration and enzymati studies of insoluble residues from prolonged acid treatment of potato starch. Cereal Chem. 51:389-406.
Ruddle K, Johnson D, Townsend PK, Rees JD. 1978. Palm Sago A Tropical Starch from Marginal Lands. Honolulu (HI): East-West Center Book.
Saguilan AA, Flores-Huicochea E, Tovar J, Garcia SF, Gutierres MF, Bello LAP. 2005. Resistant starch-rich powders prepared by autoclaving of native and lintnerized banana starch : partial characterization. J Starch. 57:405-412. Sajilata MG, Rekha SS, Puspha RK. 2006. Resistant starch –a review. J Compr
Rev in Food Sci Food Safety. 5:1-17.
Sardesai VM. 2003. Introdution to Clinical Nutrition. New York (NY): Marcel Dekker.
Singh N, Sodhi NS. 2004. Characteristics of Acetylated Starches Prepared Using Starches Separated from Different Rice Cultivars. J Food Eng. 70:117-127. Srichuwong S, Sunarti TC, Mishima T, Isno H, Hisamatsu M. 2005. Starches
from different botanical sources I: contribution of amylopectin fine structure to thermal properties and enzyme digestibility. Carbohydr Polym. 60:529-538. Srichuwong S. 2006. Starches from different plant origins: from structure to
physicochemical properties [disertasi]. Japan (JP): Mie University.
Swinkles JJM. 1985. Sources of starch, its chemistry and physics. Roels JA, Beynum GMAV, editor. New York (US): Marcel Dekker.
Wang TL, Bogracheva TY, Hedley CL. 1998. Starch: as simple as A, B, C? [ulasan]. J Exp Bot. 49:481-502.
Whistler RL, Daniel JR. 1995. Carbohydrates. Fennema OR, editor. New York (US): Marcel Decker.
Winarno FG. 1980. Kimia Pangan dan Gizi. Jakarta (ID): Gramedia Pustaka Utama.
Wirakartakusumah MA, Apriyanto A, Ma’arif M, Suliantari S, Muchtadi D, Otaka. 1986. Isolation and Characterization of Sago Liquid Sugar. Paper FAO-BPPT. Jakarta.
Wurzburg OB. 1978. Starch, modified starch and dextrin. Products of the corn refining industry : Seminar proceedings. Washington (US): Corn Refiners Association.
Wurzburg OB. 1989. Modified Starches: Properties and Uses. Boca Raton (US): CRC Press.
Wurzburg OB. 1995. Modified Starch. In Food Polysaccarides and Their Application. Stephen, editor. New York (US): Macel Dekker.
Xu XY, Miladinov V, Hanna MA. 2004. Synthesis and Characterization of Starch with High Substitution. Cereal Chem. 81(6)735-740.
Yamazaki WT. 1953. An alkaline water retention capacity test for the evaluation of cookies in baking potentialities of soft winter wheat flours. Cereal Chem. 30:242-246.
Lampiran 1 Karakterisasi bahan baku, pati kristalin dan pati nanokristalin
1. Kadar air (AOAC 2000)
Pengujian kadar air pada bahan ini tercantum dalam SNI 3729:2008 yang mengacu pada AOAC Official Method 2000 925.10. prinsipnya adalah kehilangan berat yang terjadi pada pemanasan dalam oven dengan suhu 130oC selama 1 jam. Mula-mula cawan dipanaskan dalam oven pada suhu 130±3oC selama 1 jam, kemudian didinginkan dalam desikator selama 30 menit dan ditimbang (W1). Sampel ditimbang sebanyak 2 g kemudian dimasukkan ke dalam cawan aluminium (W). Cawan dimasukkan dalam oven pada suhu 130±3oC selama 1 jam. Didinginkan dalam desikator selama 30 menit kemudian ditimbang (W2).
W = Bobot sampel (g)
W1 = Bobot cawan kosong (g) W2 = Bobot cawan + sampel (g)
2. Kadar Abu (AOAC 2000)
Pengujian kadar abu pada bahan ini tercantum dalam SNI 3729:2008 yang mengacu pada AOAC Official Method 2000 923.03. Prinsip dari uji ini adalah pengabuan sampel dalam tanur pada suhu 550oC, zat-zat organik diuraikan menjadi air dan CO2, sedangkan zat-zat anorganik yang tertinggal dihitung sebagai kadar abu. Cawan porselen dipijarkan dalam tanur pada suhu 550±10oC. Sebelumnya dipanaskan terlebih dahulu pada penangas bunsen/listrik dengan nyala api kecil selama 1 jam. Cawan kemudian didingkan dalam desikator selama 1 jam kemudian ditimbang (W1). Sebanyak 3-5 sampel (W) dimasukkan dalam cawan, kemudian diarangkan di atas penangas bunsen/listrik dengan nyala api kecil. Setelah itu diabukan dalam tanur pada suhu 550±10oC sampai putih atau kelabu selama 5-8 jam. Didinginkan dalam desikator selama 30 menit kemudian ditimbang (W2).
W = Bobot sampel (g)
W1 = Bobot cawan kosong (g) W2 = Bobot cawan + abu (g)
3. Kadar Serat Kasar (SNI 3729:2008)
ml larutan H2SO4 1.25%, kemudian didihkan selama 30 menit dengan menggunakan pendingin tegak. Ditambahkan 50 ml NaOH 3.25% dan didihkan lagi selama 30 menit. Dalam keadaan panas, saring dengan corong buchneryang berisi kertas saring Whatman yang telah dikeringkan dan diketahui bobotnya. Endapan yang terdapat pada kertas aring berturut-turut dicuci dengan H2SO4 1,25% panas, air panas, dan etanol 96%. Kertas sarig berserta isinya diangkat, dimasukkan ke dalam kotak timbang yang telah diketahui bobotnya, dikeringkan pada suhu 105oC, didinginkan dan ditimbang sampai bobot tetap (W1).
W = Bobot sampel (g)
W1 = Bobot endapan pada kertas saring (g)
4. Kadar Amilosa modifikasi metode IRRI (AOAC 1995)
- Pembuatan Kurva Standar
Sebanyak 40 mg amilosa standar ditambahkan dengan 1 ml etanol 95% dan 9 ml NaOH 1N lalu dipanaskan pada suhu 80-100oC selama ± 10 menit sampai tergelatinisasi. Kemudian larutan didinginkan lalu dimasukkan ke dalam labu takar 100 ml dan ditera dengan akuades. Selanjutnya dari labu takar tersebut dibuat beberapa konsentrasi mulai dari 50, 100, 150, sampai 300 ppm. Sampel diambil sebanyak 1ml dari masing-masing konsentrasi lalu ditambahkan 0,1 ml iod 0.2%, 0.2 ml asam asetat 1N, dan 3 ml akuades. Setelah didiamkan selama 20 menit, diukur nilai absorbansi pada spektrofotometer dengan panjang gelombang 620 nm.
- Analisa Sampel
Sebanyak 100 mg sampel dilarutkan dalam 1 ml etanol 95% dan 9 ml NaOH 1N. Kemudian larutan dipanaskan pada suhu 80-100oC selama ± 10 menit sampai tergelatinisasi. Larutan didinginkan lalu ditera pada labu takar 100 ml dengan akuades sebagai larutan induk. Selanjutnya diambil 1 ml sampel yang telah diencerkan dari larutan induk. Sampel tersebut ditambahkan dengan 0,1 ml iod 0.2%, 0.2 ml asam asetat 1 N, dan 3 ml akuades. Setelah didiamkan selama 20 menit lalu diukur nilai absorbansi pada spektrofotometer dengan panjang gelombang 620 nm.
Konsentrasi pati x faktor pengenceran bobot sampel
Kadar amilosa (%)= =
5. Total Gula pada Filtrat dengan Metode Fenol-Sulfat (Dubois et al. 1956)
Sampel sebanyak 1 ml (mengandung ≤ 100 μg karbohidrat) ditambahkan dengan 0.5 ml larutan fenol 5% kemudian dikocok-kocok dengan vortex agar homogen. Dilakukan penambahan 2.5 ml H2SO4 secara langsung pada bagian permukaan (tanpa menyentuh dinding tabung reaksi). Reaksi pencampuran didiamkan tanpa gangguan selama 10 menit. Pembacaan nilai absorbansi dilakukan minimal 30 menit setelah pengocokan pada panjang gelombang 490 nm.
Pembacaan pada spektrofotometer memberikan nilai dalam satuan absorbansi sehingga untuk mengetahui jumlah total gula dalam sampel tesebut, terlebih dahulu dibuat kurva standar glukosa. Untuk pembuatan kurva standar glukosa digunakan glukosa standar (0, 10, 20, 30, 40, 50 dan 60 ppm). Masing- masing diambil 1 ml sesuai dengan prosedur pengukuran total gula. Hasil pembacaan pada spektrofotometer dikumpulkan dan dicari persamaannya, dari persamaan inilah dapat diketahui jumlah total gula yang terdapat di dalam sampel.
6. Daya Serap Air dan Minyak
Pengukuran daya serap air dan minyak pada pati ini dilakukan berdasarkan metode Yamazaki (1953) yang dimodifikasi oleh Medcalf dan Gilles (1965). Sebanyak 5 g pati dimasukkan ke dalam tabung sentrifugasi, kemudian ditambahkan 75 ml akuades atau minyak. Suspensi pati didiamkan selama 1 jam, kemudian disentrifugasi (3000g) selama 10 menit. Bobot endapan dihitung sebagai daya serap air atau minyak.
7. Kelarutan dan Swelling Power (Modifikasi metode Bello-Perez et al. 2010)
Suspensi pati disiapkan yaitu 0.5 g sampel dicampur dengan 50 ml aquades dalam labu erlenmeyer 250 ml. Sampel ditempatkan pada penangas air pada suhu 70°C selama 2 jam dengan pengadukan secara kontinyu. Pada suspensi tersebut diambil 30 ml larutan yang jernih kemudian diletakkan pada cawan petri yang telah diketahui bobotnya. Cawan petri dikeringkan pada oven 100°C hingga bobotnya tetap, kemudian ditimbang dan dihitung kenaikan bobotnya.
Keterangan :
8. Daya Cerna Pati in Vitro (Modifikasi metode Anderson et al. 2002)
Daya cerna pati in vitro dianalisa dengan spektrofotometer yang mencakup tahapan pembuatan kurva standar maltosa dan analisa sampel sabagai berikut. - Pembuatan kurva standar larutan maltosa
Sebanyak 1 ml larutan maltosa standar yang mengandung 100,150, 200, 250, 300,350 dan 400 mg/L maltosa dimasukkan ke dalam tabung reaksi bertutup kemudian ditambahkan masing-masing 3 ml larutan dinitrosalisilat (DNS). Larutan dipanaskan dalam air mendidih selama 5 menit kemudian diukur absorbansinya dengan spektrofotometer UV-Vis pada panjang gelombang 550 nm.
- Analisa sampel
Sebanyak 0.5 g sampel pati dimasukkan ke dalam erlenmeyer lalu ditambahkan dengan 50 ml akuades. Erlenmeyer ditutup dengan aluminium foil dan dipanaskan dalam penangas air hingga mencapai suhu 90oC sambil terus diaduk lalu didinginkan. Sebanyak 1 ml larutan sampel tersebut dipipet ke dalam tabung reaksi tertutup, lalu ditambahkan 1.5 ml akuades dan 2.5 ml larutan bufer fosfat pH 7. Masing-masing sampel dibuat dua kali, yang salah satunya digunakan sebagai blanko. Tabung ditutup dan diinkubasikan pada suhu 37oC selama 15 menit. Larutan sampel dan blanko diangkat dan ditambahkan 2.5 ml larutan enzim
9. Uji Persen Asetil dan DS (Degree of Substitution) untuk Pati Terasetilasi
Uji persen asetil dan DS mengikuti prosedur yang dilakukan oleh Wurzburg (1978). Pati terasetilasi ditimbang sebanyak 1 g dan dilarutkan dalam 50 mL etanol 75% pada suhu 50oC selama 30 menit. Larutan pati didinginkan pada suhu ruang, ditambahkan 40 mL KOH 0.5 M. Kelebihan alkali dititrasi dengan 0.5 M HCl dengan menggunakan indikator fenolftalein (PP). Blanko menggunakan pati alami dari bahan yang belum dimodifikasi.
Volume blanko dan sampel yang dititrasi dalam mililiter, berat sampel dalam gram. Untuk derajat substitusi (DS) dihitung dengan persamaan berikut (Whistler dan Daniel 1995)
10. Kadar Lemak (SNI 01-2891-1992)
desikator dan ditimbang sebelum digunakan. Sebanyak 1-2 g sampel pati dimasukkan ke dalam selongsong kertas saring yang dialasi dengan kapas. Selongsong kertas yang berisi sampel disumbat dengan kapas, kemudian dikeringkan dalam oven, pada suhu tidak lebih dari 80oC selama ± 1 jam. Selongsong kertas tersebut kemudian dimasukkan ke dalam alat soxhlet yang telah dihubungkan dengan labu lemak. Lemak dalam sampel diekstraksi dengan heksana selama ± 6 jam. Heksana disuling sehingga diperoleh ekstrak lemak ekstrak lemak di dalam labu lemak kemudian dikeringkan dalam oven 105oC selama 12 jam, kemudian didinginkan di dalam desikator dan ditimbang beratnya. Pengeringan diulangi sampai diperoleh bobot tetap. Kadar lemak dihitung dalam basis kering dengan menggunakan rumus sebagai berikut :
dengan: a = bobot labu lemak setelah proses ekstraksi (g); b = bobot labu lemak sebelum proses ekstraksi (g); dan c = bobot sampel (g).
11. Kadar Protein (AOAC 1998)
12. Morfologi Pati (Srichuwong 2006)
Morfologi permukaan granula pati sagu sebelum dan setelah modifikasi diamati di bawah Scanning Electron Microscope (SEM). Serbuk pati diletakkan di atas tempat sampel dengan menggunakan isolasi double-side. Sampel kemudian dilapisi dengan emas, lalu dimasukkan ke dalam instrumen SEM. Struktur pati diamati di layar monitor dengan menggunakan skala pembesaran 500, 1500, 2000 dan 3000 kali. Hasil pengamatan kemudian difoto dengan menggunakan kamera digital.
13. Analisis Sifat Kristalinitas dengan Pola Difraksi Sinar X (Frost et al. 2009)
Sejumlah kecil sampel diletakkan pada wadah sampel, kemudian dimasukkan ke dalam alat difraksi sinar X. Analisis dilakukan pada 40kV dan 40mA dan di-scan pada 2 tetra 0-35o pada suhu kamar dengan kenaikan 0.02o. Data yang diperoleh adalah kurva hubungan antara 2 tetrao pada sumbu x dengan intensitas (a.u.) pada sumbu y. Kurva yang diperoleh kemudian dihaluskan (smoothing) dengan menggunakan software PowderX. Kurva yang sudah dihaluskan kemudian digunakan untuk menentukan daerah amorf dan kristalin.
Lampiran 2 Analisa statistik total gula pada filtrat
Analisa Sidik Ragam
Jumlah
Kuadrat
Derajat Kebebasan
Kuadrat
Tengah F Sig.
Perlakuan 92552.284 6 15425.381 342.803 0.000
Galat 314.985 7 44.998
Total 92867.269 13
Uji Homogenitas
Perlakuan N Bagian untuk alpha = 0,05
1 2 3 4 5 6
0 2 11.39286
1 2 27.464285 50.89285
2 2 66.32143
3 2 125.3929
4 2 198.6071
5 2 238.928
6 2
Lampiran 3 Analisa statistik kadar air
a. Kadar air pada pati alami, pati alami terasetilasi 3% dan pati alami terasetilasi 6%
b. Kadar air pada pati kristalin, pati kristalin terasetilasi 3% dan pati kristalin terasetilasi 6%
Tanpa proses asetilasi 2 14.025
c. Kadar air pada pati nanokristalin, pati nanokristalin terasetilasi 3% dan pati nanokristalin terasetilasi 6%
Analisa Sidik Ragam
Jumlah
Kuadrat
Derajat Kebebasan
Kuadrat
Tengah F Sig.
Perlakuan 0.699 2 0.350 21.734 0.160
Galat 0.048 3 0.016
Lampiran 4 Analisa statistik kadar abu
a. Kadar abu pada pati alami, pati alami terasetilasi 3%, dan pati alami terasetilasi 6%
Tanpa proses asetilasi 2 0.320
Sig. 1.000 1.000
c. Kadar abupada pati nanokristalin, pati nanokristalin terasetilasi 3%, dan pati nanokristalin terasetilasi 6%
Analisa Sidik Ragam
Jumlah
Kuadrat
Derajat Kebebasan
Kuadrat
Tengah F Sig.
Perlakuan 0.196 2 0.098 28.549 0.011
Galat 0.010 3 0.003
Lampiran 5 Analisa statistik kadar serat kasar
c. Kadar serat kasar pada pati nanokristalin, pati nanokristalin terasetilasi 3% dan pati nanokristlain terasetilasi 6%
Tanpa proses asetilasi 2 0.725
Lampiran 6 Analisa statistik kadar amilosa
a. Kadar amilosa pada pati alami, pati alami terasetilasi 3% dan pati alami terasetilasi 6 %
b. Kadar amilosa pada pati kristalin, pati kristalin terasetilasi 3% dan pati kristalin terasetilasi 6%
Lampiran 7 Analisa statistik daya cerna
b. Daya cerna pada pati kristalin, pati kristalin terasetilasi 3% dan pati kristalin terasetilasi 6%
Tanpa proses asetilasi 2 86.024
Sig. 0.190 1.000
Tanpa proses asetilasi 2 88.4868
c. Daya cerna pada pati nanokristalin, pati nanokristalin terasetilasi 3% dan pati nanokristalin terasetilasi 6%
Analisa Sidik Ragam
Jumlah
Kuadrat
Derajat Kebebasan
Rata
Tengah F Sig.
Perlakuan 677.706 2 338.853 274.015 0.000
Galat 3.710 3 1.237
Total 681.416 5
Uji Homogenitas
Bahan N
Bagian untuk alpha = 0,05
1 2
Terasetilasi 6 % 2 56.655
Terasetilasi 3 % 2 58.929
Tanpa proses asetilasi 2 80.251
Lampiran 8 Analisa statistik daya serap air
a. Daya serap air pada pati alami, pati alami terasetilasi 3% dan pati alami terasetilasi 6%
Analisa Sidik Ragam
b. Daya serap air pada pati kristalin, pati kristalin terasetilasi 3% dan pati kristalin terasetilasi 6%
Tanpa proses asetilasi 2 76.300
Sig. 0.609 1.000
Uji Homogenitas
Bahan N Bagian untuk alpha = 0,05
1 2 3
Terasetilasi 6 % 2 52.800
Terasetilasi 3 % 2 58.400
Tanpa proses asetilasi 2 69.600
Lampiran 9 Analisa statistik daya serap minyak
a. Daya serap minyak pada pati alami, pati alami terasetilasi 3% dan pati alami terasetilasi 6%
Analisa Sidik Ragam
Jumlah
Kuadrat
Derajat Kebebasan
Rata
Tengah F Sig.
Perlakuan 256.333 2 128.167 1.448 0.363
Galat 265.540 3 88.513
Total 521.873 5
b. Daya serap minyak pada pati kristalin, pati kristalin terasetilasi 3% dan pati kristalin terasetilasi 6%
Analisa Sidik Ragam
Jumlah
Kuadrat
Derajat Kebebasan
Kuadrat
Tengah F Sig.
Perlakuan 13.613 2 6.807 1.446 0.363
Galat 14.120 3 4.707
Total 27.733 5
c. Daya serap minyak pada pati nanokristalin, pati nanokristalin terasetilasi 3% dan pati nanokristalin 6%
Analisa Sidik Ragam
Jumlah
Kuadrat
Derajat Kebebasan
Kuadrat
Tengah F Sig.
Perlakuan 274.680 2 137.340 2.999 0.193
Galat 137.400 3 45.800
Lampiran 10 Analisa statistik swelling power
a. Swelling power pada pati alami, pati alami terasetilasi 3% dan pati alami terasetilasi 6%
b. Swelling power pada pati kristalin, pati kristalin terasetilasi 3% dan pati kristalin terasetilasi 6%
Uji Homogenitas
Bahan N
Bagian untuk alpha = 0,05
1 2
Tanpa proses asetilasi 2 28.335
Terasetilasi 3 % 2 45.595
Terasetilasi 6 % 2 52.892