FRAKSIONASI EKSTRAK KEMEDANGAN GAHARU
Aquilaria malaccensis HASIL INOKULASI YANG
BERPOTENSI SEBAGAI SENYAWA BIOAKTIF
NUR AMALLIA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Fraksionasi Ekstrak Kemedangan Gaharu Aquilaria malaccensis Hasil Inokulasi yang Berpotensi sebagai Senyawa Bioaktif adalah benar karya saya dengan arahan dari pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Januari 2015
Nur Amallia
ABSTRAK
NUR AMALLIA. Fraksionasi Ekstrak Kemedangan Gaharu Aquilaria malaccensis
Hasil Inokulasi yang Berpotensi sebagai Senyawa Bioaktif. Dibimbing oleh DUDI TOHIR dan ERDY SANTOSO.
Aquilaria malaccensis merupakan salah satu spesies penghasil gaharu. Penelitian yang sudah dilakukan terhadap A. malaccensis baru sebatas daun dan ekstrak kasar. Penelitian ini bertujuan menentukan fraksi dengan aktivitas antioksidan dan toksisitas paling tinggi dari ekstrak kemedangan gaharu A. malaccensis hasil inokulasi. Sampel dimaserasi menggunakan pelarut metanol, etil asetat, dan diklorometana. Ketiga ekstrak yang diperoleh diuji aktivitas antioksidannya menggunakan metode 2,2-difenil-1-pikrilhidrazildan toksisitasnya menggunakan larva udang. Ekstrak etil asetat memiliki aktivitas antioksidan paling tinggi, dengan nilai IC50 150 µg/mL. Ekstrak diklorometana memiliki tingkat toksisitas paling tinggi, dengan nilai LC50 130 µg/mL. Ekstrak etil asetat dan metanol masing-masing difraksionasi menggunakan kromatografi kolom, menghasilkan 7 dan 6 fraksi. Fraksi-fraksi dari ekstrak etil asetat tidak menunjukkan aktivitas antioksidan, sedangkan fraksi-fraksi dari ekstrak metanol bersifat toksik, tetapi tidak berpotensi sebagai antikanker.
Kata kunci: Aquilaria malaccensis, kromatografi kolom, IC50, LC50.
ABSTRACT
NUR AMALLIA. Fractionation of Inoculated Kemedangan Aquilaria malaccensis
Agarwood Extract and Its Potential as Bioactive Compound. Supervised by DUDI TOHIR and ERDY SANTOSO.
Aquilaria malaccensis is an agarwood-producing species. Works have been conducted on A. malaccensis, but still limited on its leaves and crude extracts. The aim of this study is to determine the fraction which has the highest antioxidant and toxicity properties of the extracts of the inoculated kemedangan A. malaccensis
agarwood. The sample was macerated using methanol, ethyl acetate, and dichloromethane. Antioxidant activity of the extracts was tested using 2,2-diphenyl-1-picrylhydrazyl method and the toxicity was tested using brine shrimp lethality test. Ethyl acetate extract has the highest antioxidant activity with IC50 value of 150.02 µg/mL, while dichloromethane extract is the most toxic with LC50 value of 129.92 µg/mL. The ethyl acetate and methanol extracts were fractionated using column chromatography, and yielded 7 and 6 fractions, respectively. Fractions of ethyl acetate extract did not show antioxidant activities, while fractions of methanol extract are toxic, but has no potential as an anticancer.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Kimia
FRAKSIONASI EKSTRAK KEMEDANGAN GAHARU
Aquilaria malaccensis HASIL INOKULASI YANG
BERPOTENSI SEBAGAI SENYAWA BIOAKTIF
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
BOGOR 2015
Judul Skripsi : Fraksionasi Ekstrak Kemedangan Gaharu Aquilaria malaccensis
Hasil Inokulasi yang Berpotensi sebagai Senyawa Bioaktif Nama : Nur Amallia
NIM : G44100110
Disetujui oleh
Drs Dudi Tohir, MS Pembimbing I
Dr Erdy Santoso, MS Pembimbing II
Diketahui oleh
Prof Dr Dra Purwantiningsih Sugita, MS Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah karena berkat rahmat, hidayah, dan karunia-Nya karya ilmiah yang berjudul Fraksionasi Ekstrak Kemedangan Gaharu Aquilaria malaccensis Hasil Inokulasi yang Berpotensi sebagai Senyawa Bioaktif berhasil diselesaikan. Karya ilmiah ini dilaksanakan pada bulan Januari−November 2014 di Laboratorium Kimia Organik, Departemen Kimia dan Pusat Studi Biofarmaka, IPB.
Terima kasih penulis ucapkan kepada Bapak Drs Dudi Tohir, MS dan Dr Erdy Santoso, MS atas bimbingan dan ilmu yang telah diberikan, Bapak Sabur, Bu Yenni, dan Mba Nia atas segala motivasi, nasihat, dan pembelajaran selama di laboratorium, juga staf dan laboran Pusat Studi Biofarmaka atas bantuannya selama ini. Ungkapan terima kasih yang teramat dalam penulis ucapkan kepada Ayah, Ibu, dan seluruh keluarga yang senantiasa mendoakan dan mendukung penulis. Selain itu, terima kasih penulis sampaikan pada Dicky, Nanda, Alif, Ferra, Ayus, Dian, Nuy, Ika, Mumu, Mba Anna, Kak Mella, Kak Kur, Kak Nanda, Kak Yugo, Kak Febrina, dan Kak Ichsan yang telah banyak membantu penulis di laboratorium.
Penulis berharap karya ilmiah ini dapat bermanfaat bagi pembaca pada umumnya dan penulis pada khususnya.
Bogor, Januari 2015
DAFTAR ISI
DAFTAR TABEL vi
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vi
PENDAHULUAN 1
BAHAN DAN METODE 2
Waktu dan Tempat 2
Bahan dan Alat 2
Preparasi Sampel 2
Metode 2
HASIL DAN PEMBAHASAN 4
Kadar Air dan Ekstrak 4
Aktivitas Antioksidan dan Toksisitas Ekstrak 4
Fraksi Ekstrak Paling Aktif Antioksidan 6
Fraksi Ekstrak Paling Toksik 8
SIMPULAN DAN SARAN 11
Simpulan 11
Saran 11
DAFTAR PUSTAKA 11
LAMPIRAN 14
DAFTAR TABEL
1 Jumlah noda dan Rf pada pemisahan ekstrak EA dengan berbagai
komposisi campuran eluen DCM-EA 7
2 Perbandingan rendemen dan IC50 ekstrak kasar dan fraksi ekstrak EA 8 3 Jumlah noda dan Rf pada pemisahan ekstrak metanol dengan berbagai
komposisi campuran eluen DCM-EA 10
4 Perbandingan rendemen dan LC50 ekstrak kasar dan fraksi ekstrak
metanol 11
DAFTAR GAMBAR
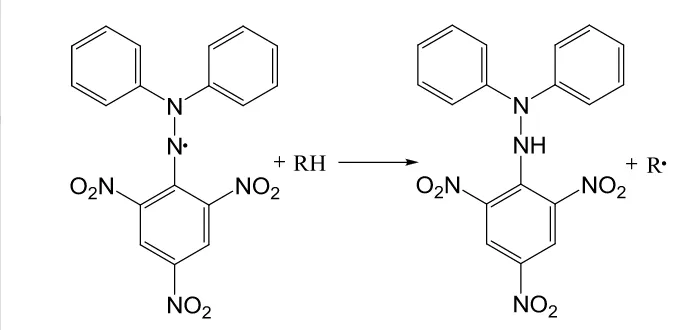
1 Reaksi penangkapan radikal bebas DPPH 5
2 Kromatogram pencarian eluen terbaik untuk ekstrak EA menggunakan pelarut tunggal n-heksana (1), DCM (2), EA (3), etanol (4), aseton (5),
dan metanol (6) pada λ 366 nm 6
3 Kromatogram pencarian eluen terbaik untuk ekstrak EA menggunakan campuran pelarut DCM-EA dengan nisbah 9:1 sampai 1:9 pada λ 366
nm 7
4 Kromatogram fraksi Ea1−7 pada λ 366 nm 8
5 Kromatogram pencarian eluen terbaik untuk ekstrak metanol menggunakan pelarut tunggal n-heksana (1), DCM (2), EA (3), etanol (4),
aseton (5), dan metanol (6) pada λ 366 nm 9
6 Kromatogram pencarian eluen terbaik untuk ekstrak metanol menggunakan campuran pelarut DCM-EA dengan nisbah 9:1 sampai 1:9
pada λ 366 nm 9
7 Kromatogram fraksi Me1−6 pada λ 366 nm 10
DAFTAR LAMPIRAN
1 Diagram alir penelitian 14
2 Kadar air simplisia kemedangan gaharu 15
3 Rendemen ekstrak kemedangan gaharu 15
PENDAHULUAN
Hutan di Indonesia menyimpan banyak keanekaragaman hayati, dan menghasilkan banyak komoditas hasil hutan berupa kayu maupun bukan kayu. Salah satu hasil hutan bukan kayu yang memiliki nilai jual sangat tinggi dan mampu meningkatkan devisa negara adalah gaharu. Gaharu, agarwood, aloewood, atau
eaglewood berupa gumpalan padat berwarna cokelat kehitaman sampai hitam dan beraroma harum. Gaharu terdapat pada bagian kayu atau akar pohon penghasil gaharu yang telah mengalami proses perubahan fisis dan kimiawi akibat terinfeksi oleh jamur. Bagian yang terinfeksi ini akan membentuk resin sebagai produk metabolit sekunder (Santoso et al. 2007). Pemanfaatan gaharu sangat luas, antara lain sebagai aromaterapi, sabun, tasbih, parfum, obat tradisional, dan dupa.
Secara alami, gaharu terbentuk dalam waktu yang sangat lama, padahal permintaan pasar sangat tinggi. Hal ini mengakibatkan pohon penghasil gaharu jenis tertentu, seperti Aquilaria dan Gyrinops kini tergolong langka dan masuk ke dalam Lampiran II Convention on International Trade on Endangered Species of Flora and Fauna (CITES). Produksi gaharu dapat direncanakan dan dipercepat melalui teknologi inokulasi jamur pembentuk gaharu (Siran 2010). Hal ini mampu mengatasi kelangkaan gaharu, sehingga gaharu menjadi komoditas ekspor andalan Indonesia. Setiap tahun, Indonesia mampu mengekspor gaharu hingga 600 ton (Gunawan 2013). Terdapat 13 jenis tumbuhan di Indonesia yang berpotensi menghasilkan resin gaharu, dan Aquilaria malaccensis merupakan jenis yang terbaik (Partomihardjo 2009).
Merujuk Standar Nasional Indonesia (SNI) 7631:2011, gaharu diklasifikasikan menjadi 3 kelompok mutu utama, yaitu gubal, kemedangan, dan serbuk. Gubal gaharu memiliki kandungan resin wangi dengan aroma agak kuat, warnanya hitam atau kehitaman berseling cokelat. Kemedangan memiliki kandungan resin wangi beraroma lemah, warnanya putih keabu-abuan sampai kecokelatan, berserat kasar, dan kayunya lunak. Serbuk gaharu adalah hasil penggilingan atau penghancuran kayu gaharu sisa pembersihan atau pengerokan.
Kemedangan gaharu telah dilaporkan mengandung senyawa metabolit sekunder flavonoid, alkaloid, fenolik (Ramadhan 2013; Annas 2014), triterpenoid (Ramadhan 2013), dan steroid (Annas 2014). Menurut Muntaqo (2012), senyawa penciri pada gaharu adalah seskuiterpena.
Huda et al. (2009) melaporkan bahwa ekstrak kasar daun A. malaccensis
2
BAHAN DAN METODE
Waktu dan Tempat
Penelitian dilaksanakan pada bulan Januari−November 2014 di Laboratorium Kimia Organik, Departemen Kimia, Institut Pertanian Bogor (IPB) dan Laboratorium Pusat Studi Biofarmaka, IPB.
Bahan dan Alat
Bahan-bahan yang digunakan antara lain kemedangan gaharu dari jenis A. malaccensis hasil inokulasi 1.5 tahun asal Kalimantan Selatan, diklorometana (DCM) teknis 1 kali distilasi, etil asetat (EA) teknis 1 kali distilasi, metanol teknis 1 kali distilasi, serbuk 2,2-difenil-1-pikrilhidrazil (DPPH), asam askorbat (vitamin C), dimetil sulfoksida (DMSO), air laut, telur Artemia salina Leach, silika gel F254 untuk kromatografi lapis tipis (KLT), serta silika gel 60 (0.040−0.063 mm) untuk kromatografi kolom.
Alat-alat yang digunakan antara lain peralatan kaca yang lazim terdapat di laboratorium, neraca analitik, oven, eksikator, radas distilasi, penguap putar, kolom kromatografi, mikropipet, aerator, microplate reader untuk uji imunosorben tertaut-enzim (ELISA), pelat 96-sumur, dan lampu ultraviolet (UV).
Preparasi Sampel
Sampel kemedangan gaharu yang digunakan merupakan jenis A. malaccensis. Sampel digiling sampai menjadi serbuk berukuran 60 mesh yang selanjutnya disebut simplisia.
Metode
Penelitian yang dilakukan dibagi menjadi beberapa tahap, yaitu preparasi sampel, penentuan kadar air, ekstraksi, uji aktivitas antioksidan, uji toksisitas, dan fraksionasi (Lampiran 1)
Penentuan Kadar Air (AOAC 2006)
Sebanyak 1 g simplisia dimasukkan ke dalam cawan porselen yang sebelumnya telah dipanaskan dalam oven bersuhu 1032 C selama 30 menit hingga bobotnya tetap. Cawan yang telah berisi sampel dipanaskan kembali di dalam oven bersuhu 1032 C selama 3 jam, lalu didinginkan di dalam eksikator dan ditimbang. Pemanasan diulangi hingga diperoleh bobot yang konstan. Kadar air contoh dihitung dengan persamaan sebagai berikut:
3
Ekstraksi
Ekstraksi dilakukan dengan cara maserasi. Maserasi dilakukan dengan pelarut metanol, EA, dan DCM. Simplisia dimaserasi dengan ketiga pelarut masing-masing sebanyak 100 g simplisia dalam 600 mL pelarut (1:6) selama 48 jam, dan dihitung rendemennya.
Uji Aktivitas Antioksidan Metode DPPH (Salazar-Alanda et al. 2009)
Sebanyak 5.0 mg serbuk DPPH dilarutkan dengan metanol dalam labu takar 100 mL sehingga diperoleh larutan DPPH dengan konsentrasi 126.80 µM. Ekstrak dengan konsentrasi 10, 25, 50, 100, 200, 300, dan 400 ppm serta larutan asam askorbat sebagai standar dengan konsentrasi 2, 4, 6, 8, 10, 12, dan 15 ppm juga disiapkan dengan pelarut metanol dalam labu takar 10 mL.
Sampel dan standar masing-masing sebanyak 100 µL dimasukkan ke dalam pelat 96-sumur. Sebagai blangko, digunakan 100 µL metanol. Larutan DPPH ditambahkan sebanyak 100 µL ke dalam setiap tabung, lalu campuran diinkubasi pada suhu 37 C selama 30 menit. Absorbans campuran diukur pada panjang gelombang 517 nm. Nilai IC50 dihitung dari persamaan garis yang menghubungkan persentase aktivitas penghambatan radikal DPPH dengan logaritma konsentrasi sampel dan standar.
Uji Toksisitas Metode Larva Udang (BSLT) (Juniarti et al. 2009)
Sebanyak ±100 mg telur Artemia salina dimasukkan ke dalam wadah berisi air laut yang diberi suplai udara menggunakan aerator selama 48 jam. Larutan stok dengan konsentrasi 2000 ppm dibuat dengan melarutkan 40 mg ekstrak dengan 20 µL DMSO, kemudian ditambahkan air laut hingga 20 mL (dalam labu takar). Larutan ekstrak dengan konsentrasi 0−1000 ppm dibuat dengan mengencerkan larutan stok tersebut.
Larva A. salina sebanyak 10 ekor dimasukkan ke dalam vial untuk pengujian, lalu ditambahkan larutan ekstrak hingga volumenya 2 mL dan diinkubasi selama 24 jam. Pengujian dilakukan 3 kali ulangan.
Jumlah larva yang mati dihitung dan ditentukan reratanya dari 3 kali ulangan. Nilai LC50 dihitung dari persamaan garis yang menghubungkan nilai probit dari persen kematian larva udang dengan logaritma konsentrasi.
Penentuan Eluen Terbaik (Houghton dan Raman 1998)
Ekstrak diaplikasikan pada pelat KLT, kemudian dikeringudarakan dan dielusi menggunakan eluen tunggal. Eluen yang digunakan adalah n-heksana, DCM, EA, etanol, aseton, dan metanol. Noda hasil pemisahan diamati di bawah lampu UV pada panjang gelombang 366 nm. Eluen yang menghasilkan banyak noda yang terpisah dengan baik ditentukan sebagai eluen terbaik. Jika diperoleh lebih dari satu eluen dengan pemisahan yang baik, dibuat campuran eluen tersebut dengan nisbah tertentu.
Fraksionasi Ekstrak
4
hasil pemisahan dideteksi di bawah lampu UV pada panjang gelombang 366 nm. Eluat yang menghasilkan noda dengan nilai Rf yang sama pada KLT digabungkan menjadi satu fraksi. Fraksi-fraksi dipekatkan, ditimbang bobotnya, kemudian masing-masing diuji kembali aktivitas antioksidan dan toksisitasnya.
HASIL DAN PEMBAHASAN
Kadar Air dan Ekstrak
Kemedangan gaharu yang diperoleh dari Kalimantan Selatan dijadikan simplisia dan ditentukan kadar airnya. Selain untuk mengetahui kandungan air dalam bahan, kadar air digunakan sebagai faktor koreksi dalam perhitungan rendemen ekstrak kasar. Menurut Manoi (2006), simplisia dengan kadar air lebih dari 10% akan mengalami proses enzimatik dan kerusakan oleh mikrob. Kadar air simplisia kemedangan gaharu dalam penelitian ini diperoleh sebesar 4.74% (Lampiran 2). Oleh karena itu, simplisia aman disimpan dalam waktu lama tanpa mengalami proses enzimatik dan kerusakan oleh mikrob.
Simplisia yang telah diketahui kadar airnya diekstraksi menggunakan pelarut metanol, EA, dan DCM untuk memperoleh komponen bioaktifnya. Pelarut metanol bersifat polar, sehingga senyawa-senyawa polar dalam sampel akan terekstraksi. Sementara pelarut EA dan DCM bersifat semipolar dan nonpolar sehingga dapat mengekstraksi senyawa-senyawa yang bersifat semipolar dan nonpolar. Hal ini berdasarkan kaidah like dissolves like. Ekstraksi dapat dilakukan dengan cara maserasi, refluks, soxhletasi, dan distilasi uap. Cara maserasi dipilih karena mudah, sederhana, dan dapat digunakan untuk sampel yang tidak tahan panas. Rendemen ekstrak metanol, EA, dan DCM berturut-turut ialah 10.35, 4.20, dan 5.53% (Lampiran 3). Rendemen ekstrak metanol lebih tinggi daripada 2 ekstrak lainnya, hal tersebut karena pelarut metanol dapat mengekstraksi senyawa-senyawa polar dan semipolar dari kemedangan gaharu.
Aktivitas Antioksidan dan Toksisitas Ekstrak
Radikal bebas terbentuk karena suatu ikatan mengalami pembelahan homolitik dan menghasilkan senyawa yang mengandung elektron tidak berpasangan. Radikal bebas sangat tidak stabil dan bereaksi dengan sangat cepat sehingga dapat merangsang pertumbuhan sel tertentu secara tidak terkendali. Hal ini dapat memicu timbulnya penyakit berbahaya, salah satunya kanker. Senyawa antioksidan dapat menghambat atau mencegah reaksi radikal bebas dalam tubuh dengan cara menyumbangkan radikal hidrogen. Dengan demikian, secara tidak langsung, senyawa antioksidan memiliki potensi sebagai antikanker.
5 radikal bebas mengubah larutan DPPH yang semula berwarna ungu menjadi senyawa takradikal, ditandai dengan warna ungu yang menjadi hilang atau pudar. Reaksi yang terjadi ditunjukkan pada Gambar 1. Berkurangnya intensitas warna ungu sebanding dengan kemampuan sampel menangkap radikal DPPH.
Aktivitas antioksidan ditentukan berdasarkan nilai IC50. Nilai tersebut menyatakan konsentrasi minimum yang dibutuhkan untuk menghambat 50% aktivitas radikal bebas. Semakin rendah nilai IC50, aktivitas antioksidan ekstrak atau senyawa semakin tinggi. Menurut Lisdawati dan Broto (2006), sampel dengan IC50 >200 µg/mL tidak memiliki aktivitas antioksidan, 100−200 µg/mL menunjukkan potensi sedang, dan ≤100 µg/mL sangat aktif sebagai senyawa antioksidan.
Perhitungan nilai IC50 ekstrak kemedangan gaharu diberikan pada Lampiran 4. Berdasarkan hasil uji, ekstrak EA memiliki aktivitas antioksidan paling tinggi dengan nilai IC50 150 µg/mL. Nilai ini menunjukkan bahwa ekstrak EA berpotensi sedang sebagai antioksidan. Sementara ekstrak metanol dan DCM dengan IC50 masing-masing 276 dan 213 µg/mL tidak memiliki aktivitas antioksidan.
Uji toksisitas dengan metode BSLT adalah uji pendahuluan untuk mengamati aktivitas farmakologi suatu ekstrak berkaitan dengan potensinya sebagai antikanker (Juniarti et al. 2009). Metode BSLT mudah dan sederhana untuk memantau aktivitas biologis ekstrak tanaman (Krishnaraju et al. 2005). Toksisitas ekstrak dinyatakan dengan LC50, yaitu konsentrasi ekstrak yang dapat membunuh 50% populasi (dalam hal ini A. salina Leach). Semakin rendah LC50, toksisitas ekstrak atau senyawa semakin tinggi. Menurut Meyer et al. (1982), ekstrak kasar dikatakan toksik bila memiliki nilai LC50 <1000 µg/mL. Sementara menurut Albuntana et al. (2011), National Cancer Institute (NCI) menyatakan bahwa suatu ekstrak dapat dikatakan berpotensi sebagai antikanker jika memiliki nilai LC50 <30 µg/mL. Nilai LC50 ekstrak kemedangan gaharu (Lampiran 5) menunjukkan bahwa ekstrak metanol, EA, dan DCM toksik dengan nilai LC50 masing-masing 134, 200, dan 130 µg/mL, tetapi tidak berpotensi sebagai antikanker.
6
Fraksi Ekstrak Paling Aktif Antioksidan
Proses fraksionasi memisahkan komponen ekstrak menjadi kelompok-kelompok senyawa (fraksi) yang memiliki kemiripan sifat secara kimia (Houghton dan Raman 1998). Fraksi yang diperoleh diharapkan memiliki aktivitas yang lebih tinggi. Ekstrak EA didapati paling aktif antioksidan dengan nilai IC50 150.02 µg/mL sehingga dipilih untuk difraksionasi dengan teknik kromatografi kolom. Sebelum itu, terlebih dahulu dipilih eluen terbaik yang mampu memisahkan senyawa dalam ekstrak dengan menggunakan KLT. Pelarut tunggal dengan kepolaran yang berbeda-beda digunakan, yaitu n-heksana, DCM, EA, etanol, aseton, dan metanol.
Eluen terbaik dipilih dengan mengamati jumlah dan jarak noda. Menurut Suirta et al. (2007), eluen yang baik mampu memisahkan noda dalam jumlah banyak dan jarak yang berjauhan. Berdasarkan kromatogram pada Gambar 2, pelarut DCM dan EA merupakan eluen yang baik untuk ekstrak EA karena menunjukkan jumlah noda yang lebih banyak dan lebih terpisah. Kedua eluen tunggal terbaik ini selanjutnya dicampurkan dengan berbagai nisbah sehingga diperoleh campuran eluen terbaik.
Gambar 2 Kromatogram pencarian eluen terbaik untuk ekstrak EA menggunakan pelarut tunggal n-heksana (1), DCM (2), EA (3), etanol (4), aseton (5), dan metanol (6) pada λ 366 nm
Campuran pelarut DCM dan EA dibuat dengan berbagai komposisi (9:1 hingga 1:9) untuk melihat komposisi yang menghasilkan pemisahan terbaik (Gambar 3). Tabel 1 menunjukkan bahwa eluen DCM-EA dengan nisbah 7:3 menghasilkan pemisahan yang baik, sehingga dipilih sebagai campuran eluen terbaik.
7
Gambar 3 Kromatogram pencarian eluen terbaik untuk ekstrak EA menggunakan campuran pelarut DCM-EA dengan nisbah 9:1 sampai 1:9 pada λ 366 nm rendemen paling tinggi adalah Ea7, yakni 26%, sedangkan fraksi Ea5 paling rendah rendemennya, hanya 1%. Rendemen yang diperoleh bergantung pada distribusi senyawa dalam eluen yang digunakan, berdasarkan kepolarannya. Semua fraksi diuji kembali aktivitas antioksidannya. Perbandingan rendemen dan nilai IC50 antara ekstrak kasar dan fraksi ditunjukkan pada Tabel 2. Nilai IC50 fraksi lebih tinggi dibandingkan dengan ekstrak EA, yakni >200 µg/mL, dari semula 150 µg/mL, yang berarti bahwa semua fraksi tidak memiliki aktivitas antioksidan. Penurunan aktivitas tersebut diduga karena dalam bentuk ekstrak kasar terjadi sinergisitas antarsenyawa (efek sinergi). Ketika difraksionasi, sinergisitas tersebut berkurang atau bahkan hilang sehingga fraksi menjadi tidak aktif antioksidan. Aktivitas antioksidan ekstrak maupun fraksi lebih rendah daripada standar vitamin
8
C. Cahaya dan suhu selama fraksionasi diduga berpengaruh. Menurut Wahyudi (2006), antioksidan secara bertahap dapat teroksidasi oleh adanya cahaya, panas, atau kontak langsung dengan oksigen. Vitamin C disimpan dalam wadah gelap pada suhu rendah, sedangkan fraksionasi dilakukan pada suhu ruang tanpa pembatasan cahaya.
Gambar 4 Kromatogram fraksi Ea1−7 pada λ 366 nm
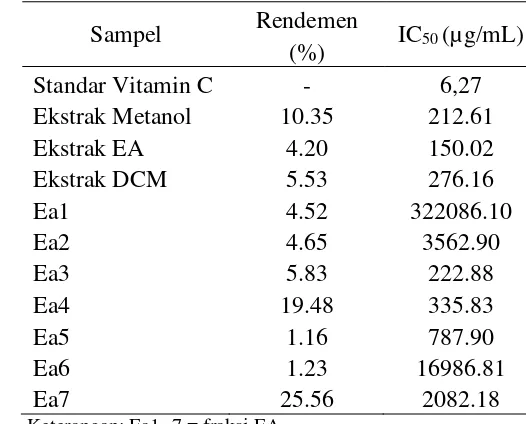
Tabel 2 Perbandingan rendemen dan IC50 ekstrak kasar dan fraksi ekstrak EA
Keterangan: Ea1−7 = fraksi EA
Fraksi Ekstrak Paling Toksik
Ekstrak DCM didapati paling toksik dengan nilai LC50 130 µg/mL. Namun, nilai LC50 ekstrak tersebut tidak berbeda jauh dengan ekstrak metanol (134 µg/mL). Rendemen ekstrak metanol jauh lebih tinggi daripada ekstrak DCM, maka ekstrak metanol dipilih untuk difraksionasi. Kromatogram pada Gambar 5 menunjukkan pelarut DCM dan EA sebagai eluen yang baik. Pencarian lebih lanjut dengan
Sampel Rendemen IC50 (µg/mL) (%)
Standar Vitamin C - 6,27
Ekstrak Metanol 10.35 212.61
Ekstrak EA 4.20 150.02
Ekstrak DCM 5.53 276.16
Ea1 4.52 322086.10
Ea2 4.65 3562.90
Ea3 5.83 222.88
Ea4 19.48 335.83
Ea5 1.16 787.90
Ea6 1.23 16986.81
Ea7 25.56 2082.18
9 menggunakan campuran DCM dan EA 9:1 hingga 1:9 (Gambar 6) menunjukkan campuran eluen DCM-EA 7:3 sebagai eluen terbaik (Tabel 3).
Gambar 5 Kromatogram pencarian eluen terbaik untuk ekstrak metanol menggunakan pelarut tunggal n-heksana (1), DCM (2), EA (3), etanol (4), aseton (5), dan metanol (6) pada λ 366 nm
Gambar 6 Kromatogram pencarian eluen terbaik untuk ekstrak metanol menggunakan campuran pelarut DCM-EA dengan nisbah 9:1 sampai 1:9 pada λ 366 nm
8:2 7:3 6:4 5:5 4:6 3:7 2:8 1:9
9:1
10
Tabel 3 Jumlah noda dan Rf pada pemisahan ekstrak metanol dengan berbagai komposisi campuran eluen DCM-EA
Eluen (DCM-EA)
Jumlah
Noda Rf
9:1 7 0.09, 0.20, 0.40, 0.59, 0.72, 0.78, 0.93 8:2 6 0.30, 0.47, 0.58, 0.77, 0.84, 0.94
7:3 8 0.25, 0.37,0.43, 0.53, 0.65, 0.80, 0.87, 0.95 6:4 6 0.46, 0.59, 0.69, 0.82, 0.89, 0.94
5:5 7 0.49, 0.55, 0.63, 0.73, 0.82, 0.90, 0.95 4:6 7 0.41, 0.58, 0.65, 0.74, 0.80, 0.86, 0.93 3:7 6 0.12, 0.63, 0.73, 0.83, 0.89, 0.96 2:8 5 0.24, 0.70, 0.77, 0.85, 0.90 1:9 3 0.72, 0.81, 0.92
Pemisahan ekstrak metanol dengan kromatografi kolom menghasilkan 6 fraksi (Gambar 7). Fraksi Me6 menghasilkan rendemen paling tinggi, yakni 35%, sedangkan fraksi dengan rendemen terendah adalah Me3, sebesar 4.5%. Keenam fraksi tersebut diuji kembali toksisitasnya. Perbandingan rendemen dan nilai LC50 antara ekstrak kasar dan fraksi diperlihatkan pada Tabel 4. Fraksi Me1, Me2, Me3, dan Me4 memiliki nilai LC50 <1000 µg/mL sehingga bersifat toksik, sedangkan fraksi Me5 dan Me6 tidak bersifat toksik. Fraksi Me1 paling toksik dengan nilai LC50 sebesar 124 µg/mL. Toksisitasnya juga lebih tinggi daripada ekstrak kasarnya. Namun, fraksi tersebut tidak berpotensi sebagai antikanker karena nilai LC50-nya >30 µg/mL.
Gambar 7 Kromatogram fraksi Me1−6 pada λ 366 nm
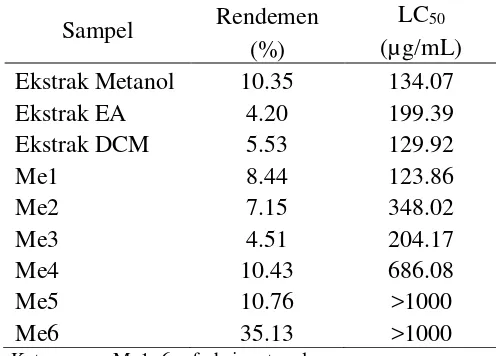
11 Tabel 4 Perbandingan rendemen dan LC50 ekstrak kasar dan fraksi ekstrak metanol
Sampel Rendemen LC50
(%) (µg/mL)
Ekstrak Metanol 10.35 134.07
Ekstrak EA 4.20 199.39
Keterangan: Me1−6 = fraksi metanol
SIMPULAN DAN SARAN
Simpulan
Ekstrak EA kemedangan gaharu A. malaccensis dari daerah Kalimantan Selatan memiliki aktivitas antioksidan paling tinggi dibandingkan ekstrak metanol dan DCM, dengan nilai IC50 150.02 µg/mL. Sementara ekstrak DCM paling toksik, dengan nilai LC50 129.92 µg/mL. Fraksionasi ekstrak EA dan metanol masing-masing menghasilkan 7 dan 6 fraksi. Fraksi-fraksi dari ekstrak EA tidak menunjukkan aktivitas antioksidan, sedangkan fraksi-fraksi dari ekstrak metanol bersifat toksik, tetapi tidak berpotensi sebagai antikanker.
Saran
Fraksionasi ekstrak dapat dilakukan menggunakan instrumen seperti KCKT preparatif untuk mengurangi galat. Sebelum difraksionasi, ekstrak metanol dapat dipartisi terlebih dahulu dengan etil asetat, sehingga ekstrak yang difraksionasi adalah ekstrak yang benar-benar polar. Fraksi Me1 yang paling toksik dapat dimurnikan lebih lanjut untuk memperoleh senyawa murni yang lebih toksik dan dicirikan strukturnya. Ekstrak juga dapat diuji pada bioaktivitas yang lain, seperti antibakteri.
DAFTAR PUSTAKA
12
Seribu, Jakarta menggunakan brine shrimp lethality test (BSLT). J Iltek Keltrop. 3:65-72.
Annas D. 2014. Fraksionasi ekstrak kemedangan gaharu Aquilaria microcarpa
hasil inokulasi berpotensi antioksidan [skripsi]. Bogor (ID): Institut Pertanian Bogor.
[AOAC]. Association of Official Analytical Chemist. 2006. Official Methods of AOAC International. Ed ke-14. Arlington (US): AOAC
[BSN] Badan Standardisasi Nasional. 2011. Gaharu. SNI 7631:2011. Jakarta (ID): BSN.
[CITES] Convention on International Trade in Endangered Species of Wild Flora and Fauna. 2004. Amendments to Appendices I and II of CITES. Sydney (AU): CITES.
Dewi KS. 2013. Toksisitas dan aktivitas antioksidan ekstrak daun pohon penghasil gaharu hasil inokulasi [skripsi]. Bogor (ID): Institut Pertanian Bogor. Gunawan H. 2013. Ekspor Gaharu Loyo. Tribunnews. Rubrik Bisnis dan Ekonomi.
[diakses 2014 Feb 4]. Tersedia pada:
http://www.tribunnews.com/bisnis/2013/09/11/ekspor-gaharu-loyo.
Houghton PJ, Raman. 1998. Laboratory Handbook for The Fractionation of Natural Extract. London (GB): Chapman & Hall.
Huda AWN, Munira MAS, Fitrya SD, Salmah M. 2009. Antioxidant activity of
Aquilaria malaccensis (Thymelaeaceae) leaves. Pharmacognosy Res. 1:270-273.
Juniarti, Osmeli D, Yuhernita. 2009. Kandungan senyawa kimia, uji toksisitas (brine shrimp lethality test) dan antioksidan (1,1-diphenyl-2-picrylhydrazyl) dari ekstrak daun saga (Abrus precatorius L.). Makara Sains. 13(1):50-59. Krishnaraju AV, Rao TVN, Sundararaju D, Vanisree M, Tsay H, Subbaraju GV.
2005. Assessment of bioactivity of Indian medicinal plants usingbrine shrimp (Artemia salina) lethality assay. Int J Appl Sci Eng. 2:125-134.
Lisdawati V, Broto S. 2006. Aktivitas antioksidan dari berbagai fraksi ekstrak daging buah dan kulit biji mahkota dewa (Phaleria macrocarpa). Media Litbang Kesehatan. 16(4):1-7.
Manoi F. 2006. Pengaruh cara pengeringan terhadap mutu simplisia sambiloto. Bul Littro.17(1):1-5.
Mardisadora O. 2010. Identifikasi dan potensi antioksidan flavonoid kulit kayu mahoni (Swietenia macrophylla king) [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Meyer BN, Ferrigni NR, Putnam JE, Jacobsen LB, Nichols DE, McLaughlin JL et al. 1982. Brine shrimp: a convenient general bioassay for active plant constituents. Planta Med. 45:31-34.
Molyneux P. 2004. The use of the stable free radical diphenylpicryl-hydrazyl (DPPH) for estimating antioxidant activity. Songklanakarin J Sci Technol. 26(2):211-219.
Muntaqo FA. 2012. Korelasi kadar seskuiterpena dengan mutu gaharu standar nasional Indonesia [skripsi]. Bogor (ID): Institut Pertanian Bogor.
13 Ramadhan PM. 2013. Aktivitas antioksidan ekstrak kemedangan pohon penghasil gaharu hasil inokulasi jenis Aquilaria microcarpa dan Gyrinops verstegii
[skripsi]. Bogor (ID): Institut Pertanian Bogor.
Salazar-Aranda R, Perez-Lopez LA, Lopez-Arroyo J, Alanis-Garza BA, de Torres NW. 2009. Antimicrobial and antioxidant activities of plants from Northeast of Mexico. Evidence-Based Complementary and Alternative Medicine. 2011:1-6. doi: 10.1093/ecam/nep127.
Santoso E, Agustini L, Sitepu IR, Turjaman M. 2007. Efektivitas pembentukan gaharu dan komposisi senyawa resin gaharu pada Aquilaria spp. J Penelitian Hutan dan Konservasi Alam. 4(6):543-551.
Siran SA. 2010. Pengembangan Teknologi Produksi Gaharu Berbasis Pemberdayaan Masyarakat. Siran SA dan Turjaman M, editor. Bogor (ID): Pusat Penelitian dan Pengembangan Hutan dan Konservasi Alam.
Suirta IW, Puspawati NM, Gumiati NK. 2007. Isolasi dan identifikasi senyawa aktif larvasida dari biji mimba (Azadirachta indika A. Juss) terhadap larva nyamuk demam berdarah (Aedes aegypti). J Kim.1(1):47-54.
14
15 Lampiran 2 Kadar air simplisia kemedangan gaharu
Ulangan Bobot Sampel (g) Kadar Air
Basah Kering (%)
1 1.0005 0.9533 4.72
2 1.0042 0.9547 4.93
3 1.0046 0.9587 4.57
Rerata 4.74
Contoh perhitungan kadar air (ulangan 1):
Kadar air =Bobot sampel basah − Bobot sampel keringBobot sampel basah
= [ . g − .. g g] × %
Kadar air = . %
Rerata kadar air =Kadar air ulangan + ulangan + ulangan
= . % + . % + . %
Rerata kadar air = . %
Lampiran 3 Rendemen ekstrak kemedangan gaharu Ekstrak
Kasar
Bobot (g) Rendemen (%) Sampel Ekstrak Basah Kering Metanol 100.07 9.8657 9.86 10.35
EA 100.05 4.0046 4.00 4.20
DCM 100.04 5.2688 5.27 5.53
Contoh perhitungan rendemen basah dan rendemen kering (metanol)
Rendemen basah % =Bobot ekstrakBobot sampel × %
= . . g × g %
Rendemen basah % = . %
Rendemen kering % =Bobot sampel − kadar air ×Bobot ekstrak %
= . g − .. g × %
16
Lampiran 4 Hasil uji antioksidan ekstrak kemedangan gaharu Standar vitamin C
Konsentrasi Absorbans % Inhibisi (%)
(µg/mL) 1 2 3 1 2 3
Konsentrasi Absorbans % Inhibisi (%)
(µg/mL) 1 2 3 1 2 3
Konsentrasi Absorbans % Inhibisi (%)
17 lanjutan Lampiran 4
Ekstrak DCM
Konsentrasi Absorbans % Inhibisi (%)
(µg/mL) 1 2 3 1 2 3
Ekstrak metanol ulangan 1, konsentrasi 10 µg/mL
% Inhibisi =Absorbans blangko − Absorbans sampelAbsorbans blangko × %
= . .− . × %
% Inhibisi = 3.72%
Kurva hubungan log konsentrasi dengan % inhibisi ekstrak metanol Persamaan regresi linear: y = 34.168x−34.32
Nilai IC50 diperoleh saat y = 50, maka 50 = 34.168x−34.32
x = 2.4684
x dalam bentuk log konsentrasi, maka nilai IC50 sebesar 294.02 µg/mL
y = 34,168x - 34,32
0,0000 0,5000 1,0000 1,5000 2,0000 2,5000 3,0000
18
lanjutan Lampiran 4
Rerata IC =IC ulangan + ulangan + ulangan
= . + . + . µg/mL
19 Lampiran 5 Hasil uji toksisitas ekstrak kemedangan gaharu
20
lanjutan Lampiran 5
Contoh perhitungan: Ekstrak metanol konsentrasi 12.65 µg/mL
Rerata larva mati =larva mati + larva mati + larva mati
= + +
Rerata larva mati = .
% Kematian larva =Jumlah larva dalam tiap vial ×Rerata larva mati %
= . × %
% Kematian larva = 3.33%
Kurva hubungan log konsentrasi dengan nilai probit ekstrak metanol Persamaan regresi linear: y = 1.7797x + 1.214
LC50 diperoleh saat y = 5, maka 5 = 1.7797x + 1.214
x = 2.1273
log konsentrasi = 2.1273, maka LC50 yang didapat sebesar 134.07 µg/mL
y = 1,7797x + 1,214 R² = 0,9922
0,00 1,00 2,00 3,00 4,00 5,00 6,00
0,0000 0,5000 1,0000 1,5000 2,0000 2,5000 3,0000
Nilai
p
ro
b
it
21