PENILAIAN AGREGASI TROMBOSIT DAN MPV
PADA PENDERITA SINDROMA METABOLIK DAN
OBESITAS
TESIS
NINDIA SUGIH ARTO
097111008 / PK
PROGRAM MAGISTER KLINIK – SPESIALIS ILMU
PATOLOGI KLINIK
FAKULTAS KEDOKTERAN
PENILAIAN AGREGASI TROMBOSIT DAN MPV PADA
PENDERITA SINDROMA METABOLIK DAN OBESITAS
T E S I S
Untuk memperoleh gelar Magister Kedokteran Klinik di Bidang
Ilmu Patologi Klinik / M. Ked (Clin.Path) pada Fakultas Kedokteran
Universitas Sumatera Utara
NINDIA SUGIH ARTO
097111008 / PK
PROGRAM MAGISTER KLINIK – SPESIALIS ILMU
PATOLOGI KLINIK
FAKULTAS KEDOKTERAN
Judul Tesis : Penilaian Agregasi Trombosit dan MPV pada
Penderita Sindroma Metabolik dan Obesitas
Nama Mahasiswa : Nindia Sugih Arto
Nomor Induk Mahasiswa : 097111008
Program Magister : Magister Kedokteran Klinik
Konsentrasi : Patologi Klinik
Menyetujui
Komisi Pembimbing
Pembimbing I
Prof. dr. Adi Koesoema Aman, Sp.PK-KH
Pembimbing II
DR. Dr. Dharma Lindarto, Sp. PD-KEMD
Disahkan oleh :
Ketua Departemen Patologi Klinik Ketua Program Studi Departemen
FK-USU/RSUP H. Adam Malik Patologi Klinik FK-USU/
Medan RSUP H. Adam Malik Medan
Prof. dr. Adi Koesoema Aman, Sp.PK-KH
NIP. 19491011 1979 01 1 001 NIP. 1948711 1979 03 2 001
Prof.DR.dr.Ratna Akbari Gani, Sp.PK-KH
Telah diuji pada
Tanggal : 17 Oktober 2013
PANITIA PENGUJI TESIS
Ketua : Prof. dr. Adi Koesoema Aman, Sp. PK-KH ...
Anggota : 1. Prof. DR. dr. Ratna Akbari Ganie, Sp.PK-KH ...
2. DR. dr. Dharma Lindarto, Sp. PD-KEMD ...
3. Prof. Herman Hariman, Ph.D, Sp. PK-KH ...
4. dr. Ricke Loesnihari, MKed (ClinPath), Sp.PK-K ...
UCAPAN TERIMA KASIH
Assalamualaikum Wr. Wb.
Puji dan syukur kehadirat Alah SWT yang telah melimpahkan
rahmat dan hidayah-Nya serta atas ridha-Nya sehingga penulis dapat
menyelesaikan penulisan tesis ini. Tesis ini disusun untuk memenuhi
persyaratan dan merupakan tugas akhir pendidikan Magister Kedokteran
Klinik di bidang Ilmu Patologi Klinik pada Fakultas Kedokteran Universitas
Sumatera Utara.
Selama penulis mengikuti pendidikan dan proses penyelesaian
penelitian untuk karya tulis ini, penulis telah banyak mendapat bimbingan,
petunjuk, bantuan dan pengarahan serta dorongan baik moril dan materil
dari berbagai pihak sehingga penulis dapat menyelesaikan pendidikan
dan karya tulis ini.
Penulis menyadari penelitian dan penulisan tesis ini masih jauh dari
kesempurnaan sebagaimana yang diharapkan. Oleh sebab itu dengan
segala kerendahan hati, penulis mengharapkan masukan yang berharga
dari semua pihak untuk perbaikan di masa yang akan datang.
Pada kesempatan ini, perkenankanlah penulis menyampaikan
penghargaan dan ucapan terima kasih yang sebesar – besarnya kepada :
1. Prof. dr. Adi Koesoema Aman, Sp. PK – KH selaku pembimbing dan Ketua Departemen Patologi Klinik FK USU yang telah
memberikan bimbingan, bantuan serta saran – saran yang sangat
berharga dalam pelaksanaan penelitian dan penyelesaian tesis ini.
2. Prof. DR. dr. Ratna Akbari Ganie, Sp.PK – KH sebagai Ketua Program Studi di Departemen Patologi Klinik FK USU yang telah
memberikan bantuan dan masukan dalam pelaksanaan penelitian
3. DR. dr. Dharma Lindarto, Sp.PD – KEMD sebagai pembimbing II dari Departemen Ilmu Penyakit Dalam FK USU/ RSUP. H. Adam
Malik Medan yang sudah memberikan bimbingan, bantuan serta
saran – saran mulai dari penyusunan proposal sampai selesainya
tesis ini.
4. Prof. dr. Herman Hariman, PhD, Sp.PK – KH selaku Sekretaris Departemen Patologi Klinik FK USU yang telah memberikan
bimbingan, pengarahan, dan saran – saran selama saya mulai
pendidikan sampai dengan selesainya penulis tesis ini.
5. dr. Ricke Loesnihari, M.Ked (Clin Path), Sp.PK(K) selaku Sekretaris Program Studi di Departemen Patologi Klinik FK USU
yang telah memberikan bimbingan dan sumbangan pemikiran
sehingga saya dapat menyelesaikan penelitian dan penulisan tesis
ini.
6. Prof. dr. Burhanuddin Nasution, Sp.PK-KN, KGEH yang telah banyak memberikan bimbingan dan pengarahan selama
pendidikan dan menyelesaikan penulisan tesis ini.
7. Rektor Universitas Sumatera Utara, Prof. DR. Dr. Syahril Pasaribu, DTM&H, MSc(CTM), Sp.A(K) yang telah memberikan kesempatan kepada penulis untuk mengikuti pendidikan Magister
Kedokteran Klinik di bidang Patologi Klinik dan Program Pendidikan
Dokter Spesialis (PPDS) Patologi Klinik di FK USU.
8. Dekan FK USU, Prof. dr. Gontar A. Siregar, Sp.PD-KGEH, yang telah memberikan kesempatan kepada penulis untuk mengikuti
pendidikan Magister Kedokteran Klinik di bidang Patologi Klinik dan
PPDS Patologi Klinik di FK USU.
9. Direktur RSUP H. Adam Malik Medan yang telah memberikan kesempatan pada penulis untuk mengikuti pendidikan selama di
10. Kepada para dosen saya dr. Muzahar, DMM, Sp.PK-K, (Alm) dr. Ardjuna, Sp.PK-K, dr. Zulfikar Lubis, Sp.PK-K, dr. Ozar Sahnuddin, Sp.PK-K, dr. Nelly E. Samosir, Sp.PK, dan dr. Ida Adhayanti, Sp.PK yang telah mengajarkan dan memberikan pengarahan selama saya mengikuti pendidikan Spesialis Patologi
Klinik dan selama penyelesaian tesis ini.
11. Teman – teman seangkatan saya yang tidak mungkin saya lupakan
Noviyanti F. Panggabean, Yasmine Mashabie, Tut Wuri Handayani,
Budi D. Sembiring, group Sero lainnya beserta Amie, Indy, Qiqi dan
Maya yang selalu saling menjaga silahturahmi dan mendukung
dalam suka dan duka, terima kasih atas dukungan dan bantuannya
selama ini.
12. Seluruh teman sejawat PPDS Patologi Klinik FK USU beserta para
analis di RSUP H. Adam Malik Medan yang telah banyak
membantu dan mengajarkan saya, serta semua pihak yang tidak
dapat disebutkan satu per satu yang telah membantu dalam
terlaksananya penelitian serta penulisan tesis ini.
Teristimewa kepada orang tua saya, Ibunda dan Ayahanda
Drg. T. Hermina Maimun dan Ir. R. Sugih Arto Yusuf yang telah memberikan kasih sayang, motivasi, dukungan dan semangat
kepada saya untuk terus belajar. Kepada kakak saya Miranda Sugih Arto, amd, S. Sos, MA, dr. Karina Sugih Arto, MKed-Ped, Sp.A dan kepada abang saya Syamsul Aidi Bachtiar Lc, MA dan
dr. Dedy Hermansyah, Sp.B
Kepada para kurcaci saya, Fawwaz, Aira, Ain dan Naia, serta seluruh keluarga yang selalu mendoakan, memberikan
dorongan, motivasi cinta dan kasih sayang, bantuan moril dan
Semoga Allah SWT senantiasa melimpahkan kasih sayang
dan karunia-Nya kepada kita semua dan segala budi baik yang
telah diberikan mendapatkan balasan yang setimpal dari Allah yang
Maha Kuasa.
Akhirnya penulis mengharapkan semoga penelitian dan
tulisan ini bermanfaat bagi kita semua. Amin, Wassalamualaikum
Wr. Wb.
Medan, November 2013
DAFTAR ISI
Lembar Pengesahan Tesis ... i
Lembar Penetapan Panita Penguji ... ii
Ucapan Terima Kasih ... iii
Daftar Isi ... vii
Daftar Tabel ... x
Daftar Lampiran ... xi
Daftar Singkatan ... xii
Abstrak ... xiv
BAB 1 PENDAHULUAN 1.1 Latar Belakang ... 1
1.2 Rumusan Masalah ... 5
1.3 Hipotesa Penelitian ... 5
1.4 Tujuan Penelitian 1.4.1 Tujuan Umum ... 6
1.4.2 Tujuan Khusus ... 6
1.5 Manfaat Penelitian ... 6
BAB 2 TINJAUAN PUSTAKA 2.1 Trombosit ... 7
2.1.1 Produksi Trombosit ... 7
2.1.2 Struktur Trombosit ... 8
2.1.3 Fungsi Trombosit ... 9
2.1.4 Pembentukan Sumbat Trombosit ... 9
2.1.4.1 Adhesi Trombosit ... 10
2.2 Tes Fungsi Trombosit ... 11
2.2.1 Light Transmission Aggregometry ... 12
2.2.1.1 Prinsip Kerja ... 12
2.2.1.2 Variabel Pemeriksaan Agregasi Trombosit ... 13
2.3.3 Patofisiologi Sindroma Metabolik ... 23
2.3.3.1 Resistensi Insulin ... 23
2.3.3.2 Obesitas ... 24
2.3.3.3 Dislipidemia ... 26
2.3.4 Trombosit Pada Sindroma Metabolik .... 28
2.4 Kerangka Teori ... 29
BAB 3 METODOLOGI PENELITIAN 3.1 Desain Penelitian ... 30
3.2 Tempat dan Waktu ... 30
3.3 Populasi dan Sampel ... 30
3.4 Perkiraan Besar Sampel ... 31
3.5 Kriteria Inklusi dan Eksklusi ... 32
3.5.1 Kriteria Inklusi ... 32
3.5.2 Kriteria Eksklusi ... 32
3.6 Bahan dan Cara Kerja ... 33
3.6.1 Bahan Yang Diperlukan ... 33
3.6.3 Pengambilan dan Pengolahan
Sampel ... 35
3.7 Pemeriksaan Laboratorium ... 35
3.7.1.1 Pemeriksaan Darah Lengkap ... 35
3.7.1.2 Pemeriksaan Kadar Gula Darah ... 35
3.7.1.3 Pemeriksaan Trigliserida ... 36
3.7.1.4 Pemeriksaan HDL-C ... 36
3.7.1.5 Pemeriksaan Agregasi Trombosit... 36
3.8 Pemantapan Kualitas ... 37
3.8.1 MPV ... 38
3.8.2 Agregasi Trombosit ... 39
3.8.3 Pemeriksaan Kimia ... 39
3.9 Definisi Operasional ... 40
3.10 Analisa Data ... 41
3.11 Ethical Clearance dan Informed Consent ... 42
3.12 Alur Penelitian ... 43
BAB 4 HASIL ... 44
BAB 5 PEMBAHASAN ... 49
BAB 6 KESIMPULAN dan SARAN 6.1 Kesimpulan ... 53
6.1 Saran ... 53
Daftar Pustaka ... 54
DAFTAR TABEL
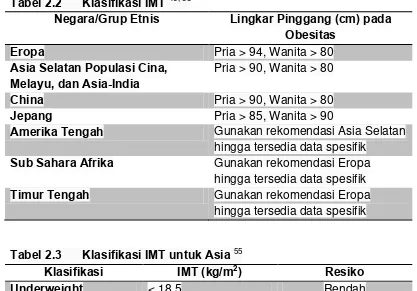
Tabel 2.1 Kriteria dari Sindroma Metabolik ... 21
Tabel 2.2 Klasifikasi IMT ... 26
Tabel 2.3 Klasifikasi BMI untuk Asia ... 26
Tabel 4.1 Karakteristik pada Kelompok Sindroma Metabolik
dan Obesitas ... 45
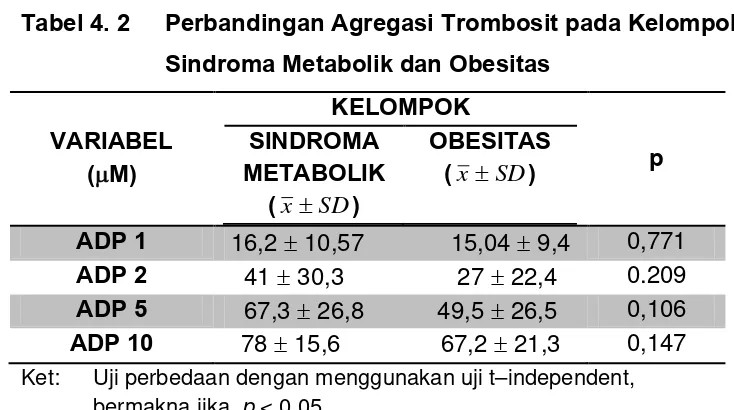
Tabel 4.2 Perbandingan Agregasi Trombosit pada Kelompok
Sindroma Metabolik dan Obesitas ... 46
Tabel 4.3 Perbandingan MPV pada Kelompok Sindroma
DAFTAR LAMPIRAN
Lampiran 1 Lembaran Penjelasan Kepada Calon Subjek Penelitian
Lampiran 2 Formulir Persetujuan Setelah Penjelasan
Lampiran 3 Status Pasien
Lampiran 4 Ethical Clearance
Lampiran 5 Data Penelitian
Lampiran 6 Tabel Quality Control
DAFTAR SINGKATAN
LTA : Light Transmission Aggregometry
MPV : Mean Platelet Volume
GP Ia : Glikoprotein Ia
ADP : Adenosin diphosphate
PDGF : Platelet derived growth factor
vWF : von Willebrand Factor
LTA : Light Transmission Aggregometry
PRP : Platelet Rich Plasma
PPP : Platelet Poor Plasma
WHO : World Health Organization
IDF : the International Diabetes Federation
NCEP : National Cholesterol Education Program
ATP III : Third Adult Treatment Panel
AACE : American Association of Clinical Endocrinologists
NEFA : Non esterified fatty acids
TNF α : Tumor necrosis factor alpha
DM : Diabetes Melitus
ROS : Reactive Oxygen Species
IMT : Indeks Masa Tubuh
TG : Trigliserida
HDL : High Density Lipoprotein
LDL : Low Density Lipoprotein
VLDL : Very low density cholesterol
HDL : High Density Lipoprotein
NO : Nitrit Oxide
PGI2 : Prostaglandin I2
PENILAIAN AGREGASI TROMBOSIT DAN MEAN PLATELET VOLUME PADA PENDERITA SINDROMA METABOLIK DAN OBESITAS
Nindia Sugih Arto,(1), Adi K Aman,(1), Dharma Lindarto,(2),
1Departemen Patologi Klinik, Fakultas Kedokteran Universitas Sumatera
Utara/RSUP H. Adam Malik Medan
2Departemen Ilmu Penyakit Dalam Divisi Endokrinologi, Fakultas
Kedokteran Universitas Sumatera Utara/RSUP H. Adam Malik Medan
ABSTRAK
Latar Belakang: Terjadinya hiperaktivitas trombosit terlihat pada penderita sindroma metabolik yang dapat diakibatkan oleh beberapa faktor seperti resistensi insulin, obesitas, dislipidemia dan hipertensi. Hiperaktivitas trombosit menyebabkan terjadinya agregasi trombosit yang dapat meningkatkan resiko terjadinya penyakit kardiovaskuler.
Tujuan: Untuk mengetahui perbedaan nilai agregasi trombosit dan MPV pada penderita sindroma metabolik dan obesitas
Metode: Penelitian dilakukan dengan metode potong lintang 30 orang yang datang ke Departemen Patologi Klinik dan Departemen Penyakit Dalam bagian Endokrin RSUP H. Adam Malik Medan periode Mei 2013 sampai Agustus 2013. Diagnosa sindroma metabolik ditegakkan berdasarkan kriteria IDF 2005.
Hasil: Dari 30 subjek didapati 11 orang sindroma metabolik dan 15 dengan obesitas. 4 orang dieksklusi karena memiliki kadar trigliserida yang tinggi (> 200mg/dL). Nilai agregasi trombosit yang didapat dengan agonis ADP tidak dijumpai bermakna antara sindroma metabolik dan obesitas. Tidak ada perbedaan yang bermakna pada nilai MPV pada penderita sindroma metabolik (9,6 ± 0,89) dengan obesitas (9,73 ± 0,74) dengan nilai p=0,672.
Kesimpulan: Tidak dijumpai perbedaan yang bermakna antara nilai agregasi trombosit dan MPV pada kelompok sindroma metabolik dibandingkan dengan kelompok obesitas.
PLATELET AGGREGATION AND MEAN PLATELET VOLUME ASSESSMENT IN PATIENTS WITH METABOLIC
SYNDROME AND OBESITY
Nindia Sugih Arto,(1), Adi K Aman,(1), Dharma Lindarto,(2), 1 Department of Clinical Pathology, School of Medicine, University of
Sumatera Utara / H. Adam Malik Medan Hospital
2 Department of Internal Medicine, School of Medicine, University of
Sumatera Utara / H. Adam Malik Medan Hospital
ABSTRACT
Background: Hyperactivity of platelet had been seen in patients with metabolic syndrome which can be caused by several factors such as insulin resistance, obesity, dyslipidemia and hypertension. Hyperactivity of platelet leads to platelet aggregation that can be increase the risk of cardiovascular disease.
Aim: To determine the platelet aggregation and mean platelet volume in patients with metabolic syndrome and obesity
Methode: 30 patients were choosen for this cross sectional study who came to the laboratory and policlinic in H. Adam Malik Medan Hospital, between May 2013 until August 2013. Diagnosis of metabolic syndrome criteria established by International Diabetic Federation 2005.
Result: From 30 patients with 15 metabolic syndrome and 15 obesity. Four patients were excluded because of the tryglyceride more than 200 mg/dl. There is no significant differences between platelet aggregation with agonist adenosin difosfat (ADP) in patient with metabolic syndrome and obesity. And there is no significant differences mean platelet volume values between metabolic syndrome (9,6 ± 0,93) and obesity (9,73 ± 0,74), with p value 0,846.
Conclusion: There is no significant differences between platelet aggregation and mean platelet volume values in metabolic syndrome and obese group
PENILAIAN AGREGASI TROMBOSIT DAN MEAN PLATELET VOLUME PADA PENDERITA SINDROMA METABOLIK DAN OBESITAS
Nindia Sugih Arto,(1), Adi K Aman,(1), Dharma Lindarto,(2),
1Departemen Patologi Klinik, Fakultas Kedokteran Universitas Sumatera
Utara/RSUP H. Adam Malik Medan
2Departemen Ilmu Penyakit Dalam Divisi Endokrinologi, Fakultas
Kedokteran Universitas Sumatera Utara/RSUP H. Adam Malik Medan
ABSTRAK
Latar Belakang: Terjadinya hiperaktivitas trombosit terlihat pada penderita sindroma metabolik yang dapat diakibatkan oleh beberapa faktor seperti resistensi insulin, obesitas, dislipidemia dan hipertensi. Hiperaktivitas trombosit menyebabkan terjadinya agregasi trombosit yang dapat meningkatkan resiko terjadinya penyakit kardiovaskuler.
Tujuan: Untuk mengetahui perbedaan nilai agregasi trombosit dan MPV pada penderita sindroma metabolik dan obesitas
Metode: Penelitian dilakukan dengan metode potong lintang 30 orang yang datang ke Departemen Patologi Klinik dan Departemen Penyakit Dalam bagian Endokrin RSUP H. Adam Malik Medan periode Mei 2013 sampai Agustus 2013. Diagnosa sindroma metabolik ditegakkan berdasarkan kriteria IDF 2005.
Hasil: Dari 30 subjek didapati 11 orang sindroma metabolik dan 15 dengan obesitas. 4 orang dieksklusi karena memiliki kadar trigliserida yang tinggi (> 200mg/dL). Nilai agregasi trombosit yang didapat dengan agonis ADP tidak dijumpai bermakna antara sindroma metabolik dan obesitas. Tidak ada perbedaan yang bermakna pada nilai MPV pada penderita sindroma metabolik (9,6 ± 0,89) dengan obesitas (9,73 ± 0,74) dengan nilai p=0,672.
Kesimpulan: Tidak dijumpai perbedaan yang bermakna antara nilai agregasi trombosit dan MPV pada kelompok sindroma metabolik dibandingkan dengan kelompok obesitas.
PLATELET AGGREGATION AND MEAN PLATELET VOLUME ASSESSMENT IN PATIENTS WITH METABOLIC
SYNDROME AND OBESITY
Nindia Sugih Arto,(1), Adi K Aman,(1), Dharma Lindarto,(2), 1 Department of Clinical Pathology, School of Medicine, University of
Sumatera Utara / H. Adam Malik Medan Hospital
2 Department of Internal Medicine, School of Medicine, University of
Sumatera Utara / H. Adam Malik Medan Hospital
ABSTRACT
Background: Hyperactivity of platelet had been seen in patients with metabolic syndrome which can be caused by several factors such as insulin resistance, obesity, dyslipidemia and hypertension. Hyperactivity of platelet leads to platelet aggregation that can be increase the risk of cardiovascular disease.
Aim: To determine the platelet aggregation and mean platelet volume in patients with metabolic syndrome and obesity
Methode: 30 patients were choosen for this cross sectional study who came to the laboratory and policlinic in H. Adam Malik Medan Hospital, between May 2013 until August 2013. Diagnosis of metabolic syndrome criteria established by International Diabetic Federation 2005.
Result: From 30 patients with 15 metabolic syndrome and 15 obesity. Four patients were excluded because of the tryglyceride more than 200 mg/dl. There is no significant differences between platelet aggregation with agonist adenosin difosfat (ADP) in patient with metabolic syndrome and obesity. And there is no significant differences mean platelet volume values between metabolic syndrome (9,6 ± 0,93) and obesity (9,73 ± 0,74), with p value 0,846.
Conclusion: There is no significant differences between platelet aggregation and mean platelet volume values in metabolic syndrome and obese group
BAB 1
PENDAHULUAN
1.1 LATAR BELAKANG
Sindroma metabolik merupakan suatu kumpulan faktor
resiko yang terdiri atas obesitas, hipertensi, hiperglikemia puasa
dan dislipidemia yang dapat menyebabkan peningkatan resiko
terjadinya diabetes mellitus tipe 2 dan penyakit kardiovaskuler.
Sindroma Metabolik telah ada sejak ± 80 tahun yang lalu,
pada tahun 1933, Kylin, seorang dokter Swedia, merupakan orang
pertama yang menggambarkan sindroma metabolik sebagai
kumpulan dari gangguan metabolik yang dapat menyebabkan
resiko penyakit kardiovaskular aterosklerosis yaitu hipertensi,
hiperglikemi dan gout. Sindroma metabolik mendapat beberapa
nama lain seperti resistensi insulin, the deadly quartet, atau
sindroma dismetabolik.
1
Reaven mengemukakan tentang the role of insulin
resistance in human disease yang meliputi tiga topik yaitu adanya
sejumlah tanda – tanda dan gejala sehingga muncul sindroma yang
disebut sindroma X, sindroma ini umumnya meliputi resistensi
insulin dan komponen lain yang berhubungan dengan resistensi
menstimulasi asupan glukosa berperan penting pada prediksi
kejadian penyakit jantung koroner (PJK).
Sementara pada penelitian Kaplan mencentuskan the deadly
quartet yang meliputi obesitas tubuh bagian atas, hipertensi,
diabetes dan hipertrigliseridemia sebagai penyebab sindroma yang
berhubungan dengan peningkatan resiko penyakit kardiovaskular. 3
Tahun 1991, Zimmet menyarankan obesitas sentral masuk
dalam sindroma dan mengubah nama sindroma X menjadi
sindroma resistensi insulin atau metabolic syndrome (MetS).
4
Patofisiologi maupun etiologi yang terjadinya sindroma
metabolik masih belum jelas, tapi resistensi insulin dan obesitas
diduga merupakan patogenesis dari kelainan tersebut.
5
Obesitas menjadi masalah di seluruh dunia karena
prevalensinya yang meningkat pada orang dewasa dan anak
remaja baik di negara maju maupun negara sedang berkembang.
Diantara negara sedang berkembang, jumlah anak usia sekolah
dengan overweight terbanyak berada di kawasan Asia yaitu 60%
populasi atau sekitar 10,6 juta jiwa. Peningkatan prevalensi
obesitas terjadi karenga bekurangnya aktivitas fisik dan perubahan
pola makan.
5,7-8
Di Amerika Serikat, tahun 2005, data dari Behavioral Risk
Factor Surveillance System memperkirakan sebanyak 60,5% orang
Obesitas merupakan salah satu penyebab terjadinya sindroma
metabolik.
Secara global insiden sindroma metabolik meningkat secara
cepat, berdasarkan data The Third National Health and Nutrition
Examination Survey (NHANES). 10
11 Penelitian Ford dkk (2002),
terjadi peningkatan prevalensi sindroma metabolik dimana terjadi
peningkatan dari 6,7% menjadi 43,5% pada usia 20 sampai 29
tahun, sedangkan pada usia 60 sampai 69 tahun menjadi 42%.
Pada negara Mexico – Amerika juga terjadi peningkatan sebanyak
31,9%.
Penelitian Soegondo (2004) menunjukkan bahwa kategori
Indeks Masa Tubuh (IMT) obesitas ≥ 25 kg/m 12
2 lebih cocok
diterapkan pada orang Indonesia. Dari hasil penelitiannya didapat
prevalensi sindroma metabolik di Indonesia adalah 13,13%.
Penelitiannya yang lain, dilakukan di Depok (2001) didapati
prevalensi sindroma metabolik sebesar 25,7% pada pria dan 25%
pada perempuan serta tidak menutup kemungkinan prevalensi ini
akan terus meningkat seiring dengan waktu.
Soewondo dkk (2006) meneliti prevalensi sindroma
metabolik dengan menggunakan kriteria ATP III mendapatkan
prevalensi sindroma metabolik pada pria sebanyak 40,3% dan
perempuan sebanyak 59,7%.
13
Sindrom metabolik diprediksi menyebabkan kenaikan dua
kali lipat resiko untuk terjadinya penyakit jantung dan resiko
terjadinya diabetes mellitus (DM) tipe 2. Pada beberapa penelitian
dikatakan bahwa adanya aktivitas trombosit yang tinggi pada
penderita sindroma metabolik.15 Seperti halnya pada penelitian
Serebruany et al mengatakan adanya aktivitas trombosit yang
tinggi yang dapat menyebabkan terjadinya penyakit jantung. Kotani
et al juga mengatakan bahwa jumlah trombosit meningkat pada
penderita sindroma metabolik.
Perhitungan maupun penilaian terhadap fungsi trombosit
sangat penting. Salah satu fungsi trombosit yang sering diperiksa
adalah agregasi trombosit. Pemeriksaan agregasi trombosit
bertujuan mendeteksi abnormalitas fungsi trombosit. 16
Salah satu tes fungsi trombosit yang sudah banyak
digunakan adalah dengan light transmission aggregometry (LTA)
yang mengukur aggregasi trombosit dan juga merupakan gold
standard dari tes fungsi trombosit.
17
Namun pemeriksaan LTA tersebut hanya dapat dilakukan
dilaboratorium khusus dan membutuhkan waktu yang cepat. Maka
ada beberapa penelitian menggunakan Mean Platelet Volume
(MPV) sebagai indikator aktivitas trombosit pada sindrom metabolik
dimana MPV tersebut berhubungan dengan terjadinya penyakit
jantung.
16,17,18
Penelitian Yusuf Tavil, et al (2007) menemukan bahwa
terjadi peningkatan MPV pada pasien sindroma metabolik dengan
menggunakan kriteria ATP III.
Binita Shah et al (2004), mendapati hasil MPV yang
meninggi pada pasien diabetes melitus tetapi tidak pada penderita
sindroma metabolik.
20
Sehubungan data – data diatas sampai saat ini, studi
tentang penilaian aktivitas trombosit pada penderita sindroma
metabolik terutama menggunakan kriteria IDF belum pernah diteliti
di Indonesia, terutama di Medan. Oleh karena itu penulis ingin
meneliti ini.
21
1.2 RUMUSAN MASALAH
Apakah ada perbedaan nilai agregasi trombosit dan MPV
pada penderita sindroma metabolik dan obesitas ?
1.3 HIPOTESIS PENELITIAN
Ada perbedaan nilai agregasi trombosit dan MPV pada
1.4 TUJUAN PENELITIAN 1.4.1 Tujuan Umum
Mengetahui perbedaan nilai agregasi trombosit dan
MPV pada penderita sindroma metabolik dan obesitas.
1.4.2 Tujuan Khusus
1. Mengetahui nilai agregasi trombosit pada penderita
sindroma metabolik dan obesitas.
2. Mengetahui nilai MPV pada penderita sindroma
metabolik dan obesitas.
3. Mengetahui nilai karakteristik antara subjek sindroma
metabolik dan obesitas
1.5 MANFAAT PENELITIAN
Dengan pemeriksaan MPV dan agregasi trombosit dapat
memberi informasi tentang aktifitas trombosit pada penderita
sindroma metabolik dan dapat memprediksi seberapa jauh resiko
yang akan terjadi.
BAB 2
TINJAUAN PUSTAKA
2.1 TROMBOSIT
2.1.1 Produksi Trombosit
Sel trombosit merupakan pecahan fragmen kecil dari
sitoplasma megakariosit, berdiameter sekitar 2 – 5 μm. Ukurannya
dapat bervariasi bergantung dari jenis kelainan yang ada.
Trombosit diproduksi di sumsum tulang dengan cara fragmentasi
sitoplasma megakariosit yang dilepaskan ke dalam sirkulasi
darah.22 Prekusor megakariosit, megakarioblast, muncul melalui
proses diferensiasi sel induk hemopoetik. Megakariosit mengalami
pematangan dengan replikasi inti endomiotik yang sinkron,
memperbesar volume sitoplasma sejalan dengan penambahan
lobus inti menjadi kelipatan duanya. Setelah replikasi berhenti
(biasanya pada saat jumlah inti mencapai delapan), sitoplasma
mengalami granulasi dan melepaskan trombosit. Tiap sel dari
megakariosit akan menghasilkan 1000 – 1500 trombosit yang
diperkirakan akan menghasilkan 3500/µl trombosit per hari. Jarak
interval waktu dimulai dari diferensiasi sel induk sampai produksi
trombosit berkisar sekitar 10 hari.
Trombopoetin merupakan pengatur utama produksi
mempunyai reseptor untuk trombopoetin dan mengeluarkannya
dari sirkulasi.23,26,27
Jumlah trombosit normal adalah sekitar 250 x 10
9/l (rentang
150-400 x 109/l) dan lama hidup trombosit yang normal adalah 7-10
hari. Hingga sepertiga dari trombosit produksi sumsum tulang dapat
terperangkap dalam limpa yang normal, tetapi jumlah ini meningkat
menjadi 90% pada kasus splenomegali berat.22,27
2.1.2 Struktur Trombosit
Membran trombosit terdiri atas 2 lapis fosfolipid dan pada
permukaannya terdapat glikoprotein. Glikoprotein ini berfungsi
sebagai reseptor. Glikoprotein permukaan sangat penting dalam
reaksi adhesi dan agregasi trombosit. Adhesi pada kolagen
difasilitasi oleh glikoprotein Ia (GP Ia). Glikoprotein Ib dan IIb/IIIa
penting dalam perlekatan trombosit pada von Willebrand factor
(vWF) dan subendotel vascular. Reseptor IIb/IIIa juga merupakan
reseptor untuk fibrinogen yang penting dalam agregasi
trombosit.
Bagian dalam pada trombosit terdapat kalsium, nukleotida
(terutama ADP, ATP dan serotonin) yang terkandung dalam
granula padat. Granula alfa mengandung antagonis heparin, faktor
pertumbuhan (PDGF), β-tromboglobulin, fibrinogen, vWF. Organel
dan peroksisom yang mengandung katalase. Selama reaksi
pelepasan, isi granula dikeluarkan ke dalam sistem
kanalikular.26,27,28
2.1.3 Fungsi Trombosit
Fungsi utama trombosit adalah pembentukan sumbat
mekanik selama respon hemostasis normal terhadap cedera
vascular. Tanpa trombosit, dapat terjadi kebocoran darah spontan
melalui pembuluh darah kecil. Reaksi trombosit berupa adhesi,
sekresi, agregasi dan fusi serta aktivitas prokagulannya sangat
penting untuk fungsinya. Trombosit memainkan peranan penting
dalam keadaan perdarahaan dan trombosis. Sebagian besar fungsi
trombosit digunakan untuk mendiagnosis pasien pada keadaan
perdarahan.28,29,30
2.1.4 Pembentukan Sumbat Trombosit
Agar dapat terjadi hemostasis primer yang normal, trombosit
harus dalam jumlah yang cukup di dalam sirkulasi, dan trombosit
tersebut harus dapat berfungsi dengan normal. Fungsi hemostasis
yang normal diperlukan peran, serta trombosit yang berlangsung
secara teratur. Hal ini melibatkan pada awalnya, adhesi trombosit,
agregasi trombosit dan akhirnya reaksi pembebasan trombosit
2.1.4.1 Adhesi Trombosit
Setelah cedera pembuluh darah, trombosit akan melekat
pada jaringan ikat subendotel yang terbuka. Trombosit menjadi
aktif apabila terpajan dengan kolagen subendotel dan bagian
jaringan yang cedera. Adhesi trombosit melibatkan suatu
interaksi antara glikoprotein membrane trombosit dan jaringan
yang terpajan atau cedera. Adhesi trombosit bergantung pada
faktor protein plasma yang disebut faktor von Willebrand, yang
memiliki hubungan yang integral dan kompleks dengan faktor
koagulasi anti hemofilia VIII plasma dan reseptor trombosit yang
disebut glikoprotein Ib membran trombosit. Adhesi trombosit
berhubungan dengan peningkatan daya lekat trombosit
sehingga trombosit berlekatan satu sama lain serta dengan
endotel atau jaringan yang cedera. Maka terbentuklah sumbat
hemostatik primer atau inisial. Pengaktifan permukaan trombosit
dan rekrutmen trombosit lain akan menghasilkan suatu massa
trombosit lengket dan dipermudah oleh proses agregasi
trombosit.29-32
2.1.4.2 Agregasi Trombosit
Agregasi merupakan suatu kemampuan trombosit untuk
melekat satu sama lain untuk membentuk suatu sumbat.
pembebasan ADP dari trombosit lain yang melekat ke
permukaan endotel. Hal ini disebut gelombang agregasi primer.
Kemudian, seiring dengan makin banyaknya trombosit yang
terlibat, maka akan lebih banyak ADP yang dibebaskan
sehingga terjadi gelombang agregasi sekunder disertai
rekrutmen lebih banyak trombosit. Agregasi berkaitan dengan
perubahan bentuk trombosit dari discoid menjadi bulat.
Gelombang agregasi sekunder merupakan suatu fenomena
ireversibel, sedangkan perubahan bentuk awal dan agregasi
primer masih reversible. 29-32
2.2 TES FUNGSI TROMBOSIT
Trombosit pertama kali diidentifikasi melalui mikroskop yang
sudah ada semenjak 120 tahun yang lalu, namun penggunaan
perhitungan trombosit dan hapusan darah tepi untuk menilai
trombosit tidak digunakan secara luas hingga tahun 1950.
Perhitungan darah rutin secara otomatis termasuk jumlah
trombosit, pertama kali pada tahun 1970-an, yang memungkinkan
untuk mengukur parameter – parameter seperti mean platelet
volume (MPV), platelet distribution width (PDW), dan platelet large
cell ratio.
Tes fungsi trombosit dilakukan dengan bleeding time in vivo
tes skreening untuk fungsi trombosit sampai awal tahun 1990–an.
Lebih kurang 10 – 15 tahun terjadi penurunan penggunaan
bleeding time karena keterbatasannya dan berkembangnya tes
penyaring lainnya.
Pengukuran aggregasi trombosit (LTA) ditemukan pada
tahun 1960–an yang dapat mengidentifikasikan diagnosis
kerusakan hemostatik primer. LTA merupakan gold standar untuk
tes fungsi trombosit, dengan menambahkan agonis dari berbagai
konsentrasi yang berbeda pada trombosit, yang dapat
memungkinkan untuk mendapatkan informasi yang banyak dari
berbagai aspek yang berbeda pada fungsi dan biokimia trombosit. 34,35
37
2.2.1 Light Transmission Aggregometry 2.2.1.1 Prinsip Kerja
Platelet agregometry bekerja berdasarkan prinsip
turbidimetri seperti yang dilakukan Born pada tahun 1962,
dimana absorbans lebih tergantung pada jumlah partikel
dibandingkan dengan ukurannya. Pada prosedur pemeriksaan
ini lebih ditekankan pada pemeriksaan agregasi trombosit
dengan menggunakan agonis ADP. Alat ini distandarisasi
memakai plasma kaya trombosit (PRP) sebagai 0% agregasi
dan plasma miskin trombosit (PPP) sebagai 100% agregasi.
trombosit yang diaduk pada suhu 37°C. Bila terbentuk aggregat
setelah penambahan agonis, dijumpai peningkatan transmisi
cahaya. Agonis yang berbeda menghasilkan pola agregasi yang
berbeda. Pola agregasi trombosit dikenal respon primer
terhadap penambahan agonis eksogen seperti ADP, diikuti
respon sekunder dari pelepasan adenine nukleotida yang
terdapat dalam granula padat trombosit. Respon tersebut
dikenal sebagai gelombang pertama dan kedua. Respon bifasik
ini dapat tidak terlihat pada penambahan agonis konsentrasi
tinggi. Dengan agonist kolagen, pola agregasi menggambarkan
adhesi trombosit dengan fibril kolagen diikuti agregasi trombosit.
Aspirin dapat menghambat agregasi trombosit dengan agonis
kolagen dosis rendah, tetapi pada dosis yang lebih tinggi
agregasi masih terjadi.35,36,37
2.2.1.2 Variabel Pemeriksaan Agregasi Trombosit a. Vena punksi
Pengambilan sampel darah pada orang dewasa sebaiknya
menggunakan jarum ukuran 18-20G dengan, sedangkan
pada anak sebaiknya menggunakan jarum ukuran 23-25G.
peningkatan respon terhadap ADP dosis rendah dijumpai
b. Antikoagulan
Antikoagulan yang digunakan untuk agregasi trombosit
adalah sitrat (0,1 dan 0,129 M) dengan rasio perbandingan 9
bagian darah dengan 1 bagian antikoagulan. Antikoagulan
yang baik untuk dipakai agregasi adalah 0,1M sodium sitrat
bufer yang juga dapat mempertahankan pH bila dilakukan
pengerjaan 1 – 2 jam.
c. Tabung Kaca vs Tabung Plastik
36,38,39
Pemeriksaan agregasi trombosit harus menggunakan
tabung plastik atau tabung kaca yang dilapisi silikon. Tabung
kaca yang tidak dilapisi akan menyebabkan terjadinya
aktivasi trombosit dan akan mempengaruhi hasil.
d. Jumlah Trombosit
36,38,39
Pemeriksaan agregasi trombosit dipengaruhi oleh jumlah
trombosit, namun masih dalam perdebatan untuk
menstandarisasi jumlah trombosit PRP yang digunakan
untuk pemeriksaan agregasi trombosit. Biasanya
pemeriksaan agregasi trombosit dilakukan pada jumlah
250.000 – 300.000/mm3.
e. pH
36,38,39
pH yang digunakan untuk pemeriksaan agregasi trombosit
pH 7,2 – 7,4. Bila pH menurun sampai 6,5 maka tidak akan
terjadi agregasi spontan. Disarankan untuk menyimpan
plasma trombosit pada tabung yang tertutup.
f. Suhu
36,38,39
Suhu yang dipakai untuk melakukan agregasi trombosit
pada suhu 370C agar menyerupai keadaan tubuh,
sedangkan suhu yang digunakan untuk menyimpan sampel
selama persiapan tes sebaiknya pada suhu ruangan.
Laporan menunjukkan penyimpanan pada suhu dingin akan
menyebabkan agregasi spontan yang terjadi sewaktu
penghangatan sampel kembali.
g. Kontaminasi Sel Darah Merah, Hemolisis dan Lipemia
36,38,39
Pemeriksaan agregasi trombosit dilakukan dengan
menggunakan transmisi optik, adanya partikel kontaminan
seperti sel darah merah dan lipid akan dapat mempengaruhi
agregometer dan penurunan persentasi agregasi. Sel darah
merah yang lisis akan melepaskan ADP, yang dapat
mengganggu jumlah ADP yang diberikan sebagai
agonis.
h. Kecepatan Putaran Agregometer
36,38,39
Agar agregasi terjadi, trombosit harus kontak satu sama lain.
Jika agonis ditambahkan pada trombosit yang tidak diputar,
maka trombosit hanya akan teraktifasi namun tidak
alat diperhitungkan berdasarkan tinggi kolom PRP, diameter
kuvet dan ukuran batangan pemutar yang digunakan.
Batasan Waktu
36,38,39
Trombosit membutuhkan waktu satu jam ”istirahat”
setelah persiapan PRP untuk mendapatkan respon stabil
pada ketiga konsentrasi (2, 5, 10 µM) dari agonis ADP yang
digunakan pada pemeriksaan agregasi. Kestabilan respon
trombosit ini akan bertahan selama 3 jam, kemudian akan
mulai menghilang dimulai dari konsentrasi ADP yang paling
rendah. Karena itu direkomendasikan untuk menyelesaikan
pemeriksaan agregasi dalam waktu kurang dari 3 jam
setelah persiapan PRP dilakukan. 36,38,39
2.2.1.3 Agonis
Penentuan agonis platelet yang akan digunakan sangat
penting sebelum melakukan pemeriksaan fungsi platelet. Agonis
merangsang platelet melalui dua macam signaling system.
Yang pertama tergantung pada phospholipase A 33, 36,37,39
2 (PLA2) dan
penggunaan COX serta sintesa thromboxane untuk
menghasilkan agonis thromboxan A2, yang akan mengaktifkan
platelet melalui reseptornya. Sistem lainnya tergantung pada
triphosphat (IP3) dan diasil gliserol (DAG). Masing – masing
mengaktifkan reseptor IP3 dan protein kinase C.
Agonis yang sering digunakan antara lain:
40,41,42
1. ADP
Konsentrasi ADP 1-10 µM sering dipakai pada pemeriksaan
agregasi trombosit. Konsentrasi ADP yang rendah (1-3 µM)
menghasilkan kurva tunggal (monophasik) atau kurva
bifasik. Pada konsentrasi yang rendah, ikatan fibrinogen
biasanya bersifat reversible dan trombosit akan disagregasi.
Konsentrasi ADP yang lebih tinggi (10-20 µM) dapat
menutupi respon biphasic yang ditimbulkan pelepasan ADP
endogen. Ini masih dianggap respon biphasic karena terjadi
pelepasan ADP tetapi tidak tampak pada kurva. Aspirin akan
menghambat respon agregasi ADP dengan konsentrasi
rendah, karena hambatan jalur siklooksigenase dan
pelepasan isi granul.
2. Epinephrin
Konsentrasi epinephrine yang dipakai 5-10 µM untuk
pemeriksaan agregasi. Respon pertama yang muncul
berupa gelombang kecil, kadang diikuti respon gelombang
kedua yang lebih besar. Gelombang kedua ini dihambat oleh
aspirin, obat anti inflamasi non steroid (NSAIDs),
merupakan agonis yang paling tidak konsistensi dari
keseluruhan agonis yang sering digunakan.
3. Kolagen
Biasanya dipakai kadar 1-5 µg/ml. Kolagen adalah agonist
yang paling kuat. Agregasi trombosit yang diinduksi kolagen
menunjukkan lag phase sekitar 1 menit, dimana pada saat
itu trombosit berikatan pada fibril kolagen dan mengalami
perubahan bentuk dan reaksi pelepasan. Respon agregasi
yang diukur adalah gelombang kedua setelah aktivasi dan
pelepasan trombosit. Pada kolagen konsentrasi rendah,
respon agregasi trombosit dapat dihambat aspirin dan obat
anti trombosit lain.
4. Asam Arakidonat
Asam arakidonat direaksikan dengan siklooksigenase, asam
arakidonat diubah menjadi tromboksan A2
5. Ristocetin
. Aspirin
menghambat siklooksigenase dan respon agregasi terhadap
asam arakidonat. Pasien yang mengkonsumsi aspirin atau
memiliki gangguan pelepasan intrinsik atau Glanzman
thromboasthenia akan memberikan hasil agregasi trombosit
yang abnormal.
Pada keadaan trombosit normal, antibiotik ristocetin dengan
tergantung GpIb/vWF. Bila responnya abnormal, dicurigai
penyakit von Willebrand atau sindroma Bernard Soulier
(kekurangan kompleks GpIb-IX-V).
6. α - Trombin
α - trombin adalah agonist trombosit yang sangat kuat.
Peptida sintetik Gly-Pro-Arg-Pro (GPRP) menghambat
polimerisasi fibrin yang diinduksi thrombin, sehingga dapat
terjadi agregasi trombosit yang diinduksi thrombin.
Konsentrasi α-trombin 0,1-0,5 U/mL dapat digunakan untuk
mengakifasi trombosit, melalui proses pencucian dan
gel-filtered.
7. TRAP
Thrombin receptor activating peptide (TRAP) adalah peptide
sintetik yang berikatan dengan sekuens asam amino
N-terminal dari “tethered ligand” yand dibentuk setelah
hidrolisis thrombin protease activated receptor (PAR1).
Penambahan TRAP 10 µM menyebabkan aktivasi respon
trombin yang sangat kuat tanpa pemecahan fibrinogen dan
pembentukan clot. Pada umumnya trombosit menunjukkan
respon agregasi normal terhadap TRAP kecuali pada
Glanzmann thromboasthenia. Sekarang ini TRAP dipakai
yang menghambat ikatan fibrinogen dengan trombosit atau
yang mengganggu reseptor PAR di trombosit.
2.2.2 MPV (Mean Platelet Volume)
MPV dan trombosit dihitung menggunakan automated blood
cells counter yang menggunakan teknologi aperture-impedance
untuk mengukur trombosit. Di samping itu, sel-sel difokuskan
melewati celah kecil secara hidrodinamik, dan gelombang listrik
yang sesuai dengan ukuran dan volume sel dihasilkan. Pemisah
“autodiscriminators” yang bergerak memisahkan antara machine
noise pada bagian bawah dan sel darah merah pada bagian atas
dari setiap distribusi volume trombosit. MPV dihitung dengan
menggunakan rumus: MPV (fL)=Pct (%)x1000 Plt (x103/µL),
dimana Plt adalah jumlah trombosit dan jumlah partikel diantara
pemisah atas dan bawah, Pct merupakan platelet crit dan dihitung
secara elektronik dari data histogram.43
2.3 SINDROMA METABOLIK 2.3.1 Definisi
Reaven mengidentifikasikan pertama kali tentang sindroma
metabolik yang disebut juga dengan sindrom X, dimana yang
termasuk kedalam sindrom tersebut adalah hiperinsulinemia,
trigliserida. Ada 3 komite yang dapat diambil sebagai kriteria
sindrom metabolik, yakni World Health Organization (WHO),
National Cholesterol Education Program - Third Adult Treatment
Panel (NCEP ATP III), dan the International Diabetes Federation
(IDF).1, 11
Tabel 2.1 Kriteria dari Sindroma Metabolik KOMPONEN
Dislipidemia TG > 150 mg/dL; HDL-C
Lain – lain Mikroalbuminuria
Kriteria
TG: Trigliserida; HDL-C: Kolesterol; DM: Diabetes Melitus : L: Laki – laki; W: Wanita, IMT: Indeks Masa Tubuh,
2.3.2 Epidemiologi
Prevalensi sindroma metabolik sangat bervariasi
berdasarkan definisi maupun populasi studi. Berdasarkan data dari
third National Health and Nutrition Examination Survey tahun 1988–
1994 dengan menggunakan kriteria NCEP – ATP III didapatkan
16% pria berkulit hitam dan 37% wanita. Prevalensi meningkat
dengan bertambahnya usia dan berat tubuh.
Prevalensi di negara Ghana didapatkan 102 (49,5%) pria
dan 104 (50,5%) wanita yang masing – masing berusia antara
40-60 tahun dengan kriteria IDF dan ATP III.
11,46,47
Prevalensi pada remaja cenderung lebih rendah daripada
prevalensi dewasa yang biasanya dikaitkan dengan overweight dan
obesitas. Di Amerika, terjadi peningkatan prevalensi sindroma
metabolik sebesar 22% baik wanita maupun pria. Peningkatan lebih
tinggi bila dihubungkan dengan overweight (20%) dan obesitas
(60%). Analisa data dari 991 orang dewasa, dari tahun 1999-2000
dengan kriteria NHNES ditemukan terjadi peningkatan disemua
gejala sekitar 6,4%.
48
Penelitian Soegondo (2004) didapatkan prevalensi sindroma
metabolik di Indonesia adalah 13,13% penelitiannya yang lain,
dilakukan di Depok (2001) didapati prevalensi sindroma metabolik
sebesar 25,7% pada pria dan 25% pada wanita. 8,11,12
2.3.3 Patofisiologi Sindroma Metabolik
Patogenesis sindroma metabolik masih tidak jelas, tetapi
kelainan dasarnya adalah resistensi insulin.48 Resistensi insulin
didefinisikan sebagai suatu kondisi dijumpainya produksi insulin
yang normal namun telah terjadi penurunan sensitivitas jaringan
terhadap kerja insulin, sehingga terjadi peningkatan sekresi insulin
sebagai bentuk kompensasi sel Beta. Resistensi insulin ini sering
mendahului onset dari diabetes tipe 2 dan mempunyai kontribusi
dalam perkembangan terjadinya keadaan hiperglikemi. Dan
resistensi insulin dijumpai pada sebagian besar pasien dengan
sindroma metabolik.6, 49
2.3.3.1Resistensi Insulin
Hipotesis yang paling diterima untuk menggambarkan
patofisiologi sindroma metabolik adalah resistensi insulin dan
obesitas sentral. Penumpukan sel lemak bebas (NEFA) akan
meningkatkan asam lemak bebas dari hasil lipolisis, yang akan
menurunkan sensitifitas terhadap insulin. Peningkatan NEFA ini di
liver akan meningkatkan glukoneogenesis, meningkatkan produksi
glukose dan menurunkan ekstraksi insulin sehingga terjadi
hiperinsulinemia. Di otot akan menurunkan pemakaian glukosa dan
di sel β pankreas akan menurunkan sekeresi insulin.49 Sel lemak
leptin yang berhubungan dengan penurunan resistensi terhadap
insulin.50 TNF α menyebabkan resistensi dengan cara menghambat
aktifitas tirosin kinase pada reseptor insulin dan menurunkan
ekspresi glucose transporter-4 (GLUT-4) di sel lemak dan otot.
Sementara adiponektin yang dapat menurunkan resistensi
terhadap insulin kadarnya menurun pada sindroma metabolik.50
Resistensi insulin dan hiperinsulinemia pada gilirannya akan
menyebabkan perubahan metabolik, sehingga timbul hipertensi,
dislipidemia, peningkatan respon inflamasi dan koagulasi, melalui
mekanisme yang kompleks, diantaranya mekanisme disfungsi
endotel dan oksidatof stres.51 Resistensi insulin semakin lama
semakin berat dan sekresi insulin akhirnya menurun, sehingga
terjadi hiperglikemia dan manifestasi DM type 2.46,50
2.3.3.2 Obesitas
Obesitas merupakan komponen utama terjadinya sindroma
metabolik, namun mekanisme yang jelas belum diketahui degan
pasti. Obesitas yang diikuti dengan meningkatnya metabolisme
lemak akan menyebabkan produksi Reactive Oxygen Species
(ROS) meningkat baik disirkulasi maupun sel adiposa.
Meningkatnya ROS didalam sel adiposa dapat menyebabkan
keseimbangan reaksi reduksi oksidasi terganggu, sehingga enzim
stres oksidatif. Meningkatnya stres oksidatif menyebabkan
disregulasi jaringan adiposa dan merupakan awal patofisiologi
terjadinya sindroma metabolik, hipertensi dan aterosklerosis.
Obesitas umumnya diakibatkan oleh ketidakseimbangan
antara asupan dan penggunaan energi, dimana asupan lebih besar
daripada penggunaan energi. Obesitas disebabkan oleh banyak hal
tetapi terutama oleh faktor genetik dan lingkungan.
53, 54
Tipe obesitas dapat dibedakan menjadi obesitas tubuh
bagian atas (upper body obesity) dan obesitas tubuh bagian bawah
(lower body obesity). Obesitas dapat dinilai dengan berbagai cara,
Metode yang lazim digunakan saat ini antara lain pengukuran IMT
(Index Massa Tubuh), lingkar pinggang, serta perbandingan lingkar
pinggang dan panggul.
53, 54
Diantara kedua pemeriksaan ini, IDF dan
NCEP ATP III lebih merekomendasikan untuk menggunakan
pemeriksaan lingkar pinggang sebagai pemeriksaan obesitas
Tabel 2.2 Klasifikasi IMT Negara/Grup Etnis
46, 55
Lingkar Pinggang (cm) pada Obesitas
Eropa Pria > 94, Wanita > 80
Asia Selatan Populasi Cina, Melayu, dan Asia-India
Pria > 90, Wanita > 80
China Pria > 90, Wanita > 80
Jepang Pria > 85, Wanita > 90
Amerika Tengah Gunakan rekomendasi Asia Selatan hingga tersedia data spesifik
Sub Sahara Afrika Gunakan rekomendasi Eropa hingga tersedia data spesifik
Timur Tengah Gunakan rekomendasi Eropa hingga tersedia data spesifik
Tabel 2.3 Klasifikasi IMT untuk Asia Klasifikasi
55
IMT (kg/m2) Resiko Underweight < 18.5 Rendah
Normal Range 18.5 – 24.99 Sedang
Ciri daripada dislipidemia adalah peningkatan trigliserida
(TG), penurunan HDL, peningkatan small dense LDL meskipun
total LDL kadang normal. Dislipidemia diduga berhubungan dengan
hiperinsulinemia. Pada resistensi insulin terjadi peningkatan
plasma selanjutnya akan meningkatkan uptake asam lemak bebas
ke dalam liver.
Asam lemak bebas yang meningkat akan menyebabkan
peningkatan trigliserida, sehingga VLDL yang terbentuk pada
keadaan resistensi insulin akan sangat kaya dengan trigliserida.
Pada resistensi insulin akan terjadi hiperinsulinemia dimana
aktifitas enzim hepatik lipase juga meningkat dan akan
menghidrolisis trigliserida yang dikandung LDL sehingga
menghasilkan LDL yang kecil dan padat. LDL tersebut sangat
mudah teroksidasi dan lebih mudah menempel pada dinding
pembuluh darah dan bersifat atherogenik. 54,57
Hal ini diperparah oleh adanya komponen apo-B yang
membuat partikel LDL tertahan lebih lama di lapisan dalam dinding
pembuluh darah lapisan intima yang menyebabkan terjadinya
oxidative stress. Oxidative stress menyebabkan terjadinya disfungsi
endotel. Disfungsi endotel ini menyebabkan terjadinya
vasokonstriksi pada dinding pembuluh darah dan bila berlangsung
lama dapat menyebabkan terjadinya atherosklerosis. 54,57-60
2.3.4 Trombosit Pada Sindrom Metabolik
Peningkatan respon trombosit terlihat pada penderita
sindroma metabolik yang diakibatkan oleh beberapa mekanisme,
seperti resistensi insulin, obesitas khususnya obesitas sentral,
dislipidemia, maupun hipertensi.
Pada keadaan resistensi insulin (dependent) terjadi
peningkatan pada konsesntrasi kalsium intraseluler yang
mempercepat degranulasi trombosit dan agregasi trombosit,
sedangkan yang tidak tergantung pada resistensi insulin terjadi
gangguan terhadap NO dan PGI2 yang meningkatkan reaktivitas
trombosit.
14,15
Obesitas juga berperan dalam disfungsi trombosit, terutama
dalam adhesi dan aktifasi, akibat meningkatmya konsentrasi
kalsium sitosolik. Abnormalitas profil lemak, khususnya trigliserida
juga mempengaruhi reaktifitas trombosit melalui mekanisme yang
berbeda termasuk merangsang terjadinya disfungsi endotel.
Disfungsi endotel akibat terjadinya penurunan produksi NO dan
PGI2 dan memicu timbulnya keadaan prothrombotic melalui
peningkatan produksi tissue factor (TF). 30,58,60
Genetik Lingkungan
Obesitas
Resistensi Insulin
Sindroma Metabolik
Disfungsi Endotel
Hiperaktivasi Trombosit
Thrombus
Atherosklerosis
PKV
BAB 3
METODE PENELITIAN
3.1 Desain Penelitian
Penelitian dilakukan dengan cara cross sectional (potong
lintang). Dimana jumlah sampel dibatasi minimal sesuai perkiraan
jumlah sampel atau sampai batas waktu pengumpulan sampel
yang ditetapkan. Pengukuran variabel dilakukan hanya satu kali.
3.2 Tempat dan Waktu
Penelitian dilakukan di Laboratorium Departemen Patologi
Klinik RSUP. H. Adam Malik Medan bekerja sama dengan
Departemen ilmu Penyakit Dalam RSUP. H. Adam Malik Medan.
Penelitian dilakukan mulai bulan Mei 2013 sampai Agustus 2013.
3.3 Populasi dan Sampel
Kelompok kasus adalah pasien – pasien dengan sindroma
metabolik yang datang ke Poliklinik Endokrin Penyakit Dalam dan
Laboratorium Patologi Klinik RSUP. H. Adam Malik Medan. Dan
sebagai pembanding adalah subjek dengan obesitas yang telah
disesuaikan umur dan jenis kelaminnya serta tidak pernah terkena
sindroma metabolik. Seluruh peserta yang ikut dalam penelitian ini
tentang prosedur penelitian dan kemungkinan efek yang kurang
menyenangkan yang mungkin timbul meskipun kecil.
3.4 Perkiraan Besar Sample
Pengambilan sampel dengan cara consecutive sampling
dimana jumlah sampel minimal sesuai perkiraan jumlah sampel
atau sampai batas waktu pengumpulan sampel yag ditetapkan.
Perkiraan besar sampel minimum dan subjek yang diteliti dipakai
rumus uji tidak berpasangan, rumus sebagai berikut:
2σ2 (Z1 - α/2 + Z1 - β)
Menurut rumus diatas maka diperlukan sampel dan kontrol
sebanyak :
n1= n2 = 2. 1,492 . (1,96 + 1,282)
2
2
2
= 11,6 = 12 sampel
3.5 Kriteria Inklusi dan Eksklusi
3.5.1 Kriteria Inklusi
1. Bersedia ikut dalam penelitian.
2. Penderita sindroma metabolik sesuai dengan kriteria
menurut IDF 2005, sebagai pembanding pada penderita
yang obesitas IMT ≥ 25 kg/m
3. Pasien dengan usia 30 – 60 tahun 2
3.5.2 Kriteria Eksklusi
1. Tidak mau ikut serta dalam penelitian ini
2. Pasien yang sedang menggunakan obat anti trombosit
(aspirin, clopidogrel, dll)
3. Perokok
4. Penderita – penderita yang secara klinis terbukti
3.6 Bahan dan Cara Kerja
3.6.1 Bahan Yang diperlukan
Bahan yang diperlukan dalam penelitian ini adalah
darah EDTA, darah sitrat dan darah tanpa antikoagulan.
3.6.2 Anamnese dan Pemeriksaan Fisik
Terhadap semua pasien yang bersedia ikut dalam penelitian
dilakukan:
a. Anamnese dan pencatatan umur, jenis kelamin, riwayat
merokok, riwayat keluarga menderita diabetes,
hipertensi, infark miokard, riwayat penggunaan obat,
serta aktifitas fisiknya.
b. Pengukuran Tinggi Badan (cm) dengan menggunakan
pengukur tinggi badan, kemudian subjek diminta
melepaskan alas kaki (sepatu/sandal), dan topi. Subjek
berdiri tegak dengan posisi kepala dan bahu bagian
belakang, lengan, bokong dan tumit menempel pada
dinding tempat microtoise di pasang. Pandangan lurus
kedepan dan tangan dalam posisi bergantung bebas.
Pencatatan dilakukan dengan ketelitian sampai satu
angka dibelakang koma.
c. Pengukuran berat badan (kg) menggunakan timbangan
merk camry. Letakkan timbangan di lantai yang rata,
pinggang, serta mengeluarkan isi kantong yang berat
seperti kunci dan lain-lain, kemudian subjek diminta naik
ke alat timbang dengan posisi kaki tepat di tengah alat
timbang tapi tidak menutupi jendela baca. Minta subjek
bersikap tenang (tidak bergerak-gerak) dan kepala tidak
menunduk (memandang lurus kedepan).
d. Pengukuran tekanan darah dengan alat
sphygmomanometer (nova), dimana pasien dibaringkan
selama 5 menit kemudian dipasang manset pada lengan
kanan dan dilakukan pengukuran sebanyak 2 kali dan
diambil nilai reratanya.
e. Pengukuran lingkar pinggang dengan pita pengukur
merk buterfly (tanpa ada penghalang seperti tali
pinggang, korset) dalam keadaan akhir ekspirasi dengan
posisi berdiri tegak tanpa alas kaki dengan jarak kedua
tungkai 20-25 cm. Pengukuran dilakukan melingkar
pertengahan antara puncak krista iliaca dan tepi bawah
kosta terakhir. Hasil pengukuran dinyatakan dengan
sentimeter. Pengukuran yang benar di lakukan dengan
menempelkan pita pengukur di atas kulit langsung.
3.6.3 Pengambilan dan Pengolahan Sampel
Darah subjek diambil setelah subjek berpuasa selama
10-12 jam sebelumnya . Dilakukan tindakan flebotomi pada
vena mediana cubiti sejumlah 12 mL darah vena yang
diambil dan dibagi kedalam 3 tabung sodium sitrat 3,2% (2,7
mL), satu tabung serum (2 mL) dan satu tabung K2EDTA (2
mL). Tempat vena terlebih dahulu dibersihkan dengan
alkohol 70% dan dibiarkan kering.
3.7 Pemeriksaan Laboratorium
Untuk pengukuran KGDP, TG, HDL-C, dilakukan segera
setelah sampel terkumpul. Sedangkan untuk pengukuran agregasi
trombosit dilakukan dengan segera.
3.7.1.1 Pemeriksaan Darah lengkap
Dengan alat automatic cell counting Sysmex XT 2000i.
Bahan sampel darah EDTA. Prinsip pemeriksaan
flowcytometri.
3.7.1.2 Pemeriksaan Kadar Gula Darah
Pemeriksaan dilakukan dengan metode enzimatik
heksokinase dengan alat Automatic Cobas 6000 C 501.
Panjang gelombang 340 nm.
Sampel stabil : 8 jam pada suhu 20 – 25 0
pada suhu 4 – 8
C, 72 jam
3.7.1.3 Pemeriksaan Trigliserida
Pemeriksaan dengan metode enzimatik kolorimetrik,
dengan alat Automatic Cobas 6000 C 501. Panjang
gelombang 512 nm.
Sampel stabil : 7 hari pada 4 0C, 3 bulan pada -20 0
Beberapa tahun -70
C,
0
3.7.1.4 Pemeriksaan HDL-C
C
Pemeriksaan dengan metode enzimatik kolorimetrik,
dengan alat Automatic Cobas 6000 C 501. Panjang
gelombang 583 nm.
Sampel stabil : 7 hari pada suhu 2-80
suhu - 70
C, 30 hari pada
0C, 7-14 hari pada suhu -200
3.7.1.5 Pemeriksaan Agregasi Trombosit
C
Menggunakan alat Platelet Aggregometer AggRam
Analyzer Helena.
Persentase aggregasi trombosit diperiksa menggunakan
light transmission aggregometre (LTA) AggRAM Helena
Laboratories yang menggunakan prinsip turbidimetri.
Tiga tabung (9 mL) darah sodium sitrat 3,2% dengan
perbandingan 9 bagian darah dengan 1 bagian
antikoagulan dihomogenkan perlahan sebanyak 4 kali
lalu diputar dengan kecepatan 500 rpm selama 10 menit.
dengan hati – hati (hindari terkena bagian buffy coat) ke
cuvette, ditutup rapat, dan didiamkan selama 15-30
menit untuk menunggu trombosit dalam posisi istirahat.
Pengolahan sampel
1. Platelet Rich Plasma (PRP)
Darah sitrat disentrifus 500 rpm selama 10 menit. Plasma yang
diperoleh adalah PRP, kemudian dipindahkan ke dalam tabung
plastik tertutup. Hindarkan kontaminasi oleh leukosit maupun
eritrosit. Jumlah trombosit PRP harus 200.000 – 300.000/uL.
2. Platelet Poor Plasma (PPP)
Sisa darah dalam tabung sitrat yang telah dipisahkan PRP-nya,
disentrifus lagi 4000 rpm selama 15 menit. Plasma yang
diperoleh adalah PPP.
3. PRP dan PPP baik pada pemutaran maupun penyimpanan
dilakukan pada suhu kamar antara 15 – 300
4. Pemeriksaan agregasi dilakukan sesudah 30 menit dari
persiapan PRP. Untuk menghindari bias, seluruh pemeriksaan
harus sudah selesai dikerjakan dalam waktu 60 menit, karena
trombosit menjadi reaktif bila dibiarkan lebih dari 2 jam. C
3.8 Pemantapan Kualitas
Pemantapan kualitas dilakukan setiap kali pada saat awal
dikerjakan. Hal – hal yang perlu diperhatikan adalah prosedur
pemeriksaan, penggunaan alat – alat yang harus sesuai dengan
petunjuk, ataupun reagensia yang digunakan. Pemeriksaan
laboratorium klinik baik apabila test tersebut teliti (precision) dan
akurat dengan batas nilai yang dikeluarkan oleh pabrik pembuatnya
(ada nilai target).
Pemantapan kualitas berguna untuk mencegah terjadinya
kesalahan dalam pemeriksaan. Untuk itu sebelum melakukan
pemeriksaan perlu dilakukan persiapan yang cukup untuk
menghindari kesalahan dalam pemeriksaan. Prosedur yang harus
diperhatikan diantaranya adalah dimulai dari preanalitik, analitik
dan postanalitik.
3.8.1 MPV
Pemantapan kualitas pada MPV dilakukan dengan cara
memasukkan darah kontrol ke dalam file kontrol pada alat sysmex
XT-2000i. Dimana darah kontrol tersebut telah diketahui nilainya
yaitu tinggi, rendah dan normal. Sebelum pemantapan kualitas
kontrol dianalisa, pastikan file pemantapan kualitas telah disiapkan.
Homogenkan darah kontrol dengan baik dan benar. Pastikan hasil
3.8.2 Agregasi Trombosit
Pemerikaan fungsi agregasi trombosit harus dilakukan
segera dan tidak dapat ditunda. Untuk itu ada pemantapan kualitas
pemeriksaan agregasi trombosit melalui kalibrasi panjang
gelombang cahaya dengan larutan Scale Set yang dilakukan setiap
bulan sebelum pemeriksaan sampel. Dicatat nilai absorben untuk
larutan jernih dan keruh. Nilai absorben untuk larutan jernih
berkisar antara 0,160 – 0,180. Nilai absorben untuk larutan keruh
berkisar antara 0,600 – 0,800. Hasil yang diperoleh (V/OD) berkisar
0,350 – 0,370. Untuk kalibrasi harian, dipakai larutan aquabidest
dengan nilai target absorben berkisar 0,160 – 0,180. Kalibarasi ini
dilakukan setiap hari sebelum pemeriksaan agregasi platelet
dilakukan.
3.8.3 Pemeriksaan Kimia
Kalibrasi alat untuk pemeriksaan KGDP C.f.a.s. (calibrator
for automated system) Lot No. 667583 dan TG digunakan C.f.a.s.
Lot No. 671262.
Kalibrasi alat untuk pemeriksaan HDL-C digunakan c.f.a.s.
lipid Lot No. 668383 .
Kalibrator dalam bentuk serbuk kemudian diencerkan
dengan 3mL aquadest, larutan dihomogenkan dengan
gelembung, kemudian dibiarkan selama 30 menit kemudian
dilakukan kalibrasi. Kalibrasi dilakukan 1 kali pada waktu membuka
reagen baru.
3.9 Definisi Operasional • Agregasi Trombosit
a. PPP
PPP merupakan plasma yang diperoleh dari memutar darah
sodium sitrat pada kecepatan 4000 rpm selama 15 menit.
b. PRP
PRP merupakan plasma yang diperoleh dari memutar darah
sodium sitrat pada kecepatan 500 rpm selama 10 menit.
• MPV
MPV menggambarkan ukuran trombosit, yang ditentukan dari
kurva histogram trombosit. Nilai normal: 7,0-10,2 fL.
• Sindroma Metabolik, adalah kumpulan kelainan metabolik lipid dan karbohidrat yang dikaitkan dengan peningkatan resiko
diabetes melitus dan penyakit kardiovaskular. Ditentukan
menggunakan kriteria IDF 2005 yang terdiri dari:
a. Obesitas
Lingkar pinggang digunakan untuk menentukan ada tidaknya
ditetapkan oleh IDF 2005 yaitu pada wanita ≥ 80cm dan
pada pria ≥ 90cm.
b. Dislipidemia
Adalah gangguan profil lipid darah, ditandai dengan
peningkatan konsentrasi trigliserida (≥150 mg/dl ) dan atau
penurunan HDL (Laki-laki < 40 mg/dl, wanita < 50 mg/dl)
atau pernah menderita dyslipidemia atau sedang minum obat
anti lipid.
a. Hipertensi
Adalah peningkatan tekanan darah (≥130/85 mmHg) atau
pernah menderita hipertensi atau sedang mengkonsumsi
obat-obat antihipertensi.
b. Intoleransi glukosa
Meliputi toleransi glukosa puasa terganggu ataupun DM tipe
2, sesuai dengan kriteria IDF 2005 yaitu kadar gula darah
puasa > 100 mg/dl.
3.10 Analisa Data
Analisa statistik dilakukan dengan menggunakan SPSS (Statistical
Package for the Social Science) versi 17. Menerangkan variabel
karakteristik antara kedua kelompok disajikan dalam bentuk
tabulasi dan dideskripsikan. Untuk melihat perbedaan nilai MPV
obesitas dilakukan uji T Independent jika data kedua kelompok
berdistribusi normal, data yang tidak berdistribusi normal dilakukan
analisis dengan menggunakan uji non parametrik yaitu Mann
Whitney. Hasil tes dikatakan bermakna apabila nilai p < 0,05
3.11 Ethical Clearance dan Informed Consent
Ethical clearance diperoleh dari komite Penelitian Bidang
Kesehatan Fakultas Kedokteran Universitas Sumatera Utara
Medan. Informed consent diminta secara tertulis dari subjek
penelitian atau diwakili oleh keluarganya yang menyatakan
bersedia ikut dalam penelitian setelah mendapat penjelasan
mengenai maksud dan tujuan dari penelitian ini.
Ethical Clearance diperoleh dari Komite Penelitian Bidang
Kesehatan Fakultas Kedokteran Universitas Sumatera Utara
3.12 Alur Penelitian dalam penelitian ini
• Pasien yang sedang menggunakan obat (aspirin, clopidogrel, dll)
• Perokok
BAB 4
HASIL
Penelitian dilakukan secara cross sectional study (potong lintang)
selama periode Mei 2013 sampai dengan Agustus 2013 dengan
melakukan pemeriksaan fungsi trombosit dan parameter lainnya.
Berdasarkan kriteria inklusi dan eksklusi akhirnya didapat 30 orang
penderita sindroma metabolik dan obesitas di Poliklinik Instalasi Penyakit
Dalam Divisi Endokrinologi RSUP Haji Adam Malik Medan. Tetapi hanya
11 dari 15 orang yang memenuhi kriteria sindroma metabolik dikarenakan
memiliki nilai trigliserida yang tinggi, dan 15 orang lagi yang tidak
memenuhi kriteria sindroma metabolik dijadikan kontrol setelah
disesuaikan umur dan jenis kelaminnya. Subjek penelitian dibagi dalam 2
Tabel 4.1 Karakteristik pada Kelompok Sindroma Metabolik dan Keterangan: *menyatakan signifikan hasil penelitian dengan p-value < 0.05
Usia, LP (Lingkar Pinggang), Tekanan Darah Sistole, Tekanan
Darah Diastole, TG (TriGliserida), HDL-C (High Density
Lipoprotein-Cholesterol), KGDP (Kadar Gula Darah Puasa). * Uji kemaknaan dengan
t-independent, bermakna jika p < 0.05.
Rata – rata umur subjek adalah 37,2 ± 4,1 tahun dan kontrol 36,5 ±
2,5 tahun dan tidak ditemukan perbedaan antara subjek dan kontrol (p =
0,503). Rata – rata lingkar pinggang pada kelompok sindroma metabolik
99,2 ± 9,3 dan kelompok obesitas 95,5 ± 7,3 dengan (p = 0.131) tidak
berbeda signifikan secara statistik. Rata – rata IMT pada kelompok
sindroma metabolik (31,3 ± 1,9) dan kelompok obesitas (29,0 ± 3,1)
dengan (p = 0.135) tidak berbeda signifikan secara statistik. Rata– rata
dan kelompok obesitas (112 ± 4,6) dengan (p = 0,507) tidak berbeda
signifikan secara statistik. Rata – rata tekanan diastole pada kelompok
sindroma metabolik (74,5 ± 9,4) dan kelompok obesitas (74 ± 6,3) dengan
(p = 0,869) tidak berbeda signifikan secara statistik. Rata – rata TG pada
kelompok SM (171 ± 16,9) lebih tinggi dibandingkan dengan kelompok
obesitas (97,7 ± 40,6) dengan ( p = 0,000) berbeda signifikan secara
statistik. Sementara rata – rata HDL-C pada kelompok sindroma metabolik
(39,8 ± 5,13) lebih rendah dibandingkan dengan kelompok obesitas (54,1
± 13,4) dengan (p = 0,001) berbeda signifikan secara statistik. Rata – rata
KGD-P pada kelompok sindroma metabolik (94,5 ± 19) dan kelompok
obesitas (84,9 ± 9,3), dengan (p = 0,145) tidak berbeda signifikan secara
statistik. Pada jumlah trombosit ditemukan berbeda secara signifikan
antara kelompok sindroma metabolik (295,0 ± 9,3) dan kelompok obesitas
(270,5 ± 34,7) dengan (p = 0.018).
Tabel 4. 2 Perbandingan Agregasi Trombosit pada Kelompok Sindroma Metabolik dan Obesitas
VARIABEL