STUDI ALKOKSILASI DENGAN GLISEROL TERHADAP HASIL
EPOKSIDASI METIL RISINOLEAT YANG DIPEROLEH DARI
MINYAK JARAK (Ricinus communis Linn)
SKRIPSI
DINA OCHA GINTING
050802005
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
STUDI ALKOKSILASI DENGAN GLISEROL TERHADAP HASIL
EPOKSIDASI METIL RISINOLEAT YANG DIPEROLEH DARI
MINYAK JARAK (Ricinus communis Linn)
SKRIPSI
Diajukan untuk melengkapi tugas akhir dan memenuhi syarat mencapai gelar sarjana sains
DINA OCHA GINTING 050802005
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul :STUDI ALKOKSILASI DENGAN GLISEROL TERHADAP HASIL EPOKSIDASI METIL RISINOLEAT YANG DIPEROLEH DARI MINYAK JARAK (Ricinus communis Linn)
Kategori : SKRIPSI
Nama : DINA OCHA GINTING Nomor Induk Mahasisiwa : 050802005
Program Studi : SARJANA (S1) KIMIA Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di,
Medan, November 2009 Komisi Pembimbing
Pembimbing II Pembimbing I
Drs. Darwis Surbakti,MS Drs. Mimpin Ginting,MS
NIP. 195307071983031001 NIP. 195510131986011001
Diketahui/Disetujui oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
STUDI ALKOKSILASI DENGAN GLISEROL TERHADAP HASIL
EPOKSIDASI METIL RISINOLEAT YANG DIPEROLEH DARI
MINYAK JARAK (Ricinus communis Linn)
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, November 2009
PENGHARGAAN
Segala Puji dan Syukur penulis panjatkan kepada Tuhan Yesus Krisus atas segala kasih karunia dan berkatNya sehingga penulis dapat meyelesaikan penelitian dan penyusunan skripsi ini.
Dalam pelaksanaan penelitian hingga penyelesaian skripsi ini, penulis menyadari banyak mendapat bantuan, motivasi adn dukungan dari berbagai pihak.Untuk itu pada kesempatan ini penulis menyampaikan terimaksih kepada :
1. Drs.Mimpin Ginting,MS sebagai pembimbing 1 dan Drs.Darwis Surbakti,MS sebagai pembimbing 2 yang dengan sabar telah memberikan dorongan , bimbingan dan saran sehingga skripsi ini dapat diselesaikan
2. DR.Rumondang Bulan Nst.M.S dan Drs.Firman Sebayang,MS sebagai ketua dan sekretaris Departemen Kimia FMIPA USU
3. Drs.Adil Ginting MSc, sebagai Kepala Laboratorium Kimia Organik FMIPA USU dan kepada bapak/ibu dosen Organik Bapak Prof.DR.Jamaran Kaban,M.Sc, Ibu Dra.Herlince Sihotang,MS, Ibu Cut Fatimah Zuhra,S.Si,M.Si, Ibu Juliati Tarigan S.Si,M.Si dan Ibu Helmina br Sembiring,S.Si,M.Si atas segala dorongan dan waktu diskusinya
4. Seluruh dosen Departemen Kimia FMIPA USU terkhusus Bapak Drs.Saut Nainggolan selaku dosen wali yang telah memberikan waktunya untuk memberikan bimbingan selama penulis mengikuti kuliah di departemen Kimia.
6. Teman-teman Asisten Laboratoium Kimia Organik(Bg daus, Yemima, Robi, Aspriadi, Maria, Meri, Christy dan Silorida )
7. Pihak-pihak yang tidak disebutkan namun tulus membantu penulis dalam penyelesaian skripsi ini.
Akhirnya saya mengucapkan terimakasih yang setinggi tingginya kepada Mama (M br Sembiring) dan kepada saudara-saudaraku tersayang (Sri Mei Budhiani, Esi Marsella dan Bredi Arianto) serta keluarga yang sangat kukasihi S Ginting dan Sarianta br Sembiring,S.Pd terima kasih atas doa dan dukungannya,
ABSTRAK
The Study of Alcoxylation Epoxidized Methyl Ricinoleic with Addition Glycerol which Derived from Castor Oil (Ricinus communis Linn)
ABSTRACT
DAFTAR ISI
Daftar Gambar xii
Lemak Campuran 17 3.3.5 Pembuatan Poliol dari Metil Risinoleat 17
3.3.6 Prosedur Analisis 18
3.3.6.1 Analisis Bilangan Iodin 18 3.3.6.2 Analisis Bilangan Hidroksi 19 3.3.6.3 Analisis Bilangan Penyabunan 19 3.3.6.4 Analisis Bilangan Asam 20 3.3.6.5 Penentuan Harga HLB (Hydrophilic
Lipophilic Balance) 20
3.4 Bagan Penelitian 21
3.4.1 Ekstraksi Minyak Jarak dari Biji Jarak 21 3.4.2 Pembuatan Metil Ester Asam Lemak Campuran dari
Biji Jarak 22
3.4.3 Pemisahan Metil Risinoleat dari Metil Ester
Asam Lemak Campuran 23
3.4.4 Pembuatan Poliol dari Metil Risinoleat 24 Bab 4 : Hasil dan Pembahasan
4.1 Hasil 29
4.2 Pembahasan 32
Bab 5 : Kesimpulan dan Saran 36
5.1 Kesimpulan 36
5.2 Saran 37
Daftar Pustaka
DAFTAR TABEL
Halaman
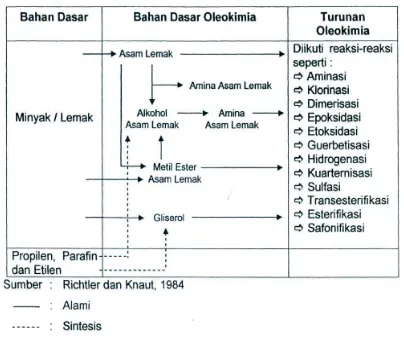
Tabel 2.2 Diagram Alur Oleokimia 7
Tabel 2.3 Komposisi Asam Lemak dari Minyak Jarak 8
Tabel 4.1 Harga Rf Hasil KLT Metil Ester Asam Lemak Campuran 28
DAFTAR GAMBAR
Halaman
Gambar 4.1 Struktur Kimia Metil Risinoleat 29 Gambar 4.2 Spektrum FT-IR Metil Risinoleat 31 Gambar 4.3 Spektrum FT-IR Senyawa 9,10,12-Trihidroksi Metil Stearat 31 Gambar 4.2 Spektrum FT-IR Senyawa metil 9-(1,2,3-trihidroksipropoksi)-
DAFTAR LAMPIRAN
Halaman
Data Penentuan Bilangan Iodin 39
Data Penentuan Bilangan Asam 39
Data Penentuan Bilangan Hidroksi 40
ABSTRAK
The Study of Alcoxylation Epoxidized Methyl Ricinoleic with Addition Glycerol which Derived from Castor Oil (Ricinus communis Linn)
ABSTRACT
BAB 1
PENDAHULUAN
1.1Latar Belakang
Pemanfaatan senyawa polihidroksi (poliol) telah banyak digunakan dalam berbagai keperluan industri, seperti halnya poliol turunan asam lemak dengan sakarida digunakan sebagai surfaktan pada formulasi bahan makann, kosmetik, maupun farmasi seperti bahan obat-obatan (Jung,S.,dkk,1998).
Senyawa poliol tersebut dapat berasal dari alam seperti senyawa karbohidrat, lignin dan juga dapat berasal dari industri petrokimia. Bahan poliol dari industri petrokimia disamping proses pembuatannya kurang ramah lingkungan, bahan bakunya juga tidak dapat diperbaharui (Gound,V.V.,2006).
Dalam proses kimia salah satu cara yang digunakan untuk menghasilkan senyawa poliol adalah memanfaatkan ikatan π pada senyawa hidrokarbon melalui transformasi kimia secara oksidasi seperti halnya dilakukan terhadap berbagai asam lemak tidak jenuh pada minyak nabati melalui reaksi epoksidasi yang diikuti dengan reaksi hidrolisis (Carlon,K.D dan Chang,S.P,1985).
Minyak jarak dapat diperoleh dari biji buah jarak (Ricinus communis Linn) melalui ekstraksi pelarut. Minyak jarak sebagai trigliserida mengandung asam risinoleat mencapai sebesar 87 %. Asam risinoleat yang terdapat dalam biji buah jarak (Ricinus communis Linn) disamping adanya ikatan π pada atom C9,10 juga terdapat
gugus hidroksi pada atom C12 (Akpan,N.G.,dkk,2006).
Adanya ikatan π pada asam risinoleat telah berhasil diepoksidasi dilanjutkan dengan hidrolisis terhadap metil risinoleat untuk menghasilkan metil -9,10,12-trihidroksi stearat (Armina,S 2007 dan Manurung,S.,2008).
bahan pembuatan polimer akan dapat merubah sifat dari bahan yang dihasilkan (Randal,D dan Lee,S,2002).
Dalam penelitian ini ingin dilakukan epoksidasi terhadap ikatan pada metil risinoleat yang diperoleh dari minyak jarak untuk menghasilkan senyawa epoksida yang selanjutnya dilakukan alkoksilasi dengan gliserol untuk mendapatkan senyawa poliol turunan asam risinoleat.
1.2Permasalahan
Berdasarkan latar belakang yang telah diuraikan diatas, maka sebagai permasalahan dalam penelitian ini adalah:
1. Apakah senyawa epoksida hasil epoksidasi dari metil risinoleat yang diperoleh dari minyak jarak (Ricinus communis Linn) dapat dialkoksilasi dengan gliserol secara insitu untuk menghasilkan senyawa poliol turunan risinoleat
1.3 Tujuan penelitian
1. Untuk menghasilkan senyawa poliol melalui alkoksilasi dengan gliserol terhadap hasil epoksidasi metil risinoleat
2. Untuk mengetahui perbedaan antara poliol hasil hidrolisis dan hasil alkoksilasi dengan gliserol terhadap hasil epoksidasi yang diperoleh dari minyak jarak (Ricinus communis Linn)
1.4Manfaat Penelitian
Hasil penelitian ini diharapkan dapat dijadikan sebagai sumber informasi terhadap industri oleokimia bahwa alkoksilasi dengan gliserol terhadap hasil epoksidasi metil risinoleat yang diperoleh dari minyak jarak (Ricinus communis Linn) dapat menghasilkan senyawa poliol yang memiliki perbedaan dengan poliol yang dihasilkan dari hidrolisis langsung terhadap hasil epoksidasi metil risinoleat.
1.5Lokasi Penelitian
BAB 2
TINJAUAN PUSTAKA
2.1 LEMAK DAN MINYAK
Lemak dan minyak adalah trigliserida atau triasilgliserol yang berarti triester dari gliserol (Fessenden,R.J dan Fessenden,J.,1984).
Lemak meliputi mentega, lemak hewan, dan bagian berlemak dari daging. Minyak terutama berasal dari tumbuhan: termasuk jagung, biji kapas, zaitun, kacang, dan minyak kedelai (Hart,H, 1990).
Lemak dan minyak biasanya dibedakan berdasarka titik lelehnya: pada suhu kamar lemak berwujud padat, sedangkan minyak berwujud cair (Wilbraham,A.C,1992).
Meskipun lemak berwujud padat dan minyak berwujud cair, keduanya memiliki struktur organik dasar yang sama (Hart,H, 1990).
Lemak dan minyak pada dasarnya tidak larut dalam air tetapi larut dalam beberapa pelarut organik seperti karbon tetraklorida, petroleum eter dan etil eter (Lawson,W.H.,2001).
Kelarutan minyak atau lemak dalam suatu pelarut ditentukan oleh sifat polaritas asam lemaknya. Asam lemak yang bersifat polar cenderung larut dalam pelarut polar, sedangkan asam lemak non polar larut dalam pelarut nonpolar.
Sifat dan daya kelarutan ini digunakan sebagai dasar pada praktek pengujian-pengujian analitis dan ekstraksi minyak dengan pelarut. Sifat minyak dan lemak yang larut dalam pelarut tertentu dipergunakan dalam pengolahan minyak secara komersial dalam ekstraksi minyak menggunakan metode solvent ekstraksi.
panjang rantai karbon maka minyak dan lemak tersebut semakin sukar larut dalam pelarut polar. Minyak dan lemak yang tidak jenuh lebih mudah larut dalam pelarut organik daripada asam lemak jenuh dengan panjang rantai karbon yang sama. Asam lemak yang derajat ketidakjenuhannya tinggi akan lebih mudah larut daripada asam lemak dengan derajat ketidakjenuhan rendah (Ketaren,S, 2008).
Lemak hampir sebagian besar mengandung ester-ester dan pada dasrnya lemak mempunyai komposisi yang sederhana. Ester-ester lemak adalah non-volatil dan tidak berbau, tetapi mempunyai semua sifat-sifat yang karakteristik dari ester-ester pada umumnya. Lemak terbentuk dari gliserol yang dapat mengadakan penggabungan dengan asam-asam organik yang disebut asam lemak membentuk rangkaian alifatik yang lurus. Hampir selalu asam-asam yang membentuk lemak mempunyai jumlah atom C genap per molekulnya, biasanya jumlah atom karbon antara C8 hingga C24.
Telah dikenal adanya harga-harga khusus yang digunakan untuk menentukan sifat-sifat lemak seperti: derajat ketidakjenuhan, keasaman dari hidrolisis dan rata-rata Berat Molekul. Sifat-sifat ini tergantung pada asal dari lemak. (Sastrohamidjojo,H,2005)
1. Angka asam: mengukur derajat dari hidrolisis atau ketengikan (rancidity) dari lemak, yang diartikan berapa mg KOH yang dibutuhkan untuk menetralisir asam lemak bebas dalam 1 gram lemak 2. Angka sabun (saponifikasi): berapa mg KOH yang dibutuhkan untuk
menyabunkan 1 gram dari lemak
3. Angka iod: mengukur derajat ketidakjenuhan dari lemak yang diartikan berapa gram iod yang ditambahkahkan pada100 gram lemak
2.2 OLEOKIMIA
Oleokimia merupakan bahan kimia yang berasal dari minyak/lemak alami, baik tumbuhan maupun hewan. Pada saat ini industri oleokimia masih berbasis kepada minyak/trigliserida sebagai bahan bakunya. Asam lemak bersama-sama dengan gliserol, merupakan penyusun utama minyak nabati atau lemak dan merupakan bahan baku untuk semua lipida pada makhluk hidup.
Secara alami, asam lemak bisa berbentuk bebas (karena lemak yang terhidrolisis) maupun terikat sebagai gliserida. Asam lemak merupakan salah satu basic oleochemical (Tambun,R,2006).
Oleokimia merupakan turunan gliserol dengan asam lemak yang berubah dalam bentuk turunannnya yang digunakan baik sebagai surfaktan, deterjen, polimer, aditif bahan bakar dan sebagainya. Bahan dasar oleokimia seperti gliserol, asam lemak, alkil ester asam lemak, amina asam lemak dan alkohol asam lemak dapat diperoleh dengan mengubah lipida baik dari yang berasal hewan maupun tumbuhan menmjadi gliserol dan turunan asam lemak.
Tabel 2.2 Diagram Alur Oleokimia
2.3 MINYAK JARAK
Minyak jarak adalah cairan kental berwarna kuning pucat yang diperoleh dari biji tanaman Ricinus communis Linn, dapat juga dikenal sebagai minyak ricinus. Minyak jarak merupakan salah satu gliserida yang terdapat secara alami dalam bentuk senyawa yang murni, dimana perbandingan asam lemaknya hampir 9 per 10 adalah risinoleat.
H3C -( C H2)5-C -C H2- C H = C H - (C H2)7-C -O H H
O H
A s a m R is in o le a t
O
proses yang paling memuaskan adalah dengan pengepresan hidraulik diikuti dengan ekstraksi pelarut.
Minyak jarak dan turunannya digunakan dalam produksi cat, pernis dan pelapis pelindung lainnya, pelumas, cairan hidraulik, sabun, tinta print, linoleum, sebagai bahan mentah dalam berbagai industri kimia dan juga digunakan dalam produksi pemlastis dan nilon (Akpan,U.G.,Jimoh,A.,Mohammad,A.D.,2006)
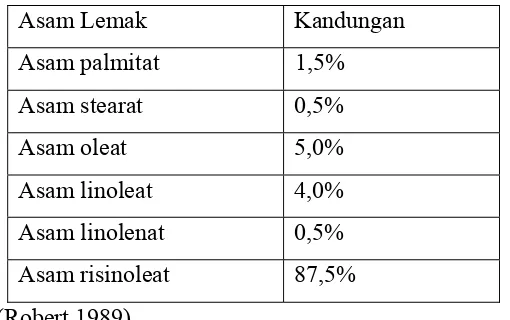
Tabel 2.3 Komposisi Asam Lemak dari Minyak Jarak
Asam Lemak Kandungan
Asam palmitat 1,5%
Asam stearat 0,5%
Asam oleat 5,0%
Asam linoleat 4,0%
Asam linolenat 0,5% Asam risinoleat 87,5% (Robert,1989)
Asam risinoleat merupakan komposisi utama dari trigliserida minyak jarak yaitu asam lemak yang memiliki struktur yang unik dibandingkan dengan asam lemak lainnya, yaitu turunan asam oleat (C18:1) yang pada posisi ω-7 memiliki gugus hidroksil serta
mengandung ikatan π pada posisi ω-9 (Miller,A.J and Newel,F.E, 1988) Adapun struktur asam risinoleat sebagai berikut:
Minyak jarak bersifat toksik, disamping kandungan asam lemak essensialnya sangat tinggi. Hal yang demikian menyebabkan minyak jarak tidak dapat digunakan sebagai minyak makan dan bahan pangan.
Minyak jarak mempunyai rasa asam yang dapat dibedakan dengan trigliserida lainnya karena bobot jenis, kekentalan (viskositas), dan bilangan asetil serta kelarutannya dalam alkohol relatif tinggi (Ketaren,S, 2008).
Pada penggunaannya gugus hidroksil tidak jenuh ini sering diubah menjadi gugus fungsi reaktif lainnya. Untuk memisahkan asam risinoleat dengan asam lemak lainnya yang masih berada dalam bentuk trigliseridanya, maka terlebih dahulu minyak jarak dimetil esterkan secara esterifikasi maupun interesterifikasi.
Minyak yang mengandung asam lemak hidroksil merupakan bahan yang sangat penting. Asam lemak hidroksil ini digunakan dalam pembuatan polimer, seperti nilon 66, pelapis (coating), dan cat (Armina,S 2007 dan Manurung,S.,2008).
2.4 EPOKSIDA
Epoksida (oksirana) ialah eter siklik dengan cincin beranggota tiga yang mengandung satu atom oksigen (Hart,H, 1990).
Senyawa epoksida pada sintesa organik merupakan zat antara yang potensial dimanfaatkan untuk beragam bentuk senyawa dengan berbagai keperluan sehingga penelitian tentang epoksidasi baik kondisi reaksi, keberlanjutan hasil reaksi maupun manfaat hasil reaksi terus dikembangkan (Wisewan,1978).
Dalam proses industri, hasil epoksidasi terhadap asam lemak beserta turunannya telah umum digunakan sebagai plstisizer dan stabilizer dalam pembuatan polimer (Lutz,dkk,1980).
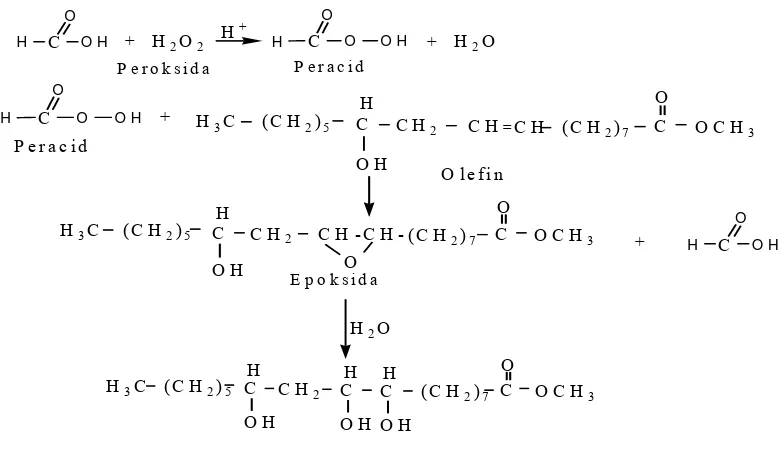
Jenis-jenis bahan pereaksi yang digunakan untuk epoksidasi tanpa pemutusan ikatan π yang umum digunakan untuk menghasilkan epoksida adalah senyawa peroksi (peracid). Dalam epoksidasi ini pereaki dipersiapkan melalui reaksi asam karboksilat dengan peroksida (H202) dengan bantuan katalis asam (Hasibuan,M.H.E.,2000).
O
pada kereaktifan yang tinggi dari cincin oksiran, epoksida juga dapat dipakai untuk berbagai jenis bahan kimia yaitu alkohol, glikol, alkanolamin, senyawa karbonil, senyawa olefin, dan polimer seperti poliuretan yang reaksinya dapat ditunjukkan dibawah ini ( Harry O`kuru,R.E,dkk,2005).
Ada empat teknik yang dapat digunakan untuk menghasilkan epoksida dari molekul olefin:
1. Epoksida dengan asam perkarboksilat yang sering digunakan dalam industri dan dapat dipercepat dengan bantuan katalis atau enzim
2. Epoksida dengan peroksida organik dan anorganik, termasuk epoksidasi alkali dengan hydrogen peroksida nitril dan epoksida yang dikatalisis logam transisi. 3. Epoksida dengan halohidrin, menggunakan asam hipohalogen (HOX) dengan
garamnya sebagai reagen, dan epoksida olefin dengan defisiensi elektron ikatan rangkap.
4. Epoksida dengan menggunakan molekul oksigen, untuk minyak nabati jarang digunakan karena dapat menyebabkan degadrasi dari minyak menjadi senyawa yang lebih kecil seperti aldehid dan keton atau asam dikarboksilat berantai pendek sehingga oksidasi dengan O2 merupakan metode yang tidak efisien
Secara umum, reaksi epoksidasi dan dilanjutkan dengan hidrolisis dtuliskan sebagai berikut.
2.5 ESTER ASAM LEMAK
Ester asam lemak di alam terdapat dalam bentuk ester antara gliserol dengan asam lemak ataupun terkadang ada gugus hidroksilnya yang teresterkan tidak dengan asam lemak tetapi dengan phosphat seperti pada phospolipid. Disamping itu ada juga ester antara asam lemak dengan alkoholnya yang membentuk monoester seperti yang terdapat dalam minyak jojoba. Dalam hal ester asam lemak yang dimaksud adalah ester hasil sintesis ataupun transformasi untuk menghasilkan ester asam lemak dengan monoalkohol maupun polialkohol.
Ester asam lemak yang paling sederhana adalah ester antara metanol dengan asam lemak yang dikenal luas sebagai metil ester asam lemak pada industri oleokimia. Metil Ester Asam Lemak yang merupakan bagian daripada ester asam lemak monoalkohol merupakan zat antara dalam industri oleokimia disamping dapat digunakan sebagai bahan bakar diesel. Metil Ester Asam Lemak ini dapat dibuat dengan cara transesterifikasi lipida dengan metanol menggunakan katalis asam sulfat dalam pelarut benzena (Ozgul,S and Turkay,S.,1993)
Reaksi selengkapnya adalah sebagai berikut:
Interesterifikasi (penukaran ester atau transesterifikasi) menyangkut pertukaran gugus asil antara trigliserida. Karena trigliserida mengandung tiga gugus ester per molekul, maka peluang untuk pertukaran tersebut cukup banyak. Gugus asil dapat bertukar posisinya dalam satu molekul trigliserida, atau diantara molekul trigliserida.
Dengan proses hidrolisa lemak akan terurai menjadi asam lemak dan gliserol. Proses ini dapat berjalan dengan menggunakan asam, basa, dan enzim tertentu.
Dalam proses hidrolisa, lemak atau minyak akan diubah menjadi asam-asam lemak bebas dan gliserol. Reaksi hidrolisa dapat mengakibatkan kerusakan minyak atau lemak terjadi karena terdapatnya sejumlah air dalam minyak atau lemak tersebut. Reaksi ini akan mengakibatkan ketengikan hidrolisa yang menghasilkan flavor dan bau tengik pada minyak tersebut. (Ketaren,S,2008).
2.6 SENYAWA POLIOL
Epoksidasi asam lemak tidak jenuh baik sebagai trigliserida, asam lemak bebas maupun dalam bentuk alkil ester asam lemak yang dilanjutkan hidrolisis juga telah banyak dilakukan untuk menghasilkan senyawa poliol (Swern,dkk,1959).
Reaksi epoksida tersebut melalui metanolisis disamping terbentuk gugus poliol juga terbentuk gugus eter yaitu gugus metoksi sehingga senyawa yang terbentuk lebih dikenal dengan poliol polieter (Lin,2008).
Poliol dari minyak nabati telah banyak dikembangkan untuk dapat menggantikan petroleum berbasis poliol dalam pembuatan poliuretan dan poliester, juga telah banyak digunakan sebagai bahan pemlastis dan matrik polimer untuk menghasilkan suatu material, demikian juga sebagai pelunak maupun pemantap yang bertujuan agar diperoleh kekerasan dan kalunakan tertentu sehingga material tersebut mudah dibentuk ke berbegai jenis barang sesuai kebutuhan (Andreas, 1990).
Dalam industri polimer digunakan sebagai bahan pengemulsi seperti halnya untuk material dalam pembuatan PVC (Meffert,A,1984).
Dengan adanya sifat hidrofil dan lipofil menyebabkan senyawa poliol banyak digunakan sebagai surfaktan dalam makanan, kosmetik maupun keperluan farmasi seperti obat-obatan (Jung,S.,dkk,1998).
Beberapa minyak nabati diupayakan dalam pembuatan poliol dengan memanfaatkan asam lemak tidak jenuh terutama oleat (C18:1), linoleat (C18:2) maupun
linolenat (C18:3) (Trans.,dkk,2005).
Adapun reaksi-reaksi poliol sebagai berikut:
Poliuretan mempunyai sifat yang sama dengan nilon, tetapi karena sukar diwarnai dan titik lelehnya lebih rendah, polimer ini pada awalnya tidak diperdagangkan. Akan tetapi, kemudian terjadi kemajuan pesat pada kimia poliuretan yang menghasilkan busa, elastomer, pelapis permukaan, serat, dan perekat poliuretan.
Poliuretan dapat dibentuk dengan mereaksikan poliol dengan diisosianat. Poliuretan digunakan dalam pembuatan elastomer. Sifat mekanisnya baik, yakni tahan kikisan dan tahan sobek. Akan tetapi, harganya tinggi sehingga penggunaannya terbatas. Dalam bidang pelapisan permukaan, keberhasilan cat dan pernis poliuretan bertahan di pasaran karena ketahanannya terhadap cuaca dan kikisan.
Poliester sering dipakai dengan serat kaca untuk membuat badan mobil atau perahu dan poliester ini memiliki titik ketidakjenuhan atau ikatan rangkap sepanjang rantai. (Coed,M.A, 1991). 1. Reaksi poliol menjadi poliester
OCN R NCO + HO R' OH OCN R NH CO O R' OH
(CO NH R NH CO O R' O )n
2. Reaksi poliol menjadi poliuretan
reaksi dengan monomer-monomer berikutnya Diol
Dikarboksilat Poliester
Diisosianat Diol
BAB 3
METODE PENELITIAN
3.1 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah: - Alat Vakum Fisons - Kertas Saring Biasa
- Neraca Analitis Mettler PM 480 - Alat Shaker KL 2 Edmund Buhler - Gelas Erlenmeyer 250 ml Pyrex
- Gelas Ukur 100 ml Pyrex - Gelas Beaker 250 ml Pyrex - Erlenmeyer Vakum Pyrex - Spektrofotometer FT-IR Shimadzu - Tabung CaCl2 Pyrex
- Corong Pisah Pyrex - Corong Penetes Pyrex - Botol Akuades
- Magnetik Bar - Mortar dan Stamfer
- Labu leher tiga Pyrex - Termometer 150oC Fisons - Kondensor Bola Pyrex - Buret (100 ml ± 0,1 ml) Pyrex - Rotarievaporator Heidolph - Hotplate Sirrer Fisons - Kolom Kromatografi
3.2 Bahan-Bahan
- Biji Jarak
- 2-Propanol Fisons
- Natrium Sulfat Anhidrous p.a.(E.Merck) - Metanol p.a.(E.Merck) - Benzena p.a.(E.Merck) - Asam Sulfat 98% p.a.(E.Merck)
- n-Heksana p.a.(E.Merck)
- Akuades p.a.(E.Merck)
- Silika Gel G 60F p.a.(E.Merck)
- Alkohol 96% p.a.(E.Merck)
- Asam Formiat 90% Fisons
- Hidrogen Peroksida 30% p.a.(E.Merck) - Natrium Hidroksida (pellet) p.a.(E.Merck) - Kalium Hidroksida (pellet) p.a.(E.Merck) - Dietil Eter p.a.(E.Merck) - Aseton Fisons
- Gliserol p.a.(E.Merck)
- Sikloheksana p.a.(E.Merck)
- Larutan Wijs p.a.(E.Merck)
- Kalium Iodida p.a.(E.Merck)
- Natrium Tiosulfat (s) p.a.(E.Merck)
- Amilum p.a.(E.Merck)
- Asam Asetat Anhidrida
- Pyridin Fisons
3.3 Prosedur Penelitian
3.3.1 Pembuatan Reagen dan Standarisasi
3.3.1.1 Pembuatan Larutan HCl 0,5 N
Diukur sebanyak 10,45 ml larutan HCl 37% lalu diencerkan dengan akuades dalam labu takar 250 ml sampai garis batas dan distandarisasi dengan menggunakan larutan KOH 0,1 N dan indikator BTB.
3.3.1.2 Pembuatan Larutan KOH-Alkohol 0,5 N
Ditimbang KOH sebanyak 7,0125 gram dan dilarutkan dengan alkohol dalam labu takar 250 ml sampai garis batas dan distandarisasi dengan menggunakan larutan H2C2O4 0,1 N dan indikator Fenolptalein.
3.3.1.3 Pembuatan Larutan KOH 0,1 N
Ditimbang KOH sebanyak 1,4 gram dan dilarutkan dengan akuades dalam labu takar 250 ml sampai garis batas dan distandarisasi dengan menggunakan larutan H2C2O4 0,1 N dan indikator Fenolptalein.
3.3.1.4 Pembuatan Larutan KOH 0,02 N
Diukur sebanyak 50 ml larutan KOH 0,1 N dan diencerkan dalam labu takar 250 ml dengan menggunakan akuades dan distandarisasi dengan menggunakan larutan H2C2O4 0,1 N dan indikator Fenolptalein.
3.3.1.5 Pembuatan Larutan H2C2O4 0,1 N
Ditimbang 1,575 gram H2C2O4.2H2O dimasukkan kedalam labu takar 250 ml
dan diencerkan dengan akuades sampai garis tanda.
3.3.1.6 Pembuatan Larutan Indikator Phenolptalein
Ditimbang 1 gram Fenolptalein dan dilarutkan dengan alkohol dalam labu takar 100 ml.
3.3.1.7 Pembuatan Alkohol Netral
3.3.1.8 Pembuatan Larutan KI 10%
Ditimbang 10 gram kristal KI, dilarutkan dengan akuades dalam labu takar 100 ml sampai garis tanda.
3.3.1.9 Pembuatan Larutan Na2S2O3 0,1 N
Ditimbang 6,25 gram kristal Na2S2O3.5H2O dilarutkan dengan akuades dan
diencerkan dalam labu takar 250 ml sampai garis tanda lalu distandarisasi dengan larutan K2Cr2O7 0,1 N menggunakan indikator amilum mengikuti titrasi secara
iodometri
3.3.1.10 Pembuatan Larutan Indikator Amilum
Ditimbang 1 gram serbuk amilum dan dilarutkan dengan 100 ml akuades dan dipanaskan sambil diaduk di atas pemanas hingga mendidih dan disaring dalam keadaan panas.
3.3.1.11 Pembuatan Reagen Asetilasi
Sebanyak 25 ml asam asetat anhidrida dimasukkan kedalam labu takar 100 ml dan diencerkan dengan piridin sampai garis batas.
3.3.1.12 Pembuatan Larutan KOH 0,5 N
Ditimbang KOH sebanyak 7 gram dan dilarutkan dengan akuades dalam labu takar 250 ml sampai garis batas dan distandarisasi dengan menggunakan larutan larutan H2C2O4 0,5 N dan indikator Fenolptalein.
3.3.1.13 Pembuatan Larutan Indikator BTB
Ditimbang BTB sebanyak 1 gram dan ditambahkan 10 ml NaOH 0,1 N kemudian dimasukkan kedalam labu takar 100 ml dan diencerkan dengan akuades sampai garis batas.
3.3.2 Ekstraksi minyak jarak dari biji jarak (Ricinus communis Linn)
Biji jarak dipisahkan dari cangkang lalu dikeringkan dan dihaluskan. Biji jarak halus sebanyak 500 gram dimaserasi dengan 2-propanol selama ± 2 hari. Ekstrak disaring dan filtrat ditambahkan Na2SO4 anhidrous kemudian disaring. Filtrat hasil
3.3.3 Pembuatan Metil Ester Asam Lemak Campuran dari Minyak Jarak
Ke dalam labu alas bulat leher tiga dimasukkan sebanyak 100 mL minyak jarak, 50 mL metanol dan 100 ml benzen sambil diaduk dan didinginkan dan melalui corong penetes diteteskan sebanyak 2 mL H2SO4(p) secara perlahan-lahan, kemudian
dirangkai alat refluks dan dilengkapi dengan tabung CaCl2 dan direfluks selama 5
jam. Kelebihan metanol dan pelarut diuapkan dengan rotarievaporator. Residu yang diperoleh dilarutkan dalam 50 ml dietileter, kemudian dicuci dengan akuades sebanyak 2 kali masing-masing sebanyak 10 ml. Lapisan eter dikeringkan dengan CaCl2 anhidrous dan disaring selanjutnya dikeringkan dengan Na2SO4 anhidrous dan
disaring. Filtrat yang diperoleh dirotarievaporasi. Selanjutnya hasil yang diperoleh diidentifikasi melalui analisis spektroskopi FT-IR dan diikuti analisis penentuan bilangan iodin, bilangan hidroksi dan penentuan harga HLB.
3.3.4 Pemisahan Metil Risinoleat dari Metil Ester Asam Lemak Campuran
Metil risinoleat dipisahkan dari metil ester asam lemak campuran melalui cara kromatografi kolom dengan menggunakan adsorben silika gel G 60F dan eluennya n-heksana : etanol = 9 : 1 (v/v). Setelah dipisahkan dari eluen yang digunakan, metil risinoleat yang diperoleh diidentifikasi melalui analisis spektroskopi FT-IR dan diikuti analisis penentuan bilangan iodin, bilangan hidroksi dan penentuan harga HLB.
3.3.5 Pembuatan Poliol dari Metil Risinoleat
Ke dalam labu alas bulat leher tiga dimasukkan 20 ml asam formiat 90%, kemudian ditambahkan 10 ml H2O2 30%. Lalu campuran diaduk dengan
menggunakan magnetik stirer. Kemudian melalui corong penetes, secara perlahan-lahan ditambahkan 20 gram metil risinoleat dan dipertahankan suhunya pada 40-45oC sambil diaduk selama 2 jam lalu dibagi menjadi 2 bagian, yaitu:
1. Bagian I (Hidrolisis Terhadap Senyawa Epoksida)
Campuran didiamkan selama 1 malam lalu dirotarievaporasi. Residu yang diperoleh dilarutkan dalam 50 ml dietileter, kemudian dicuci dengan 10 ml NaOH 0,2 N dilanjutkan dengan akuades sebanyak 2 kali masing-masing sebanyak 10 ml. Lapisan eter dikeringkan dengan CaCl2 anhidrous dan
disaring selanjutnya filtrat yang diperoleh dikeringkan dengan Na2SO4
diikuti analisis penentuan bilangan iodin, bilangan hidroksi dan penentuan harga HLB.
2. Bagian II (Alkoksilasi dengan Gliserol Terhadap Senyawa Epoksida) Hasil epoksidasi dipisahkan dari fase air, kemudian dimasukkan ke dalam labu leher dua value 500 ml yang telah dihubungkan dengan pengaduk magnet serta kondensor yang ujungnya terhubung dengan tabung CaCl2. Selanjutnya ditambahkan 70 ml aseton dan 0,5 ml H2SO4(p) dan sambil diaduk melalui
corong penetes ditambahkan sebanyak 12 gram gliserol. Campuran kemudian direfluks selama 6 jam. Hasil reaksi kemudian diuapkan melalui rotarievaporator, selanjutnya residu dilarutkan dalam 50 ml dietil eter. Larutan dicuci dengan 10 ml NaOH 0,2 N dilanjutkan dengan akuades sebanyak dua kali masing-masing 10 ml. Lapisan eter dikeringkan dengan CaCl2 anhidrous
dan disaring dan filtrat dikeringkan kembali dengan Na2SO4 anhidrous dan
disaring. Filtrat yang diperoleh dirotarievaporasi. Selanjutnya hasil yang diperoleh diidentifikasi melalui analisis spektroskopi FT-IR dan diikuti analisis penentuan bilangan iodin, bilangan hidroksi serta penentuan nilai HLB.
3.3.6 Prosedur Analisis
3.3.6.1 Analisis Bilangan Iodin
Analisis ini dilakukan terhadap metil risinoleat, senyawa 9,10,12-trihidroksi metil stearat dan senyawa metil 9-(2,3-dihidroksipropoksi)-10,12-dihidroksioktadekanoat.
Ditimbang sampel sebanyak ± 0,5 gram ke dalam gelas Erlenmeyer 250 ml yang bertutup lalu ditambahkan 20 ml sikloheksana kemudian dikocok/diguncang untuk memastikan sampel telah benar-benar larut. Ditambahkan 25 ml larutan Wijs kedalamnya kemudian ditutup dan dikocok agar campuran telah benar-benar bercampur dan disimpan bahan tersebut dalam ruang gelap selama ± 30 menit. Diambil bahan tersebut dari tempat penyimpanan dan ditambahkan 25 ml larutan KI 10% dan 150 ml air suling. Dititrasi dengan larutan Na2S2O3 0,1 N sampai warna
kuning hampir hilang (kuning pucat). Ditambahkan 1-2 ml indikator amilum ke dalamnya dan dititrasi kembali sampai warna biru hilang.
Bilangan iodin =
Dimana: B = Volume Titrasi Blanko(ml) S = Volume Titrasi Sampel(ml) N = Normalitas Na2S2O3
3.3.6.2 Analisis Bilangan Hidroksi
Analisis ini dilakukan terhadap metil risinoleat, senyawa 9,10,12-trihidroksi metil stearat dan senyawa metil 9-(2,3-dihidroksipropoksi)-10,12-dihidroksioktadekanoat.
Ditimbang sampel sebanyak ± 1 gram dan dimasukkan ke dalam labu dan ditambahkan 5 ml reagen asetilasi (asam asetat anhidrida dalam pyridin) dan direfluks pada suhu 95-100oC selama 1 jam. Setelah dingin ditambah 1 ml akuades, dan dipanaskan selama 10 menit. Setelah dingin ditambah 5 ml alkohol netral dan dipindahkan larutan kedalam gelas Erlenmeyer kemudian ditambahkan 2-3 tetes indikator Fenolptalein selanjutnya dititrasi dengan larutan KOH-alkohol 0,5 N. Dilakukan titrasi terhadap larutan blanko pada kondisi yang sama.
Ditentukan bilangan asam terhadap sampel dan dihitung bilangan hidroksi dengan rumus:
3.3.6.3 Analisis Bilangan Penyabunan
Analisis ini dilakukan terhadap metil risinoleat, senyawa 9,10,12-trihidroksi metil stearat dan senyawa metil 9-(2,3-dihidroksipropoksi)-10,12-dihidroksioktadekanoat
Ditimbang ± 0,1 gram sampel dan dimasukkan ke dalam gelas Erlenmeyer. Kemudian ditambahkan 25 ml larutan KOH-alkohol 0,5 N dan dipanaskan hingga mendidih. Didinginkan dan ditambah 3 tetes indikator Fenolptalein kemudian dititrasi dengan larutan HCl 0,5 N hingga warna merah muda hilang.
Bil.penyabunan=
3.3.6.4 Analisis Bilangan Asam
Analisis ini dilakukan terhadap metil risinoleat, senyawa 9,10,12-trihidroksi metil stearat dan senyawa metil 9-(2,3-dihidroksipropoksi)-10,12-dihidroksioktadekanoat.
Sebanyak ± 0,1 gram sampel dimasukkan kedalam gelas Erlenmeyer. Kemudian ditambah 10 ml larutan alkohol netral. Erlenmeyer tersebut ditututup dengan plastik dan dipanaskan sampai mendidih. Larutan tersebut didinginkan dan ditambahkan 3 tetes indikator Fenolptalein dan dititrasi dengan larutan KOH 0,02 N sampai terbentuk warna merah muda.
Dihitung volume KOH yang dipakai dan dihitung bilangan asam dengan menggunakan rumus:
3.3.6.5 Penentuan Harga HLB (Hidrofilic Lipofilic Balance)
Analisis ini dilakukan terhadap metil risinoleat, senyawa 9,10,12-trihidroksi metil stearat dan senyawa metil 9-(2,3-dihidroksipropoksi)-10,12-dihidroksioktadekanoat Harga HLB dapat diperoleh dari bilangan asam dan bilangan penyabunan dari senyawa ester dengan menggunakan rumus:
Biji Jarak
Dikeringkan Dihaluskan
Biji Jarak Halus (milt)
Dimaserasi dengan 2-propanol selama 2 hari
Disaring
Residu Filtrat
Dikeringkan dengan Na2SO4 anhidrous Disaring
Residu Filtrat
Dirotarievaporasi
Minyak jarak
3.4 Bagan Penelitian
3..4.2. Pembuatan Metil Ester Asam Lemak Campuran dari Minyak Jarak
100 ml minyak jarak
Dimasukkan kedalam labu alas Ditambah 50 ml metanol Ditambah 100 ml benzena
Diaduk dan diteteskan 2 ml H2SO4(P)
Campuran
Direfluks pada suhu 800C selama 5 jam Dirotarievaporasi
Residu Pelarut
Dilarutkan dalam 50 ml dietil eter
Dicuci dengan 10 ml akuades sebanyak 2 kali
Lapisan Bawah Lapisan atas
Dikeringkan denganCaCl2anhidrous Disaring
Residu Filtrat
Dirotarievaporasi
Metil Ester Asam Lemak Campuran (Residu)
Dikeringkan dengan Na2SO4 anhidrous Disaring
3.4.3. Pemisahan Metil Risinoleat dari Metil Ester Asam Lemak Campuran
Metil Ester Asam Lemak Campuran
kromatografi Lapis Tipis (developer) n-heksana : etanol = 9 : 1 (v/v) dan adsorben silika gel G 60
kromatografi kolom (eluen n-heksana : etanol = 9 : 1 (v/v) dan adsorben silika gel G 60F
Metil Risinoleat
Analisa FT-IR Penentuan Bilangan Iodin
Penentuan Bilangan Hidroksi
3.4.4. Pembuatan Poliol dari Metil Risinoleat
20 ml HCOOH 90%
dimasukkan kedalam labu leher tiga 10 ml H2O2 30% setetes demi setetes 2 ml H2SO4(p)
diaduk pada suhu 40-45oC selama 2 jam dan ditambah 20 gram metil risinoleat melalui corong penetes
Campuran
diaduk pada suhu 40-45oC selama 2 jam dan dibagi 2 bagian
Bagian I
didiamkan selama 1 malam
dirotarievaporasi
Residu Filtrat
50 ml dietil eter
dicuci dengan 10 ml NaOH 0,2 N dicuci dengan akuades
sebanyak 2 kali masing-masing 10 ml
Lapisan atas(eter) Lapisan bawah(air)
diaduk pada suhu 50-60oC sambil di tambahkan gliserol sebanyak 12 gram se tetes demi setetes
dicuci dengan 10 ml NaOH 0,2 N dicuci dengan akuades
sebanyak 2 kali masing-masing 10 ml
Lapisan atas(eter) Lapisan bawah(air)
BAB 4
HASIL DAN PEMBAHASAN
4.1 HASIL
Minyak jarak diperoleh dengan cara ekstraksi maserasi menggunakan pelarut 2-propanol. Dari 500 gram biji jarak halus diperoleh minyak jarak sebanyak 279 gram (55,8%). Pembentukan metil ester asam lemak campuran secara interesterifikasi dengan metanol menggunakan katalis asam H2SO4 dengan pelarut benzena diperoleh
rendemen sebesar 78,88%.
Sebelum dipisahkan metil risinoleat dari metil ester asam lemak, maka metil ester asam lemak campuran dianalisis melalui kromatografi lapis tipis (KLT) dengan menggunakan adsorben silika gel, dan ditentukan harga Rf setiap noda.
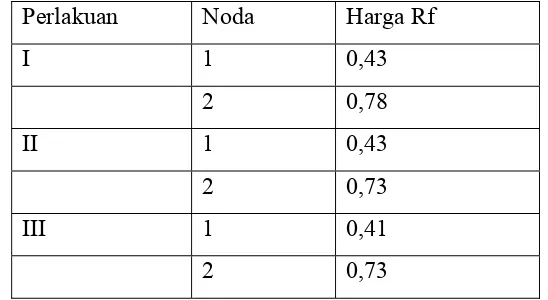
Hasil analisis KLT dari metil ester asam lemak campuran dengan pengembang n-heksan : etanol = 9 : 1 (v/v) menggunakan penampak noda uap iodin adalah sebagai berikut:
Tabel 4.1. Harga Rf Hasil KLT Metil Ester Asam Lemak Campuran
Perlakuan Noda Harga Rf
I 1 0,43
2 0,78
II 1 0,43
2 0,73
III 1 0,41
2 0,73
H3C-(CH2)5-C-CH2-CH=CH-(CH2)7-C-OCH3 H
OH
Metil Risinoleat
O
Pada proses pemisahan melalui kromatografi kolom setiap fraksi sebanyak 10 ml dilakukan pengujian melalui analisis KLT menggunakan penampak noda uap iodin dimana diperoleh hasil yaitu dari sebanyak 39,6 gram metil ester asam lemak campuran yang dipisahkan secara kromatografi kolom diperoleh metil risinoleat total sebanyak 29,1 gram yang berarti rendemen metil risinoleat dari minyak jarak adalah 73,48 %.
Untuk mengetahui bahwa pemisahan telah sempurna, dilakukan analisis KLT dan melalui penentuan harga Rf-nya.
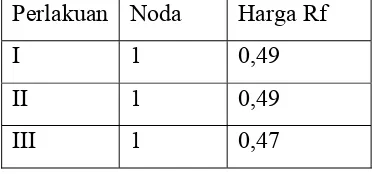
Hasil analisis KLT dari metil risinoleat dengan eluen n-heksana : etanol = 9 : 1 (v/v) dan adsorben silika gel G 60 memberikan noda tunggal dengan harga Rf sebagai berikut:
Tabel 4.2 Harga Rf Kasil Kromatografi Lapis Tipis (KLT) Metil Risinoleat Perlakuan Noda Harga Rf
I 1 0,49
II 1 0,49 III 1 0,47
Adapun struktur metil risinoleat adalah:
Metil risinoleat yang diperoleh diidentifikasi melalui analisis spektroskopi FT-IR dan diperoleh spektrum seperti pada gambar 4.2
Dari analisis senyawa dengan menggunakan spektrofotometer FT-IR diperoleh spektrum dengan puncak-puncak serapan pada daerah bilangan gelombang 3398,3 cm-1: 3050 cm-1: 1654,8 cm-1: 1720,4 cm-1: 1176,5 cm-1: 2854,5 cm-1 dan 1438,8 cm-1.
senyawa metil risinoleat dari minyak jarak adalah 82,87 dan analisis bilangan hidroksi sebesar 194,84 serta nilai HLB diperoleh sebesar 10,66.
Hasil epoksida dari senyawa metil risinoleat diperoleh dengan cara mereaksikannya dengan campuran HCOOH 90% dan H202 30% dan diikuti dengan
proses hidrolisis sehingga dihasilkan senyawa 9,10,12-trihidroksi metil stearat.
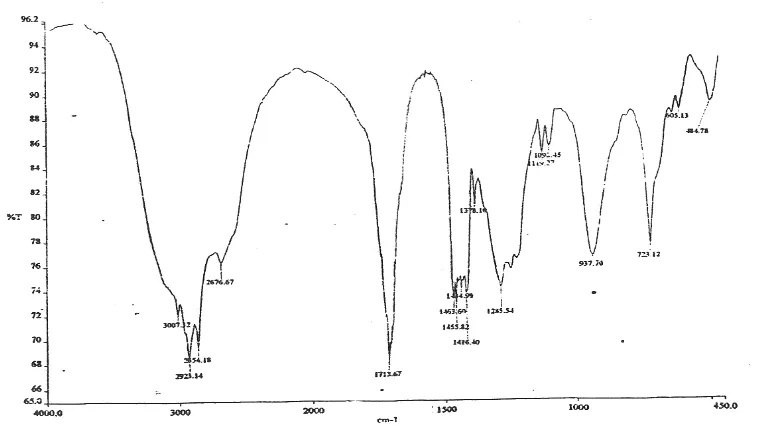
Asam formiat dan Hidrogen peroksida direaksikan membentuk senyawa peracid pada suhu 40-45oC yang selanjutnya diikuti penambahan metil ester asam risinoleat dari minyak jarak dan karena adanya air menyebabkan reaksi hidrolisis pada cincin epoksida. Dari hasil analisis senyawa 9,10,12-trihidroksi metil stearat menggunakan spektrofotometer FT-IR diperoleh puncak-puncak serapan pada daerah bilangan gelombang 3007,32 cm-1; 1713,67 cm-1; 2923,14-2854,18 cm-1; 1463,60-1416 cm-1 dan 1285,54 cm-1 dan diperoleh spektrum seperti pada gambar 4.3
Nilai bilangan iodin untuk senyawa 9,10,12-trihidroksi metil stearat adalah sebesar 10,76 dan analisis bilangan hidroksi sebesar 294,816 serta nilai HLB diperoleh sebesar 14,08.
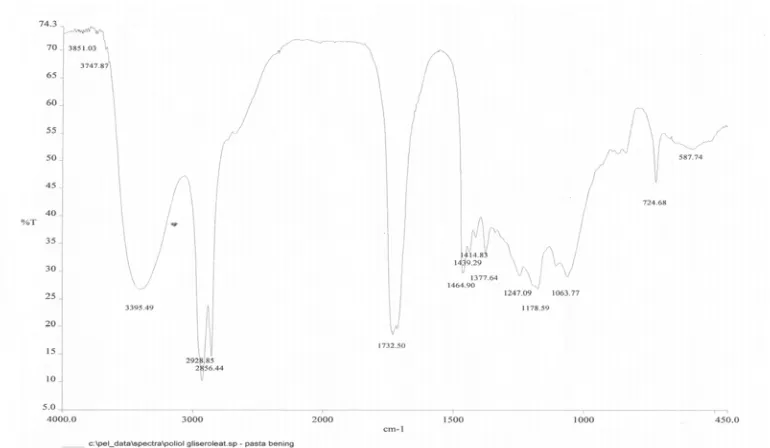
Alkoksilasi dengan gliserol terhadap hasil epoksidasi dari metil risinoleat diperoleh sebagai metil 9-(2,3-dihidroksipropoksi)-10,12-dihidroksioktadekanoat. Dari hasil analisis senyawa dengan menggunakan spektrofotometer FT-IR diperoleh spektrum dengan puncak-puncak serapan pada daerah bilangan gelombang 3395,49 cm-1; 2928,85-2856,44 cm-1; 1732,50 cm-1 :1464,9-1414,83 cm-1 dan 1247,09 cm-1 dan diperoleh spektrum seperti pada gambar 4.4.
Gambar 4.2 Spektrum FT-IR dari Metil Risinoleat
4.2
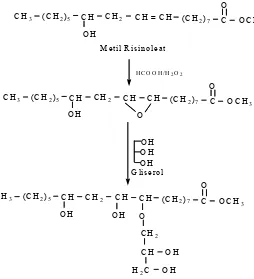
PEMBAHASANMinyak jarak yang diperoleh dengan cara maserasi dengan menggunakan pelarut 2-propanol. Minyak jarak dimetanolisis secara refluks menggunakan katalis H2S04(P) dan pelarut benzena pada suhu 80oC membentuk metil ester asam lemak
campuran dari minyak jarak dengan reaksi sebagai berikut;
O
Metil Risinoleat merupakan komponen urtama dalam minyak jarak dipisahkan menggunakan kromatografi kolom yang terlebih dahulu metil ester asam lemak campuran dianalisis melalui Kromatografi Lapis Tipis (KLT).
Adanya gugus OH pada atom C12 menyebabkan metil risinoleat lebih polar
daripada metil ester asam lemak lainnya pada metil ester asam lemak campuran, sehingga pada anlisis KLT menggunakan adsorben silika gel dan eluen n-heksana : etanol = 9 : 1 9v/v) menghasilkan nilai Rf yang lebih kecil sedangkan noda yang memiliki harga Rf yang lebih besar merupakan metil ester asam lemak yang lainnya yang berupa campuran.
Pemisahan metil risinoleat dari metil ester asam lemak campuran melalui kromatografi kolom menggunakan adsorben silika gel G 60 F dan eluen n-heksana : etanol = 9 : 1 (v/v). Metil risinoleat akan tertahan dalam adsorben silika gel sedangkan metil ester asam lemak lainnya akan lebih cepat turun bersama pengelusi sehingga memberikan harga Rf yang lebih besar. Metil risinoleat yang tertahan dalam adsorben dielusi dengan etanol tunggal.
Adapun struktur metil risinoleat adalah sebagai berikut:
Metil risinoleat yang diperoleh dianalisis dengan spektrofotometer FT-IR menghasilkan spektrum seperti pada gambar 4.2 memberikan puncak serapan pada daerah bilangan gelombang 3398,3 cm-1 yang merupakan serapan khas untuk gugus hidroksil (-OH), pada bilangan gelombang lebih kurang 3050 cm-1 merupakan puncak serapan untuk C-H sp2 dari gugus –CH=CH- dan didukung dengan serapan pada bilangan gelombang 1654,8 cm-1 yang merupakan serapan khas dari ikatan C=C. Pada bilangan gelombang 1720,4 cm-1 merupakan serapan khas dari gugus karbonil (C=O) dari ester dan didukung dengan puncak vibrasi C-O-C pada daerah bilangan gelombang 1176,5 cm-1, sehingga dapat disimpulkan adanya gugus ester. Pada daerah bilangan gelombang 2854,5 cm-1 menunjukkan adanya vibrasi stretching dari C-H sp3 yang didukung vibrasi bending C-H sp3 pada bilangan gelombang 1438,8 cm-1.
Metil Risinoleat yang diperoleh dari minyak jarak selanjutnya diepoksidasi dengan campuran HCOOH 90% dan H2O2 30%. Hasil epoksidasi ini kemudian dibagi
menjadi 2 bagian.yaitu:
a) Bagian I (Alkoksilasi dengan Gliserol terhadap Senyawa Epoksida)
C H3
Gambar 4.5 Reaksi Alkoksilasi dengan Gliserol terhadap Hasil Epoksidasi Metil Risinoleat
Pemasukan gugus alkoksi pada atom C9 dan bukan pada atom C10, hal ini disebabkan
halangan sterik pada C10 (interaksi 1,3 (a,a) pada C10 dan C12) karena bentuk struktur
ruang dari metil risinoleat adalah sebagai berikut:
Adanya gugus OH pada atom C12 terjadi halangan ruang sehingga lebih
dominan terjadi alkoksilasi pada C9.
Senyawa metil 9-(2,3-dihidroksipropoksi)-10,12-dihidroksioktadekanoat yang diperoleh dianalisis dengan spektrofotometer FT-IR menghasilkan spektrum seperti pada gambar 4.3 memberikan puncak serapan pada daerah bilangan gelombang
C O H
3395,49 cm-1 yang merupakan serapan khas gugus hidroksi (-OH). Pada daerah ini puncak serapan semakin melebar yang menunjukkan gugus hidroksi semakin banyak. Pada bilangan gelombang 2928,85,-2856,44 cm-1 menunjukkan serapan khas khas dari vibrasi CH sp3 dan pada daerah bilangan gelombang 1464,90-1414,83 cm-1 menunjukkan serapan khas dari vibrasi bending CH sp3. Pada bilangan gelombang 1247,09 cm-1 menunjukkan serapan khas dari gugus C-O-C dan pada bilangan gelombang 1732,5 cm-1 menunjukkan serapan khas karbonil (C=O) menunjukkan adanya gugus ester.
b) Bagian II (Hidrolisis terhadap Hasil Epoksidasi Metil Risinoleat) Reaksinya dapat digambarkan sebagai berikut:
Gambar 4.6 Hidrólisis terhadap Hasil Epoksidasi Metil Risinoleat
Puncak serapan dari gugus OH pada spectrum tersebut secara teoritis muncul pada daerah bilangan gelombang 3500 cm-1 tetapi kemungkinan karena gugus OH tersebut dapat membentuk interaksi ikatan Hidrogen puncak tersebut tidak jelas, hanya saja pada spectrum tersebut membentuk lekukan yang membesar dan bukan tajam.
Analisis bilangan iodin dari metil risinoleat diperoleh sebesar 82,87 ; senyawa 9,10,12-trihidroksi metil stearat sebesar 10,76 dan metil 9-(2,3-dihidroksipropoksi)-10,12-dihidroksioktadekanoat sebesar 10,93.
Penurunan bilangan iodin menunjukkan adanya penurunan jumlah ikatan rangkap dan ada terjadi reaksi oksidasi terhadap ikatan rangkap pada senyawa metil risinoleat.
Analisis bilangan hidroksi senyawa metil ester asam risinoleat dari minyak jarak diperoleh sebesar 194,84, senyawa 9,10,12-trihidroksi metil stearat sebesar 294,816 dan senyawa 9-(2,3-dihidroksipropoksi)-10,12-dihidroksioktadekanoat sebesar 484,59. Kenaikan bilangan hidroksi menunjukkan adanya kenaikan gugus – OH sehingga dapat dikatakan ada terjadi reaksi epoksiodasi yang diikuti dengan reaksi hidrolisis dan reaksi alkoksilasi dengan gliserol pada senyawa metil risinoleat.
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Senyawa metil 9-(2,3-dihidroksipropoksi)-10,12-dihidroksioktadekanoat dapat diperoleh dari minyak jarak (Ricinus communis Linn) melalui reaksi metanolisis, epoksidasi yang diikuti dengan reaksi alkoksilasi dengan gliserol 2. Senyawa metil 9-(2,3-dihidroksipropoksi)-10,12-dihidroksioktadekanoat
memiliki jumlah gugus hidroksi yang lebih banyak dibandingkan dengan senyawa 9,10,12-trihidroksi metil stearat yang didukung dengan nilai bilangan hidroksi yang lebih besar.
3. Senyawa metil 9-(2,3-dihidroksipropoksi)10,12-dihidroksioktadekanoat memiliki bilangan iodin sebesar 10,93 dan analisa bilangan hidroksi sebesar 484,59 serta penentuan harga HLB (Hydrophylic Lipophylic Balance) sebesar 15,22
5.2 Saran
DAFTAR PUSTAKA
Akpan,U.G.,Jimoh,A and Mohammad,A.D.,2006.Extraction Characterization and Modification of Castor Seed Oil.Nigeria:Leonardo Journal of Sciences.
Andreas,H.,In Gachter,R and Muller,H.,1990.PVC Stabilizer and Plastics Additives Handbook.Germany:Hanser Publishers,Munich.
Armina,S.,2007.Pembuatan dan Karakterisasi Sabun Natrium 9,10,12-trihidroksi Stearat Campuran yang Diturunkan dari Minyak Jarak (Ricinus communis Linn).Medan:Skripsi Departemen Kimia FMIPA USU.
Brasil,M.C,Gerbase,A.E de Luca,M.A and Gregio,J.R.,2007.Organic-Inorganic Hybrid Films Based on Hydroxylated Soybean Oil.USA: J.am.Oil.Chem.Soc.Vol 84(1),284-295.
Carlon,K.D and Chang,S.P.1985.Chemical Epoxidation of Natural Unsaturated Epoxy Seed Oil From Vernonia Galameasis and a Look Epoxy Oil Market.JAOCS,Vol.62(5),147-151.
Coed, M.A.1991.Kimia Polimer.Bandung:Penerbit ITB.
Dal,H.,Yang,L.,Wang,C and Shi,G.,2007.Synthesis and Characterization of The Different Soy-Based Polyols by Ring Opening of Epoxidized Soybean Oil with Methanol 1,2-Ethanediol and 1,2-Propanediol. USA: J.am.Oil.Chem.Soc.Vol 86(3),261-267.
Fessenden,R.J. dan Fessenden, J.1984. Kimia Organik.Edisi Ketiga.Jilid 2.Jakarta:Erlangga.
Harry O`kuru,R.E.,Gordon,S.H and Biawas,A,2005.A Facile Synthesis of Aminihydroxy Triglycerides From New Crop Oils. USA:J.am.Oil.Chem.Soc.Vol 82.207.
Hart,H.1990. Kimia Organik. Edisi Keenam. Jakarta: Erlangga.
Hasibuan,M.H.E.2000.Modifikasi dan Penggunaan Pemlastis Turunan Asam Oleat dari Asam Lemak Sawit Destilat (ALSD) pada Matriks Polivinil Klorida.Tesis
Program Pasca Sarjana Kimia.Medan:USU.
Jung,S.,Goulan,M.,Girardin and Ghoul,M.1998. Structure and Surface Active Properties Determination of Fructose Monoleats.J of Surfactans and Detergents,Vol.I(1),53-57
Ketaren,S.2008.Pengantar Teknologi Lemak dan Minyak Pangan.Jakarta:UI-Press.
Lawson,W.H.2001.Standarts For Oil and Fat.Connecticut:AVI Publishing Company.
Lin,B.,Yang,L.,Dal,H dan Yi,A.2008.Kinetic Studies on Oxirane Cleavage Of Epoxidized Soybean Oil by Methanol and Characterization of Polyols. J.Am.Oil.Chem.Soc.85:113-117.
Lutz,J.T.,Jr.1980.Epoxidation in Encyclopedia of Chemical Technology.Vol.9.Edited by M.Grayson,John Wiley & Sons,New York,pp.251-266.
Manurung,S. 2008. Sintesis Senyawa N-etanol-9,10,12-Trihidroksi Stearamida Melalui Amidasi Metil Trihidroksi Stearat dengan Etanolamin. Medan:Tesis Sekolah Pascasarjana.USU.
Meffert,a.1984.Technical Uses of Fatty Acid Esthers.J.Am.Oil.Chem.Soc.61(2) 255.
Ozgul,S and Turkay,S.1993.In Situ Estherification of Fatty Acid with Methanol and Ethanol.USA: J.Am.Oil.Chem.Soc.Vol 70.145.
Randal,D.,dan Lee,S.,2002,The Polyurethanes Book, John Wiley & Son, LTD, Everberg.
Ricthler,m.j and Knaut,J.1984.Challenges to Nature Industry, Marketing and Economics of Oleochemicals in Western Europe.USA: J.Am.Oil.Chem.Soc.Vol 61.160.
Sastrohamidjojo,H.2005.Kimia Organik.Gadjah Mada University Press.Yogyakarta.
Swern,D.,Scanian,J.T and Dickel,G.B.1959.Organic Synthesis Coll.Vol.39,p.15.
Tambun, R.2006. Teknologi Oleokimia. Medan: USU-Press.
Trans,P.,Daniel,G and Ramani,N,2005.Ozon Mediated Polyol Synthesis from Soybean Oil. J.Am.Oil.Chem.Soc.82(9),653-659.
Wilbraham,A.C.1992. Pengantar Kimia Organik dan Hayati. Bandung: ITB-Press.
Lampiran
DATA PENENTUAN BILANGAN IODIN
Sampel Massa Sampel (gram) Volume Titrasi (ml) Bilangan
Iodin
m1 m2 m3 m V1 V2 V3 V
Blanko - - - - 39,90 39,70 39,80 39,80 -
Metil Risinoleat 0,3499 0,2618 0,2674 0,2930 17,58 22,30 22,15 20,67 82,87 Senyawa
9,10,12-0,3180 0,2410 0,3260 0,2950 33,74 38,89 39,15 37,26 10,93
DATA PENENTUAN BILANGAN ASAM
Sampel Massa Sampel (gram) Volume Titrasi (ml) Bilangan
DATA PENENTUAN BILANGAN HIDROKSI
Sampel Massa Sampel (gram) Volume Titrasi (ml) Bilangan
Hidroksi
m1 m2 m3 m V1 V2 V3 V
Blanko - - - - 65 64 64,5 64,50 -
Metil Risinoleat 1,003 1,001 1,002 1,001 62,3 62,2 62,3 62,30 194,8 Senyawa 9,10,12-trihidroksi
metil stearat
2,001 2,002 2,002 2,002 51,8 51,8 51,7 51,80 294,816
Metil 9-(2,3- dihidroksipropoksi)-10,12-dihidroksioktadekanoat
1,002 1,001 1,001 1,001 51,9 51,8 51,9 51,97 397,55
DATA PENENTUAN BILANGAN PENYABUNAN
Sampel Massa Sampel (gram) Volume Titrasi (ml) Bilangan
Penyabunan
m1 m2 m V1 V2 V3 V
Blanko - - - 19,0 19,1 19,0 19,0 -
Metil Risinoleat 0,103 0,105 0,106 0,105 17,9 18,8 18,6 18,77 62,18 Senyawa
9,10,12-trihidroksi metil stearat
0,106 0,107 0,109 0,107 18,9 18,8 18,9 18,87 34,49
Metil 9-(2,3- dihidroksipropoksi)-
10,12-dihidroksioktadekanoat
Perhitungan Harga HLB Menggunakan Metode Titrasi
HLB Senyawa Metil Risinoleat HLB 20(1-S/A)
= 20(1-62,18/133,07) = 10,66
HLB Senyawa 9,10,12-trihidroksi metil stearat HLB = 20(1-S/A)
= 20(1-34,49/116,52) = 14,08
HLB Senyawa Metil 9-(2,3-dihidroksipropoksi)-10,12-dihidroksioktadekanoat HLB = 20(1-S/A)