TONGKOL JAGUNG (Zea Mays) TERHADAP PENURUNAN KADAR BESI (Fe), TOTAL PADATAN TERSUSPENSI (TSS), TOTAL PADATAN TERLARUT (TDS),
KEKERUHAN DAN pH PADA AIR RAWA
SKRIPSI
RENITA SIMBOLON 060802003
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PENGARUH PENAMBAHAN ARANG TONGKOL JAGUNG DAN SERBUK TONGKOL JAGUNG (Zea Mays) TERHADAP PENURUNAN KADAR BESI (Fe), TOTAL PADATAN TERSUSPENSI (TSS), TOTAL PADATAN TERLARUT (TDS),
KEKERUHAN DAN pH PADA AIR RAWA
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
RENITA SIMBOLON 060802003
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
ii
PERSETUJUAN
Judul : PENGARUH PENAMBAHAN ARANG
TONGKOL JAGUNG DAN SERBUK TONGKOL JAGUNG (Zea Mays) TERHADAP PENURUNAN KADAR BESI (Fe), TOTAL PADATAN TERSUSPENSI (TSS), TOTAL PADATAN TERLARYT ( TDS), KEKERUHAN, DAN pH PADA AIR RAWA
Kategori : SKRIPSI
Nama : RENITA SIMBOLON
Nnomor Iduk Mahasiswa : 060802003 Program studi : SARJANA (S1)
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, Desember 2011
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Drs. Ahmad Darwin Bangun, M.Sc Drs.Saut Nainggolan NIP. 195211161980031001 NIP. 194701251974031001
Disetujui oleh
Departemen Kimia FMIPA USU Ketua,
iii
PERNYATAAN
PENGARUH PENAMBAHAN ARANG TONGKOL JAGUNG DAN SERBUK TONGKOL JAGUNG (Zea Mays) TERHADAP PENURUNAN KADAR BESI ( Fe), TOTAL PADATAN TERSUSPENSI (TSS), TOTAL PADATAN TERLARUT (TDS), KEKERUHAN, DAN pH PADA AIR RAWA
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ri ngkasan yang masing-masing disebutkan sumbernya.
Medan, Desember 2011
PENGHARGAAN
Segala Pujidan Syukur penulis panjatkan kepada Allah Bapa Yang Maha Kasih, berkat kasih dan AnugrahNya penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini.
v
ABSTRAK
THE ADDITION EFFECT CHARCOAL AND CORN COBS POWDER (Zea Mays) TO THE DECREASE OF CONTENT IRON (Fe), TOTAL SUSPENDED SOLID (TSS),
TOTAL DISOLVED SOLID (TDS), TURBIDITY AND pH ON SWAMP WATER
ABSTRACT
vii
Daftar Lampiran x
Daftar Gambar xi
Daftar Tabel xii
Bab 1 Pendahuluan
1.1Latar Belakang 1
1.2Permasalahan 2
1.3Pembatasan masalah 3
1.4Tujuan Penelitian 3
1.5Manfaat Penelitian 3
1.6Lokasi Penelitian 3
1.7Metodologi Penelitian 3
Bab 2 Tinjauan Pustaka
2.1 Air Permukaan 5
2.2 Air Tanah 6
2.3 Polusi Air 7
2.3.1 Sifat-sifat Air 8
2.3.1.1 Nilai pH 8
2.3.1.2 Kekeruhan dan Warna 10
2.3.1.3 Besi (Fe) 11
2.3.1.4 Zat Padat dalam Air 12
2.4 Arang 13
2.5 Pembuatan Arang 14
2.5.1 Metode Tradisional 15
2.5.2 Metode Diperbaharui 15
2.6 Adsorpsi 16
2.6.1 Adsorpsi Gas oleh Zat Padat 16
2.6.2 Adsorpsi Zat Terlarut olehZat Padat 16
Bab 3 Bahan dan Metode Penelitian
3.1 Alat 18
3.2 Bahan 18
3.3 Prosedur Penelitian 19
3.3.1 Penyediaan Sampel Air Rawa 19
3.3.2 Pembuatan Pereaksi danLarutan Standar
Untuk Penentuan Ion Fe Total ( metodeSpektrofotometri) 19
3.3.3 Pengukuran pH Sampel 21
3.3.4 Penentuan Ion Fe Total dengan Metode Spektrofotometri 21 3.3.5 Penentuan Kekeruhan dengan Metode Turbidimetri 21 3.3.6 Penentuan Padatan Terlarut dan
Padatan Tersuspensi dalam Air 21
3.3.7 Penentuan Panjang Gelombang Maksimum 22
3.3.8 Penentuan Waktu Operasi 22
3.3.9 Pembuatan Kurva Standar Fe(NH4)2(SO4)2.6H2O 22 Dengan Metode Spektrofotometri
3.4 Bagan Penelitian
3.4.1 Preparasi Sampel Air Rawa 23
3.4.2 Preparsi Pembuatan Arang 23
3.4.3 Preparasi Pembuatan Serbuk tongkol jagung 24 3.4.4 Penambahan Arang kedalam Sampel Air Rawa 24
3.4.5 Penentuan pH Sampel Air Rawa 25
3.4.6 Penetuan Turbiditas Sampel Air 25
3.4.7 Penentuan Ion Fe Total dalam Sampel Air Rawa 26 3.4.8 Penetuan Padatan Terlarut (TDS) dan
Padatan Tersuspensi (TSS) dalam Sampel Air Rawa 26
Bab 4 Hasil dan Pembahasan
4.1 Hasil dan Pengolahan Data 28
4.1.1 Hasil Penelitian 28
4.1.2 Data Persen Penurunan Kadar 28
4.2 Perhitungan 28
4.2.1 Penurunan Persamaan Garis Regresi Ion Fe Total
dengan Metode Kurva Kalibrasi 28
4.2.2 Penentuan Kadar Ion Fe Total dalam Sampel 30 4.2.2.1 Penentuan Kadar Ion Fe total dalam Sampel Air Rawa Sebelum Penambahan SerbukTongkol Jagung
Dan Arang TongkolJagung 30
4.2.2.2 Penentuan Kadar Ion Fe total dalam Sampel Air Rawa Setelah Penambahan Serbuk Tongkol Jagung
Dan Arang TongkolJagung 31
4.2.2.3 Persen Penurunan Kadar Ion Fe Total 31 4.2.3 Penentuan Turbiditas (Kekeruhan) dalam Sampel 32
ix Sebelum Penambahan Serbuk TongkolJagung
Dan ArangTongkolJagung 32
4.2.3.2 Penentuan Turbiditas (Kekeruhan) secara Turbidimetri pada Sampel Air Rawa
Setelah Penambahan Serbuk TongkolJagung
dan ArangTongkolJagung 32
4.2.3.3 Persen PenurunanTurbiditas (Kekeruhan)
Dalam Sampel Air Rawa 32
4.2.4 Penentuan Total PadatanTerlarut (TDS)
dan Total PadatanTersuspensi (TSS dalam sampel 33 4.2.4.1 Penentuan Total Padatan Tersuspensi (TSS)
Dalam sampel air rawa sebelum Penambahan
Serbuk Tongkol Jagung danArang Tongkol Jagung 34 4.2.4.2 Penentuan Total Padatan Tersuspensi (TSS)
Dalam sampel air rawa Setelah
Penambahan Serbuk Tongkol Jagung 34 4.2.4.3 Penentuan Total Padatan Tersuspensi (TSS)
dalam Sampel Air Rawa Setelah 34 Penambahan Arang Tongkol Jagung
4.2.4.4 Persen Penurunan Total Padatan Tersuspensi
dalam Larutan (TSS) 35
4.2.4.5 Penentuan Total Padatan Terlarut (TDS) dalam Sampel Air Rawa Sebelum Penambahan
Serbuk Tongkol Jagungdan Arang Tongkol Jagung 35 4.2.4.6 Penentuan Total Padatan Terlarut (TDS) dalam
sampel air rawasetelah penambahan Serbuk Tongkol
Jagung 36
4.2.4.7 Penentuan Total Padatan Terlarut (TDS) dalam sampel air rawa setelah penambahan
Arang Tongkol Jagung 36
4.2.4.8 Persen Penurunan Total Padatan Terlarut (TDS) 36 4.2.5 Penentuan pH pada sampel air rawa Sebelum
PenambahanSerbukTongkol Jagung
dan Arang Tongkol Jagung 37
4.2.5.1 Penentuan pH pada sampel air rawa
Setelah Penambahan Serbuk Tongkol Jagung 37 4.2.5.2 Penentuan pH pada Sampel Air Rawa
Setelah PenambahanArang TongkolJagung 37
4.3. Pembahasan 38
Bab 5 Kesimpulan dan Saran
5.1. Kesimpulan 40
5.2 Saran 40
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Penentuan Panjang Gelombang Maksimum dari
Larutan StandarFe(NH4)2( SO4)2 6H2O0,8 mg/L 42 Lampiran 2. Gambar grafik penentuan panjang gelombang maksimum untuk
larutan seri standar Fe(NH4)2(SO4)2.6H2O 0,8 mg/L 42 Lampiran 3. Penentuan Waktu Operasi dari Larutan
Standar Besi (Fe) 0,8 mg/L 43 Lampiran 4. Gambar grafik penentuan waktu operasi larutan seri standar
Fe(NH4)2(SO4)2.6H2O 0,8 mg/L 43 Lampiran 5. Pembuatan Kurva Kalibrasi Standar Besi (Fe) 44 Lampiran 6. Gambar grafik kurva kalibrasi larutan
Standar Fe(NH4)2(SO4)2.6H2 44 Lampiran 7. Data Hasil Pengukuran Kadar Besi (Fe) sebelum dan Setelah
PenambahanArang Tongkol Jagung dan Serbuk Tongkol Jagung 45 Lampiran 8. Data Hasil Pengukuran Turbiditas (Kekeruhan) sebelum dan
Setelah Penambahan Arang Tongkol Jagun dan Serbuk Tongkol Jagung 45 Lampiran 9. Data Hasil Pengukuran Nilai pH sebelum dan Setelah
Penambahan Arang Tongkol Jagung dan Serbuk Tongkol Jagung 46 Lampiran 10.Data Hasil Pengukuran Berat Kertas Saring sebelum dan
Setelah Penambahan Arang Tongkol Jagung dan Serbuk Tongkol Jagung 46 Lampiran 11.Data Hasil Pengukuran Berat Gelas Beaker sebelum dan Setelah
Penambahan Arang Tongkol Jagung dan Serbuk Tongkol Jagung 47 Lampiran 12. Data hasil pengukuran nilai parameter sifat fisik dan sifat kimia
dalam sampel air rawa serta penurunannya 47 Lampiran 13. Daftar persyaratan kualitas air bersih menurut Peraturan
x DAFTAR GAMBAR
Halaman
Gambar 1. Alat Turbidimeter 50
Gambar 2. Alat Spektrofotometer spektonik 20 50
DAFTAR TABEL
Halaman
Tabel 2.1 Komposisi kimia tongkol jagung 17
Tabel 4.1 Data Hasil Penurunan Persamaan Regresi untuk Logam Besi (Fe) 29 Tabel4.2.Data hasil pengukuran nilai parameter sifat fisik dan sifat kimia dan
v
ABSTRAK
THE ADDITION EFFECT CHARCOAL AND CORN COBS POWDER (Zea Mays) TO THE DECREASE OF CONTENT IRON (Fe), TOTAL SUSPENDED SOLID (TSS),
TOTAL DISOLVED SOLID (TDS), TURBIDITY AND pH ON SWAMP WATER
ABSTRACT
BAB 1
PENDAHULUAN
1.1.Latar Belakang
Air merupakan sumber daya alam yang diperlukan oleh banyak orang, bahkan oleh semua
mahluk hidup. Oleh karena itu, sumber daya air harus dilindungi agar tetap dapat dimanfaatkan
dengan baik oleh manusia serta mahluk hidup yang lain. Saat ini masalah utama yang dihadapi
oleh sumber daya air meliputi kuantitas air yang sudah tidak mampu memenuhi kebutuhan yang
terus meningkat dan kualitas air untuk keperluan domestik yang semakin menurun.
Kualitas air meliputi sifat air dan kandungan mahluk hidup, zat, energi, atau komponen
lain dalam air. Kualitas air dinyatakan dengan beberapa parameter, yaitu parameter fisika
meliputi suhu, kekeruhan, padatan terlarut sedangkan parameter kimia meliputi pH, oksigen
terlarut, BOD, kadar logam dan sebagainya. Pengolahan sumber daya air sangat penting, agar
dapat dimanfaatkan secara berkelanjutan dengan tingkat mutu yang diinginkan. Salah satu jenis
air permukaan adalah air rawa, dimana pengertian air rawa adalah lahan genangan
ilmiah yang terjadi terus-menerus atau musiman akibat
mempunyai ciri-ciri khusus secara
dijumpai memiliki warna coklat kemerahan, seperti yang banyak terdapat di daerah Tapanuli
Utara yang diduga mengandung kadar besi (Fe) yang tinggi yang tidak baik bagi kesehatan.
Banyak cara dan metode yang digunakan pada pengolahan air agar dapat digunakan
sebagai air bersih dalam rumah tangga, dimana dengan cara menambahkan adsorben yang
berfungsi untuk menurunkan beberapa kadar parameter air. Bebarapa adsorben yang biasa
Dari beberapa jenis adsorben diatas penulis tertarik untuk menggunakan adsorben dari
tongkol jagung dimana dilihat dari produksinya, jagung merupakan tanaman terpenting kedua
setelah padi, dengan besarnya produksi jagung di Indonesia khususnya di daerah Tapanuli Utara
tepatnya Kecamatan Garoga yang sebagian besar penduduk bertani jagung, maka akan semakin
besar pula limbah tongkol jagung yang dihasilkan oleh tanaman palawija ini. Masalah dari
limbah tongkol ini dapat diatasi dengan menjadikan tongkol jagung menjadi produk yang
bernilai dan bermanfaat bagi masyarakat.
Telah banyak penelitian sebelumnya yang menggunakan beberapa adsorben untuk
menurunkan kadar zat pencemar yaitu MS Saeni pada tahun 1989 dengan judul pengaruh kontak
langsung air dengan pasir, tanah liat, dan arang terhadap sifat- sifat fisik dan kimia air dan Sari
Sulistyawati dengan judul modifikasi tongkol jagung sebagai adsorben logam berat Pb (II).
Dari uraian diatas peneliti tertarik untuk mengetahui bagaimana daya serap arang tongkol
jagung dan serbuk tongkol jagung terhadap penurunan beberapa parameter air sebelum dan
sesudah ditambahkan dengan arang tongkol jagung dan serbuk tongkol jagung pada sampel air
rawa yang terdapat di daerah Garoga dimana air rawa tersebut digunakan masyarakat sebagai air
kebutuhan sehari-hari, dimana sifat fisika yang diuji adalah kekeruhan, total padatan tersuspensi
(TSS), dan total padatan terlarut (TDS) sedangkan sifat kimia yang diuji adalah pH dan besi (Fe).
1.2.Permasalahan
Bagaimana pengaruh penambahan masing-masing arang tongkol jagung dan serbuk tongkol
3
1.3.Pembatasan Masalah
Penelitian ini dibatasi pada penentuan pH, besi (Fe), kekeruhan (turbiditas) dan Total Padatan
Tersuspensi (TSS), Total Padatan Terlarut (TDS) sebelum penambahan dan sesudah
penambahan masing-masing arang tongkol jagung dan serbuk tongkol jagung selama 24 jam,
dan tidak melihat jenis dari tongkol jagung yang digunakan.
1.4.Tujuan Penelitian
Penelitian ini bertujuan untuk menentukan persen penurunan kadar dari pH, besi (Fe), kekeruhan
(turbiditas) dan Total Padatan Tersuspensi (TSS), Total Padatan Terlarut (TDS) pada air rawa
dengan penambahan masing-masing arang tongkol jagung dan serbuk tongkol jagung.
1.5.Manfaat Penelitian
Hasil penelitian ini dapat digunakan sebagai sumber informasi yang berguna tentang pengolahan
air rawa sebagai air bersih yang digunakan masyarakat.
1.6.Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Analitik Fakultas Matematika dan Ilmu
Pengetahuan Alam Universitas Sumatera Utara.
Pengambilan sampel air rawa dan tongkol jagung diambil dari desa Garoga Tapanuli Utara.
1.7.Metodologi Penelitian
1. Pengambilan sampel air rawa dilakukan secara acak
2. Pengambilan tongkol jagung dilakukan pada jagung yang sudah tua dan kering
3. Penelitian ini merupakan eksperimen laboratorium
5. Penentuan kadar besi (Fe) dilakukan dengan metode spektrofotometri
6. Penentuan kekeruhan (turbiditas) dilakukan dengan metode turbidimetri
7. Penentuan Total Padatan Tersuspensi (TSS), Total Padatan Terlarut (TDS) dilakukan
dengan metode gravimetri.
8. Waktu perendaman arang tongkol jagung di dalam air rawa adalah 1 kali 24 jam.
BAB 2
TINJAUAN PUSTAKA
2.1. Air permukaan ( surface Water)
Air tawar berasal dari dua sumber, yaitu air permukaan (surface water) dan air tanah (ground
water). Air permukaan adalah air yang berada di sungai, danau, waduk, rawa dan badan air lain,
yang tidak mengalami infiltrasi ke bawah tanah. Areal tanah yang mengalirkan air ke suatu
badan air disebut watersheads atau drainage basins. Air yang mengalir dari daratan menuju suatu
badan air disebut limpasan permukaan (surface run off) dan air yang mengalir di sungai menuju
laut disebut aliran air sungai (river run off). Sekitar 60 % air yang masuk ke sungai berasal dari
hujan, pencairan es/salju (terutama untuk wilayah ugahari), dan sisanya berasal dari air
tanah.Wilayah di sekitar daerah aliran sungai yang menjadi tangkapan air disebut catchment
basin.
Air hujan yang jatuh ke bumi dan menjadi air permukaan memiliki kadar bahan-bahan
terlarut atau unsur hara yang sangat sedikit. Air hujan biasanya bersifat asam, dengan nilai pH
sekitar 4,2. Hal ini disebabkan air hujan melarutkan gas-gas yang terdapat di atmosfer, misalnya
gas karbondioksida (CO2), sulfur (S), dan nitrogen oksida (NO2) yang dapat membentuk asam lemah. Setelah jatuh ke permukaan bumi, air hujan mengalami kontak dengan tanah dan
melarutkan bahan-bahan yang terkandung di dalam tanah.
Perairan permukaan diklasifikasikan menjadi dua kelompok utama, yaitu badan air
tergenang (standing waters atau lentik) dan badan air mengalir (flowing waters atau lotik).
Perairan tergenang meliputi danau, kolam, waduk, rawa dan sebagainya. Perairan tergenang
intensitas cahaya dan perbedaan suhu pada kolam air yang terjadi secara vertikal. Sedangkan
perairan mengalir (lotik) contohnya adalah sungai. Sungai dicirikan oleh arus yang searah dan
relatif kencang, dengan kecepatan berkisar antara 0,1 – 1,0 m/detik serta sangat dipengaruhi oleh
waktu, iklim, dan pola drainase. Pada perairan sungai, biasanya terjadi pencampuran massa air
secara menyeluruh dan tidak terbentuk stratifikasi vertikal kolom air seperti pada perairan lentik.
Kecepatan arus, erosi, dan sedimentasi merupakan fenomena yang biasa terjadi di sungai
sehingga kehidupan flora dan fauna sangat dipengaruhi oleh ketiga variabel tersebut.
Klasifikasi perairan lentik sangat dipengaruhi oleh intensitas cahaya dan perbedaan suhu
air, sedangkan klasifikasi perairan lotik justru dipengaruhi oleh kecepatan arus atau pergerakan
air, jenis sedimen dasar, erosi, dan sedimentasi.(Hefni. E 2003)
2.2. Air Tanah (Groundwater)
Air tanah (groundwater) merupakan air yang berada di bawah permukaan tanah. Air
tanah ditemukan pada aliran air di bawah permukaan tanah. Pergerakan air tanah sangat lambat,
kecepatan arus berkisar antara 10-10-10-3 m/det dan dipengaruhi oleh porositas, permeabilitas dari lapisan tanah, dan pengisian kembali air. Karakteristik utama yang membedakan air tanah dari
air permukaan adalah pergerakan yang sangat lambat dan waktu tinggal yang sangat lama, dapat
mencapai puluhan bahkan ratusan tahun. Karena pergerakan yang sangat lambat dan waktu yang
tinggal lama tersebut, air tanah akan sulit untuk pulih kembali jika mengalami pencemaran.
Daerah di bawah tanah yang terisi air disebut daerah saturasi. Pada daerah saturasi, setiap
pori tanah dan batuan berisi oleh air, yang merupakan air tanah (groundwater). Batas atas daerah
saturasi yang banyak mengandung air dan daerah belum saturasi/jenuh yang masih mampu
menyerap air. Jadi, daerah saturasi berada di bawah daerah unsaturated.
Pada dasarnya air tanah dapat berasal dari air hujan, baik melalui proses infiltrasi secara
7
Air yang terdapat di rawa-rawa sering kali dikategorikan sebagai peralihan antara air permukaan
dan air tanah.
Pergerakan air tanah pada hakikatnya terdiri atas pergerakan horizontal air tanah,
infiltrasi air hujan, sungai, danau dan rawa ke lapisan akifer, dan menghilangnya atau keluarnya
air tanah melalui spring (sumur), pancaran air tanah, serta aliran air tanah memasuki sungai dan
tempat-tempat lain yang merupakan tempat keluarnya air tanah. Daerah yang merupakan tempat
masuknya air tanah disebut recharge area, sedangkan daerah tempat keluarnya air tanah atau
tempat penyadapan/pengambilan air tanah disebut discharge area. Sungai, danau, rawa, waduk,
dan genangan air lainya dapat berperan sebagai recharge maupun discharge area.
Air tanah yang berasal dari lapisan deposit pasir memiliki kandungan karbondioksida
tinggi dengan kandungan bahan terlarut (total dissolved solid/TDS) rendah. Air tanah yang
berasal dari lapisan deposit kapur juga memiliki kadar karbondioksida yang rendah(karena
karbondioksida bereaksi dengan kapur), namun memiliki nilai TDS yang tinggi.
Air tanah biasanya memiliki kandungan besi relatif tinggi. Jika air tanah mengalami
kontak dengan udara dan mengalami oksigenasi, ion ferri pada ferri hidroksida yang banyak
terdapat dalam air tanah akan teroksidasi menjadi ion ferro, dan segera mengalami pengendapan
serta membentuk warna kemerahan pada air. (Hefni E,2003)
2.3. Polusi Air
Polusi air adalah penyimpangan sifat-sifat air dari keadaan normal, bukan dari
kemurniannya. Air permukaan dan air sumur biasanya mengandung bahan-bahan terlarut seperti
Na, Mg, Ca, dan Fe. Air yang mengandung komponen-komponen tersebut dalam jumlah tinggi
disebut air sadah. Ciri-ciri air yang mengalami polusi sangat bervariasi tergantung dari jenis air
dan komponen yang mengakibatkan polusi. Sebagai contoh air minum yang terpolusi mungkin
8
Persyaratan fisis untuk air ditentukan oleh faktor-faktor kekeruhan (turbidity), warna, bau
maupun rasa. Dari keempat indikator tersebut, hanya bau saja penilaiannya ditentukan secara
subyektif, dengan jalan air diencerkan secara berturut-turut sampai pengenceran berapakah ia
masih tetap ber bau pada larutan yang paling encer. Jumlah pengenceran itu akan merupakan
angka bau (odor number) dari air yang diperiksa. Umumnya penilaian bau maupun rasa sering
dilakukan bersamaan sebagai suatu indikator, di mana antara keduanya sulit dipisahkan secara
kualitatif.
Sedangkan persyaratan kimia untuk air dilihat dari bahan-bahan kimia yang terlarut
khususnya timbal balik perlu dinilai kadarnya untuk mengetahui sejauh mana bahan-bahan
terlarut itu mulai dapat dikatakan membahayakan eksistensi organisme maupun mengganggu bila
digunakan untuk suatu keperluan. ( Slamet R, 1984)
Untuk mengetahui apakah suatu air terpolusi atau tidak, diperlukan pengujian untuk
menentukan sifat-sifat air sehingga dapat diketahui apakah terjadi penyimpangan dari
batasan-batasan polusi air.
2.3.1 Sifat-Sifat Air
Sifat-sifat air yang umum diuji yaitu :
2.3.1.1 Nilai pH
Pada prinsipnya pengukuran suatu pH adalah didasarkan pada potensial elektro kimia
yang terjadi antara larutan yang terdapat didalam elektroda gelas (membrane gelas) yang telah
diketahui dengan larutan yang terdapat diluar elektroda gelas yang tidak diketahui. Hal ini
9
ukurannya relatif kecil dan aktif, elektroda gelas tersebut akan mengukur potensial elektrokimia
dari ion hidrogen atau diistilahkan dengan potential of hidrogen.
pH menunjukkan kadar asam atau basa dalam suatu larutan, melalui konsentrasi ion
hidrogen H+. Ion hidrogen merupakan faktor utama untuk mengerti reaksi kimiawi dalam ilmu teknik penyehatan karena :
- H+ selalu ada dalam keseimbangan dinamis dengan air/H2O, yang membentuk suasana untuk semua reaksi kimiawi yang berkaitan dengan masalah pencemaran air dimana
sumber ion hidrogen tidak pernah habis.
- H+ tidak hanya merupakan unsur molekul H2O saja tetapi juga merupakan unsur banyak senyawa lain, hingga jumlah reaksi tanpa H+ dapat dikatakan hanya sedikit saja. (G.Alaerts, 1984)
Nilai pH air yang normal adalah sekitar netral, yaitu antara 6 sampai 8, sedangkan pH
yang terpolusi berbeda-beda tergantung dari jenis buangannya. Perubahan keasaman pada air
buangan, baik ke arah alkali maupun ke arah asam, akan sangat mengganggu kehidupan.
(Srikandi F,1992)
pH juga mempengaruhi toksisitas suatu senyawa kimia. Senyawa amonium yang dapat
terionisasi banyak ditemukan pada perairan yang memiliki pH rendah. Amonium bersifat tidak
toksik. Namun, pada suasana alkalis (pH tinggi) lebih banyak ditemukan amonia yang tak
terionisasi dan bersifat toksik.
Dalam penentuan pH larutan secara potensiometri menggunakan emf sel galvani yang
cenderung mengukur keaktifan ion hidrogen, kesetimbangan konsentrasi ion hidrogen. Maka
pengertian penetapan pH diambil sebagai : pH = - log H+. Akan tetapi penggunaan pengertian pH akan mendapatkan kesulitan secara eksperimental, karena tak mungkin untuk mengukur
2.3.1.2 Kekeruhan dan Warna
Prinsip kerja turbidimeter pada pengukuran tingkat kekeruhan dimana alat akan memancarkan
cahaya pada media atau sample, dan cahaya tersebut akan diserap dan ada yang diteruskan,
dipantulkan atau menembus media tersebut. Cahaya yang menembus/diserap media akan diukur
dan ditransfer kedalam bentuk angka yang merupakan tingkat kekeruhan, semakin banyak
cahaya yang diserap maka semakin keruh
Kekeruhan merupakan sifat optik air yang ditentukan berdasarkan banyaknya cahaya
yang diserap dan dipancarkan oleh bahan-bahan yang terdapat dalam air. Kekeruhan disebabakan
oleh adanya bahan organik dan anorganik yang tersuspensi dan terlarut(misalnya lumpur dan
pasir halus), maupun bahan anorganik dan organik yang berupa plankton dan mikroorganisme
lain.
Ada tiga metode pengukuran kekeruhan yaitu:
1. Metode Nefelometrik ( unit kekeruhan nefelometrik FTU atau NTU)
2. Metode Hellige Turbidimetri (Unit kekeruhan Silika)
3. Metode Visual ( Unit kekeruhan Jackson)
Prinsip metoda nefelometrik adalah perbandingan antara intensiti cahaya yang
dihamburkan dari suatu sampel air dengan intensiti cahaya yang dihamburkan oleh suatu larutan
keruh standard pada kondisi yang sama. Makin tinggi intensiti cahaya yang dihamburkan, maka
makin tinggi pula kekeruhannya. Sebagai standar kekeruhan dipergunakan suspensi polimer
formazin.
Kekeruhan dinyatakan dalam satuan unit turbiditas, yang setara dengan 1 mg/liter SiO2. Peralatan yang pertama kali digunakan untuk mengukur turbiditas atau kekeruhan adalah
Jackson Candler Turbidimeter, yang dikalibrasi dengan menggunakan silika. Kemudian Jackson
Candler Turbidimeter dijadikan sebagai alat baku atau standar bagi pengukuran kekeruhan. Satu
11
Warna air yang terdapat di alam sangat bervariasi, misalnya air di rawa-rawa berwarna
kuning, coklat atau kehijauan, air sungai biasanya berwarna kuning kecoklatan karena
mengandung lumpur, dan air buangan yang mengandung besi dalam jumlah tinggi berwarna
coklat kemerahan. Warna air yang tidak normal biasanya menunjukkan adanya polusi. Warna
air dapat dibedakan atas dua macam yaitu warna sesungguhnya yang di sebabkan oleh
bahan-bahan kimia terlarut, dan warna tampak yang selain disebabkan oleh adanya bahan-bahan-bahan-bahan terlarut
juga karena adanya bahan-bahan tersuspensi, termasuk yang bersifat koloid.
Warna perairan ditimbulkan oleh adanya bahan organik dan bahan anorganik, karena
keberadaan plankton, humus, dan ion-ion logam, serta bahan-bahan lain. Warna dapat diamati
secara langsung ataupun diukur berdasarkan skala platinum kobalt, dengan membandingkan
warna air sampel dan warna standar. Perairan alami tidak berwarna, air dengan nilai warna lebih
kecil dari 10 PtCo biasanya tidak memperlihatkan warna yang jelas. Air yang berasal dari
rawa-rawa yang biasanya berwarna kuning kecokelatan hingga kehitaman memiliki nilai warna sekitar
200-300 PtCo karena adanya asam humus. (Srikandi F,1992)
2.3.1.3 Besi
Keberadaan besi pada kerak bumi menempati posisi keempat terbesar. Besi ditemukan dalam
bentuk kation ferro (Fe2+) dan ferri (Fe3+). Pada perairan alami dengan pH sekitar 7 dan kadar oksigen terlarut yang cukup, ion ferro yang bersifat mudah larut dioksidasi menjadi ion ferri.
Pada oksidasi ini terjadi pelepasan elektron. Sebaliknya, pada reduksi ferri menjadi ferro terjadi
penangkapan elektron.
Pada perairan alami, besi berikatan dengan anion membentuk senyawa FeCl2, Fe(HCO3), dan FeSO4. Pada perairan domestik pengendapan ion ferri dapat mengakibatkan warna kemerahan pada porselin, bak mandi, pipa air, dan pakaian. Kelarutan besi meningkat dengan
banyak, ini dicirikan dengan rendahnya pH dan disertai dengan kadar oksigen terlarut yang
rendah.
Pada umumnya, besi yang dalam air dapat bersifat ;
- Terlarut sebagai Fe2+ (fero) atau Fe3+ (feri)
- Tersuspensi sebagai butir koloidal ( diameter < 1 µm atau lebih besar seperti Fe2O3, FeO, FeOOH, Fe(OH)3
- Tergabung dengan zat organis atau zat padat yang anorganis seperti tanah liat.
Prinsip analisa Fe adalah dimana didihan dalam asam dan hidroksilamin serta
penggabungannya dengan 1,10 fenantrolin akan mengubah semua zat besi menjadi Fe2+ yang terlarut. Besi (II) bereaksi dengan 1,10 fenantrolina membentuk kompleks merah jingg
[Fe(C12H8N2)3]2+. Intensitas warnanya tidak bergantung pada keasaman dalam jangka pH 2-9, dan stabil untuk waktu yang lama. Besi (III) dapat direduksi dengan hidroksilamonium klorida.
(Vogel 1994)
2.3.1.4. Zat Padat dalam Air
Padatan total (residu) adalah bahan yang tersisa setelah air sampel mengalami pengeringan pada
suhu tertentu. Residu dianggap sebagai kandungan total bahan terlarut dan tersuspensi dalam air.
Padatan tersuspensi total ( Total Suspended Solid atau TSS) atau bahan-bahan tersuspensi (diameter > 1µm) yang tertahan pada saringan millipore dengan diameter pori 0,45 µm. TSS
terdiri atas lumpur dan pasir halus serta jasad-jasad renik, yang terutama disebabkan oleh kikisan
tanah atau erosi tanah yang terbawa ke badan air. Prinsip analisanya bila zat padat dalam sampel
dipisahkan dengan menggunakan filter kertas atau fiber glass dan kemudian zat padat yang
13
Settleable solid adalah jumlah padatan tersuspensi yang dapat diendapkan selama periode waktu tertentu. Padatan terlarut total (Total Dissolved Solid atau TDS) adalah bahan-bahan terlarut (diameter < 10-6 mm) dan koloid (diameter 10-6 mm – 10-3mm) yang berupa senyawa-senyawa kimia dan bahan-bahan lain, yang tidak tersaring pada kertas saring. (Hefni E, 2003)
Prinsip analisa Zat padat terlarut yaitu zat padat yang lolos filter pada analisa zat
tersuspensi kemudian diuapkan dan dikeringkan pada suhu 1050C. Residu yang tertinggal adalah zat padat terlarut.
Dalam metode analisa zat padat pengertian zat padat total adalah semua zat-zat yang
tersisa sebagai residu dalam suatu bejana, bila sampel air dalam bejana tersebut dikeringkan pada
suhu tertentu. Zat padat total terdiri dari zat padat terlarut dan zat padat tersuspensi yang bersifat
organis dan inorganis.
Zat Padat Tersuspensi sendiri dapat diklasifikasikan sekali lagi menjadi antara lain zat
padat terapung yang selalu bersifat organis dan zat padat terendap yang dapat bersifat organis
dan inorganis. Zat padat terendap adalah zat padat dalam suspensi yang dalam keadaan tenang
dapat mengendap setelah waktu tertentu karena pengaruh gaya beratnya. Dimensi dari zat-zat
padat di atas adalah dalam mg/L atau g/L, namun sering pula ditemui % berat yaitu kg zat padat /
kg larutan atau % volume yaitu dm3 zat padat / liter larutan. (G. Alaerts, 1984)
2.4 Arang
Arang adalah padatan berpori yang terdiri dari karbon yang berbentuk amorf. Arang juga
merupakan suatu jaringan atom dengan komponen utama karbon, berwarna hitam dan dapat
dihasilkan dalam bentuk serbuk, butiran, maupun bongkahan. Bahan yang mengandung
hidrokarbon dapat digunakan sebagai sumber atau bahan baku pembuatan arang antara lain :
batubara, residu petrokimia, kayu, cangkang kelapa, tongkol jagung, tulang dan lain sebagainya.
Dalam pembutan arang yang memegang peranan penting adalah fixed karbon yang terdapat
pengarangan (pirolisis) merupakan suatu “ evolusi “ pembentukan dari bahan baku
menjadi arang melalui beberapa tahapan. Proses pembuatan arang dibagi atas 4 (empat) tahapan
sebagai berikut :
1. Pada permulaan pemanasan, air menguap, kemudian selulosa terurai pada suhu antara
200-2600C
2. Pada suhu 260-310oC selulosa terurai secara intensif, pada tingkatan ini banyak dihasilkan cairan piroligneous, gas, dan ter
3. Pada suhu 310-500oC lignin terurai dan ter yang dibentuk lebih banyak, sedangkan cairan piroligneous dan gas menurun
4. Pada suhu lebih besar dari 500oC, diperoleh gas hidrogen yang sukar dikondensasikan dan tahapan ini merupakan proses pemurnian arang.
Arang dapat dibedakan menurut penggunaannya dan jenisnya, sebagai berikut :
1. Arang keras ( hard charcoal), banyak digunakan sebagai reduktan pengolahan biji logam,
metalurgi, arang aktif, serbuk hitam dan karbon disulfida.
2. Arang sedang ( moderate charcoal) digunakan sebagai bahan bakar dan untuk
obat-obatan kimia seperti karbon disulfida, natrium sianida dan lain sebagainya.
3. Arang lunak (soft charcoal), merupakan bahan baku untuk pembuatan arang aktif dan
briket arang.
Arang selain digunakan sebagai bahan bakar juga dapat digunakan sebagai adsorben
bahan penyeerap. Daya serap ditentukan luas permukaan partikel dan kemampuan ini dapat
menjadi lebih tinggi jika terhadap arang tersebut dilakukan aktivasi dengan aktivator
bahan-bahan kimia ataupun dengan pemanasan pada temperatur tinggi. Dengan demikian arang akan
mengalami perubahan sifat-sifat fisika dan kimia, arang yang demikian disebut arang aktif. (Ita
15
2.5 Pembuatan Arang
Ada bermacam-macam metode pembuatan arang, baik metode tradisional maupun
metode yang lebih diperbaharui. Perbedaan metode-metode ini dapat berupa alat atau teknik
yang dipakai dalam pembuatannya, yang mana setiap metode mempunyai kelebihan dan
kekurangan.
2.5.1 Metode Tradisional
Metode tradisional yang dikenal serta umum digunakan oleh masyarakat di dalam pembuatan
arang, yaitu berupa metode lubang tanah. Selain itu dikenal juga metode lain yang sudah
berkembang dengan pengaturan ventilasi udara yang lebih terkontrol serta penggunaan bahan
lain sebagai media tungku. Beberapa metode tersebut antara lain adalah metode tungku drum
serta tungku batu bata.( H. Iskandar, 2005)
2.5.2 Metode Diperbaharui
Pembuatan karbon dengan metode yang diperbaharui dilakukan dengan dua tahap, yaitu
tahap pengarangan (karbonisasi) dan tahap pengaktifan (aktivasi). Dalam metode ini bahan baku
dipanaskan dengan jumlah udara seminimal mungkin agar rendemen yang dihasilkan cukup
besar. Hasil yang diperoleh dengan metode ini berupa karbon yang memberikan keaktifan dan
rendemen yang cukup besar terhadap karbon aktif cara di atas.
Menurut Cheremisinoff dan A.C Morresi, dikemukakan bahwa proses pembuatan arang aktif
terdiri dari tiga tahap yaitu :
1. Dehidrasi : proses penghilangan air
Bahan baku dipanaskan sampai suhu 270o C
Temperatur diatas 170oC akan menghasilkan CO, CO2 dan asam asetat. Pada temperatur 275oC, dekomposisi menghasilkan tar, metanol, dan hasil sampingan lainnya. Pembentukan karbon terjadi pada temperatur 400-600 oC.
3. Aktivasi : Dekomposisi tar dan perluasan pori-pori
Dapat dilakukan dengan uap atau CO2 sebagai aktivator. (Dhanny H, 2001)
2.6. Adsorpsi
Bila dua fasa bertemu (terjadi kontak antar fasa), maka diantara kedua fasa terjadi daerah
antar muka yang sifatnya berbeda dengan fasa ruah kedua fasa tersebut. Pada kondisi dan
tekanan tertentu, molekul-molekul dalam daerah ini dapat mengalami ketidakseimbangan gaya
tersebut tercapai. Melekatnya atom atau molekul suatu zat pada permukaan zat lain disebut
adsorpsi. Zat yang teradsorpsi biasanya terkonsentrasi pada permukaan, hal ini menyebabkan
pengurangan dari tegangan permukaan dan adsorpsi akan berlangsung terus sampai energi bebas
permukaan minimum. (Benefield dkk, 1982)
2.6.1. Adsorpsi Gas oleh Zat Padat
Daya serap zat padat terhadap gas tergantung dari jenis adsorben, jenis gas, luas
permukaan adsorbens, temperatur gas, dan tekanan gas. Makin luas permukaan adsorbens, makin
banyak gas yang diserap. Luas permukaan sukar ditentukan, hingga biasanya daya serap dihitung
tiap satuan massa adsorbens. Pada adsorpsi gas dipermukaan zat padat, terjadi kesetimbangan
antara gas yang terserap dengan gas sisa.
2.6.2. Adsorpsi Zat Terlarut oleh Zat Padat
Penyerapan zat dari larutan, mirip dengan penyerapan gas oleh zat padat. Penyerapan
17
lebih, zat yang satu akan diserap labih kuat dari yang lain. Zat-zat yang dapat menurunkan
tegangan permukaan lebih kuat diserap.
Menurut jenisnya, adsorpsi pada antar muka dapat dibagi menjadi dua bagian yaitu :
1. Adsorpsi Fisika
2. Adsorpsi Kimia
Adsorpsi fisika dihasilkan karena adanya gaya-gaya Van Der Walls. Biasanya adsorpsi
fisika terjadi pada semua zat. Jika molekul-molekul yang diadsorpsi itu mempunyai gugus
hidroksil, maka adsorpsi fisika dapat berlangsung disebabkan terbentuknya ikatan hidrogen.
Adsorpsi kimia adalah peristiwa dimana ikatan kimia terbentuk antara permukaan zat
pada (adsorben) dan molekul-molekul yang diadsorpsi, dan sifat kimia adsorbat mula-mula beda
dengan sifat kimia dari keadaan setelah adsorpsi. (Sukardjo, 1989)
2.7.Jagung
Jagung (Zea mays L.) merupakan salah sat
selain
menargetkan produksi jagung sebesar 16,5 juta ton dari kebutuhan 13 juta ton. Dengan besarnya
produksi jagung di Indonesia maka akan semakin besar pula limbah tongkol jagung yang
dihasilkan oleh tanaman palawija ini.
Limbah tongkol jagung selama ini kurang dimanfaatkan, kebanyakan limbah tongkol jagung
hanya digunakan untuk bahan tambahan makanan ternak atau untuk kayu bakar.
Masalah dari limbah tongkol jagung ini dapat diatasi dengan menjadikan tongkol jagung
menjadi produk yang bernilai. Tongkol jagung banyak sekali mengandung senyawa jenis
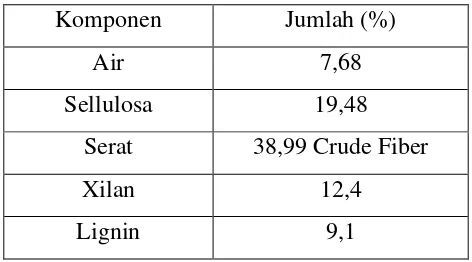
Tabel 2.1 Komposisi kimia tongkol jagung
Komponen Jumlah (%)
Air 7,68
Sellulosa 19,48
Serat 38,99 Crude Fiber
Xilan 12,4
Lignin 9,1
BAB 3
BAHAN DAN METODE PENELITIAN
3.1.Alat – alat
Alat – alat yang digunakan dalam penelitian ini adalah :
1. Neraca elektrik Mettler PM 400
2. pH meter WTW
3. Spektrofotometer Milton Roy
4. Turbidimeter HF scientific
5. Oven Fisher
6. Alat – alat gelas Pyrex
7. Mikro Pipet Pyrex
8. Kertas Saring Whatman
9. Botol Cuci
10.Kaleng
11.Kolom
12.Statif dan Klem
3.2. Bahan – bahan
Bahan – bahan yang digunakan dalam penelitian ini adalah :
Tongkol jagung
HCl(p) P.a E.Merck
H2SO4(p) P.a E.Merck
1,10 fenantrolin P.a E.Merck
CH3COOH Glasial P.a E.Merck
CH3COONH4 P.a E.Merck
NH2OH.HCl P.a E.Merck
Akuades
Fe(NH4)2(SO4)2.6H2O P.a E.Merck
KMnO4 P.a E.Merck
3.3. Prosedur Penelitian
3.3.1. Penyediaan Sampel Air Rawa
Sampel air rawa diambil, kemudiaan dimasukkan kedalam botol plastik yang terlebih
dahulu dibilas dengan air rawa tersebut.
3.3.2. Pembuatan Pereaksi dan Larutan Standar Fe(NH4)2(SO4)2.6H2O untuk Penentuan ion Fe total dengan Metode Spektrofotometri
a. Larutan Hidroksilamin (NH2OH.HCl)
Sebanyak 10 g NH2OH.HCl dilarutkan dengan akuades, kemudian diencerkan di dalam labu takar 100 mL sampai garis tanda dan dihomogenkan.
b. Larutan Buffer Ammonium Asetat
Sebanyak 25 g NH4.C2H3O2 dilarutkan dengan 15 mL akuades dan ditambahkan 70 mL asam asetat glasial, kemudian diencerkan di dalam labu ukur 100 mL sampai garis tanda dan
21
c. Larutan 1,10 Fenantrolin
Sebanyak 0,1 g kristal 1,10 fenantrolin monohidrat (C12H8N2.H2O) dilarutkan dalam 100 mL akuades, kemudian dipanaskan sampai suhu 80oC (tidak boleh mendidih)
d. Larutan induk Fe(NH4)2(SO4)2.6H2O 1000 mg/L
Di dalam labu ukur 1L diisi 50 mL akuades, kemudian ditambahkan dengan hati-hati 20
mL H2SO4 pekat, kemudian larutkan kedalamnya sebanyak 7,0225 g Fe(NH4)2(SO4)2.6H2O. Tambahkan larutan KMnO4 0,1 N sedikit demi sedikit sampai warna merah muda. Diencerkan dengan akuades sampai garis tanda kemudian dihomogenkan.
e. Larutan standar Fe(NH4)2(SO4)2.6H2O 100 mg/L
Sebanyak 5 mL larutan induk Fe(NH4)2(SO4)2.6H2O 1000 mg/L dimasukkan dalam labu ukur 50 mL lalu diencerkan dengan akuades sampai garis tanda dan dihomogenkan.
f. Larutan standar Fe(NH4)2(SO4)2.6H2O 10 mg/L
Sebanyak 25 mL larutan induk 100 mg/L dimasukkan dalam labu ukur 250 mL lalu
diencerkan dengan akuades sampai garis tanda dan dihomogenkan.
g. Larutan seri standar Fe(NH4)2(SO4)2.6H2O 0,6; 0,8; 1,0; 1,2; 1,4; 1,6; 1,8; 2,0 mg/L
Sebanyak 6, 8, 10, 12,14,16,18 dan 20 mL larutan standar 10 mg/L dan dimasukkan ke dalam
masing-masing labu ukur 100 mL, kemudian diencerkan dengan akuades sampai garis tanda dan
dihomogenkan.
Sebanyak 100 mL sampel air rawa dimasukkan kedalam gelas beaker 250 mL. Terlebih
dahulu pH meter dikalibrasi dengan larutan buffer pH = 7, kemudian pH sampel diukur dengan
menggunakan pH meter (Perlakuan dilakukan sebanyak 3 kali).
3.3.4. Penentuan ion Fe total dengan metode spektrofotometri
Sebanyak 25 mL sampel di pipet ke dalam erlenmeyer 250 mL kemudian ditambah 1 mL
HCl(p) dan 0,5 mL NH2OH.HCl kemudian dididihkan 15 sampai 20 menit diatas hot plate. Setelah itu, didinginkan kemudian ditambah 5 mL larutan buffer ammonium asetat dan 1 mL
1,10 fenantrolin kemudian didiamkan selama 10 menit sehingga dihasilkan larutan berwarna
merah orange. Transmitansi larutan diukur dengan spektrofotometer Spektronik 20 pada λ = 510 nm (perlakuan dilakukan sebanyak 3 kali)
3.3.5. Penentuan Kekeruhan dengan metode Turbidimetri
Sebanyak 100 mL sampel dimasukkan ke dalam kuvet sampai tidak terdapat gelembung
udara, kemudian ditutup dan dimasukkan kedalam turbidimeter yang diukur kekeruhannya.
3.3.6. Penentuan Padatan Terlarut dan Padatan Tersuspensi dalam Air
Sebanyak 50 mL sampel disaring menggunakan kertas saring whatman no 42 dan
ditampung di dalam gelas beaker 250 mL. Yang terlebih dahulu massa kertas saring whatman
no.42 dan gelas beaker 250 mL telah diukur massa kosongnya dengan menggunakan neraca
elektrik. Setelah itu, kertas saring whatman no.42 dan endapan dikeringkan di dalam oven
sampai suhu 105oC dan dimasukkan ke dalam desikator, kemudian diukur massa kertas saring yang diukur sebagai padatan tersuspensi dan gelas beaker 250 mLyang berisi larutan sampel
diuapkan diatas hot plate sampai air menguap, kemudian dimasukkan di dalam oven sampai suhu
23
3.3.7. Penentuan Panjang Gelombang Maksimum (λ maks)
Sebanyak 25 mL Larutan seri standar Fe(NH4)2(SO4)2.6H2O 0,8 mg/L dimasukkan ke dalam Erlenmeyer 250 mL, kemudian ditambahkan 1 mL HCl(p), 0,5 mL NH2OH.HCl, 5 mL larutan buffer amonium asetat dan 1 mL 1,10 fenantrolin sehingga didapat larutan berwarna
merah orange. Setelah itu, didiamkan 10 menit, kemudian diukur transmitansi larutan dengan
spektrofotometer sinar tampak spektronik 20,dengan variasi panjang gelombang
500,505,510,515, dan 520 nm
3.3.8. Penentuan Waktu Operasi
Sebanyak 25 mL Larutan seri standar Fe(NH4)2(SO4)2.6H2O 0,8 mg/L dimasukkan ke dalam Erlenmeyer 250 mL, kemudian ditambahkan 1 mL HCl(p), 0,5 mL NH2OH.HCl, 5 mL larutan buffer amonium asetat dan 1 mL 1,10 fenantrolin sehingga didapat larutan berwarna
merah orange. Setelah itu, didiamkan dengan variasi waktu 5 menit, kemudian diukur
transmitansi larutan dengan spektrofotometer sinar tampak spektronik 20, dengan panjang
gelombang 510 nm, dilakukan perlakuan yang sama dengan vaiasi waktu 10, 15,20, dan 25
menit.
3.3.9. Pembuatan Kurva Larutan Standar Fe(NH4)2(SO4)2.6H2O dengan metode Spektrofotometri
Sebanyak 25 mL Larutan seri standar Fe(NH4)2(SO4)2.6H2O 0,6 mg/L dimasukkan ke dalam erlenmeyer 250 mL, kemudian ditambahkan 1 mL HCl(p), 0,5 mL NH2OH.HCl, 5 mL larutan buffer amonium asetat dan 1 mL 1,10 fenantrolin sehingga didapat larutan berwarna
merah orange. Setelah itu, didiamkan 10 menit, kemudian diukur absorbansi larutan dengan
spektrofotometer spektronik 20 λ = 510 nm (perlakuan yang sama dilakukan sebanyak 3 kali dan
3.4. Bagan penelitian
3.4.1. Preparasi sampel Air Rawa
Air Rawa
Ditutup hingga tidak terdapat gelembung udara
Sampel Air Rawa
Dimasukkan ke dalam botol plastik 5 L
3.4.2. Preparasi Pembuatan Arang
Tongkol Jagung
Dimasukkan ke dalam kaleng Dipotong kecil-kecil
Dipasang tutup kaleng dan cerobong asap pada bagian atas kaleng
Dibakar sampai semua bahan baku menjadi arang
Arang
Disaring dengan Ayakan Listrik Ukuran 80 Mesh Dihaluskan arang
25 3.4.3. Preparasi Pembuatan Serbuk Tongkol Jagung
Tongkol Jagung
Dihaluskan dengan menggunakan blender Dipotong kecil-kecil
Disaring dengan Ayakan listrik 80 Mesh
Serbuk Tongkol Jagung
3.4.4. Penambahan Arang Tongkol Jagung Kedalam Sampel Air Rawa
200 g Arang
Ditambahkan 1 L sampel Air Rawa Dimasukkan ke dalam kolom
Ditutup dengan plastik
Didiamkan selama 24 jam
Larutan jernih disaring dan ditampung ke dalam gelas beaker 1 L Larutan jernih dan Endapan Arang
Larutan jernih air rawa
3.4.5. Penentuan pH Sampel Air Rawa
pH- Meter
dihidupkan dengan menekan tombol-ON disambung dengan elektroda
dibiarkan 15 menit
elektroda dicuci dan dikeringkan
harga pH diatur pada angka 7 dengan menekan tombol "Cal" elektroda dicelupkan kedalam larutan buffer pH 7
diulangi dengan menggunakan pH 4 dan 9
pH Meter terkalibrasi
elektroda dicelupkan kedalam sampel air rawa
Hasil
Catatan : Perlakuan yang sama dilakukan sebanyak 3 kali, sebelum dan sesudah
penambahan arang dan serbuk tongkol jagung
3.4.6. Penentuan Turbiditas Sampel Air Rawa
Sampel Air Rawa
ditutup hingga tidak terdapat gelembung udara dimasukkan ke dalam kuvet
diukur turbiditasnya dengan menggunakan turbidimeter
Hasil
Catatan : Perlakuan yang sama dilakukan sebanyak 3 kali, sebelum dan sesudah
27
3.4.7. Penentuan Ion Fe Total Dalam Sampel Air Rawa
25 mL Sampel Air Rawa
dimasukkan kedalam gelas erlenmeyer 250 mL
ditambahkan 1 mL HCl(p)
ditambahkan 0,5 mL NH2OH.HCl
dididihkan diatas hot plate selama 15-20 menit
ditambahkan 1 mL 1,10 fenantrolin
didiamkan selama 10 menit
larutan berwarna merah orange
Diukur transmitansi dengan spektrofotometer pada max = 510 nm
Hasil
ditambahkan 5 mL buffer amonium asetat
Catatan : Perlakuan yang sama dilakukan sebanyak 3 kali, sebelum dan sesudah
penambahan Arang dan Serbuk Tongkol Jagung
3.4.8. Penentuan Padatan Terlarut (TDS) Dan Padatan Tersuspensi (TSS) Dalam Sampel Air Rawa
a. Penentuan Berat Awal (Berat kosong) gelas beaker
Gelas Beaker 250 mL
dibersihkan
dikeringkan dalam oven pada suhu ± 105oC
dimasukkan kedalam desikator
ditimbang berat
Catatan : Perlakuan yang sama dilakukan untuk kertas saring Whatman No. 42, dan
pengukuran yang sama dilakukan sebanyak 3 kali, sebelum dan sesudah
penambahan arang dan serbuk tongkol jagung.
b. Penentuan Berat Akhir Padatan Terlarut (TDS) dan Padatan Tersuspensi (TSS) dari Sampel Air Rawa
50 mL Sampel Air Rawa
disaring
Filtrat
dimasukkan kedalam gelas beaker
dikeringkan diatas hot plate
dimasukkan kedalam desikator
ditimbang berat gelas beaker
Berat akhir
dihitung sebagai TDS
Hasil Endapan
dikertas saring
dikeringkan di dalam oven pada suhu 105 ± oC
dimasukkan kedalam desikator
ditimbang berat kertas saring
Berat akhir
dihitung sebagai TSS
Hasil
Catatan : Perlakuan yang sama dilakukan sebanyak 3 kali, sebelum dan sesudah
penambahan arang dan serbuk tongkol jagung.
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil dan Pengolahan Data
4.1.1. Hasil Penelitian
Hasil analisis sifat fisik yaitu Turbiditas, Padatan Total Terlarut (TDS), Padatan Total
Tersuspensi (TSS) dan sifat Kimia yaitu pH, Besi (Fe), pada sampel air rawa sebelum dan
sesudah penambahan tongkol jagung kedalam air rawa dapat dilihat pada tabel 4.2.
4.1.2. Data Persen Penurunan Kadar
Data hasil percobaan yang diperoleh ditunjukkan dalam tabel 4.2, dalam pembahasan. Persen
penurunan kadar diperoleh dari hasil perhitungan dengan rumus sebagai berikut :
Persen penurunan = x100% awal
akhir awal−
4.2. Perhitungan
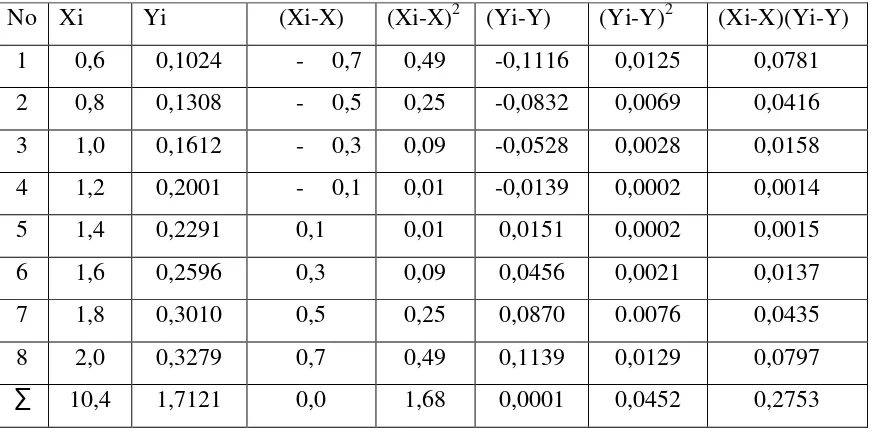
4.2.1. Penurunan Persamaan Garis Regresi Fe(NH4)2(SO4)2.6H2O dengan metode kurva kalibrasi
garis linier dapat dilihat pada lampiran. Persamaan garis regresi untuk kurva kalibrasi ini dapat
diturunkan dengan metode Least Square dapat dilihat pada tabel berikut :
Tabel 4.1. Data Hasil Penurunan Persamaan Regresi untuk Larutan
Fe(NH4)2(SO4)2.6H2O
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan garis :
y = ax + b
Sehingga diperoleh harga a :
31
Harga Intersept (b) diperoleh melalui subsitusi harga (a) ke persamaan berikut :
Y = ax + b
b = Y – ax
= 0,2140 – ( 0,1639 x 1,3 )
= 0,2140 – 0,2131
= 0,0009
Maka persamaan garis regresi yang diperoleh adalah :
Y = 0,1639x + 0,0009
4.2.2. Penentuan Kadar Ion Fe Total dalam Sampel
Kadar ion Fe total dapat ditentukan dengan menggunakan metode kurva kalibrasi dengan
mensubsitusikan nilai Y (Absorbansi) yang diperoleh dari hasil pengukuran terhadap persamaan
garis regresi dari kurva kalibrasi.
4.2.2.1. Penentuan Kadar Ion Fe Total dalam Sampel Air Rawa sebelum penambahan Serbuk Tongkol Jagung dan Arang Tongkol Jagung
Dengan mensubstitusikan nilai Y (absorbansi) yang terdapat dalam lampiran 7, ke persamaan
garis regresi berikut :
Y = 0,1639x + 0,0009
Maka diperoleh
X1 = 1,8309 mg/L X2 = 1,7785 mg/L X3 = 1,7785 mg/L
Dengan demikian kadar besi (Fe) pada sampel air rawa adalah :
n Xi X =
∑
_
4.2.2.2. Penentuan Kadar Ion Fe Total dalam Sampel Air Rawa setelah penambahan Serbuk Tongkol Jagung dan Arang Tongkol Jagung
Dengan mensubstitusikan nilai Y (absorbansi) yang terdapat dalam lampiran 7, ke persamaan
garis regresi berikut :
Y = 0,1639x + 0,0009
Maka diperoleh :
Untuk Serbuk tongkol jagung :
X1 = 0,7566 mg/L X2 = 0,7566 mg/L X3 = 0,7926 mg/L Untuk Arang tongkol jagung :
X1 = 1,1361 mg/L X2 = 1,0964 mg/L X3 = 1,0964 mg/L
Dengan demikian kadar ion Fe total pada sampel air rawa setelah penambahan Serbuk Tongkol
Jagung dan Arang Tongkol Jagung adalah :
n
4.2.2.3. Persen Penurunan Kadar Ion Fe Total
Persen penurunan kadar ion Fe total = x100% awal
akhir awal−
Serbuk tongkol jagung
= 57,20 %
Arang tongkol jagung
%
4.2.3 Penentuan Turbiditas (Kekeruhan) dalam Sampel
4.2.3.1 Penentuan Turbiditas (Kekeruhan ) secara turbidimetri pada sampel air rawa sebelum penambahan Serbuk Tongkol Jagung dan Arang Tongkol Jagung
Dari masing-masing turbiditas yang terdapat dalam lampiran 8, sehingga didapat nilai turbiditas
rata-rata yaitu :
n d d =
∑
_
Sehingga didapat : 18,05 NTU
4.2.3.2 Penentuan Turbiditas (Kekeruhan ) secara turbidimetri pada sampel air rawa setelah penambahan Serbuk Tongkol Jagung dan Arang Tongkol Jagung
Dari masing-masing turbiditas yang terdapat dalam lampiran 8, sehingga didapat nilai turbiditas
10,86 NTU dan dengan penambahan arang tongkol jagung sebesar 9,76 NTU
4.2.3.3. Persen Penurunan turbiditas (kekeruhan ) dalam sampel air rawa
Persen penurunan turbiditas = x100% awal
akhir awal−
Untuk Serbuk tongkol jagung :
%
Untuk Arang tongkol jagung :
%
4.2.4. Penentuan Total Padatan Terlarut dalam larutan (TDS) dan Total Padatan Tersuspensi dalam larutan (TSS) dalam sampel.
Penentuan Total Padatan Terlarut (TDS) dan Total Padatan Tersuspensi (TSS) dalam sampel
dapat dihitung dengan rumus sebagai berikut :
)
Keterangan : A = Berat awal (berat kosong) gelas beaker sebelum ditambah sampel air
Keterangan : A = Berat awal (berat kosong) kertas saring sebelum ditambah sampel air
Dari masing-masing berat kertas saring yang terdapat dalam lampiran 10, didapat nilai berat
rata-rata yaitu :
n W Wk =
∑
i−
sehingga di dapatkan : =
−
k
W 0,009 g
= 9 mg
Dengan mensubstitusikan nilai berat rata-rata ini ke rumus diatas maka diperoleh total padatan
tersuspensi dalam larutan adalah :
TSS = 180 mg/L
4.2.4.2. Penentuan Total Padatan Tersuspensi (TSS) dalam sampel air rawa setelah penambahan Serbuk Tongkol Jagung
Dari masing-masing berat kertas saring yang terdapat dalam lampiran 10, didapat nilai berat
rata-rata yaitu :
sehingga di dapatkan : =
−
k
W 0,003 g
= 3 mg
Dengan mensubstitusikan nilai berat rata-rata ini ke rumus diatas maka diperoleh total padatan
tersuspensi dalam larutan adalah :
4.2.4.3. Penentuan Total Padatan Tersuspensi (TSS) dalam sampel air rawa setelah penambahan Arang Tongkol Jagung
Dari masing-masing berat kertas saring yang terdapat dalam lampiran 10, didapat nilai berat
rata-rata yaitu :
n W Wk =
∑
i−
sehingga di dapatkan : =
−
k
W 0,008 g
= 8 mg
Dengan mensubstitusikan nilai berat rata-rata ini ke rumus diatas maka diperoleh total padatan
tersuspensi dalam larutan adalah :
TSS = 160 mg/L
4.2.4.4. Persen Penurunan Total Padatan Tersuspensi dalam larutan (TSS)
Persen penurunan TSS = x100% awal
akhir awal−
Untuk Serbuk tongkol jagung :
%
Untuk arang tongkol jagung :
4.2.4.5. Penentuan Total Padatan Terlarut (TDS) dalam sampel air rawa sebelum penambahan Serbuk Tongkol Jagung dan Arang Tongkol Jagung.
Dari masing-masing berat gelas beaker yang terdapat dalam lampiran 11, sehingga didapat nilai
berat rata-rata yaitu :
n W WG =
∑
i−
Sehingga di dapatkan : =
−
G
W 0,011 g
= 11 mg
Dengan mensubstitusikan nilai berat rata-rata ini ke rumus diatas maka diperoleh total padatan
terlarut dalam larutan adalah :
TDS = 220 mg/L
4.2.4.6. Penentuan Total Padatan Terlarut (TDS) dalam sampel air rawa setelah penambahan Serbuk Tongkol Jagung
Dari masing-masing berat gelas beaker yang terdapat dalam lampiran 11, sehingga didapat nilai
berat rata-rata yaitu :
n W WG =
∑
i−
Sehingga di dapatkan : =
−
G
W 0,006 g
= 6 mg
Dengan mensubstitusikan nilai berat rata-rata ini ke rumus diatas maka diperoleh total padatan
terlarut dalam larutan adalah :
TDS = 120 mg/L
4.2.4.7. Penentuan Total Padatan Terlarut (TDS) dalam sampel air rawa setelah penambahan Arang Tongkol Jagung
berat rata-rata yaitu :
n W WG =
∑
i−
Sehingga di dapatkan : =
−
G
W 0,007 g
= 7 mg
Dengan mensubstitusikan nilai berat rata-rata ini ke rumus diatas maka diperoleh total padatan
terlarut dalam larutan adalah :
TDS = 140 mg/L
4.2.4.8. Persen Penurunan Total Padatan Terlarut (TDS)
Persen penurunan TDS = x100% awal
akhir awal−
Untuk Serbuk tongkol jagung :
%
Untuk arang tongkol jagung :
%
4.2.5. Penentuan pH pada sampel air rawa sebelum ditambahkan Serbuk Tongkol Jagung dan Arang Tongkol Jagung
Dari masing-masing nilai pH yang terdapat dalam lampiran 9, sehingga didapat nilai pH rata-rata
yaitu :
n pH pH =
∑
−
Sehingga didapat : 6,72
4.2.5.1. Penentuan pH pada sampel air rawa setelah ditambahkan Serbuk Tongkol Jagung
Dari masing-masing nilai pH yang terdapat dalam lampiran 9, sehingga didapat nilai pH rata-rata
yaitu :
n pH pH =
∑
−
Sehingga didapat : 7,40
4.2.5.2. Penentuan pH pada sampel air rawa setelah ditambahkan Arang Tongkol Jagung
Dari masing-masing nilai pH yang terdapat dalam lampiran 9, sehingga didapat nilai pH rata-rata
yaitu :
n pH pH =
∑
−
Sehingga didapat : 7,7
Di dalam penelitian ini, pembuatan arang tongkol jagung dilakukan dengan secara tradisional
dan pembuatan serbuk tongkol jagung dihaluskan.Sehingga diperoleh arang yang memiliki unsur
karbon yang tinggi dan serbuk tongkol jagung yang kemudian disaring dengan menggunakan
ayakan listrik ukuran ± 80 mesh. Setelah didapat arang tongkol jagung dan serbuk tongkol
jagung yang berukuran ± 80 mesh kemudian masing-masing dimasukkan dalam kolom dan
ditambahkan air rawa yang telah ditentukan parameter Air untuk mewakili sifat-sifat fisik dan
kimia pada air rawa tersebut. Dari hasil analisis yang sudah dilakukan terhadap sampel air rawa
yang telah ditambahkan arang tongkol jagung dan serbuk tongkol jagung diperoleh perubahan
kadar sifat-sifat fisik dan sifat-sifat kimia pada sampel air rawa yaitu :
Tabel 4.2. Data Hasil pengukuran nilai parameter sifat fisik dan sifat kimia dalam sampel air rawa serta penurunannya.
Dari hasil yang didapatkan dalam tabel 4.2 dapat dilihat bahwa terjadi perubahan pada kadar
atau nilai beberapa parameter air yang terdapat dalam air rawa ini menunjukkan bahwa adanya
peranan arang tongkol jagung dan serbuk tongkol jagung yang berfungsi sebagai adsorben yang
ditambahkan didalam sampel air rawa yang berada dalam kolom. Dari kedua bahan adsorben
yang ditambahkan kedalam air rawa dapat diketahui bahwa terjadi peningkatan nilai pH ini
disebabkan karena komposisi dari tongkol jagung yang dominan bersifat basa, dan juga mampu
menurunkan kadar kekeruhan, Total padatan tersuspensi (TSS), Total padatan terlarut (TDS) dan
besi (Fe) pada air rawa, hal ini disebabkan juga dari komposisi tongkol jagung yang banyak
mengandung selulosa dan serat. Adsorben serbuk tongkol jagung memiliki daya serap yang lebih
tinggi dibandingkan arang tongkol jagung, dimana arang tongkol jagung memiliki unsur karbon
sedangkan serbuk tongkol jagung memiliki komposisi yang alami yaitu selulosa dan serat.
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari penelitian ini diperoleh hasil sebagai berikut :
Persen penurunan kadar parameter besi (Fe), Total Padatan Tersuspensi (TSS), Total Padatan
Terlarut (TDS), dan Kekeruhan lebih tinggi dengan menggunakan adsorben serbuk tongkol
jagung dibandingkan dengan arang tongkol jagung (lampiran 12).
5.2. Saran
Pada penelitian ini dilakukan dengan ukuran adsorben 80 mesh dimana % penurunan kadar dari
setiap parameter berkisar 50 %, sehingga pada penelitian selanjutnya disarankan menggunakan
ukuran adsorben yang lebih halus dan variasi pengaktifan untuk mendapatkan hasil yang lebih
baik.
Alaerts, G. 1984. Metode Penelitian Air.Surabaya : Usaha Nasional.
Benelfild, L.N. 1982.Process Chemistry for Water and Wastewater Treatment. New Jersey : Prentice Hall Inc.
Effendi, H. 2003.Telaah Kualitas Air.Yogyakarta : Kanisius
Fardiaz, S. 1992. Polusi Air dan Udara. Yogyakarta : Kanisius
Greenberg, A. et al. 1985. Standard Methods for The Examination of Water and Wastewater. Sixth Edition. Washington DC : American Publish Health Association.
Hermawan, D. 2001. Studi Perbandingan Analisis Logam Tembaga (Cu2+) dan Logam Besi (Fe3+) Dengan Menggunakan Arang Aktif Sekam Kayu dan Arang Aktif Komersial Dengan Metode Spektrofotometri Serapan Atom. Skripsi Sarjana jurusan Kimia. FMIPA-USU. Medan
Iskandar, H. et al. 2005. Panduan Singkat Cara Pembuatan Arang Kayu. Jakarta. PT Inti Prima Karya
Miller, J C. 1991. Statistika Untuk Kimia Analitik. Bandung. Penerbit ITB
Mulja, M. 1995. Analisis Instrument. Surabaya : Airlangga University Press
Pasaribu, Farida A. 2009. Peranan Gliserol Sebagai Plastisiser Dalam Film Pati Jagung Dengan Pengisi Serbuk Halus Tongkol Jagung. Tesis Pascasarjana – USU.
Medan
Ryadi, S. 1984. Pencemaran Air. Surabaya : Karya Anda
Silalahi, Ita K.1996. Pengaruh Kecepatan Aliran Gas Nitrogen (N2) Pada Proses Karbonisasi Terhadap Luas Permukaan Arang. Skripsi Sarjana. Jurusan Kimia FMIPA – USU. Medan
Sukardjo. 1989. Kimia Fisika. Jakarta : Bina Aksara
Vogel. 1994. Kimia Analisis Kuantitatif Anorganik. Edisi Keempat. Jakarta : Buku Kedokteran
Lampiran 1. Data Penentuan Panjang Gelombang Maksimum dari Larutan Seri Standar Fe(NH4)2( SO4)2 6H2O 0,8 mg/L
No Panjang Gelombang (nm)
% T Absorbansi
1 500 75 0,1249
2 505 74 0,1308
3 510 73 0,1367
4 515 74 0,1308
5 520 76 0,1192
Lampiran 2. Gambar grafik penentuan panjang gelombang maksimum untuk larutan seri standar Fe(NH4)2(SO4)2.6H2O 0,8 mg/L
45
0,115 0,12 0,125 0,13 0,135 0,14
495 500 505 510 515 520 525
A
bso
rba
nsi
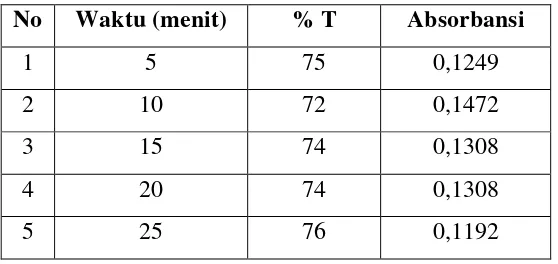
Lampiran 3. Data Penentuan Waktu Operasi dari Larutan Standar Fe(NH4)2(SO4)2.6H2O 0,8 mg/L
No Waktu (menit) % T Absorbansi
1 5 75 0,1249
2 10 72 0,1472
3 15 74 0,1308
4 20 74 0,1308
5 25 76 0,1192
Lampiaran 4. Gambar grafik penentuan waktu operasi larutan seri standar Fe(NH4)2(SO4)2.6H2O 0,8 mg/L
46
0 0,02 0,04 0,06 0,08 0,1 0,12 0,14 0,16
0 5 10 15 20 25 30
A
bso
rba
nsi
4 2 4 2 2
No Konsentrasi % T Absorbansi
1 0,6 79 0,1024
2 0,8 74 0,1308
3 1,0 69 0,1612
4 1,2 63 0,2001
5 1,4 59 0,2291
6 1,6 55 0,2596
7 1,8 50 0,3010
8 2,0 47 0,3279
Lampiran 6. Gambar grafik kurva kalibrasi larutan Standar Fe(NH4)2(SO4)2.6H2O
47
Y = 0,1639X + 0,0009 R² = 0,9992
0 0,05 0,1 0,15 0,2 0,25 0,3 0,35
0 0,5 1 1,5 2 2,5
A
bso
rba
nsi
Lampiran 7. Data Hasil Pengukuran Absorbansi Ion Fe Total Sebelum dan setelah Penambahan Arang Tongkol Jagung dan Serbuk Tongkol Jagung
Perlakuan Hasil Pengukuran sebelum penambahan arang / serbuk tongkol jagung
Hasil Pengukuran setelah penambahan
% T Absorbansi Arang Tongkol
Lampiran 8. Data Hasil Pengukuran Turbiditas (Kekeruhan) sebelum dan Setelah Penambahan Arang Tongkol Jagung dan Serbuk Tongkol Jagung
Perlakuan Hasil pengkuran Kekeruhan (NTU) sebelum penambahan
arang / serbuk tongkol jagung
Arang Tongkol Jagung dan Serbuk Tongkol Jagung
Perlakuan Hasil pengkuran pH sebelum penambahan arang / serbuk
tongkol jagung
Hasil pengkuran pH setelah penambahan
Lampiran 10. Data Hasil Pengukuran Berat Kertas Saring sebelum dan Setelah Penambahan Arang Tongkol Jagung dan Serbuk Tongkol Jagung
Perlakuan Hasil Pengukuran sebelum penambahan arang / serbuk
tongkol jagung
Lampiran 11. Data Hasil Pengukuran Berat Gelas Beaker sebelum dan Setelah Penambahan Arang Tongkol Jagung dan Serbuk Tongkol Jagung
Perlakuan Hasil Pengukuran sebelum penambahan arang / serbuk tongkol
jagung
Hasil Pengukuran setelah penambahan Arang Tongkol
Kesehatan R.I No : 416/MENKES/PER/IX/1990
No Parameter Satuan Kadar Maksimum
yang diperbolehkan
4 Chloroform (total isomer)
mg/L 0,007
6 2,4-D mg/L 0,10
7 DDT mg/L 0,03
8 Detergen mg/L 0,5
9 1,2 Dichloroethene mg/L 0,01
10 1,1 Dichloroethene mg/L 0,0003
11 Heptachlor dan Hepctachlor epoxide
mg/L 0,003
12 Hexachlorobenzena mg/L 0,00001
13 Gamma- HCH (Lindane)
mg/L 0,004
14 Methoxychlor mg/L 0,010
15 Pentachloropenol mg/L 0,01
16 Pestisida Total mg/L 0,10
17 2,4,6-trichlorophenol mg/L 0,01
18 Zat Organik (KmnO4) mg/L 10 2 Koliform tinja belum
diperiksa
1 Aktivitas Alpha (Gross Alpha Activity)
Bg/L 0,1
2 Aktivitas Beta (Gross Beta Activity)
Bg/L 1,0
Gambar 1. Alat Turbidimeter
Gambar 2. Alat Spektrofotometer spektonik 20