ISOLASI DAN PENCIRIAN ENZIM PROTEASE
KERATINOLITIK DARI USUS BIAWAK AIR
ARINI MEGIANDARI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
ARINI MEGIANDARI. Isolasi dan Pencirian Enzim Protease Keratinolitik dari
Usus Biawak Air. Dibimbing oleh DONDIN SAJUTHI dan IRMA H SUPARTO.
Enzim protease yang diisolasi dari lapisan atas (mukosa) usus biawak air
(
Varanus salvator
) memiliki aktivitas proteolitik. Penelitian ini bertujuan
mengisolasi dan mencirikan protease dari lapisan mukosa usus biawak air.
Lapisan mukosa usus biawak air (2%) dilarutkan dalam 50mM bufer fosfat
pH 7,0, kemudian disentrifus pada kecepatan 6000 G dan suhu 4 ºC selama 10
menit. Dari hasil sentrifus didapatkan ekstrak kasar enzim, kemudian dilakukan
analisis aktivitas enzim maksinum dengan memanaskan ekstrak pada selang suhu
45–65 ºC dan selang waktu 5–20 menit. Dari hasil analisis aktivitas enzim
maksimum didapatkan pada suhu 55 ºC waktu inkubasi 5 menit untuk sampel
duodenum, jejenum, ileum, dan kolon masing-masing sebesar 4,3482 U/ml,
3,9247, 3,9176 U/ml, dan 3,0353 U/ml. Protease dari ekstrak kasar enzim terdiri
atas tujuh pita dengan ukuran bobot molekul 66,54 kDa, 57,61 kDa, 48,94 kDa,
48,47 kDa, 36,80 kDa, 24,28 kDa, 12,80 kDa. Enzim ini bekerja pada suhu
optimum 55 ºC dan pH optimum 9, serta dihambat oleh ion Ca
2+dan Mg
2+.Uji
in vitro
menggunakan substrat tepung bulu ayam tidak ditemukan adanya suatu
aktivitas keratinolitik.
ABSTRACT
ARINI MEGIANDARI. Isolation and Characterization of Protease Keratinolytic
Enzyme in Water Monitor Lizard Intestine. Supervised by DONDIN SAJUTHI
and IRMA H SUPARTO.
Protease enzyme isolated from mucosa layer in intestine water monitor
lizard (
Varanus salvator
) showed proteolytic activity. Therefore, the purpose of
this research was to isolate and characterize of protease produced by water
monitor lizard intestine.
ISOLASI DAN PENCIRIAN ENZIM PROTEASE
KERATINOLITIK DARI USUS BIAWAK AIR
ARINI MEGIANDARI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Isolasi dan Pencirian Enzim Protease Keratinolitik dari Usus Biawak
Air
Nama : Arini Megiandari
NIM : G44204018
Disetujui
Prof. drh. Dondin Sajuthi, MST, PhD
Dr. dr. Irma H. Suparto, MS
NIP 130 536 684
NIP 131 606 776
Diketahui
Dekan Falkultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Dr. drh. Hasim, DEA
NIP 131 578 806
PRAKATA
Puji dan syukur penulis panjatkan ke hadirat Allah SWT atas segala rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan penelitian dan karya ilmiah ini. Penelitian ini dilaksanakan dari bulan Juni sampai dengan November 2008 dengan judul Isolasi dan Pencirian Enzim Protease Keratinolitik dari Usus Biawak Air. Penelitian di lakukan di Laboratorium Pusat Studi Satwa Primata (PSSP), Lembaga Penelitian dan Pemberdayaan Masyarakat, Institut Pertanian Bogor (IPB).
Penyusunan karya ilmiah ini tidak akan terwujud tanpa bantuan, bimbingan, dan saran dari berbagai pihak. Oleh karena itu dengan selesaainya laporan ini, penulis mengucapkan terima kasih kepada Prof. Drh. Dondin Sajuthi, MST, PhD dan Dr. dr Irma H. Suparto, MS selaku pembimbing yang telah memberikan waktu, bimbingan, saran, dan pengarahan kepada penulis dalam menyelesaikan karya ilmiah ini.. Ucapan terima kasih penulis sampaikan untuk keluargaku tercinta Bapak, Mama, Kakak, Suami, dan Anakku Annindya Luviana Iriani yang telah memberikan dukungan moral maupun material, Bapak mertua, iparku, dan adik sepupuku yang selalu memberikan doa, serta seluruh keluarga besarku di Bogor, Sukabumi, Purworejo, dan Cilacap. Penelitian ini juga tidak lepas dari bantuan beberapa pihak, oleh karena itu penghargaan penulis sampaikan kepada Kak Willy, Bu Eni, Bu Nani, dan semua pegawai PSSP lainnya atas bantuan yang diberikan. Terima kasih penulis ucapkan kepada Dhesti, Tri, Anti, Asnel, Rima, teman-teman Kimia Angkatan 41 lainnya dan angkatan 40 atas diskusi dan masukan-masukan yang sangat berharga. Terima kasih juga penulis sampaikan kepada Kak Eko dan Mas Hery atas bantuannya selama ini.
Semoga karya ilmiah ini bermanfaat.
Bogor, Desember 2008
RIWAYAT HIDUP
Penulis dilahirkan di Bogor pada tanggal 8 Mei 1986 dari ayah Sugiardi dan
ibu Wagiyem. Penulis merupakan putri kedua dari dua bersaudara. Tahun 2006
penulis menikah dan dikaruniai saeorang anak bernama Annindya Luviana Iriani
pada 26 Februari 2007.
Tahun 2004 penulis lulus dari SMU PGRI 4 Bogor dan pada tahun yang sama
penulis lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB.
Penulis diterima di Program Studi Kimia, Departemen Kimia, Fakultas
Matematika dan Ilmu Pengetahuan Alam, IPB.
DAFTAR ISI
Halaman
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN... ix
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Biawak Air (
Varanus salvator
) ... 1
Enzim
Keratinase ... 2
Sodium Dodecyl sulphate Polyacrilamide Gel Electrophoresis ... 3
BAHAN DAN METODE
Bahan dan Alat ... 3
Metode Penelitian
... 4
HASIL DAN PEMBAHASAN
Kadar
Protein ... 5
Ciri
Enzim
Protease... 5
Bobot
Molekul
(SDS-PAGE) ... 8
Uji
In Vitro
Aktivitas Keratinase ... 8
SIMPULAN DAN SARAN
Simpulan... 8
Saran
... 9
DAFTAR PUSTAKA ...
9
DAFTAR GAMBAR
Halaman
1 Biawak air ...
1
2 Pengaruh waktu inkubasi pada aktivitas protease...
5
3 Pengaruh suhu pada aktivitas enzim protease ...
6
4 Pengaruh pH pada aktivitas enzim protease...
6
5 Pengaruh ion logam pada aktivitas enzim protease ...
7
6 Analisis SDS-PAGE ...
8
7 Uji
in vitro
... 8
DAFTAR LAMPIRAN
Halaman
1 Bagan alir penelitian ... 12
2 Prosedur pembuatan pereaksi kimia ... 13
3 Pembuatan kurva standar Bradford... 15
4 Data penentuan aktivitas enzim maksimum ... 16
5 Penentuan aktivitas maksimum ... 17
6
Contoh perhitungan aktivitas enzim... 18
7 Data pengaruh suhu, pH, dan ion logam pada aktivitas enzim maksimum .. 19
PENDAHULUAN
Latar Belakang
Biawak merupakan kelas reptil yang kulitnya banyak dimanfaatkan sebagai bahan perhiasan juga dagingnya sebagai bahan makanan dan dipercaya dapat digunakan untuk obat kulit. Jenis biawak yang paling banyak dimanfaatkan dan dikonsumsi adalah
biawak air (Varanus salvator). Hasil limbah
dari pemanfaatan biawak tersebut belum banyak digunakan seperti bagian organ dalamnya, antara lain saluran cernanya. Biawak merupakan hewan karnivora yang memangsa berbagai jenis burung, ayam, ikan, serta mamalia kecil seperti tikus dan cecurut. Reptil ini memangsa korbannya hidup-hidup termasuk dengan bulunya kemudian hasil pencernaannya dikeluarkan dalam bentuk feses tanpa ada sisa bulu ayam ataupun burung. Hal ini diduga di dalam saluran pencernaannya terdapat suatu zat atau enzim yang dapat menghancurkan bulu tersebut. Komponen utama pada bulu adalah protein keratin yang kaya akan sistein dan sistin. Oleh karena itu diduga terdapat suatu enzim keratinase di dalam saluran cerna biawak.
Keratinase termasuk enzim protease yang merupakan enzim ekstraseluler. Enzim ini dihasilkan di dalam sel tetapi dikeluarkan ke dalam media untuk menghidrolisis dan mendegradasi komponen kompleks menjadi senyawa sederhana yang mudah larut. Enzim keratinase banyak digunakan pada kosmetik dan teknologi kulit. Secara komersial enzim
tersebut dapat diekstraksi dari Streptomyces
frandiae danStreptomyces mikrolavus. Enzim
ini baik sekali untuk memecah ikatan disulfida keratin pada bulu (Winarno 1983). Selain untuk kosmetik, penggunaan enzim banyak digunakan untuk pengolahan limbah dan juga pakan hewan. Contohnya, enzim keratinase ini dapat diaplikasikan pada limbah bulu ayam yang dijadikan tepung bulu ayam sebagai bahan pakan alternatif yang mempunyai kandungan protein tinggi. Enzim keratinase ini ditambahkan agar dapat mendegradasi bulu ayam tersebut. Hal ini karena bulu ayam mengandung keratin yang merupakan protein serat khusus, tidak larut dalam air dan sulit dicerna (Rawn 1989).
Penelitian ini bertujuan mengisolasi dan mengetahui pencirian enzim protease yang mempunyai aktivitas keratinase dari ekstrak kasar lapisan atas (mukosa) usus biawak air. Hasil penelitian ini diharapkan dapat memberi informasi adanya suatu enzim keratinase
dalam saluran cerna biawak sehingga dapat meningkatkan nilai ekonomi dari hewan tersebut.
TINJAUAN PUSTAKA
Biawak Air (Varanus salvator)
Biawak merupakan hewan yang masuk dalam golongan kadal besar, suku biawak-biawakan (varanidae). Biawak dalam bahasa lain disebut sebagai bayawak (Sunda), menyawak atau nyambik (Jawa), berekai
(Madura), dan monitor lizard atau goanna
(Inggris). Biawak banyak macamnya, yang terbesar dan terkenal ialah biawak komodo (V. komodoensis), yang panjangnya dapat
melebihi 3 m.
Hewan berdarah dingin ini kerap ditemui di desa-desa dan perkotaan di Indonesia barat. Jenis biawak yang paling banyak adalah
biawak air dari jenis Varanus salvator.
Habitatnya di sekitar sungai dan rawa karena merupakan hewan yang semi-akuatik, oleh karena itu disebut sebagai biawak air.
Umumnya biawak dewasa mempunyai panjang tubuh (moncong hingga ujung ekor) sekitar 1 m, meskipun ada pula yang dapat mencapai 2.5 m. Bobot badan biawak jantan biasanya lebih besar sampai dua kali lipat dibandingkan betina. Biawak bereproduksi dengan bertelur dan paling tinggi pada bulan April sampai dengan Oktober (Bennet 1998). Ciri-ciri lainnya adalah adanya garis hitam dengan tepian kuning sepanjang tubuhnya dari kepala sampai ekor. Hewan ini biasanya beRwarna kecoklatan (Byers 2000). Gambar 1 memperlihatkan gambar dari biawak air.
Gambar 1 Biawak air (Tan 2001).
Keratin merupakan protein serat yang membentuk rambut, bulu, dan kuku, serta kaya akan sistein dan sistin. Protein ini 14% terdiri dari sistin dan disulfida sebagai
jembatan antar molekul (Moran et al. 1966).
Menurut Lehninger (1995), -keratin kaya akan residu sistin yang dapat memberikan jembatan disulfida di antara rantai polipeptida yang berdekatan. Sistin terdiri atas dua molekul sistein.
Komponen utama pada bulu adalah protein keratin. Adanya ikatan silang yang terbelit dalam bentuk heliks dan saling berhubungan melalui ikatan disulfida, ikatan hidrogen dan interaksi hidrofobik, menyebabkan keratin sangat stabil, tidak larut dalam air, tahan terhadap asam atau basa kuat dan tahan terhadap enzim proteolitik yang disekresikan
oleh kelenjar pencernaan (Lin et al. 1992).
Keratin dapat dipecah menjadi molekul sederhana melalui reaksi kimia dan enzim. Kemudian molekul ini dapat dicerna oleh tripsin dan pepsin.
Tiap molekul protein dalam keratin mempunyai bentuk spiral, yang disebut spiral-- kanan. Kanan menunjukkan arah putaran dalam spiral itu. Tiap putaran spiral mengandung 3,6 residu asam amino. Jarak dari satu kumparan ke kumparan berikutnya adalah 5,4Å. Bentuk spiral ini tidak berubah terutama berkat ikatan hidrogen antara satu gugus amida-karbonil dan suatu gugus NH yang jaraknya 3,6 satuan asam amino. Bentuk spiral ini menghasilkan produk yang kuat, lunak, dan bersifat serat (Girindra 1986). Ikatan hidrogen antara suatu gugus asam amino dengan suatu gugus karboksil merupakan suatu penyumbang pada bentuk suatu molekul protein. Interaksi inter dan antar molekul juga menentukan struktur (Wijaya 2001).
Enzim adalah biokatalis yang diproduksi oleh sel hidup. Enzim mengkatalis reaksi biokimia spesifik pada substrat dan sering kali banyak enzim yang berbeda dibutuhkan sehingga terbentuk kerja sama dan keberhasilan reaksi metabolik yang dilakukan sel (Wijaya 2001).
Faktor yang mempengaruhi aktivitas enzim adalah pH, suhu, konsentrasi substrat, konsentrasi enzim, dan waktu inkubasi. Suhu meningkatkan aktivitas enzim sampai suhu optimum, setelah itu protein enzim akan terdenaturasi dan terjadi inaktivasi. Begitu pula halnya dengan pH, pada pH optimum aktivitasnya akan maksimum, sedangkan diluar pH optimum aktivitasnya akan turun. Konsentrasi substrat dan enzim, juga waktu
inkubasi yang bertambah akan meningkatkan aktivitas enzim sampai tingkat tertentu, setelah itu aktivitasnya tetap (Sears & Walsh 1993).
Klasifikasi enzim berdasarkan jenis reaksi yang dikatalisis terdiri atas enam kelompok, yaitu oksidoreduktase, transferase, hidrolase, liase, isomerase, dan ligase (Suhartono 1989). Protease merupakan enzim yang berperan dalam reaksi yang melibatkan pemecahan protein. Enzim ini dalam kerjanya membutuhkan air dan termasuk kelas hidrolase. Enzim protease dihasilkan secara ekstraseluler oleh tanaman, hewan, maupun mikrob, dan mempunyai peranan yang sangat penting dalam metabolisme sel dan keteraturan proses dalam sel (Ward 1983). Keratinase termasuk enzim protease yang merupakan enzim ekstraseluler. Enzim ekstraseluler adalah enzim dihasilkan di dalam sel tetapi dikeluarkan ke dalam media untuk menghidrolisis dan mendegradasi komponen kompleks menjadi senyawa sederhana yang mudah larut dan diserap oleh mikroorganisme. Enzim intraseluler dihasilkan di dalam sel dan melakukan aktivitasnya juga didalam sel. Enzim protease berdasarkan cara kerjanya dapat digolongkan dalam dua kelompok besar yaitu endopeptidase dan eksopeptidase (Winarno 1983).
Menurut Kim et al. (1992) aktivitas
keratinase dapat dideteksi dengan memakai kultur supernatan yang mengandung endapan amonium sulfat. Enzim ini melakukan aktivitas hidrolitik terhadap bulu secara optimal pada suhu 45°C dengan pH 8,5.
Sodium Dodecyl sulphate Polyacrilamide Gel Electrophoresis (SDS-PAGE)
Elektroforesis adalah teknik pemisahan komponen-komponen dengan pengaruh arus listrik (dalam medan listrik) sehingga terjadi laju perpindahan. Jika suatu zat bermuatan diberi potensial, maka zat tersebut akan berpindah sepanjang medium yang kontinu ke arah katode atau anode sesuai dengan muatan yang dibawanya. Menurut Khopkar (1990), elektroforesis diklasifikasikan menjadi tiga
kelompok utama, yaitu elektroforesis Free
Boundary, elektroforesis zona/wilayah dan
elektroforesis kontinu.
ISOLASI DAN PENCIRIAN ENZIM PROTEASE
KERATINOLITIK DARI USUS BIAWAK AIR
ARINI MEGIANDARI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
ARINI MEGIANDARI. Isolasi dan Pencirian Enzim Protease Keratinolitik dari
Usus Biawak Air. Dibimbing oleh DONDIN SAJUTHI dan IRMA H SUPARTO.
Enzim protease yang diisolasi dari lapisan atas (mukosa) usus biawak air
(
Varanus salvator
) memiliki aktivitas proteolitik. Penelitian ini bertujuan
mengisolasi dan mencirikan protease dari lapisan mukosa usus biawak air.
Lapisan mukosa usus biawak air (2%) dilarutkan dalam 50mM bufer fosfat
pH 7,0, kemudian disentrifus pada kecepatan 6000 G dan suhu 4 ºC selama 10
menit. Dari hasil sentrifus didapatkan ekstrak kasar enzim, kemudian dilakukan
analisis aktivitas enzim maksinum dengan memanaskan ekstrak pada selang suhu
45–65 ºC dan selang waktu 5–20 menit. Dari hasil analisis aktivitas enzim
maksimum didapatkan pada suhu 55 ºC waktu inkubasi 5 menit untuk sampel
duodenum, jejenum, ileum, dan kolon masing-masing sebesar 4,3482 U/ml,
3,9247, 3,9176 U/ml, dan 3,0353 U/ml. Protease dari ekstrak kasar enzim terdiri
atas tujuh pita dengan ukuran bobot molekul 66,54 kDa, 57,61 kDa, 48,94 kDa,
48,47 kDa, 36,80 kDa, 24,28 kDa, 12,80 kDa. Enzim ini bekerja pada suhu
optimum 55 ºC dan pH optimum 9, serta dihambat oleh ion Ca
2+dan Mg
2+.Uji
in vitro
menggunakan substrat tepung bulu ayam tidak ditemukan adanya suatu
aktivitas keratinolitik.
ABSTRACT
ARINI MEGIANDARI. Isolation and Characterization of Protease Keratinolytic
Enzyme in Water Monitor Lizard Intestine. Supervised by DONDIN SAJUTHI
and IRMA H SUPARTO.
Protease enzyme isolated from mucosa layer in intestine water monitor
lizard (
Varanus salvator
) showed proteolytic activity. Therefore, the purpose of
this research was to isolate and characterize of protease produced by water
monitor lizard intestine.
ISOLASI DAN PENCIRIAN ENZIM PROTEASE
KERATINOLITIK DARI USUS BIAWAK AIR
ARINI MEGIANDARI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Isolasi dan Pencirian Enzim Protease Keratinolitik dari Usus Biawak
Air
Nama : Arini Megiandari
NIM : G44204018
Disetujui
Prof. drh. Dondin Sajuthi, MST, PhD
Dr. dr. Irma H. Suparto, MS
NIP 130 536 684
NIP 131 606 776
Diketahui
Dekan Falkultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Dr. drh. Hasim, DEA
NIP 131 578 806
PRAKATA
Puji dan syukur penulis panjatkan ke hadirat Allah SWT atas segala rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan penelitian dan karya ilmiah ini. Penelitian ini dilaksanakan dari bulan Juni sampai dengan November 2008 dengan judul Isolasi dan Pencirian Enzim Protease Keratinolitik dari Usus Biawak Air. Penelitian di lakukan di Laboratorium Pusat Studi Satwa Primata (PSSP), Lembaga Penelitian dan Pemberdayaan Masyarakat, Institut Pertanian Bogor (IPB).
Penyusunan karya ilmiah ini tidak akan terwujud tanpa bantuan, bimbingan, dan saran dari berbagai pihak. Oleh karena itu dengan selesaainya laporan ini, penulis mengucapkan terima kasih kepada Prof. Drh. Dondin Sajuthi, MST, PhD dan Dr. dr Irma H. Suparto, MS selaku pembimbing yang telah memberikan waktu, bimbingan, saran, dan pengarahan kepada penulis dalam menyelesaikan karya ilmiah ini.. Ucapan terima kasih penulis sampaikan untuk keluargaku tercinta Bapak, Mama, Kakak, Suami, dan Anakku Annindya Luviana Iriani yang telah memberikan dukungan moral maupun material, Bapak mertua, iparku, dan adik sepupuku yang selalu memberikan doa, serta seluruh keluarga besarku di Bogor, Sukabumi, Purworejo, dan Cilacap. Penelitian ini juga tidak lepas dari bantuan beberapa pihak, oleh karena itu penghargaan penulis sampaikan kepada Kak Willy, Bu Eni, Bu Nani, dan semua pegawai PSSP lainnya atas bantuan yang diberikan. Terima kasih penulis ucapkan kepada Dhesti, Tri, Anti, Asnel, Rima, teman-teman Kimia Angkatan 41 lainnya dan angkatan 40 atas diskusi dan masukan-masukan yang sangat berharga. Terima kasih juga penulis sampaikan kepada Kak Eko dan Mas Hery atas bantuannya selama ini.
Semoga karya ilmiah ini bermanfaat.
Bogor, Desember 2008
RIWAYAT HIDUP
Penulis dilahirkan di Bogor pada tanggal 8 Mei 1986 dari ayah Sugiardi dan
ibu Wagiyem. Penulis merupakan putri kedua dari dua bersaudara. Tahun 2006
penulis menikah dan dikaruniai saeorang anak bernama Annindya Luviana Iriani
pada 26 Februari 2007.
Tahun 2004 penulis lulus dari SMU PGRI 4 Bogor dan pada tahun yang sama
penulis lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB.
Penulis diterima di Program Studi Kimia, Departemen Kimia, Fakultas
Matematika dan Ilmu Pengetahuan Alam, IPB.
DAFTAR ISI
Halaman
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN... ix
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Biawak Air (
Varanus salvator
) ... 1
Enzim
Keratinase ... 2
Sodium Dodecyl sulphate Polyacrilamide Gel Electrophoresis ... 3
BAHAN DAN METODE
Bahan dan Alat ... 3
Metode Penelitian
... 4
HASIL DAN PEMBAHASAN
Kadar
Protein ... 5
Ciri
Enzim
Protease... 5
Bobot
Molekul
(SDS-PAGE) ... 8
Uji
In Vitro
Aktivitas Keratinase ... 8
SIMPULAN DAN SARAN
Simpulan... 8
Saran
... 9
DAFTAR PUSTAKA ...
9
DAFTAR GAMBAR
Halaman
1 Biawak air ...
1
2 Pengaruh waktu inkubasi pada aktivitas protease...
5
3 Pengaruh suhu pada aktivitas enzim protease ...
6
4 Pengaruh pH pada aktivitas enzim protease...
6
5 Pengaruh ion logam pada aktivitas enzim protease ...
7
6 Analisis SDS-PAGE ...
8
7 Uji
in vitro
... 8
DAFTAR LAMPIRAN
Halaman
1 Bagan alir penelitian ... 12
2 Prosedur pembuatan pereaksi kimia ... 13
3 Pembuatan kurva standar Bradford... 15
4 Data penentuan aktivitas enzim maksimum ... 16
5 Penentuan aktivitas maksimum ... 17
6
Contoh perhitungan aktivitas enzim... 18
7 Data pengaruh suhu, pH, dan ion logam pada aktivitas enzim maksimum .. 19
PENDAHULUAN
Latar Belakang
Biawak merupakan kelas reptil yang kulitnya banyak dimanfaatkan sebagai bahan perhiasan juga dagingnya sebagai bahan makanan dan dipercaya dapat digunakan untuk obat kulit. Jenis biawak yang paling banyak dimanfaatkan dan dikonsumsi adalah
biawak air (Varanus salvator). Hasil limbah
dari pemanfaatan biawak tersebut belum banyak digunakan seperti bagian organ dalamnya, antara lain saluran cernanya. Biawak merupakan hewan karnivora yang memangsa berbagai jenis burung, ayam, ikan, serta mamalia kecil seperti tikus dan cecurut. Reptil ini memangsa korbannya hidup-hidup termasuk dengan bulunya kemudian hasil pencernaannya dikeluarkan dalam bentuk feses tanpa ada sisa bulu ayam ataupun burung. Hal ini diduga di dalam saluran pencernaannya terdapat suatu zat atau enzim yang dapat menghancurkan bulu tersebut. Komponen utama pada bulu adalah protein keratin yang kaya akan sistein dan sistin. Oleh karena itu diduga terdapat suatu enzim keratinase di dalam saluran cerna biawak.
Keratinase termasuk enzim protease yang merupakan enzim ekstraseluler. Enzim ini dihasilkan di dalam sel tetapi dikeluarkan ke dalam media untuk menghidrolisis dan mendegradasi komponen kompleks menjadi senyawa sederhana yang mudah larut. Enzim keratinase banyak digunakan pada kosmetik dan teknologi kulit. Secara komersial enzim
tersebut dapat diekstraksi dari Streptomyces
frandiae danStreptomyces mikrolavus. Enzim
ini baik sekali untuk memecah ikatan disulfida keratin pada bulu (Winarno 1983). Selain untuk kosmetik, penggunaan enzim banyak digunakan untuk pengolahan limbah dan juga pakan hewan. Contohnya, enzim keratinase ini dapat diaplikasikan pada limbah bulu ayam yang dijadikan tepung bulu ayam sebagai bahan pakan alternatif yang mempunyai kandungan protein tinggi. Enzim keratinase ini ditambahkan agar dapat mendegradasi bulu ayam tersebut. Hal ini karena bulu ayam mengandung keratin yang merupakan protein serat khusus, tidak larut dalam air dan sulit dicerna (Rawn 1989).
Penelitian ini bertujuan mengisolasi dan mengetahui pencirian enzim protease yang mempunyai aktivitas keratinase dari ekstrak kasar lapisan atas (mukosa) usus biawak air. Hasil penelitian ini diharapkan dapat memberi informasi adanya suatu enzim keratinase
dalam saluran cerna biawak sehingga dapat meningkatkan nilai ekonomi dari hewan tersebut.
TINJAUAN PUSTAKA
Biawak Air (Varanus salvator)
Biawak merupakan hewan yang masuk dalam golongan kadal besar, suku biawak-biawakan (varanidae). Biawak dalam bahasa lain disebut sebagai bayawak (Sunda), menyawak atau nyambik (Jawa), berekai
(Madura), dan monitor lizard atau goanna
(Inggris). Biawak banyak macamnya, yang terbesar dan terkenal ialah biawak komodo (V. komodoensis), yang panjangnya dapat
melebihi 3 m.
Hewan berdarah dingin ini kerap ditemui di desa-desa dan perkotaan di Indonesia barat. Jenis biawak yang paling banyak adalah
biawak air dari jenis Varanus salvator.
Habitatnya di sekitar sungai dan rawa karena merupakan hewan yang semi-akuatik, oleh karena itu disebut sebagai biawak air.
Umumnya biawak dewasa mempunyai panjang tubuh (moncong hingga ujung ekor) sekitar 1 m, meskipun ada pula yang dapat mencapai 2.5 m. Bobot badan biawak jantan biasanya lebih besar sampai dua kali lipat dibandingkan betina. Biawak bereproduksi dengan bertelur dan paling tinggi pada bulan April sampai dengan Oktober (Bennet 1998). Ciri-ciri lainnya adalah adanya garis hitam dengan tepian kuning sepanjang tubuhnya dari kepala sampai ekor. Hewan ini biasanya beRwarna kecoklatan (Byers 2000). Gambar 1 memperlihatkan gambar dari biawak air.
Gambar 1 Biawak air (Tan 2001).
Keratin merupakan protein serat yang membentuk rambut, bulu, dan kuku, serta kaya akan sistein dan sistin. Protein ini 14% terdiri dari sistin dan disulfida sebagai
jembatan antar molekul (Moran et al. 1966).
Menurut Lehninger (1995), -keratin kaya akan residu sistin yang dapat memberikan jembatan disulfida di antara rantai polipeptida yang berdekatan. Sistin terdiri atas dua molekul sistein.
Komponen utama pada bulu adalah protein keratin. Adanya ikatan silang yang terbelit dalam bentuk heliks dan saling berhubungan melalui ikatan disulfida, ikatan hidrogen dan interaksi hidrofobik, menyebabkan keratin sangat stabil, tidak larut dalam air, tahan terhadap asam atau basa kuat dan tahan terhadap enzim proteolitik yang disekresikan
oleh kelenjar pencernaan (Lin et al. 1992).
Keratin dapat dipecah menjadi molekul sederhana melalui reaksi kimia dan enzim. Kemudian molekul ini dapat dicerna oleh tripsin dan pepsin.
Tiap molekul protein dalam keratin mempunyai bentuk spiral, yang disebut spiral-- kanan. Kanan menunjukkan arah putaran dalam spiral itu. Tiap putaran spiral mengandung 3,6 residu asam amino. Jarak dari satu kumparan ke kumparan berikutnya adalah 5,4Å. Bentuk spiral ini tidak berubah terutama berkat ikatan hidrogen antara satu gugus amida-karbonil dan suatu gugus NH yang jaraknya 3,6 satuan asam amino. Bentuk spiral ini menghasilkan produk yang kuat, lunak, dan bersifat serat (Girindra 1986). Ikatan hidrogen antara suatu gugus asam amino dengan suatu gugus karboksil merupakan suatu penyumbang pada bentuk suatu molekul protein. Interaksi inter dan antar molekul juga menentukan struktur (Wijaya 2001).
Enzim adalah biokatalis yang diproduksi oleh sel hidup. Enzim mengkatalis reaksi biokimia spesifik pada substrat dan sering kali banyak enzim yang berbeda dibutuhkan sehingga terbentuk kerja sama dan keberhasilan reaksi metabolik yang dilakukan sel (Wijaya 2001).
Faktor yang mempengaruhi aktivitas enzim adalah pH, suhu, konsentrasi substrat, konsentrasi enzim, dan waktu inkubasi. Suhu meningkatkan aktivitas enzim sampai suhu optimum, setelah itu protein enzim akan terdenaturasi dan terjadi inaktivasi. Begitu pula halnya dengan pH, pada pH optimum aktivitasnya akan maksimum, sedangkan diluar pH optimum aktivitasnya akan turun. Konsentrasi substrat dan enzim, juga waktu
inkubasi yang bertambah akan meningkatkan aktivitas enzim sampai tingkat tertentu, setelah itu aktivitasnya tetap (Sears & Walsh 1993).
Klasifikasi enzim berdasarkan jenis reaksi yang dikatalisis terdiri atas enam kelompok, yaitu oksidoreduktase, transferase, hidrolase, liase, isomerase, dan ligase (Suhartono 1989). Protease merupakan enzim yang berperan dalam reaksi yang melibatkan pemecahan protein. Enzim ini dalam kerjanya membutuhkan air dan termasuk kelas hidrolase. Enzim protease dihasilkan secara ekstraseluler oleh tanaman, hewan, maupun mikrob, dan mempunyai peranan yang sangat penting dalam metabolisme sel dan keteraturan proses dalam sel (Ward 1983). Keratinase termasuk enzim protease yang merupakan enzim ekstraseluler. Enzim ekstraseluler adalah enzim dihasilkan di dalam sel tetapi dikeluarkan ke dalam media untuk menghidrolisis dan mendegradasi komponen kompleks menjadi senyawa sederhana yang mudah larut dan diserap oleh mikroorganisme. Enzim intraseluler dihasilkan di dalam sel dan melakukan aktivitasnya juga didalam sel. Enzim protease berdasarkan cara kerjanya dapat digolongkan dalam dua kelompok besar yaitu endopeptidase dan eksopeptidase (Winarno 1983).
Menurut Kim et al. (1992) aktivitas
keratinase dapat dideteksi dengan memakai kultur supernatan yang mengandung endapan amonium sulfat. Enzim ini melakukan aktivitas hidrolitik terhadap bulu secara optimal pada suhu 45°C dengan pH 8,5.
Sodium Dodecyl sulphate Polyacrilamide Gel Electrophoresis (SDS-PAGE)
Elektroforesis adalah teknik pemisahan komponen-komponen dengan pengaruh arus listrik (dalam medan listrik) sehingga terjadi laju perpindahan. Jika suatu zat bermuatan diberi potensial, maka zat tersebut akan berpindah sepanjang medium yang kontinu ke arah katode atau anode sesuai dengan muatan yang dibawanya. Menurut Khopkar (1990), elektroforesis diklasifikasikan menjadi tiga
kelompok utama, yaitu elektroforesis Free
Boundary, elektroforesis zona/wilayah dan
elektroforesis kontinu.
akrilamida dengan N’N’-metilen bis-akrilamida sehingga terbentuk ikatan silang karena polimerisasi akrilamida sendiri hanya menghasilkan ikatan linear yang tidak membentuk gel kaku (Girindra 1993).
Polimerisasi dapat terjadi dengan cepat pada suhu kamar dengan adanya katalis dan inisiator. Katalis dan inisiator yang umum digunakan adalah N,N,N’,N’-tetrametiletilendiamin (TEMED) dan ammonium persulfat (APS) yang berperan sebagai sumber radikal bebas yang akan menginisiasi pembentukan polimer (Girindra 1993). Pada metode ini, digunakan sodium dodesil sulfat (SDS) dan 2-merkaptoetanol. Sodium Dodesil Sulfat (SDS) merupakan detergen anionik yang bersama dengan 2-merkaptoetanol dan pemanasan menyebabkan rusaknya struktur tiga dimensi protein menjadi konfigurasi acak. Hal ini disebabkan karena pecahnya ikatan disulfida yang selanjutnya tereduksi menjadi gugus-gugus sulfhidrin (Girindra 1993).
Bufer tris digunakan dalam proses elektroforesis SDS-PAGE ini. Bufer tris berfungsi sebagai medium penyangga untuk mengarahkan dan mengatur arus, juga digunakan sebagai pelarut materi sampel. Jadi, arus antara elektrode diatur oleh ion sampel dan bufer dalam larutan, sedangkan arus lainnya diatur oleh elektron (Girindra 1993). Pergerakan partikel di dalam media tergantung pada ukuran partikel dan ukuran media penunjang. Ukuran pori dari gel akan ditentukan oleh konsentrasi gel poliakrilamida. Protein yang besar mempunyai mobilitas yang lebih lambat dibandingkan dengan kompleks protein yang lebih kecil. Bobot molekul protein dapat ditentukan dengan kalibrasi menggunakan standar protein yang sudah diketahui bobot molekulnya. Teknik elektroforesis gel banyak digunakan baik di bidang kimia maupun biokimia karena memiliki banyak keuntungan, diantaranya memiliki daya resolusi tinggi, sederhana, dan mudah dibawa (Girindra 1993).
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah usus biawak air dewasa ukuran 1 m, akrilamida, bis-akrilamida, buffer Tris-HCl pH 8.8 dan 6.8, buffer fosfat 50 mM pH 7, larutan buffer universal pH 3-12, tirosin 5 mM, TCA (trichloro acetic acid) 0.1 M, Na2CO3 0.4 M,
kasein Hammarsten, pereaksi Folin-Ciocalteau, bovine serum albumin (BSA) fraksi v, pereaksi Bradford, bulu ayam, TEMED (N,N,N’,N’-tetrametiletilendiamina), larutan SDS 10% (b/v), glisin, gliserol 50% (v/v), larutan 2-merkaptoetanol, ammonium
persulfat, marker low molecular weight
(LMW) (Bio-Rad), bromfenol biru 1% (b/v),
coomassie brilliant blue R-250, metanol, asam
asetat glasial, dan NaCl, KCl, MgCl2, CaCl2.
Alat-alat yang digunakan Spektronik (Hexios), perangkat sel SDS-PAGE (Bio-Rad), sentrifus mikro berpendingin (Beckman), tabung eppendorf, mikroskop fotostereo (Labophot-2 Nikon).
Metode Penelitian
Ekstraksi dan preparasi sampel usus
Usus biawak air dicuci dengan akuades dan diidentifikasi bagian-bagian ususnya. Kemudian dibelah dan dipotong sesuai bagiannya, yaitu duodenum, jejenum, ileum, dan kolon sehingga terlihat bagian dalamnya. Bagian dalam usus dikerok dengan hati-hati untuk memperoleh lapisan atas usus (mukosa) Lapisan atas usus (mukosa) (2% v/v) dilarutkan dalam 50 mM bufer fosfat pH 7,0 dan diaduk dengan vorteks selama satu menit. Kemudian larutan tersebut dipisahkan dengan sentrifus pada kecepatan 6000 G dan suhu 4 °C selama 10 menit. Supernatan yang diperoleh berupa ekstrak enzim. Ekstrak enzim ini merupakan ekstrak kasar dari usus yang kemudian digunakan untuk pencirian enzim keratinase.
Kadar protein
Kadar protein ditentukan dengan metode
Bradford (1976), menggunakan bovine serum
albumin (BSA) sebagai standar protein.
Sebanyak 100 µl enzim ditambahkan ke dalam tabung yang berisi 1ml akuades dan 1 ml pereaksi Bradfofd. Perlakuan pada blanko, larutan enzim diganti dengan akuades. Selanjutnya larutan tersebut diaduk dengan vorteks dan didiamkan selama 20 menit pada suhu ruang. Absorbans larutan diukur pada panjang gelombang 595 nm.
Kurva standar protein menggunakan BSA Fraksi V dengan kisaran konsentrasi 0,1–1,0 mg/ml. Konsentrasi protein enzim ditentukan berdasarkan persamaan garis linier hubungan antara konsentrasi standar protein dan absorbansi.
Pencirian enzim protease diuji secara kuantitatif dengan metode spektrofotometri (Bregmeyer 1983) meliputi: pengaruh suhu, pengaruh pH, dan pengaruh ion logam serta SDS-PAGE untuk menentukan bobot molekul pita protein
Analisis aktivitas protease
Aktivitas protease diukur secara kuantitatif dengan metode Bergmeyer (1983) dengan menggunakan substrat kasein Hammarsten (2% b/v). Ada tiga perlakuan analisis yang dilakukan, yaitu blanko, standar, dan sampel. Sebanyak 50 µl larutan enzim ditambahkan ke dalam tabung eppendorf yang berisi 250 µl kasein 2% b/v dan 250 µl bufer fosfat 50 mM, pH 7. Perlakuan pada blanko dan standar, larutan enzim digantikan dengan akuades dan tirosin 5 mM.
Larutan tersebut diinkubasi pada suhu 55 °C selama 5 menit (suhu dan waktu inkubasi optimum enzim). Reaksi hidrolisis dihentikan dengan cara penambahan 500 µl TCA 0,1 M. Pada blanko dan standar ditambahkan 50 µl larutan enzim, sedangkan pada sampel ditambahkan 50 µl akuades. Selanjutnya, larutan diinkubasi kembali pada suhu 37 °C selama 10 menit, dilanjutkan dengan sentrifus pada kecepatan 6000 G dan suhu 4 °C selama 10 menit.
Sebanyak 375 µl supernatan ditambahkan ke dalam tabung berisi 1,25 ml Na2CO3 0,4 M
dan 250 µl pereaksi Folin-Ciocalteau, lalu diinkubasi kembali pada suhu 37 °C selama 20 menit. Absorbans larutan diukur pada panjang gelombang 578 nm. Satu unit aktivitas protease didefinisikan sebagai jumlah enzim yang dapat menghasilkan 1 µmol produk tirosin per menit pada kondisi pengukuran. Aktivitas enzim diukur berdasarkan persamaan berikut:
Aktivitas protease (U/ml) =
asi waktuinkub enceran faktorpeng Ablanko dar As Ablanko Asampel Χ − − tan
Pengaruh suhu terhadap enzim
Penentuan suhu optimum dilakukan dengan uji aktivitas enzim pada berbagai suhu (45 65 °C) dalam 50mM bufer fosfat pH 7,0 selama 0–20 menit, lalu disentrifugasi pada kecepatan 6000 G dan suhu 4 °C selama 10 menit. Supernatan berupa filtrat enzim diuji aktivitasnya secara kuantitatif.
Pengaruh pH terhadap enzim
Optimasi pH enzim dilakukan pada suhu optimum dengan cara analisis aktivitas enzim dengan menggunakan bufer universal pH
12.
Pengaruh ion logam terhadap enzim
Pengaruh aktivitas protease terhadap ion logam ditentukan dengan cara inkubasi 100 µl enzim dan 100 l larutan ion logam dengan konsentrasi akhir 5 mM selama 1 jam pada suhu ruang, lalu dianalisis aktivitas proteinnya secara kuantitatif. Ion logam yang digunakan yaitu NaCl, MgCl2, CaCl2, KCl.
SDS-PAGE
Analisis SDS-PAGE bertujuan mengetahui berapa banyak pita yang muncul pada gel (kualitatif) dan untuk menentukan nilai bobot molekul dari pita yang terbentuk (kuantitatif).
Tahapan kerja yang dilakukan dalam analisis SDS-PAGE meliputi: preparasi gel pemisah dan penahan, preparasi sampel dan
loading, kondisi running, pewarnaan gel, dan
pelunturan warna
Preparasi gel pemisah dan gel penahan
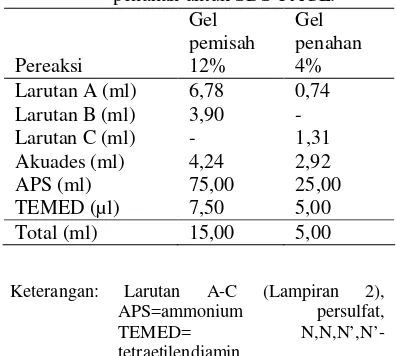
Pembuatan gel pemisah 12% dan gel penahan 4% untuk SDS-PAGE dilakukan dengan komposisi yang tertera pada Tabel 1.
Tabel 1 Komposisi gel pemisah dan gel penahan untuk SDS-PAGE.
Keterangan: Larutan A-C (Lampiran 2), APS=ammonium persulfat, TEMED= N,N,N’,N’-tetraetilendiamin.
Preparasi sampel danloading
Khusus SDS-PAGE, sebanyak 20 µl sampel ditambahkan dengan 10 µl bufer sampel yang mengandung 2-merkaptoetanol, lalu dipanaskan pada suhu 100 °C selama 2-5 menit, volume marker LMW yang digunakan adalah 10 µl.
Pereaksi Gel pemisah 12% Gel penahan 4%
Larutan A (ml) 6,78 0,74
Larutan B (ml) 3,90
-Larutan C (ml) - 1,31
Akuades (ml) 4,24 2,92
APS (ml) 75,00 25,00
TEMED (µl) 7,50 5,00
Kondisi running, pewarnaan, dan pelunturan warna
Gel dijalankan (running) pada tegangan
150 V selama 1 jam dalam bufer elektroforesis. Pada SDS-PAGE, setelah elektroforesis, gel langsung diwarnai dengan
larutan pewarna (coomassie brilliant blue
R-250) selama 15 menit. Pelunturan warna pada gel dilakukan dengan larutan peluntur (metanol, asam asetat glasial, akuades) berulang kali hingga didapatkan pita protein biru dengan latar belakang gel tidak bewarna.
UjiIn Vitro Aktivitas Keratinase
Uji in vitro dilakukan dengan
menggunakkan substrat bulu ayam yang dibuat tepung dan dilakukan pengenceran pada substrat tersebut untuk uji aktivitas dari enzim keratinase.
Persiapan substrat tepung bulu ayam
Bulu ayam dicuci bersih dan dijemur dengan menggunakan sinar matahari sampai kering. Setelah kering bulu ayam digiling sampai halus sehingga didapatkan tepung bulu ayam yang dapat digunakan sebagai substrat
Uji aktivitas keratinase secara in vitro
Uji ini dilakukan penganceran sustrat tepung bulu ayam dengan konsentrasi akhir 1%, 0,5%, 0,25%,0,125% yang ditambahkan 0,5 ml ekstrak kasar enzim dari lapisan mukosa usus biawak air kemudian diinkubasi selama 1 jam dan 3 jam yang kemudian dilihat menggunakan mikroskop.
HASIL DAN PEMBAHASAN
Kadar Protein Ekstrak Kasar UsusV. salvator
Penentuan kadar protein berdasarkan metode Bradford (1976), dengan menggunakan BSA sebagai standar protein. Hasil analisis kadar protein untuk masing-masing bagian usus, yaitu duodenum, jejenum, ileum, kolon didapatkan kadar protein masing-masing sebesar 1,6956 mg/ml, 1,4615 mg/ml, 1,3946 mg/ml, dan 0,5585 mg/ml. Hasil ini menunjukkan adanya suatu protein di dalam ekstrak kasar lapisan mukosa usus biawak air. Kandungan protein yang tertinggi pada bagian duodenum.
Ciri Enzim Protease
Pencirian enzim protease diuji secara kuantitatif dengan metode Bergmeyer (1983) yang meliputi pengaruh suhu, pengaruh pH, pengaruh ion logam serta SDS-PAGE untuk
menentukan bobot molekul dari pita protein enzim.
Analisis aktivitas enzim protease
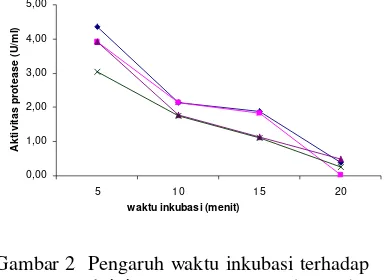
Penentuan aktivitas enzim protease maksimum dilakukan pada suhu optimum dan waktu optimum. Pengaruh waktu inkubasi pada suhu 55 °C dapat dilihat pada Gambar 2.
0,00 1,00 2,00 3,00 4,00 5,00
5 10 15 20
waktu inkubasi (menit)
Aktivi ta s pro teas e (U/ m l)
Gambar 2 Pengaruh waktu inkubasi terhadap aktivitas protease pada suhu
optimum dengan = duodenum,
= jejenum, = ileum, x =
kolon.
Aktivitas enzim protease tertinggi pada waktu inkubasi 5 menit dengan suhu 55 ºC (Gambar 2). Aktivitas enzim protease maksimum didapatkan untuk sampel duodenum, jejenum, ileum, dan kolon masing-masing sebesar 4, 3482 U/ml, 3,9247 U/ml, 3,9176 U/ml, dan 3,0353U/ml. Sedangkan aktivitas enzim spesifik duodenum, jejenum, ileum, dan kolon adalah 2,5643 U/mg, 2,68532 U/mg, 2,6090 U/mg, dan 5,4344 U/mg. Semakin bertambahnya waktu inkubasi terlihat bahwa aktivitas dari enzim menurun hingga pada waktu inkubasi 20 menit aktivitas enzim mendekati nol atau hampir tidak adanya aktivitas dari enzim tersebut. Menurut Rahayuet al. (1989) prinsip
kerja metode ini, yaitu substrat kasein akan terhidrolisis oleh protease dengan menggunakan bantuan air menjadi peptida dan asam amino.
Laju pembentukan peptida dan asam amino tersebut dapat dijadikan tolok ukur aktivitas katalisis protease. Asam amino yang terbentuk harus dipisahkan dari substrat yang tidak terhidrolisis. Umumnya pemisahan ini dilakukan dengan penambahan TCA (trichloro acetic acid) menyebabkan produk
protease. Asam-asam amino tirosin dan triptofan yang larut dalam TCA akan bereaksi dengan reagen folin menghasilkan warna biru.
Penambahan Na2CO3 bertujuan untuk
mendapatkan pH sekitar 11,5 yang merupakan pH optimum untuk intensitas dan stabilitas warna (Novo 1981). Warna yang terbentuk diukur absorbansinya pada daerah sinar tampak 578 nm. Besarnya serapan berbanding lurus dengan konsentrasi protein yang terhidrolisis.
Pengaruh suhu terhadap enzim
Umumnya setiap enzim memiliki aktivitas maksimum pada suhu tertentu, aktivitas enzim akan semakin meningkat dengan bertambahnya suhu hingga suhu optimum tercapai. Setelah itu kenaikan suhu lebih lanjut akan menyebabkan aktivitas enzim menurun. Pengaruh suhu terthadap enzim protease ekstrak kasar lapisan atas (mukosa) usus biawak air dapat dilihat pada Gambar 3.
0,00 1,00 2,00 3,00 4,00 5,00
45 55 65
suhu (C) akti vitas pro tease (U/ ml )
Gambar 3 Pengaruh suhu terhadap aktivitas
enzim protease, dengan =
duodenum, = jejenum, = ileum,x= kolon.
Aktivitas enzim protease kasar dari lapisan mukosa usus biawak air yang tertinggi terdapat pada suhu 55 °C. Suhu optimum
enzim dari bakteriMicrobacteriumsp adalah
50 °C(Thys & Brandelli 2006), 55 °C dari
bakteri Chryseobacterium sp. (Riffel et al.
2003) dan 60 °C dari bakteri Bacillus
licheniformis (Suntornsuket al. 2004).
Untuk kebanyakan enzim, suhu optimum adalah suhu sel atau di atas sel tempat enzim-enzim berada. Kenaikan kecepatan aktivitas enzim di bawah suhu optimum disebabkan oleh kenaikan energi kinetik molekul-molekul yang bereaksi. Akan tetapi bila suhu tetap dinaikkan terus, energi kinetik molekul-molekul enzim menjadi demikian besar sehingga melampaui penghalang energi untuk memecahkan ikatan-ikatan sekunder yang
mempertahankan enzim dalam keadaan aslinya atau keadaan katalitik enzim aktif. Akibatnya struktur sekunder dan tersier hilang disertai hilangnya aktivitas biologi (Harper 1979).
Suhu mempengaruhi laju reaksi katalisis enzim dengan dua cara. Pertama, kenaikan suhu akan meningkatkan energi molekul substrat dan pada akhirnya meningkatkan laju reaksi enzim. Peningkatan suhu juga berpengaruh terhadap perubahan konformasi substrat sehingga sisi reaktif substrat mengalami hambatan untuk memasuki sisi aktif enzim dan menyebabkan turunnya aktivitas enzim.
Kedua, peningkatan energi termal molekul yang membentuk struktur protein enzim itu sendiri akan menyebabkan rusaknya interaksi-interaksi non kovalen (ikatan hidrogen, interaksi van der Waals, interaksi hidrofobik, dan interaksi elektrostatik) yang menjaga struktur 3 dimensi enzim secara bersama-sama sehingga enzim mengalami denaturasi. Denaturasi menyebabkan struktur lipatan enzim membuka pada bagian permukaannya sehingga sisi aktif enzim berubah dan terjadi penurunan aktivitas enzim (Hames & Hooper 2000).
Pengaruh pH terhadap enzim
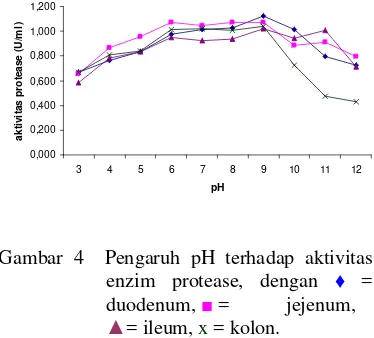
Semua reaksi enzim dipengaruhi oleh pH medium tempat reaksi terjadi. Sebab itulah, pada setiap percobaan dengan enzim diperlukan bufer untuk mengontrol pH reaksi. Pengaruh enzim protease terhadap pH dapat dilihat pada Gambar 4.
0,000 0,200 0,400 0,600 0,800 1,000 1,200
3 4 5 6 7 8 9 10 11 12 pH aktivi tas pro tease (U/m l)
Gambar 4 Pengaruh pH terhadap aktivitas
enzim protease, dengan =
duodenum, = jejenum, = ileum,x= kolon.
sebesar 1,120 U\ml, 1,048 U/ml, 1,021 U/ml, 0,980 U/ml. Pada pH yang sangat asam (dalam hal ini pH 3) aktivitasnya sangat kecil yang menunjukkan gugus fungsionil pada sisi
aktif enzim terganggu dengan adanya ion H+
yang berlebihan, demikian juga pada pH 4–6. Pada pH 7–9, enzim relatif bekerja lebih maksimum hingga pada pH 9 enzim mencapai tingkat ionisasi yang diinginkan enzim sehingga aktivitas enzim mencapai maksimum. Sedangkan pada pH 10–12 aktivitas relatif enzim mengalami penurunan karena ion OH- yang berlebihan.
Perubahan pH pada skala deviasi kecil menyebabkan turunnya aktivitas enzim sehubungan dengan perubahan ionisasi gugus-gugus fungsionilnya karena pada hakekatnya enzim adalah protein yang tersusun atas asam amino yang dapat mengadakan ionisasi (mengikat) dan melepaskan proton atau ion hidrogen pada gugus amino, karboksil dan gugus fungsionil lainnya. Sebaliknya, pada skala deviasi pH yang besar, perubahan pH akan mengakibatkan enzim mengalami denaturasi sehubungan dengan adanya gangguan terhadap berbagai interaksi non kovalen yang menjaga kestabilan struktur 3 dimensi enzim. Gugus ionik berperan penting dalam menjaga konformasi sisi aktif enzim untuk mengikat dan mengubah substrat menjadi produk (Hames &Hooper 2000). Perubahan pH yang tidak begitu besar mempengaruhi keadaan ion enzim dan sering keadaan ion substrat juga. Bila aktivitas enzim diukur pada berbagai pH, aktivitas optimum umumnya didapatkan antara nilai pH 5,0 dan 9,0. Akan tetapi, beberapa enzim, misalnya pepsin aktif pada nilai pH diluar batas itu. Bentuk kurva aktivitas pH ditetapkan oleh faktor denaturasi enzim pada nilai pH yang sangat tinggi atau rendah dan pengaruh terhadap keadaan muatan listrik sustrat atau enzim. Untuk enzim, perubahan muatan dapat mempengaruhi aktivitas baik dengan perubahan struktur maupun dengan perubahan muatan pada residu asam amino yang berfungsi mengikat substrat atau katalis. Faktor lain yang penting adalah perubahan konformasi enzim bila pH diubah-ubah. Suatu gugus yang bermuatan jauh dari bagian dimana substrat terikat mungkin perlu untuk mempertahankan struktur tersier atau kuartener yang aktif. Bila muatan pada gugus ini diubah, molekul protein dapat terbuka atau menjadi lebih kompak (Harper 1979).
Pada kondisi optimum, aktivitas maksimal protease lapisan mukosa usus biawak air dicapai pada pH 9 (50 mM bufer fosfat).
Enzim keratinase memiliki pH optimum dari bakteriMicrobacteriumsp adalah 7,5 (Thys &
Brandelli 2006), 8,0 dari bakteri
Streptomyces. (Tapia &Contiero 2008) dan
8,5 dari bakteri Bacillus licheniformis
(Suntornsuket al. 2004).
Pengaruh ion logam terhadap enzim
Beberapa enzim membutuhkan ion logam sebagai kofaktor untuk mendukung efisiensi katalitik enzim. Logam tersebut membantu reaksi katalitik dengan cara mengikat substrat pada sisi pemotongan. Selain berperan dalam pengikatan antara enzim dengan substrat, beberapa logam juga dapat mengikat enzim secara langsung untuk menstabilkan konformasi aktifnya atau menginduksi formasi sisi pengikatan atau sisi aktif suatu enzim. Pengaruh ion logam pada enzim keratinase dapat dilihat pada Gambar 5.
0 20 40 60 80 100 120
NaCl CaCl2 MgCl2 KCl Kontrol ion logam ak tivitas re lat if (% )
Gambar 5 Pengaruh ion logam terhadap aktivitas relatif enzim protease,
dengan = duodenum, =
jejenum, = ileum, = kolon.
Pada Gambar 5 menunjukkan CaCl2 dan
MgCl2 sama-sama menghambat dengan kuat
aktivitas ekstrak kasar hingga aktivitas relatifnya kurang dari 15%. Sedangkan untuk NaCl dan KCl tidak menghambat aktivitas ekstrak kasar enzim. Pada NaCl sampel jejenum dan ileum menghambat lemah aktivitas ekstrak kasar enzim. Hal ini
disebabkan Ca2+ dan Mg2+ merupakan ion
divalen yang memiliki bilangan koordinasi yang lebih besar daripada ion logam
monovalen, yaitu Na+ dan K+ sehingga
mengubah konformasi dan sisi aktif enzim menjadi berubah. Menurut Thys dan Brandelli
(2006) Zn2+ dan Mg2+ menghambat aktivitas
enzim keratinase dari bakteriMicrobacterium
sp., sedangkan menurut Tapia dan Contiero
(2008) CaCl2, ZnCl2, dan BaCl2 sedikit
menghambat enzim keratinase dari bakteri
Bobot molekul (SDS-PAGE)
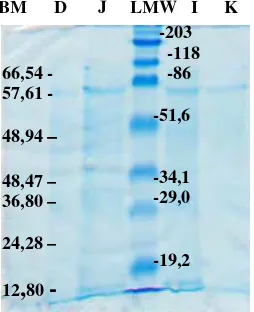
Penentuan bobot molekul dari masing-masing pita protein pada ekstrak kasar enzim protease dari lapisan mukosa usus biawak air dengan metode elektroforesis SDS-PAGE 12%. Pada Gambar 6 dapat dilihat hasil elektroforesis SDS-PAGE.
Gambar 6 Analisis SDS-PAGE 12% ekstrak kasar enzim protease dari lapisan
mukosa usus biawak air, dengan
D=duodenum, J=jejenum, I=ileum, K=kolon, BM=bobot molekul, LMW=low molecular weight.
Hasil analisis SDS-PAGE terhadap seluruh bagian usus diperoleh tujuh pita yang sama bobot molekulnya, yaitu 66,54 kDa, 57,61 kDa, 48,94 kDa, 48,47 kDa, 36,80 kDa, 24,28 kDa, dan 12,80 kDa. Hasil ini menunjukkan bahwa jenis protein yang terdapat dalam masing-masing bagian usus adalah sama.
Menurut Suntornsuk et al. (2004) bobot
molekul enzim keratinase dari bakteriBacillus licheniformis sebesar 35 kDa. Thys dan
Brandelli (2006) melaporkan bahwa bobot molekul enzim keratinase dari bakteri
Microbacterium sp. adalah sebesar 42 kDa,
sedangkan menurut Bockleet al. (1995) bobot
molekul enzim keratinase dari bakteri
Streptomyces pactum sebesar 30 kDa. Bobot
molekul enzim protease pada mukosa usus biawak air yang kemungkinan suatu keratinase adalah antara 24,28 kDa sampai dengan 48,94 kDa.
Ujiin vitro aktivitas keratinase
Aktivitas dari enzim keratinase pada ekstrak kasar dari lapisan mukosa usus biawak
air (Varanus salvator) diuji in-vitro
menggunakan tepung bulu ayam sebagai substrat yang kemudian di inkubasi pada suhu
55 ºC selama 1 jam dan 3 jam. Pada jam pertama dan ketiga dilakukan pengamatan menggunakan mikroskop dengan pembesaran 40 kali. Hasil foto dengan mikroskop dapat dilihat pada Gambar 7.
KN KP 1,00% 0,50% 0,25% 0,12%
Gambar 7 Uji in-vitro aktivitas
keratinase dengan berbagai konsentrasi tepung bulu ayam sebagai substrat yaitu 1%; 0,50%; 0,25; 0,12% pada inkubasi 1 jam KN=kontrol negatif, KP=kontrol positif, pembesaran 40 .
Hasil pengamatan uji in vitro untuk
aktivitas keratinase menunjukkan tidak adanya perubahan atau lisis dari tepung bulu ayam sebagai substrat dengan berbagai konsentrasi yang ditambahkan ekstrak kasar enzim lapisan mukosa usus biawak air. Demikian pula hasil pengamatan pada 3 jam tidak ada perubahan aktivitas. Hal ini menandakan tidak ditemukan adanya suatu aktivitas enzim keratinase.
SIMPULAN DAN SARAN
Simpulan
Pencirian ekstrak kasar enzim protease pada lapisan atas (mukosa) usus biawak air (Varanus salvator) mempunyai aktivitas
optimum pada suhu 55 °C dan pH 9. Ion-ion yang menghambat aktivitasnya adalah ion Ca2+ dan Mg2+.
Analisis SDS-PAGE ditemukan tujuh pita protein dengan bobot molekul yang berbeda-beda, yaitu 66,54 kDa, 57,61 kDa, 48,94 kDa, 48,47 kDa, 36,80 kDa, 24,28 kDa, 12,80 kDa. Seluruh sampel mempunyai pita yang sama.
Hasil uji in vitro menggunakan substrat
tepung bulu ayam tidak menemukan adanya suatu aktivitas enzim keratinase pada bagian usus biawak air.
BM D J LMW I K
66,54 57,61 -48,94– 48,47 – 36,80 – 24,28 –
12
,
80Saran
Sebaiknya dilakukan penelitian lebih lanjut dengan ekstrak kasar yang dimurnikan, perlu digunakan substrat keratinase, dan perlunya mengisolasi dari bakteri usus biawak air.
DAFTAR PUSTAKA
Bennett D. 1998. Monitor Lizard, Natural
History, Biology and Husbandary 2nd
edition. Frankfurt: Chimaira edition.
Bergmeyer HU, Grassl M. 1983. Methods of
Enzymatic Analysis. Vol 2. Weinheim:
Verlag Chemie. hlm 1007-1009. Bockle B, Galunnsky B, Muller R. 1995.
Characterization of keratinolytic serin protease from Streptomyces pactum DSM 40530. Apll. Environ. Microbiol. 10: 3705–3710.
Bradford MM. 1976. A rapid and sensitive method For quantitation of microgram quantities of protein utilizing the
principle of protein dye-binding. Anal
Biochem 72: 234-254.
Byers D. 2000. Varanus salvator.
http://animaldiversity.Ummz.edu/site/ac counts/information/Varanus_salvator.ht ml. [17 Des 2008].
Girindra A. 1986. Biokimia I. Jakarta: PT
Gramedia Pustaka Utama.
Girindra A. 1993. Immunokimia. Bogor:
PAU-IPB.
Grzimek B. 1996. Grizimek’s Animal Life Encyclopedia. Vol. 6. New York: Nostrand Reinhold Co.
Hames BD, Hooper NM. 2000. Biochemistry: The Instant Notes. Ed. Ke-2. Hongkong: Spingerr-Verlag. Hlm 83– 84.
Harper H, Rodwel VW, Mayes PA. 1979. Biokimia. Jakarta: Buku Kedokteran EGC.
Khopkar SM. 1990. Konsep Dasar Kimia
Analitik. Jakarta: UI-Press.
Kim YB, Lee JB, Seong JB, Lee NH. 1992. Effects of physical processing on protein content and pepsin-digestibility
of feather meals. Poult Sci
64:1729-1741.
Lehninger AL. 1995. Dasar-Dasar Biokimia.
Ed. Ke-5. Terjemahan Maggy Thenawidjaja. Jakarta: Erlangga. Lin X, Lee C, Casale ES, Shih JCH. 1992.
Purification and characterization of a keratinase from a feather degrading
Bacillus licherniformis strain. Appl
Environ Microbiol 58:3271-3275. Moran ET, Summers JD, Linger SJ. 1966.
Keratin as a Source for The Growing Chick. 1. Amino acid imbalance as the cause for inferior performance of feather meal and the implication of disulfide bounding in raw feather as the reason for poor digestibility. Poult Sci 45:1257.
Novo. 1981. Novo’s Handbook of Practical Biotechnology. Denmark: Novo. Rahayu PW, Sutrosno D, Sastraatmadja DD.
1989. Produksi Rennet Mikroba dariM.
Pusillus[Laporan Penelitian]. Bogor:
Laboratorium Mikrobiologi Pangan dan Gizi, PAU, IPB.
Rawn JD. 1989.Biochemistry.Ed ke-1. USA:
Neil Patherson.
Riffel A, Lucas F, Heeb P, Brandelli A. 2003. Characterization of a new keratinolytic bacterium that completely degrades native feather keratin. Arc Microbiol 179: 258–265.
Sears A, Walsh G. 1993. Industrial Enzyme Application: using these concepts to match animal, enzyme and substrate in feed industry application, hlm 89-111.
Di dalam the Use of Scientifically
Proyen Natural Product to Increase Practical Value.
Suhartono MT. 1989. Enzim dan
Bioteknologi. Bogor: IPB PAU
Bioteknologi.
Suntornsuk W et al. 2004. Purification and
characterisation of keratinase from a thermotolerant feather-degrading bacterium.
Tan R. 2001.Malayan Water Monitor Lizard.
www.natura.per.sg.
http://www.naturia.per.sg/index.htm [06 Feb 2008].
Tapia D, Contiero J. 2008. Production and partial characterization of keratinase produced by a microorganism isolated from poultry processing plant
wastewater. African Biotechnol .3:
296–300.
Thys RCS, Brandelli A. 2006. Purification and properties of a keratinolytic
metalloprotease from microbacterium
sp.Appl Microbiol. 101: 1259–1268.
Ward OP. 1983. Proteinase. Di dalam WM Fogarty (Ed.) Microbial and Enzyme Biotechnology.Appl Sci.
Neotermes dalbergia[skripsi]. Bogor:
Lampiran 1 Bagan alir penelitian
Biawak air
bagian duodenum,
jejenum, ileum, kolon
Cuci dengan akuades
dan kerok lapisan
atasnya (mukosa
Ekstraksi enzim protease
Analisis aktivitas keratinase
(
in vitro
)
Analisis kadar protein
Pencirian enzim
Lampiran 2 Prosedur pembuatan pereaksi kimia
Pereaksi untuk analisis aktivitas enzim dan kadar protein
•
Kasein Hammarsten 2% b/v
Sebanyak 1 g kasein ditimbang, lalu dilarutkan dalam 40 ml bufer fosfat 50 mM, pH
7,0 kekeruhan larutan dihilangkan dengan penambahan NaOH 1 M, lalu diatur
hingga pH 7 dengan penambahan HCl 1 M dan ditera dengan akuades hingga
volume total 50 ml.
•
Tirosin 5 mM
Sebanyak 0,0453 g tirosin dilarutkan dalam 40 ml akuades dan ditambahkan NaOH
1 M hingga larut, lalu dinetralkan hingga pH 7,0 dengan HCl 1 M. Selanjutnya,
larutan ditera dengan akuades hingga volume 50 ml.
•
TCA 0.1 M
Larutan stok TCA 1 M dibuat dengan cara melarutkan 16,339 g TCA dalam 100 ml
akuades, lalu diaduk dengan pengaduk magnetik hingga homogen. Larutan kerja
TCA 0,1 M dibuat dengan cara mengencerkan 10 ml larutan TCA 1 M dengan
akuades hingga volume 100 ml.
•
Na
2CO
30,4 M
Sebanyak 4,2397 g Na
2CO
3dilarutkan dalam 100 ml akuades, lalu diaduk dengan
pengaduk magnetik hingga homogen.
•
Pereaksi Folin-Ciocalteau (1:2)
Sebanyak 10 ml pereaksi Folin-Ciocalteau diencerkan dengan akuades hingga
volume 30 ml.
•
Pereaksi Bradford
Stok larutan Bradford dibuat dengan cara melarutkan 0,1 g
Coomassie Brilliant Blue
G-250 dalam 50 ml etanol 95% v/v dan 100 ml asam fosfat 85% v/v, lalu ditera
dengan akuades hingga volume 200 ml. Larutan kerja Bradford dibuat dengan cara
mengencerkan 5 ml larutan stok Bradford dengan akuades hingga volume total 50
ml.
Pereaksi untuk analisis SDS-PAGE dan zimografi
•
Larutan A (40% (b/v) akrilamida; 2 % (b/v) bis-akrilamida)
Sebanyak 4,38 ml akrilamida dan 2,40 bis-akrilamida untuk gel pemisah dan
Sebanyak 0,48 ml akrilamida dan 0,26 ml bis-akrilamida untuk gel penahan.
•
Larutan B (bufer gel pemisah, Tris-HCl 1,5 M pH 8,8)
•
Larutan C (bufer gel penahan, Tris-HCl 1,5 M pH 6,8)
Sebanyak 1,26 ml larutan Tris-HCl pH 6,8 dan 50 µl larutan SDS 10% (b/v) untuk
gel penahan.
•
Ammonium persulfat 10% (b/v)
Sebanyak 0,1 g ammonium persulfat dilarutkan hingga homogen dengan 1 ml
akuades.
•
Bufer elektroforesis
Sebanyak 1.803 g Tris, 8,648 g glisin, dan 0,6 g SDS dilarutkan dengan 600 ml
akuades, lalu ditera hingga pH 8,3 dengan HCl 1 M.
•
Bufer sampel
1. SDS-PAGE
Sebanyak 0,3 ml Tris-HCl 1 M pH 6,8, 2,5 ml gliserol 50% (v/v), 1 ml SDS
10% (b/v), 0,25 ml 2-merkaptoetanol, 0,5 ml bromfenol biru 1% (b/v), dan 0,45
ml akuabides sampai volume total 5 ml.
2. Zimografi
Sebanyak 0,5 g SDS, 1 ml gliserol 50% (v/v), 1 ml bromfenol biru 1% (b/v),
0,625 ml Tris-HCl 1 M pH 6,8, dan 2.,75 ml akuabides sampai volume total 5
ml.
•
Larutan pewarna
Sebanyak 0,5 g
Coomassie Brilliant Blue
R-250 dilarutkan dalam campuran 225 ml
metanol, 50 ml asam asetat glasial, dan 225 ml akuades sampai volume total 500 ml.
•
Larutan peluntur
Komposisi larutan peluntur terdiri atas 50 ml metanol, 50 ml asam asetet glasial, dan
400 ml akuades sampai volume total 500 ml.
Larutan berbagai bufer
Lampiran 3 Pembuatan kurva standar Bradford.
y = 0,0299x + 0,0643 R2 = 0,9614
0,000 0,010 0,020 0,030 0,040 0,050 0,060 0,070 0,080 0,090 0,100
0,00 0,20 0,40 0,60 0,80 1,00 1,20
[BSA]m g/m l
Abs
or
bansi
(nm)
Sampel Absorbansi
kadar protein
duodenum 0,115 1,6956
jejenum 0,108 1,4615
ileum 0,106 1,3946
kolon 0,081 0,5585
[BSA] (mg/ml)
Absorbansi (nm)
0,10 0,064
0,20 0,070
0,30 0,074
0,40 0,079
0,50 0,080
0,60 0,082
0,70 0,087
0,80 0,089
0,90 0,090
Lampiran 4 Penentuan absorbansi enzim maksimum protease dari bagian usus biawak
air
Waktu (menit)
A Blanko (nm)
A Standar
(nm) A Sampel (nm)
Duodenum Jejenum Ileum Kolon
5 2,115 2,354 2,783 2,642 2,609 2,616
10 2,291 2,312 2,414 2,396 2,385 2,380
15 2,398 2,429 2,602 2,613 2,481 2,480
20 2,014 2,149 2,512 2,404 2,428 2,413
Suhu 55°C Waktu (menit)
A Blanko (nm)
A Standar
(nm) A Sampel (nm)
Duodenum Jejenum Ileum Kolon
5 2,129 2,299 2,745 2,685 2,684 2,645
10 2,186 2,287 2,548 2,546 2,484 2,479
15 2,150 2,226 2,506 2,497 2,363 2,361
20 2,265 2,468 2,528 2,277 2,596 2,436
Suhu 65°C Waktu (menit)
A Blanko (nm)
A Standar
(nm) A Sampel (nm)
Duodenum Jejenum Ileum Kolon
5 2,118 2,273 2,396 2,332 2,316 2,255
10 2,259 2,326 2,516 2,519 2,559 2,545
15 2,286 2,318 2,345 2,318 2,346 2,359
20 2,167 2,338 2,372 2,329 2,325 2,324
Lampiran 5 Penentuan aktivitas maksimum enzim spesifik dari bagian usus biawak air
Suhu 45
Waktu
(menit) Aktivitas enzim (U/ml) Aktivitas enzim Spesifik (U/mg)
Duodenum Jejenum Ileum Kolon Duodenum Jejenum Ileum Kolon
5 3,3540 2,6460 2,4803 2,5155 1,9780 1,8104 1,7785 4,5038
10 3,5143 3,0000 2,6857 2,5428 2,0725 2,0526 1,9257 4,5527
15 2,6322 2,7742 1,0710 1,0581 1,5523 1,8981 0,7679 1,8944
20 1,1066 0,8666 0,9200 0,8867 0,6526 0,5929 0,6597 1,5875
Suhu 55 Waktu
(menit) Aktivitas enzim (U/ml) Aktivitas enzim Spesifik (U/mg)
Duodenum Jejenum Ileum Kolon Duodenum Jejenum Ileum Kolon
5 4,3482 3,9247 3,9176 3,0353 2,5643 2,6853 2,8091 5,4345
10 2,1505 2,1386 1,7703 1,7406 1,2682 1,4633 1,2693 3,1164
15 1,8737 1,8263 1,1215 1,1105 1,1050 1,2496 0,8041 1,9883
20 0,3887 0,0177 0,4892 0,2527 0,2292 0,0121 0,3507 0,4525
suhu 65 Waktu
(menit) Aktivitas enzim (U/ml) Aktivitas enzim Spesifik (U/mg)
Duodenum Jejenum Ileum Kolon Duodenum Jejenum Ileum Kolon
5 2,1523 1,6567 1,5330 1,0606 1,2693 1,1335 1,0992 1,8990
10 2,3015 2,3284 2,6865 2,5612 1,3573 1,5931 1,9263 4,5856
15 0,7375 0,4000 0,7500 0,9125 0,4349 0,2737 0,5378 1,6338
Lampiran 6 Contoh perhitungan aktivitas enzim (U/ml) dan aktivitas spesifik (U/mg).
Perhitungan aktivitas enzim (U/ml)
Aktivitas protease (U/ml) =
asi waktuinkub
enceran faktorpeng
Ablanko dar
As
Ablanko Asampel
Χ −
− tan
Contoh perhitungan pada suhu 45 °C selama 5 menit sampel duodenum Aktivitas keratinase (U/ml) =
5
6
115
,
2
351
,
2
115
,
2
783
,
2
Χ
−
−
=3,3540 U/ml
Perhitungan kadar protein (mg/ml)
Persamaan dari kurva standar:
y = 0,0299x + 0,0643 x = [BSA] mg/ml Y = Absorbansi (nm) Contoh perhitungan pada sampel duodenum dengan nilai absorbansi 0,115
y = 0,0299x + 0,0643 0,115 = 0,0299x + 0,0643 x = 1,6356 mg/ml
[protein] (mg/ml) = 1,6356 mg/ml
Perhitungan aktivitas spesifik enzim (U/mg) Aktivitas Enzim spesifik (U/mg) =
)
/
](
[Pr
)
/
(
ml
mg
otein
mg
U
nzim
aktivitase
Contoh perhitungan pada suhu 45 °C selama 5 menit sampel duodenum Aktivitas Enzim Spesifik (U/mg) =
6356
,
1
3540
,
3
Lampiran 7 Data Pengaruha Suhu, pH dan ion logam pada aktivitas enzim maksimum dari ekstrak kasar enzim protease lapisan atas (mukosa) usus biawak air (Varanus salvator).
Pengaruh suhu
Suhu (°C)
Blanko (nm)
Standar
(nm) Sampel (nm) Aktivitas enzim (U/ml)
Duodenum Jejenum Ileum Colon Duodenum Jejenum Ileum Colon
45 2,115 2,354 2,783 2,642 2,609 2,616 3,354 2,6460 2,4803 2,5154
55 2,129 2,299 2,745 2,685 2,684 2,645 4,3482 3,9247 3,9176 3,0353
65 2,118 2,273 2,396 2,332 2,316 2,255 2,1523 1,6568 1,5329 3,0353
Pengaruh pH
pH
Blanko (nm)
Standar
(nm) Sampel (nm) Aktivitas enzim (U/ml)
Duodenum Jejenum Ileum Colon Duodenum Jejenum Ileum Colon
3 1,340 1,980 1,696 1,689 1,652 1,695 0,668 0,654 0,585 0,666
4 1,307 1,932 1,705 1,759 1,715 1,727 0,764 0,868 0,783 0,806
5 1,275 1,981 1,767 1,836 1,765 1,770 0,836 0,954 0,833 0,841
6 1,283 1,941 1,818 1,871 1,803 1,838 0,976 1,072 0,948 1,012
7 1,301 1,979 1,873 1,893 1,823 1,879 1,012 1,048 0,924 1,023
8 1,362 1,982 1,892 1,918 1,846 1,883 1,026 1,076 0,937 1,008
9 1,217 2,116 2,056 2,002 1,982 1,998 1,120 1,048 1,021 1,042
10 1,328 1,984 1,883 1,813 1,844 1,724 1,015 0,887 0,944 0,724
11 1,285 1,935 1,716 1,780 1,831 1,542 0,796 0,914 1,008 0,474
12 1,266 1,996 1,708 1,750 1,699 1,529 0,727 0,796 0,712 0,432
Pengaruh ion logam
ion
Blanko (nm)
Standar
(nm) Sampel (nm) Aktivitas enzim (U/ml)
Duedenum Jejenum Ileum Colon Duedenum Jejenum Ileum Colon
NaCl 0,095 0,313 0,164 0,134 0,153 0,132 0,0317 0,0179 0,0266 0,0170
Cacl2 0,064 0,239 0,068 0,066 0,073 0,069 0,0023 0,0011 0,0051 0,0029
MgCl2 0,097 0,325 0,101 0,102 0,098 0,104 0,0018 0,0022 0,0004 0,0031
KCl 0,071 0,321 0,148 0,141 0,132 0,112 0,0308 0,0280 0,0244 0,0164
Lampiran 8 Pembuatan kurva standar SDS-PAGE.
Standar Sampel
BM (KDa) Log BM
Rf
(cm) Rf (Cm) Log BM BM
203 2,3075 0,0794 0,1666 1,8231 66,54
118 2,0719 0,1508 0,2381 1,7605 57,61
86 1,9345 0,2143 0,3190 1,6897 48,94
51,6 1,7126 0,3809 0,3238 1,6855 48,47
34,1 1,5327 0,5714 0,4603 1,5659 36,80
29 1,4624 0,6984 0,6666 1,3853 24,28
19,2 1,2833 0,9127 0,9841 1,1073 12,80
y = -1,142x + 2,2486 R2 = 0,9404
0 0,5 1 1,5 2 2,5
0 0,2 0,4 0,6 0,8 1
Rf (cm)
Lo
g B
ISOLASI DAN PENCIRIAN ENZIM PROTEASE
KERATINOLITIK DARI USUS BIAWAK AIR
ARINI MEGIANDARI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ISOLASI DAN PENCIRIAN ENZIM PROTEASE
KERATINOLITIK DARI USUS BIAWAK AIR
ARINI MEGIANDARI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Isolasi dan Pencirian Enzim Protease Keratinolitik dari Usus Biawak
Air
Nama : Arini Megiandari
NIM : G44204018
Disetujui
Prof. drh. Dondin Sajuthi, MST, PhD
Dr. dr. Irma H. Suparto, MS
NIP 130 536 684
NIP 131 606 776
Diketahui
Dekan Falkultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Dr. drh. Hasim, DEA
NIP 131 578 806
PENDAHULUAN
Latar Belakang
Biawak merupakan kelas reptil yang kulitnya banyak dimanfaatkan sebagai bahan perhiasan juga dagingnya sebagai bahan makanan dan dipercaya dapat digunakan untuk obat kulit. Jenis biawak yang paling banyak dimanfaatkan dan dikonsumsi adalah
biawak air (Varanus salvator). Hasil limbah
dari pemanfaatan biawak tersebut belum banyak digunakan seperti bagian organ dalamnya, antara lain saluran cernanya. Biawak merupakan hewan karnivora yang memangsa berbagai jenis burung, ayam, ikan, serta mamalia kecil seperti tikus dan cecurut. Reptil ini memangsa korbannya hidup-hidup termasuk dengan bulunya kemudian hasil pencernaannya dikeluarkan dalam bentuk feses tanpa ada sisa bulu ayam ataupun burung. Hal ini diduga di dalam saluran pencernaannya terdapat suatu zat atau enzim yang dapat menghancurkan bulu tersebut. Komponen utama pada bulu adalah protein keratin yang kaya akan sistein dan sistin. Oleh karena itu diduga terdapat suatu enzim keratinase di dalam saluran cerna biawak.
Keratinase termasuk enzim protease yang merupakan enzim ekstraseluler. Enzim ini dihasilkan di dalam sel tetapi dikeluarkan ke dalam media untuk menghidrolisis dan mendegradasi komponen kompleks menjadi senyawa sederhana yang mudah larut. Enzim keratinase banyak digunakan pada kosmetik dan teknologi kulit. Secara komersial enzim
tersebut dapat diekstraksi dari Streptomyces
frandiae danStreptomyces mikrolavus. Enzim
ini baik sekali untuk memecah ikatan disulfida keratin pada bulu (Winarno 1983). Selain untuk kosmetik, penggunaan enzim banyak digunakan untuk pengolahan limbah dan juga pakan hewan. Contohnya, enzim keratinase ini dapat diaplikasikan pada limbah bulu ayam yang dijadikan tepung bulu ayam sebagai bahan pakan alternatif yang mempunyai kandungan protein tinggi. Enzim keratinase ini ditambahkan agar dapat mendegradasi bulu ayam tersebut. Hal ini karena bulu ayam mengandung keratin yang merupakan protein serat khusus, tidak larut dalam air dan sulit dicerna (Rawn 1989).
Penelitian ini bertujuan mengisolasi dan mengetahui pencirian enzim protease yang mempunyai aktivitas keratinase dari ekstrak kasar lapisan atas (mukosa) usus biawak air. Hasil penelitian ini diharapkan dapat memberi informasi adanya suatu enzim keratinase
dalam saluran cerna biawak sehingga dapat meningkatkan nilai ekonomi dari hewan tersebut.
TINJAUAN PUSTAKA
Biawak Air (Varanus salvator)
Biawak merupakan hewan yang masuk dalam golongan kadal besar, suku biawak-biawakan (varanidae). Biawak dalam bahasa lain disebut sebagai bayawak (Sunda), menyawak atau nyambik (Jawa), berekai
(Madura), dan monitor lizard atau goanna
(Inggris). Biawak banyak macamnya, yang terbesar dan terkenal ialah biawak komodo (V. komodoensis), yang panjangnya dapat
melebihi 3 m.
Hewan berdarah dingin ini kerap ditemui di desa-desa dan perkotaan di Indonesia barat. Jenis biawak yang paling banyak adalah
biawak air dari jenis Varanus salvator.
Habitatnya di sekitar sungai dan rawa karena merupakan hewan yang semi-akuatik, oleh karena itu disebut sebagai biawak air.
[image:42.595.338.492.536.686.2]Umumnya biawak dewasa mempunyai panjang tubuh (moncong hingga ujung ekor) sekitar 1 m, meskipun ada pula yang dapat mencapai 2.5 m. Bobot badan biawak janta