PEMERIKSAAN KANDUNGAN MINERAL BESI DAN KALSIUM DALAM BUAH SUKUN (Artocarpus communis Forst) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI Di
ajukan untuk melengkapi salasatu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Su matera Utara
OLEH:
M. BUDI ARMANSYAH HASIBUAN NIM 111524010
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PEMERIKSAAN KANDUNGAN MINERAL BESI DAN KALSIUM DALAM BUAH SUKUN (Artocarpus communis Forst) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
M. BUDI ARMANSYAH HASIBUAN NIM 111524010
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PEMERIKSAAN KANDUNGAN MINERAL BESI DAN KALSIUM DALAM BUAH SUKUN (Artocarpus communis Forst) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
OLEH:
M. BUDI ARMANSYAH HASIBUAN NIM 111524010
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : 02 Agustus 2013
Pembimbing I, Panitia Penguji,
Dra. Masfria, M.S., Apt. Drs. Chairul A. Dalimunthe, M.Sc., Apt.
NIP 195707231986112001 NIP 194907061980021001
Pembimbing II, Dra. Masfria, M.S., Apt. NIP 195707231986112001
Dra. Tuty R. Pardede, M.Si., Apt. Dra. Salbiah, M.Si., Apt. NIP 195401101980032001 NIP 194810131987012001
Drs. Immanuel S. Meliala, M.Si., Apt. NIP 195001261983031002
Medan, Oktober 2013 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Bismillahirrahmanirrahiim,
Puji syukur penulis ucapkan kepada Allah SWT atas segala limpahan
rahmat dan karunianya, sehingga penulis dapat menyelesaikan penelitian dan
penyusunan skripsi ini, serta shalawat beriring salam untuk Rasulullah
Muhammad SAW sebagai suri tauladan dalam kehidupan. Skripsi ini disusun
untuk melengkapi salah satu syarat mencapai gelar Sarjana Farmasi pada
Fakultas Farmasi Universitas Sumatera Utara, dengan judul Pemeriksaan
Kandungan Mineral Besi dan Kalsium dalam Buah Sukun (Artocarpus
communis, Forst) secara Spektrofotometri Serapan Atom.
Pada kesempatan ini dengan segala kerendahan hati penulis
mengucapkan terima kasih yang sebesar-besarnya kepada, Ibu Dra. Masfria,
M.S., Apt., dan Ibu Dra. Tuti Roida Pardede, M.Si., Apt., yang telah
membimbing dan memberikan petunjuk serta saran-saran selama penelitian
hingga selesainya skripsi ini. Bapak Prof. Dr. Sumadio Hadisahputra, Apt.,
selaku Dekan Fakultas Farmasi USU Medan, yang telah memberikan fasilitas
sehingga penulis dapat menyelesaikan pendidikan. Bapak Drs. Chairul Azhar
Dalimunthe, M.Sc., Apt., dan Ibu Dra. Salbiah, M.Si., Apt., serta Bapak Drs.
Immanuel S. Meliala, M.Si., Apt., selaku dosen penguji yang telah
memberikan kritik, saran dan arahan kepada penulis dalam menyelesaikan
skripsi ini. Bapak dan Ibu staf pengajar Fakultas Farmasi USU Medan yang
selaku penasehat akademik yang selalu memberikan bimbingan, perhatian dan
motivasi kepada penulis selama masa perkuliahan. Ibu Dra. Masfria, M.Si.,
Apt., selaku kepala Laboratorium Kimia Farmasi Kualitatif USU dan Bapak
Prof. Dr. rer. nat. Effendy De Lux Putra, S.U., Apt., selaku kepala
Laboratorium Penelitian USU yang telah memberikan izin dan fasilitas untuk
penulis sehingga dapat mengerjakan dan menyelesaikan penelitian.
Penulis juga mengucapkan terima kasih dan penghargaan yang tiada
terhingga kepada Ayahanda Masri Hasibuan dan Ibunda Mariatun yang telah
memberikan cinta dan kasih sayang yang tidak ternilai dengan apapun,
pengorbanan baik materi maupun motivasi serta doa yang tulus yang tidak
pernah berhenti. Adikku tercinta Nurhayani, Nurhakiki dan seluruh keluarga
yang selalu mendoakan dan memberikan semangat. Sahabat-sahabat ekstensi
2011, terima kasih untuk dorongan, semangat dan kebersamaan nya selama ini,
serta seluruh pihak yang telah ikut mebantu penulis yang tidak dapat di
sebutkan satu persatu.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih
jauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis
menerima kritik dan saran demi kesempurnaan skripsi ini. Akhirnya, penulis
berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, Agustus 2013
Penulis,
PEMERIKSAAN KANDUNGAN MINERAL BESI DAN KALSIUM DALAM BUAH SUKUN (Artocarpus communis, Forst) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM ABSTRAK
Buah sukun (Artocarpus communis, Forst) merupakan bahan pangan alternatif yang mempunyai potensi cukup besar yang belum dimanfaatkan sebagai makanan bergizi, namun kini mulai cukup populer dan dikembangkan diberbagai daerah di Indonesia dan memiliki keuntungan lebih karena mempunyai kandungan mineral (kalsium, fosfor, dan zat besi) dan vitamin dua atau tiga kali lebih banyak dari sereal dan umbi-umbian yang dibutuhkan oleh manusia. Komposisi gizi dari buah sukun berbeda, ditentukan oleh daging, kulit, dan tingkat kematangannya (sangat tidak matang, belum matang, matang, dan sangat matang). Berdasarkan informasi yang diperoleh dari masyarakat, buah sukun lebih banyak dikonsumsi dalam keadaan matang dibanding keadaan sangat matang. Buah sukun belum matang tidak dikonsumsi. Tujuan penelitian ini adalah untuk menetapkan kadar besi dan kalsium dalam buah sukun matang dan sangat matang.
Penetapan kadar dilakukan menggunakan spektrofotometer serapan atom dengan nyala udara-asetilen. Analisis kuantitatif dilakukan pada panjang gelombang 248,3 nm untuk besi dan 422,7 nm untuk kalsium.
Hasil penelitian menunjukkan bahwa kadar besi pada buah sukun matang (1,1155 ± 0,0375) mg/100 g dan sangat matang (2,2123 ± 0,0155) mg/100 g. Kadar kalsium pada buah sukun matang (49,7035 ± 2,1597) mg/100 g dan sangat matang (13,5377 ± 0,2464) mg/100 g. Secara statistika uji beda rata-rata kandungan besi dan kalsium antara buah sukun matang dan sangat matang dengan menggunakan distribusi F, menyimpulkan bahwa kandungan besi pada buah sukun sangat matang lebih tinggi secara signifikan dari buah sukun matang, sedangkan kandungan kalsium pada buah sukun matang lebih tinggi secara signifikan dari buah sukun sangat matang.
EXAMINATION OF MINERAL LEVEL IRON AND CALCIUM IN BUAH SUKUN (Artocarpus communis, Forst) BY ATOMIC
ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Buah Sukun (Artocarpus communis, Forst) is an alternative food that has considerable potential that have not been used as a nutritious food, but is now getting quite popular and developed in various regions in Indonesia and has an advantage because it has more mineral content (calcium, phosphorus, and iron) and vitamin two or three times more than cereals and tubers required by humans. Nutritional composition of buah sukun different, determined by the meat, skin, and the level of maturity (very immature, immature, mature, and very mature ). Based on information obtained from the community, buah sukun much more is consumed the mature state than is consumed very mature. The immature buah sukun is not consumed. The purpose of this study was to determine levels of iron and calcium content in buah sukun mature and very mature.
Determination of iron and calcium using atomic absorption spectrophotometer with acetylene-air flame. Quantitative analysis performed at a wavelength of 248.3 nm and 422.7 nm for iron to calcium.
The results showed that the iron content in the mature buah sukun (1.1155 ± 0.0375) mg/100 g and very mature (2.2123 ± 0.0155) mg/100 g. Calcium levels in the mature buah sukun (49.7035 ± 2.1597) mg/100 g and very mature (13.5377 ± 0.2464) mg/100 g. Of the statistical test average difference between the content of iron and
calcium buah sukun mature and very mature with using the F
distribution, concluded that the iron content in the fruit is very mature
buah sukun significantly higher than ripe buah sukun, while the calcium content in the ripe buah sukun higher significantly from very ripe buah sukun.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR . ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Sukun ... 5
2.2 Mineral ... 9
2.2.1 Besi ... 9
2.2.2 Kalsium ... 10
2.3.1 Instrumentasi Spektrofotometri Serapan Atom ... 12
2.3.2 Gangguan-gangguan pada Spektrofotometri Serapan Atom ... 13
2.4 Validasi metode Analisis ... 15
BAB III METODE PENELITIAN ... 18
3.1 Tempat dan Waktu Penelitian ... 18
3.2 Bahan-bahan ... 18
3.2.1 Sampel ... 18
3.2.2 Pereaksi ... 18
3.3 Alat-alat ... 18
3.4 Identifikasi sampel ... 19
3.5 Pembuatan Pereaksi ... 19
3.5.1 Larutan HNO3 (1:1) . ... 19
3.5.2 Larutan HNO3 1 N ... 19
3.5.3 Larutan Kalium Heksasianoferat (II) 10% ... 19
3.5.4 Larutan Amonium Tiosianat 8% ... 19
3.5.5 Larutan Asam Sulfat 1 N ... 20
3.6 Prosedur Penelitian ... 20
3.6.1 Pengambilan Sampel ... 20
3.6.2 Penyiapan Bahan ... 20
3.6.3 Proses Destruksi ... 20
3.6.4 Pembuatan Larutan Sampel ... 21
3.6.5.1 Analisis Kualitatif Besi Untuk Buah Sukun
Matang ... 22
3.6.5.1.1 Reaksi warna dengan Kalium heksasianoferat(II) trihidrat ... 22
3.6.5.1.2 Reaksi warna dengan Amonium tiosianat ... 22
3.6.5.2 Analisis Kualitatif Besi Untuk Buah Sukun Sangat Matang ... 22
2.6.5.2.1 Reaksi warna dengan Kalium heksasianoferat(II) trihidrat ... 22
2.6.5.2.2 Reaksi warna dengan Amonium tiosianat ... 22
3.6.5.3 Analisis Kualitatif Kalsium Untuk Buah Sukun Matang ... 23
3.6.5.3.1 Reaksi Uji Nyala ... 23
3.6.5.3.2 Reaksi Kristal Kalsium Dengan Asam Sulfat 1 N ... 23
3.6.5.4 Analisis Kualitatif Kalsium Untuk Buah Sukun Sangat matang ... 23
3.6.5.3.1 Reaksi Uji Nyala ... 23
3.6.5.3.2 Reaksi Kristal Kalsium Dengan Asam Sulfat 1 N ... 23
3.6.6 Analisis Kuantitatif ... 24
3.6.6.1 Pembuatan Kurva Kalibrasi Besi ... 24
3.6.6.2 Pembuatan Kurva Kalibrasi Kalsium ... 24
3.6.6.3 Penetapan Kadar Besi dan Kalsium dalam Sampel ... 24
3.6.6.3.2 Penetapan Kadar Besi dalam Buah
Sukun Sangat Matang ... 25
3.6.6.3.3 Penetapan Kadar Kalsium dalam Buah Sukun Matang ... ... 25
3.6.6.3.4 Penetapan Kadar Kalsium dalam Buah Sukun Sangat Matang ... 26
3.6.7 Analisis Data Secara Statistik ... 27
3.6.7.1 Penolakan Hasil Pengamatan ... 27
3.6.7.2 Pengujian Beda Nilai Rata-rata Antar Sampel ... 27
3.6.8 Uji Perolehan Kembali (Recovery) ... 29
3.6.9 Simpangan Baku Relatif... 29
3.6.10 Penentuan Batas Deteksi dan batas kuantitasi ... 30
BAB IV HASIL DAN PEMBAHASAN ... 31
4.1 Analisis Kualitatif ... 31
4.2 Analisis Kuantitatif ... 32
4.2.1 Kurva Kalibrasi Besi dan Kalsium ... 32
4.2.2 Analisis Kadar Besi dan Kalsium dalam Sukun Matang dan Sangat Matang ... 33
4.2.3 Uji Perolehan Kembali (Recovery) ... 35
4.2.4 Simpangan Baku Relatif ... 36
4.2.5 Batas Deteksi dan Batas Kuantitasi ... 37
BAB V KESIMPULAN DAN SARAN ... 38
5.1 Kesimpulan ... 38
DAFTAR PUSTAKA ... 39
DAFTAR TABEL
Halaman
Tabel 1. Proporsi Bagian Buah Sukun ... 6
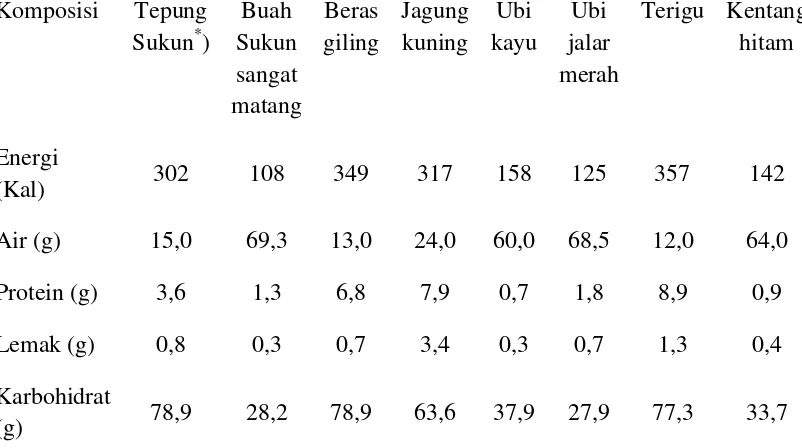
Tabel 2. Komposisi zat gizi buah sukun per 100 g bahan ... 8
Tabel 3. Perbandingan kandungan zat gizi sukun per 100 g dengan
beberapa bahan pangan lainnya ... 8
Tabel 4. Hasil Analisis Kualitatif dalam Sampel ... 31
Tabel 5. Hasil Analisis Kuantitatif Kadar Besi dan kalsium dalam
Sampel ... 34
Tabel 6. Hasil Uji Beda Nilai Rata-rata Besi dan Kalsium dalam
Sampel ... 34
DAFTAR GAMBAR
Halaman
Gambar 1. Instrumentasi Spektrofotometer Serapan Atom ... 12
Gambar 2. Kurva Kalibrasi Besi ... 32
Gambar 3. Kurva Kalibrasi Kalsium ... 33
Gambar 4. Buah Sukun Matang ... 43
Gambar 5. Buah Sukun Sangat Matang ... 44
Gambar 6. Kristal Kalsium Sulfat (Perbesaran 10x40) ... 47
Gambar 7. Hasil Analisis Kualitatif Besi ... 47
Gambar 8. Spektrofotometer Serapan Atom hitachi Z-2000 ... 48
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Hasil Identifikasi Sampel ... 42
Lampiran 2. Gambar Sampel yang Digunakan ... 43
Lampiran 3. Bagan Alir Proses Dekstruksi Kering ... 45
Lampiran 4. Bagan Alir Proses Pembutan Larutan Sampel ... 46
Lampiran 5. Hasil Analisis Kualitatif Besi dan Kalsium ... 47
Lampiran 6. Gambar Alat yang Digunakan ... 48
Lampiran 7. Data Absorbansi Kalibrasi Besi, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi ... 49
Lampiran 8. Data Kalibrasi Kalsium, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi ... 50
Lampiran 9. Hasil Analisis Kadar Besi dan Kalsium dalam Sampel ... 51
Lampiran 10. Contoh Perhitungan Kadar Besi dan Kalsium dalam Buah Sukun Matang ... 52
Lampiran 11. Contoh Perhitungan Kadar Besi dan Kalsium dalam Buah Sukun Sangat Matang ... 53
Lampiran 12. Perhitungan Statistik Kadar Besi ... 54
Lampiran 13. Perhitungan Statistik Kadar Kalsium ... 57
Lampiran 14. Pengujian Beda Rata-rata Kadar Besi dalam Sampel ... 60
Lampiran 15. Pengujian Beda Rata-rata Kadar Kalsium dalam Sampel ... 62
Lampiran 16. Hasil Uji Perolehan Kembali Besi dan Kalsium Setelah Penambahan Larutan Baku ... 64
Lampiran 18. Perhitungan Simpangan Baku Relatif (RSD) ... 69
Lampiran 19. Perhitungan Batas Deteksi dan Batas Kuantitasi ... 71
Lampiran 20. Tabel Distribusi t ... 73
Lampiran 21. Tabel Distribusi F ... 74
PEMERIKSAAN KANDUNGAN MINERAL BESI DAN KALSIUM DALAM BUAH SUKUN (Artocarpus communis, Forst) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM ABSTRAK
Buah sukun (Artocarpus communis, Forst) merupakan bahan pangan alternatif yang mempunyai potensi cukup besar yang belum dimanfaatkan sebagai makanan bergizi, namun kini mulai cukup populer dan dikembangkan diberbagai daerah di Indonesia dan memiliki keuntungan lebih karena mempunyai kandungan mineral (kalsium, fosfor, dan zat besi) dan vitamin dua atau tiga kali lebih banyak dari sereal dan umbi-umbian yang dibutuhkan oleh manusia. Komposisi gizi dari buah sukun berbeda, ditentukan oleh daging, kulit, dan tingkat kematangannya (sangat tidak matang, belum matang, matang, dan sangat matang). Berdasarkan informasi yang diperoleh dari masyarakat, buah sukun lebih banyak dikonsumsi dalam keadaan matang dibanding keadaan sangat matang. Buah sukun belum matang tidak dikonsumsi. Tujuan penelitian ini adalah untuk menetapkan kadar besi dan kalsium dalam buah sukun matang dan sangat matang.
Penetapan kadar dilakukan menggunakan spektrofotometer serapan atom dengan nyala udara-asetilen. Analisis kuantitatif dilakukan pada panjang gelombang 248,3 nm untuk besi dan 422,7 nm untuk kalsium.
Hasil penelitian menunjukkan bahwa kadar besi pada buah sukun matang (1,1155 ± 0,0375) mg/100 g dan sangat matang (2,2123 ± 0,0155) mg/100 g. Kadar kalsium pada buah sukun matang (49,7035 ± 2,1597) mg/100 g dan sangat matang (13,5377 ± 0,2464) mg/100 g. Secara statistika uji beda rata-rata kandungan besi dan kalsium antara buah sukun matang dan sangat matang dengan menggunakan distribusi F, menyimpulkan bahwa kandungan besi pada buah sukun sangat matang lebih tinggi secara signifikan dari buah sukun matang, sedangkan kandungan kalsium pada buah sukun matang lebih tinggi secara signifikan dari buah sukun sangat matang.
EXAMINATION OF MINERAL LEVEL IRON AND CALCIUM IN BUAH SUKUN (Artocarpus communis, Forst) BY ATOMIC
ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Buah Sukun (Artocarpus communis, Forst) is an alternative food that has considerable potential that have not been used as a nutritious food, but is now getting quite popular and developed in various regions in Indonesia and has an advantage because it has more mineral content (calcium, phosphorus, and iron) and vitamin two or three times more than cereals and tubers required by humans. Nutritional composition of buah sukun different, determined by the meat, skin, and the level of maturity (very immature, immature, mature, and very mature ). Based on information obtained from the community, buah sukun much more is consumed the mature state than is consumed very mature. The immature buah sukun is not consumed. The purpose of this study was to determine levels of iron and calcium content in buah sukun mature and very mature.
Determination of iron and calcium using atomic absorption spectrophotometer with acetylene-air flame. Quantitative analysis performed at a wavelength of 248.3 nm and 422.7 nm for iron to calcium.
The results showed that the iron content in the mature buah sukun (1.1155 ± 0.0375) mg/100 g and very mature (2.2123 ± 0.0155) mg/100 g. Calcium levels in the mature buah sukun (49.7035 ± 2.1597) mg/100 g and very mature (13.5377 ± 0.2464) mg/100 g. Of the statistical test average difference between the content of iron and
calcium buah sukun mature and very mature with using the F
distribution, concluded that the iron content in the fruit is very mature
buah sukun significantly higher than ripe buah sukun, while the calcium content in the ripe buah sukun higher significantly from very ripe buah sukun.
BAB I PENDAHULUAN
1.1 Latar Belakang
Buah sukun (Artocarpus communis, Forst) merupakan bahan pangan
alternatif yang sekarang mulai cukup populer dan dikembangkan diberbagai
daerah di Indonesia. Buah sukun segar bisa dimanfaatkan sebagai bahan
pangan, lazimnya yaitu dengan cara menggoreng daging buahnya (Ditjen
BPPHP, 2002). Sukun masuk dalam lampiran Perjanjian Internasional tentang
Sumber Daya Genetik untuk Pangan dan Pertanian sehingga sukun
berkontribusi terhadap upaya global dalam menjamin ketahanan pangan (Jones,
et al., 2011).
Buah sukun memiliki potensi cukup besar yang belum dimanfaatkan
sebagai makanan bergizi, dan memiliki keuntungan lebih karena mempunyai
kandungan mineral dan vitamin dua atau tiga kali lebih banyak dari sereal dan
umbi-umbian (Ijarotimi dan Aroge, 2005).
Di Nigeria buah sukun di jadikan sebagai makanan pengganti ASI
dikalangan masyarakat berpenghasilan rendah. sedangkan di Indonesia buah
sukun sangat sedikit dimanfaatkan sebagai makanan bergizi. Pada buah sukun
selain karbohidrat, protein dan lemak, buah sukun juga mengandung vitamin
B1, B2, dan vitamin C, serta mineral (kalsium, fosfor, dan zat besi) yang
dibutuhkan oleh manusia, terutama bagi anak-anak dan ibu yang sedang hamil
Berdasarkan informasi yang diperoleh dari masyarakat, buah sukun
umumnya dikonsumsi dalam keadaan matang daripada buah sukun sangat
matang, sedangkan buah sukun belum matang tidak dikonsumsi oleh
masyarakat. Bagian yang dikonsumsi adalah daging buah, sedangkan kulit dan
hati buah tidak ikut dikonsumsi. Buah sukun memiliki jumlah karbohidrat yang
tinggi namun rendah kalori, sehingga di sebagian daerah di Indonesia, buah
sukun merupakan bahan pangan alternatif sebagai pengganti beras. Buah sukun
matang dapat diolah menjadi keripik, goreng sukun, gulai sukun dan kolak
sukun, sedangkan buah sukun sangat matang terbatas pengolahannya (Ijarotimi
dan Aroge, 2005).
Menurut widayati dan Damayanti (2000), buah sukun matang memiliki
kandungan kalsium 57 mg/100 g dan zat besi (belum diketahui), sedangkan
pada buah sukun sangat matang memiliki kandungan kalsium 21 mg/100g dan
zat besi 0,4 mg/100 g. Komposisi gizi dari buah sukun berbeda, ditentukan
oleh daging, kulit, dan tingkat kematangannya (sangat tidak matang, belum
matang, matang, dan sangat matang) (Ragone, 1996).
Mineral merupakan unsur essensial bagi fungsi normal sebagian enzim.
Mineral merupakan konstituen tulang dan gigi, yang memberikan kekuatan
kepada jaringan misalnya Fe, Ca, P dan Mg (Budianto,2009). Besi penting bagi
manusia untuk pembentukan eritrosit, sehingga kekurangan besi dalam tubuh
akan mempengaruhi pembentukan hemoglobin (Hb). Besi yang terikat dengan
hemoglobin mempunyai beberapa fungsi essensial di dalam tubuh : sebagai alat
sel dan sebagai unsur, besi merupakan bagian terpenting dari reaksi enzim di
dalam jaringan tubuh (Almaitser, 2004). Kalsium penting bagi balita yang
sudah lepas menyusui dan anak-anak sampai remaja yang sedang dalam masa
pertumbuhan (Budianto, 2009).
Analisis kuantitatif besi dapat dilakukan secara spektrofotometri sinar
tampak, gravimetri, kompleksometri dan spektrofotometri serapan atom,
sedangkan kalsium dapat ditentukan antara lain dengan cara: metode titrasi,
metode gravimetri dan metode spektrofotometri serapan atom (Bassett, dkk.,
1994).
Dalam penelitian ini digunakan Spektrofotometri Serapan Atom,
pemilihan ini didasarkan pada ketelitian alat, kecepatan analisis, tidak
memerlukan pemisahan pendahuluan, dan dapat menentukan kadar suatu unsur
dengan konsentrasi yang rendah (Khopkar, 2008).
Berdasarkan uraian di atas, penulis melakukan penelitian kandungan
besi dan kalsium yang terdapat pada buah sukun matang dan buah sukun sangat
matang.
1.2 Perumusan Masalah
Berdasarkan uraian diatas, maka permasalahan dalam penelitian ini
dapat dirumuskan sebagai berikut :
a. Berapakah kadar besi dan kalsium pada buah sukun (Artocarpus
communis, Forst) matang dan sangat matang?
b. Apakah terdapat perbedaan kadar besi dan kalsium pada buah sukun
1.3 Hipotesis
a. Buah sukun (Artocarpus communis, Forst) matang dan sangat matang
mengandung mineral besi dan kalsium dalam jumlah tertentu.
b. Terdapat perbedaan kadar besi dan kalsium pada buah sukun matang
dan sangat matang.
1.4 Tujuan Penelitian
a. Untuk mengetahui kadar besi dan kalsium pada buah sukun (Artocarpus
communis, Forst) matang dan sangat matang.
b. Untuk mengetahui perbedaan kadar besi dan kalsium pada buah sukun
matang dan sangat matang.
1.5 Manfaat Penelitian
Untuk memberikan informasi kepada masyarakat tentang kandungan
mineral besi dan kalsium yang terkandung dalam buah sukun matang dan buah
BAB II
TINJAUAN PUSTAKA 2.1 Sukun
Sukun merupakan tanaman tahunan yang tumbuh baik pada lahan
kering (daratan), dengan tinggi pohon dapat mencapai 10 m atau lebih dan
mempunyai cabang-cabang yang melebar kesamping dengan tajuk sekitar 5 m.
Daunnya berbentuk oval panjang dengan belahan daun simetris yang ditunjung
dengan tulang daun yang menyisip simetris pula. Permukaan daun bagian atas
halus dan berwarna hijau mengkilap sedang bagian bawah kasar berbulu dan
berwarna kusam (Widowati, dkk., 2010).
Sukun masuk dalam lampiran Perjanjian Internasional tentang Sumber
Daya Genetik untuk Pangan dan Pertanian sehingga sukun berkontribusi
terhadap upaya global dalam menjamin ketahanan pangan. Dalam bidang
kehutanan, sukun merupakan salah satu jenis pohon yang dipilih dalam
kegiatan Gerakan Nasional Rehabilitasi Hutan dan Lahan (Jones, et al., 2011).
Menurut MEDA (2013), taksonomi tanaman sukun sebagai berikut:
Kingdom : Plantae
Divisio : Spermatophyta
Classes : Dicotyledoneae
Ordo : Urticales
Famili : Moraceae
Genus : Artocarpus
Buah sukun (Artocarpus communis, Forst) merupakan sumber
karbohidrat potensial yang mempunyai nama daerah, yaitu sakon (Aceh), Suku
(Nias), Sukun ( Jawa,Sunda, Bali), Bakara (Sulawesi Selatan). Terdapat dua
jenis sukun, yaitu sukun tanpa biji dan sukun dengan biji. Di Indonesia, jenis
pertama lebih populer dengan sebutan sukun yang diolah menjadi produk
makanan, sedangkan sukun dengan biji lebih dikenal dengan sebutan kluwih
dan biasanya dimanfaatkan sebagai sayur (Widowati, dkk., 2010).
Pembentukan buah sukun tidak didahului dengan proses pembuahan
bakal biji, maka buah sukun tidak memiliki biji. Pada mulanya kulit memiliki
kulit yang kasar mirip duri; selanjutnya kulit seolah tertarik dan terbentang
sehingga berbekas seperti gambar heksagonal dengan titik ditengahnya, dan
kulit menjadi halus. Buah sukun akan menjadi tua setelah tiga bulan sejak
munculnya bunga betina. Buah yang muncul awal akan menjadi tua lebih
dahulu, kemudian diikuti oleh buah berikutnya (Widowati, dkk., 2010).
Buah sukun terdiri dari tiga bagian yaitu kulit, hati dan daging yang
merupakan bagian yang dapat dimakan. Persentase setiap bagian buah dengan
tingkat kematangan yang berbeda dapat dilihat pada Tabel 1. Daging buah
yang masih muda berwarna putih, sedangkan bila sudah masak akan berwarna
kekuning-kuningan (Widowati, dkk., 2010).
Tabel 1. Proporsi bagian buah sukun.
Bagian Buah matang (%) Buah sangat matang (%)
Kulit 22 12
Daging 70 78
Sumber : Widowati, dkk. (2010).
Menurut Ragone (1997), berdasarkan tingkat kematangannya buah
sukun dikategorikan menjadi:
1. Buah sukun sangat belum matang; memiliki getah yang banyak jika
tangkai buah di tusuk atau dilukai, daging buah cepat berubah warna dan
menjadi gelap ketika dipotong serta belum siap untuk dimakan.
2. Buah sukun belum matang; memiliki ukuran sedikit lebih besar dan
getahnya lebih sedikit, tidak cepat berubah warna (gelap) ketika dilukai
atau ditusuk.
3. Buah sukun matang; ukuran lebih besar dari buah sukun belum matang,
warna kulitnya tergantung pada jenis dan warnanya hijau sedikit agak
kekuningan serta daging buahnya berwarna putih-krem dan tidak cepat
berubah warna saat di potong.
4. Buah sukun sangat matang; kulit berwarna kuning-kecokelatan memiliki
retakan atau celah. Daging buahnya cukup kuning dan lembut, rasanya
manis dan memiliki aroma yng khas.
Menurut Ijarotimi dan Aroge (2005), buah sukun (Artocarpus
communis, Forst) mengandung berbagai jenis nutrisi yaitu karbohidrat (25%),
protein (1,5%) dan lemak (0,3%) dari berat buah sukun. Selain itu, buah sukun
juga banyak mengandung unsur-unsur mineral serta vitamin yang sangat
dibutuhkan oleh tubuh. Unsur-unsur mineral yang terkandung dalam buah
sedangkan vitamin yang menonjol antara lain adalah vitamin B1, B2, dan
vitamin C. Kandungan air dalam buah sukun cukup tinggi yaitu sekitar 63,3 %.
Komposisi zat gizi buah sukun dapat dilihat pada Tabel 2 dan perbandingan
kandungan zat gizi utama pada sukun dengan beberapa bahan pangan lainnya
disajikan pada Tabel 3.
Tabel 2. Komposisi zat gizi buah sukun per 100 g bahan
Zat Gizi Sukun
Matang
Sukun Sangat Matang
Tepung Sukun
Karbohidrat (g) 9,2 28,2 78,9
Lemak (g) 0,7 0,3 0,8
Protein (g) 2,0 1,3 3,6
Vitamin B1 (mg) 0,12 0,12 0,34
Vitamin B2 (mg) 0,06 0,05 0,17
Vitamin C (mg) 21,00 17 47,6
Kalsium (mg) 59 21 58,8
Fosfor (mg) 46 59 165,2
Zat besi (mg) - 0,4 1,1
Sumber : Widayati dan Damayanti (2000).
Tabel 3. Perbandingan kandungan zat gizi sukun per 100 g dengan beberapa bahan pangan lainnya.
Komposisi Tepung
Sukun*)
Buah Sukun sangat matang
Beras giling
Jagung kuning
Ubi kayu
Ubi jalar merah
Terigu Kentang hitam
Energi
(Kal) 302 108 349 317 158 125 357 142
Air (g) 15,0 69,3 13,0 24,0 60,0 68,5 12,0 64,0
Protein (g) 3,6 1,3 6,8 7,9 0,7 1,8 8,9 0,9
Lemak (g) 0,8 0,3 0,7 3,4 0,3 0,7 1,3 0,4
Karbohidrat
Abu (g) 2,0 0,9 - - - -
Ca (mg) 58,8 21,0 10,0 9,0 33,0 49,0 16,0 34,0
Fe (mg) 1,1 0,4 0,8 2,1 0,7 0,7 1,2 0,2
P (mg) 165,2 59,0 140,0 148,0 40,0 0,7 106,0 75,0
Vit B 0,34 0,12 0,12 264 230 2310 0 0
Vit B 0,17 0,06 0 0,33 0,06 0,09 0,12 0,02
Vit C (mg) 47,6 17,0 0 0 0 20,0 0 38,0
Sumber : Widowati, dkk. (2010).
2.2. Mineral
Mineral merupakan bagian dari tubuh dan memegang peranan penting
dalam pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, dan organ.
Mineral digolongkan ke dalam mineral makro dan mineral mikro. Mineral
makro adalah mineral yang dibutuhkan tubuh dalam jumlah lebih dari 100 mg
sehari, sedangkan mineral mikro dibutuhkan kurang dari 100 mg sehari. Yang
termasuk mineral makro antara lain: natrium, klorida, kalium, kalsium, fosfor,
dan magnesium, sedangkan yang termasuk mineral mikro antara lain: besi,
mangan dan tembaga (Almatsier, 2004).
Mineral merupakan unsur essensial bagi fungsi normal sebagian enzim.
Mineral merupakan konstituen tulang dan gigi, yang memberikan kekuatan
kepada jaringan misalnya Fe, Ca, P dan Mg. Tubuh tidak mampu mensintesa
mineral sehingga unsur-unsur ini harus disediakan lewat makanan
(Budianto,2009). Secara tidak langsung, mineral banyak yang berperan dalam
lainnya, kekurangan atau kelebihan salah satu mineral akan berpengaruh
terhadap kerja mineral lainnya (Pudjiadi, 1993).
2.2.1 Besi
Besi merupakan mineral mikro yang paling banyak terdapat di dalam
tubuh manusia dan hewan. Besi mempunyai beberapa fungsi esensial di dalam
tubuh : sebagai alat angkut oksigen dari paru-paru ke jaringan tubuh, sebagai
alat angkut elektron di dalam sel, dan sebagai bagian terpadu berbagai reaksi
enzim di dalam jaringan tubuh (Almatsier, 2004).
Kebutuhan akan zat besi untuk berbagai jenis kelamin dan golongan
usia adalah sebagai berikut: untuk laki-laki dewasa 10 mg/hari, wanita yang
mengalami haid 12 mg/hari, dan anak-anak 8-15 mg/hari. Zat besi yang tidak
mencukupi bagi pembentukan sel darah, akan mengakibatkan anemia,
menurunkan kekebalan tubuh, sehingga sangat peka terhadap serangan
penyakit (Budianto, 2009).
Tubuh sangat efisien dalam penggunaan besi. Sebelum diabsorpsi,
didalam lambung besi dibebaskan dari ikatan organik seperti protein. Sebagian
besar besi dalam bentuk feri direduksi menjadi bentuk fero. Hal ini terjadi
dalam suasana asam di dalam lambung dengan adanya HCl dan vitamin C yang
terdapat di dalam makanan. Absorpsi terutama terjadi di bagian atas usus halus
(duodenum) dengan alat angkut protein khusus (Almatsier, 2004). 2.2.2 Kalsium
Kalsium merupakan mineral yang paling banyak terdapat di dalam
sebanyak 1 kg. Dari jumlah ini, 99% berada didalam jaringan keras, yaitu
tulang dan gigi terutama dalam bentuk hidroksiapatit selebihnya kalsium
tersebar luas di dalam tubuh. Absorpsi kalsium terutama terjadi di bagian atas
usus halus yaitu duodenum (Almatsier, 2004). Peningkatan kebutuhan akan
kalsium terjadi pada masa pertumbuhan, kehamilan, dan menyusui (Ijarotimi
dan Aroge, 2005).
Mineral kalsium dibutuhkan untuk perkembangan tulang. Kalsium
sangat penting terutama untuk anak-anak, wanita hamil, dan wanita menyusui.
Jumlah yang dianjurkan per hari untuk anak-anak sebesar 500 mg, remaja
600-700 mg, dan dewasa sebesar 800 mg (Almatsier, 2004).
Kekurangan kalsium pada masa pertumbuhan dapat menyebabkan
gangguan pertumbuhan. Tulang kurang kuat, mudah bengkok dan rapuh.
Tulang menjadi rapuh dan mudah patah disebut juga osteoporosis yang dapat
dipercepat oleh keadaan stres sehari-hari. Osteoporosis lebih banyak terjadi
pada wanita daripada laki-laki dan lebih banyak pada orang kulit putih
daripada kulit berwarna (Almatsier, 2004).
2.3 Spektrofotometri Serapan Atom
Spektrofotometri serapan atom digunakan untuk analisis kuantitatif
unsur-unsur logam dalam jumlah sekelumit (trace) dan sangat kelumit
(ultratrace). Cara analisis ini memberikan kadar total unsur logam dalam suatu
sampel dan tidak tergantung pada bentuk molekul dari logam dalam sampel
kepekaan yang tinggi (batas deteksi kurang dari 1 ppm), pelaksanaannya relatif
sederhana, dan interferensinya sedikit (Gandjar dan Rohman, 2009).
Spektrofotometri serapan atom didasarkan pada penyerapan energi
sinar oleh atom-atom netral dan sinar yang diserap biasanya sinar tampak atau
ultraviolet. Secara garis besar, prinsip spektrofotometri serapan atom sama saja
dengan spektrofotometri sinar tampak dan ultraviolet. Perbedaan nya terletak
pada bentuk spektrum, cara pengerjaaan sampel dan peralatannya. Metode
Spektrofotometri Serapan Atom (SSA) mendasarkan pada prinsip absorbsi
cahaya oleh atom. Atom-atom akan menyerap cahaya pada panjang gelombang
tertentu, tergantung pada sifat unsurnya (Gandjar dan Rohman, 2009).
Jika suatu larutan yang mengandung suatu garam logam (atau suatu
senyawa logam) dihembuskan kedalam suatu nyala (misalnya asetilena yang
terbakar di udara) maka terbentuk uap yang mengandung atom-atom logam itu.
Atom logam bentuk gas tersebut tetap berada dalam keadaan tak tereksitasi
atau dengan perkataan lain, dalam keadaan dasar. Jadi jika cahaya dengan
panjang gelombang yang khas dengan logam tersebut dilewatkan nyala yang
mengandung atom-atom yang bersangkutan, maka sebagian cahaya tersebut
akan diserap dan jauhnya penyerapan akan berbanding lurus dengan banyaknya
atom keadaan dasar yang berada dalam nyala. Inilah asas yang mendasari
spektrofotometri serapan atom (SSA) (Bassett, dkk., 1994).
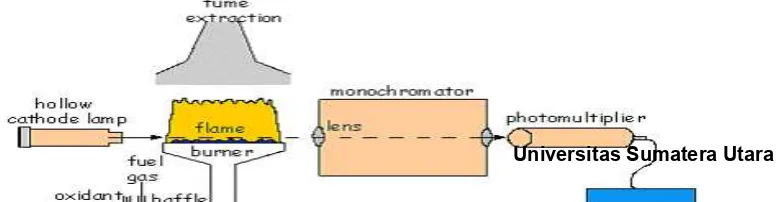
2.3.1 Instrumentasi Spektrofotometri Serapan Atom
[image:30.595.136.525.734.835.2]Sistem peralatan spektrofotometer serapan atom dapat dilihat pada
Gambar 1. Instrumentasi Spektrofotometer Serapan Atom
a. Sumber sinar
Sumber sinar yang lazim dipakai adalah lampu katoda berongga
(hollow catodhe lamp). Lampu ini terdiri atas tabung kaca tertutup yang
mengandung suatu katoda dan anoda. Katoda sendiri berbentuk silinder
berongga yang terbuat dari logam atau dilapisi dengan logam tertentu (Gandjar
dan Rohman, 2009).
b. Tempat sampel
Dalam analisis dengan spektrofotometri serapan atom, sampel yang
akan dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam
keadaan dasar (Gandjar dan Rohman, 2009).
c. Monokromator
Pada spektrofotometri serapan atom, monokromator dimaksudkan
untuk memisahkan dan memilih panjang gelombang yang digunakan untuk
analisis (Gandjar dan Rohman, 2009).
Detektor digunakan untuk mengukur intensitas cahaya yang melalui
tempat pengatoman (Gandjar dan Rohman, 2009).
e. Readout
Readout merupakan suatu sistem pencatatan hasil yang berupa hasil
pembacaan. Hasil pembacaan dapat berupa angka atau kurva.
2.3.2 Gangguan-gangguan pada Spektrofotometri Serapan Atom
Gangguan-ganguan pada SSA adalah peristiwa-peristiwa yang
menyebabkan pembacaan absorbansi unsur yang dianalisis menjadi lebih kecil
atau lebih besar dari nilai yang sesuai dengan konsentrasinya dalam sampel.
Gangguan-gangguan yang dapat terjadi dalam SSA adalah sebagai berikut
(Gandjar dan Rohman, 2009):
a. Gangguan yang berasal dari matriks sampel yang dapat mempengaruhi
banyaknya sampel yang mencapai nyala
Sifat-sifat tertentu matriks sampel dapat mengganggu analisis yakni
matriks tersebut dapat berpengaruh terhadap laju aliran bahan bakar gas
pengoksidasi. Sifat-sifat tersebut adalah viskositas, tegangan permukaan, berat
jenis dan tekanan uap. Gangguan matriks yang lain adalah pengendapan unsur
yang dianalisis sehingga jumlah atom yang mencapai nyala menjadi lebih
sedikit dari konsentrasi yang seharusnya yang terdapat dalam sampel (Gandjar
dan Rohman, 2009).
b. Gangguan kimia yang dapat mempengaruhi jumlah/banyak nya atom
Terbentuknya atom-atom netral yang masih dalam keadaan dasar di
dalam nyala sering terganggu oleh dua peristiwa kimia yaitu: disosiasi
senyawa-senyawa yang tidak sempurna dan ionisasi atom-atom di dalam nyala.
Terjadi disosiasi yang tidak sempurna disebabkam oleh terbentuknya
senyawa-senyawa yang bersifat refraktorik (sukar diuraiakan di dalam nyala api).
Contoh senyawa refraktorik adalah garam-garam fosfat, silikat, aluminat dari
logam alkali tanah. Dengan terbentuknya senyawa ini, maka akan mengurangi
jumlah atom netral yang ada di dalam nyala. Ionisasi atom-atom di dalam nyala
dapat terjadi jika suhu yang digunakan untuk atomisasi terlalu tinggi. Prinsip
analisis dengan SSA adalah mengukur absorbansi atom-atom netral yang
berada dalam keadaan dasar. Jika terbentuk ion maka akan mengganggu
pengukuan absorbansi atom netral karena atom-atom yang mengalami ionisasi
tidak sama spektrum atom dalam keadaan netral (Gandjar dan Rohman, 2009).
c. Gangguan oleh penyerapan non-atomik (non atomic absorption)
Gangguan jenis ini berarti terjadinya penyerapan cahaya dari sumber
sinar yang bukan berasal dari atom-atom yang akan dianalisis. Penyerapan non
atomik dapat disebabkan oleh adanya penyerapan cahaya oleh partikel-partikel
padat yang berada di dalam nyala (Gandjar dan Rohman, 2009).
2.4 Validasi Metode Analisis
Menurut Harmita (2004), validasi metode analisis adalah suatu tindakan
penilaian terhadap parameter tertentu berdasarkan percobaan laboratorium
penggunaannya. Beberapa parameter analisis yang harus dipertimbangkan
dalam validasi metode analisis adalah sebagai berikut:
a. Kecermatan
Menurut Harmita (2004), kecermatan adalah ukuran yang menunjukkan
derajat kedekatan hasil analisis dengan kadar analit yang sebenarnya.
Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit
yang ditambahkan. Kecermatan ditentukan dengan dua cara, yaitu:
- Metode simulasi
Metode simulasi (Spiked-placebo recovery) merupakan metode yang
dilakukan dengan cara menambahkan sejumlah analit bahan murni ke dalam
suatu bahan pembawa sediaan farmasi (plasebo), lalu campuran tersebut
dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan
(kadar yang sebenarnya) (Harmita, 2004).
- Metode penambahan baku
Metode penambahan baku (standard addition method) merupakan
metode yang dilakukan dengan cara menambahkan sejumlah analit dengan
konsentrasi tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode
yang akan divalidasi. Hasilnya dibandingkan dengan sampel yang dianalisis
tanpa penambahan sejumlah analit. Persen perolehan kembali ditentukan
dengan menentukan berapa persen analit yang ditambahkan ke dalam sampel
dapat ditemukan kembali (Harmita, 2004).
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau
koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang
menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode
dilakukan secara berulang untuk sampel yang homogeny (Harmita, 2004).
c. Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuannya yang
hanya mengukur zat tertentu secara cermat dan seksama dengan adanya
komponen lain yang ada di dalam sampel (Harmita, 2004).
d. Linearitas dan rentang
Linearitas adalah kemampuan metode analisis yang memberikan respon
baik secara langsung maupun dengan bantuan transformasi matematika,
menghasilkan suatu hubungan yang proporsional terhadap konsentrasi analit
dalam sampel (Harmita, 2004).
e. Batas deteksi (Limit of detection) dan batas kuantitasi (Limit of quantitation)
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang
dapat dideteksi yang masih memberikan respon signifikan, sedangkan batas
kuantitasi merupakan kuantitas terkecil analit dalam sampel yang masih dapat
memenuhi kriteria cermat dan seksama (Harmita, 2004).
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Farmasi Kualitatif dan
Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara pada
bulan April 2013 - Juni 2013.
3.2 Bahan-bahan 3.2.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah buah sukun matang
Medan, Sumatera Utara (Gambar dapat dilihat pada Lampiran 2, halaman 42
dan 43).
3.2.2 Pereaksi
Bahan yang digunakan dalam penelitian ini jika tidak dinyatakan lain
mempunyai kualitas pro analis produksi E. Merck yaitu Larutan standar Fe
1000 mcg/ml, larutan baku kalsium 1000 mcg/ml, H2SO4 96% v/v, etanol 96%
v/v, asam nitrat 65% b/v, ammonium tiosianat ≥ 99% b/b, kalium
heksasianoferat (II) trihidrat 99,0-102,0% b/b, dan akuabides (PT.
Ikapharmindo Putramas).
3.3 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah Spektrofotometer
Serapan Atom (Hitachi Z-2000) lengkap dengan lampu Fe dan Ca, tanur
(Philips Harris Ltd.Shenstone), Kertas Whatman no.42, Neraca analitik
(Shimadzu), Botol gelap, Kurs porselen, Cawan penguap, Hot plate (Shott),
Alat-alat gelas (Pyrex dan Oberoi).
3.4 Identifikasi Sampel
Identifikasi buah sukun dilakukan oleh Laboratorium Taksonomi
Tumbuhan Departemen Biologi Fakultas Matematika dan Ilmu Pengetahuan
Alam Universitas Sumatera Utara.
3.5 Pembuatan Pereaksi 3.5.1 Larutan HNO3 (1:1) v/v
Larutan HNO3 (1: 1) dibuat dengan cara mengencerkan 100 ml HNO3
3.5.2 Larutan HNO3 1 N v/v
Larutan HNO3 1 N dibuat dengan cara mengencerkan 69 ml HNO3 65%
diencerkan dengan air suling hingga 1000 ml(Ditjen POM, 1979).
3.5.3 Larutan Kalium Heksasianoferat (II) trihidrat 10% b/v
Larutan Kalium heksasianoferat (II) trihidrat 10% b/v dibuat dengan
cara melarutkan sebanyak 10 g kalium heksasianoferat (II) trihidrat dengan 100
ml air suling (Ditjen POM, 1995).
3.5.4 Larutan Amonium Tiosianat 8% b/v
Larutan Amonium tiosianat 8% b/v dibuat dengan cara melarutkan
sebanyak 8 g Amonium tiosianat dengan 100 ml air suling (Ditjen POM,
1995).
3.5.5 Larutan Asam Sulfat 1 N v/v
Sebanyak 3 ml larutan H2SO4 96 % v/v diencerkan dengan akuades
hingga 100 ml (Ditjen POM, 1979).
3.6 Prosedur Penelitian 3.6.1 Pengambilan Sampel
Metode pengambilan sampel dilakukan dengan cara sampling purposif
yang dikenal juga sebagai sampling pertimbangan dimana sampel ditentukan
atas pertimbangan bahwa populasi sampel adalah homogen dan sampel yang
tidak diambil mempunyai karakteristik yang sama dengan sampel yang sedang
diteliti (Sudjana, 2005).
Sampel yang digunakan adalah buah sukun matang dan buah sukun
sangat matang. Masing-masing buah sukun diambil langsung dari pohon yang
sama dan dikupas kulitnya (buah sukun matang dikupas kulit yang berwarna
hijau setipis mungkin, sedangkan buah sukun sangat matang dikupas dengan
cara dikuliti) kemudian seluruh bagian daging buah dipotong kecil lalu
dihaluskan dengan blender, kemudian ditimbang masing-masing daging buah
sebanyak ± 50 g ke dalam krus porselen (Crussible).
3.6.3 Proses Dekstruksi
Sampel yang telah ditimbang dalam krus porselen (Crussible),
diarangkan di atas hot plate, lalu diabukan dalam tanur dengan temperatur awal
100℃ dan perlahan – lahan temperatur dinaikkan hingga suhu 600℃ dengan
interval 25℃ setiap 5 menit. Pengabuan dilakukan selama 16 jam (dihitung
saat suhu sudah 600℃), lalu setelah suhu tanur ±27℃, krus porselen
dikeluarkan dan dibiarkan hingga dingin pada desikator. Hasil destruksi
ditambahkan 5 ml HNO3 (1:1), kemudian diuapkan pada hot plate sampai
hampir kering. Krus porselen dimasukkan kembali ke dalam tanur dengan
temperatur awal 100℃ dan perlahan – lahan temperatur dinaikkan hingga suhu
600℃ dengan interval 25℃ setiap 5 menit. Pengabuan dilakukan selama 1 jam
dan dibiarkan hingga dingin pada desikator (Helrich, 1990, dengan modifikasi).
Bagan alir proses destruksi dapat dilihat pada Lampiran 3, halaman 44.
3.6.4 Pembuatan larutan Sampel
Sampel hasil destruksi dilarutkan dalam 5 ml HNO3 (1:1), lalu
akuabides sebanyak tiga kali dan dicukupkankan dengan akuabides hingga
garis tanda. Kemudian disaring dengan kertas saring Whatman No. 42 dimana
5 ml filtrat pertama dibuang untuk menjenuhkan kertas saring kemudian filtrat
selanjutnya ditampung ke dalam botol (Helrich, 1990, dengan modifikasi).
Larutan ini digunakan untuk analisis kualitatif dan kuantitatif. Perlakuan yang
sama diulang sebanyak 6 kali untuk masing-masing sampel. Bagan alir
pembuatan larutan sampel dapat dilihat pada Lampiran 4,halaman 45.
3.6.5 Analisis kualitatif
3.6.5.1 Analisis Kualitatif Besi untuk Buah Sukun Matang
3.6.5.1.1 Reaksi warna dengan Kalium heksasianoferat (II) trihidrat
Ke dalam tabung reaksi dimasukkan 2 ml larutan sampel hasil
destruksi, ditambahkan 10 tetes kalium heksasianoferat (II) tihidrat. Dihasilkan
larutan dengan endapan berwarna biru tua (Svehla, 1990).
3.6.5.1.2 Reaksi warna dengan Amonium tiosianat
Ke dalam tabung reaksi dimasukkan 2 ml larutan sampel hasil
destruksi, ditambahkan 3 tetes amonium tiosianat. Dihasilkan larutan berwarna
merah (Svehla, 1990).
3.6.5.2.1 Reaksi warna dengan Kalium heksasianoferat (II) trihidrat
Ke dalam tabung reaksi dimasukkan 2 ml larutan sampel hasil
destruksi, ditambahkan 10 tetes kalium heksasianoferat (II) trihidrat.
Dihasilkan larutan dengan endapan berwarna biru tua (Svehla, 1990).
3.6.5.2.2 Reaksi warna dengan Amonium tiosianat
Ke dalam tabung reaksi dimasukkan 2 ml larutan sampel hasil
destruksi, ditambahkan 3 tetes amonium tiosianat. Dihasilkan larutan berwarna
merah (Svehla, 1990).
3.6.5.3 Analisis Kualitatif Kalsium untuk Buah Sukun Matang 3.6.5.3.1 Reaksi Uji Nyala
Dicelupkan kawat nikel-krom yang sudah bersih (tidak memberikan
nyala yang spesifik) kedalam sampel. Kemudian dibakar di nyala Bunsen. Jika
terdapat kalsium maka nyala akan berwarna merah bata (Svehla, 1990).
3.6.5.3.2 Reaksi kristal kalsium dengan asam sulfat 1 N
Larutan sampel hasil destruksi sebanyak 1-2 tetes, diteteskan pada
objek glas. Kemudian ditetesi dengan larutan asam sulfat 1 N dan etanol 96%
akan terbentuk endapan putih lalu diamati dibawah mikroskop. Terlihat kristal
berbentuk jarum (positif kalsium) (Svehla, 1990).
3.6.5.4.1 Reaksi Uji Nyala
Dicelupkan kawat nikel-krom yang sudah bersih (tidak memberikan
nyala yang spesifik) kedalam sampel. Kemudian dibakar di nyala Bunsen. Jika
terdapat kalsium maka nyala akan berwarna merah bata (Svehla, 1990).
3.6.5.4.2 Reaksi kristal kalsium dengan asam sulfat 1 N
Larutan sampel hasil destruksi sebanyak 1-2 tetes, diteteskan pada
objek glas. Kemudian ditetesi dengan larutan asam sulfat 1 N dan etanol 96%
akan terbentuk endapan putih lalu diamati dibawah mikroskop. Terlihat kristal
berbentuk jarum (positif kalsium) (Svehla, 1990).
3.6.6 Analisis kuantitatif
3.6.6.1 Pembuatan Kurva Kalibrasi Besi
Larutan baku besi (konsentrasi 1000 µ g/ml) dipipet sebanyak 5 ml,
dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda
dengan akuabides (konsentrasi 50 µg/ml). Larutan untuk kurva kalibrasi besi dibuat dengan memipet (1; 2; 3; 4 dan 5) ml larutan baku 50 µg/ml,
masing-masing dimasukkan ke dalam labu tentukur 25 ml dan dicukupkan hingga garis
tanda dengan akuabides (larutan ini mengandung (2,0; 4,0; 6,0; 8,0 dan 10,0)
µg/ml dan diukur absorbansi pada panjang gelombang 248,3 nm dengan nyala
udara-asetilen.
Larutan baku kalsium (konsentrasi 1000 µg/ml) dipipet sebanyak 5 ml,
dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda
dengan akuabides (konsentrasi 100 µg/ml). Larutan untuk kurva kalibrasi
kalsium dibuat dengan memipet (0,5; 1,0; 1,5; 2,0; dan 2,5) ml larutan baku
100 µg/ml, masing-masing dimasukkan ke dalam labu tentukur 25 ml dan
dicukupkan hingga garis tanda dengan akuabides (larutan ini mengandung (2,0;
4,0; 6,0; 8,0 dan 10,0) µg/ml dan diukur absorbansi pada panjang gelombang
422,7 nm dengan nyala udara-asetilen.
3.6.6.3 Penetapan Kadar Besi dan Kalsium dalam Sampel
Sebelum dilakukan penetapan kadar besi dan kalsium dalam sampel,
terlebih dahulu alat spektrofotometer serapan atom dikondisikan sesuai dengan
mineral yang akan diperiksa.
3.6.6.3.1 Penetapan Kadar Besi dalam Buah Sukun Matang
Larutan sampel hasil destruksi dipipet sebanyak 4 ml dimasukkan ke
dalam labu tentukur 10 ml dan dicukupkan dengan akuabides hingga garis
tanda (Faktor pengenceran = 10 ml/4 ml = 2,5 kali). Lalu diukur absorbansinya
dengan menggunakan spektrofotometer serapan atom yang telah dikondisikan,
pada panjang gelombang 248,3 nm dengan nyala udara-asetilen. Nilai
absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan
baku besi. Konsentrasi besi dalam sampel ditentukan berdasarkan persamaan
garis regresi dari kurva kalibrasi.
Larutan sampel hasil destruksi dipipet sebanyak 2 ml dimasukkan ke
dalam labu tentukur 10 ml dan dicukupkan dengan akuabides hingga garis
tanda (Faktor pengenceran = 10 ml/2 ml = 5 kali). Lalu diukur absorbansinya
dengan menggunakan spektrofotometer serapan atom yang telah dikondisikan,
dimana penetapan kadar besi dilakukan pada panjang gelombang 248,3 nm
dengan nyala udara-asetilen. Nilai absorbansi yang diperoleh harus berada
dalam rentang kurva kalibrasi larutan baku besi. Konsentrasi besi dalam
sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.6.6.3.3 Penetapan Kadar Kalsium dalam Buah Sukun Matang
Larutan sampel hasil destruksi dipipet sebanyak 0,25 ml dimasukkan ke
dalam labu tentukur 25 ml dan dicukupkan dengan akuabides sampai garis
tanda (Faktor pengenceran = 25 ml/0,25 ml = 100 kali). Lalu diukur
absorbansinya dengan menggunakan spektrofotometer serapan atom yang telah
dikondisikan, dimana penetapan kadar kalsium dilakukan pada panjang
gelombang 422,7 nm dengan nyala udara-asetilen. Nilai absorbansi yang
diperoleh harus berada dalam rentang kurva kalibrasi larutan baku kalsium.
Konsentrasi kalsium dalam sampel ditentukan berdasarkan persamaan garis
regresi dari kurva kalibrasi.
3.6.6.3.4 Penetapan Kadar Kalsium dalam Buah Sukun Sangat Matang
Larutan sampel hasil destruksi dipipet sebanyak 0,5 ml dimasukkan ke
dalam labu tentukur 25 ml dan dicukupkan dengan akuabides sampai garis
tanda (Faktor pengenceran = 25 ml/0,5 ml = 50 kali). Lalu diukur
dikondisikan, dimana penetapan kadar untuk kalsium dilakukan pada panjang
gelombang 422,7 nm dengan nyala udara-asetilen. Nilai absorbansi yang
diperoleh harus berada dalam rentang kurva kalibrasi larutan baku kalsium.
Konsentrasi kalsium dalam sampel ditentukan berdasarkan persamaan garis
regresi dari kurva kalibrasi.
Kadar mineral besi dan kalsium dalam sampel dapat dihitung dengan
cara sebagai berikut:
n pengencera Faktor
x (g)
Sampel Berat
(ml) Volume x
(µg/ml) i
Konsentras (µg/g)
Logam Kadar
3.6.7 Analisis Data Secara Statistik 3.6.7.1 Penolakan Hasil Pengamatan
Menurut Sudjana (2005), kadar besi dan kalsium yang diperoleh dari
hasil pengukuran masing-masing larutan sampel dianalisis dengan uji distribusi
t dengan rumus:
t hitung =
n SD
X Xi
/
Untuk mencari SD digunakan rumus:
SD =
1 -n
X -Xi 2
Keterangan :
X = Kadar rata-rata sampel
Xi = Kadar sampel
n = Jumlah pengulangan
dan untuk menentukan kadar mineral di dalam sampel dengan interval
kepercayaan 99%, α = 1%, dk = n-1, dapat digunakan rumus:
Kadar Mineral : µ = X ± (t(α/2, dk) x SD / √n )
Keterangan :
X = Kadar rata-rata sampel
SD = Standar Deviasi
n = jumlah pengulangan
α = taraf kepercayaan
dk = Derajat kebebasan (dk = n-1)
3.6.7.2 Pengujian Beda Nilai Rata-Rata Antar Sampel
Menurut Sudjana (2005), sampel yang dibandingkan adalah independen
dan jumlah pengamatan masing-masing lebih kecil dari 30 dan variansi (σ)
tidak diketahui sehingga dilakukan uji F untuk mengetahui apakah variansi
kedua populasi sama (σ1 = σ2)atau berbeda (σ1 ≠ σ2) dengan menggunakan
rumus:
Fo = 2
2 2 1
S S
Keterangan : Fo = Beda nilai yang dihitung
S1 = Standar deviasi terbesar
S2 = Standar deviasi terkecil
Apabila dari hasilnya diperoleh Fo tidak melewati nilai kritis F maka
dilanjutkan uji dengan distribusi t dengan rumus:
(X1– X2)
to =
Sp = �1−1 �1 +2 �2−1 �22
�1+ �2−2
Keterangan :
X1 = kadar rata-rata sampel 1 n 1 = Jumlah pengulangan sampel 1
X2 = kadar rata-rata sampel 2 n 2 = Jumlah pengulangan sampel 2
Sp = Simpangan baku
Jika Fo melewati nilai kritis F, dilanjutkan uji dengan distribusi t dengan rumus
(X1– X2)
to =
Sp√S12/n1 + S22/n2
Keterangan :
X1 = kadar rata-rata sampel 1 S1 = Standar deviasi sampel 1
X2 = kadar rata-rata sampel 2 S2 = Standar deviasi sampel 2
n1 = Jumlah pengulangan sampel 1 n2 = Jumlah pengulangan sampel 2
Kedua sampel dinyatakan berbeda apabila to yang diperoleh melewati
nilai kritis t, dan sebaliknya (Sudjana, 2005).
3.6.8 Uji Perolehan Kembali (Recovery)
Uji perolehan kembali atau recovery dilakukan dengan metode
penambahan larutan standar (standard addition method). Dalam metode ini,
kadar mineral dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan
penentuan kadar mineral dalam sampel setelah penambahan larutan standar
dengan konsentrasi tertentu (Ermer and McB. Miller, 2005). Larutan baku yang
ditambahkan yaitu, 0,25 ml larutan baku besi (konsentrasi 1000 µg/ml) dan 2,5
ml larutan baku kalsium (konsentrasi 1000 µg/ml).
Buah sukun sangat matang yang telah dihaluskan ditimbang secara
larutan baku besi (konsentrasi 1000 µg/ml) dan 2,5 ml larutan baku kalsium
(1000 µg/ml), kemudian dilanjutkan dengan prosedur destruksi kering seperti
yang telah dilakukan sebelumnya.
Menurut Harmita (2004), persen perolehan kembali dapat dihitung
dengan rumus di bawah ini:
Persen Perolehan Kembali = ��−��
��∗
�
100 %
Keterangan : CA = Kadar logam dalam sampel sebelum penambahan baku
CF = Kadar logam dalam sampel setelah penambahan baku
C*A = Kadar larutan baku yang ditambahkan
3.6.9 Simpangan Baku Relatif
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau
koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang
menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode
dilakukan secara berulang untuk sampel yang homogen. Nilai simpangan baku
relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode
yang dilakukan.
Menurut Harmita (2004), simpangan baku relatif dapat dihitung
dengan rumus di bawah ini:
RSD = 100%
X SD
Keterangan :
X = Kadar rata-rata sampel SD = Standar Deviasi
3.6.10 Penentuan Batas Deteksi (Limit of Detection) dan Batas Kuantitasi (Limit of Quantitation)
Menurut Harmita (2004), batas deteksi merupakan jumlah terkecil
analit dalam sampel yang dapat dideteksi yang masih memberikan respon
signifikan. Sedangkan batas kuantitasi merupakan kuantitas terkecil analit
dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama.
Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat
dihitung dengan rumus sebagai berikut:
Simpangan Baku (SY X ) =
2 2
n Yi Y
Batas deteksi (LOD) =
slope X SY x 3
Batas kuantitasi (LOQ) =
slope X SY x 10
BAB IV
HASIL DAN PEMBAHASAN
4.1 Analisis kualitatif
Analisis kualitatif dilakukan sebagai analisis pendahuluan untuk
mengetahui ada atau tidaknya besi dan kalsium dalam sampel. Data dan
[image:49.595.109.322.314.471.2]Gambar dapat dilihat pada Tabel 4 dan Lampiran 5, halaman 46.
Tabel 4. Hasil Analisis Kualitatif
Tingkat Kematangan
Sukun
Ion yang dianalisis
Matang
Kalsium
Asam sulfat 1 N +
etanol 96% Kristal jarum
+
Uji Nyala Nikelkrom Nyala merah bata +
Besi
Kalium heksasianoferat (II)
Larutan dengan endapan biru tua
+
Amonium tiosianat Larutan merah tua +
Sangat
Matang Kalsium
Asam sulfat 1 N +
etanol 96% Kristal jarum
+
Uji Nyala Nikelkrom Nyala merah bata +
Besi
Kalium heksasianoferat (II)
Larutan dengan endapan biru tua
+
Amonium tiosianat Larutan merah tua +
Keterangan : + = Mengandung ion
Tabel 4 di atas menunjukkan bahwa berdasarkan hasil reaksi warna
maupun reaksi kristal dari masing-masing kedua ion tersebut membuktikan
larutan sampel mengandung ion besi dan ion kalsium. Sampel dikatakan positif
mengandung ion kalsium jika menghasilkan endapan putih berbentuk kristal
jarum dengan penambahan asam sulfat 1 N dan etanol 96% v/v dan
memberikan warna merah bata pada uji nyala Nilkel-krom, serta mengandung
ion besi jika menghasilkan endapan berwarna biru tua dengan penambahan
larutan kalium heksasianoferat (II) dan larutan merah dengan penambahan
amonium tiosianat.
Hasil absorbansi dengan spektrofotometer serapan atom menunjukkan
adanya absorbansi pada panjang gelombang besi yaitu 248,3 nm dan kalsium
422,7 nm. Hal ini juga membuktikan secara kualitatif bahwa sampel
mengandung mineral besi dan mineral kalsium.
4.2 Analisis kuantitatif
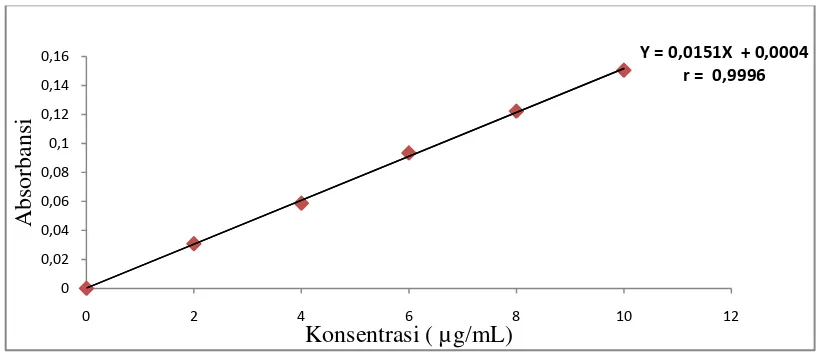
[image:50.595.106.539.98.281.2]Kurva kalibrasi besi dan kalsium diperoleh dengan cara mengukur
absorbansi dari larutan baku besi dan kalsium pada panjang gelombang
[image:51.595.112.521.262.442.2]masing-masing. Hasil kurva kalibrasi besi dan kalsium dapat dilihat pada
Gambar 2 dan 3. Dari pengukuran kurva kalibrasi untuk kedua mineral tersebut
diperoleh persamaan garis regresi yaitu Y = 0,0151X + 0,0004 untuk besi dan
[image:51.595.110.522.267.620.2]Y = 0,0255X + 0,0071 untuk kalsium.
Gambar 2. Kurva kalibrasi Larutan Standar Besi
Gambar 3. Kurva Kalibrasi Larutan Baku Kalsium
Berdasarkan Gambar 2 dan 3 di atas diperoleh hubungan yang linear
antara konsentrasi dengan absorbansi, dengan koefisien korelasi (r) besi 0
0,02 0,04 0,06 0,08 0,1 0,12 0,14 0,16
0 2 4 6 8 10 12
Absor
ba
nsi
Konsentrasi ( µg/mL)
Y = 0,0151X + 0,0004 r = 0,9996
0 0,05 0,1 0,15 0,2 0,25 0,3
0 2 4 6 8 10 12
Absor
ba
nsi
Konsentrasi ( µg/mL)
[image:51.595.114.516.428.642.2]sebesar 0,9996 dan kalsium sebesar 0,9986. Nilai r ≥ 0,97 menunjukkan
adanya korelasi linier yang menyatakan adanya hubungan antara X
(Konsentrasi) dan Y (Absorbansi) (Ermer and McB. Miller, 2005). Data hasil
pengukuran absorbansi larutan baku besi dan kalsium dan perhitungan
persamaan garis regresi dapat dilihat pada Lampiran 7 dan Lampiran 8,
halaman 48,49.
4.2.2 Analisis Kadar Besi dan Kalsium dalam Buah Sukun Matang dan Sangat
Matang
Penentuan kadar besi dan kalsium dilakukan secara spektrofotometri
serapan atom. Konsentrasi mineral besi dan kalsium dalam sampel ditentukan
berdasarkan persamaan garis regresi kurva kalibrasi larutan baku
masing-masing mineral. Faktor pengenceran untuk penentuan kadar besi pada buah
sukun matang adalah sebesar 2,5 kali, dan faktor pengenceran untuk penentuan
kadar besi pada buah sukun sangat matang adalah sebesar 5 kali. Sedangkan
faktor pengenceran untuk penentuan kadar kalsium pada buah sukun matang
adalah sebesar 100 kali, dan faktor pengenceran untuk penentuan kadar
kalsium pada buah sukun sangat matang adalah sebesar 50 kali. Data dan
contoh perhitungan dapat dilihat pada Lampiran 10 dan 11 halaman 51 dan 52.
Analisis dilanjutkan dengan perhitungan statistik (Perhitungan dapat
dilihat pada Lampiran 12 danLampiran 13, halaman 53 dan 56). Hasil analisis
[image:52.595.112.509.683.739.2]kuantitatif mineral besi dan kalsium pada sampel dapat dilihat pada Tabel 5.
Tabel 5. Hasil Analisis Kadar Besi dan Kalsium dalam Sampel
No. Sampel Kadar Besi
(mg/100g)
Kadar Kalsium (mg/100g)
2. BSSM 2,2123 ± 0,0155 13,5377 ± 0,2464
Keterangan :
BSM : Buah Sukun Matang
BSSM: Buah Sukun Sangat Matang
Data yang didapat kemudian diuji kembali secara statistik untuk
mengetahui beda nilai kadar rata-rata mineral antar kedua sampel (Perhitungan
dapat dilihat pada Lampiran 14 dan Lampiran 15, halaman 59 dan 61). Hasil
[image:53.595.113.493.311.464.2]perhitungan uji statistik dapat dilihat pada Tabel 6.
Tabel 6. Hasil Uji Beda nilai rata-rata kadar besi dan kalsium antar sampel
No. Kadar Sampel t hitung t table Hasil
1.
Besi
BSM
-109,1789 -3,1693 Beda
BSSM
2.
Kalsium
BSM
67,0859 0,2713 Beda
BSSM
Keterangan :
BSM : Buah Sukun Matang
BSML : Buah Sukun Sangat Matang
Berdasarkan Tabel 5 dan 6 di atas dapat diketahui bahwa kadar besi
dalam buah sukun sangat matang lebih besar dibandingkan kadar besi di dalam
buah sukun matang sedangkan kadar kalsium lebih besar dalam buah matang
daripada kadar kalsium dalam buah sukun sangat matang. Hal ini karena
kandungan mineral di dalam tanaman dipengaruhi oleh fisiologi tumbuhan
(Lakitan, 2011). Besi merupakan bagian dari protein yang berfungsi sebagai
pembawa elektron pada fase terang fotosintesis dan respirasi. Pada saat buah
sukun masih matang, kulit buah masih berwarna hijau yang artinya
tumbuhan untuk pertumbuhan dan pembentukan biji. Saat buah sukun sudah
matang, maka absorbsi kalsium dari akar menjadi berkurang atau berhenti,
sementara pada buah sukun sangat matang, kadar air bertambah dan kepadatan
daging buah berkurang. Pada buah sukun yang sangat matang, kalsium akan
membentuk garam oksalat dan terdeposit di bagian kulit dalam bentuk
kristal-kristal kalsium oksalat (Dwidjoseputro, 1980).
4.2.3 Uji Perolehan Kembali (Recovery)
Hasil uji perolehan kembali (recovery) kadar besi dan kalsium setelah
penambahan masing-masing larutan baku besi dan kalsium dalam sampel dapat
dilihat pada Lampiran 16,halaman 63. Persen recovery besi dan kalsium dalam
[image:54.595.111.500.406.491.2]sampel dapat dilihat pada Tabel 7.
Tabel 7. Persen Uji Perolehan Kembali (recovery) Kadar besi dan kalsium
No. Mineral yang dianalisis Recovery (%) Syarat rentang persen
recovery (%)
1. Fe 99,68
80-120
2. Ca 101,05
Berdasarkan Tabel 7 di atas, dapat dilihat bahwa rata-rata hasil uji
perolehan kembali (recovery) untuk kandungan besi adalah 99,68%, dan untuk
kandungan kalsium adalah 101,05%. Persen recovery tersebut menunjukkan
kecermatan kerja yang memuaskan pada saat pemeriksaan kadar besi dan kadar
kalsium dalam sampel. Hasil uji perolehan kembali (recovery) ini memenuhi
syarat akurasi yang telah ditetapkan, jika rata-rata hasil perolehan kembali
(recovery) berada pada rentang 80-120% (Ermer and McB. Miller, 2005).
Dari perhitungan yang dilakukan terhadap data hasil pengukuran kadar
mineral besi dan kalsium pada buah sukun, diperoleh nilai simpangan baku
(SD) sebesar 0,0493 mg/100 g untuk mineral besi; 0,1632 mg/100 g untuk