E D O T E M N A I J A K G N E
P NEARI NFRARED(NIR )UNTUK N
A K A P U T U M I S A U L A V
E AYAMBROILER
T A P E C A R A C E
S DANAKURAT
N I M A N O R K U Y S . M
A N A J R A S A C S A P H A L O K E S
R O G O B N A I N A T R E P T U T I T S N I
R O G O B
l u d u
J Tesis : Pengkaijan Metode Nea rInfrared (NIR )un tu Ek valuas i u
t u
M PakanAyamBroliersecaraCepa tdanAkurat a
m a
N : M .SyukronAmin M
I
N : D051050111
s i D etujui
g n i b m i b m e P i s i m o K
. r I .r
D AhmadDarobinLubis ,M.Sc D.rI .rI .WayanBudiasrta ,M .Agr a
u t e
K Anggota
e k i
D tahui:
KetuaDepatremen a.n.DekanSekolahPascaSajranaI PB n
a d i s ir t u N u m
lI Teknolog iPakan S ekretair sProgramMagister
. r I .r
D Ida tGailhPermana , . cMS .Agr D .rI r .NaresworoNugroho ,MS
n a ij U l a g g n a
xxi
DAFTAR ISI
Halaman
DAFTAR TABEL ... xxiii
DAFTAR GAMBAR ... xxv
DAFTAR LAMPIRAN ... xxvii
PENDAHULUAN ... 1
Latar Belakang ... 1
Perumusan Masalah ... 2
Tujuan Penelitian... 3
Manfaat Penelitian... 3
TINJAUAN PUSTAKA ... 5
Pakan Ayam Broiler ... 5
Komposisi Nutrien Pakan ... 6
Near Infrared (NIR) untuk Analisa Pakan Ternak ... 10
MATERI DAN METODE PENELITIAN ... 17
Tempat dan Waktu Penelitian ... 17
Materi Penelitian ... 17
Metode Penelitian ... 17
Preparasi Sampel ... 17
Metode Uji Kimia ... 18
Metode Pengujian Menggunakan NIR ... 23
Uji Banding ... 29
Analisis Data ... 30
HASIL DAN PEMBAHASAN ... 31
Hasil Kalibrasi NIR ... 31
Spektra ... 31
Spektra kadar Air ... 32
Spektra kadar Abu ... 33
Spektra kadar Protein Kasar ... 33
Spektra kadar Lemak Kasar ... 34
Spektra kadar Serat Kasar ... 34
Spektra Kalsium ... 35
Spektra Fosfor ... 35
Hasil Statistik Kalibrasi dan Validasi NIR ... 36
Kadar Air dan Protein Kasar ... 38
Kadar Abu ... 39
Kadar Lemak Kasar, Serat Kasar dan Fosfor ... 40
Kalsium ... 42
xxii
SIMPULAN DAN SARAN... 47
Simpulan ... 47
Saran ... 47
DAFTAR PUSTAKA ... 49
xxiii
DAFTAR TABEL
Halaman
1. Persyaratan mutu pakan ayam broiler starter dan finisher ... 6
2. Metode uji kimia ... 18
3. Jumlah sampel dan spektra untuk kalibrasi NIR ... 31
4. Statistik Hasil Kalibrasi NIR ... 36
5. Statistik Hasil Validasi NIR ... 37
6. Statistik nilai uji metode kalibrasi NIR dan metode kimia serta uji t ... 44
7. Hubungan hasil uji metode kimia dan prediksi kalibrasi NIR
xxv
DAFTAR GAMBAR
Halaman
1. Struktur umum protein ... 8
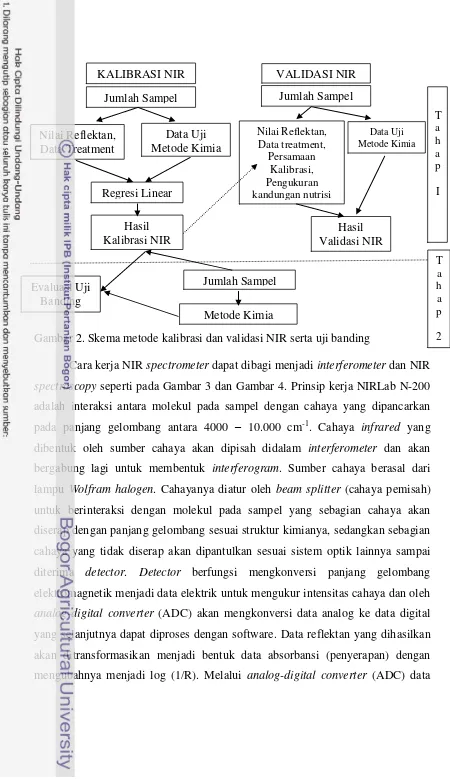
2. Skema metode kalibrasi dan validasi NIR serta uji banding ... 24
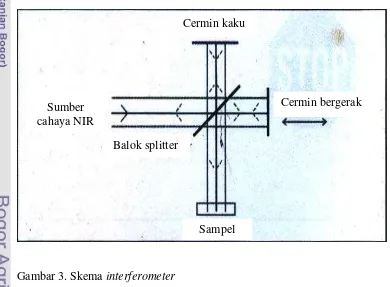
3. Skema interferometer ... 25
4. Skema NIR Spectroscopy ... 26
5. Spektra asli sebelum dilakukan kalibrasi NIR ... 32
6. Spektra kadar Air ... 32
7. Spektra kadar Abu ... 33
8. Spektra kadar Protein Kasar ... 33
9. Spektra kadar Lemak Kasar ... 34
10. Spektra kadar Serat Kasar ... 34
11. Spektra Kalsium ... 35
12. Spektra Fosfor ... 35
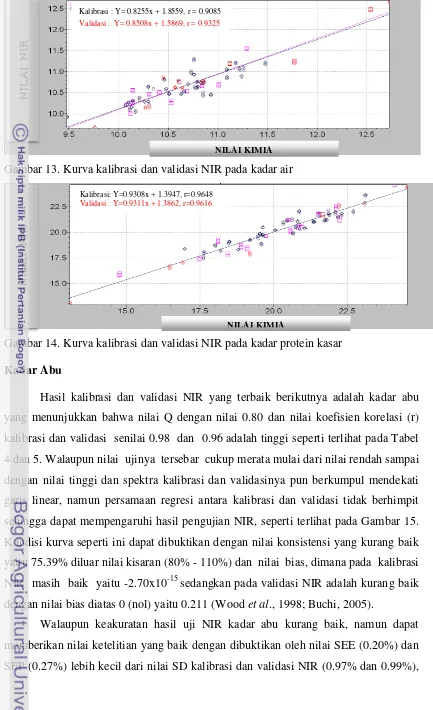
13. Kurva kalibrasi dan validasi NIR pada Kadar Air ... 39
14. Kurva kalibrasi dan validasi NIR pada Kadar Protein Kasar ... 39
15. Kurva kalibrasi dan validasi NIR pada Kadar Abu... 40
16. Kurva kalibrasi dan validasi NIR pada Kadar Lemak Kasar ... 41
17. Kurva kalibrasi dan validasi NIR pada Kadar Serat Kasar ... 41
18. Kurva kalibrasi dan validasi NIR pada Fosfor ... 42
19. Kurva kalibrasi dan validasi NIR pada Kalsium ... 42
xxvii
DAFTAR LAMPIRAN
Halaman
1. Hasil kalibrasi dan validasi NIR pada Kadar Air ... 53
2. Hasil kalibrasi dan validasi NIR pada Kadar Abu ... 55
3. Hasil kalibrasi dan validasi NIR pada Kadar Protein Kasar ... 58
4. Hasil kalibrasi dan validasi NIR pada Kadar Lemak Kasar ... 60
5. Hasil kalibrasi dan validasi NIR pada Kadar Serat Kasar ... 63
6. Hasil kalibrasi dan validasi NIR pada Kalsium ... 65
7. Hasil kalibrasi dan validasi NIR pada Fosfor Total ... 67
8. Hasil uji banding antara hasil uji kimia dengan kalibrasi NIR
kadar air, abu dan protein kasar ... 70
9. Hasil uji banding antara hasil uji kimia dengan kalibrasi NIR
kadar lemak kasar dan serat kasar ... 74
10. Hasil uji banding antara hasil uji kimia dengan kalibrasi NIR
PENDAHULUAN
Latar Belakang
Keberhasilan usaha peternakan sangat dipengaruhi oleh berbagai faktor
antara lain : bibit, pakan, kesehatan hewan, manajemen dan sumberdaya peternak.
Pakan merupakan faktor yang paling berperan dalam usaha peternakan yaitu
sekitar 70 – 80 % dari jumlah biaya produksi. Pada tahun 2009, produksi pakan
tercatat sebesar 9,68 juta ton, tahun 2010 menjadi 10,27 juta ton dan tahun 2011
kebutuhan pakan diperkirakan akan meningkat tipis menjadi 10,30 juta ton
(Natalia 2011). Untuk memenuhi kebutuhan pakan ternak, pada saat ini di
Indonesia terdapat 60 pabrik pakan skala besar di 8 propinsi, yaitu Sumatera Utara
(9 pabrik), Lampung (4 pabrik), Banten (10 pabrik), DKI Jakarta (4 pabrik), Jawa
Barat (8 pabrik), Jawa Tengah (6 pabrik), Jawa Timur (17 pabrik), Sulawesi
Selatan (3 pabrik) (Ditjennak 2009).
Pakan yang diproduksi pabrik pakan yang diedarkan ke agen/distributor
dan peternak diharapkan konsisten mutunya sesuai persyaratan mutu pakan.
Pemerintah mengawasi mutu pakan yang beredar yang mengacu pada Peraturan
Menteri Pertanian no. 65/Permentan/ OT.140/9/2007 tentang Pedoman
Pengawasan Mutu Pakan. Pengujian mutu pakan dilakukan untuk membantu
pengawas mutu pakan atau petugas mutu pakan yang berada di
provinsi/kabupaten/kota dalam melakukan tindak lanjut, apabila ditemukan hasil
uji yang tidak sesuai dengan persyaratan mutu pakan yang berlaku. Oleh karena
itu, hasil pengujian yang diterbitkan lembaga penguji diupayakan secepat
mungkin bisa diterima oleh pengawas mutu pakan atau petugas mutu pakan di
daerah agar kemungkinan terjadinya penyimpangan mutu pakan dapat diantisipasi
dengan baik.
Pengujian mutu pakan dapat dilakukan secara uji fisik, uji kimia dan uji
biologis. Umumnya pengujian yang banyak dilakukan adalah pengujian yang
menggunakan kimia. Parameter uji yang umum dilakukan dalam rangka
pengawasan mutu pakan ayam broiler adalah kadar air, abu, protein kasar, lemak
kasar, serat kasar, kalsium dan fosfor total. Parameter uji ini adalah pengujian
mutu pakan secara kasar yang prosedurnya mengacu pada metode Association of
Hasil uji ini dapat digunakan untuk mengetahui mutu pakan ternak dan akan
disesuaikan dengan persyaratan mutu yang berlaku. Pakan yang bermutu sesuai
standar belum tentu akan memberikan performance ternak yang baik, apabila
tidak sesuai dengan kebutuhan nutrisi ternaknya. Walaupun demikian, pemerintah
menetapkan standar yaitu batas ambang minimal atau maksimal dari kandungan
pakan tersebut untuk mempermudah pengawas/petugas mutu pakan di daerah
dalam melakukan pengawasan mutu pakan.
Metode Near Infrared (NIR) adalah salah satu alternatif cara menguji yang
cepat dan murah. Metode ini pengoperasionalannya tanpa bahan kimia dengan
sampel yang telah digiling pada ukuran partikel 0.75 mm (AOAC 2005).
Kelemahan metode ini adalah tidak dapat langsung digunakan, tetapi terlebih
dahulu dilakukan kalibrasi dan validasi NIR. Metode NIR dapat diterapkan untuk
pengujian, apabila telah dilakukan uji banding dengan metode kimia. Untuk itu
perlu dilakukan suatu pengkajian agar metode NIR ini valid dan dapat digunakan
dalam pengawasan mutu pakan.
Perumusan Masalah
Pakan yang diproduksi pabrik pakan yang beredar di masyarakat belum
secara keseluruhan diawasi mutunya karena pakan yang diambil untuk
pengawasan oleh pemerintah provinsi/kabupaten/kota masih dalam jumlah
terbatas. Hal ini terjadi, karena pakan yang diuji di lembaga penguji
membutuhkan waktu uji lama dan biaya mahal, sehingga pakan yang beredar di
wilayah provinsi/kabupaten/kota dilakukan pengawasan dalam jumlah terbatas.
Berdasarkan data pakan yang diproduksi pabrik pakan menurut SNI
19-0428-1998 tentang petunjuk pengambilan contoh padatan, mestinya dari jumlah
produksi tersebut dilakukan pengujian sekitar 5.187 sampel/tahun dan
kenyataannya pakan ternak yang diuji di Balai Pengujian Mutu Pakan Ternak
(BPMPT) Bekasi, Direktorat Jenderal Peternakan dan Kesehatan Hewan,
Kementerian Pertanian pada tahun 2010 adalah sekitar 2.158 sampel (BPMPT
3
pengujian dalam rangka pengawasan mutu pakan. Belum semua produk pabrik
pakan dilakukan pengawasan mutu pakan karena salah satu faktor penyebabnya
adalah lamanya waktu pengujian.
Pengujian dengan metode kimia tidak dapat memberikan hasil uji yang
cepat, selain peralatannya yang rumit dalam pengoperasian juga perlu tenaga
penguji yang terlatih serta perhatian khusus terhadap penanganan limbah kimia.
Pada saat ini sejumlah teknik instrumentasi yang didasarkan pada sifat
fisik pakan telah dikembangkan yang pekerjaannya cepat dan akurat. Salah satu
teknik tersebut adalah pengukuran reflektan cahaya near infrared (NIR) yang
dipancarkan ke pakan. Keuntungan metode NIR adalah pengukuran yang
dilakukan tanpa persiapan sampel yang rumit pada material yang sudah digiling
atau bentuk tepung, namun bisa juga bentuk utuh (non-destructive), mudah
ditransfer, cepat, murah, beberapa hasil uji pada sampel yang sama, mudah
digunakan dan ramah lingkungan (Buchi 2006).
Selama ini beberapa pabrik pakan dan lembaga penelitian yang
menggunakan alat NIR sebagai metode uji masih menilai prediksi alat NIR
dengan cara kimia. Belum dilakukan uji banding antara hasil kalibrasi NIR
dengan melakukan uji banding antara metode NIR dengan metode kimia untuk
mengukur validitas metode NIR. Untuk itu BPMPT Bekasi ingin memastikan
hasil uji metode NIR dengan metode cara kimia yang lebih akurat pada sampel
yang sama dalam rangka menerapkan kompetensi persyaratan pengujian sesuai
SNI ISO 17025 2008.
Tujuan Penelitian
Tujuan penelitian ini adalah melakukan pengkajian metode NIR untuk
evaluasi mutu pakan ayam broiler secara cepat dan akurat.
Manfaat Penelitian
Hasil penelitian ini diharapkan dapat membantu BPMPT Bekasi, industri
pakan dan peternak dalam mengevaluasi pakan ayam broiler dengan cepat dan
akurat, sehingga apabila terdapat penyimpangan pada pakan tersebut dapat cepat
Ayam broiler merupakan salah satu jenis ternak sumber pangan bagi
manusia yang banyak mengandung gizi. Budidaya ayam broiler agar dapat
berlangsung cepat dan aman untuk konsumsi manusia, maka diperlukan pakan
yang bermutu dengan formulasi pakan pada komposisi zat makanan yang
seimbang sesuai kebutuhan gizi ternak. Pakan adalah campuran dari beberapa
bahan baku pakan, baik yang sudah lengkap maupun yang masih akan dilengkapi,
yang disusun secara khusus untuk dapat dipergunakan sebagai pakan sesuai
dengan jenis ternaknya (Deptan 2007; Mulyantini 2010). Mutu pakan yang baik
harus ada keseimbangan antara protein, energi, vitamin, mineral dan air.
Kebutuhan pakan untuk ayam bergantung pada strain, umur, besar ayam,
aktivitas, suhu lingkungan, kecepatan tumbuh, kesehatan dan imbangan zat pakan.
Zat makanan untuk ternak umumnya terdiri dari 6 jenis, yaitu air, karbohidrat,
protein, lemak, vitamin dan mineral. Untuk mengetahui berapa jumlah zat-zat gizi
yang diperlukan oleh tubuh ternak serta bagaimana menyusun pakan, diperlukan
pengetahuan mengenai mutu dan kuantitas zat-zat gizi. Untuk itu diperlukan
pengujian terhadap kandungan air, mineral, protein kasar, lemak kasar, serat
kasar, asam amino, vitamin dan energi termetabolis (Amrullah 2004; Wahju 1997;
Mulyantini 2010).
Menurut Wahju (1997), faktor-faktor yang mempengaruhi kebutuhan
zat-zat makanan dan yang sangat penting harus diperhatikan adalah
hubungan-hubungan antara : (1) makanan dan genetik; (2) makanan dan penyakit,
cekaman-cekaman lainnya; dan (3) hubungan-hubungan yang menyangkut fungsi-fungsi
khusus seperti mempertahankan mutu daging.
Beberapa perusahaan menggolongkan pakan ayam broiler dalam 3 fase
yaitu pakan fase starter untuk ayam dari umur 1-18 hari, pakan grower 19-30 hari
dan pakan finisher 31-42 hari (Mulyantini 2010). Menurut BSN (2006), jenis
pakan ayam broiler dibedakan menjadi dua jenis yaitu :
1. Pakan ayam broiler starter, biasa disebut BR1 merupakan pakan berbentuk
tepung, pelet atau crumble yang diberikan kepada ayam broiler (ayam
6
2. Pakan ayam broiler finisher, biasa disebut BR2 merupakan pakan berbentuk
tepung, pelet atau crumble yang diberikan kepada ayam broiler (ayam
pedaging) mulai umur 22 hari sampai panen.
Tabel 1. Persyaratan mutu pakan ayam broiler starter dan finisher
No. Jenis pengujian Kandungan nutrisi pakan (%)
Ayam broiler Starter Ayam broiler Finisher
1. Air Max 14 Max 14
2. Abu Max 8 Max 8
3. Protein Kasar Min 19 Min 18
4. Lemak kasar Max 7,40 Max 8
5. Serat Kasar Max 6 Max 6
6. Kalsium 0,90 - 1,20 0,90 - 1,20
7. Fosfor Total 0,60 - 1,00 0,60 - 1,00
Sumber : Badan Standardisasi Nasional (BSN) Tahun 2006
Perbedaan ayam broiler starter dengan finisher terdapat pada kandungan
nutrisinya (Tabel 1). Hal ini mengacu kepada tingkat imbangan energi metabolis
dan protein yang berbeda untuk kedua masa atau umur ayam broiler.
Formula pakan ayam broiler umumnya terdiri dari bahan pakan : jagung
40-50%, bungkil kedelai 25-30%, dedak/pollar 3%, bungkil kelapa 10%, tepung
ikan/tepung daging dan tulang 5 %, minyak kelapa 3 %, mineral
(limestone/dicalsiumphosphat)+vitamin 1-1,5% (Amrullah 2004).
Komposisi Nutrien Pakan
Mutu pakan ayam broiler merupakan faktor yang sangat penting
diperhatikan di dalam industri pakan ternak. Bila suatu pakan tidak memenuhi
persyaratan mutu yang telah ditetapkan, maka pertumbuhan atau produksi ternak
akan tidak sesuai dengan yang diharapkan. Kecuali air, yang hanya satu macam,
kini tidak kurang 15-21 macam mineral, 2 asam lemak, 8-11 asam amino
dianggap esensial bagi hidup ternak. Disamping itu masih terdapat lagi 13-15
vitamin dan bermacam-macam zat makanan yang berupa karbohidrat dan
kompleks dan disederhanakan dengan mengelompokkan zat-zat makanan
berdasarkan sifat fisik dan kimianya. Metode ini dikenal dengan Analisis
Proksimat, yaitu metode terdekat dalam menggambarkan komposisi zat makanan
suatu bahan makanan (Amrullah 2004; Tillman dkk. 1998). Pengujian kimia yang
umum dilakukan pada pakan ayam broiler adalah air, abu, protein kasar, lemak
kasar, serat kasar, kalsium dan fosfor. Pengujian kimia masih menjadi metode uji
yang akurat untuk memberikan hasil uji suatu produk.
Kadar Air
Kadar air dalam pakan berhubungan erat dengan stabilitas pada saat
penyimpanan. Jika pakan ayam broiler yang diproduksi pabrik pakan mengandung
air yang tinggi, maka pabrik pakan akan mengalami kerugian akibat penyusutan.
Kandungan air yang tinggi dapat menyebabkan tumbuhnya bakteri dan jamur
yang dapat menurunkan mutu pakan dan membahayakan ternak yang
mengkonsumsinya. Hal tersebut berakibat menurunkan reputasi pabrik pakan
ternak yang memproduksinya. Oleh karena itu, kadar air dalam pakan perlu
dikontrol (Bates 1993; Tillman dkk. 1998; Amrullah 2004). Menurut BSN (2006),
kandungan air pakan ayam broiler baik starter maupun finisher adalah maksimal
14 %.
Kadar Abu
Kadar abu pada analisis proksimat tidak memberikan nilai nutrisi yang
penting. Jumlah abu dalam makanan hanya penting untuk menentukan
perhitungan BETN. Komponen unsur-unsur mineral dalam bahan makanan yang
berasal dari tanaman sangat bervariasi sehingga nilai abu tidak dapat dipakai
sebagai indeks untuk menentukan jumlah unsur mineral tertentu atau kombinasi
unsur-unsur yang penting. Pada bahan makanan yang berasal dari hewan, kadar
abu berguna sebagai indeks untuk menaksir kadar kalsium dan fosfor. Apabila
kadar abu pakan ayam broiler tinggi, maka nilai mineral terutama kalsium juga
tinggi, begitu sebaliknya, namun agar lebih pasti dilakukan pengujian terhadap
mineral (Tillman dkk. 1998). Menurut BSN (2006) kandungan abu pakan ayam
8
Kadar Protein Kasar
Protein merupakan nutrisi utama yang mengandung nitrogen dan
merupakan unsur utama dari jaringan dan organ tubuh hewan dan juga senyawa
nitrogen lainnya seperti asam nukleat, enzim, hormone, vitamin dan lain-lain.
Protein dibutuhkan sebagai sumber energi utama karena protein ini terus menerus
diperlukan dalam makanan untuk pertumbuhan, produksi ternak dan perbaikan
jaringan yang rusak (Wahju 1998). Menurut BSN (2006), kandungan protein
kasar pakan ayam broiler baik starter maupun finisher adalah berturut-turut
minimal 19 % dan 18 %.
Protein mengandung karbon sebanyak 50–55 %, hidrogen 5-7 % dan
oksigen 20-25 %, juga mengandung nitrogen rata-rata 16 %, sebagian lagi
merupakan unsur sulfur dan sedikit mengandung fosfat dan besi (Perlak I.L.
2009). Protein-protein tersebut dibentuk oleh berbagai kombinasi asam amino
yang terdiri dari 25 atau lebih asam amino yang berikatan dengan ikatan peptida.
Ikatan-ikatan peptida ini dengan berbagai jumlah asam amino menghasilkan
formasi protein seperti pada Gambar 1 (Perry et al. 2003; Tillman dkk. 1998).
COOH O H
R C NH C R
H NH2
Gambar 1. Struktur umum protein
Kadar Lemak Kasar
Lemak dalam pakan ayam broiler digunakan untuk memenuhi kebutuhan
energi pakan, mempertinggi palatabilitas, mencegah pemisahan bahan baku
pakan, menaikkan penyerapan vitamin A dan karoten, mengangkut zat nutrisi non
lemak tertentu, seperti vitamin A, D, E, dan K dan membantu penyerapan
mineral-mineral tertentu, seperti kalsium. Keberadaan lemak juga dapat
menyebabkan pakan menjadi cepat tengik, untuk itu perlu ditambahkan
Faktor kritis yang perlu diperhatikan mengenai lemak yang terkandung di
dalam pakan adalah potensi terjadinya oksidasi selama penyimpanan. Hal ini
disebabkan oleh rasio antara hidrogen dan oksigen pada lemak sangat besar,
sehingga potensi terjadinya pengikatan oksigen menjadi besar. Pengikatan
oksigen di titik dimana adanya ikatan rangkap pada asam lemak tidak jenuh
menyebabkan terbentuknya aldehid dan keton. Aldehid dan keton ini
menyebabkan bau tengik pada pakan (Perry et al. 2003). Menurut BSN (2006),
kandungan lemak kasar pakan ayam broiler baik starter maupun finisher adalah
berturut-turut minimal 7,4 % dan 8 %.
Kadar Serat Kasar
Karbohidrat bermacam-macam jenisnya dan berbeda-beda pula
manfaatnya bagi tubuh. Karbohidrat menjadi dua komponen yaitu serat kasar
yang sukar dicerna dan bahan ekstrak tanpa nitrogen (BETN) yang bersifat mudah
dicerna. Serat kasar adalah karbohidrat yang tidak larut setelah dimasak oleh asam
dan basa. Serat kasar diduga kaya akan lignin dan selulosa sehingga sulit dicerna
oleh monogastrik, sebaliknya BETN yang berisi zat-zat mono, di, tri, dan
polisakaride terutama pati dan kesemuanya mudah larut dalam larutan asam dan
basa mempunyai daya cerna yang tinggi. Serat kasar terdiri dari hemiselulosa,
selulosa dan lignin. Ayam dapat menggunakan hemiselulosa sebagai sumber
energi tapi dalam keadaan terbatas, karena ayam tidak mempunyai enzim selulose.
Pakan yang mengandung serat yang tinggi akan menurunkan mutu nutrisi dan
palatabilitas ternak. Pakan yang lebih tinggi kandungan serat kasarnya lebih amba
dan umumnya lebih rendah nilai energinya. (Tillman dkk. 1998; Amrullah 2004).
Menurut BSN (2006), kandungan serat kasar pakan ayam broiler baik starter
maupun finisher adalah maksimal 6 %.
Kalsium dan Fosfor
Mineral dibutuhkan dalam jumlah kecil, tetapi peranannya mencakup
seluruh fungsi pengelolaan, pertumbuhan dan produksi. Terdapat 16 mineral
esensial yang dibagi menjadi dua golongan, yaitu 7 macam mineral makro dan 9
macam mineral mikro. Pembagian ini didasarkan kepada konsentrasi yang
10
ayam broiler adalah kalsium dan fosfor total. Mineral ini berfungsi membantu
pembentukan dan pemeliharaan struktur kerangka tubuh, sistem-sistem enzim,
transpor energi, pembekuan darah, kontraksi otot dan saraf serta keseimbangan
asam basa. Kelebihan kalsium akan mengganggu penggunaan magnesium,
mangan dan seng serta menyebabkan terbentuknya Ca3(PO4)2 tak larut, yang akan
menyebabkan defisiensi fosfor. Kekurangan Ca dan P akan mengalami gangguan
pada tulang dan paruh, lunaknya tulang, lemahnya urat daging dan pertumbuhan
terhambat (Tillman dkk. 1998; Amrullah 2004).
Menurut Mulyantini (2010), kebutuhan mineral, khususnya Ca dan P
sangat mungkin akan banyak direvisi apabila fitase, enzim pendagradasi kompleks
mioinositol, dipertimbangkan perannya dalam pakan. Kalsium dan P merupakan
mineral esensial yang saling berhubungan dalam proses biologis unggas. Oleh
karena itu imbangan kedua mineral tersebut sangat penting. Level P dapat
berpengaruh terhadap penyerapan Ca. Imbangan optimum Ca dan P tersedia
dalam pakan unggas berkisar 1:1 sampai 2:1. Vitamin D dapat membantu
penyerapan kalsium.
Menurut BSN (2006), kandungan kalsium dan fosfor total pakan ayam
broiler baik starter maupun finisher adalah berturut-turut 0,9-1,2 % dan 0,6-1 %.
Near Infrared (NIR) untuk Analisa Pakan Ternak
Metode NIR dapat diterapkan dalam pengujian, apabila telah dilakukan
validasi metode yaitu membandingkannya dengan metode kimia. Untuk itu perlu
dilakukan suatu pengkajian agar metode NIR ini valid dan dapat digunakan dalam
pengawasan mutu pakan di daerah.
Prinsip kerja NIR adalah bila suatu radiasi berinteraksi dengan sampel, ia
akan diabsorpsi, diteruskan atau dipantulkan. Hukum konservasi energi
memungkinkan kejadian tersebut dapat diperhitungkan. Total energi radiasi pada
sampel sama dengan jumlah energi yang diabsorbsi, diteruskan dan dipantulkan.
Dengan demikian bila energi yang dipantulkan dapat diukur dan energi yang
diteruskan diatur supaya mempunyai nilai nol maka energi yang diabsorbsi dapat
Suatu molekul mempunyai energi dalam berbagai bentuk misalnya energi
vibrasi yang disebabkan perubahan periodik pada atomnya dari posisi
kesetimbangannya. Di samping itu molekul juga mempunyai energi rotasi
berdasarkan atas perputaran terhadap pusat gravitasinya. Besarnya perbedaan
energi vibrasi dan rotasi pada molekul yang diradiasi akan mempengaruhi
absorbsi near infrared (Adrizal 2007)
Data absorbsi near infrared sangat potensial digunakan untuk analisis
mutu pakan ternak. Keuntungan penggunaan near infrared adalah cepat, murah,
persiapan sampel sederhana, tanpa menggunakan bahan kimia (Leeson &
Summers 1997, 2001; Fontaine et al. 2001; Farrel 1999; Wrigley 1999). Prediksi
dengan metode ini hanya membutuhkan beberapa gram sampel dalam bentuk
tepung dengan ketebalan sampel pada cawan petri minimal 1 mm sampai dengan
7 mm, kemudian disinari menggunakan near infrared. Data reflektan dari
penyinaran tersebut dikonversi menjadi nilai absorbsi, kemudian digunakan untuk
memprediksi komposisi kandungan pakan. Kalibrasi hubungan antara data
absorbsi near infrared dengan masing-masing kandungan gizi pakan adalah
sangat penting. Proses kalibrasi membutuhkan sampel yang banyak dan algoritma
yang sesuai, tetapi bila proses kalibrasi telah selesai maka proses analisis untuk
setiap sampel membutuhkan waktu beberapa menit saja sekitar 10 menit
(Williams & Norris 1990; Osborne et al. 1993).
Basis near infrared spectroscopy adalah chemometric yang
mengaplikasikan matematika ke analisis kimia. Teknik ini merupakan integrasi
spectroscopy, statistik dan ilmu komputer. Model matematika dibangun atas dasar
hubungan antara komposisi kimia dengan absorbansi radiasi sinar near infrared
pada panjang gelombang antara 4000 – 10.000 cm-1 . Pada spektrum tersebut kita
mengukur terutama vibrasi hidrogen pada ikatan kimia dimana hidrogen terikat
dengan atom lain seperti nitrogen, oksigen dan karbon. Pada umumnya pakan
ternak tidak tembus cahaya, oleh sebab itu analisis near infrared cenderung
menggunakan reflektan daripada transmitan. Cahaya yang dipantulkan oleh
sampel digunakan secara tidak langsung untuk mengukur jumlah energi yang
diabsorbsi oleh sampel. Analisis near infrared mengukur absorbs radiasi oleh
12
gelombang tertentu. Komponen lain juga mengabsorbsi energi, namun bersifat
mengganggu. Untuk mengurangi efek tersebut dilakukan perlakuan matematik
dan regresi linear atau prosedur statistik lainnya pada data tersebut (Williams &
Norris 1990; Osborne et al. 1993).
Menurut Buchi (2006), metode kalibrasi yang banyak digunakan adalah
Multiple Linear Regression (MLR), Principal Component Regression (PCR), dan
Partial Least Squares Regression (PLS). MLR adalah metode penetapan
kuantitatif yang klasik, dimana sudah banyak yang tidak menggunakan lagi.
Metode ini adalah kalibrasi multivariat, dimana tujuannya adalah untuk
memprediksi konsentrasi konstituen berdasarkan pada spektrumnya untuk
mendapatkan persamaan regresi dari semua dimensi secara sederhana. Panjang
gelombang yang digunakan adalah 4000 – 10.000 cm-1.
Menurut Harjono (2008), Principal components analysis (PCA) secara
umum dikenal sebagai teknik interprestasi multivariat, dimana “the loading”
dipilih untuk menjelaskan secara maksimal keragaman di dalam variabel. Akan
tetapi, kita akan mempertimbangkan disini sebagai alat statistik melalui
penggunaan komponen-komponen yang diturunkan adalam sebuah model regresi
untuk memprediksi variabel respon yang tidak teramati menggunakan komponen
utama. Komponen utama bertujuan untuk menjelaskan sebanyak mungkin
keragaman data dengan kombinasi linier yang ditemukan yang saling bebas satu
sama lain dan didalam arah keragaman paling besar. Tiap-tiap komponen utama
merupakan kombinasi linier dari semua variabel. Komponen utama pertama
menjelaskan variasi terbesar dari data diikuti dengan komponen utama kedua dan
seterusnya. Terdapat komponen utama yang jumlahnya sama dengan jumlah
variabel yang ada, tetapi biasanya hanya memilih sedikit komponen utama
pertama untuk analisis regresi.
Partial least squares (PLS) adalah sebuah metode reduksi dimensi data,
sejenis dengan PCA, untuk mencari faktor-faktor yang paling relevan dalam
memprediksi dan menginterprestasi data. Regresi PLS meningkatkan
kemampuannya model dari PCA dengan menggunakan variabel respon secara
aktif dalam dekomposisi bilinier prediktor. PCA terfokus pada keragaman di
prediktor-prediktor. Dengan jalan menyeimbangkan informasi antara prediktor
dan respon, PLS mereduksi dampak dari banyaknya prediktor yang tidak relevan
dengan keragaman data. Estimasi kesalahan prediktor ditingkatkan dengan cara
validasi silang. PCA yang dilanjutkan dengan pemodelan regresi dan PLS-R
dapat diterapkan untuk kalibrasi yang melibatkan dimensi prediktor relatif besar
dengan respon yang relatif sedikit.
Principal Component Regression (PCR) merupakan teknik analisis
multivariat yang dilakukan dengan terlebih dahulu mereduksi komponen dengan
teknik Principal omponent Analysis (PCA) dilanjutkan dengan teknik analisis
regresi antara komponen utama yang baru terhadap respon. PCA telah mulai
dilakukan oleh Pearson (1901) dan kemudian dikembangkan oleh Hotelling
(1933). Aplikasi dari PCA didiskusikan oleh Rao (1964), Cooley dan Lohnes
(1971), dan Gnanadesikan (1977). Perlakuan statistik yang menakjubkan dengan
PCA ditemukan oleh Kshirsagar (1972), Morrison (1976), dan Mardia, Kent, dan
Bibby (1979).
PCR secara khas digunakan untuk model-model regresi linier, dimana
jumlah variabel bebas (prediktor) p adalah sangat banyak, atau dimana antar
prediktor berkorelasi tinggi (multikolinieritas). Salah satu aplikasi PCR yang
cukup penting adalah kalibrasi multivariat, dimana tujuannya adalah untuk
memprediksi konsentrasi konstituen berdasarkan pada spektrumnya. Spektrum
secara khas terdiri dari nilai-nilai yang menjangkau panjang gelombang dengan
kisaran yang luas, sehingga terdiri dari ratusan komponen yang harus dianalisis,
sedangkan faktor konsentrasi umumnya terbatas.
Keuntungan utama dari kalibrasi PCR adalah sebagai berikut:
a. Dekomposisi dari matrik absorbansi menjadi matrik ortogonal yang lebih kecil
memungkinkan terjadinya pengurangan permasalahan dimensional dalam
kasus sistem yang dikondisikan buruk. Jadi, jika terdapat spektrum dengan
korelasi yang tinggi, kita akan selalu memperoleh solusi yang terbaik dalam
hal matrik yang mendekati tunggal.
b. Komponen tambahan yang tidak diketahui atau komponen background dapat
secara otomatis dimodelkan sebagai komponen utama jika konsentrasi dari
14
Partial Least-squared regression (PLS-R) pertama kali dikembangkan
oleh Herman Wold, yang tertarik pada aplikasi untuk ilmu sosial khususnya
bidang ekonomi. Namun demikian, PLS-R pertama kali dipopulerkan oleh ahli
kimia dan telah digunakan untuk mengatasi permasalahan kalibrasi dengan
dimensi yang besar, sebagai contoh penggunaan jumlah pengukuran reflektan
yang banyak untuk mengestimasi konsentrasi suatu larutan. PLS juga telah
digunakan oleh Davies dalam kalibrasi multivariat pada angka oktan
menggunakan 226 panjang gelombang NIR.
PLS-R adalah sama dengan PCR yang bertujuan untuk mengestimasi
koefisien regresi dalam model regresi linier dimana terdapat jumlah variabel x
dengan multikolinieritas yang tinggi. Dalam tahap pertama PCR, skor diperoleh
dengan mengekstraksi informasi yang ada didalam variabel x dengan menerapkan
analisis komponen utama (PCA) tanpa menggunakan informasi apapun mengenai
variabel y. Sebaliknya, skor dalam PLS-R dihitung dengan memaksimalkan
kriteria kovarian antara variabel x dan y sehingga dalam teknik ini respon telah
dilibatkan dalam analisis sejak awal. PLS dapat menangani multikolinieritas,
jumlah prediktor yang banyak, dan akibat fokus prediksi, bukan penjelasan, tidak
adanya pemahaman yang baik mengenai hubungan respon terhadap prediktor
tidak menjadi suatu masalah.
Keunggulan utama dari metode PLS-R didasarkan pada proses
dekomposisi matrik konsentrasi C dan matrik absorbansi A yang saling
berhubungan, sehingga dengan algoritma ini dapat diperoleh model kalibrasi yang
sempurna.
Fontaine et al. (2001), telah menggunakan NIR untuk memprediksi
kandungan asam amino esensial beberapa bahan pakan yaitu kedelai, rapeseed
meal, tepung biji bunga matahari, kacang polong, tepung ikan, tepung daging dan
tepung produk samping pemotongan ayam (poultry meal). Kalibrasi dilakukan
dengan Modified Partial Least Squares Regression (MPLS). Hasil terbaik dari
kalibrasi dan validasi untuk tepung ikan menunjukkan koefisien korelasi (r)
berkisar antara 0,92 – 0,96. Hasil validasi menunjukkan koefisien determinasi
(R2) sebesar 0,89 – 0,93. SEC berkisar 0,026 % - 1.545 % untuk koefisien
Valdes dan Leesons (1992), telah menggunakan NIR dengan metode
MPLS untuk memprediksi kandungan energi metabolis pada pakan unggas dan
menunjukkan nilai SEP yaitu 58 kkal/kg pakan dari rata-rata 2996 kkal/kg dan
standar deviasi (SD) sebesar 211 kkal/kg. Cozzolino dan Moron (2004), telah
menggunakan NIR dengan metode MPLS untuk memprediksi kandungan trace
mineral dari bahan pakan leguminosa di Uruguay. Hasil yang diperoleh adalah
akurasi yang masih rendah dimana rasio SD/SEP berkisar antara 1.61 sampai
3.70. Prediksi komposisi nutrien pakan kelinci telah dilakukan oleh Xiccato et al.
(1999) dengan mendapatkan nilai SEC dan SEP protein sebesar 0.75 % dan
MATERI DAN METODE PENELITIAN
Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Balai Pengujian Mutu Pakan
Ternak (BPMPT) – Kecamatan Setu, Kabupaten Bekasi dan beberapa
laboratorium pabrik pakan. Penelitian ini dilakukan pada bulan Juni 2008 sampai
dengan bulan Maret 2010.
Materi Penelitian
Bahan penelitian yang digunakan adalah pakan ayam broiler starter (BR1)
dan finisher (BR2) dari berbagai pabrik pakan di Indonesia. Bahan yang
digunakan adalah Kjeltec tablet, H2SO4, NaOH, methyl merah dan biru, H3BO3,
HCl (Protein kasar), heksan, selongsong lemak (Lemak kasar), H2SO4, NaOH,
etanol, kertas saring (serat kasar), HCl, HNO3, La2O3, NH4OH, standar kalsium
(Kalsium), Ammonium molibdat – vanadat, HClO4, dan standar fosfor (Fosfor).
Peralatan penelitian yang digunakan adalah oven, tanur, digestor protein,
kjeltec destilasi, buret, soctex, kompor serat kasar, spektrofotometer, atomic
absorption spectrophotometer (AAS) dan Near Infrared (NIR) merk Buchi
NIRLab N-200.
Metode Penelitian
Preparasi Sampel
Pakan ayam broiler starter (BR1) dan finisher (BR2) dari beberapa produk
pabrik pakan dikumpulkan minimal 60 sampel. Sampel tersebut diperoleh dari
sampel yang datang ke BPMPT Bekasi sebagai pelanggan dan dari beberapa
pabrik pakan yang disertai dengan hasil ujinya. Selanjutnya semua pakan
dilakukan pengujian kimia dengan mengacu metode Association of Official
Analytical Chemists (AOAC), metode pabrik pakan atau Standar Nasional
Indonesia (SNI) yang dikerjakan di BPMPT Bekasi dan laboratorium beberapa
pabrik pakan seperti pada Tabel 2. Jenis pengujian yang dilakukan adalah kadar
Tabel 2. Metode uji kimia
Jenis uji Metode uji kimia
Air Oven 105 ºC, 3 jam
Abu Tanur 600 ºC, 2 jam
Protein kasar Kjeldahl, katalis Cu, H3BO4 4%, HCl 0,1 N
Lemak kasar Soctex, pelarut heksan
Serat kasar Ekstraksi H2SO4 1,25% dan NaOH 3,25 %
Kalsium AAS
Fosfor Spektrofotometer
Metode Uji Kimia
Metode Pengujian Kadar Air
Penentuan kadar air menurut SNI 01-2891-1992 butir 5.1 adalah untuk
mengetahui persentase kadar air yang terkandung dalam pakan. Prinsip metode uji
ini adalah kehilangan berat pada pemanasan selama 3 jam menggunakan oven
pada suhu 105 ºC dianggap sebagai kadar air yang terdapat pada pakan.
Sampel ditimbang sebanyak 2 gram dimasukkan ke dalam vochdoos dan
dipanaskan sesuai metode uji. Berat sampel setelah dipanaskan dicatat sampai
bobot konstan dengan selisih penimbangan 10 mg. Kadar air dihitung dengan
rumus :
W1 - W2
Kadar Air = x 100 % ……...…...……...………...……….. 1
W
dimana W = berat sampel (g)
W1 = berat sampel sebelum dikeringkan (g)
W2 = berat sampel setelah dipanaskan (g)
Metode Pengujian Kadar Abu
Metode uji penentuan kadar abu menurut Association of Official Analytical
Chemists (AOAC 2005) Metode 942.05, adalah untuk mengetahui persentase
kadar abu yang terkandung dalam pakan. Prinsip metode uji ini adalah proses
19
organik diuraikan menjadi H2O, CO2 dan gas lain yang menguap, sedangkan
sisanya yang tertinggal adalah berupa oksida mineral (abu).
Sampel ditimbang sebanyak 2 gram dimasukkan ke dalam crusibel dan
dipanaskan sesuai metode uji. Berat sampel setelah dipanaskan dicatat sampai
bobot konstan dengan selisih penimbangan 10 mg. Kadar abu dihitung dengan
rumus :
W2 - W1
Kadar Abu = x 100 % ….……...………...……….. 2
W
dimana W = berat sampel (g)
W1 = berat crusibel kosong setelah dipanaskan (g)
W2 = berat crusibel + sampel setelah dipanaskan (g)
Metode Pengujian Kada Protein Kasar
Metode uji penentuan kadar protein kasar menurut Association of Official
Analytical Chemists (AOAC 2005) Metode 2001.11 (Kjeldahl), adalah untuk
mengetahui persentase kadar protein kasar yang terkandung dalam pakan. Prinsip
metode uji ini adalah pengubahan N menjadi NH3 dengan proses destruksi,
destilasi dan titrasi.
Sampel ditimbang sekitar 0,5-1 gram dimasukkan ke dalam tabung
destruksi 250 ml, ditambahkan 2 tablet katalisator (kjeltab Cu) atau 7 g
CuSO4.5H2O + 0,8 g K2SO4, lalu ditambahkan 15 ml H2SO4 97% dan dipanaskan
dengan kompor digestor pada suhu 420ºC dalam lemari asam selama 1 jam atau
sampai larutan menjadi biru jernih, kemudian didinginkan. Pindahkan tabung
destruksi ke alat destilasi (Kjeltec), tambahkan akuades 75 ml dan 60 ml NaOH
40%. Letakkan larutan penerima pada erlenmeyer 250 ml yang berisi 25 ml
larutan H3BO4 4% dan 3 tetes mix indicator (campuran 0,0667 g metil biru dan
0,1333 g metil merah, kemudian dilarutkan dengan ethanol sampai 100 ml sampai
homogen), kemudian lakukan destilasi sampai tertampung kira-kira 150 ml
destilat dalam erlenmeyer. Larutan destilat dititrasi dengan HCl 0,1N sampai
terjadi perubahan warna menjadi abu-abu. Lakukan juga penetapan blanko. Kadar
nitrogen (N %) dihitung dengan rumus :
(ml HCl – ml blanko) x normalitas HCl x 14.007
N (%) = x 100 % ….….. 3 mg sampel
Berdasarkan persentase N dapat ditentukan kadar protein kasar dengan persamaan
4 berikut :
Protein kasar (%) = % N x 6,25 ………..………. 4
Metode Pengujian Lemak Kasar
Metode uji penentuan kadar lemak kasar menurut AOAC Metode 2003.06
(AOAC 2005) ekstraksinya menggunakan soxtec, adalah untuk mengetahui
persentase kadar lemak kasar yang terkandung dalam pakan. Prinsip metode uji
ini adalah lemak dapat diekstraksi dengan menggunakan heksan/zat pelarut lemak
lainnya, bila zat pelarutnya diuapkan maka akan tertinggal lemak kasarnya.
Sampel ditimbang sebanyak 2 gram dimasukkan ke dalam selongsong
kertas, lalu ditutup dengan kapas non lemak dan masukkan ke dalam alat soxtec.
Letakkan wadah lemak berisi heksan 70 ml pada alat soxtec dan selongsong kertas
yang berisi sampel harus terendam heksan. Lakukan ekstraksi selama 1 jam pada
suhu 140 ºC dengan tahapan pembakaran 20 menit, pencucian 30 menit dan
penguapan 10 menit. Selanjutnya wadah yang berisi lemak hasil ekstraksi
dipanaskan dalam oven pada suhu 105 ºC selama 1 jam. Berat sampel setelah
dipanaskan dicatat sampai bobot konstan dengan selisih penimbangan 10 mg.
Kadar lemak kasar dihitung dengan rumus :
W2 - W1
Kadar lemak kasar = x 100 % ….………...……….……….. 5 W
dimana W = berat sampel (g)
W1 = berat wadah lemak kosong setelah dipanaskan (g)
W2 = berat wadah lemak + sampel setelah dipanaskan (g)
Metode Pengujian Kadar Serat Kasar
Metode uji penentuan kadar serat kasar menurut SNI 01-2891-1992 butir
21
pakan. Prinsip metode uji ini adalah semua senyawa organik akan larut dalam
perebusan dengan H2SO4 1,25 % dan NaOH 3,25 % kecuali serat kasar dan abu,
bila ampas yang tidak larut kemudian dibakar sempurna maka serat kasarnya akan
menguap menjadi gas dan sisanya berupa abu.
Sampel ditimbang sebanyak 2 gram dimasukkan ke dalam beaker gelas
500 ml, lalu penghilangan lemak dengan ditambah heksan 15 ml lalu larutan
lemak yang ada di bagian atas dibuang dan sampel didiamkan sampai kering, lalu
direbus/ekstraksi dengan ditambah 50 ml H2SO4 1,25 % selama 30 menit dan 50
ml NaOH 3,25 % selama 30 menit selanjutnya disaring dengan kertas saring no.41
dan bilas sampai netral secara beturut-turut dengan larutan H2SO4 1,25% panas,
akuades panas dan ethanol secukupnya. Setelah itu lakukan pemanasan dan
pembakaran sampel. Kertas saring berisi sampel dimasukkan ke dalam crusibel
untuk dipanaskan didalam oven pada suhu 105 ºC selama 2-3 jam dan selanjutnya
dibakar didalam tanur pada suhu 550ºC selama 2 jam. Berat sampel setelah
dipanaskan dicatat sampai bobot konstan dengan selisih penimbangan 10 mg.
Kadar serat kasar dihitung dengan rumus :
W1 - W2 - B
Kadar serat kasar = x 100 % ……….……….. 6 W
dimana W = berat sampel (g)
W1 = berat crucibel + sampel setelah dipanaskan oven (g)
W2 = berat crusibel + sampel setelah dibakar tanur (g)
B = berat kertas saring setelah dioven (g)
Metode Pengujian Kadar Kalsium
Metode uji penentuan kadar kalsium menurut AOAC metode 968.08
(AOAC 2005), adalah untuk mengetahui persentase kadar kalsium yang
terkandung dalam pakan. Prinsip metode uji ini adalah abu sampel yang
dilarutkan dalam asam ditambahkan dengan lanthanum oksida untuk mencegah
terbentuknya ion selain kalsium pada saat penetapan dengan menggunakan alat
Atomic Absorption Spectrophotometer (AAS).
Penentuan kadar kalsium diawali dengan pengabuan sampel pada suhu 550
dipanaskan selama 10 menit pada suhu 70-80 ºC, dilanjutkan pembuatan larutan
sampel pada labu takar dengan menyaring larutan tersebut dan dibilas dengan
akuades sampai volume 200 ml. Membuat larutan kurva standard pada
konsentrasi 0, 2, 4, 8, 12, 16 dan 20 mg/l dan ambil 2-5 ml dari larutan sampel,
masing – masing dimasukkan pada labu takar 50 ml yang sudah ditambahi larutan
lanthanum oksida (La2O3) sebanyak 10 ml, lalu dibaca dengan alat Atomic
Absorption Spectrophotometer (AAS) yang sudah diverifikasi. Kadar kalsium
dihitung dengan rumus :
C xV1 x V3
Kadar kalsium = ………...………..……….. 7 W x V2 x 10.000
dimana W = berat sampel (g)
V1 = volume larutan sampel (ml)
V2 = volume larutan yang diambil dari larutan sampel (ml)
V3 = volume larutan sampel final yang akan dibaca AAS (ml)
C = konsentrasi sampel (mg/l) diambil dari persamaan
linear,yaitu:
C = (y-a)/b, dimana y = absorbansi sampel,
b = slope dan
a = intercept
10.000 = nilai konstanta hasil konversi dari mg/l menjadi persen (%)
Metode Pengujian Kadar Fosfor
Metode uji penentuan kadar fosfor menurut AOAC metode 965.17
(AOAC, 2005), adalah persentase kadar fosfor yang terkandung dalam pakan.
Prinsip metode ini adalah abu sampel yang dilarutkan dalam asam ditambahkan
dengan larutan molybdate-vanadate untuk memberikan warna yang dapat diserap
sinar yang dipancarkan oleh spektrofotometer pada panjang gelombang tertentu.
Penentuan kadar fosfor sama seperti kadar kalsium sampai pada proses
pembuatan larutan sampel yang diawali dengan pengabuan sampel sampai
memperoleh larutan sampel 200 ml. Membuat larutan kurva standard pada
konsentrasi 0, 2, 4, 8 dan 12 mg/l dan ambil 5-10 ml dari larutan sampel, masing –
23
molybdate-vanadate sebanyak 10 ml, lalu dibaca dengan alat spektrofotometer
yang sudah dikalibrasi. Kadar fosfor dihitung dengan rumus :
C xV1 x V3
Kadar fosfor = ………..………..…….….. 8 W x V2 x 10.000
dimana W = berat sampel (g)
V1 = volume larutan sampel (ml)
V2 = volume larutan yang diambil dari larutan sampel (ml)
V3 = volume larutan sampel final yang akan dibaca (ml)
C = konsentrasi sampel (mg/l) diambil dari persamaan linear,
C = (y-a)/b, dimana y= absorbansi sampel,
b= slope,
a= intercept
10.000 = nilai konstanta hasil konversi dari mg/l menjadi persen (%)
Metode Pengujian menggunakan NIR
Kalibrasi NIR
Kalibrasi NIR merupakan tahapan pertama sebelum alat NIR digunakan.
Hasil uji kimia dan sampel pakan yang mencukupi minimal 60 sampel dalam
keadaan sudah halus dengan ukuran partikel 0.75 mm, dimasukkan pada cawan
petri secukupnya dan ditekan, lalu dimasukkan ke alat NIR. Data tersebut akan
diubah menjadi spektrum. Kumpulan spektrum/spektra dibagi menjadi 2 (dua)
yaitu 2/3 bagian untuk kalibrasi NIR dan 1/3 bagian untuk validasi. Validasi NIR
bertujuan untuk memastikan bahwa kalibrasi NIR sudah baik dan dapat digunakan
sebagai alat pengujian. Parameter yang digunakan dalam menganalisa kalibrasi
NIR adalah nilai Q, koefisien korelasi (r), Standard Error of Estimation (SEE),
Standard Error of Prediction (SEP), konsistensi, bias dan metode NIR yaitu
Principle Component Regression (PCR) dan Partial Least Squares Regression
Gambar 2. Skema metode kalibrasi dan validasi NIR serta uji banding
Cara kerja NIR spectrometer dapat dibagi menjadi interferometer dan NIR
spectroscopy seperti pada Gambar 3 dan Gambar 4. Prinsip kerja NIRLab N-200
adalah interaksi antara molekul pada sampel dengan cahaya yang dipancarkan
pada panjang gelombang antara 4000 – 10.000 cm-1. Cahaya infrared yang
dibentuk oleh sumber cahaya akan dipisah didalam interferometer dan akan
bergabung lagi untuk membentuk interferogram. Sumber cahaya berasal dari
lampu Wolfram halogen. Cahayanya diatur oleh beam splitter (cahaya pemisah)
untuk berinteraksi dengan molekul pada sampel yang sebagian cahaya akan
diserap dengan panjang gelombang sesuai struktur kimianya, sedangkan sebagian
cahaya yang tidak diserap akan dipantulkan sesuai sistem optik lainnya sampai
diterima detector. Detector berfungsi mengkonversi panjang gelombang
elektromagnetik menjadi data elektrik untuk mengukur intensitas cahaya dan oleh
analog-digital converter (ADC) akan mengkonversi data analog ke data digital
yang selanjutnya dapat diproses dengan software. Data reflektan yang dihasilkan
akan ditransformasikan menjadi bentuk data absorbansi (penyerapan) dengan
mengubahnya menjadi log (1/R). Melalui analog-digital converter (ADC) data KALIBRASI NIR
Nilai Reflektan, Data Treatment
Data Uji Metode Kimia
Regresi Linear
Hasil Kalibrasi NIR Jumlah Sampel
Data Uji Metode Kimia
Nilai Reflektan, Data treatment,
Persamaan Kalibrasi, Pengukuran kandungan nutrisi
Hasil Validasi NIR Jumlah Sampel
Evaluasi Uji Banding
Jumlah Sampel
Metode Kimia
T a h a p
I
T a h a p
25
analog akan dikonversi ke data digital. Selanjutnya diproses dengan Fourier
transformation (FFT) untuk menghasilkan spektrum (Buchi, 2005).
Aplikasi pengukuran dibuat sesuai parameter uji, yaitu air, abu, protein
kasar, lemak kasar, serat kasar, kalsium dan fosfor.
Ssampel akan direspon dengan melakukan pre-treatment pada spektra.
Berikut ini faktor-faktor dalam membuat spektra kalibrasi dan validasi NIR yang
dilakukan secara otomatis oleh Software NIRCal adalah sebagai berikut :
1. Tipe/jenis pretreatment yang dipilih
Tipe/jenis pretreatment pada software NIRCal ini terdapat 19 jenis, dimana
untuk melakukan kalibrasi dapat menggunakan satu atau dua jenis
pretreatment tergantung metode yang digunakan PCR atau PLS.
2. Metode yang dipilih
Metode yang digunakan dalam membuat kalibrasi NIR ada 3 (tiga) jenis,
yaitu MLR, PCR dan PLS, tetapi yang banyak digunakan adalah PLS dan
PCR
Gambar 3. Skema interferometer
Sumber cahaya NIR
Sampel Balok splitter
Cermin kaku
Gambar 4. Skema NIR Spectroscopy
Pretreatment spektra digunakan untuk memperbaiki dan meminimalkan
pengaruh yang tidak diinginkan. Spektra NIR dipengaruhi oleh berbagai
parameter seperti variasi kimia dan fisik dari sampel pada proses pengukuran dan
perubahan pada spektrometer yang akan mempengaruhi hasil spektrum. Beberapa
pengaruh yang umumnya muncul sebagai masalah adalah : serapan yang tumpang
tindih, tidak linear, pemisahan cahaya dan gangguan acak data. Salah satu cara
untuk memperbaiki masalah tersebut adalah signal spektra original akan
ditransformasi secara matematika yang disebut pretreatment. NIRCal membagi
jenis data pretreatment dan akan diseleksi oleh NIRCal software.
Spektra diperoleh umumnya ditentukan oleh fungsi PRESS (Predicted
Residual Error Sum Square) atau jumlah perbedaan antara nilai data uji (original)
dan nilai prediksi dari NIR. Pretreatment ditentukan juga oleh panjang
gelombang. Adapun rumus PRESS adalah sebagai berikut :
N
PRESS = ∑ (Xn– Yn)2 n=1
27
Keterangan :
Xn = nilai data uji (original)
Yn = nilai prediksi (NIR)
n = nomor spektra (data kalibrasi atau validasi)
Jenis grafik spektra yang umum dipilih oleh NIRCal software adalah :
1. Normalization by Closure (NC). Jenis grafik ini masih seperti aslinya hanya
memperbaiki signal yang diperoleh. Adapun rumusnya menurut (Buchi 2006)
sebagai berikut :
N.T NC = ---
N ∑ Ti i=1
Keterangan :
N = jumlah data
T = transmisi atau reflektan (NIR)
i = nomor spektra (data kalibrasi atau validasi)
2. Turunan pertama BCAP untuk mengeliminasi ordinat linear yang tidak dipakai
Rumus kedua dari turunan pertama BCAP sebagai berikut :
f(Xi+2) + f(Xi+1)- f(Xi-1) – f(Xi-2) f’(Xi) = ---
4
Keterangan ;
f ‘ = jumlah data yang diturunkan X = ordinat
i = nomor spektra (data kalibrasi atau validasi)
3. Vector Normalization to Unit Length (VN) untuk mengurangi variasi dari
baseline dan mengeliminasi ordinat linear yang tidak dipakai. Rumus ketiga
dari Vector Normalization to Unit Length sebagai berikut :
T T
Keterangan :
T = transmisi atau reflektan (NIR)
4. Multiplicative Scatter Correction (MSC full) untuk mengurangi atau
meningkatkan pengaruh baseline yang disebabkan oleh pemisahan cahaya.
Adapun rumus MSC full sebagai berikut :
bT + Ē MSC full = ---
b
Keterangan :
b = slope regresi
T = rata-rata
E = error
5. Smooth Savitzky-Golay 9 Points untuk mengurangi gangguan dalam spektra
dan resolusi spektra serta masih seperti spektra original. Adapun rumus
Smooth Savitzky-Golay 9 Points sebagai berikut :
( -21f(Xi+4)+14f(Xi+3)+39f(Xi+2)+54f(Xi+1)+59f(Xi)+54f(Xi-1)+39f(Xi-2) + 14f(Xi-3) - 21f(Xi-4)
f smooth (Xi) = --- 231
Keterangan :
f = jumlah data yang diturunkan
X = ordinat
i = nomor spektra (data kalibrasi atau validasi)
Parameter yang diukur dari kalibrasi dan validasi NIR adalah nilai Q,
koefisien korelasi (r), Standard Error of Estimation (SEE), Standard Error of
Prediction (SEP), konsistensi, bias dan metode NIR (PCR/PLS).
Indikator keberhasilan kalibrasi dan validasi NIR adalah :
1. Nilai Q adalah indikator kualitas kalibrasi / validasi NIR secara keseluruhan
dengan nilai mendekati 1.
2. Nilai r adalah hubungan antara data uji kimia dengan data uji NIR dengan
29
3. Standard Error of Estimation (SEE) dan Standard Error of Prediction (SEP)
adalah standar deviasi yang diperoleh dari proses kalibrasi dan validasi untuk
mengukur ketelitian nilai. Semakin kecil semakin baik
4. Bias adalah rata-rata deviasi nilai prediksi NIR dengan nilai kimia mendekati
0 (nol)
5. Konsistensi : perbandingan nilai SEE dan SEP untuk mengukur keakuratan
dengan nilai kisaran 80 % - 110 %
6. Metode kalibrasi (PLS/PCR) : teknik analisis multivariat yang dilakukan
dengan mereduksi komponen dengan teknik Principal Component Analysis
(PCA) dilanjutkan dengan teknik analisis regresi antara komponen utama
yang baru terhadap respon
Adapun rumus KVhitung dan KVHorwitz adalah :
SEE atau SEP
KVhitung : --- x 100 % Rata-rata (X)
KVHorwitz : 2^1-0.5log(X/100)
Keterangan :
SEE : Standar Error of Estimation (data kalibrasi)
SEP : Standar Error of Prediction (data validaasi)
X : Rata-rata (dari data kalibrasi atau validasi)
Uji Banding
Tahap ini bertujuan untuk memvalidasi metode NIR hasil kalibrasi.
Metode uji banding seperti pad Gambar 2, yaitu dengan cara membandingkan
metode NIR dan metode kimia. Metode kimia mengacu pada AOAC (2005) dan
SNI (1992) seperti pada Tabel 2. Sampel pakan pada penelitian ini menggunakan
pakan BR1 dan pakan BR2 sebanyak 63 sampel. Seluruh sampel diuji kadar air
dan serat kasar mengacu metode SNI (1992), sedangkan abu, protein kasar, lemak
kasar, kalsium dan fosfor mengacu metode AOAC (2005). Selanjutnya sampel
Lama waktu uji menggunakan metode AOAC dan/atau SNI sekitar 3 hari
per sampel sedangkan menggunakan metode NIR sekitar 10 menit per sampel.
Analisis Data
Keakuratan metode NIR dapat dihitung menggunakan perhitungan uji t,
yaitu t-hitung ≤ t-tabel (Williams & Norris 1990) dan uji ketelitian/ keragaman
yaitu Koefisien Varian (KV) (Nasoetion 1970; Wood et al. 1998). Apabila hasil
perhitungan metode NIR ≤ t-tabel, berarti metode tersebut akurat dengan metode
kimia.
Hipotesis dari penelitian ini adalah :
H0 : Kandungan nutrisi prediksi dengan NIR = kandungan nutrisi dengan
metode kimia
H1 : Kandungan nutrisi prediksi dengan NIR ≠ kandungan nutrisi dengan
HASIL DAN PEMBAHASAN
Hasil Kalibrasi NIR
Spektra
Kalibrasi NIR dapat dilakukan apabila telah terkumpul data uji minimal 60
sampel yang telah diubah menjadi spektrum. Pada penelitian ini telah terkumpul
jumlah sampel pakan broiler dan spektra dari tiap jenis uji seperti pada Tabel 3.
Tabel 3. Jumlah sampel dan spektra untuk kalibrasi NIR
Jenis uji Jumlah sampel/ spektra
Jumlah Spektra Kalibrasi
Jumlah Spektra Validasi
Air 60 (180 spektra) 120 60
Abu 74 (222 spektra) 148 74
Protein Kasar 60 (180 spektra) 120 60
Lemak Kasar 280 (840 spektra) 560 280
Serat kasar 60 (180 spektra) 120 60
Kalsium 60 (180 spektra) 120 60
Fosfor 220 (660 spektra) 440 220
Hasil kalibrasi diperoleh dari proses penyinaran Infrared pada sampel dengan
panjang gelombang antara 4000 – 10.000 cm-1. Radiasi yang dipancarkan ini adalah
khas karena mempunyai panjang gelombang yang karakteristik pada ikatan kimia
yang dimiliki tiap nutrien. Dasar analisis menggunakan teknik NIR adalah bahwa
dengan mengukur besarnya absorbsi oleh ikatan kimia dari suatu nutrien, maka
konsentrasi nutrien itu dapat ditentukan. Semakin besar absorbsinya, maka
konsentrasinya semakin besar (Buchi 2005; Williams & Norris 1990). Absorbansi
NIR dipengaruhi oleh jumlah dan tipe ikatan C-H, N-H dan O-H yang unsur
pokoknya adalah molekul organik dalam pakan dan ukuran partikel sampel (Osborne
et al. 1993; Williams & Norris 1990).
Near Infrared (NIR) adalah sebuah metode vibrasi spekroskopi yang sangat
penting dalam industri obat-obatan, pakan dan pangan (Buchi 2006; Frederick H
2008). Hasil pengukuran NIR dengan panjang gelombang 4000 – 10000 cm-1 pada
pakan ayam broiler memiliki spektra yang berbeda-beda berkaitan dengan ikatan
ayam broiler memiliki kandungan air, abu, protein kasar, lemak kasar, serat kasar,
kalsium dan fosfor.
Pretreatment spektra digunakan untuk memperbaiki dan meminimalkan
pengaruh yang tidak diinginkan. Spektra NIR dipengaruhi oleh berbagai parameter
seperti variasi kimia dan fisik dari sampel pada proses pengukuran dan perubahan
pada spectrometer yang akan mempengaruhi hasil spektrum. Beberapa pengaruh yang
umumnya muncul sebagai masalah adalah : serapan yang tumpang tindih, tidak linear,
pemisahan cahaya dan gangguan acak data. Salah satu cara untuk memperbaiki
masalah tersebut adalah signal spektra original akan ditransformasi secara matematika
yang disebut pretreatment.
Spektra semua parameter uji (air, abu, protein kasar, lemak kasar, serat kasar,
Ca dan P) pada pakan ayam broiler sebelum dilakukan kalibrasi NIR mempunyai
bentuk tampilan grafik yang sama seperti pada Gambar 5.
Gambar 5. Spektra asli sebelum dilakukan kalibrasi NIR
Spektra pada masing-masing parameter uji setelah proses kalibrasi NIR
dilakukan adalah seperti :
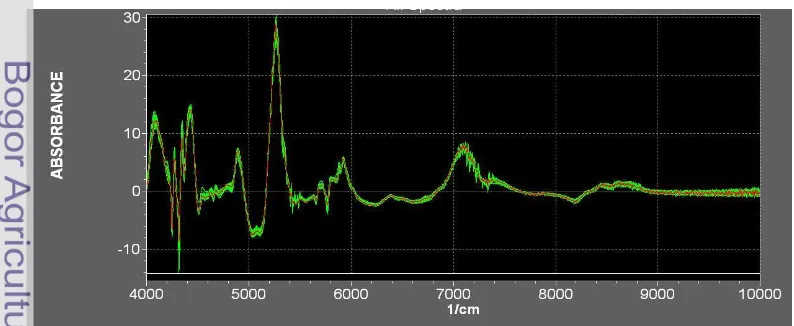
1. Spektra kadar air
33
Spektra kadar air seperti pada Gambar 6 diperoleh dari 180 data uji yang
digunakan untuk kalibrasi sebanyak 132 data (2/3 nya) dan validasi sebanyak 48 data
(1/3nya). Jenis grafik spektra yang dipilih adalah Normalization by Closure (NC).
Jenis grafik ini masih seperti aslinya hanya memperbaiki signal yang diperoleh.
2. Spektra kadar abu
Gambar 7. Spektra kadar abu hasil kalibrasi NIR
Spektra kadar abu seperti pada Gambar 7 diperoleh dari 220 data uji yang
digunakan untuk kalibrasi sebanyak 169 data (2/3 nya) dan validasi sebanyak 51 data
(1/3nya). Jenis spektra yang dipilih adalah Normalization by Closure (NC), turunan
pertama BCAP dan Vector Normalization to Unit Length (VN). Jenis grafik ini
gabungan tiga jenis pretreatment. Tujuan dari Normalization adalah untuk
mengurangi variasi dari baseline sedangkan turunan pertama BCAP adalah untuk
mengeliminasi ordinat linear yang tidak dipakai
3. Spektra kadar protein kasar
Spektra kadar protein kasar seperti pada Gambar 8 diperoleh dari 180 data uji
yang digunakan untuk kalibrasi sebanyak 132 data (2/3 nya) dan validasi sebanyak 48
data (1/3nya). Jenis grafik spektra yang dipilih adalah Normalization by Closure (NC)
dan turunan pertama BCAP. Jenis grafik ini gabungan dari dua jenis pretreatment.
Tujuan dari turunan pertama BCAP adalah untuk mengeliminasi ordinat linear yang
tidak dipakai.
4. Spektra kadar lemak kasar
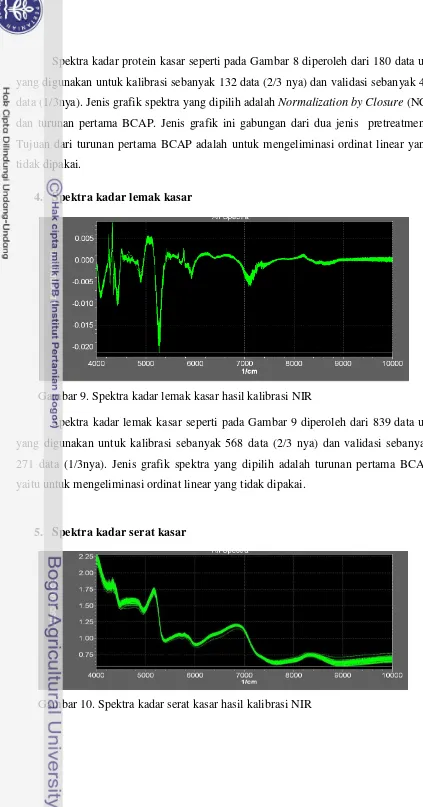
Gambar 9. Spektra kadar lemak kasar hasil kalibrasi NIR
Spektra kadar lemak kasar seperti pada Gambar 9 diperoleh dari 839 data uji
yang digunakan untuk kalibrasi sebanyak 568 data (2/3 nya) dan validasi sebanyak
271 data (1/3nya). Jenis grafik spektra yang dipilih adalah turunan pertama BCAP
yaitu untuk mengeliminasi ordinat linear yang tidak dipakai.
5. Spektra kadar serat kasar
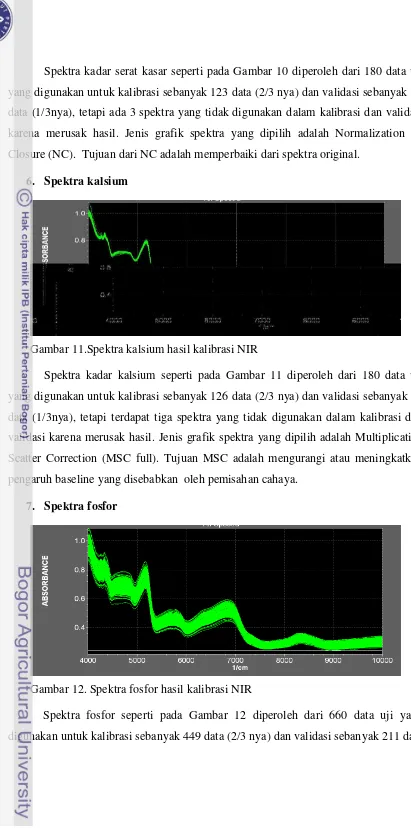
35
Spektra kadar serat kasar seperti pada Gambar 10 diperoleh dari 180 data uji
yang digunakan untuk kalibrasi sebanyak 123 data (2/3 nya) dan validasi sebanyak 54
data (1/3nya), tetapi ada 3 spektra yang tidak digunakan dalam kalibrasi dan validasi
karena merusak hasil. Jenis grafik spektra yang dipilih adalah Normalization by
Closure (NC). Tujuan dari NC adalah memperbaiki dari spektra original.
6. Spektra kalsium
Gambar 11.Spektra kalsium hasil kalibrasi NIR
Spektra kadar kalsium seperti pada Gambar 11 diperoleh dari 180 data uji
yang digunakan untuk kalibrasi sebanyak 126 data (2/3 nya) dan validasi sebanyak 51
data (1/3nya), tetapi terdapat tiga spektra yang tidak digunakan dalam kalibrasi dan
validasi karena merusak hasil. Jenis grafik spektra yang dipilih adalah Multiplicative
Scatter Correction (MSC full). Tujuan MSC adalah mengurangi atau meningkatkan
pengaruh baseline yang disebabkan oleh pemisahan cahaya.
7. Spektra fosfor
Gambar 12. Spektra fosfor hasil kalibrasi NIR
Spektra fosfor seperti pada Gambar 12 diperoleh dari 660 data uji yang
(1/3nya). Jenis grafik spektra yang dipilih oleh NIRCal software adalah Smooth
Savitzky-Golay 9 Points. Tujuan dari smoothing adalah untuk mengurangi gangguan
dalam spektra dan resolusi spektra serta masih seperti spektra original.
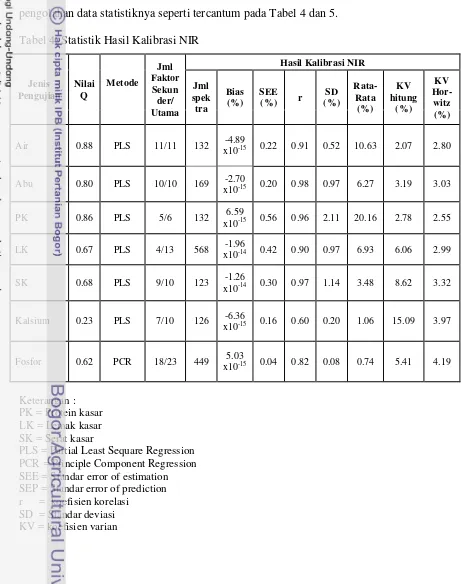
Hasil Statistik Kalibrasi dan Validasi NIR
Proses kalibrasi NIR juga menghasilkan kurva kalibrasi dan validasi serta
pengolahan data statistiknya seperti tercantum pada Tabel 4 dan 5.
Tabel 4. Statistik Hasil Kalibrasi NIR
Jenis Pengujian
Nilai Q
Metode
Jml Faktor
Sekun der/ Utama
Hasil Kalibrasi NIR
Jml spek tra
Bias (%)
SEE
(%) r
SD (%)
Rata- Rata
(%)
KV hitung
(%)
KV Hor-witz (%)
Air 0.88 PLS 11/11 132 -4.89
x10-15 0.22 0.91 0.52 10.63 2.07 2.80
Abu 0.80 PLS 10/10 169 -2.70
x10-15 0.20 0.98 0.97 6.27 3.19 3.03
PK 0.86 PLS 5/6 132 6.59
x10-15 0.56 0.96 2.11 20.16 2.78 2.55
LK 0.67 PLS 4/13 568 -1.96
x10-14 0.42 0.90 0.97 6.93 6.06 2.99
SK 0.68 PLS 9/10 123 -1.26
x10-14 0.30 0.97 1.14 3.48 8.62 3.32
Kalsium 0.23 PLS 7/10 126 -6.36
x10-15 0.16 0.60 0.20 1.06 15.09 3.97
Fosfor 0.62 PCR 18/23 449 5.03
x10-15 0.04 0.82 0.08 0.74 5.41 4.19
Keterangan : PK = Protein kasar LK = Lemak kasar SK = Serat kasar
PLS = Partial Least Sequare Regression PCR = Principle Component Regression SEE = Standar error of estimation SEP = Standar error of prediction r = koefisien korelasi